Инфракрасные спектры молекул
Тема
Инфракрасные спектры молекул
ИСХОДНЫЕ ДАННЫЕ:
Изучить особенности спектроскопии молекул в инфракрасном диапазоне
СОДЕРЖАНИЕ
Введение
. Особенности исследования молекул в
матричной изоляции
. Особенности исследования щелочно - галоидных
кристаллов
3.
Инфракрасные спектры молекул
. Пример спектра газа
Заключение
Список
использованной литературы
ВВЕДЕНИЕ
В последнее время в спектроскопии молекул образовался разрыв между
теорией и экспериментом, который существенно тормозил развитие научных
исследований. С одной стороны, современные спектральные приборы, большей частью
Фурье-спектрометры, обеспечивали измерение колебательных переходов с
разрешением лучше 0.01 см-1 и при этом выдавали обилие информации в
широком спектральном диапазоне, с хорошими параметрами: отношением сигнал -
шум, точностью измерения частоты, временным разрешением и т.д. С другой
стороны, теоретические подходы затрудняли обработку экспериментальных данных. В
частности, распространенный метод теории возмущений Рэлея - Шредингера требовал
пересмотра.
Интерес к молекулам, находящимся в матрице ионного кристалла, во многом
определяется специфическим характером взаимодействия заряженных молекул между
собой и с окружающими их ионами кристалла. Проблема взаимодействия заряженной
молекулы с окружающими ее атомарными или молекулярными ионами в настоящее время
недостаточно изучена, хотя она, несомненно, фундаментальна и важна для многих
разделов физики. С заряженными молекулярными системами мы имеем дело,
рассматривая ионизированные молекулы в верхних слоях атмосферы, химические
реакции, взаимодействия между отдельными заряженными фрагментами одной сложной
молекулы, примесные молекулярные ионы в ионных кристаллах.
1. Особенности исследования молекул в матричной изоляции
По сравнению с другими проблемами спектроскопии, которые решаются в
настоящее время в физике конденсированных сред, для молекул в окружении
кристаллической матрицы (матричной изоляции) характерен ряд полезных свойств.
Одно из них - маленькая полуширина колебательных полос. Например, при
температуре жидкого гелия полуширина колебательной полосы иона SH- в KCl
меньше 0.01 см-1. Исследования таких систем гораздо более
информативно даже в сравнении с изучением свободных молекул. По сравнению с
последними, молекулы в матрице имеют заторможенное вращение даже при комнатных
температурах. И, как правило, при понижении температуры они переходят в
состояние с фиксированной ориентацией. Что позволяет тщательнее изучить их
спектральные характеристики.
Другая особенность данных систем заключается в том, что они не являются
электронейтральными. Специфику колебаний заряженных систем, можно рассмотреть
на примере двухатомного иона. В процессе колебательного движения молекулярного
иона его электронная плотность может перераспределяться между атомами в
молекуле, что приведет к смещению центра заряда молекулы относительно ее центра
масс. Т.е. центр заряда будет совершать осцилляции с частотой колебаний
молекулы и, таким образом, возникнут дополнительные поляризационные эффекты окружающей
среды. В силу того, что возмущение от осциллирующего заряда более
дальнодействующее по сравнению с дипольным возмущением, можно ожидать
существенное влияние этого эффекта на оптические свойства кристалла.
Отличие заряженных систем от электронейтральных наиболее ярко проявляется
для примесных молекул в ионных кристаллах вследствие заряженности примесной
молекулы и ионного характера структуры кристалла, влияние которого существенно
на типичных для кристалла небольших расстояниях между молекулярным дефектом и
его кристаллическим окружением. Вероятно, такое взаимодействие и приводит к
наблюдающемуся переносу энергии в ЩГК с центров окраски (ЦО) на колебательные
уровни CN- или OH-, что приводит в первом случае к интенсивной
люминесценции CN-, а во втором - к тушению люминесценции ЦО.
. Особенности исследования щелочно-галоидных кристаллов
Высокая температура плавления ЩГК дает возможность исследовать
температурные зависимости физических свойств в широком интервале температур.
Важно еще и то, что большая часть примесных дефектов типа XH- легко
встраивается в кристаллическую решетку. Примером может служить молекула OH-,
которая входит практически во все ЩГК, замещая ион галоида. Наличие атома
водорода в молекуле XH- приводит к тому, что частота собственных
колебаний молекулярного иона лежит значительно выше колебаний кристаллической
решетки, что существенно облегчает проведение эксперимента.
Другие важные достоинства имеют водородсодержащие примесные молекулы. Они
проявляются в том, что среди всех двухатомных ионов наибольшие изменения
колебательных спектральных характеристик при внедрении молекулы в кристалл
отмечены именно для таких молекул. При внедрении молекулярного иона в кристалл
его физические свойства изменяются в соответствии с кристаллическим окружением.
Изменения в ближайшем кристаллическом окружении OH-, например, в
результате образования радиационных дефектов при γ-облучении, приводят к существенным
перераспределениям интенсивностей в спектрах поглощения. Последнее отчетливо
проявляется в колебательных спектрах. Легкий атом водорода служит своего рода
индикатором, чутко реагирующим на изменения окружения. В этом смысле изучение
молекулярных дефектов дает информацию не только о самом дефекте, но и об
окружающей его кристаллической матрице. Такой метод исследования предполагает
знание основных физических свойств примесного иона.
инфракрасный спектр матричный кристалл молекула
3. Инфракрасные спектры молекул
В отличие от видимого и ультрафиолетового диапазонов, которые обусловлены
главным образом переходами электронов из одного стационарного состояния в
другое, в инфракрасном диапазоне спектра проявляются в основном колебательные и
вращательные степени свободы движения атомов. Это могут быть, к примеру,
колебательные движения атомов в молекуле, вращение молекулы как целого вокруг
оси проходящей через центр масс или коллективные колебания атомов
кристаллической решетки, так называемые фононы, и т.д. Оказывается, что
изучение данных видов движения современными теоретическими и экспериментальными
средствами спектроскопии, является мощным инструментом, которые позволяют не
только объяснить особенности колебательных спектров, но и выявить структуру колеблющейся
системы, изучить физику протекающих в ней процессов.
Теоретическая спектроскопия, изучающая переходы атомной системы с одного
энергетического уровня на другой под действием электромагнитного излучения,
начинается с изучения собственных значений энергии системы. Они находятся в
результате решения уравнения Шредингера
Hψ = Εψ,
где H - гамильтониан системы,
ψ и Ε - собственные функции и значения.
Поскольку молекула состоит из ядер и электронов, ее гамильтониан можно
представить как сумму двух частей:
H = Hяд+ Hэл.
Первое слагаемое описывает движение ядер, второе - электронов «вокруг»
ядер. Ядра имеют массу более чем на три порядка превышающую массу электрона, и
поэтому движутся значительно медленнее их. В первом приближении можно считать
движения ядер и электронов независимыми. Приближение о независимости движений
электронов и ядер называется адиабатическим, или приближением
Борна-Оппенгеймера, которые ввели его в 1927 году.
Пользуясь данным приближением, Борн и Оппенгеймер показали, что с хорошей
точностью полную энергию молекулы можно представить как сумму трех независимых
вкладов:
E = Eэл + Eкол + Eвращ.
Здесь Eэл - энергия электронов,
Eкол - энергия колебаний ядер
(подразумевается колебательное отклонение ядер от равновесного положения при неподвижном
центре масс молекулы),
Eвращ - энергия вращения молекулы как
целого.
Существенно, что Eэл>>Eкол>>Eвращ. Такое соотношение определяет
своеобразную структуру энергетических уровней молекулы. Каждый электронный
уровень, который мы будем обозначать квантовым числом υ=0, 1, … , сопровождается своим
набором колебательных уровней, квантовые числа n=0, 1, … , а те, в свою очередь, имеют вращательную
структуру, квантовые числа j = 0,
1, ….

. Пример спектра газа
Пример колебательно-вращательного спектра газа 1H35Cl в основном электронном состоянии (υ=0) приведен на рисунке 2 (a). Здесь по горизонтальной оси
отложено волновое число (волновое число определяется как единица, деленная на
длину волны в сантиметрах). На рисунке 2 (b) изображена схема энергетических уровней и переходов,
соответствующих колебательно-вращательным линиям рисунке 2 (a). Серия линий A является чисто вращательной - она
возникает благодаря только переходам между вращательными уровнями основного
колебательного состояния (n=0).
Переходы с уровня n=0 на уровни n=1 и n=2 ответственны за линии B и C.
Чисто колебательные переходы, когда вращательное квантовое число не изменяется
(Δj=0), для молекул HCl запрещены правилами отбора. Поэтому в сериях B и C
отсутствуют центральные линии. В случае, когда вращательная степень свободы
отсутствует (например, для молекул в матрицах), отсутствует и серия A, а вместо серий B и С имеют место одиночные линии на
месте «пропущенных» центральных линий, соответствующие переходам n=0→n=1 и n=0→n=2 соответственно. Переходы с
нулевого на первый колебательный уровень (B) называются основным тоном или первой гармоникой, переходы с
нулевого на второй (C) - первым
обертоном (или второй гармоникой) и т.д. Конечно, возможны переходы n=0→n=3 - второй обертон (третья гармоника), n=0→n=4 - третий обертон (четвертая гармоника) и т.д. Однако
интенсивности соответствующих им линий низки и данные линии на рисунке 2 не
отображены.
Однако заметим, что при комнатных температурах, когда размеры молекул
малы по сравнению с характерными размерами матрицы, вращательные степени
свободы могут проявляться в виде вибрационных спектров или даже в виде спектров
почти свободного (заторможенного) вращения.
Для наглядности высота группы линий C на рисунке увеличена в 10 раз. В верхней части рисунка
показаны те же группы линий A, B и C, что и внизу, но в более удобном для визуального
сопоставления масштабе. (b)
Колебательно-вращательные энергетические уровни молекулы 1H35Cl.
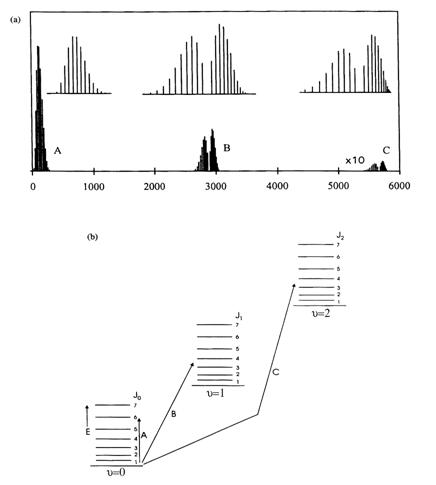
Рисунок 2 (a). Схема
вращательно-колебательного спектра 1H35Cl
Стрелками показаны переходы, соответствующие линиям в спектре. Переходы с
нулевого колебательного уровня на первый (B) называются основным тоном, переходы с нулевого на второй (C) - первым обертоном.
ЗАКЛЮЧЕНИЕ
Несмотря на большое число научных публикаций, ряд важных оптических
свойств иона OH- и других водородсодержащих двухатомных примесных ионов не
достаточно исследованы. Так, даже данные о частотах основных колебательных
переходов наиболее изученного примесного дефекта OH- были отрывочные,
практически отсутствовали сведения о важнейших спектральных характеристиках
двухатомных ионов - механической и электрооптической ангармоничностях.
Здесь следует подчеркнуть, что знание столь важных электрооптических
параметров позволяет эффективно применять физические методы для решения ряда
теоретических и практических задач физики твердого тела. Хорошо известно, что
исследования спектральных характеристик изолированных в кристалле двухатомных
примесных ионов и проявлений их межионных взаимодействий методами спектроскопии
позволяют решить не только прямую задачу спектроскопии, т.е. предсказать
оптические свойства, но и обратную - определить по спектрам природу
взаимодействий и построить модель центра.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Казаков К.
В. // Опт. и спектр. 2014. Т.
97. №5. с. 772.
2. Алексеев
П.Д, Мальцев К.А. Природа ИК-спектров монокристаллов.
3. Наберухин
Ю.И. Лекции по молекулярной спектроскопии/ Ю.И.
4. Пентин
Ю.А. Основы молекулярной спектроскопии / Ю.А. Пентин, Г.М. Курамшина. - М.:
Мир; БИНОМ. Лаборатория знаний, 2010. - 398 с.