Анализ соотношения смертности и заболеваемости населения Республики Беларусь при злокачественных новообразованиях различной локализации
Министерство
образования Республики Беларусь
Учреждение
образования
Международный
государственный экологический университет
имени А.Д.
Сахарова
Факультет
заочного обучения
Кафедра
радиационной гигиены и эпидемиологии
Дипломная
работа
Анализ
соотношения смертности и заболеваемости населения Республики Беларусь при
злокачественных новообразованиях различной локализации
Студентка 6-го курса
Дрозд Ольга Александровна
Минск 2013
Реферат
Цель работы - проанализировать тенденции в
смертности и заболеваемости населения Республики Беларусь при злокачественных
новообразованиях различной локализации, провести анализ соотношения двух
показателей при различных локализациях злокачественных новообразований и в
динамике.
Проанализированы эпидемиологические
закономерности в заболеваемости населения республики злокачественными
новообразованиями.
Проанализированы эпидемиологические
закономерности в смертности населения от злокачественных новообразований.
Проанализировано соотношение смертности и
заболеваемости при злокачественных новообразованиях различной локализации в
динамике, по административным территориям.
Проведен расчет и анализ индексов подобия и
накапливаемости при злокачественных новообразованиях различной локализации.
Рэферат
Мэта працы - прааналізаваць
тэндэнцыі ў суадносінах смяротнасці і захворвання насельніцтва Рэспублікі
Беларусь пры злаякасных наватворах рознай лакалізацыі.
Прааналізаваны эпідэміялагічныя
заканамернасці ў захворвання насельніцтва рэспублікі злаякаснымі наватворамі.
Прааналізаваны эпідэміялагічныя
заканамернасці ў смяротнасці насельніцтва ад злаякасных новаўтварэнняў.
Прааналізавана суадносіны
смяротнасці і захворвання пры злаякасных наватворах ў дынаміцы, па
адміністрацыйных тэрыторыях і па лакалізацыі працэсу.
Праведзены разлік і аналіз індэксаў
падабенства і накаплення пры злаякасных наватворах рознай лакалізацыі.
Abstract
aim of the work is to analyze trends
in the ratio of mortality and morbidity of the population of the Republic of
Belarus in the malignant neoplasms of different localization.the
epidemiological patterns of disease in the population of the Republic of
malignant neoplasms.the epidemiological patterns in mortality from malignant
neoplasms.the ratio of mortality and morbidity with malignant neoplasms in dynamics
on administrative territories and for the localization process.calculation and
the analysis of the indexes of similarity and index of accumulation in
malignant neoplasms of different localization.
Введение
Мировой наукой накоплен
огромный достоверный материал, свидетельствующий о том, что злокачественные
опухоли, объединяемые под общим названием «рак», распространены повсеместно и
поражают население всех континентов, народностей и рас. Неоспоримым является и
то, что число вновь заболевших в мире неуклонно растет, причем ежегодный
прирост составляет от 0,5 до 7% по разным локализациям в различных регионах
Земли [34,35].
Этим объясняется то пристальное внимание,
которое человечество уделяет проблемам онкологии. Несмотря на то, что благодаря
огромным усилиям многих стран в последние десятилетия достигнуты ощутимые
успехи в диагностике и лечении заболевших, проблема продолжает обостряться,
т.к. смертность от рака в большинстве стран возрастает, и злокачественные
новообразования как причина смерти занимают второе место после
сердечно-сосудистых заболеваний.
По материалам ВОЗ, в 2009 г. в мире было
зарегистрировано 16 млн. случаев заболевания злокачественными новообразованиями
и 10,6 млн. умерших от них.
Согласно прогнозам, к 2020 г. число новых
случаев заболевания раком достигнет 16 млн. в год, а случаев смерти- 10 млн..
Значительная часть этого увеличения в абсолютном выражении обусловлена
старением населения - явлением, получившим название «демографический переход»
[2].
Находясь в центре Европы, Беларусь не стала
исключением, и все связанные с онкологической заболеваемостью и смертностью
проблемы развитых стран непосредственно касаются и ее населения. На протяжении
многих лет в Республике Беларусь наблюдается постоянный рост общей
онкологической заболеваемости [32].
Как свидетельствуют данные официальной
медицинской статистики, в настоящее время злокачественные новообразования в РБ
составляют 0,5% всей первичной заболеваемости населения, занимая 13-е ранговое
место. Злокачественные новообразования по числу заболевших уступают
неонкологическим болезням органов дыхания, кровообращения и многим другим.
Однако структура смертности населения Республики Беларусь представляет собой
совершенно иную картину. Злокачественные новообразования, составляющие 0,5% в
общей структуре первичной заболеваемости населения, являются причиной смерти в
13,7% от общей смертности населения и стоят на втором месте, уступая лишь
смертности от болезней системы кровообращения.
Кроме того, злокачественные новообразования
занимают также второе место в структуре первичной инвалидности населения
Беларуси, составляя 20,4% и уступая опять же лишь инвалидности от болезней
системы кровообращения. Динамика первичной инвалидности населения
трудоспособного возраста вследствие злокачественных новообразований имеет
четкую тенденцию к увеличению [5].
1. ЭПИДЕМИОЛОГИЧЕСКИЕ АСПЕКТЫ ЗАБОЛЕВАЕМОСТИ
ЗЛОКАЧЕСТВЕННЫМИ НОВООБРАЗОВАНИЯМИ
.1 Закономерности
распространения опухолей
Опухоли могут появиться у человека в любом
возрасте. Около 80% больных, впервые заболевших в течение года злокачественными
новообразованиями - лица старше 50 лет, достигая максимума к 65 годам. Однако и
в более молодом возрасте заболеваемость сравнительно велика. Для младших
возрастных групп существует два пика заболеваемости: до 4 - 7 лет и в 11 - 12
лет. У детей младшего возраста чаще регистрируются заболевания крови, опухоли
почек (Вильмса), нервной ткани (нейробластомы). В подростковом возрасте -
опухоли костей и лимфатической ткани.
Несмотря на то, что риску ракового заболевания подвержен
любой орган, частота поражений различных участков тела далеко не одинакова.
Ранговое распределение первых пяти мест (в бывших республиках СНГ,
установившееся после середины 80 - х годов) частоты регистрации опухолей у
мужчин и женщин следующее:
Таблица 1.1-Ранговое распределение частоты
опухолей у мужчин и женщин
|
Ранговое
место
|
|
Мужчины
|
|
Женщины
|
|
1
место -
|
|
рак
легкого;
|
|
Рак
кожи;
|
|
2
место -
|
|
рак
желудка;
|
|
рак
молочной железы;
|
|
3
место -
|
|
рак
кожи;
|
|
рак
желудка;
|
|
4
место -
|
|
опухоли
лимфатической ткани
|
|
рак
шейки матки;
|
|
5
место -
|
|
рак
прямой и ободочной кишки.
|
|
рак
легкого.
|
Если попытаться оценить заболеваемость раком у
представителей обоего пола, то печальное первенство принадлежит злокачественным
опухолям пищеварительной системы (пищевода, желудка, кишечника и др.)
В цивилизованных странах каждый четвертый (1:4)
человек рано или поздно в течение своей жизни заболевает той или иной формой
злокачественной опухоли. Каждый пятый (1:5) умирает от рака; только сердечно -
сосудистые заболевания по смертности опережают злокачественные новообразования.
В развивающихся странах частота раковых больных
была всегда ниже, чем в странах с высоким техническим уровнем. Причиной тому -
низкая продолжительность жизни. В последнее время и в этих странах - с увеличением
продолжительности жизни повышается онкологическая заболеваемость. К тому же,
вредные привычки из развитых стран становятся трагическим достоянием
развивающихся стран [13].
Вместе с тем, существуют определенные этнически
- географические отличия структуры отдельных форм злокачественных
новообразований.
Казахи, туркмены и другие коренные жители
Средней Азии часто страдают раком пищевода, что определенным образом связано с
обычаями и особенностями приема пищи.
В Юго-Восточной Азии, в некоторых регионах Африки
и Тюменской области распространен первичный рак печени. Для одних - причиной
высокой частоты рака печени является использование в пищу злаковых культур
(арахиса и др.), которые поражаются плесневым грибком, вырабатывающего
афлотоксин. Последний оказался выраженным канцерогеном (ракообразующим агентом)
с излюбленным действием на печень. Для других - причина высокой частоты кроется
в высокой паразитарной инвазии желчных путей, как, например, описторхозом
населения Тюменской области.
Люди с белой кожей и голубыми глазами чаще
страдают раком кожи, чем чернокожие, и наоборот, чернокожие более подвержены
риску развития пигментных опухолей.
У горожан рак легких встречается во много раз
чаще, чем у жителей сельских местностей (в свою очередь у сельских жителей встречается
чаще рак кожи); рак полости рта чаще наблюдается у жителей среднеазиатских
республик СССР. Причем поражает болезнь по преимуществу коренное население этих
республик и крайне редко представителей других национальностей [10].
В горах Урала, Алтая, Памира в почвенных водах
содержится очень мало йода, столь необходимого человеку. В результате наступают
нарушения деятельности щитовидной железы - она увеличивается. А ведь именно в
этих районах относительно чаще регистрируются случаи злокачественных опухолей
щитовидной железы. Между тем профилактический прием йода избавляет человека от
опасности подобного заболевания. Замечено, что чем ближе к экватору, тем чаще у
населения наблюдаются злокачественные опухоли костей - саркомы [4].
В развитых странах одной из ведущих проблем
мужчин становиться рак предстательной железы (РПЖ). Считалось, что РПЖ - это
проблема долголетия (тех, кому за 65). Однако сейчас установлено, что это
длительное и скрытое заболевание, начало которому молодой и средний возраст,
только проявляющее себя в пожилом и преклонном возрасте. Для юношей и молодых
мужчин большую опасность представляют опухоли яичек. Следует отметить, что в
диагностике и лечении этих форм опухолей в последнее время достигнуты
значительные успехи.
1.2 Факторы риска
развития злокачественных новообразований
Злокачественное новообразование возникает в
результате генетических повреждений в одной клетке. Единичного генетического
повреждения, как правило, недостаточно для превращения клетки в опухолевую.
Лишь накопление 5-10 мутаций в течение продолжительного времени, часто многих
лет, приводит к злокачественному новообразованию[11]. Генетические нарушения
способствуют либо активации протоонкогенов, стимулирующих пролиферацию клеток,
либо подавлению генов - супрессоров опухолевого роста, тормозящих пролиферацию.
Неправильная работа генов, контролирующих рост и деление клеток вызывает
неконтролируемую клеточную пролиферацию. Только около 5-10% случаев рака
являются наследственными, а остальные случаи рака являются результатом мутаций,
возникающих в течение жизни в соматических клетках. Но даже при наследственной
передаче предрасположенности к раку злокачественное новообразование возникает
только в результате дополнительных соматических мутаций[12].
Возникновение мутаций происходит вследствие
воздействия либо внешних факторов (курение, химические вещества, радиация,
инфекционные агенты, солнечное излучение, алкоголь), либо внутренних (гормоны,
иммунная система, наследуемые мутации). Причинные факторы могут действовать
совместно или поочередно, вызывая или активизируя карциногенез.
Вероятность злокачественных новообразований
резко увеличивается с возрастом: до 39 лет заболевает 1 из 58 мужчин и 1 из 52
женщин, в период 40-59 лет - 1 из 13 мужчин и 1 из 11 женщин, в период 60-79
лет 1 из 3 мужчин и 1 из 4 женщин [16]. Около 76% всех случаев рака выявляются
после 55 лет.
Существенный вклад в развитие ряда
онкологических заболеваний вносит курение. С курением связывают 87% смертности
от рака легкого и большую часть заболеваний раком гортани, ротовой полости,
пищевода и мочевого пузыря[31]. Кроме того, имеется тесная ассоциация курения с
развитием и смертностью от рака почки, поджелудочной железы, шейки матки,
печени, носовой полости и колоректального рака. Курение наносит вред здоровью
не только курящим, пассивное курение также значительно повышает риск рака
легких.
Малоподвижный образ жизни связывают с развитием
рака молочной железы, толстого кишечника, предстательной железы и эндометрия.
Некоторые виды рака связывают с инфекционными агентами: вирусами гепатита В и С
(рак печени), вирусом папилломы человека типа 16 и 18 (рак шейки матки,
лимфомы, саркома Капоши), вирусом иммунодефицита человека (рак шейки матки,
лимфомы, саркома Капоши), геликобактером (рак желудка), описторхозом (рак
желчных протоков), шистосомозом (рак мочевого пузыря). Перечисленные
возбудители относятся к наиболее опасной группе канцерогенов для человека.
Дозозависимые отношения существуют между
потреблением алкоголя и риском рака ротовой полости, пищевода, гортани, печени
и молочной железы. Курение потенцирует влияние алкоголя, и оба они относятся к
наиболее опасной группе канцерогенов.
Риск рака тела матки, молочной железы, толстой
кишки, предстательной железы пропорционален степени ожирения[26]. У женщин с
ожирением по мужскому типу риск рака молочной железы в постменопаузе
значительно повышен и не зависит от степени ожирения. Предрасположенность к
раку тела матки и раку молочной железы при ожирении объясняется избыточным
образованием эстрогенов в жировой ткани.
В настоящее время доказан повышенный риск
некоторых форм рака среди родственников пациентов первой (родители, дети,
братья и сестры (сибсы)) и второй (бабушки, дедушки, тети, дяди, внуки,
племянники, племянницы) степеней родства. Для врожденных видов рака характерно:
развитие поражения в парных органах, ранний возраст заболевания, высокая
пенетрантность (частота проявления заболевания у носителей мутаций),
вертикальная передача (от родителей к детям) и связь с другими типами опухолей.
Благодаря успехам молекулярной генетики выделены гены, связанные с врожденной
подверженностью раку, разработаны рекомендации по скринингу пациентов с
повышенным риском рака и членов их семей.
При изучении факторов риска используется понятие
относительного риска, измеряющего силу связи между факторами риска и
определенным раком. Относительный риск отражает отношение вероятности рака у
человека с определенным фактором риска с вероятностью рака у человека с
отсутствием этого фактора. Например, относительный риск рака у курящего мужчины
равен 20, что означает, что вероятность развития рака у него в 20 раз выше, чем
у некурящего.
1.2.1 Рак легкого
Факторы риска
· Возраст >55 лет.
· Курение.
· Химические вещества - асбест, радон.
· Хроническая обструктивная болезнь
легких.
· Семейный анамнез.
· Индивидуальный анамнез рака.
· Идиопатический фиброзирующий
альвеолит.
Профилактика
· Борьба с курением.
· Исключение контакта с асбестом и
радоном.
· Высокое потребление овощей и
фруктов.
1.2.2 Колоректальный
рак
Факторы риска
· Семейный анамнез рака и/или полипов.
· Наследственный неполипозный
колоректальный рак.
· Семейный аденоматозный полипоз.
· Воспалительные заболевания кишечнике
(неспецифический язвенный колит и болезнь Крона).
· Курение.
· Малоподвижный образ жизни.
Профилактика
· Отказ от курения.
· Регулярные физические нагрузки.
· Ограничение потребления животных
жиров.
· Заместительная гормонотерапия в
постменопаузе.
· Регулярный скрининг.
· Нестероидные противовоспалительные
средства (аспирин в малых дозах [75 мг/сут], пироксикам, сулиндак).
1.2.3 Рак желудка
Факторы риска
· Возраст >50 лет.
· Хронический атрофический гастрит с
кишечной метаплазией.
· Пернициозная анемия.
· Аденоматозные полипы.
· Семейный аденоматозный полипоз.
· Употребление соленых, сушеных,
копченых и плохо консервированных продуктов, дефицит овощей и фруктов.
· Курение.
· Инфекция Helicobacter pylori.
· Семейный анамнез рака желудка.
· Гастроэзофагеальный рефлюкс.
· География: Япония, Китай, Корея,
Южная и Центральная Америка, страны Европы, Скандинавские страны, Россия.
Профилактика
· Высокое потребление овощей, фруктов и цельных
злаков.
· Ограничение соленой и
консервированной пищи.
· Правильное хранение продуктов.
· Борьба с курением.
· Лечение гастроэзофагеальной
рефлюксной болезни.
1.2.4 Рак кожи
Факторы риска
· Пигментные поражения (диспластического или
атипичного невуса и нескольких крупных обычных невусов).
· Семейный анамнез.
· Внешние признаки - плохо загорающие,
имеющие веснушки, светлый цвет кожи и глаз, белокурые или рыжие волосы.
· Инсоляция.
Профилактика
Ведущие медицинские организации в качестве
первичной профилактики рака кожи рекомендуют следующие мероприятия:
· Избегать пребывания на солнце в период с 10 до
16 часов.
· Ношение защищающей одежды
(широкополые шляпы, длинные брюки, солнцезащитные очки).
· Использование солнцезащитных кремов,
блокирующих ультрафиолетовые лучи типа А и В (с фактором защиты 15 и выше).
Использование солнцезащитных средств не заменяет ограничения пребывания на
солнце. У людей, использующих солнцезащитные средства, риск меланомы может быть
выше за счет увеличения времени пребывания на солнце.
· Отказ от использования аппаратуры
для загара.
· В качестве меры вторичной
профилактики может быть полезен регулярный самоосмотр, особенно в группе
высокого риска.
1.2.5 Рак молочной
железы
Факторы риска
· Возраст >50 лет.
· Женский пол.
· Семейный анамнез.
· Рак молочной железы в анамнезе.
· Атипичная гиперплазия по результатам
биопсии молочной железы.
· Фиброкистозная мастопатия, особенно
при наличии клеточной пролиферации или атипии.
· Воздействие ионизирующей радиации.
· Длительность детородного периода
(ранние менструации, поздняя менопауза).
· Отсутствие беременностей, поздние
первые роды.
· Заместительная гормонотерапия в
постменопаузе эстрогенами или их комбинацией с прогестероном.
· Злоупотребление алкоголем.
Пациент относится к группе повышенного риска
наследственного рака молочной железы при наличии хотя бы одного признака из
следующих [33]:
ü Рак молочной железы в возрасте до 40
лет.
ü Рак молочной железы и яичников у
пациента или близкого родственника (первой, второй или третьей степени
родства).
ü Рак молочной железы, ассоциированный
со следующими видами рака у близкого родственника: рак молочной железы у
мужчин, рак щитовидной железы, саркома, карцинома надпочечника, опухоли
головного мозга, лейкемия/лимфома.
ü Член семьи с известной мутацией в
генах, ответственных за рак молочной железы.
ü Популяции высокого риска (например,
частота носительства мутированных генов BRSA1/BRSA2 среди евреев-ашкенази
составляет 1:50, тогда как в целом частота равна 1:800).
ü Кроме того, заболеваемость раком
молочной железы связана с географическим, культурным, расовым, этническим,
социально-экономическим положением.
Профилактика
· Регулярные физические нагрузки с молодых лет
· Поддержание нормальной массы тела.
· Рождение ребенка в молодом возрасте.
· Продолжительная лактация.
1.2.6 Рак шейки матки
Факторы риска
· Папилломавирусная инфекция.
· ВИЧ-инфекция.
· Умеренная дисплазия в мазке с шейки
матки с окраской по Папаниколау в течение последних 5 лет.
· Раннее начало половой жизни и
многочисленные половые партнеры.
· Низкий социально-экономический
уровень.
· Курение.
· Пероральная контрацепция.
Профилактика
· Профилактика папилломавирусной и ВИЧ-инфекции.
· Отказ от курения.
.2.7 Рак предстательной
железы
Факторы риска
· Возраст >65 лет.
· Семейный анамнез.
· Диета с высоким содержанием животных
жиров.
Курение.
Профилактика
· Употребление овощей и фруктов.
· Отказ от курения.
1.3 Тенденции
онкологической заболеваемости населения Республики Беларусь
Ежегодно более 42 000 жителей Республики
Беларусь заболевают каким-либо злокачественным новообразованием. На конец 2011
г. на диспансерном учете по поводу злокачественного новообразования находилось
почти 252 761 жителей республики, что составило более 2% ее населения. Возросло
и число ежедневно выявляемых случаев злокачественных новообразований. Если в
2000 г. оно составляло 92 [29], то в 2011 г. число ежедневно выявляемых случаев
злокачественных опухолей возросло до 107. В качестве исторической справки:
число ежедневно выявляемых больных в 1970 г. не превышало 38 случаев[20]. В
целом за период 1970 - 2011 гг.. в Беларуси взято на учет 1053714 случаев
заболевания раком [32]. Следует отметить ряд моментов, значимых для оценки
современной онкоэпидемиологической ситуации в Беларуси. Заболеваемость раком
мужского населения в рассматриваемый период значительно превышает
заболеваемость женского населения: на 25% - в 2000 г. и на 18% - в 2011 г. (по
грубым показателям); на 59% - в 2000 г. [21] и 51% - в 2011 г. (по
стандартизованным показателям).
За этот же период произошли изменения в самой
структуре онкологической заболеваемости. Установлено, что частота поражаемости
раком отдельных органов у мужчин и женщин также имеет свои различия[6].
Стандартизованные по возрасту показатели
заболеваемости свидетельствуют, что при превышении общей онкологической
заболеваемости мужского населения по сравнению с женским в 1,5 раза наиболее
выраженное превышение характерно для рака гортани - в 33 раза, пищевода - в 17,
легкого - в 11,2, мочевого пузыря - в 7,5 раза. Менее выражены различия при
раке желудка - в 2,6 раза, прямой кишки - в 1,8, почки - в 2 раза. Довольно
близка у мужчин и женщин частота рака кожи (1,2 раза), ободочной кишки
(1,3),лимфогранулематоза (1,0), множественной миеломы (1,1). Только
злокачественные опухоли щитовидной железы встречаются у женщин в 3,7 раза чаще,
чем у мужчин.
Динамика заболеваемости раком отдельных органов
у мужчин и женщин также различается. За период 2000-2011 гг. на фоне увеличения
у мужчин общей онкологической заболеваемости на 10% снижается заболеваемость
раком губы (в 2 раза), желудка (в 1,1 раза), гортани (в 1,2 раза), легкого (в
1,1 раза). Наиболее выраженное увеличение заболеваемости отмечено для рака
предстательной железы (в 1,6 раза), кожи (в 1,6 раза), почки (в 1,3 раза),
ободочной кишки (в 1,3 раза), прямой кишки (в 1,2 раза).
У женщин за период 2000-2011 гг. общая
онкологическая заболеваемость возросла на 17%, при этом снизилась в 1,2 раза
только частота рака желудка. Увеличение заболеваемости характерно для рака кожи
(в 1,6 раза), молочной железы (в 1,1 раза), шейки матки (в 1,2 раза), тела
матки (в 1,3 раза), почки (в 1,3 раза), щитовидной железы (в 1,3 раза).
Анализ онкоэпидемиологической ситуации
показывает, что имеются также значительные различия в показателях
заболеваемости у городского и сельского населения[6]. Из-за значительных
различий в возрастной структуре городского и сельского населения Беларуси
грубый интенсивный показатель общей онкологической заболеваемости (рассчитываемый
как отношение общего числа заболевших к общей численности населения и
умноженный на 100 000) за весь десятилетний период на 10 -24% выше у сельского
населения.
Стандартизованный показатель общей
онкологической заболеваемости (позволяющий нивелировать влияние на величину
показателя различий в возрастной структуре сравниваемых групп населения)
свидетельствует об обратном. Если бы возрастная структура городского и
сельского населения Беларуси была одинаковой, то заболеваемость городских
жителей была бы на 19,5 - 17% выше, чем жителей села.
Имеются определенные различия общей
онкологической заболеваемости со среднегодовыми темпами ее прироста в областях
республики. Так, при среднегодовом темпе прироста заболеваемости за период
2000-2011 гг. в Беларуси на 2,6% наиболее высокими темпами возрастала
заболеваемость в г. Минске (3,6%) и Гомельской области (3,2%), а наиболее
низкими - в Брестской и Могилевской областях (1,9%)[7].
Отмеченные моменты обусловили особенности
современной онкоэпидемиологической ситуации в Беларуси.
Так, у мужчин наибольший удельный вес в
структуре онкологической заболеваемости занимает рак легкого (18,9%), за ним
следует рак кожи (13,2%), предстательной железы (10,2%), желудка (10,1%). Менее
1% составляют болезнь Ходжкина (0,8%), рак губы (0,7%),множественная миелома
(0,7%), опухоли костей (0,3%) и другие. У женщин наибольший удельный вес в
структуре онкологической заболеваемости занимает рак кожи (19,6%), молочной
железы (17,7%), тела матки (7,4%),желудка (6,8%). Менее одного процента
составляют болезнь Ходжкина (0,8%), рак губы (0,3%), опухоли костей (0,2%) и
другие.
В Беларуси с 2011 г. прогнозируется постоянное
увеличение численности населения в возрасте 55-75 лет . Число жителей этого
возраста к 2024 г . может возрасти с 1 835 808 до 2 312 297, т .е. увеличится
на 500000 человек . А так как возраст человека является одним из решающих
факторов, который определяет вероятность заболевания раком, то даже при
сохранении повозрастных показателей заболеваемости на нынешнем уровне в последующие
годы следует ожидать значительного увеличения числа случаев заболеваний - до 45
500 в 2017 г. и 52 000 в 2027 г.
1.4 Тенденции
смертности населения от злокачественных новообразований
Анализ смертности от пяти наиболее
распространенных в РБ злокачественных опухолей в зависимости от возраста
показал, что в возрастной группе до 15 лет у лиц обоего пола лидировали
лейкозы. В возрастной группе 40 лет и старше у мужчин 1-е ранговое место
занимал рак легкого, 2-е - рак желудка, 3-е - рак ободочной и прямой кишки. На
4-м ранговом месте в возрастной группе 15-39 лет находился рак желудка, 40-69
лет - рак поджелудочной железы, 70 лет и старше - рак предстательной
железы[28].
У женщин основной причиной смерти от
злокачественных опухолей в возрасте 40-69 лет был рак молочной железы, 1-е
ранговое место в возрастной группе 15-39 лет занимал рак шейки матки. В
возрастной группе 70 лет и старше лидировал рак ободочной и прямой кишки. С
увеличением возраста женщин рак желудка перемещался с 5-го рангового места (в возрастной
группе 15-39 лет) на 3-е (в возрастной группе 40-69 лет), а затем на 2-е (в
возрастной группе 70 лет и старше). Опухоли ЦНС занимали 2-е место в возрастной
группе 0-14 лет, а в возрастной группе 15-39 лет были уже на 4-м. Рак шейки
матки перемещался с 1-го рангового места в возрастной группе 15-39 лет на 5-е в
возрастной группе 40-54 года, а рак легкого - с 5-го в возрастной группе 55-69
лет на 4-е в возрастной группе 70 лет и старше[28].
В Республике Беларусь смертность и первичная
инвалидность от злокачественных опухолей устойчиво занимают второе место после
сердечно-сосудистых заболеваний.
В 2011 году раком заболело 0,5 процента
населения Беларуси. Выявляемость больных злокачественными новообразованиями на
1-2й стадиях составила 59 процентов[32]. Одногодичная летальность (процент
больных, умерших в течение года с момента установления диагноза) составляет в
Республике Беларусь 27,6 процента. Удельный вес умерших от рака в структуре
общей смертности населения в 2011 году составил 13,8 процента. В ведущих
странах Европы (Евросоюз) каждый год от онкологических заболеваний умирает 19,2
процента больных, в Германии - 22, Франции - 25,2, США - 23,1, Великобритании -
28 процентов, то есть практически каждый третий житель страны[34]. Следует
учитывать, что в условиях «демографического перехода» старение населения
приведет к увеличению доли злокачественных опухолей в общей структуре
смертности, и такая тенденция отмечается в большинстве развитых стран мира.
1.5 Профилактика рака
Профилактика онкологии - ряд мероприятий,
проводимых на разных этапах развития раковых заболеваний. Профилактика раковых
заболеваний бывает первичная (доклиническая), вторичная (клиническая) и
третичная (противорецидивная) профилактика рака[9].
Онкологическая патология занимает первые места и
в причинах смерти во многих странах мира. Причина столь высокой смертности от
злокачественных новообразований кроется прежде всего в особенностях этой
патологии и в том, что лишь 25% из числа больных этого профиля,
госпитализируемых для стационарного лечения находятся в сравнительно ранней
стадии заболевания, когда еще доступно и вполне перспективно предпринимаемое
лечение, а при таких наиболее часто локализациях рака, как рак желудка, рак
легкого госпитализация в первой стадии заболевания не достигает и 10%[1]. В то
же время современный уровень знаний и медицинской техники позволяет
диагностировать важнейшие формы злокачественных новообразований на ранних
стадиях их развития, а также устранить предшествующие им предопухолевые
состояния и предраковые изменения.
1.5.1 Первичная
профилактика злокачественных новообразований
Под первичной профилактикой злокачественных
новообразований понимается предупреждение возникновения злокачественных
опухолей и предшествующих им предопухолевых состояний путем устранения или
нейтрализации воздействий неблагоприятных факторов окружающей среды и образа
жизни, а также путем повышения неспецифической резистентности организма. Эта
система мероприятий должна охватывать всю жизнь человека.
В соответствии с современными данными о
механизмах канцерогенеза у человека и роли воздействия канцерогенных факторов в
возникновении онкологических заболеваний, первичная профилактика рака
проводится по следующим направлениям[13].
Онкогигиеническая профилактика, т.е. выявление и
устранение возможности действия на человека канцерогенных факторов окружающей
среды, а также выявление и использование возможностей уменьшения опасностей
такого воздействия. Спектр форм воздействия в этом направлении чрезвычайно
обширен и можно конкретизировать лишь основные из них. Такими являются образ
жизни и питание человека.
Ведущее значение в оздоровлении образа жизни
придается контролю курения. В учебных заведениях некоторых стран введен
специальный курс о последствиях курения и строгий контроль соответствующих
органов за динамикой заболеваемости населения, связанной с курением. Такое
внимание к контролю курения обусловлено тем, что табак и табачный дым содержат
более 3800 химических веществ, из которых многие относятся к полициклическим
ароматическим углеводородам (ПАУ), нитросоединениям и ароматическим аминам,
являющимися сильнейшими канцерогенами. По данным литературы атрибутивный риск
рака легкого, т.е. доля случаев этого заболевания, вызванных курением,
составляет 80-90% у мужчин и 70% у женщин. Велика роль курения в возникновении
рака пищевода, поджелудочной железы, мочевого пузыря.
Весьма значительно повышается онкологическая
заболеваемость и при употреблении алкоголя, особенно крепких напитков. Так
человек, систематически потребляющий 120 г и более чистого алкоголя в день,
имеет риск заболеть раком пищевода в 101 раз выше, чем сопоставимый с ним, но
не употребляющий алкоголя. Атрибутивный риск этой вредной привычки существенно
возрастает, если она сочетается с курением.
Большое значение в возникновении злокачественных
опухолей придается действию ионизирующих излучений, ультрафиолетовому
облучению, а также неионизирующим электромагнитным излучениям радио- и
микроволнового диапазона.
Установлена отчетливая связь между
катастрофическими событиями (стрессовыми ситуациями) в жизни человека и
возникновением злокачественных новообразований. Риск возникновения этих
заболеваний резко возрастает при эмоциональной подавленности невротического
характера вследствие нервно-психической травмы, отмечается также высокая корреляция
между депрессией (за исключением психических больных) и опухолевым процессом.
Весьма важное значение в возникновении
опухолевых заболеваний имеет характер питания (диеты) человека. Рекомендуемая
сбалансированная диета должна содержать жиров, особенно насыщенных, не более
75,0 в день для мужчин и 50,0 - для женщин. Она должна быть богата продуктами
растительного происхождения и витаминами, особенно А, В, С, Е, которые
оказывают на канцерогенез ингибирующее воздействие. Перечень факторов и воздействий
на канцерогенез не ограничивается перечисленными выше и является достаточно
обширным.
Биохимическая профилактика имеет целью
предотвращение бластоматозного эффекта от действия канцерогенов путем
применения определенных химических препаратов и соединений. Так, например,
общеизвестна роль нитратно-нитритного загрязнения окружающей среды в развитии
прежде всего злокачественных новообразований желудочно-кишечного тракта,
который является основным путем их проникновения в организм человека.
Канцерогенное воздействие воды и пищи возрастает также в случае загрязнения
водоисточников соединениями мышьяка, галогенов, а также загрязнения воздушной
среды различными химическими веществами и особенно асбестовой пылью,
бластомогенное действие которой при поступлении ее в организм ингаляционным
путем в настоящее время является общепризнанным. Канцерогенны химического
происхождения окружают человека и в бытовой обстановке: полициклические
ароматические углеводороды (ПАУ) и окислы азота при сжигании газа, формальдегид
и смолы содержатся в пластиках, нитросоединения появляются в дыму при жарении
пищи и т.д. Поэтому биохимическому направлению в профилактике онкологических
заболеваний придается большое значение, однако реализация возможностей этого
направления представляется весьма сложной: многие специалисты считают, что для
организации мероприятий по предотвращению бластоматозного действия химических
канцерогенов и контроля эффективности мер защиты необходим биохимический
мониторинг.
Теоретически эффективность мероприятий по онкогигиенической
и биохимической профилактике оцениваются снижением онкологической
заболеваемости на 70-80%, так как по данным Международного агенства изучения
рака (Лион, Франция) 80-90% злокачественных новообразований детерминировано
средовыми факторами.
Медико-генетическая профилактика. К числу других
направлений профилактики злокачественных новообразований относится
медико-генетическая профилактика путем выделения семей с наследуемыми
предрасположенностями к предопухолевым и опухолевым заболеваниям, лиц с
хромосомной нестабильностью и организации мероприятий по снижению опасности
возможного действия на них канцерогенных факторов. В механизмах наследственной
предрасположенности часто решающее значение имеют эндокринные факторы. Так,
дочери матери, больной раком молочной железы, имеют риск заболеть этим
заболеванием в 4,5 раза выше, чем их сверстницы, не имеющие такого анамнеза.
Сестры больной раком молочной железы, если их мать страдала этим же
заболеванием, имеют вероятность возникновения такой опухоли в 47-51 раз выше,
чем их сверстницы с неотягощенной наследственностью. Женщинам, имеющим
отягощенный анамнез относительно рака молочной железы, не рекомендуется грудное
вскармливание детей, употребление кофе, прием некоторых медикаментов, особенно
резерпина и группы раувольфии. Доброкачественные опухоли молочной железы среди
женщин, имеющим это заболевание в семейном анамнезе, встречаются в 4 раза чаще.
Иммунобиологическая профилактика проводится
путем выделения людей или формирования групп с иммунологической
недостаточностью и организации мероприятий по ее коррекции или устранении
одновременно с защитой от возможных канцерогенных воздействий. Это направление
приобретает особо важное значение при продолжительной иммунодепрессивной
терапии после гомологичной пересадки органов и тканей, а также лечении
аутоиммунных заболеваний.
Эндокринно-возрастная профилактика проводится
путем выявления и коррекции дисгормональных состояний и возрастных нарушений
гомеостаза, способствующих возникновению и развитию злокачественных
новообразований.
Теоретическая эффективность каждого из этих
направлений оценивается снижением онкологической заболеваемости на 10%.
Вторичная профилактика злокачественных
новообразований. Вторичная профилактика злокачественных новообразований
представляет собой комплекс мероприятий, направленных на выявление
предопухолевых заболеваний и состояний, а также раннюю диагностику
онкологических заболеваний, что обеспечивает наиболее высокую эффективность их
хирургического (и других видов противоопухолевого) лечения. В осуществлении
этого вида профилактики большое значение имеет применение цитологических,
гистологических, эндоскопических, рентгенологических и других специальных
методов обследования, так как простой визуальный осмотр и применение обычных
методов врачебного обследования без применения перечисленных выше методик
недостаточно эффективны для выявления ранних стадий онкологических заболеваний.
В СССР визуальному обследованию и профилактическим осмотрам ежегодно
подвергалось около 100 млн. человек, а выявленные при этих осмотрах (без
применения специальных дополнительных методов обследования) больные
злокачественными новообразованиями составляли всего лишь около 7% от общего
числа первично диагностируемых заболеваний такого рода. Однако учитывая значимость
и возрастающую тенденцию роста онкологической заболеваемости это направление
вторичной профилактики не утратило своего положительного значения. Методы
коллективной профилактики должны реализоваться прежде всего путем строгого
соблюдения положений соответствующих нормативных и регламентирующих документов
об охране здоровья населения, а методы индивидуальной профилактики также и
путем систематической пропаганды необходимых медицинских знаний и создания
условий для здорового образа жизни.
В индивидуальной профилактике сохраняет свое
большое значение диспансеризация, при проведении которой всеми
врачами-специалистами должна проявляться онкологическая настороженность, т.е.
исключение бластоматозной природы заболевания и опухолевых процессов
обследуемой области, включая при необходимости и применение специальных методов
исследования[18]. Такой образ действия в процессе диспансеризации в достаточной
степени обеспечивает своевременное выявление ранних стадий онкологических
заболеваний и лиц с повышенным риском их возникновения, что позволяет
формировать группы риска. Лица, отнесенные к этим группам, должны подвергаться
специальным методам исследования (в зависимости от показаний - цитологическим,
гистологическим, эндоскопическим, УЗИ, рентгенологическим, лабораторным и т.д.)
с соблюдением строгой периодичности их проведения. В такие группы, помимо
определенных соответствующими положениями, встречаются также страдающие
некоторыми формами анемии, зобом, ожирением II-III ст., хроническими
заболеваниями легких и желудочно-кишечного тракта, прежде всего воспалительной
природы, в возрасте старше 40 лет. В эти группы включаются курильщики и
страдающие алкогольной зависимостью, лица имеющие кровных родственников больных
или болевших онкологическими заболеваниями, прежде всего раком легкого, раком
желудка, толстой и прямой кишки, раком молочной железы и др. В группы риска
должны включаться также лица, у которых обнаружена триада: гипертоническая
болезнь, диабет, ожирение.
Одним из наиболее информативных методов,
подтверждающих риск заболевания злокачественными новообразованиями, стали
опухолевые маркеры крови. Метод основан на выявлении в крови белков,
вырабатываемых раковыми клетками. При разных видах злокачественных
новообразований набор этих «меток» различен. Онкомаркеры дают информацию о
наличии опухоли на той стадии, когда традиционными методами ее сложно
обнаружить.
Третичная профилактика злокачественных
новообразований. Третичная профилактика рака - предупреждение возникновения, а
также раннее выявление и лечение возможных рецидивов заболевания в период после
завершения основного курса лечения.
Третичная профилактика рака, по сути, есть
заключительный этап вторичной и переход к решению задач, непосредственно
связанных с лечением и реабилитацией онкологического больного, выявленного на
предыдущих этапах.
В рамках подсистемы «третичная профилактика»
окончательно формируется модель новой системы, в которой фактором, образующим
систему, является не заболеваемость, а смертность от рака. Компоненты,
связанные с заболеваемостью, составляют важную часть (подсистему) новой
системы, ее исходную количественную и качественную величину[8].
Создание современной лечебной и диагностической
базы онкологической службы, развитие специализированных ее подразделений,
подготовка кадров врачей-онкологов различных специальностей - все это является
неотъемлемой составной частью третичной профилактики рака. Конечным результатом
функционирования подсистемы «третичная профилактика» должно быть сохранение или
продление жизни онкологическим больным. Критериями оценки эффективности
деятельности подсистемы являются снижение, как одногодичной летальности, так и
улучшение отдаленных результатов лечения.
Диспансеризация онкологических больных является
важным элементом, обеспечивающим эффективность третичной профилактики рака.
Вследствие особенностей развития опухолевого
процесса сам больной далеко не всегда может определить начало рецидива болезни
после специального лечения. Больной, как правило, обращается к врачу за помощью
только тогда, когда произошло значительное прогрессирование болезни.
В этой ситуации эффективное лечение рецидива
становится если не невозможным, то затруднительным. Поэтому во многих странах
существует активная диспансеризация онкологических больных. Она опирается на
стандартизованные раковые регистры, руководствующиеся одними и теми же
основополагающими принципами, разработанными ВОЗ.
Таким образом, особенности функционирования
подсистемы «первичная профилактика» определяют, с одной стороны, частоту
за6олеваемости злокачественными новообразованиями на определенной территории
вследствие воздействия комплекса факторов окружающей среды и образа жизни
населения, а с другой, - пути управления этим процессом с целью его
предотвращения роста заболеваемости. Снижение смертности от рака в рамках этой
подсистемы всецело зависит от возможности снижения заболеваемости раком
различных органов. Подсистема «вторичная профилактика» решает задачи выявления
и оздоровления больных предопухолевыми заболеваниями и раннее выявление рака.
Подсистема «третичная профилактика» обеспечивает своевременность и качество
диагностики и лечения рака и реабилитацию онкологических больных в процессе их
диспансерного наблюдения. Все это вместе призвано обеспечить снижение
смертности от рака и должно быть основой комплексной государственной программы
профилактики рака.
1.6 Организация
онкологической службы
Онкологическая сеть в Республике Беларусь имеет
следующую структуру: областной, городской, межрайонный онкологические
диспансеры, которые являются основными специализированными
лечебно-профилактическими учреждениями, обеспечивающими организацию и оказание
онкологической помощи населению на закрепленной за ним территорий. НИИ
онкологии и медицинской радиологии им. Н.Н. Александрова является главным
республиканским онкологическим учреждением, выполняющим одновременно функции
областного онкологического диспансера для Минской области[19].
Структура, мощность и штаты онкологического
диспансера устанавливаются местными органами здравоохранения, которые
руководствуются штатными нормативами, с учетом численности закрепленного
населения, уровня и структуры онкологической заболеваемости и
эпидемиологической обстановки в каждом конкретном регионе.
В организационной структуре онкологического
диспансера должны быть предусмотрены диспансерно-поликлиническое отделение,
организационно-методический кабинет [23].
Основными задачами диспансеров являются:
·
организация
онкологической помощи в районе деятельности диспансеров
·
оказание
квалифицированной консультативно-диагностической и специализированной лечебной
помощи (амбулаторной и стационарной) больным со злокачественными
новообразованиями, доброкачественными опухолями и некоторыми предопухолевыми
заболеваниями
·
диспансеризация
больных со злокачественными и предопухолевыми заболеваниями, организация
диспансеризации в онкологических кабинетах и лечебно-профилактических
учреждениях (ЛПУ) обшей лечебной сети
·
методическое
руководство организации онкологической помощи в территориальных больницах и
поликлиниках, женских консультациях и ведомственных ЛПУ
·
осуществление
полного учета больных злокачественными новообразованиями на закрепленной
территории и составление отчетов об онкологической заболеваемости
·
проведение
систематического анализа состояния онкологической заболеваемости и смертности,
причин позднего выявления злокачественных новообразований на закрепленной
территории
·
разработка
планов и мероприятий по улучшению организации онкологической помощи в районе и
снижению уровня запущенности и смертности
·
организация
и проведение учебы врачей общей лечебной сети и среднего медперсонала по
повышению онкологической грамотности и организации онкологической помощи на
местах
·
проведение
анализа эффективности и качества лечебной помощи онкологическим, больным, в
неспециализированных ЛПУ и оказание им консультативной помощи
·
осуществление,
проверки обоснованности установления диагноза злокачественного новообразования
в свидетельствах о смерти, выдаваемых медработниками в учреждениях ЗАГС
·
организация
и проведение санитарно-просветительной работы и противораковой пропаганды среди
населения совместно с центрами здоровья
·
разработка,
освоение и внедрение в практику современных методов и средств организаций,
диагностики и лечения онкологических больных
·
составление
отчетов о своей деятельности и состояний онкологической заболеваемости и
смертности на закрепленной территорий по утвержденным формам и в установленные
законом сроки.
Важным звеном онкологической помощи населению
являются онкологические кабинеты, которые создается в структуре центральных
районных больниц (поликлиник) и центральных городских больниц при отсутствии на
территорий города онкологического диспансера.
За последние годы важное место в деле борьбы со
злокачественными опухолями заняли смотровые кабинеты, организующиеся в каждой
районной (городской) поликлинике и работающие в тесном контакте с районными
онкологическими кабинетами. Смотровой кабинет осуществляет проведение
профилактического осмотра пациентов на предмет раннего выявления предопухолевых
заболеваний и опухолей, относящихся к визуально доступным локализациям. При
выявлении патологии осуществляет направление больных к соответствующему
специалисту для уточнения диагноза и организации лечения. Проводит учет и
регистрацию профилактических осмотров и результатов цитологических исследований.
Кроме того, в онкологических учреждениях
создаются экспертные комиссии по раннему выявлению онкологических
заболеваний[22], которые осуществляют разбор запушенных случаев (III
стадии визуальных форм и всех случаев IV
стадии) онкологических заболеваний с использованием данных протоколов
запущенности, амбулаторных карт, историй болезни и другой медицинской
документации. Экспертная комиссия проводит анализ причин диагностических
ошибок, повлекших несвоевременную диагностику злокачественных опухолей, и выносит
предложения по их недопущению. Результаты обсуждения доводятся территориальным
диспансерам и руководителям ЛПУ, в которых имела место запущенность[24,25].
смертность заболеваемость онкологический зависимость
2. ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
2.1 Объекты
исследования
Материалом для исследования были официальные
статистические данные Министерства здравоохранения Республики Беларусь и данные
Белорусского канцер-регистра.
В настоящей работе проведен анализ
заболеваемости и смертности населения Республики Беларусь онкологическими
заболеваниями различной локализации за период с 2000 г. по 2011 г.
2.2 Расчет интенсивных
показателей
Показатель частоты, уровня, распространенности
процессов, явлений, совершающихся в определенной среде. Он показывает, как часто
встречается изучаемое явление в среде, которая его продуцирует (заболеваемость,
смертность, рождаемость и т.д.).
Интенсивные показатели используются как для
сравнения, сопоставления динамики частоты изучаемого явления во времени, так и
для сравнения, сопоставления частоты этого же явления в один и тот же
промежуток времени, но в различных учреждениях, на различных территориях и т.д.
Для расчета интенсивного показателя необходимо
иметь данные об абсолютном размере явления и среды, его продуцирующей. Абсолютное
число, характеризующее размер явления, делится на абсолютное число,
показывающее размер среды, внутри которой произошло данное явление, и
умножается на 100, 1000 и т.д.
Таким образом, способ получения интенсивного
показателя выглядит следующим образом:
Интенсивный число случаев заболеваний
показатель
= х 10 000
заболеваемости средняя численность населении
2.3 Расчет экстенсивных
показателей
Это показатель удельного веса, доли части в
целой совокупности, показатель распределения совокупности на составляющие ее
части, т.е. показатель структуры.
Для его расчета необходимо иметь данные о
численности всей совокупности и составляющих ее частях (или отдельной части
этой совокупности). Рассчитывается обычно в процентах, где совокупность в целом
принимается за 100%, а отдельные части - за "X".
Способ получения экстенсивной величины выглядит
следующим образом:
Удельный вес заболевших число заболевших данной
нозологией
данной нозологией =
C
100
в общем количестве заболевших число всех
заболевших
Таким образом, для получения экстенсивного
показателя нужна совокупность и ее составные части или отдельная часть.
Экстенсивный показатель отвечает на вопрос, сколько процентов приходится на
каждую конкретную часть совокупности. В зависимости от того, что характеризуют
экстенсивные показатели, их называют:
показатели удельного веса части в целом,
например, удельный вес гриппа среди всех заболеваний;
показатели распределения или структуры
(распределение всей совокупности зарегистрированных врачом заболеваний за год
на отдельные заболевания).
Это показатель статики, т.е. с его помощью можно
анализировать конкретную совокупность в конкретный момент. По экстенсивным
показателям нельзя сравнивать различные совокупности - это приводит к
неправильным, ошибочным выводам.
2.4 Метод анализа
многолетней тенденции заболеваемости
.4.1 Расчет темпа
прироста
Темп прироста рассчитывается как отношение между
абсолютным приростом данного периода и абсолютным уровнем предшествующего
периода и выражается в процентах.
Средний абсолютный прирост вычисляют по формуле:
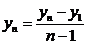
где 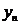 и
и 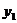 -
показатели конечного и начального периодов соответственно,
-
показатели конечного и начального периодов соответственно,  - число периодов.
- число периодов.
Средний темп роста показывает
среднюю скорость изменения уровня в динамическом ряду. Для определения среднего
темпа роста следует вычислять среднюю геометрическую.
Средний темп роста как правило
выражают в процентах и определяют следующим образом:
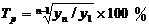
где 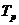 -
средний темп роста,
-
средний темп роста, 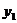 и
и 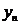 - показатели начального и
конечного периодов соответственно,
- показатели начального и
конечного периодов соответственно,  -
число членов динамического ряда.
-
число членов динамического ряда.
При логарифмировании это выражение
примет вид:
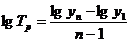
После антилогарифмирования и
умножения на 100% определяется средний темп роста.
Для определения среднегодового темпа
прироста 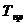 используется
следующая формула:
используется
следующая формула:
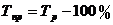
2.4.2
Линейный регрессионный анализ для определения тенденций заболеваемости
Для выявления тенденций заболеваемости строились
уравнения линейной регрессии по следующей формуле :
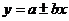
где: у - теоретический (расчетный) уровень
заболеваемости населения;
x - порядковый номер
года исследования;
а - пороговый уровень заболеваемости;
b - коэффициент,
указывающий на величину возрастания или убывания заболеваемости населения.
Для оценки коэффициентов а и b
используется метод наименьших квадратов. Когда имеется только одна независимая
переменная x, коэффициенты a
и b вычисляются по следующим формулам :
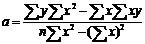

где n -
количество лет наблюдения.
Коэффициент детерминированности R2
показывает, насколько хорошо уравнение, полученное с помощью регрессионного
анализа, объясняет взаимосвязи между переменными. При этом сравниваются
фактические значения y и значения, получаемые из уравнения прямой. Для каждой
точки вычисляется квадрат разности между прогнозируемым значением y и
фактическим значением y. Сумма этих квадратов разностей называется остаточной
суммой квадратов. Затем подсчитывается сумма квадратов разностей между
фактическими значениями y и средним значением y, которая называется общей
суммой квадратов. Чем меньше остаточная сумма квадратов по сравнению с общей
суммой квадратов, тем больше значение коэффициента детерминированности R2.
Коэффициент детерминированности
нормируется от 0 до 1. Если он равен 1, то имеет место полная корреляция с
моделью, т.е. нет различия между фактическим и оценочным значениями y. В
противоположном случае, если коэффициент детерминированности равен 0, то
уравнение регрессии неудачно для предсказания значений y.
В зависимости от величины
коэффициента детерминированности оценивается устойчивость ряда :
- от 0,7 до 1 - ряд с выраженной
устойчивой тенденцией;
- от 0,4 до 0,69 - с неустойчивой
тенденцией;
от 0 до 0,39 - ряд с отсутствием
тенденции или неясной тенденцией.
2.5
Методические подходы к оценке зависимости смертности и заболеваемости
.5.1
Расчет коэффициента соотношения смертность/заболеваемость
Интенсивные показатели
заболеваемости и смертности отражают частоту изучаемых явлений в популяции, но
не позволяют соотнести сами явления между собой. Расчет коэффициента
смертность/заболеваемость расширяет возможности для анализа. Данный подход
использован нами при оценке исходов новообразований. Этот показатель можно
рассчитывать в виде индекса смертность/заболеваемость, при этом, чем меньше
величина, тем выше выживаемость заболевших. Индекс может быть выражен в
процентах (смертность/заболеваемость х 100). Показатель отражает вероятность
умереть (по отношению к общему числу заболевших лиц). Если из 100 вычесть
значение коэффициента в процентах, то получаем процент выживаемости.
2.5.2
Индекс подобия
Ввиду того, что при
новообразованиях контингенты больных накапливаются, а больные, во многом
благодаря ранней диагностике и качеству лечения, не умирают в первый год с
момента постановки диагноза, интерес представляет относительная интенсивность
смертности по отношению к общей заболеваемости или отношение числа умерших к общему
числу больных (индекс подобия). Показатель общей заболеваемости (prevalence)
рассчитывается как совокупность лиц, взятых на учет в связи с впервые в жизни
установленным диагнозом злокачественного новообразования, и лиц, состоящих на
учете по поводу злокачественных новообразований, впервые выявленных в
предыдущие годы, отнесенных к среднегодовой численности населения.
.5.3 Индекс накапливаемости
Об изменении результативности работы
онкологической службы в республике можно судить и по индексу накапливаемости.
3. РЕЗУЛЬТАТЫ СОБСТВЕННЫХ
ИССЛЕДОВАНИЙ
3.1. Анализ
заболеваемости злокачественными новообразованиями населения Республики Беларусь
с 2000 по 2011 г.г.
На протяжении многих лет в Республике Беларусь
наблюдается постоянный рост общей онкологической заболеваемости.
За период 2000-2011 гг. абсолютное число вновь
выявленных случаев заболеваний возросло с 33 613 в 2000 г. до 42316 в 2011 г.,
т.е. на 26,8%. Злокачественные новообразования, составляющие 0.5% в общей
структуре первичной заболеваемости населения, являются причиной смерти в 13,7 %
от общей смертности населения и стоят на втором месте, уступая лишь смертности
от болезней системы кровообращения.
На рисунке 1 приведена динамика интенсивных
показателей заболеваемости злокачественными новообразованиями среди населения
Республики Беларусь за изученный период времени.
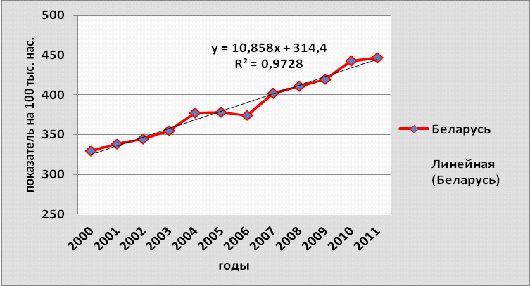
Рисунок 3.1- Динамика заболеваемости
злокачественными новообразованиями населения Беларуси, 2000-2011гг.
Динамика заболеваемости населения Республики
Беларусь злокачественными новообразованиями имеет четкую устойчивую тенденцию к
увеличению. Грубые интенсивные показатели (на 100 тыс. населения) возросли на
35,4 % (329,7 - в 2000 г. до 446,7- в 2011). Прирост грубого интенсивного
показателя заболеваемости в значительной мере определен неблагоприятным
направлением демографических процессов в Беларуси, обусловливающим ”постарение”
населения. Коэффициенты детерминированности (R2),
полученные в результате анализа динамических рядов заболеваемости населения по
параболе первого порядка позволили достоверно определить направленность
тенденции заболеваемости, где за изучаемый период выявлена тенденция к
увеличению показателей заболеваемости злокачественными новообразованиями.
На рисунках 3.2-3.8 приведена динамика
интенсивных показателей заболеваемости злокачественными новообразованиями по
областям Республики Беларусь и г. Минска за изученный период времени.
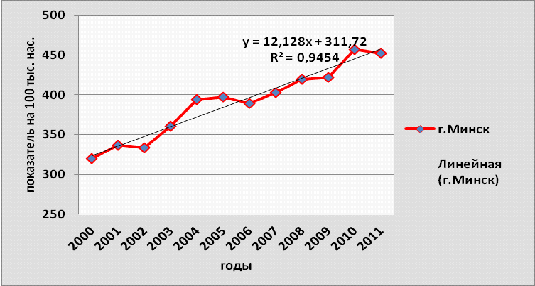
Рисунок 3.2- Динамика заболеваемости
злокачественными новообразованиями населения г. Минска, 2000-2011гг.
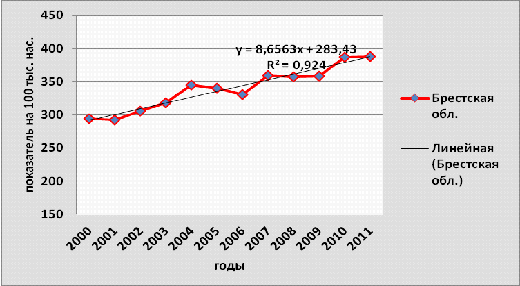
Рисунок 3.3- Динамика заболеваемости
злокачественными новообразованиями населения Брестской области, 2000-2011гг.
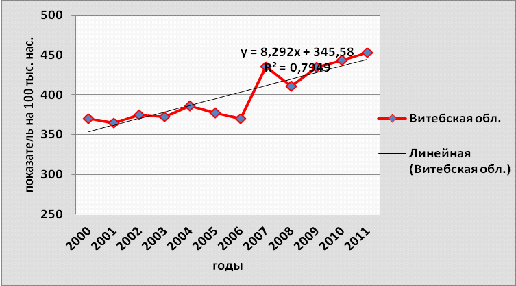
Рисунок 3.4- Динамика заболеваемости
злокачественными новообразованиями населения Витебской области, 2000-2011гг.
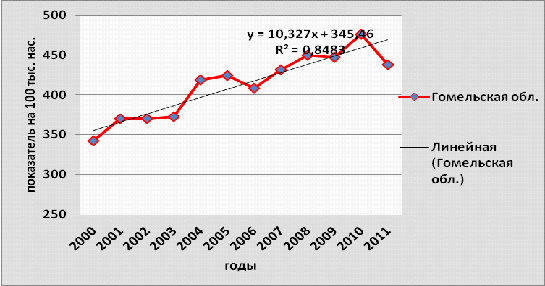
Рисунок 3.5- Динамика заболеваемости
злокачественными новообразованиями населения Гомельской области, 2000-2011гг.
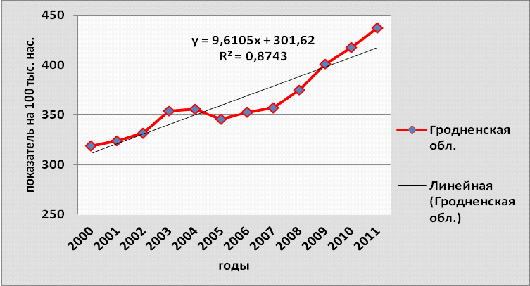
Рисунок 3.6- Динамика заболеваемости
злокачественными новообразованиями населения Гродненской области, 2000-2011гг.
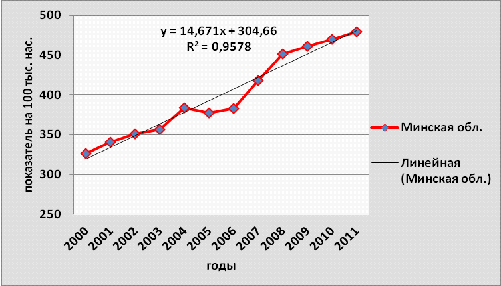
Рисунок 3.7- Динамика заболеваемости
злокачественными новообразованиями населения Минской области, 2000-2011гг.
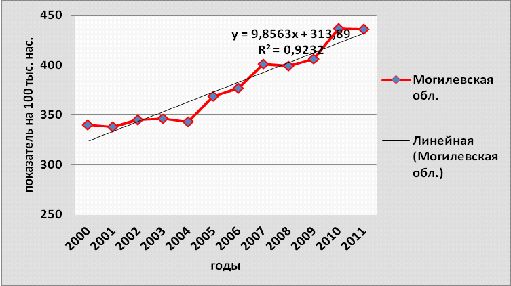
Рисунок 3.8- Динамика заболеваемости
злокачественными новообразованиями населения Могилевской области, 2000-2011гг.
Динамика заболеваемости населения
злокачественными новообразованиями по областям Республики Беларусь и г. Минска
имеет тенденцию к увеличению. Имеются определенные различия общей
онкологической заболеваемости в областях республики. Грубые интенсивные
показатели (на 100 тыс. населения) сильно возросли в г. Минске на 41,3%, в
Минской области на 47%, менее выражено возросли в Брестской и Могилевской
областях.
Имеются также значительные различия в
показателях заболеваемости у городского и сельского населения (рис.3.9).
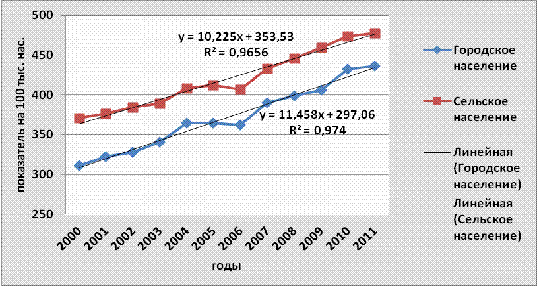
Рисунок 3. 9- Динамика заболеваемости городского
и сельского населения Республики Беларусь злокачественными новообразованиями ,
2000-2011гг.
Из-за значительных различий в возрастной
структуре городского и сельского населения Беларуси грубый интенсивный
показатель общей онкологической заболеваемости за весь десятилетний период на
10 -24% выше у сельского населения. Заболеваемость злокачественными
новообразованиями городского населения за изученный период увеличилась на 40%,в
то время как заболеваемость среди сельского населения на протяжении всех 5 лет
была практически стабильной, а начиная с 2007 года резко возросла.
Анализ заболеваемости злокачественными
новообразованиями населения Республики Беларусь дифференцировано по полу
показал, что в период с 2000-2011 гг. заболеваемость мужского населения в
среднем превышала на 1,2 раза заболеваемость женского, но при этом отмечался
рост заболеваемости как у мужчин, так и у женщин (рисунок 3.10).
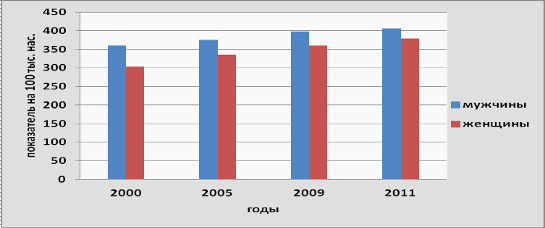
Рисунок 3.10- Уровень заболеваемости мужского и
женского населения в Республике Беларусь за 2000, 2005, 2009, 2011 года.
Структура онкологической заболеваемости в разные
периоды времени существенно различалась. Это связано в первую очередь со значимыми
различиями во временной динамике частоты опухолей отдельных локализаций.
В настоящее время структура онкологической
заболеваемости может быть представлена следующим образом ( рисунок 3.11, 3.12).
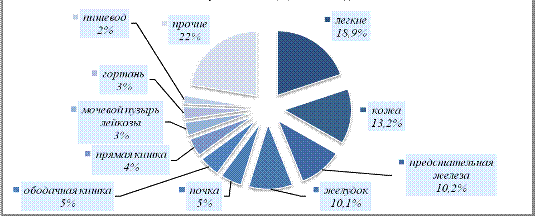
Рисунок 3.11- Структура заболеваемости мужского
населения Республики Беларусь злокачественными новообразованиями (%) за 2011
год.
Первые места в структуре заболеваемости
злокачественными новообразованиями мужского населения Республики Беларусь
распределены: рак легкого (18,9%), за ним следует рак кожи (13,2%),
предстательной железы (10,2%), желудка (10,1%). Менее 1% составляют болезнь
Ходжкина (0,8%), рак губы (0,7%),множественная миелома (0,7%), опухоли костей
(0,3%) и другие.
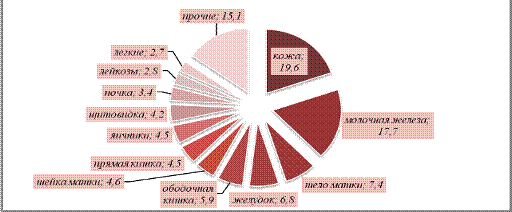
Рисунок 3.12 - Структура заболеваемости женского
населения Республики Беларусь злокачественными новообразованиями (%) за 2011
год.
Анализ повозрастных показателей заболеваемости
населения Республики Беларусь злокачественными
новообразованиями показал, что рост
онкозаболеваемости отмечается в более старших возрастных группах, начиная после
50 лет. Пик заболеваемости приходится на возрастную группу 75-79 лет в 2011
году. Высокий уровень заболеваемости отмечается в группах 65-69, 70-74, 80-84
(рисунок 3.13).
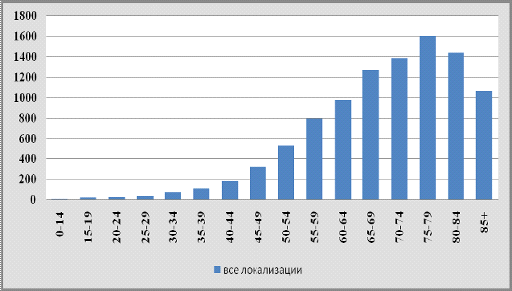
Рисунок 3.13- Повозрастные показатели
заболеваемости населения Беларуси злокачественными новообразованиями за 2011 г.
(на 100тыс. населения соответствующей возрастной группы)
На конец 2011 г. состояли на диспансерном учете
в Республике Беларусь 252671 пациентов, что в 8 раз больше числа заболевших в
2000 году. Численный состав больных, состоявших на учете на конец 2011 г. по
локализациям, представлен в табл. 3.1.
Таблица 3.1- Численный состав больных, состоявших
на учете на конец 2011 г., по локализациям
|
Локализация
|
Число
больных
|
Удельный
вес, %
|
|
Молочная
железа
|
38088
|
15,07
|
|
Кожа
|
30004
|
11,87
|
|
Тело
матки
|
15531
|
6,15
|
|
Щитовидная
железа
|
14938
|
5,91
|
|
Желудок
|
12082
|
4,78
|
|
Шейка
матки
|
12945
|
5,12
|
|
Ободочная
кишка
|
9872
|
3,91
|
|
Почка
|
9605
|
3,80
|
|
Легкие
|
9067
|
3,59
|
|
Прямая
кишка
|
9025
|
3,57
|
|
Предстательная
железа
|
7799
|
3,09
|
|
Мочевой
пузырь
|
6277
|
2,48
|
|
Яичники
|
5747
|
2,27
|
|
Лимфома
Ходжкина
|
3833
|
1,52
|
|
Неходжкинская
лимфома
|
2810
|
1,11
|
|
ЦНС
|
2346
|
0,93
|
|
Прочие
|
62702
|
24,82
|
|
всего
|
252671
|
100
|
Ведущими локализациями в общей (оба пола)
структуре больных злокачественными новообразованиями, состоящих на диспансерном
учете в Республике Беларусь являются: молочная железа(15,07%), кожа(11,87%),
тело матки(6,15%), щитовидная железа(5,91%) желудок(4,78%).
3.2 Анализ смертности
населения Республики Беларусь от злокачественных новообразований
Показатели смертности от
злокачественных новообразований представляют интерес прежде всего в плане
интегральной оценки эффективности организации противораковой борьбы, поскольку
во многом зависят как от состояния своевременной диагностики опухолей, так и от
организации лечебной работы и ее результатов. В структуре смертности населения
республики злокачественные новообразования занимают второе место, уступая только
сердечно-сосудистым заболеваниям.
В последние годы во многих странах отмечается
снижение смертности от злокачественных новообразований. Проблема снижения
смертности от рака - одна из наиболее актуальных, стоящих перед медицинской
наукой и здравоохранением в настоящее время.
В последнее десятилетие наблюдалась стабилизация
показателей смертности от злокачественных новообразований, однако рассматривая
динамику с 2000-2011 гг. в целом мы получаем умеренно выраженное снижение
смертности от злокачественных патологий так как, начиная с 2003 года,
отмечается четкое снижение показателей смертности по сравнению с предыдущими
годами.
Грубые интенсивные показатели (на 100 тыс.
населения) снизились на 5,3 % с 199,1- в 2000 году до 188,5- в 2011 году
(рисунок 3.14).
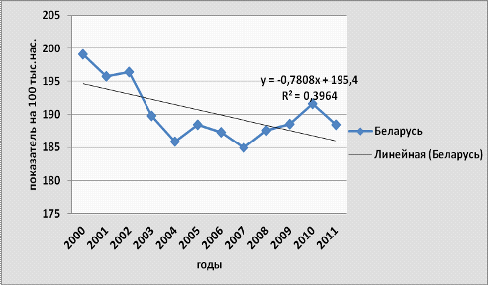
Рисунок 3.14-Динамика смертности от
злокачественных новообразований в Республике Беларусь,2000-2011 гг.
Имеются определенные различия смертности
населения от злокачественных новообразований в областях республики. Грубые
интенсивные показатели (на 100 тыс. населения) значительно снизились в
Витебской области на 10,6%, Гродненской области на 13,8%, в Минской области на
7%, менее выражено снижение отмечено в других областях и г. Минске (рисунок
3.15-3.22).
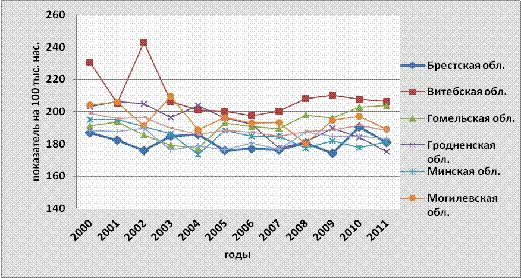
Рисунок 3.15-Динамика смертности от
злокачественных новообразований в Республике Беларусь и по областям, 2000-2011
гг.
Коэффициенты детерминированности (R2)
, полученные в результате анализа динамических рядов смертности населения по
параболе первого порядка не позволили достоверно определить направленность
тенденции смертности в областях республики, кроме Гродненской(R2
=0,77 ) и Минской (R2 =0,49),
где за изучаемый период выявлена тенденция к устойчивому снижению показателей
смертности злокачественными новообразованиями (рисунок 3.19,3.20).
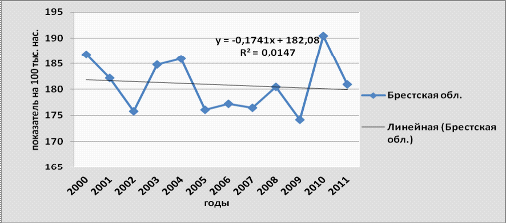
Рисунок 3.16-Динамика смертности от
злокачественных новообразований в Брестской области, 2000-2011 гг.

Рисунок 3.17-Динамика смертности от
злокачественных новообразований в Витебской области, 2000-2011 гг.
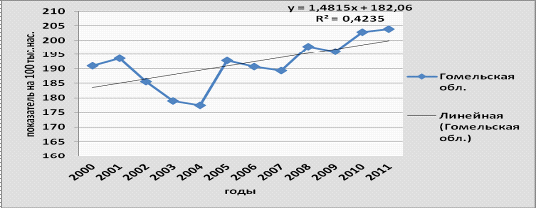
Рисунок 3.18-Динамика смертности от
злокачественных новообразований в Гомельской области, 2000-2011 гг.
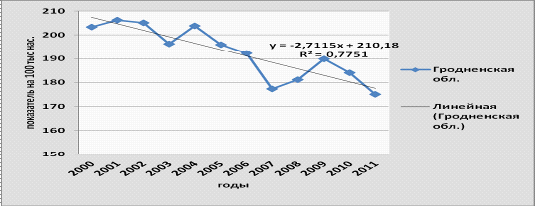
Рисунок 3.19-Динамика смертности от
злокачественных новообразований в Гродненской области, 2000-2011 гг.
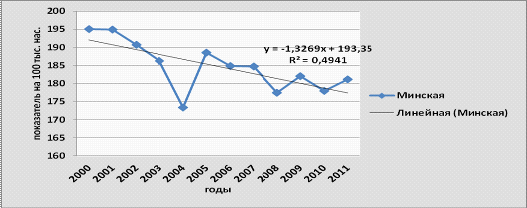
Рисунок 3.20-Динамика смертности от
злокачественных новообразований в Минской области, 2000-2011 гг.

Рисунок 3.21-Динамика смертности от
злокачественных новообразований в Могилевской области, 2000-2011 гг.
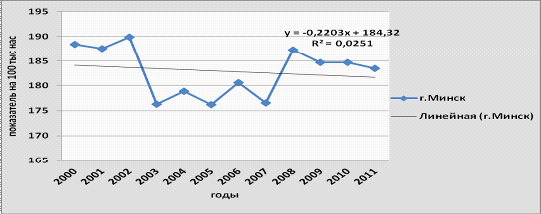
Рисунок 3.22-Динамика смертности от
злокачественных новообразований в г. Минске, 2000-2011 гг.
Смертность сельского населения выше, чем
городского, но при этом в последние годы отмечается сближение показателей
смертности городского и сельского населения за счет снижения уровня смертности
среди сельских и стабилизации процесса среди городских жителей. Грубые
интенсивные показатели (на 100 тыс. населения) увеличились у городского
населения на 0,6% (175.8- в 2000 до 176.9- в 2011 году), у сельского населения
на 11.2% (252.6- в 2000 до 224.2- в 2011 году) (рис.3.23).
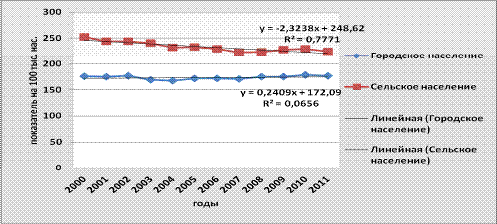
Рисунок 3.23- Динамика смертности от
злокачественных новообразований городского и сельского населения Республики
Беларусь, 2000-2011 гг.
Анализ смертности от злокачественных
новообразований населения Республики Беларусь дифференцировано по полу показал
выраженное снижение интенсивных показателей смертности, как у мужчин, так и
среди женщин. Коэффициент детерминированности R2
соответственно 0,7791
и 0,8009 (рис. 3.24.)

Рисунок 3.24- Динамика смертности от
злокачественных новообразований женского и мужского населения Республики
Беларусь, 2000-2011 гг.
В Республике Беларусь в
последние годы отмечается снижение смертности от злокачественных
новообразований: стандартизованные показатели (мировой стандарт, на 100 тыс.
населения) снизились среди мужчин с 251,3 в 2000 г. до 225,6 в 2011 г., у
женщин - с 155,0 до 136,1 соответственно.
Рост смертности от
злокачественных новообразований отмечается в более старших возрастных группах,
начиная после 50 лет. Пик смертности в 2011 году приходится на возрастную
группу 75-79 лет . Высокий уровень смертности отмечается в группах 65-69,
70-74, 80-84 лет (рисунок 3.25).
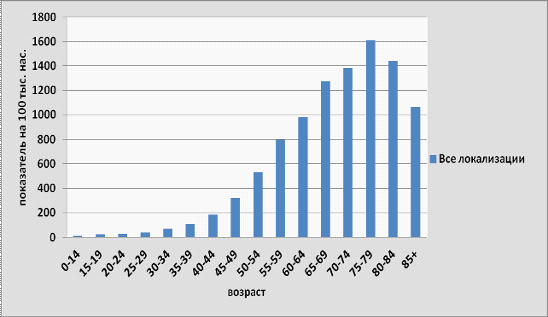
Рисунок 3.25- Повозрастные показатели смертности
населения Беларуси от злокачественных новообразований за 2011г.
3.3
Соотношение смертности и заболеваемости населения Республики Беларусь при
злокачественных новообразованиях различной локализации
Интенсивные показатели
заболеваемости и смертности отражают частоту изучаемых явлений в популяции, но
не позволяют соотнести сами явления между собой. Расчет коэффициента
смертность/заболеваемость расширяет возможности для анализа. На основании
такого соотношения наиболее распространенные локализации злокачественных
новообразований можно разделить на три группы: локализации с хорошим прогнозом
(соотношение составляет 0,3 и менее), с относительно хорошим прогнозом (от 0,3
до 0,5), с плохим прогнозом (более 0,5).
В табл. 3.2 приведены данные о
динамике коэффициента смертность/заболеваемость или прогностический индекс,
которые являются свидетельством улучшения исходов лечения новообразований в
Республике Беларусь, что обусловлено более своевременным выявлением больных в
результате проведения целевых медицинских осмотров и большей информативностью
используемых диагностических методов, а также улучшением качества лечения
больных.
Таблица 3.2- Динамика
коэффициента смертность/заболеваемость в регионах Республики Беларусь в
2000-2011 гг.
|
Регион
|
Годы
|
|
2000
|
2003
|
2007
|
2009
|
2011
|
|
г.
Минск
|
-
|
0,6
|
0,53
|
0,45
|
0,4
|
|
Брестская
область
|
0,69
|
0,67
|
0,63
|
0,52
|
0,48
|
|
Витебская
область
|
0,7
|
0,67
|
0,6
|
0,55
|
0,46
|
|
Гомельская
область
|
0,65
|
0,62
|
0,56
|
0,49
|
0,43
|
|
Гродненская
область
|
0,73
|
0,67
|
0,65
|
0,58
|
0,42
|
|
Минская
область
|
0,69
|
0,61
|
0,6
|
0,51
|
0,39
|
|
Могилевская
область
|
0,61
|
0,74
|
0,61
|
0,54
|
0,44
|
|
Республика
Беларусь
|
0,68
|
0,64
|
0,59
|
0,51
|
0,43
|
В таблице 3.3 приведены значения
прогностического индекса - соотношение числа умерших от злокачественных
новообразований различной локализации и числа заболевших в динамике.
Таблица 3.3-Соотношение числа
умерших и числа заболевших (прогностический индекс) при злокачественных
новообразованиях различной локализации
|
Локализация
опухоли
|
2000
|
2005
|
2009
|
2011
|
|
Губа
|
0,32
|
0,38
|
0,31
|
0,3
|
|
Полость
рта и глотки
|
0,81
|
0,78
|
0,75
|
0,71
|
|
Пищевод
|
0,96
|
0,89
|
0,93
|
0,8
|
|
Желудок
|
0,82
|
0,86
|
0,76
|
0,7
|
|
Ободочная
кишка
|
0,69
|
0,64
|
0,59
|
0,51
|
|
Прямая
кишка
|
0,7
|
0,72
|
0,64
|
0,55
|
|
Гортань
|
0,73
|
0,82
|
0,7
|
0,92
|
|
Легкое
|
0,84
|
0,84
|
0,8
|
0,77
|
|
Кожа
|
0,08
|
0,07
|
0,03
|
0,03
|
|
Молочная
железа
|
0,49
|
0,5
|
0,36
|
0,3
|
|
Шейка
матки
|
0,65
|
0,59
|
0,47
|
0,35
|
|
Тело
матки
|
0,41
|
0,4
|
0,26
|
0,2
|
|
Яичники
|
0,77
|
0,68
|
0,65
|
0,61
|
|
Предстательная
железа
|
0,6
|
0,58
|
0,4
|
0,3
|
|
Мочевой
пузырь
|
0,56
|
0,56
|
0,42
|
0,35
|
|
Щитовидная
железа
|
0,15
|
0,1
|
0,07
|
0,05
|
|
Все
локализации
|
0,68
|
0,61
|
0,51
|
0,43
|
Ввиду того, что при
новообразованиях контингенты больных накапливаются, а больные, во многом
благодаря ранней диагностике и качеству лечения, не умирают в первый год с
момента постановки диагноза, интерес представляет относительная интенсивность
смертности по отношению к общей заболеваемости или отношение числа умерших к
общему числу больных (индекс подобия).
В 1990 г. в республике в
среднем умерло 16,6% общей численности контингента онкологических больных; в
1995 г. - 14,9% (официальные статистические данные) ; в 2000 г. - 14,5%; в 2011
г. - 6,6%. (таблица 3.4.) Таким образом, вероятность умереть от злокачественных
новообразований уменьшилась за 21 год на 46,2%, что подтверждает факт улучшения
деятельности системы здравоохранения и онкологической службы. Территориальные различия
индекса подобия в 2000, 2009 и 20011гг. представлены в таблице 3.4.
Приведенные данные
свидетельствуют, что в 2000 г. диапазон колебаний вероятности умереть от
новообразований составлял от 11,5% (Гомельская область) до 17,3% (Минская
область). В 2011 г., спустя 11 лет, вероятность умереть от той же патологии
снизилась во всех регионах, а диапазон колебаний составил от 6,1% (Гомельская
область) до 8,1% (Гродненская и Брестская области). Процент улучшения данного
показателя был самым высоким в Минской области (61,8), а наиболее низким - в г.
Минске и Гомельской области (46,9%).
Таблица 3.4.- Территориальные показатели
относительной интенсивности (индекс подобия) смертности от новообразований по
отношению к численности контингентов онкологических больных в динамике
(2000-2011 гг.)
|
Регион
|
индекс
подобия
|
%
снижения
|
|
2000
|
2009
|
2011
|
|
|
г.
Минск
|
12,1
|
8,9
|
7
|
42,1
|
|
Брестская
область
|
16,3
|
10,8
|
8,1
|
50,3
|
|
Витебская
область
|
16,2
|
10,1
|
7,7
|
52,4
|
|
Гомельская
область
|
11,5
|
7,7
|
6,1
|
46,9
|
|
Гродненская
область
|
16,3
|
12
|
8,1
|
50,3
|
|
Минская
область
|
17,3
|
9,4
|
6,6
|
61,8
|
|
Могилевская
область
|
12,7
|
8,5
|
6,4
|
49,6
|
|
Республика
Беларусь
|
14,5
|
9,4
|
6,6
|
54,5
|
Об изменении результативности
работы онкологической службы в республике можно судить и по индексу
накапливаемости, представляющий собой отношение численности контингента
онкологических больных к числу впервые зарегистрированных (первичная
заболеваемость). Индекс накапливаемости онкологических больных в Республике
Беларусь представлен в таблице 3.5.
Полученные данные
свидетельствуют, что снижение вероятности умереть у онкологических больных
сказалось на накапливаемости лиц, состоящих на диспансерном учете по поводу
новообразований. С 2000 г. индекс накапливаемости в Республике Беларусь
увеличился с 4,85 до 5,97, то есть на 23%.
Таблица 3.5.- Индекс
накапливаемости онкологических больных в Республике Беларусь в динамике.
|
Год
|
Накопленный
контингент
|
Число
первично заболевших
|
Индекс
накапливаемости
|
|
2000
|
159554
|
32886
|
4,85
|
|
2001
|
165496
|
33782
|
4,9
|
|
2002
|
172317
|
34349
|
5,02
|
|
2003
|
178872
|
34743
|
5,15
|
|
2004
|
187128
|
37016
|
5,06
|
|
2005
|
196031
|
35893
|
5,46
|
|
2006
|
202834
|
36442
|
5,57
|
|
2007
|
212176
|
39003
|
5,44
|
|
2008
|
222107
|
39792
|
5,58
|
|
2009
|
234161
|
39911
|
5,87
|
|
2010
|
242298
|
42034
|
5,76
|
252761
|
42316
|
5,97
|
Выводы
. Заболеваемость населения Республики Беларусь
злокачественными новообразованиями в период с 2000 по 2011 годы возросла на
35,4%. Заболеваемость мужского населения в среднем превышала в 1,2 раза
заболеваемость женского.
. Наиболее высокие показатели заболеваемости в
течение всего периода наблюдения отмечались в Минской области, а с 2003 г. в г.
Минске. Относительно благополучная ситуация по заболеваемости населения
злокачественными новообразованиями складывалась в Брестской и Могилевской
областях.
. Показатели общей онкологической заболеваемости
у сельского населения в разные годы на 10 -24% были выше, чем у горожан, при
относительной их стабильности в динамике. Для городского населения характерна
более выраженная тенденция роста онкозаболеваемости. Максимальный риск заболеть
злокачественными новообразованиями приходился на возрастную группу 75-79 лет.
. За период с 2000 по-2011гг. уровень смертности
от злокачественных новообразований снизился на 5,3%. Отмечено сближение
показателей смертности городского и сельского населения.
. На данном этапе злокачественные новообразования
в целом можно отнести к группе патологий с относительно хорошим прогнозом, на
что указывает соотношение смертности и заболеваемости, являющееся индикатором
«тяжести» онкозаболеваемости. Неблагополучный прогноз имеют две локализации:
злокачественные новообразования органов пищеварения (пищевода, желудка) и рак
легкого. Подтверждением тому является снижение более чем на 50% индекса
подобия.
6. Снижение вероятности умереть
у онкологических больных сказалось на накапливаемости лиц, состоящих на диспансерном
учете С 2000 г. индекс накапливаемости увеличился на 23%.
СПИСОК ИСТОЧНИКОВ
1. Авдеева,
Л.В. Лечение и профилактика онкологических заболеваний Л.В.Авдеева. - Донецк,
1998. - 313 с.
. Анисимов,
В.В. Меланома кожи /В.В. Анисимов, Р.И. Вагнер, А.С. Барчук. - СПб: Питер,
1995. - 151с.
. Боев,
В.М. Химические канцерогены среды обитания и злокачественные новообразования /
В.М.Боев, В.Ф.Куксанов, В.В.Быстрых. - Москва: Медицина, 2002. - 342с.
. Василенко,
В. А. Популярный медицинский справочник / В.А. Василенко.- М. : Вече. - 2007. -
17-18 с.
. Вестник
российского онкологического научного центра им. Н.Н. Блохина. - Москва, 2007. -
77с.
. Ганцев,
Х.Ш. Общая онкология / Х.Ш. Ганцев. - Москва, 2006. - 356с.
. Гарелик,
П.В. Опухоли: Общ. вопр. онкологии / П.В. Гарелик, И.Я. Макшанов, К.Н.
Угляница. - Гродно, 1999. - 107 с.
. Залуцкий,
И.В. Эпидемиология злокачественный новообразований в Беларуси/ И.В. Залуцкий,
Ю.И. Аверкин, Н.А. Артемова. - Минск: Зорны верасень, 2006. - 27 с.
. Зильбер,
Л.А.Вирусогенетическая теория возникновения опухолей/ Л.А. Зильбер. - Москва,
1968. - 112с.
. Злокачественные
новообразования кожи в Алтайском крае / Я.Н.Шойхет [и др.]; под общ. ред. Я.Н.
Шойхет. - Барнаул: АГМУ, 2003. - 163 с.
. Злокачественные
новообразования в Беларуси, 1997―2006
/ Министерство здравоохранения Республики Беларусь, ГУ "Белорусский центр
медицинских технологий и экономики здравоохранения": [статистический
сборник]. - Минск: Белорусский центр медицинских технологий, информатики,
управления и экономики здравоохранения, 2007. - 197 с.
. Злокачественные
новообразования в Беларуси, 2000 - 2011: статистический сборник / Министерство
здравоохранения Республики Беларусь, ГУ "Белорусский центр медицинских
технологий, информатики, управления и экономики здравоохранения". - Минск:
БелЦМТ, 2010. - 193 с.
. Злокачественные
новообразования в Беларуси, 1995 - 2004: статистический сборник / Министерство
здравоохранения Республики Беларусь, ГУ "Белорусский центр медицинских
технологий, информатики, управления и экономики здравоохранения". - Минск:
БелЦМТ, 2005. - 179 с.
. Итоги
научных исследований по комплексной проблеме "Злокачественные
новообразования" за 1971-1975 гг.: (Науч. обзор) / М-во здравоохранения
СССР. Всесоюз. НИИ мед. и мед.-техн. информации. АМН СССР. Науч. совет по
комплексной проблеме "Злокачественные новообразования".... - Москва,
1976. - 62 с.
. Клиническая
онкология: Сб. науч. работ / Мин. гос. мед. ин-т. - Мн.: МГМИ, 1999. - 249с.
. Клиническая
онкология: справ. пособие / Фрадкин С.З., Залуцкий И.В., Аверкин Ю.И. [и др.].;
под ред. С.З.Фрадкина., И.В. Залуцкого - Минск, 2003. - 784 с.
. Лечись,
пока здоров: Профилактика опухолей и кож. болезней. - Киев, 2003. - 293с.
. Манак,
,Б.А. Экономико-географический анализ демографической ситуации и размещение
населения на территории Республики Беларусь / Б.А. Манак, Е.А. Антипова. -
Минск: БГУ.1999. -292с.
. Материалы
III съезда онкологов и
радиологов СНГ // Ч. 1. - Минск: ОДО «Топник», 2004. - 424 с.
. Материалы
III съезда онкологов и
радиологов СНГ // Ч. 2. - Минск: ОДО «Топник», 2004. - 418 с.
. Основные
научные результаты и достижения по проблеме "Злокачественные
новообразования в 1975 году в СССР и за рубежом" / М-во здравоохранения
СССР. Всесоюз. НИИ мед. и мед.-техн. информации.... - Москва, 1976. - 50 с.
. Поляков,
С.М. Злокачественные новообразования в Беларуси 2010-2011 гг. / С.М. Поляков,
Л.Ф. Левин, Н.Г. Шебеко. - Минск: БелЦМТ, 2012.-194 с.
. Преображенский,
В. Профилактика и лечение рака. / В. Преображенский. - Ростов н/Д : БАРО-ПРЕСС,
2000. - 64 с.
. Приказ
МЗ РБ № 205 от 27 августа 2004 г. «О мерах по совершенствованию работы
онкологической службы Республики Беларусь».
. Приказ
МЗ РБ № 75 от 23 апреля 2003 г. «Об утверждении форм учетной медицинской
документации по онкологии и Указаний по их заполнению».
. Приказ
МЗ РБ № 48 от 25 января 2006 г. «О диспансеризации больных онкологическими
заболеваниями».
. Приказ
МЗ РБ № 76А от 12 февраля 2004 г. «Об утверждении протоколов диагностики и
лечения злокачественных новообразований в системе МЗ РБ».
. Профилактика
рака тела матки / И. А. Косенко [и др.]. - Минск: Издательский центр
Белорусского государственного университета, 2007. - 38c.
. Советско-американское
сотрудничество по проблеме "Злокачественные новообразования":
Автореф. дис. на соиск. учен. степени канд. мед. наук:/ Акад. мед. наук. Онкол.
науч. центр. - Москва, 1975. - 20 с.
. Смертность
в Республике Беларусь за 2005-2010 гг.: Официальный статистический сборник. -
Минск: ГУ РНМБ, 2011. - 181 с.
. Статистика
онкологических заболеваний в Республике Беларусь, 1998-2008: Стат. сб. /
Науч.-исслед. ин-т онкологии и мед. радиологии им. Н.Н.Александрова. - Минск.:
БелЦНМИ: НИИ ОМР, 2009. - 162 с.
. Сущевич,
В.В. Анализ многолетней динамики экологически-индуцированной патологии:
Учебно-методическое пособие к практическим занятиям по курсу «Эпидемиология».
В.В. Сущевич. - Мн.: МГЭУ им.А.Д.Сахарова, 2002. - 17-23 с.
. Тризна,
Н. М. Организация онкологической службы и диспансеризация больных со
злокачественными опухолями челюстно-лицевой области: учебно-методическое
пособие / Н. М. Тризна, С. В. Самсонов, Л. Е. Мойсейчик. - Минск: БГМУ, 2010. -
31с.
. Чиссова,
В.И. / Клиническая онкология / В.И. Чиссова, С.Л. Дарьялова ; под ред. В.И.
Чиссова. - Москва, 2000. - 735 с.
. Шабада,
Л.М. Успехи в изучении рака / Л.М. Шабада. - Москва, 2004. - 187с.
. Эпидемиология
и профилактика рака. - Вильнюс: Мокслас, 1984. - 164с.
37. Cancer
Incidence in Five Continents / IARC Publications, Vol. IX, - Lyon, IARC Press,
2007. - 103 p.
. Garabrandt,
D. DDT and related compounds and risk of cancer. / D. Garabrandt, J. Held, B.
Langhols et al. - J.Natl Cancer Inst, 1992. - 84 p.
. Garcia
M. et al. Global cancer facts Figures. - Atlanta,2007.
. Stewart
B.W.,Kleihue s P. WHO cancer report. - Lyon:IARC Press,2003.