Экологические проблемы промышленного производства
Введение
1. Экологические проблемы при производстве тантала и ниобия
.1 Сырье для производства тантала и ниобия
.2 Получение тантала и ниобия
.3 Разложение танталито-колумбитовых концентратов
.4 Разделение тантала и ниобия
.5 Получение металлического тантала и ниобия
.6 Экологические проблемы производства тантала и ниобия
.7 Схемы переработки перовскитового концентрата и утилизации
радионуклидов
.8 Проблемы переработки лопаритового концентрата
.9 Экологические проблемы переработки плюмбомикролитового
концентрата
Выводы по главе
. Экологические проблемы при производстве свинца
.1 Применение
.2 Источники загрязнения окружающей среды свинцом
.3 Загрязнение окружающей среды в процессе получения свинца
.4 Свинцовый аккумулятор - загрязнитель окружающей среды
.5 Выбросы автотранспорта - основной источник загрязнения
окружающей среды ионами свинца
.6 Октановое число
.7 Влияние на организм человека. Общий характер действия.
Токсическое действие свинца
.8 Влияние ионов свинца на почву и растения
.9 Способы борьбы с массовым загрязнением ионами свинца
.10 Совершенствование способов очистки
Выводы по главе
. Экологические проблемы стекольного производства
.1 Виды стекол
.2 Технологический процесс создания стекла
.3 Последние разработки
Выводы по главе
. Экологические проблемы фармоиндустрии
Выводы по главе
Список использованной литературы
Введение
Человек в процессе эволюции стремится облегчить свою жизнь, сделать ее
более комфортабельной и безопасной, менее независящей от окружающего мира.
Блага, создаваемые им, все больше делаю нашу планету искусственной, оставляя
все меньше естественных незатронутых территорий созданные природой. Начиная с
18 века и вплоть до середины 20, человек не задумываясь, строил множество
фабрик и заводов, которые в процессе своей деятельности выбрасывали в
окружающую среду отходы, которые впоследствии негативно сказались на здоровье
всей планеты, тем самым уменьшая популяции многих живых существ и
жизнедеятельности растительного мира. Но лишь только тогда, когда был нанесен
неисправимый ущерб, многие ученые стали задумываться, каким образом можно
уменьшить негативные последствия деятельности человека. В 20 веке появилось
множество организации, которые активно призывают защищать природу, следят за
тем, как крупные предприятия следят за отходами своей деятельности и т. д. С
вступлением человечества в 21 век, и активным развитием наноиндустрии, ученые
попытаются решить многие экологические проблемы. И в действительности в этом
направлении много сделано. К примеру, полученные наночастицы TiO2 нанесенные на оксидную матрицу под
действием энергии света, кислорода из воздуха и воды образуют свободные
радикалы, которые способны разрушить органические и неорганические загрязнители
атмосферы. Таким образом добавки диоксида титана снижают концентрации оксидов
азота, серы аммиака, жиоксида углерода, летучих органических соединений, что
благоприятно сказывается на чистоте окружающего воздуха и способствует решению
проблем городского смога.
Но в итоге, с активно растущим промышленным производствам НЧ, появились
новые экологические проблемы. Как оказалось многие частицы сильно токсичны, а
так как их размер расположен в диапазоне нанометров, они способны проникать и
задерживаться в легких живых организмов, а также они практически не оседают, и
циркулируют в атмосфере, создавая опасные аэрозоли. И наверно теперь с этой
каждый год усиливающейся проблемой, теперь сможет справиться развитие
пикотехнологий. А пикотехнологии, в свою очередь очевидно создадут новые
проблемы, создавая такой вот эффект бумеранга.
Но так как в настоящее время промышленное производство НЧ исчисляется в
тысячах тонн, то производство черной и цветной металлургии исчисляется в
десятках и сотнях тысяч тонн. Поэтому, в своем реферате под название
«экологические проблемы при создании новых материалов» расскажу вам про
следующие производства, а также экологические проблемы, которые они влекут за
собой:
Экологические проблемы при производстве тантала и ниобия.
Экологические проблемы при производстве свинца.
Экологические проблемы стекольного производства
Экологические проблемы производства пластмасс
Экологические проблемы при утилизации лекарственных препаратов
1.
Экологические проблемы при производстве тантала и ниобия.
.1 Сырье для
производства тантала и ниобия
Главные минералы, содержащие тантал и ниобий: колумбит, танталит,
пирохлор, лопарит. Кроме того, тантал получают и из оловянных руд, как побочный
продукт при производстве олова (шлаки оловянных заводов содержат 3 - 15%
(Ta,Nb)2O5). Наибольшим предпочтением пользуются два танталсодержащих минерала
- это танталит (Fe,Mn)Ta2O6 и колумбит (Fe,Mn)(Nb,Ta)2O6. В настоящее время
добыча тантала идет в Австралии, Бразилии, Египте, Таиланде, Китае, Канаде
(самое богатое месторождение Берник-Лейк в юго-восточной Манитобе), Мозамбике,
Нигерии, Заире, Бурунди, Руанде, Конго, Казахстане и России (на Кольском
полуострове и в Забайкалье). Танталит и колумбит почти всегда содержат примеси
титана, олова, вольфрама и ряда других элементов.
.2 Получение
тантала и ниобия
Основным способом обогащения руд, содержащих танталит и колумбит,
является гравитационное обогащение (мокрая отсадка, обогащение на столах). В
результате получают обычно коллективный концентрат, содержащий, кроме танталита
и колумбита, касситерит, вольфрамит и некоторые другие минералы. Дальнейшее обогащение
ведут, применяя флотацию и электромагнитное разделение. Примерный состав
танталитовых концентратов: 12 - 30 % Nb2O5; 58 - 59,6 % Ta2O5; 2,09 - 15,7 % Fe2O3; 2,95 - 17,2 % MnO; 0,25 - 6,4 % TiO2; 0,12 - 0,9 % SiO2.
Переработку концентратов обычно осуществляют в три стадии:
1) вскрытие или разложение;
) разделение тантала и ниобия и получение их чистых химических
соединений;
) восстановление и рафинирование тантала.
Для вскрытия танталового концентрата применяют сплавление со щелочами
(NaOH, КОН) или разложение плавиковой кислотой. В первом способе в результате
плавления концентрата при 750 - 800 °С с избытком щелочи образуются ортосоль (Na3TaO4) и
оксиды железа, марганца. После обработки сплава водой образуются
малорастворимые политанталиты (Na8Ta6O19∙25H2O), которые разлагают
соляной кислотой, получая гидратированные оксиды тантала, которые затем
перерабатывают на чистые соединения.
Разложение плавиковой кислотой в настоящее время является основным
способом; в этом случае тонко измельченный танталитовый концентрат при
нагревании разлагают концентрированной плавиковой кислотой.
.3 Разложение
танталито-колумбитовых концентратов
загрязнение свинец
утилизация радионуклид
Переработка хлорированием. Хлорирование титано-тантало-нио-биевого сырья
- один из наиболее перспективных методов его переработки. Образующиеся
хлоропроизводные элементов, содержащихся в концентратах, обладают различной
температурой кипения. Это дает возможность фракционно их разделить при возгонке
и конденсации. Перед проведением процесса в шахтной электропечи концентрат и
углесодержащий восстановитель (древесный уголь, нефтяной кокс и др.)
брикетируют. В качестве связующего применяют сульфит-целлюлозный щелок (отход
бумажного производства), пек, кормовую патоку и др. Углерод берут с избытком 7
- 10%. так как меньшее содержание углерода снижает извлечение Nb, Та и Ti. Повышенное содержание в шихте углерода не увеличивает
извлечение ценных составляющих, но снижает загрузку по концентрату. Брикеты
сушат, а затем нагревают без доступа воздуха при 800 - 900° С. При этом
полностью удаляются влага и летучие компоненты шихты. На брикеты действуют
газообразным хлором при 600 - 800° С. Хлор должен содержать минимальное
количество влаги, чтобы не было гидролиза продуктов хлорировании.
Смесь концентрата и восстановителя можно хлорировать и без
предварительного брикетирования. Для этой цели реакционную смесь предварительно
сушат и вместе с хлором вводят в расплав малолетучие хлориды (NaCl, КСl). Окислы в составе концентратов реагируют с хлором и углеродом:
Nb2O5 + 5Cl2 +5С = 2NbСl5 + 5CO (1)O5 + 3Сl2 + 3C = 2NbCCl3 + 3СО (2)
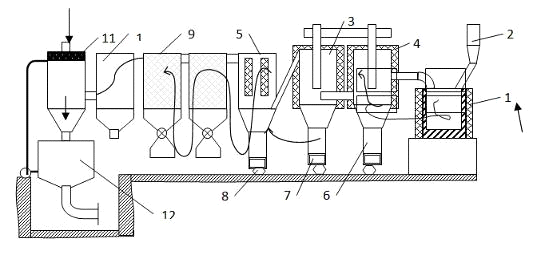
Рис. 2. Схема установки для переработки лопаритового концентрата
хлорированием:
- шахтная электропечь; 2 - бункер, 3 - конденсаторы; 4 - теплоизолирующая
рубашка; 5 - рукавный фильтр; 6 - контейнер; 7 - электрообогреватель; 8 -
прижимное устройство; 9 - трубчатые конденсаторы; 10 - ловушка; 11 - скруббер;
12 - емкость со щелочью.
Продолжительность хлорирования конкретного вида сырья устанавливают
экспериментальные зависимости от скорости подачи хлора, от избытка хлора, температуры,
величины брикетов и от других факторов.
В соответствии с рисунком 2 пылегазовая смесь, выходящая из хлоратора,
проходит последовательно через аппараты для улавливания хлоридов. Основное
количество хлоридов Nb, Та, Fe, Al (твердые хлориды) улавливается в обогреваемых конденсаторах.
В первом конденсаторе (140 - 160 °C) улавливается 40 - 70% общего количества твердых хлоридов, во втором
(120 - 160 °C) - 20 - 40% и в рукавном фильтре
(110 - 140°) - 3 - 15%. В трубчатые конденсаторы (температура газов 10 - 20 °C) увлекается не более 1 - 2% твердых
хлоридов. Хлориды TiCl4 и SiCl4 конденсируются в основном в
трубчатых конденсаторах. Содержание нерастворимого остатка в техническом TiCl4 равно 0,33%. Твердое содержимое от
жидкого отделяли фильтрованием или декантацией с последующей отгонкой TiCl4. Отходящие газы нейтрализуют
раствором щелочи в скруббере.
Продуктами вышеописанной схемы являются: плав, содержащий хлориды РЗМ,
конденсат хлоридов тантала и ниобия и технический тетрахлорид титана.
Для получения смеси оксидов тантала и ниобия конденсат хлоридов
подвергается гидролитическому разложению:
NbOCl3 + (x +3)H2O = Nb2O5 * xH2O + 6HCl (3)
2TaCl5 + (x + 5)H2O = Ta2O5 * xH2O + 10HCl (4)
В кислый раствор переходит большая часть примесей железа, алюминия и частично
титана. Полученная смесь, содержащая до 90 % (Nb, Ta)2O5 (в прокаленном продукте), поступает на очистку и разделение
тантала и ниобия. Другой путь переработки конденсата, содержащего NbOCl3, NbCl5, TaCl5, хлориды железа, алюминия и др., заключается в
получении смеси чистых пентахлоридов NbCl5 и TaCl5, которые затем можно
разделить методом ректификации.
Технические хлориды ниобия с целью дальнейшей переработки гидролизуют при
температуре около 100 °C. Выделяющийся газообразный хлорид HCl улавливают разбавленной соляной кислотой. Гидролиз
осуществляют при отношении Т : Ж=1 : 3. Технический TiCl4 содержит растворимые в нем примеси других хлоридов -
ниобия, тантала, железа, алюминия, кремния, а также продукты частичного
гидролиза TiCl4. Тетрахлорид титана, очищенный
двойной ректификацией от примесей, представляет продукт, пригодный для
получения металлического титана и TiO2.
.4 Разделение
тантала и ниобия
Разделение тантала и ниобия из-за сходства свойств их химических
соединений является сложной задачей.
В основном разделение и очистку ниобия и тантала проводят по двум
принципиальным схемам.
Наиболее распространенным является вариант, по которому из сильнокислых
растворов, коллективно извлекают ниобий и тантал; органическую фазу, содержащую
сумму металлов, отмывают от примесей раствором HF и (или) минеральной кислоты (H2SO4, HNO3, HCl). Разделение тантала и ниобия осуществляют путем
отмывки ниобия из очищенного от примесей экстракта раствором минеральной
кислоты, после чего тантал реэксграгируют (чаще водой). Поскольку вместе с
ниобием отмывается и часть тантала, то обычно из ниобийсодержащего водного
раствора проводят доизвлечение следов тантала.
.5 Получение
металлического тантала и ниобия
Металлический тантал получают восстановлением его соединений высокой
чистоты. Применяют восстановление тантала из Ta2O5 сажей в одну или две стадии
(с предварительным получением ТаC из
смеси Ta2O5 с сажей в атмосфере СО или H2 при 1800 - 2000 °C) -
карботермический способ. Электрохимическое восстановление из расплава,
содержащего фторотанталат калия К2TaF7 и оксид Ta2O5 - электролитический
способ. Восстановление натрием K2TaF7 при нагревании - натриетермический
способ. Возможны также процессы термической диссоциации хлорида или
восстановление из него тантала водородом. Обычно получают металл в виде
танталового порошка чистотой 98-99 %.
Получение металла в компактном виде осуществляют путем спекания
предварительно спрессованных из порошка заготовок прямым пропусканием тока при
2500 - 2700 °C или косвенным нагреванием при 2200 - 2500 °С в вакууме. При этом
чистота металла повышается до 99,9 - 99,95 %. Для получения больших слитков и
для рафинирования применяют электровакуумную плавку в дуговых печах с
расходуемым электродом и в электронно-лучевых печах. В процессе вакуумного
переплава общее содержание кислорода, азота и углерода снижается от 0,1 - 0,5
до 0,01 - 0,05 %. Особо чистый компактный тантал (монокристаллы) получают
бестигельной электронно-лучевой плавкой.
.6 Экологические проблемы производства тантала и ниобия
Условия проведения основных операций при производстве тантала и ниобия
зависят от состава растворов и требований к продукции. В хлорной технологии
радионуклиды концентрируются в плаве хлоридов редкоземельных элементов (РЗЭ).
При вскрытии лопаритового концентрата серной кислотой радионуклиды уранового и
ториевого рядов переходят в осадок в виде малорастворимых двойных сульфатных
солей, а при вскрытии азотной или соляной кислотами - в раствор. Все
технологические схемы переработки лопаритового концентрата предусматривают
выделение и утилизацию в специальных хранилищах ториевых отходов. В настоящее
время в хлорной технологии радионуклиды выводятся из технологического цикла в
виде двух продуктов, направляемых на захоронение:
. Плав отработанных расплавов солевых оросительных фильтров - 113т/1000т
ЛК.
Содержание тория в радиоактивном кеке дезактивации плава хлоридов РЗЭ
составляет в сухом продукте в среднем 6,43% ThO2., что позволяет считать данные
отходы потенциальным сырьем для получения чистых соединений тория. Поскольку
торий и его соединения практически не востребованы на рынке, то схемы
концентрирования тория не реализовываются на практике. Схема концентрирования
тория из хлоридных растворов подробно изучена нами при переработке
перовскитового концентрата (ПК).
В сернокислотной технологии образующиеся при разложении ЛК осадки
сульфатов РЗМ, кальция, стронция, а также тория, урана и продуктов их распада,
подвергаются конверсии в карбонаты с помощью раствора (NH4)2CO3. Далее
карбонаты обрабатывают азотной кислотой до достижения рН=0,3-0,6. Нейтрализация
пульпы 5%-ным раствором аммиака до рН=3,5 с введением в пульпу нитрата бария
(50-60 г на 1 кг Ln2O3) позволяет получать дезактивированные растворы нитратов
РЗЭ. Контроль эффективности выполненной дезактивации производили по
концентрации в продуктах тория и мезотория (88Ra228). Уран на 99% осаждался при
нейтрализации совместно с торием. Схема получения чистых ториевых продуктов в
сернокислотной технологии разработана в ФГУП ВНИИХТ и здесь нами не
рассматривается.
Разложение ЛК азотной или соляной кислотами имеет определенные
преимущества перед сернокислотным методом, а именно: исключается конверсия
сульфатов РЗМ, кальция, стронция, тория с расходом (NH4)2CO3 и образованием
раствора Na2SO4 и (NH4)2SO4.
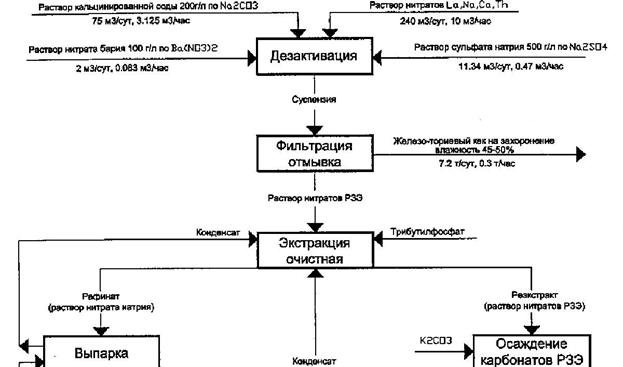
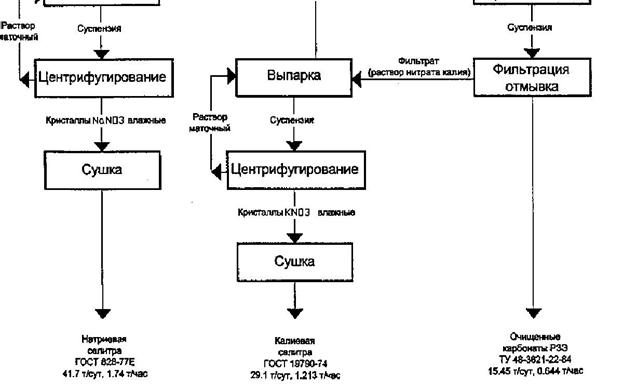
Рис. 4. Переработка нитратных растворов от разложения ЛК
При переработке ЛК по азотнокислотно-гидрофторидной технологии выход
радиоактивного железо-ториевого кека составляет 0,13-0,18 т/т ЛК. Содержание в
нем ThO2 составило 2,5-3,5%. Выход кека возможно снизить в три раза за счет
концентрирования радионуклидов.
Практический опыт использования азотнокислотного вскрытия ЛК имелся на
Приднепровском химическом заводе (г.Днепропетровск) и ГАО «Силмет»
(г.Силламяэ). При переработке нескольких тысяч тонн ЛК был накоплен полезный,
положительный опыт получения раствора нитратов РЗЭ, тория, кaльция, стронция,
нaтрия и кека гидратированных оксидов титана, ниобия и тантала. Раствор
перерабатывается по стандартной технологии: поднейтрализация, осаждение и
отделение радиоактивных элементов; далее осаждение неактивных неочищенных
карбонатов РЗМ, содержащих кальций и стронций, либо экстракция с целью
отделения РЗМ от примесных элементов, осаждение очищенных карбонатов РЗМ или
экстракционное разделение РЗМ.
Объединенный азотнокислый раствор - фильтрат и промывной раствор -
освобождают от радиоактивных и других примесей (рис. 4). Для этого азотную
кислоту вначале нейтрализуют раствором соды. Нейтрализация приводит к выпадению
в осадок гидроксидов тория и железа по реакциям:
Th(NO3)4 + 2Na2CO3 + 2H2O = Th(OH)4 + 4NaNO3 + 2CO2
Fe(NO3)3 + 3Na2CO3 + 3H2O = 2Fe(OH)3 + 6NaNO3 + 3CO2
.7 Схемы
переработки перовскитового концентрата и утилизации радионуклидов
Перовскитовый концентрат (ПК) Африканского месторождения является
наиболее подготовленным потенциальным сырьем для промышленной переработки.
Существуют различные варианты комплексной технологии переработки ПК,
позволяющие получать пентаоксиды тантала и ниобия, пигментный диоксид титана,
РЗЭ концентрат. Все варианты схем предусматривают выделение радионуклидов. По
некоторым схемам возможно их концентрирование, что сокращает выход отходов.
Перспективным вариантом технологии является вскрытие перовскита соляной
кислотой с переводом кальция, РЗЭ и тория в раствор, а титана, ниобия и тантала
- в осадок, которые в дальнейшем перерабатывается на товарную продукцию по
схемам (рис. 5 - 6). Хлоридные растворы после отделения титана, ниобия и
тантала содержат (г/л): 100-200 HCl, 100-150 CaCl2, 0,1-0,2 ThO2, 6-10 Ln2O3,
6-10 Fe2O3, 1-10 TiO2; кроме того, в растворах присутствуют натрий, алюминий,
ванадий, марганец и другие элементы. С целью уменьшения потоков, регенерации
HCl (возвращаемой на вскрытие перовскита) и улучшения экстракции тория растворы
упариваются до концентрации CaCl2 300 г/л и выше.
Высокое извлечение тория достигается при экстракции из растворов без
добавления HCl, упаренных до содержания CaCl2 более 350 г/л. При Vo:Vв = 1:1
извлечение тория за одну ступень для растворов состава (г/л) 113 HCl, 376 СaCl2
и 76 HCl, 449 CaCl2 составляет соответственно 80 и 93%.
До извлечения тория из раствора удаляли железо экстракцией н-октанолом
(ОКЛ). Поскольку в исследуемой системе часть железа находится в виде не
экстрагируемого Fe(II) (до 20 мас.% в сумме Fe(II) +Fe(III)), то Fe(II)
окисляли до Fe(III) добавлением небольшого количества H2O2. В этом случае ОКЛ
при Vo:Vв = 0,8:1 извлекает более 98% железа.
Из рафината после экстракции тория ТБФ проводили соосаждение радия на
BaSO4 и далее - нейтрализацию раствора известковым молоком с получением
концентрата редкоземельных элементов. Содержание ThO2 в фильтрате по данным
химического анализа менее 0,001 г/л. Фильтрат, представляющий собой практически
раствор CaCl2, может быть переработан с выделением соединений кальция.
.8 Проблемы
переработки лопаритового концентрата
При хлорировании лопаритового концентрата образуются отходы в виде
отработанных расплавов оросительного солевого фильтра.
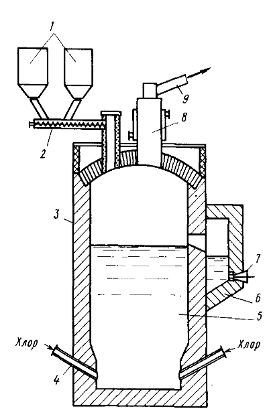
Рис. 7. Хлоратор для хлорирования лопаритового концентрата в солевом
расплаве: 1 - бункеры для концентрата и кокса; 2 - шнековый питатель; 3 -
хлоратор, футерованный шамотным кирпичом; 4 - фурмы; 5 - расплав; 6 -
копильник; 7 - летка; 8 - охлаждаемый газоход;
9 - патрубок вывода ПГС в систему конденсации
Хлоратор представляет собой шахту прямоугольного сечения. В процессе
хлорирования избыточный расплав непрерывно переливается через переточный канна
в копильник 6. Нагревается расплав с помощью графитированных электродов,
смонтированных в стенки хлоратора. Пылегазовая смесь из хлоратора через
патрубок 9 попадает в солевой фильтр.
Отработанные расплавы солевого оросительного фильтра процесса
хлорирования лопаритовых концентратов содержат естественные радионуклиды.
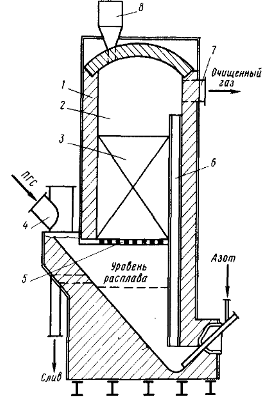
Рис. 8. Схема солевого фильтра с аэролифтной циркуляцией расплава: 1 -
корпус, футерованный шамотным кирпичом; 2 - каплеуловительная камера; 3 -
инертная керамическая насадка; 4 - газоход; 5 - колосниковая решетка; 6 -
аэролифтная труба; 7 - патрубок вывода
ПГС; 8 - загру-зочный бункер кусков NaCl
Растворы, содержащие, % масс: 2,5 ThCl4, 20 АlСl3, 7 LnCl3, а также
примеси TiCl4, NbCl3, ТаСl5, NaCl, KCl, MgCl2, CaCl2, водонерастворимый остаток
(5%), - растворяют в воде при Ж:Т=4:1. Пульпу обрабатывают магнезиальным
молоком до рН 9,0±0,5, затем обрабатывают раствором, содержащим 100 г/дм3
сульфата натрия, раствором, содержащим 100 г/дм3 хлорида бария, после в пульпу
вводят 0,8 дм3 раствора, содержащего 5 г/дм3 Fe3+. Затем пульпу обрабатывют
0,1%-ным раствором полиакриламида, выдерживают без перемешивания 1 час и
фильтруют, радиоактивный осадок отделяют от маточного раствора, промывают
сначала 1,5 объемами воды на 1 объем осадка, затем раствором, содержащим хлорид
магния в количестве 1,5 объема на 1 объем осадка, осадок смешивают с
магнийсодержащими оксидными минеральными материалами, взятыми в количестве 600
г MgO на 1 кг осадка, образующуюся пастообразную композиционную смесь помещают
в формы и прессуют при одновременном нагревании до 100°С.
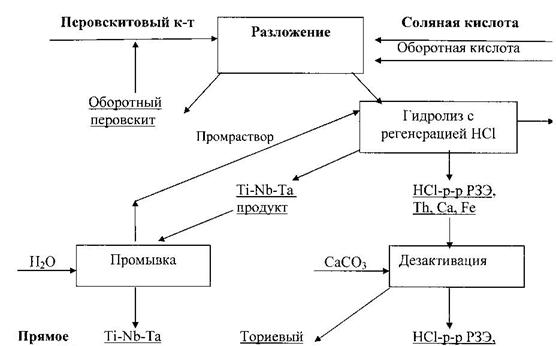
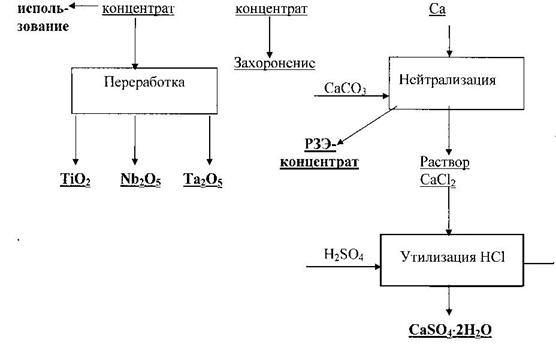

Рис. 5. Принципиальная соляно-кислотная схема переработки перовскитового
концентрата
Процесс дезактивации растворов от естественных радионуклидов дает возможность
дезактивировать радиоактивные отходы (РАО) до установленных норм, а перевод
радиоактивных осадков в отвержденное состояние обеспечивает их экологически -
безопасное складирование без нанесения ущерба окружающей природной среде,
здоровью населения и обслуживающего персонала: полученные в соответствии с
предлагаемым способом "блоки", как показали испытания, устойчивы к
колебаниям температуры окружающей среды (от -50 до +50°С), не пылят,
водонерастворимы и устойчивы к воздействию атмосферных осадков, грунтовых и
подпочвенных вод.
.9 Экологические проблемы переработки плюмбомикролитового концентрата
Переработка плюмбомикролитового концентрата при производстве ниобия и
тантала представляет определенные сложности ввиду наличия радиактивных веществ.
Состав плюмбомикролита: Nb2O5 - 7,75 %, Ta2O5 - 68,43 -
77,0%, TiO2 - 0 - 1,58, Ce2O3 - 0,17 - 4,20 %, Y2O3 - 0,24 - 11,34 %, UO2 - 0 - 4,21 %, UO3 - 0 - 1,59 %.
Схема представленная на рисунке 9 включает следующие основные
технологические переделы:
измельчение и рассев ПМК;
разложение концентрата смесью фтористоводородной и азотной кислот при
температурах 90 - 120 oC с
последующей фильтрацией охлажденной пульпы;
обработку фильтрата концентрированной серной кислотой с целью очистки
растворов от свинца и радионуклидов;
экстракционное выделение тантала, а затем ниобия с отделением примесей и
радионуклидов;
растворение в горячей воде осадка, содержащего соединения свинца, фториды
примесных элементов, неразложившийся ПМК, с переводом свинца в хорошо
растворимую соль азотнокислого свинца.
Из анализа технологической схемы следует:
. Для снижения пыления и попадания мельчайших частиц в воздух
производственных помещений процесс измельчения концентрата проводится мокрым
способом.
. При высокотемпературном вскрытии ПМК в окружающую среду выделяются пары
HF, диоксида азота, а также
радиоактивных газов (радон). Для решения этой проблемы реакторы снабжены
обратными холодильниками, которые обеспечивают охлаждение кислотных паров, их
конденсацию и сброс образующихся кислот обратно в реактор. Улавливание радона
возможно с помощью физических (адсорбционные, криогенные и др.) и химических
методов.
. Необходима утилизация растворов (рафинатов) после экстракционного
отделения ниобия от примесных элементов и радионуклидов (в частности от урана),
а также образуемых осадков, содержащих неразложившийся ПМК, PbSO4 и другие соединения.
. Для использования раствора Pb(NО3)2 в качестве товарного продукта
необходима разработка метода очистки его от радия-226 и свинца-214.
Выводы по главе
. Отечественное титано-редкометалльное сырье в основном являются
естественно-радиоактивным. Торий, уран и элементы их радиоактивного распада в
значительной мере определяют радиологическую токсичность минеральных
концентратов и продуктов их переработки.
. В целом, из полученных результатов можно сделать вывод об эффективности
комбинированных технологий, как радиационно-безопасных, включающих методы
экстракции и осаждения для выделения концентратов радионуклидов и попутного
извлечения РЗЭ из сложных и многокомпонентных растворов, получаемых при
гидрометаллургической переработке титано-редкометалльного сырья.
. По данным Радиевого института им. В.Г.Хлопина конечные сбросные
растворы переработки перовскитового концентрата и твердый отход - гипс не имеют
ограничений использования по радиационным факторам, т.к. не представляют
опасности для внешней среды по данным показателям.
2.
Экологические проблемы при производстве свинца
Загрязнение окружающей среды свинцом и его соединениями является для
России наиболее острым и опасным. Свинец поставляет цветная металлургия, в том
числе 94 % этого металла выбрасывается в атмосферу 5 предприятиями. Это
Среднеуральский медеплавильный завод, АО “Святогор” - Красноуральский
медеплавильный завод, Кировоградский медеплавильный комбинат, АО
"Динополиметалл", завод "Электроцинк". Как видим, главные
отравители воздуха свинцом находятся на территории Свердловской области, и эти
предприятия привносят в атмосферу России 68,7 % всех свинцовых выбросов.
Однако, основным источником загрязнения атмосферного воздуха свинцом в РФ
является автотранспорт, использующий свинецсодержащий бензин. автомобильный
парк выбрасывает ежегодно в атмосферу 10 млрд. абсолютно смертельных доз свинца
или в весовых единицах 250 килотонн металла. Так общее количество свинца,
выбрасываемое в воздух в результате сгорания топлива в двигателях, в 2010 году
составляло 301 килотонну, или примерно две-три смертельные дозы на человека в
год.
Не малую роль в загрязнении свинцом играют отработанные аккумуляторы,
отравляющие почву и воду соединениями свинца.
Столь масштабное загрязнение окружающей среды доказывает немаловажный
факт: воды рек выносят в год 17-18 тыс. т. свинца, что примерно в 200 раз
меньше количества выплавляемого металла.
Свинец влияет на нервную систему человека, что приводит к снижению
интеллекта, вызывает изменение физической активности, координации слуха,
воздействует на сердечно-сосудистую систему, приводя к заболеванию сердца. Это
оказывает негативное влияние на состояние здоровья населения и в первую очередь
детей, которые наиболее восприимчивы к свинцовым отравлениям.
В России постепенно увеличивается численность людей, имеющих
профессиональный контакт со свинцом. Случаи хронической свинцовой интоксикации
зафиксированы в 14 отраслях промышленности.
Среди профессиональных интоксикаций свинцовая занимает первое место,
причем имеет место тенденция к её увеличению. Среди рабочих, пострадавших от
воздействия свинца, около 40 % составляют женщины. Для них свинец представляет
особую опасность, так как этот элемент обладает способностью проникать через
плаценту и накапливаться в грудном молоке. Как правило, наиболее высокая
концентрация свинца в атмосферном воздухе наблюдается в зимний период, что
связано с дополнительными выбросами в атмосферу продуктов сжигания топлива.
Неблагоприятные метеорологические условия в этот период года также способствуют
накоплению свинца в нижних слоях атмосферы.
.1 Применение
Легкоплавкий, удобный в переработке, свинец широко применяется в наши
дни. Из свинца изготавливают оболочки кабелей, электроды аккумуляторов, аноды,
используемые при хромировании; им покрывают изнутри сосуды предназначенные для
хранения серной кислоты, также изготовляют змеевики холодильников и другие
ответственные части аппаратуры. Свинец идет на изготовление боеприпасов и на
выделку дроби. Он входит в состав многих сплавов, например сплавов для
подшипников, типографского металла. Свинец хорошо поглощает рентгеновское и
радиоактивное излучение, и его используют для защиты от излучения при работе с
радиоактивными веществами. Применяют для получения тетраэтилсвинца (ТЭС) и
других соединений свинца.
2.2 Источники загрязнения окружающей среды свинцом
Получение свинца. 1)Восстановительный обжиг. Обогащенный флотацией
галенит обжигают на воздухе для удаления серы и образующийся оксид свинца (II)
восстанавливают коксом или чаще - монооксидом углерода в шахтных печах:
2PbS+3O2=2PbO+2SO2+CO=Pb+CO2
В результате получают черновой свинец, из которого выделяют медь,
серебро, железо, олово, мышьяк и сурьму, висмут остается вместе со свинцом.
Особо чистый свинец получают электролитическим рафинированием с использованием
фторосиликатного электролита.
) Окислительный обжиг. Особенно чистую руду PbS подвергают частичному
окислению до PbO, а затем смесь прокаливают:
+2PbO=3Pb+SO2
)Из солей свинца с помощью электролиза.
)Взаимодействие солей свинца с цинком:
Pb(NO3)2+Zn=Zn(NO3)2+Pb
или восстановление оксида свинца (II) током водорода:
PbO+H2=Pb+H2O.
2.3 Загрязнение окружающей среды в процессе получения свинца
При процессах производства свинца и его сплавов в атмосферу выбрасывается
значительное количество свинцовой пыли. Свинец, содержащийся в этой пыли,
вовлекается в биологический круговорот, негативно воздействуя при этом на все
живое.
Несомненно, огромный вклад в загрязнение окружающей среды свинцом
превносят Химические источники тока.
Рассмотрим принцип действия свинцового (кислотного) аккумулятора.
Готовый к употреблению свинцовый аккумулятор состоит из решётчатых
свинцовых пластин, одни из которых заполнены диоксидом свинца, а другие -
металлическим губчатым свинцом. Пластины погружены в 35-40 % раствор H2SO4; при этой концентрации удельная
электрическая проводимость раствора серной кислоты максимальна.
При работе аккумулятора - при его разряде - в нем протекает
окислительно-восстановительная реакция, в ходе которой металлический свинец
окисляется:
+SO42-=PbSO4+2e-
а диоксид свинца восстанавливается:
PbO2+SO42-+4H++2e-=PbSO4+2H2O.
Электроны, отдаваемые атомами металлического свинца при окислении,
принимаются PbO2 при восстановлении; электроны передаются от одного электрода к
другому по внешней цепи.
Таким образом, металлический свинец служит в свинцовом аккумуляторе
анодом и заряжен отрицательно, а PbO2 служит катодом и заряжен положительно.
Во внутренней цепи(в растворе H2SO4) при работе аккумулятора происходит перенос ионов. Ионы SО42- движутся к аноду, а ионы Н+ - к
катоду. Направление этого движения обусловлено электрическим полем, возникающим
в результате протекания электродных процессов: у анода расходуются анионы, а у
катода - катионы. В итоге раствор остается электронейтральным. Если сложить
уравнения, отвечающие окислению свинца и восстановлению PbO2, то получится
суммарное уравнение реакции, протекающей в свинцовом аккумуляторе при его
работе (разряде):
Pb+PbO2+4H++2SO42-=2PbSO4+2H2O
ЭДС заряженного свинцового аккумулятора равна 2 В. По мере разряда
аккумулятора материалы его катода (PbO2) и анода (Pb) расходуются. Расходуется и
серная кислота. При этом напряжение на зажимах аккумулятора падает. Когда оно
становится меньше значения, допускаемого условиями эксплуатации, аккумулятор
вновь заряжают. Для зарядки аккумулятор подключают к внешнему источнику тока.
При этом ток протекает через аккумулятор в направлении, обратном тому, в
котором он проходил при разряде аккумулятора. В результате этого
электрохимические процессы на электродах “обращаются”. На свинцовом электроде
теперь происходит процесс восстановления:
PbSO4+2e-=Pb+SO42-
т.е. этот электрод становится катодом.
На электроде из PbO2 при зарядке идет процесс окисления:
PbSO4+2H2O=PbO2+4H++SO42-+2e-
следовательно, этот электрод является теперь анодом. Ионы в растворе
движутся в направлениях, обратных тем, в которых они перемещались при работе
аккумулятора. Складывая два последние уравнения, получим уравнение реакции,
протекающей при зарядке аккумулятора:
2PbSO4+2H2O=Pb+PbO2+4H++2SO42-.
Нетрудно заметить, что этот процесс противоположен тому, который
протекает при работе аккумулятора; при зарядке аккумулятора в нем вновь
получаются вещества, необходимые для его работы.
Свинцовый аккумулятор используется как автономный источник электрической
энергии, главным образом применяется в транспорте.
.4 Свинцовый аккумулятор - загрязнитель окружающей среды
Опасности для человека, окружающей среды возникают преимущественно на
этапе утилизации отработавших аккумуляторов. По-прежнему много батарей после
использования выбрасывается в мусоропроводы. По экспертным оценкам, на свалках,
транспортных площадках и других местах на всей территории России в настоящее
время находится до 1 млн. т свинца в отработавших свой срок аккумуляторах. При
существующем положении с их переработкой эта величина возрастает на 50-60 тыс.
т ежегодно. На свалках или установках для компостирования аккумуляторы
разлагаются, при этом в почву и подземные воды попадает большое количество
свинца. При рециклинге также происходит загрязнение окружающей среды, особенно
пылью, содержащей свинец. При изготовлении свинцовых аккумуляторов образуются
значительные количества пылевидных частиц, содержащих соединения свинца. Как
видно, свинцовые аккумуляторы привносят немалый вклад в загрязнение окружающей
среды.
Помимо свинцового аккумулятора широко применяются и многие другие виды аккумуляторов.
В среднем на каждый кв. метр приходится по одному аккумулятору; очевиден
процесс массового загрязнения окружающей среды тяжелыми металлами,
концентрированными электролитами и другими вредными химическими соединениями.
.5 Выбросы автотранспорта - основной источник загрязнения окружающей
среды ионами свинца
Без сомнения, наиболее важным источником загрязнения в Свердловской
области является автомобильный транспорт, использующий этилированный бензин.
Численность автомобильного парка Свердловской области увеличилась в 1997 году
более чем на 5 % и превысило 1 млн. единиц, при этом опережающими темпами
растет число легковых автомашин (на 10-12 % в год). В городах Екатеринбурге,
Каменск-Уральском, Первоуральске, Верхней Пышме, Нижнем Тагиле, Берёзовском
выбросы автотранспортных средств составляют 30-70 % от общего объема выбросов
загрязняющих веществ в атмосферу.
Автотранспорт вносит значительный вклад в загрязнение атмосферы свинцом.
Таблица №3. Выбросы некоторых загрязняющих веществ от автомобильного
транспорта по городам области в 1997 году (в тоннах).
|
Город
|
СО
|
Свинец
|
Город
|
СО
|
Свинец
|
|
Алапаевск
|
1846
|
0,3
|
Красноуральск
|
984,8
|
0,2
|
|
Асбест
|
5228,8
|
4,3
|
Лесной
|
1042,6
|
0,2
|
|
Верхняя Пышма
|
2427,4
|
1,8
|
Нижний Тагил
|
18084,1
|
16,1
|
|
Верхняя Салда
|
1598,6
|
0,2
|
Нижняя Тура
|
1202,5
|
0,6
|
|
Екатеринбург
|
66063,1
|
128,4
|
Первоуральск
|
6391
|
4,8
|
|
Ирбит
|
2550,7
|
0,3
|
Полевской
|
2264,1
|
2,1
|
|
Качканар
|
2212,6
|
Ревда
|
1880,9
|
1,3
|
|
Кировоград
|
1365,6
|
0,4
|
Серов
|
2680,3
|
1,9
|
|
Краснотурьинск
|
3100,6
|
1
|
Тавда
|
1790,3
|
0,9
|
Самое большое количество свинца и окиси углерода выбрасывается
автомобилями городов Екатеринбурга, Нижнего Тагила и Первоуральска. Наблюдается
тенденция роста уровня загрязнения атмосферного воздуха по свинцу в крупных
городах области. На передвижные источники загрязнения приходится свыше 70 %
суммарных выбросов свинца. Высокими остаются уровни загрязнения воздушного
бассейна городов диоксидом азота, формальдегидом, оксидом углерода. В целом
область значительно загрязнена свинцом. Общая площадь загрязненных сильной
степени земель составляет более 68 тыс. га. Очевиден стабильный вклад
автотранспорта в загрязнение окружающей среды городов Свердловской области
свинцом. Так каким же образом свинец попадает в двигатели внутреннего сгорания
и рассеивается автомобилями вдоль автомагистралей.
.6 Октановое число
Автомобильный бензин представляет собой горючее с низкими детонационными
характеристиками. Детонацией называют такой характер горения, при котором
воспламенение горючей смеси происходит в нескольких точках цилиндра или по
всему объему сразу. При этом возникают очень высокие пики давления и двигатель
может быть поврежден. Детонационные характеристики количественно определяются
так называемым октановым числом, которое принято равным нулю для н-гептана,
весьма подверженного детонации, и равным 100 для изооктана (2,2,4-3метилпентан)
- углеводорода, стойкого к детонации. Если конкретное топливо и смесь н-гептана
с изооктаном имеют одинаковые детонационные свойства, то содержание последнего
(в % по объему) определяет октановое число рассматриваемого топлива. Например,
бензин с октановым числом 76 детонирует также, как смесь 24 % н-гептана с 76 %
изооктана. Чем выше октановое число, тем лучше эксплуотационные качества
бензина. В основном с помощью тетраэтилсвинца (ТЭС) и увеличивают октановое число.
Механизм антидетонационного действия алкилов свинца до конца не установлен.
Очевидно, тетраэтилсвинец, поступает в цилиндр в виде паров вместе с топливной
смесью, и вследствие возрастания температуры распадается с образованием частиц
твердого оксида свинца. Эти частицы блокируют активные атомы кислорода, которые
инициируют реакцию, приводящую к взрыву. Дибром - и дихлорэтаны действуют как
раскислители и, вступая во взаимодействие с оксидом свинца, образуют летучий
хлорбромид свинца, выносящийся из цилиндров отработавшими газами.
Недостатки применения ТЭС - негативное действие на всю биосферу, более
быстрый износ двигателя и невозможность применения каталитической системы
очистки отработавших газов вследствие её отравления антидетонатором. Вот
почему, несмотря на все достоинства ТЭС, применение его нежелательно, как и
нежелательно применение самого бензина, потому что выхлопные газы,
образовавшиеся в результате сгорания топлива, оказывают негативное влияние на
всю биосферу Земли.
.7 Влияние на организм человека. Общий характер действия. Токсическое
действие свинца
В природе свинец встречается повсеместно, но жизненно необходимым он не
является. За последние десятилетия уровень концентрации в природе все более
повышается вследствие антропогенных нагрузок. Главным источником, из которого
свинец попадает в организм человека, служит пища, наряду с этим важную роль
играет вдыхаемый воздух, а у детей также заглатываемая ими свинецсодержащая
пыль. Вдыхаема пыль примерно на 30-50 % задерживается в легких, значительная
доля её всасывается током крови. Всасывание в желудочно-кишечном тракте
составляет в целом 5-10 %, у детей - 50 %. Дефицит кальция и витамина Д
усиливает всасывание свинца в желудочно-кишечном тракте. В среднем за сутки
организм человека поглощает 26-42 мкг свинца. Это соотношение может
варьировать. Около 90 % общего количества свинца в человеческом теле находится
в костях, у детей - 60-70 %. Биологический период полураспада в костях - около
10 лет. Количество свинца, накопленного в костях, с возрастом увеличивается, и
в 30-40 лет (фаза насыщения) у лиц, по роду занятий не связанных с загрязнением
свинца, составляет 80-200 мг. Особую опасность представляет свинец для женщин,
так как этот элемент обладает способностью проникать через плаценту и накапливаться
в грудном молоке.
.8 Влияние ионов свинца на почву и растения
Вследствие глобального загрязнения окружающей среды свинцом, он стал
вездесущим компонентом любой растительной и животной пищи и кормов.
Растительные продукты в целом содержат больше свинца, чем животные.
Причины летнего листопада - высокое содержание свинца в воздухе. Но,
концентрируя свинец, деревья тем самым очищают воздух. В течении вегетативного
периода одно дерево обезвреживает соединения свинца, содержащиеся в 130 л.
бензина. Наименее восприимчивым к свинцу является клен, а наиболее восприимчивы
орешник и ель. Сторона деревьев, обращенная к автомобильным магистралям, на
30-60 % “металличнее”. Хвоя ели и сосны обладает свойствами хорошего фильтра по
отношению к свинцу. Она его накапливает и не обменивает с окружающей средой.
Накопление свинца ведут интенсивно грибы, мхи и лишайники и доводят его
концентрацию до 64,76 частей на миллион соответственно. А вот более знакомые
нам овес и клевер уже при концентрации свинца 50 частей на миллион начинают
замедлять рост и урожайность снижается.
Установлено, что в слое глубиной до 5 см свинец накапливается более
интенсивно, чем медь, молибден, железо, никель и хром. И это печально,
поскольку из всего этого ряда свинец - самый ядовитый. Ученые изучали почву и
растительность в районах расположения свинцово-цинкового завода и завода по
производству аккумуляторов. И, конечно же, свинец в почве обнаружили в
количествах, превышающих раз в 40-50 среднее. При такой “подкормке” растения
“свинцевеют”. Отмечено интересная особенность растений - различных своих частях
накоплять различное количество свинца. Например, салат и сельдерей в листьях
накапливают значительно больше свинца, чем в корнях, а морковь и одуванчик -
наоборот.
Отмечено активное накопление свинца в капусте и корнеплодах, причем
именно в тех, которые повсеместно употребляются в пищу; например, отмечают
большое содержание свинца в картофеле.
Выявили интересную особенность репчатого лука. Оказалось, что на фоновых
участках он содержит свинца всего 0,07 частей на 1 млн. частей сухого вещества.
На придорожных участках его концентрация гораздо меньше, но степень возрастания
этой концентрации десятикратная. Так что и у репчатого лука “свинцовые фильтры”
не вполне надежны. Но вот, что особенно странно: зеленый лук и ежа сборная
оказались самыми устойчивыми к накоплению свинца из всех изученных растений;
содержание свинца в них не превышало 4 частей на 1 млн.
Водное растение эйхорния, которое преимущественно произрастает в Америке,
удивило ученых своим свойством жадно поглощать всяческую “химию”, в частности
свинец. Эйхорния оказалась великолепным работником по очистке водоема от
химических соединений, причем работает она очень быстро. Это объясняется тем,
что у эйхорнии длинные, разветвленные корни. Заметим, что поглощая большие
количества свинца, сама эйхорния остается здоровой. Оказалось, что и после
насыщения ядами эйхорния может быть полезна. Её подвергают газификации и
получают газ, по свойствам близкий к природному. А из золы извлекают металлы:
свинец, ртуть, кадмий.
Но, пожалуй, рекордсменом среди растений по стойкости к соединениям
свинца являются дрожжи. Биологи утверждают, что дрожжи могут поглощать огромные
количества свинца в виде уксуснокислой соли - до 15 тысяч частей на миллион
частей веса дрожжей - без всякого угнетения обмена веществ. Так может быть
дрожжи помогут в борьбе с загрязнением солями свинца? Хлористый и йодистый
свинец угнетают брожение. Однако, повторяю, дрожжи - рекордсмен по
“свинцовостойкости”. Увы! Этим замечательным свойством обладают не все
растения.
.9 Способы борьбы с массовым загрязнением ионами свинца
Рекомендации по защите биосферы от вредного влияния ионов свинца.
I.
Совершенствование
производственных технологий:
1) Изменение технологии производства
свинца и его сплавов.
2) Проведение технического
перевооружения аккумуляторных заводов.
3) Отказ от использования свинцовых
пигментов в производстве декоративных красок, замена их ферритами, титанитами,
алюминатами.
4) Внедрение передовых технологических
процессов и оборудования для производства высокооктановых, не содержащих
свинец, бензинов.
Дооборудование автотранспортных средств с целью замены этилированного
бензина альтернативными видами топлива. Интересной альтернативой бензину
представляется метиловый спирт, полностью сгорающий до углекислого газа и воды.
До недавнего времени метанол использовался главным образом для
производства различных органических производных, однако в настоящее время все
более заметна роль в производстве моторных топлив. В Германии и других странах
7-15 % метилового спирта добавляют к бензину с целью экономии последнего.
Полная же его замена метиловым спиртом сдерживается необходимостью
конструкционных изменений в двигателе и ещё недостаточными объемами
промышленного выпуска подобного горючего, доступность которого определится
технологическими успехами в производстве водорода из воды. Если же в качестве
углеродсодержащего компонента удастся использовать углекислый газ, избыток
которого накапливается в атмосфере, то технология производства метанола
существенно удешевится.
Как топливо будущего рассматривается и гидразин, достоинства которого
определяются неисчерпаемостью и дешевизной сырья: азот из воздуха и водород из
воды. К недостаткам следует отнести канцерогенность самого гидразина и выделение
им аммиака при разложении.
Водородное топливо. В наши дни очень серьезно обсуждается эта проблема.
Двигатель не будет подвержен большим конструкционным изменениям .Водородное
топливо в 10 раз калорийнее бензина, а в атмосферу выбрасываются только пары воды.
Если оно будет применено, то, по-видимому, не раньше, чем истощится природное
органическое топливо и будут созданы термоядерная и солнечная энергетики,
способные обеспечить дешевой энергией технологию разложения воды.
Автомобильное газовое топливо, топливо для автомобильных двигателей,
бывает двух видов: сжиженный газ, компримированный газ. Сжиженный газ состоит
из пропана или смеси пропана с бутаном. Эти УВ, находящиеся при комнатной
температуре и нормальном давлении в газообразном состоянии, под давлением
сжижаются и могут закачиваться в специальные баллоны. Сжиженный газ получают
при добыче нефти и природного газа и производят также на нефтеперегонных
заводах. Компримированный (сжатый) - природный газ метан. Ученые всего мира
расценивают ХХ1 век как “эпоху метана” прежде всего потому, что это
экологически чистое (основными продуктами сгорания являются углекислый газ и
вода) и надежное топливо и, что особенно важно, его запасы значительно
превышают запасы нефти. Имеющиеся в России запасы природного газа позволяют
сохранить достигнутый уровень его добычи в течение минимум двух столетий.
Широкое использование сжатого природного газа в качестве моторного топлива и
массовое переоборудование автотранспорта города позволит резко снизить
количество вредных токсичных выбросов:
·
окислов углерода
в 2-2,5 раза
·
окислов азота в
1,3 раза
·
УВ в 1,4 раза
·
ТЭС - полное
отсутствие
·
Дымность
отработанных газов дизельных двигателей в 8-10 раз.
Техническое устройство газобаллонного оборудования практически исключает
возгорание автомобиля при самых невероятных автомобильных авариях или при
неумелой эксплуатации, потому что компримированный природный газ легче воздуха,
а баллоны достаточно прочны. Установка газобаллонного оборудования не приводит
к потере возможности работать на бензине. Заправленный бензином бак можно
держать в резерве.
1) Переход на более современные
технологии производства консервированных продуктов. Выяснилось, что одним из
существенных источников поступления свинца в организм человека являются консервированные
продукты. К примеру, содержание свинца в мышцах тунца при сушке и размалывании
увеличивается в 400 раз, а после упаковки в запаянные консервные банки - в 4000
раз. Причина этого понятна - при сушке концентрация увеличивается за счет
потери влаги, а при упаковке в банки используется припой, содержащий свинец.
Так, при исследовании консервов “Мясо тушеное” после 11-16 лет хранения в их
составе было обнаружено 19-28 частей на 1 млн. частей свинца. Правда, это
исключительный случай. Обычно содержание металла не превышает 2-3 части на 1
млн. Однако учеными установлено, что переход свинца в продукт не связан с
длительностью хранения консервов. Многие исследователи мира рекомендуют не
применять при консервировании пищевых продуктов полуду, которая содержит
свинец. Эксперты Всемирной организации здравоохранения сообщают, что молоко,
обработанное фабричным путем, содержит значительно больше свинца, чем свежее
коровье молоко, которое имеет концентрацию свинца, близкому к женскому молоку.
.10 Совершенствование способов очистки.
) Создание мощностей по переработке вторичного свинцового сырья.
) Реабилитация территорий, загрязненных свинцом. Существует несколько
способов выведения свинца из пищевой цепи путем введения в почвы некоторых
веществ. Предложены специальные ”антисвинцовые” препараты. Так, в Японии
запатентовано средство для обработки почв, содержащее меркапто-8-триазин он
связывает свинец и другие тяжелые металлы и выводит их из биологического
круговорота. В Германии предложено в тех же целях вносить в почву хелатные
смолы. И в нашей стране ведутся широкие поиски активных химических средств.
Так, на кафедре ботаники Московского лесотехнического института получен ряд
составов, включающих азотнокислый торий, пятиокись ванадия, азотнокислой
кобальт и некоторые другие соединения. Эти составы названы адаптогенами. Они
помогают растениям “приспособиться” к воздействию повышенных концентраций
вредных веществ. Адаптогены уже прошли широкую проверку и показали свою высокую
эффективность.
Отмечено благоприятное действие и неорганического фосфора на жизненный
цикл “освинцованных” растений.
3) Замена антидетонатора ТЭС более “чистыми” соединениями, но не
уступающими по свойствам ТЭС.
Возможны несколько путей повышения октанового числа бензина без помощи
тетраэтилсвинца. Одним из таких путей заключается в применении антидетонаторов,
не уступающих или по крайней мере приближающихся по свойствам к ТЭС, но не
обладающих его отрицательными качествами.
Достойными соперниками ТЭС оказались некоторые карбонилы металлов.
Таблица №9. Реальные соперники тетраэтилсвинца
|
Формула
|
Fe(CO)5
|
Mn2(CO)10
|
Ni(CO)4
|
|
Название
|
Пентакарбонил
железа
|
Декакарбонил марганца
|
Тетракарбонил никеля
|
|
Причина невостребованности
|
Не достаточно устойчив.
Отрицательные качества усугубляются его превращением при горении бензина в
оксид железа (III), который оседает на стенки цилиндра и резко ускоряет износ
двигателя
|
Не достаточно устойчив
|
Чрезвычайно ядовит
|
|
Формула
|
C5H5 Mn(CO)3
|
CH3C5H4(CO)3
|
|
Название
|
Дегизобутилен пентакарбонил
железа
|
Циклопентадиенил трикрбонил
марганца (ЦТМ)
|
Метил-ЦТМ
|
|
Причина невостребованности
|
Нет окончательных данных о
его влиянии на двигатель и окружающую среду.
|
Дорогостоящий, но
высокоэффективный, устойчивый и нетоксичный антидетонатор
|
Нет. Высокоэффективный, в
достаточной степени устойчивый и нетоксичный антидетонатор. Как более
дешёвый, чем ЦТМ, начинает вытеснять ТЭС.
|
|
|
|
|
|
|
Выводы по главе
В процессе работы над рефератом
1) Установлено, что в целом Свердловская
область значительно загрязнена соединениями свинца, который главным образом
попадает в окружающую среду с выбросами автотранспорта;
2) Рассмотрено влияние ионов свинца на
всю биосферу. Свинец медленно, постепенно убивает живой организм;
3) Изучена методика определения окиси
углерода в выхлопных газах автомобилей. Определено канцерогенное действие
оксида углерода (II) на человеческий организм;
4) Сформулированы рекомендации по
предотвращению попадания свинца в окружающую среду в целях защиты биосферы от
вредного его влияния. Установлено, что самый возможный из сформулированных
способов очистки - замена этилированного бензина газовым топливом;
5) Доказано что загрязнение окружающей
среды свинцом происходит только в результате деятельности человека.
Остается надеяться, что здравый смысл возобладает над индустриальным
азартом и удастся остановить массовое загрязнение окружающей среды свинцом,
негативно влияющим на биохимические процессы живых организмов.
3.
Экологические проблемы стекольного производства
Стекло - вещество и материал, один из самых древних и, благодаря
разнообразию своих свойств, - универсальный в практике человека.
Физико-химически - неорганическое вещество, твёрдое тело, структурно - аморфно,
изотропно; все виды стёкол при формировании преобразуются в агрегатном
состоянии - от чрезвычайной вязкости жидкого до так называемого стеклообразного
- в процессе остывания со скоростью, достаточной для предотвращения
кристаллизации расплавов, получаемых плавлением сырья (шихты). Температура
варки стёкол, от 300 до 2500 °C, определяется компонентами этих стеклообразующих
расплавов (оксидами, фторидами, фосфатами и др.). Прозрачность (для видимого
человеком спектра) не является общим для всех видов существующих как в природе,
так и в практике стёкол.
В настоящее время разработаны материалы чрезвычайно широкого, поистине -
универсального диапазона применения, чему служат и присущие изначально
(например, прозрачность, отражательная способность, стойкость к агрессивным
средам, красота и многие другие) и не свойственные ранее стеклу -
синтезированные его качества (например - жаростойкость, прочность,
биоактивность, управляемая электропроводность и т. д.). Различные виды стёкол
используется во всех сферах человеческой деятельности: от строительства,
изобразительного искусства, оптики, медицины - до измерительной техники,
высоких технологий и космонавтики, авиации и военной техники. Изучается
физической химией и другими смежными и самостоятельными дисциплинами.
3.1 Виды
стекол
В зависимости от основного используемого стеклообразующего вещества,
стекла бывают оксидными (силикатные, кварцевое, германатные, фосфатные,
боратные), фторидными, сульфидными и т. д.
Базовый метод получения силикатного стекла заключается в плавлении смеси
кварцевого песка (SiO2), соды (Na2CO3) и извести (CaO). В результате получается
химический комплекс с составом Na2O*CaO*6SiO2.
Кварцевое стекло получают плавлением кремнезёмистого сырья высокой
чистоты (обычно кварцит, горный хрусталь), его химическая формула - SiO2.
Кварцевое стекло может быть также природного происхождения (см. выше -кластофульгуриты),
образующееся при попадании молнии в залежи кварцевого песка (этот факт лежит в
основе одной из исторических версий происхождения технологии).
Кварцевое стекло характеризуется весьма малым коэффицинтом температурного
расширения и потому его иногда используют в качестве материала для деталей
точной механики, размеры которых не должны меняться при изменении температуры.
Примером служит использование кварцевого стекла в точных маятниковых часах.
Оптическое стекло - применяют для изготовления линз, призм, кювет и др.
.2 Технологический процесс создания стекла
Стекло - это аморфный изотропный материал, получаемый переохлаждением
расплавов неметаллических оксидов и бескислородных соединений. Материалами,
склонными к переохлаждению и к переходу в стеклообразное состояние, являются
главным образом силикаты, бораты, фосфаты.
Производство стекла складывается из подготовки сырьевых материалов,
смешивания этих материалов и приготовления однородной шихты, варки, формования
и отжига стекла. В некоторых случаях требуется химическая, механическая и
термическая обработка отформованных изделий. Характерной особенностью
технологии стекла является общность методов подготовки сырья, составления шихты
и стекловарения для различных производств; это обстоятельство позволяет
рассматривать общие закономерности поступления загрязняющих веществ в
окружающую среду на примере практически любого типичного предприятия отрасли.
Сырьевые материалы, применяемые в производстве стекла, делятся на главные
стеклообразующие и вспомогательные материалы. Наряду с главными
стеклообразующими для варки хрустальных стекол и хрусталя применяют оксид
свинца PbO (от 10% в малосвинцовом стекле до 80% в свинцовом хрустале по
массе), который вводят в стекло в виде свинцового сурика Pb3O4 (тяжелый порошок
светло-красного цвета) или реже свинцового глета PbO (тяжелый порошок
темно-желтого цвета). Оксид свинца также применяют для получения ювелирных
стекол, силикатных обжиговых красок и эмалей для стекла и керамики. Некоторое
количество соединений свинца в виде примесей основных сырьевых материалов.
Варка стекла осуществляется при температурах около 1400-1450оС,
осветление и гомогенизация - при 1500о, остудка - при 1200о. При этих
температурах происходит интенсивное выделение компонентов шихты, поступающих с
отходящими газами в атмосферных воздух.
На основании результатов экспериментальных исследований и оценки
материального баланса свинца в производстве можно заключить, что потери
свинцовых соединений при варке в газопламенных печах составляет 8-10%, а при
варке в электрических печах с ручной выработкой и газоотапливаемыми
выработочными бассейнами - 2-5,7%, для электрических печей с
электрообогреваемыми выработочными устройствами с индивидуальными наборными
ячейками - 1-2%.
Условно общие потери соединений свинца в производстве свинцовых стекол и
хрусталя можно представить в виде нескольких составляющих, отнесенных к
нескольким операциям и процессам:
· приготовления шихты в составном цехе,
· транспортировки и загрузки в печь,
· поступления в воздух рабочей зоны свинца через смотровые, наборные
окна, загрузочные проемы и др.,
· стекловарения с последующими залипанием на сводах и стенах в полости
печи, а также конденсацией и осаждением пылевидных частиц отходящих газов в
регенераторах, дымоотводных каналах и трубах,
· выброса в атмосферу,
· выщелачивания из готовых изделий в ходе механической или химической
обработки,
· отбраковки (со стеклобоем).
Отметим, что указанные потери вносят вклад соответственно в формирование
потоков соединений свинца, поступающих в атмосферный воздух как от
организованных (через трубы составных и стекловаренных цехов), так и
неорганизованных источников (производственные корпуса и промплощадка в целом).
То же можно сказать и о сбросах соединений свинца (в канализацию и с
поверхностным стоком с территории предприятия). Не исключена также вероятность
поступления некоторой части оксидов свинца с просыпями на полигон в составе
твердых отходов предприятия.
Заводы по производству листового стекла загрязняют окружающую среду в
малых количествах. В процессе производства образуются следующие отходы:
Твердые отходы: стеклобой, пыль при транспортировке шихты, отходы от
упаковочных материалов, порошковые отходы цехов обработки стекла, отходы
огнеупорных материалов печей и др.,
Газообразные выбросы: продукты сгорания природного газа, содержащие СО2 и
No2, потоки стекловарения и подготовки шихты и др.,
Сточные воды: от моечной машины, водные суспензии с пылью шихты и т.д.,
Токсичные растворы и выбросы: испарения расплава олова.
А так же при работе автопогрузчика и машин для вывоза готовой продукции
образуются выхлопные газы.
Во всем мире ведутся интенсивные поисковые работы в направлении «
улучшения» сырья. Предлагается традиционные материалы заменять более химически
активными, менее тугоплавкими и летучими (бораты, силикаты, щёлочи). В
результате уменьшается температура взаимодействия и ускоряется
силикатообразование. Это особенно важно, если в состав стекла входят компоненты
высоких классов токсичности. Для снижения температуры стеклообразования предложены
синтетический силикат и искусственный продукт, заменяющий соду. Последний
представляет собой силикат натрия, модифицированный небольшим количеством
оксидов титана и железа. Все это может значительно снизить вред, наносимый
стекольным производством окружающее среде.
Если в соответствии с предусмотренными техническими решениями и расчетами
рассеивания в атмосфере вредных веществ, размер санитарно-защитной зоны для
предприятия получается больше, чем размер, установленный санитарными нормами
проектирования промышленных предприятий, то необходимо пересмотреть проектные
решения и обеспечить выполнение требований санитарных норм за счет уменьшения
количества выбросов вредных веществ в атмосферу или увеличения высоты выброса,
чтобы обеспечить требования норм по чистоте воздушного бассейна в зоне жилой
застройки.
Множество различных отходов может быть использовано вторично. Для каждого
типа сырья есть соответствующая технология переработки. Для разделения отходов
на различные материалы используются различные виды сепарации, например, для
извлечения металла - магнитная.
3.3 Последние разработки
Ученые из Нидерландов представили последние разработки в сфере
переработки отходов - улучшенную технологию, которая без предварительной
сортировки, в рамках одной системы, разделяет и очищает все отходы, которые
туда поступают, до первоначального сырья. Система полностью перерабатывает все
виды отходов (медицинские, бытовые, технические) в закрытом цикле, без остатка.
Сырье полностью очищается от примесей (вредных веществ, красителей и т. д.),
пакуется и может быть использовано вторично. При этом система экологически
нейтральна.
В Германии построен и протестирован TUV (немецкой Службой технического
контроля и надзора) завод, который успешно работает по данной технологии 10 лет
в тестовом режиме. На данный момент правительство Нидерландов рассматривает
вопрос о строительстве на территории своей страны.
В настоящее время существует достаточно большое количество технологий по
переработке стекла. Все они отличаются друг от друга по различным параметрам,
но имеют одно общее свойство - в долевом отношении приблизительно одна четверть
от объема стекла, подлежащего утилизации, преобразуется в новые изделия. Три
четверти от объема при переработке отбрасываются.
Процесс утилизации "бытового" стекла начинается с правильной
организации процесса сборки использованных изделий. В странах Западной Европы
проблема сборки и хранения стеклоотходов решается достаточно просто. В жилом
секторе буквально возле каждого дома устанавливаются специальные контейнеры,
маркированные цветом и запоминающейся "символикой", в которые жители
домов выбрасывают пустые бутылки и прочую стеклотару. За нарушение этого
установленного порядка налагаются штрафы, но эта мера применяется крайне редко,
так как не возникает такой необходимости (видимо, сказывается природная
дисциплинированность западноевропейцев). Согласно статистическим данным, в той
же Германии специальными контейнерами для стеклотары оборудовано более 97%
придомовых территорий.
Следующим этапом после сборки бытового стекла является его очистка от
инородных материалов (например, бумажных этикеток, пластмассовых пробок,
алюминия и т. д.). Этот процесс выполняется уже на перерабатывающих
предприятиях, куда "бытовое" стекло доставляется из жилого сектора.
На этом этапе процедуры утилизации редко возникают какие-либо затруднения:
более 98% использованной стеклотары поддаются очистке и только 1-2% бракуются
окончательно.
И вот наконец, после всех предварительных приготовлений
"бытовое" стекло поступает на перерабатывающие установки. В настоящее
время при утилизации стекла предпочтение отдается тем технологиям, которые не
оказывают вредного воздействия на окружающую среду и не требуют больших затрат
энергии. В этой сфере широкое распространение получили такие методы, как
использование новейших перерабатывающих систем с циркуляционным движением
теплоносителя, расплавление и фильтрация стекла по современной
"газовой" технологии и т. д.
После соответствующей переработки полученная стекломасса может
использоваться для изготовления различных строительных материалов, конструкций
и изделий: стеклоблоков, стеклопакетов, обычного оконного стекла, изоляционных
материалов и других видов продукции.
Выводы по главе
Для современных стекольных заводов характерно сочетание ряда факторов:
высокой температуры воздуха, лучистой теплоты, загрязнения воздушной среды
пылью и химическими соединениями, производственного шума.
Из изложенного очевидно, что экологические проблемы в стекольной
промышленности нужно решать в следующих направлениях:
. Для уменьшения пылевыделения и летучести компонентов стекла
необходимо улучшение процессов подготовки сырья и шихты или самих материалов и
шихт.
. Снижение рабочих температур в печи позволит уменьшить расход
газообразного топлива и снизить выбросы оксидов углерода и азота.
. Разработка экологически безопасных видов топлива, окислителя или
принципиально новых источников тепловой энергии, позволяющих минимизировать или
исключить токсичные выбросы.
. Поиск принципиально новых методов, позволяющих получать стекло
без стадии варки.
4.
Экологические проблемы формоиндустрии
Фармоиндустрия по обороту находится в первых рядах бизнеса.[1] Оборот
мирового фармацевтического рынка составляет 850 - 900 млрд. дол. в год и растет
на 3% в год.[2] Общее количество лекарственных средств [3] и их комбинаций в
мире уже превышает 200 тысяч. За один год человечество принимает миллионы тонн
различных лекарственных химиопрепаратов. [4] Большое количество лекарственных
(фармацевтических) средств населением не используется и попадает в мусорные
контейнеры. [5] Все чаще обнаруживаются в водной среде медикаменты и их
метаболиты. [6] Современные химические фармацевтические средства очень сложные
и чистые вещества, поэтому при их производстве применяется очень большое
количество различных дополнительных химических веществ. Все это приводит к
значительным отходам. Для оценки их количества в зеленой химии используется
Е-фактор (отношение массы всех побочных продуктов к массе целевого продукта).
Фармацевтический синтез имеет самый высокий Е-фактор (25-100), что и означает
значительное количество отходов.
После употребления лекарственные средства [7] разными путями попадают в
окружающую среду и создают ФАРМАЦЕВТИЧЕСКОЕ ЗАГРЯЗНЕНИЕ. Особенно опасно
их нахождение в воде (pharmaceuticals in drinking water, drugs in drinking
water). Дело в том, что
из организма само лекарственное средство или их метаболиты выводится с калом и
мочой и через канализацию попадает в водоемы и почву. Очистные сооружения, как
правило, не приспособлены для улавливания или разложения, как самих
лекарственных средств, так и множества средств гигиены. Эффективным способом
для очистки сточных вод могло быть озонирование, фотокаталитическая деструкция,
мембранная фильтрация, обратный осмос, установки термического обезвреживания,
активированным углем и др. [9] Предлагают даже создать специальные туалеты для
очистки и переработки мочи (в больницах, амбулаториях). [10] Стоимость
дополнительной очистки воды составит 5 - 20 евро в год на человека.
При использовании обычных процессов обработки воды, таких как
хлорирование, можно удалить примерно 50% фармацевтических средств, в то время
как более современные процессы обработки, такие как озонирование,
усовершенствованное окисление, фильтрование на основе активированного угля,
нанофильтрование и обратный осмос, позволяют достичь более высоких
коэффициентов удаления. Так, например, с помощью обратного осмоса можно удалить
более 99% крупных молекул фармацевтических средств.
Традиционные методы способы утилизации лекарственных препаратов заключаются
в сжигании, высокотемпературной обработке с доступом или без доступа кислорода
воздуха, или захоронению их на полигонах твердых бытовых отходов. Недостаток -
загрязнение атмосферы высокотоксичными соединениями: оксидами углерода, серы,
фосфора, мышьяка, селена, фосгеном, дицианом, диоксинами и другими
соединениями. Термическая утилизация - весьма высоко затратный процесс
утилизации.
Предложены экологически безопасные методы утилизации. Они достигаются
последовательными операциями электролитической и электрохимической
деструкции лекарственных препаратов, посредством их щелочного гидролиза в
гидролизаторах при насыщении щелочного раствора кислородом воздуха и
электрохимической обработки полученного гидролизата в электролизерах с
нерастворимыми и растворимыми электродами, соответственно.
Вот конкретные факты загрязнения среды фармацевтическими средствами и
последствия от этого:
лет назад (1995) в водопроводной воде в Берлине ученые обнаружили ото
кислоту, которая используется при производстве лекарств, снижающих уровень
холестерина. Это самый первый случай, когда было официально объявлено, что в
водопроводе крупного города обнаружены следы медикаментов. На очистных
сооружениях Гётеборга обнаружено 14 препаратов в концентрациях, которые
варьировали от нанограммов до миллиграммов на литр, широко применяемое
противовоспалительное и болеутоляющее средство - ибупрофен - было обнаружено в наибольшей
концентрации: 7 мг/л.
• Серьезный урон источникам пресной воды наносят фармацевтические,
особенно гормональные препараты, которые попадают в воду через канализацию, или
же после отправки их на мусорную свалку, где они смываются дождевой водой в грунт,
а оттуда в водоемы.
• Фармацевтические заводы в Индии захоронивают большое количество опасных
химических отходов. Шведские исследователи обнаружили в Хайдарабаде, Индия в
2007 году, очень высокие концентрации антибиотиков и других лекарств в
очищенных сточных водах фармацевтических производителей. В США и Канаде, вода
вблизи всех крупных городов, сильно загрязнена фармацевтическими отходами. [3]
Более 180 из 3000 разрешенных активных веществ уже обнаружены в водах Германии,
в том числе антибиотики, психотропные и противозачаточные средства, женские
половые гормоны.[39] Поверхностные воды в Германии содержат около 2 мг/литр
женского полового гормона эстрогена.
• Было проверено около 1500 рыб в 50 реках и озёрах Великобритании. Не
менее трети этих рыб приобрело женские признаки. Эти рыбы изменили свой пол и
превратились в самок. Реки Великобритании насыщены женским противозачаточным
гормоном эстрогеном.
В 2004 году до 86 процентов всех самцов рыб, выловленных в 51 городе
Великобритании, оказались гермафродитами. Основная причина таких мутаций -
повышенное содержание в воде рек этинилэстрадиола, входящего в состав
гормональных контрацептивов.
Антиандрогены содержатся в воде большинства рек Англии. Именно они
являются причиной блокировки мужского гормона у многих видов рыб, и
способствуют мутации репродуктивной системы самцов.
В Великобритании в питьевой воде обнаружен также бензолегонин - вещество,
находящееся в моче после употребления кокаина. Помимо бензолегонина в воде
также были обнаружены значительные количества кофеина, болеутоляющего
ибупрофена и противоэпилептического лекарственного средства карбамазепина.
Диклофенак (обезболивающее)( служит причиной массовой гибели грифов в
некоторых странах Азии. [35] В воде Балтии обнаружен также диклофенак.
Из всего изложенного вывод напрашивается сам собой - фармацевтические
загрязнения (Pharmaceutical pollution, Drugs in Drinking Water,Pharmaceuticals
In Drinking Water) всей Земли являются реальностью нашего времени. Уже более
сорока лет об этом известно ученым. С 1990-х загрязнение воды фармацевтическими
препаратами стало серьезной экологической проблемой мирового масштаба. Хотя
концентрация лекарственных средств небольшая (порядка микрограмма на литр), но
их длительное воздействие на флору и фауну могут имет нередсказуемые вредные
воздействия (снижение иммунитета, генетические нарушения, устойчивость
возбудителей к антибиотикам и др). Особый вред наносит наличие женского гармона
эстрогена в воде для организмов в воде и человека от репродуктивных расстройств
до формирования у самцов половых особенностей самок (снижения числа
сперматозоидов и рост бесплодия среди мужчин, живущих в промышленных
государствах, могут быть связаны с гормональным загрязнением воды, рак яичек и
простаты, а также остеопороз могут быть следствием чрезмерно высокой
концентрации эстрогена в теле человека). [51] Пиво содержит большое количество
фитоэстрогенов. В воду из пластиковых бутылок попадают хим. вещества, подобные
по хим.составу с женским гормоном эстрогеном (так называемые эндокринные дисрупторы
- вещества, нарушающие гормональный обмен).
В человеческом обществе сформировался и действует миф, что с помощью
лекарственных средств (синтетических химических препаратов) [20] можно вылечить
почти все болезни. Врачи и реклама активно этому содействуют. Такая
"фарморелигия" очень кстати и людям: можно не вести здоровый образ
жизни, а проглотить очередную таблетку. Назначение пациенту лекарственного
препарата превратилось в определенный лечебный ритуал. Без рецепта и пациет и
врач психологически не могут считать лечебное действо завершенным. В этом
смысле в человеческом обществе возникла новая форма лекарственной зависимости
(аддикция [79]) - фармозависимость. О чем обоснованно предупреждает Луи Брауэр.
Необходимо социально-психологический аспект лекарственной зависимости пациентов
и врачей рассмотреть на одном из ежегодных российских конгрессов «Человек и
лекарство».
Если учесть экспериментально доказанный факт существования нескольких
пиков биологической активности веществ, то проблема очистки вод от химических
лекарственных препаратов при сверхнизкой их начальной концентрации значительно
усложняется. Поскольку готовые гомеопатические препараты также попадают в
окружающую среду, то необходимы специальные исследования. Возможно, что при
многократном разбавлении и обычные лечебные препараты могут в окружающей среде
превращаться в гомопатические с непредсказуемыми последствиями для человека.
Однако для 75% лекарственных средств при сверхмалых концентрациях (порядка
10-17 моля
на литр) эффективность возрастает почти до прежнего уровня. Это позволит
резко сократить вредные последствия от приема больших доз препаратов на
организм, а также сократить выбросы хмимических препаратов в окружающую среду.
Необходимы также исследования по гомеопатическим загрязнителям в
окружающей среде. Наиболее серьезное влияние по последствиям оказывает наличие
в воде женского гармона и антибиотиков. Женский горомон оказывает
феминизирующее воздействие на организмы, а при наличии антибиотиков в воде
возбудители болезней приобретают к ним устойчивость (резистентность) .
Несколько снижает вредное воздействие женского гормона то, что гормональные
контрацептивы частично метаболизируются и выходят из организма в неактивной
форме. Cовременные препараты содержат чрезвычайно мало эстрогена и
прогестерона. Реальная угроза возникла для рыб из-за наличия в воде женского
гармона. Одной из причин значительного снижения уровня у мужчин мужского
гармона тестостерона можно также объяснить наличием женского гормона в питьевой
воде.
В связи увеличением продолжительности жизни населения и предполагаемого
роста потребления лекарственных средств в ближайшие 20 лет до 30% тенденция
загрязнения среды ими будет усиливаться. Следует одобрить опыт Швеции по
переходу на применение "зеленых" таблеток. [33] Необходимо также
дополнить очистные сооружения системами по очистке воды от лекарственных
средств и гигиенических препаратов. К сожалению, фармоиндустрия не торопится
вкладывать средства в разрешения этой проблемы. Как временный выход из
положения, можно рекомендовать использовать домашние очистители питьевой воды
от лекарственных препаратов. [100] В фармоиндустрии и медицине важно
повсеместно использовать принципы зеленой химии Фармозагрязнения должны стать
предметом ЛЕКАРСТВЕННОЙ ЭКОЛОГИИ (Drug ecology), предметом которой является
экологически чистый процесс химического синтеза лекарственных средств,
нанолекарства, хранение, использование, а также их утилизация. Лекарственная
экология является составной частью медицинской экологии (англ. Environmental
medicine), а также экологии болезней Жака Мея (May J.).[38]
В 2011 году ВОЗ опубликовала технический доклад "Фармацевтические
средства в питьевой воде(Pharmaceuticals in drinking-water)[108] из которого
следует, что уровни концентрации фармацевтических средств в поверхностных
водах, грунтовых водах и в частично обработанной воде были обычно ниже 0,1 µg/l
(или 100 ng/l), в то время как уровни концентрации в обработанной воде были,
как правило, ниже 0,05 µg/l (или 50 ng/l). ВОЗ считает, что такие концентрации
пока не требуют дорогостоящей дополнительной очистки питьевой воды, поскольку
риск для здоровья человека крайне незначительный. Однако приведенные нами факты
все же свидетельствуют о другом.
На наш взгляд, если не принять серьезных мер, то вред от лекарственных средств
может превзойти их пользу. Необходимо переходить на производство ЭКОЛОГИЧЕСКИ
ЧИСТЫХ ЛЕКАРСТВ (экологически безопасные лекарства). "Это лекарственные
препараты, которые, после оказания человеку необходимой помощи, будут быстро
разрушаться, превращаясь в биологически неактивные осколки еще до того момента,
как покинут организм. В крайнем случае, это должно происходить в очень короткие
сроки после их попадания в природную среду." Наличие малых и сверхмалых
доз лекарственных препаратов в окружающей среде может привести к экологической
катастрофе с непредсказуемыми последствиями.
Когда вся вода будет загрязнена лекарственными средствами, то
человечеству придется добывать чистую воду из недр Земли, перерабатывая минерал
рингвудит.
Для предотвращения экологической химической фармацевтической катастрофы
XXI века необходимо иметь новое направление в экологической науке - ЭКОЛОГИЯ
ЛЕКАРСТВЕННЫХ СРЕДСТВ. Точнее: экологическая токсикология лекарственных средств
(ЛС) - изучение жизненного цикла ЛС в окружающей среде и воздействия остатков
лекарств на разнообразные живые организмы . К счастью, оно фактически возникло
еще в 1999 году.
Как временный выход для предотвращения интоксикации организма от
лекарственных препаратов в питьевой воде можно предложить такой: пить
бутилированную минеральную воду добытую из глубоких слоев земли.
Выводы по главе
В заключении, можно сделать вывод, что чем бы ни пользовался человек, что
бы он не изобретал, оно с одной стороны приносит ощутимую пользу в одном
направлении, но в то же время непременно наносит вред другому. Это не означает,
что нужно забросить все что вредно и опасно, а говорит о том, что нужно все
делать обдуманно, извлекая из полученного как можно большую пользу, и принося
куда то, как можно меньший вред.
Список использованной литературы
1. ХИМИЧЕСКОЕ
ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ И ЕГО ПОСЛЕДСТВИЯ. 2012 г.
(http://polbu.ru/brower_mafia/ch51_all.html)
2. Горькая
пилюля СПб Ведомости Выпуск № 076 от 24.04.2013
(http://www.spbvedomosti.ru/article.htm?id=10298468@SV_Article)
. Piluli
- Медицина от А до Я (http://www.piluli.kharkov.ua/liter/)
. Лекарства
и лекарственная болезнь
(http://www.medn.ru/statyi/lechenie-solyu-skipidarom-kerosinom/lekarstva-i-lekarstvennaya-bolezn.html)
5. Safe
Disposal to Reduce Medicines in the Environment
(http://www.takebackyourmeds.org/why/medicines-in-the-environment)
6. Очистка
сточных вод фармацевтической промышленности
(http://www.enviro-chemie.ru/public/farm.htm)
. От
чего сегодня нужно защищать Балтику? (http://www.nkj.ru/news/21917/)
. ПРОБЛЕМЫ
И ТЕХНОЛОГИИ ОБЕЗВРЕЖИВАНИЯ ОТХОДОВ ФАРМАЦЕВТИЧЕСКОЙ ПРОМЫШЛЕННОСТИ ДЛЯ
ПРЕДОТВРАЩЕНИЯ ЗАГРЯЗНЕНИЯ ОКРУЖАЮЩЕЙ СРЕДЫ
http://past.tpu.ru/files/nu/ignd/section14-06.pdf
9. Is
Your Daily Shower Polluting the Water Supply?
(http://www.rodale.com/pharmaceuticals-environment)
10. Ройзман
С. А. МИКРОФИТОТЕРАПИЯ - СВЯЗУЮЩЕЕ ЗВЕНО ИНТЕГРАТИВНОЙ МЕДИЦИНЫ (http://www.kinesio.ru/book/pb0007.html)
. Химия
и технология редких и рассеянных элементов. Часть 3. Под ред. К. А. Большакова.
М:, «Высшая школа», 1976;
. А.
Н. Зеликман, Б. Г. Коршунов. Металлургия редких металлов. М:, Металлургия,
1991;
. http://www.kolasc.net.ru/russian/sever07/sever07_4.pdf
. “Вредные
вещества в промышленности” том 1, справочник, под ред. Лазарева Н.В. и Левиной
Э.Н. Ленинград “Химия” 1976 г.
. “Второе
дыхание марафонца” Лебедев Ю.А. Москва “Металлургия” 1984 г.
. “Государственный
доклад о состоянии окружающей среды в Свердловской области” Свердловск 1997
год.
. “Ключ
Земли”№10 1997.
. “Неорганическая
химия” Ахметов Н.С. Москва “Высшая школа” 1988 г.
. “Общая
химия” Глинка Н.Л. Ленинградское отделение 1987 г.
. “Охрана
природы. Атмосфера” ГОСТ 17.2.2.03-81
. “Планета
Земля глазами химика” Опаловский А.А. Москва “Наука” 1990 г.
. “Тяжелые
металлы” Орлов Д.С. Москва “Металлургия” 1985 г.
. “Химия”
Молочко В.А., Крышкина С.В. Москва “Высшая школа” 1990 г.
. “Химия”
10 класс Рудзитис Г.Е., Фельдман Ф.Г. Москва “Просвещение” 1993 г.
. Энциклопедический
словарь - справочник “Окружающая среда” Фельдман Л.Р. Москва “Прогресс” 1993 г.
. .Основы
промышленной экологии. А.А.Челюков, Л.Ф.Ющенко.
. Экология,
здоровье и охрана окружающей среды в России. В.Ф.Протасов
. Технология
пластических масс, под редак. В.В.Коршака
. Пластические
массы. В.П. Померанцев
. Экология
для технических вузов В.М.Гарин, И.А.Клёнова.
. Шульц
М.М. О природе стекла // Природа № 9. 1986
. Качалов
Н. Стекло. Издательство АН СССР. Москва. 1959.
. Доклад
"О свинцовом загрязнении окружающей среды Российской Федерации и его
влиянии на здоровье населения" (Белая книга). - М.:РЭФИА, 1997. - 48c.
. Пути
совершенствования охраны окружающей среды в свинцово-цинковой подотрасли.
Сборник научных трудов.: Усть-Каменогорстк, 1986. - С. 39.
. Чехов
О.С. Вопросы экологии в стекольном производстве, 1990.
. Гринин
А.С., Новиков В.Н. Промышленные и бытовые отходы: Хранение, утилизация,
переработка. - М.:ФАИР-ПРЕСС, 2002
. А
так же отчёты «Солнечногорского экологического департамента».