|
Донор
|
Условия
|
Суммарный
выход, (%)
|
Соотношение
б/в
|
|
69a
|
(p-СH3)PhSO3H,125оС
|
71a/71a+72
|
33+2
|
29/71
|
|
69a
|
(p-СH3)PhSO3H,
CH2Cl2
|
71a/71a
|
67
|
4/96
|
|
69a
|
(p-СH3)PhSO3H,
Yb(OTf)3, CH2Cl2
|
71a
|
61
|
10/90
|
|
70b
|
(p-СH3)PhSO3H,
CH2Cl2
|
71b/71b
|
40
|
15/85
|
|
70c
|
ZnCl2, CH2Cl2
|
71c/71c
|
60
|
11/89
|
|
70b
|
ZnCl2, CH2Cl2
|
71d/71d
|
40
|
5/95
|
3. Материалы и методика исследования
Температуры плавления определяли на приборе ПТП,
оптическое вращение при 20-25 °С - на поляриметре Polamat-A (l
= 546 нм).
Анализ состава реакционных смесей, чистоты
синтезированных соединений, а также мониторинг реакций, проводили методом
тонкослойной хроматографии (ТСХ) на пластинках Sorbfil-АФВ-УФ
(«Сорбполимер», Россия). Для проявления хроматограмм использовали системы
растворителей: бензол-изопропиловый спирт, 10:1(А), хлороформ - изопропиловый
спирт 15:1 (B). Зоны веществ
обнаруживали 5% раствором серной кислоты в этаноле при нагревании до 200-300 оС
или УФ-облучением при длине волны 254 нм. Выделение индивидуальных веществ
осуществляли колоночной хроматографией на силикагеле Kieselgel
60 (0.063-0.200 мм).
1Н
ЯМР спектры получены на спектрометрах Varian Mercury-400 (400 МГц), внутренний
стандарт - Me4Si. Приведены химические сдвиги (ХС) (м.д., d-шкала)
и константы спин-спинового взаимодействия (КССВ, J, Гц).
Использовали 15-краун-5 (Merck, Германия), карбонат
калия (хч), пропан-2-ол (ч) (Технохим), бромид ртути (Технохим), ацетонитрил
(Сфера Сим, чда), хлороформ (чда), ацетон (чда), бензол (чда)
(Крымлаборреактив).
Пиразо[4,5-c]изохинолины 74, 76, 78, 80
синтезированы отделом химии биологически активных соединений Институтом
физико-органической химии и углехимии им. Л.М. Литвиненко НАН Украины.
Синтез
8-[4-(2-aцетамидо-3,4,6-три-О-ацетил-2-дезокси-в-D-глюкопиранозилокси)фенил]-3-метил-5,6-диметокси-1-фенилпиразо[4,5-c]изохинолина
(75)
Схема 19
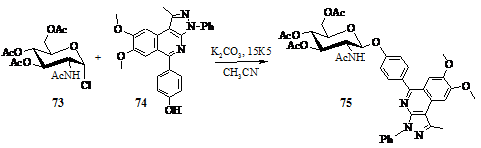
Смесь 500 мг (1,4 ммоль) б-хлорида
73, 562 мг (1,4 ммоль) пиразолоизохинолина 74, 869 мг (6,3 ммоль) безводного
карбоната калия и 54 мкл (0,28 ммоль) 15-краун-5 в 15 мл безводного
ацетонитрила перемешивали при температуре 20-22 С до полной конверсии
гликозил-донора (ТСХ, система A). Твердую фазу отделяли фильтрованием, осадок
промывали на фильтре ацетонитрилом (2Ч5 мл), растворитель удаляли досуха при
пониженном давлении. Выход продукта 75 после колоночной хроматографии
(градиентное элюирование: хлороформ-изопропиловый спирт, 100:1 →
хлороформ-изопропиловый спирт, 30:1) составил 700 мг (66%); т.пл. 274 оС,
[б]546 -25о (c 1,0; хлороформ).
1Н ЯМР
(DMSO-d6, 400 МГц): 1,83с (3H, NAc), 1,98с (3H, OAc), 2,03с (6H,
OAc), 3,79с (3Н, ОCH3), 4,10м
(5Н, Н-2, Н-6аb, ОCH3), 4,23м
(2Н, Н-5, Н-6аb), 4,97дд
(1Н, Н-4, J4,5 10,0 Гц), 5,27дд (1Н, Н-3, J3,4 10,0 Гц),
5,52д (1Н, Н-1, J1,2 8,0 Гц), 7,28дд (3Н, NPh),.
7,51с (1Н, СНаром.), 7,54д (2Н, NPh), 7,72с
(1Н, СНаром.), 7,8д (2Н, СНаром.), 8,16д (1Н, NН, J2,NH
8,0 Гц), 8,32д (2Н, СНаром.).
Синтез
8-[4-(2-aцетамидо-3,4,6-три-О-ацетил-2-дезокси-в-D-глюкопиранозилокси-3-метокси)фенил]-5,6-диметокси-1-фенил-3-этилпиразо[4,5-c]изохинолина
(77)
Схема 20
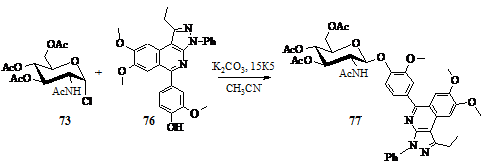
Аналогично, по методике синтеза
соединения (75) из 400 мг (1,1 ммоль) б-хлорида 73 и 483 мг (1,1 ммоль)
пиразолоизохинолина 76 получили продукт 77 с выходом 420 мг (49%); т.пл. 230оС,
[б]546 -6,25о (c 1,0; хлороформ).
1Н ЯМР
(DMSO-d6, 400 МГц): 1,50т (3Н, СН3), 1,82с (3H, NAc),
1,98с (3H, OAc), 2,03с (6H, OAc), 3,80с (3Н, ОCH3), 3,83с
(3Н, ОCH3), 4,08м
(6Н, H-2, Н-5, Н-6аb, ОCH3), 4,25дд
(1Н, Н-6аb, J6a,6b 12 Гц),
4,97дд (1Н, Н-4, J4,5 10,0 Гц), 5,29дд (1Н, Н-3, J3,4 10,0
Гц), 5,49д (1Н, Н-1, J1,2 8,0 Гц), 7,35м (3Н, NPh),.
7,44с (1Н, СНаром.), 7,54м (3Н, NPh, СНаром.),
7,66с (1Н, СНаром.), 8,15д (1Н, NН, J2,NH 12,0 Гц), 8,35д
(2Н, СНаром.).
Синтез
8-[4-(2-aцетамидо-3,4,6-три-О-ацетил-2-дезокси-в-D-глюкопиранозилокси)фенил]-5,6-диметокси-1-фенил-3-этилпиразо[4,5-c]изохинолина
(79)
Схема 21
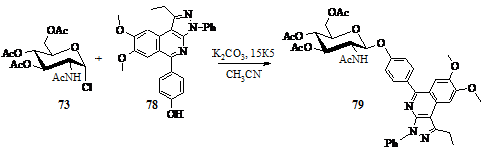
Аналогично, по методике синтеза
соединения (75) из 500 мг (1,4 ммоль) б-хлорида 73 и 562 мг (1,4 ммоль)
пиразолоизохинолина 78 получили продукт 79 с выходом 636 мг (60%); т.пл. 269 оС,
[б]546 -8,33о (c 1,0; хлороформ).
1Н ЯМР
(DMSO-d6, 400 МГц): 1,51т (3Н, СН3), 1,83с (3H, NAc),
1,98с (3H, OAc), 2,03с (6H, OAc), 3,8с (3Н, ОCH3), 4,08м
(5Н, Н-2, H-6ab, ОCH3), 4,23м
(2Н, Н-5, H-6ab), 4,97дд (1Н, Н-4, J4,5 10,0 Гц), 5,27дд
(1Н, Н-3, J3,4 10,0 Гц), 5,55д (1Н, Н-1, J1,2 8,0 Гц),
7,27м (3Н, NPh),.
7,52с (1Н, СНаром.), 7,55д (2Н, NPh.), 7,66с
(1Н, СНаром.), 7,8д (2Н, СНаром.), 8,17д (1Н, NН, J2,NH
12,0 Гц), 8,33д (2Н, СНаром.).
Синтез 8-[4-(2-aцетамидо-3,4,6-три-О-ацетил-2-дезокси-в-D-глюкопиранозилокси)фенил]-3-метил-5,6-диметокси-пиразо[4,5-c]изохинолина
(81)
Схема 22
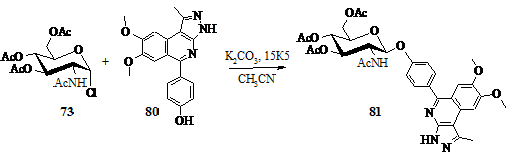
Аналогично, по методике синтеза
соединения (75) из 300 мг (0,8 ммоль) б-хлорида 73 и 288 мг (0,8 ммоль)
пиразолоизохинолина 80 получили продукт 81 с выходом 230 мг (42%); т.пл. 248 оС,
[б]546 -8,33о (c 1,0; хлороформ).
1Н ЯМР
(DMSO-d6, 400 МГц): 1,83с (3H, NAc), 1,97с (3H, OAc), 2,02с (6H,
OAc), 2,82 с (3Н, СН3), 3,76с (3Н, ОCH3), 4,08м
(5Н, Н-2, H-6ab, ОCH3), 4,23м
(2Н, Н-5, H-6ab), 4,97дд (1Н, Н-4, J4,5 8,0 Гц), 5,26дд
(1Н, Н-3, J3,4 10,0 Гц), 5,50д (1Н, Н-1, J1,2 8,0 Гц),.
7,21д (2Н, СНаром.), 7,46с (1Н, СНаром.), 7,67с (1Н, СНаром.),
7,71д (2Н, СНаром.), 8,16д (1Н, NН, J2,NH 8,0 Гц), 13,29с
(1Н, NH).
Синтез 1-(2-aцетамидо-3,4,6-три-О-ацетил-2-дезокси-b-D-глюкопиранозил)-3,8-диметил-5,6-диметокси-пиразо[4,5-c]изохинолина
(83)
Схема 23

В 10 мл безводного толуола
растворили 450 мг (1,2 ммоль)
б-хлорида
73
и 300 мг (1,2 ммоль)
пиразолоизохинолина 82. В реакционную смесь внесли 471
мг (1,3 ммоль) бромида
ртути (II)
и
кипятили до полной конверсии б-хлорида 73. (ТСХ, система A). Твердую
фазу отделяли фильтрованием, осадок промывали на фильтре толуолом (2Ч5 мл),
растворитель удаляли досуха при пониженном давлении. Выход продукта 83 после
колоночной хроматографии (градиентное элюирование: хлороформ-изопропиловый
спирт, 100:1 → хлороформ-изопропиловый спирт, 30:1) составил 72 мг (10%);
т.пл. 270-275 оС, [б]546 -25о (c 1,0;
хлороформ).
1Н ЯМР
(DMSO-d6, 400 МГц): 1,48с (3H, NAc), 1,97с (3H, OAc), 1,98c (3H, OAc),
2,03с (3H, OAc), 2,76c (3Н, СН3), 2,93с (3Н, СН3),
3,96м (5Н, Н-2, H-6ab, ОCH3), 4,03с
(3Н, ОСН3), 4,21м (2Н, Н-5, H-6ab, J6a,6b 12,0
Гц), 5,04дд (1Н, Н-4, J4,5 10,0 Гц), 5,53дд (1Н, Н-3, J3,4 10,0
Гц), 6,49д (1Н, Н-1, J1,2 8,0 Гц), 7,55с (1Н, СНаром.),
7,56с (1Н, СНаром.), 8,00д (1Н, NН, J2,NH 8,0 Гц).
4. Охрана труда и безопасность в чрезвычайных
ситуациях
Дипломная работа выполнялась в лаборатории
кафедры органической и биологической химии Таврического национального
университета имени В.И. Вернадского, оборудованной с соблюдением всех правил
охраны труда. При работе неукоснительно соблюдались правила техники
безопасности, обязательные для химической лаборатории.
При выполнении дипломной работы нами
использовались следующие вещества:
2-ацетамидо-3,4,6-три-О-ацетил-2-дезокси-б-D-глюкозаминил-хлорид, изихинолин (C9H7N),
карбонат калия (K2CO3), хлороформ (CHCl3)
ацетонитрил (CH3CN), пропан-2-ол (CH3-CH(OH)-CH3),ацетон
(CH3-C(O)-CH3), бромид ртути (HgBr2),
краун-эфир (15К5) [27-30].
Общие правила техники безопасности:
) В химической лаборатории необходимо содержать
рабочее место в чистоте и порядке, следить за исправностью аппаратуры и
приборов. Перед уходом из лаборатории убрать рабочее место,
) Перед началом работы необходимо надеть
спецодежду и иметь индивидуальные средства защиты, предусмотренные инструкцией.
) Необходимо соблюдать меры предосторожности,
указанные в специальной инструкции по технике безопасности и в методическом
руководстве.
) В лаборатории категорически запрещается
принимать пищу, хранить продукты, пить, курить. Перерывы работы, связанные с
приёмом пищи и курением, делаются с ведома руководителя и только после
тщательного мытья рук.
) Категорически запрещается работать в
лаборатории одному.
) Все опыты с ядовитыми веществами проводятся в
вытяжном шкафу.
) Категорически запрещается держать в
лаборатории вещества и растворы в посуде без надписи названия вещества и
концентрации.
) Требования безопасности по окончанию работы:
• Отключит от сети все приборы,
устройства.
• Убрать с рабочих мест реактивы,
растворы.
• Тщательно вымыть использованную посуду,
колбы, пробирки.
• Произвести влажную уборку помещений.
• Проветрить помещение.
Техника безопасности при работе с кислотами и
щелочами:
) Склянки с кислотами и щелочами необходимо
переносить только в специальных ящиках, выложенных асбестом.
) Работающим с кислотами и щелочами необходимо
пользоваться резиновыми перчатками и предохранительными очками.
) Переливать кислоты и щелочи в мелкую тару
необходимо с помощью сифона или ручного насоса.
) Помнить о том, что при приготовлении растворов
серной кислоты ее необходимо переливать в воду тонкой струйкой при непрерывном
перемешивании.
) Растворять щелочи необходимо путем медленного
прибавления к воде небольших кусочков, при непрерывном перемешивании, куски
щелочи необходимо брать только щипцами.
Техника безопасности при работе со стеклом:
) Тонкостенную посуду нельзя нагревать на
открытом огне, следует использовать асбестовую сетку.
) Большие химические стаканы с жидкостью следует
поднимать только двумя руками, поддерживая одной рукой дно.
) При разламывании надрезанных стеклянных трубок
их нужно растягивать, а не сгибать.
) Вставляя стеклянную трубку в резиновую пробку,
нужно ее ввинчивать, смочив водой, вазелином или глицерином. Конец трубки должен
быть оплавлен.
.1. Карбонат калия
При работе с карбонатом калия наблюдается
изъявления слизистой носа. Вдыхание пыли может вызвать раздражение дыхательных
путей, конъюнктивит. Происходит снижение функции дыхательного аппарата.
ПДК 2 мг/м3 (по степени воздействия
на организм человека относится к веществам 3-го класса опасности).
Меры безопасности: не допускать попадания на
кожу. Все работы проводить в резиновых перчатках.
Способы защиты: производственные помещения и
лаборатории, в которых проводится работа с углекислым калием, должны быть
оборудованы приточно-вытяжной механической вентиляцией.
.2 Ацетонитрил
Не зависимо от путей поступления в организм при
остром отравлении наблюдается вначале головная боль, апатия, тошнота,
головокружение, бледность, падение температуры и кровяного давления, судороги,
потеря сознания. После выздоровления в течение некоторого времени (до 3 недель)
- депрессия, головная боль, сердцебиение, особая слабость мышц верхних
конечностей, повышенный диурез, белок в моче, повышенное содержание цианидов в
крови и роданидов в моче.
Ацетонитрил менее токсичен, чем ряд других
нитрилов жирного ряда. Как полагают, действие ацетонитрила определяется целой
молекулой в комбинации с медленно отщепляющейся СN-группой. Характерны
вызываемые ацетонитрилом, судороги, влияние на щитовидную железу и вызываемый
им отек легких.
В организме ацетонитрил предположительно
превращается в роданиды, муравьиную кислоту и аммиак. Возможно окислительное
разрушение.
ПДК 10 мг/мі; ЛД50 1670 мг/кг (по
степени воздействия на организм человека относится к веществам 2-го класса
опасности).
Меры предосторожности: избегать попадания на
кожу.
.3 Хлороформ
Наркотик, действующий токсически на обмен
веществ и внутренние органы, в особенности на печень. Смерть при отравлении
хлороформом обычно наступает от прекращения дыхания. При очень высоком
содержании хлороформа в воздухе возможна смерть от остановки сердца.
Острое отравление может вызвать тяжелые
последствия и смерть через некоторое время после вдыхания. В более легких
случаях наблюдаются рвота, головокружение, слабость, желудочные боли,
возбужденное состояние. В крови - анемия, лейкоцитоз.
Даже в относительно невысоких концентрациях
хлороформ может вызвать профессиональное хроническое отравление с
преимущественным поражением печени. При частом попадании на кожу может вызывать
дерматиты, экземы.
Наркотическая концентрация, вызывающая изменение
скорости развития рефлекторного мышечного напряжения: 0,25-0,5 мг/л при
40-минутиом вдыхании.
ПДК 120 мг/м3, класс опасности - 2.
Меры предосторожности: избегать попадания на
кожу. Все работы проводить под тягой.
Способы защиты: резиновые перчатки, нарукавники,
фартуки, противогаз.
.4 Изопропиловый спирт
Действуют сходно с этиловым спиртом, но при
равной концентрации паров сильнее его. Пары изопропилового спирта раздражают
слизистые глаз и верхних дыхательных путей.
Работающие с изопропиловым спиртом жалуются на
резь в глазах слезотечение, светобоязнь, обостряющиеся со временами. Отмечались
сужение поля зрения и конъюнктивит; признаки неврита зрительного нерва с
понижением остроты зрения. Восстановление наступило после 2 недель лечения и
прекращения работы.
ПДК 10 мг/м3, класс опасности - 2.
Меры предосторожности: фильтрующий противогаз,
местная и общая вентиляция.
.5 Ацетон
Наркотик, последовательно поражающий все отделы
центральной нервной системы. При вдыхании в течение длительного времени
накапливается в организме; токсический эффект зависит не только от
концентрации, но и от времени действия. Медленное выделение из организма
увеличивает возможность хронического отравления.
Ацетон может попадать в организм в виде паров
при дыхании, а может всасываться через кожу. На участках кожи, подвергавшихся в
течение рабочего дня воздействию ацетона, уменьшается рН и количество холестерина,
угнетается функция сальных желез, что приводит к покраснению.
ПДК 200 мг/м3, класс опасности - 3.
Меры предосторожности: избегать попадания на
кожу. Все работы проводить под тягой.
.6
Бромид ртути (II)
Интоксикация солями ртути проявляется головной
болью, саливацией, покраснением, набуханием и кровоточивостью десен, появлением
на них темной каймы сульфида ртути, стоматитом, набуханием лимфатических и
слюнных желез. Часто повышается температура. Возникают расстройства
пищеварения. В сравнительно легких случаях через 2-3 недели нарушенные функции
восстанавливаются, в тяжелых - развиваются резкие изменения в почках
(некротический нефроз). В последнем случае через 5-6 дней наступает смерть.
ПДК 0,1 мг/м3, класс опасности - 1.
Меры предосторожности: избегать попадания на
кожу. Все работы проводить под тягой.
.7 Краун-эфиры
Предварительные результаты по испытанию
токсичности на мышах по-казывают, что при разовом приеме внутрь доза 300 мг/кг
для жизни не опасна [31].
.8 Электробезопасность
При выполнении работы использовалось следующее
электрооборудование: лабораторные электроплитки, магнитные мешалки ММ-5,
компьютер. Приборы были снабжены изоляцией и заземлением, необходимым для
безопасного обращения.
Воздействия электрического тока на организм
могут быть следующими:
. Тепловое действие. Следствием теплового
действия электрической дуги, раскаленной спирали нагревательного прибора и т.д.
являются ожоги кожного покрова, практически не отличающиеся от термических
ожогов.
. Химическое действие. Прохождение тока через
электролит - плазму крови - ведет к изменению её состава и разрушению
эритроцитов. Результатом этого вида воздействия является нарушение обмена
веществ.
. Биологическое действие проявляется обычно
ярче, чем другие виды, и ведет к нарушению режима дыхания, частоты сердечных
сокращений. Примерно через 0,5-2 с от начала контакта может наступить
фибрилляция и кровообращение практически останавливается. Работа сердца
прекращается в результате повреждения нервных клеток, управляющих его
иннервацией.
Порядка 70-75 % всех электротравм приходится на
электроудар, связанный с биологическим воздействием тока на организм. Предельно
допустимым током считается ток 0,005 А. Установлено, что большая часть
электротравм происходит от напряжения переменного тока в 220 В при
непосредственном контакте с оголенными проводами и в условиях повышенной
влажности через мокрую одежду, по причине высокой её токопроводимости.
Меры предосторожности: не допускать работу с
неисправными, незаизолированными электроприборами. Не допускать попадания влаги
внутрь электроприборов. Категорически запрещается прикасаться к оголенным
токоведущим жилам и нагревательным элементам, когда прибор включен в
электросеть
4.9 Техника безопасности при работе с
персональным компьютером
) Требования безопасности перед началом работы:
[32]
• Подготовить рабочее место, убедиться в
достаточной освещенности.
• Убедиться в исправности компьютера,
произведя его внешний осмотр. При осмотре обращать внимание на наличие и
исправность предусмотренных защитных устройств токоведущих частей, исправность
коммутационных устройств кнопок, клавиш, целостность изоляции питающего кабеля,
вилок, розеток.
) Требования безопасности во время работы:
• Не оставлять компьютер включенным при
уходе с рабочего места. При длительном перерыве в работе компьютер следует
обесточить, отсоединив от сети.
• При появлении неисправностей прекратить
работу, компьютер отключить от электросети (или поступить в соответствии с
требованиями руководства по эксплуатации).
• При работе с текстами на бумаге, листы
надо располагать как можно ближе к экрану, чтобы избежать частых движений
головой и глазами при переводе взгляда. Подставку с документами необходимо установить
в одной плоскости с экраном и на одной с ним высоте.
• Во время регламентированных перерывов с
целью снижения нервно-эмоционального напряжения, зрительного и общего утомления
целесообразно выполнять комплексы упражнений, рекомендованных санитарными
нормами и правилами.
Компьютер необходимо установить на столе, где
достаточно места не только для монитора и клавиатуры, но и также - для
размещения документов. При этом расстояние от края стола до клавиатуры не может
быть менее 30 см, а от экрана монитора до работника - менее 50 сантиметров. Сам
монитор должен находиться на уровне глаз.
Необходимо помнить - постоянную работу за
компьютером ни в коем случае нельзя исполнять без регламентированных перерывов.
Причем при 8-часовой смене перерывы на 15-20 минут должны делаться через каждые
два часа работы. А в последние четыре часа 12-часовой смены - через каждые 60
минут.
5. Обсуждение результатов
Ранее сотрудниками кафедры органической и
биологической химии было показано успешное применение межфазной системы
«твердый К2СО3 - безводный CH3CN» с
использованием краун-эфира для получения широкого ряда в-D-глюкозаминидов с
агликонами различной природы [33-36]. Этот подход позволил синтезировать
фенилглюкозаминиды, несущие в о-, м- и п-положениях ароматического ядра
различные гетероароматические радикалы, такие как 1,3,4-оксдиазол-5-ил,
хинолин-4-ил, хиназолин-4-ил. Таким образом, обсуждаемый способ построения
1,2-транс-глюкозаминидной связи может быть эффективным инструментом для
введения углеводных остатков в молекулы гетероциклических соединений на основе
изохинолина - пиразолоизохинолинов, и позволит получить глюкозаминиды для
дальнейшего изучения спектра их биологических свойств.
Глюкозаминилирование пиразолоизохинолинов 74,
76, 78, 80 б-D-глюкозаминилхлоридом 73 проводили в межфазной системе «твердый К2СО3
- безводный CH3CN» с использованием катализатора 15К5 при комнатной
температуре. Реакция протекала в течение 2-3 ч при стехиометрическом
соотношении гликозил-донора и пиразолоизохинолина, 4,5-кратном избытке
основания (по субстрату - хлориду 73) и 20 моль% краун-эфира. Во всех случаях,
в реакционной среде по данным тонкослойной хроматографии присутствовали
следовые количества оксазолина и ряд не идентифицированных продуктов деструкции
углеводов. Выходы глюкозаминидов 75, 77, 79, 81 после колоночной хроматографии
составили 49-66%.
Строение целевых соединений 75, 77, 79 доказано 1Н
ЯМР - спектроскопией. В 1Н ЯМР спектрах соединений 75, 77, 79
однозначно идентифицированных как О-в-глюкозаминиды (дублеты аномерных протонов
в области 5,49-5,55 м.д. с КССВ 8,0 Гц). В спектрах также идентифицированы
сигналы скелетных протонов, протонов О- и N-ацетильных защитных групп
углеводного остатка, сделано отнесение сигналов как протонов углеводного
остатка, так и протонов агликонов.
Пиразолоизохинолин 80, содержащий свободный атом
азота пиразольного цикла, в реакции гликозилирования может привести к
образованию второго основного продукта реакции - бис-производного с различной
природой гликозидной связи. Было обнаружено, что конверсия
б-D-глюкозаминилхлорида 73 в условиях межфазного катализа сопровождалась
образованием только одного основного продукта О-гликозида 81, выход которого
составил 42%. В данных условиях атом азота пиразольного цикла не участвовал в
реакции, что однозначно подтверждено наличием в1Н ЯМР спектре
глюкозаминида 81 синглета протона группы NH
пиразольного цикла с ХС 13,29 м.д. 1,2-транс-Диаксиальное расположение протонов
в остатке N-ацетилглюкозамина подтверждается величиной КССВ 8,0 Гц и ХС 5,50
м.д. Сравнение области протонов углеводного остатка в 1Н ЯМР спектре
гликозида 75 с аналогичными областями в спектрах соединений 75, 77, 79 показало
однотипное расположение сигналов.
Для введения остатка N-ацетилглюкозамина по
свободному атому азота пиразольного цикла, реакцию б-D-глюкозаминилхлорида 73 с
пиразолоизохинолином 82 проводили с использованием бромида ртути(II)
[37, 38]. Выход целевого N-гликозида 83 оказался невысоким
- 10%, что связано с заметной деструкцией гликозил-донора в условиях реакции.
Таким образом, очевидна перспективность продолжения исследований в данном
направлении для оптимизации условий реакции глюкозаминилирования
пиразолоизохинолина 82. В 1Н ЯМР спектре N-b-гликозида
83 наблюдалось значительное смещение в слабое поле сигнала аномерного протона (d
6,49 м.д.) по сравнению с дублетами Н-1 глюкозаминидов пиразолоизохинолинов 75,
77, 79, 81 (рис. 1). При этом КССВ составила 8,0 Гц. В спектре идентифицированы
сигналы скелетных протонов, протонов О- и N-ацетильных защитных групп
углеводного остатка, а также сигналов ароматических протонов агликона с ХС 7,55
и 7,56 м.д.
Таким образом, пиразолоизохинолины 74,76,78, 80
являются удобными объектами исследования межфазных процессов гликозилирования с
целью получения глюкозаминидов для изучения их медико-биологических свойств.
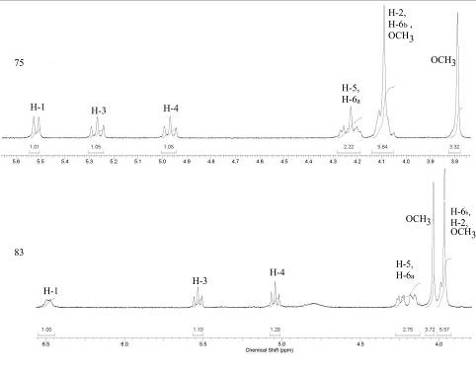
Рис. 1.
Область сигналов скелетных протонов в 1Н ЯМР спектрах соединений 75 и 83.
Выводы
. Осуществлен синтез в условиях
межфазного катализа глюкозаминидов пиразолоизохинолинов.
. Установлено, что в обсуждаемом
межфазном процессе наблюдается образование только O-в-D-2-ацетамидо-2-дезоксиглюкопиранозидов
пиразолоизохинолинов.
. Получен новый N-в-глюкозаминид
пиразолоизохинолина.
Список литературы
1. Использование производных
изохинолина в качестве лекарственных средств
#"823150.files/image025.gif">
Рисунок 1. 1Н ЯМР спектр соединения
75.
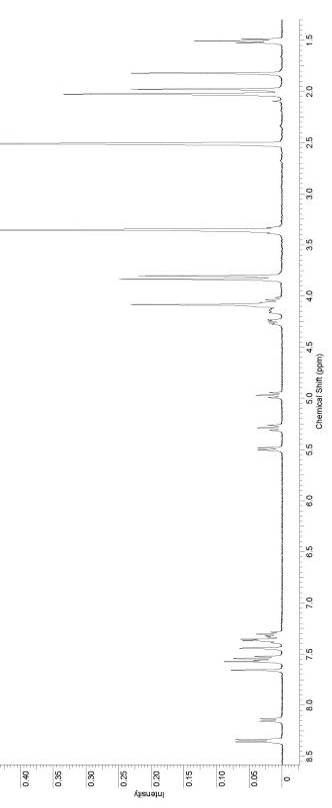
Рисунок 2. 1Н ЯМР спектр соединения
77.
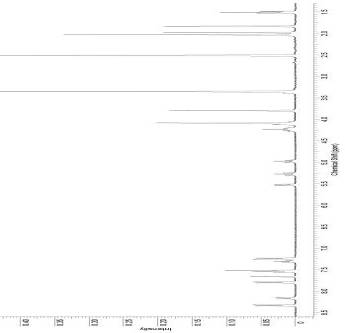
Рисунок 3. 1Н ЯМР спектр соединения
79.
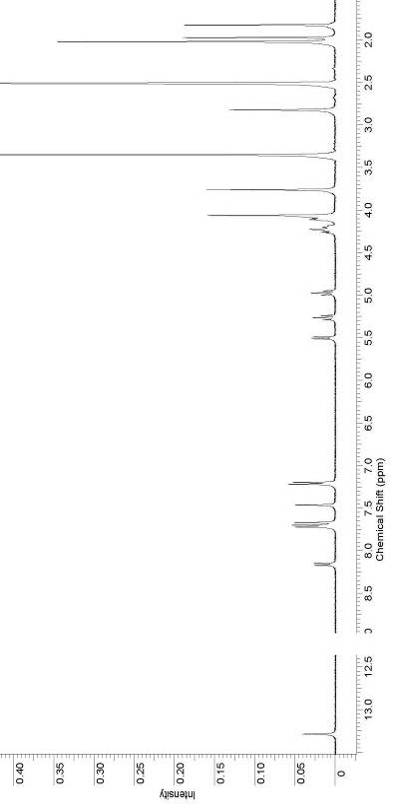
Рисунок 4. 1Н ЯМР спектр соединения
81.
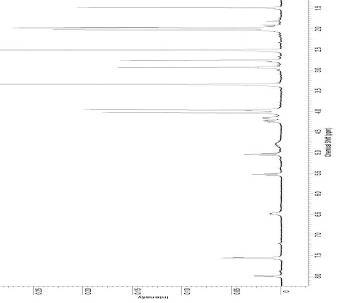
Рисунок 5. 1Н ЯМР спектр соединения
83.