Синтез 4-гидрокси-3-((4-гидрокси-2-оксо-2H-хромен-3-ил) фенилметил)-2Н-хромен-2-она и его реакция с эфиратом трехфтористого бора
КУРСОВАЯ РАБОТА
Синтез
4-гидрокси-3-((4-гидрокси-2-оксо-2H-хромен-3-ил) фенилметил)-2Н-хромен-2-она и
его реакция с эфиратом трехфтористого бора
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
.
Литературный обзор
1.1 Основные
особенности строения кумаринов
1.2 Получение
кумаринов
1.3 О-гетероциклизация
4-оксикумаринов
. Цель
исследования
2.1 Синтез исходного соединения и обсуждение
результатов
3.
Экспериментальная часть
.1 Основные
физико-химические методы, используемые в работе
.2 Список
использованных реактивов
.3
4-Гидрокси-3-((4-гидрокси-2-оксо-2Н-хромен-3-ил)(фенил)метил)-2Н-хромен-2-он
(14) и
4-гидрокси-3-((4-гидрокси-2-оксо-2Н-хромен-3-ил)(4-метоксифенил)метил)-2Н-хромен-2-он
.4 13-b-Гидрокси-7-фенил-7,7`a-дигидро-6H-пирано[3,2-с:5,6-с’]дихромен-6,8(13bH)-дион
ВЫВОДЫ
СПИСОК
ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
ВВЕДЕНИЕ
Сложнопостроенные полиоксосоединения, включающие в свой состав
кумариновый (хромен-2-оновый) фрагмент, являются весьма перспективными в
теоретическом и прикладном отношении веществами.
Известно, что многие соединения, содержащие кумариновый фрагмент, имеют
высокую фармакологическую активность, как антибактериальные, антифаговые агенты
/1/. Дикумарины, неодикумарин, фепромарон являются известными антикоагулянтами
/4-7/. Синтетические кумарины и их аналоги могут быть использованы как
антиоксиданты /2/, антимикробные /4/, антивирусные и противоопухолевые
препараты, инсектициды. Производные 4-гидроксикумарина находят свое применение
в фармацевтической промышленности, производстве духов, агрохимикатов, а также
инсектицидов.
Кумарины - это кислородсодержащие гетероциклические соединения,
производные 5,6-бензо-α-пиронов (кумарины) и 3,4-бензо-α-пиронов (изокумарины). Эти
соединения были выделены из листьев и плодов вишни, листьев мускатной земляники
и сливы, некоторых видов роз, винограда, облепихи и т.д. /1/.
.1 Основные особенности строения кумаринов
Кумарины (2-хроменоны) - обычно кристаллические вещества, бесцветные или
слабо окрашенные в желтый цвет с запахом свежескошенного сена и горьким вкусом
(порог запаха для человека 1,72.10-9 г/л). Простые кумарины, гидрокси- и
метоксикумарины и их гликозиды хорошо растворяются в воде и разведенных
спиртах. Остальные кумарины практически нерастворимы в воде, но хорошо растворяются
в органических растворителях: хлороформе, диэтиловом эфире, этиловом спирте,
кроме того, растворяются в жирных маслах.
Все природные кумарины легко возгоняются при нагревании до 1000 С.
Кумарины способны флюоресцировать в УФ-свете ярко-синим, ярко-голубым,
фиолетовым, зеленоватым или желтым светом. В присутствии щелочей флюоресценция
усиливается.
Химические свойства кумаринов обусловлены наличием в структуре
бензольного и лактонного кольца. Лактонное кольцо отличается большой
устойчивостью, не расщепляется при нагревании в воде, не взаимодействует с
аммиаком и кислотами и раскрывается лишь при нагревании с едкими щелочами. При
этом образуются соли цис-орто-кумаровой кислоты (кумаринаты) и появляется
желтое окрашивание. При подкислении раствора α-пироновое кольцо замыкается и
кумарины регенерируются в неизменном виде (окраска исчезает).
Кумарины способны к азосочетанию при взаимодействии с солью диазония в
щелочной среде. Реакции со щелочами и азосочетания используют для обнаружения
кумаринов в растительном сырье /2/.
1.2 Получение кумарина
В промышленности кумарин получают по реакции Перкина, которая заключается
во взаимодействии ароматических альдегидов с ангидридами кислот в присутствии
солей этих же кислот. Примером того служит реакция салицилового альдегида и
уксусного ангидрида в присутствии ацетата Na или К либо взаимодействии фенола с
эфирами акриловой кислоты при повышенном давлении в растворе уксусной к-ты в
присутствии ацетатов Pd и Сu2+ /3/:
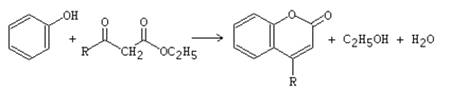
Также кумарины получают конденсацией фенолов с эфирами β-кетокислот в присутствии кислотных
катализаторов. В реакцию вступают разнообразные фенолы. Наличие донорных
заместителей в мета-положении существенно облегчает реакцию, а
орто-заместители, как правило, затрудняют ее. Кроме различных β-кислот могут быть использованы
малеиновая, фумаровая, ацетондикарбоновая и яблочная кислоты /5/.
.3 О-гетероциклизация 4-оксикумаринов
Число известных реакций О-гетероциклизации замещённых 4-оксикумаринов
весьма ограничено.
При получении натриевых солей 4-оксикумарина было замечено, что он
энергично взаимодействует с водным раствором бикарбоната натрия; при этом
выделяется углекислый газ и образуется раствор соответствующей соли. Для
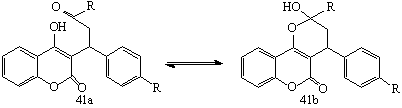
3`-производных 4-оксикумарина с общей формулой (41а) характерна пониженная
кислотность по сравнению с 4-оксикумарином. Данное явление объясняется
внутримолекулярной О-гетероциклизацией. При помощи спектроскопических методов
было выяснено, что подобные соединения существуют преимущественно в О-гетероциклической
форме (41a - 95%, 41b - 5%) /36/:
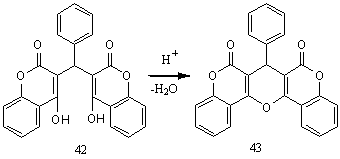
Недавно
была исследована О-гетероциклизация производного дикумарина
3,3'-(фенилметилен)бис(4-гидрокси-2H-хромен-2-она) (42), которая проходит в
кислой среде, без участия лактонного карбонила по механизму обычной
дегидратации c образованием пирана (43) /9/:
кумарин кислородсодержащий гетероциклический бензопирон
2. Цель исследования и обсуждение результатов
Анализ данных периодической печати свидетельствует, что реакционная
способность замещённых кумаринов изучена достаточно полно. Многоцентровость
молекул делает их ценными субстратами в синтезе O-, N-содержащих
гетероциклических соединений, практически важных в современной медицине. В связи
с этим, целью данной работы является синтез
4-гидрокси-3-((4-гидрокси-2-оксо-2H-хромен-3-ил)фенилметил)-2Н-хромен-2-она по
известной методике и изучение его свойств на примере реакции с эфиратом
трёхфтористого бора.
.1 Синтез исходного соединения и его взаимодействие с эфиратом
трехфтористого бора
Синтез исходного вещества осуществлялся по известной, модифицированной
методике. Соединение возникает в результате конденсации 4-оксикумарина с
бензальдегидом. Образование соединения осуществляется через интермедиат,
претерпевающий вторичную конденсацию Михаэля с молекулой 4-оксикумарина/8-9/:
Проведение
данной реакции, согласно литературным данным, возможно при кипячении реагентов
в смеси метанол-хлороформ (3:1). Было установлено, что замена данной смеси на
этанол существенно не влияет на выход продукта. Так, при осуществлении реакции
в смеси метанол-хлороформ выход составил 70%, в этаноле - 73%. Таким образом,
предложен не менее эффективный метод без использования токсичного растворителя.
|
t пл., оС
|
Элементный анализ
|
|
Вычислено
|
Найдено
|
|
207-209
|
С: 72,81; Н: 3,91
|
С: 71,98; Н: 4,02
|
Известно, что при кипячении в смеси ледяной уксусной кислоты и уксусного
ангидрида (в качестве водоотнимающего средства) имеет место внутримолекулярная
О-гетероциклизация при участии 1,5-диоксофрагмента с образованием 4Н-пиранов,
стабилизированных электроноакцепторным действием карбонильных групп.
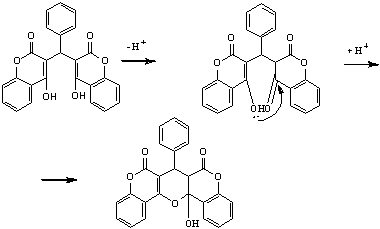
Вследствие чего, ожидаемая реакция солеобразования не произошла. Однако в
качестве продукта реакции был выделен полукеталь, что возможно вызвано наличием
воды в реакционной среде.
|
t пл., оС
|
Элементный анализ
|
|
Вычислено
|
Найдено
|
|
>300
|
С: 72,81; Н: 3,91
|
С: 72,50; Н: 3,74
|
3. Экспериментальная часть
.1 Основные физико-химические методы, используемые в работе
ИК спектры записывались на ИК Фурье-спектрометре ФСМ 1201 в таблетке с
КВr.
ТСХ анализ проводился на пластинках Silufol UV-254; элюент гексан-эфир-ацетон (3:1:1),
гексан-этилацетат-ацетон (2:2:1), проявитель - пары йода, УФ- излучение.
.2 Список использованных реактивов
Ацетонч.ГОСТ 2603-71
Гексанх.ч.ТУ 6-09-3375-73
Хлороформ ч.д.а. ТУ 6-09-1710-72
Уксусная кислота ч.д.а. ГОСТ 61-75
.3
4-Гидрокси-3-((4-гидрокси-2-оксо-2Н-хромен-3-ил)(фенил)метил)-2Н-хромен-2-он
(14) и
4-гидрокси-3-((4-гидрокси-2-оксо-2Н-хромен-3-ил)(4-метоксифенил)метил)-2Н-хромен-2-он
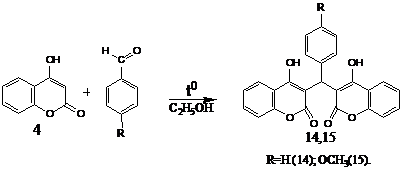
В
круглодонную колбу, снабжённую обратным холодильником, помещают 20 мл
этанола-ректификата, в котором растворяют при нагревании 5 г (3.1 ммоль)
4-гидрокси-2H-хромен-2-она 4. После его растворения добавляют 3.2
мл (3.1 ммоль) бензальдегида и кипятят в течение 48 часов. Затем реакционную
смесь охлаждают, выпавшие кристаллы соединения 14 отфильтровывают, промывают
этанолом и сушат под тягой. Получают 4.64 г (выход 73%) соединения 14, Т.пл. =
207-209оС.
.4
13-b-Гидрокси-7-фенил-7,7`a-дигидро-6H-пирано[3,2-с:5,6-с’]дихромен-6,8(13bH)-дион
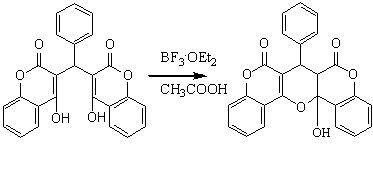
В круглодонную колбу объёмом 100 мл, снабжённую
обратным холодильником приливают смесь (3:1) 30 мл ледяной уксусной кислоты и
10 мл уксусного ангидрида, растворяют при нагревании 1 г (2.4 ммоль)
3,3’-(фенилметилен)бис(4а,8а-дигидро-2Н-хромен-2,4(3Н)-диона). Добавляют 0.34
мл (2.4 ммоль) эфирата трёхфтористого бора и кипятят реакционную смесь в
течение пяти часов. Выпавшие кристаллы отфильтровывают и промывают водой.
Получают 0.85 г. (85%) 13-b-Гидрокси-7-фенил-7,7`a-дигидро-6H-пирано[3,2-с:5,6-с’]дихромен-6,8(13bH)-диона, Тпл> 300°С.
ВЫВОДЫ
1. Обобщены
новые данные о синтетических возможностях арилметилбискумаринов, содержащих
фармакофорные фрагменты 4-оксикумарина
2. Ожидаемая
реакция с образованием соли тетраборфтората не произошла. В качестве продукта
был выделен 13-b-гидрокси-7-фенил-7,7`a-дигидро-6H-пирано[3,2-с:5,6-с’]дихромен-6,8(13bH)-дион
. Строение
синтезированного вещества доказано с привлечением данных элементного анализа
Список использованных источников
1. RDH
Murray, J. Medez, С.А. Браун, природные кумарины: Встречаемость в химии и
биохимии, New York, 2011
. М.
Maheswara, В. Siddaiah, Г. Lakishmi V. Damu, YK Рао CV Рао, журнал
Молекулярного Катализа: Химическая 255 (2012) p. 49-52
. Л.А.
Хейфиц Общая органическая химия, т. 9, М. 1985. с. 61-74
. Cook,
Journal Organic Chemistry 30, 4114 (1965)
6. Шутов Р.В.
Журнал общей химии, 2006 г., т.76 №5 с 850-857
7. Радионова
О.А. Журнал общей химии, 2012 г., т.78, вып.1,с.156-157
8. Седавкина
В.А. Конденсации ароматических соединений, 1986 г., с.4-33
. Вишнякова
Г., Смирнова Т., Курковская Л. и др. // Изв. ВУЗов. Хим. и хим. тех. 2009. №3.
С. 111-113.