Равновесные состояния при фазовых переходах
Содержание
Введение
. Равновесные состояния при фазовых
переходах
.1 Равновесие газ - жидкий раствор в
двухкомпонентных системах
.1.1 Зависимость растворимости газов
в жидкостях от природы газа и растворителя
.1.2 Зависимость растворимости газов
в жидкостях от давления
.1.3 Зависимость растворимости газов
в жидкостях от температуры
. Равновесие жидкость - жидкость в
двухкомпонентных системах
. Равновесие пар - жидкий раствор в
двухкомпонентных системах
.1 Равновесие пар-жидкий раствор в
системах с неограниченной взаимной растворимостью жидкостей
.2 Равновесие пар - жидкий раствор в
системах с ограниченной взаимной растворимостью жидкостей
.3 Равновесие пар-жидкий раствор в
системах с взаимно нерастворимыми жидкостями
. Равновесие кристаллы-жидкий
раствор в двухкомпонентных системах
.1 Диаграммы плавкости
двухкомпонентных систем
.1.1 Системы без образования
химических соединений
.1.2 Системы с образованием
химических соединений, плавящихся конгруэнтно
.1.3 Системы с образованием
химических соединений, плавящихся инконгруэнтно
.1.4 Системы с неограниченной
растворимостью компонентов в жидком и ограниченной взаимной растворимостью в
твердом состояниях
. Экспериментальная часть
Заключение
Список используемой литературы
Введение
До конца 20 в. основным методом изучения
химических систем являлся препаративный метод, основанный на выделении из
системы данного вещества различными способами(кристаллизация, перегонка и др.)
и изучении его свойств и свойств(оптических, магнитных и др.). Препаративный
метод имеет большое значение для развития химии и широко применяется до
настоящего времени, особенно в органической химии. Однако этот метод, оказался
недостаточным при изучении многих систем, таких, как растворы, расплавы, смолы,
стекла и другие многокомпонентные системы.
На базе учения о химическом равновесии был
разработан новый метод исследования химических систем- метод физико-химических
свойств химической системы от факторов, определяющих ее равновесие. В этом
методе применяются геометрический анализ диаграмм, построенных в координатах
физическое свойство- фактор равновесия(Р,Т, состав). Анализ таких диаграмм
позволяет установить протекающие в системе качественные изменения, характер
взаимодействия между компонентами, области существования и составы равновесных
фаз [1].
Гетерогенная система - система, состоящая из
нескольких фаз. Фазой называется совокупность гомогенных (однородных) частей
системы, одинаковых по составу, химическим и физическим свойствам и
отграниченных от других частей системы поверхностью. Поверхности раздела фаз
образуются некоторым количеством молекул, расположенных на границе области,
заполненной данной фазой. Молекулы, образующие поверхностный слой, находятся в
особых условиях, вследствие чего поверхностный слой обладает особыми
свойствами, не присущими веществу, находящемуся в глубине фазы. Образования,
составленные из небольшого числа молекул, не могут быть разделены на
поверхностный слой и внутреннюю массу вещества, поэтому к образованиям с очень
малым объемом понятие фаза неприменимо. Жидкие и твердые фазы называются
конденсированными.
Составляющее вещество системы - это каждое
вещество системы, которое может быть выделено из системы и существовать вне ее.
Если в системе не протекает химическая реакция, то количество каждого из
веществ не зависит от количеств других веществ. Если в системе протекает
химическая реакция, то состав фаз равновесной системы можно определить, зная
концентрацию только части веществ. Составляющие вещества, концентрации которых
определяют состав фаз данной равновесной системы, называют независимыми
составляющими веществами или компонентами системы. Свойства системы
определяются не только природой компонентов, но и их числом. Число компонентов
совпадает с числом составляющих веществ при отсутствии химической реакции или меньше
при наличии химической реакции.
1. Равновесные состояния при фазовых переходах
.1 Равновесие газ- жидкий раствор в
двухкомпонентных системах
При растворении газов в жидкостях
устанавливается равновесие между жидкой фазой, содержащей растворитель и
растворенный газ, и газовой фазой, содержащей данный газ и пары растворителя.
Если растворитель относительно мало летуч, то установится равновесие между
раствором и практически чистым растворяемым газом. Растворимость вещества
определяется его концентрацией в насыщенном растворе.
Растворимость газов в жидкостях зависит от
природы растворяемого газа и растворителя, давления газа, температуры и от
присутствия в растворе различных веществ, особенно электролитов. Растворимость
газов в жидкостях характеризуют коэффициентом растворимости α
или коэффициентом поглощения β.
Коэффициент растворимости равен объему газа, выраженному в кубических метрах,
растворенному в 1 м3 растворителя при данной температуре и
приведенному к давлению Па (1 атм). Коэффициент поглощения равен объему газа,
выраженному в кубических метрах, растворенному в 1 м3 растворителя и
приведенному к Р= Па (1 атм) и Т= 273 К.
.1.1 Зависимость растворимости газов в жидкостях
от природы газа и растворителя
Растворимость различных газов в одном и том же
растворителе при одинаковых условиях изменяется в очень широких пределах.
Растворимость газов повышается при химическом взаимодействии растворяемого газа
с растворителем.
На растворимость газов в жидкостях оказывает
влияние и природа растворителя. Если растворители относятся к одному и тому же
классу соединений, то растворимость газа часто мало зависит от индивидуальных
свойств растворителя. В присутствии электролитов растворимость газов в
жидкостях уменьшается. Влияние электролитов на растворимость газов в водных
растворах описывается уравнением И.М. Сеченова:
lg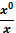
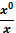 = kc (1)
= kc (1)
где х0 и х -
растворимость газа в воде и в растворе электролита соответственно; k -
постоянная, характерная для данного электролита; с - концентрация электролита,
моль/л.
Уменьшение растворимости газов в
присутствии солей называется высаливанием. Высаливающее действие иона
повышается с ростом заряда и уменьшается с увеличением радиуса иона. Уменьшение
растворимости газов в присутствии электролитов объясняется в основном тем, что
ионы притягивают молекулы воды и не притягивают неполярные и слабо поляризуемые
молекулы газов, вследствие чего увеличивается фугитивность растворенного газа.
.1.2 Зависимость растворимости газов
в жидкостях от давления
Если газ химически не
взаимодействует с растворителем, то зависимость растворимости газа в жидкости
от давления выражается законом Генри. Закон Генри справедлив только тогда,
когда растворение газа в жидкости не связано с процессами диссоциации или
ассоциации молекул растворенного газа. При наличии диссоциации или ассоциации
молекул закон Генри следует применять отдельно к каждому роду молекул,
концентрации которых не произвольны, а связаны между собой законами химического
равновесия и могут быть выражены через общую концентрацию газа в растворе. В
этом случае общая концентрация газа уже сложным образом связана с давлением
газа над раствором. Однако в ряде случаев пропорциональность сохраняется, и
тогда закон Генри остается справедливым. С изменением давления газа
растворимость различных газов меняется неодинаково, и подчинение закону Генри
наблюдается лишь в области невысоких давлений. Различие в растворимости
определяется взаимным влиянием отдельных газов друг на друга в газовой фазе и
взаимным влиянием растворенных газов в жидкой фазе. При низких давлениях, когда
взаимное влияние отдельных газов невелико, закон Генри справедлив для каждого
газа, входящего в газовую смесь, в отдельности.
.1.3 Зависимость растворимости газов
в жидкостях от температуры
При небольших давлениях
растворимость газов в жидкостях с повышением температуры обычно уменьшается.
При высоких давлениях растворимость газов в жидкостях с ростом температуры
может и увеличиваться. Так, например, растворимость водорода, гелия, неона и
других газов в органических растворителях и водорода в жидком аммиаке
увеличивается при повышении температуры. В ряде случаев растворимость газов в
жидкостях с ростом температуры проходит через минимум. Количественную
зависимость растворимости газов в жидкости от температуры можно найти из
условий равновесия между раствором, содержащим растворенный газ, и газовой
фазой, которая при малой летучести растворителя представляет собой чистый
растворяемый газ. Эта зависимость выражается уравнением:
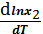
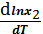 =
= 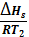
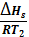 (2)
(2)
где ΔHs -изменение
энтальпии в процессе перехода 1 моль газа из газообразного состояния в состояние
насыщенного раствора или последняя теплота растворения.
При низких температурах обычно 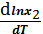
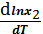 < 0, т.е. растворимость газов в
жидкостях уменьшается с ростом температуры. В области высоких температур
< 0, т.е. растворимость газов в
жидкостях уменьшается с ростом температуры. В области высоких температур 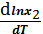
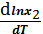 > 0, т.е. растворимость газов в
жидкостях увеличивается с ростом температуры. При температуре, которой
соответствует ΔHs = 0,
растворимость газа в жидкости будет минимальной. В небольшом температурном
интервале последняя теплота растворения практически постоянна. Тогда в
соответствии с уравнением (5) логарифм растворимости газа в жидкости линейно
зависит от 1/Т.
> 0, т.е. растворимость газов в
жидкостях увеличивается с ростом температуры. При температуре, которой
соответствует ΔHs = 0,
растворимость газа в жидкости будет минимальной. В небольшом температурном
интервале последняя теплота растворения практически постоянна. Тогда в
соответствии с уравнением (5) логарифм растворимости газа в жидкости линейно
зависит от 1/Т.
газ жидкость двухкомпонентный
плавкость
2. Равновесие жидкость-жидкость в
двухкомпонентных системах
Растворы жидкостей в жидкостях очень
разнообразны по твоей природе и свойствам. Растворимость жидкостей в жидкостях
зависит от природы растворителя и растворенного вещества, температуры,
присутствия в растворе посторонних веществ. Существуют растворы с
неограниченной взаимной растворимостью, ограниченной взаимной растворимостью и
с практически полной взаимной нерастворимостью жидкостей. Ограниченная взаимная
растворимость двух жидкостей наблюдается в системах со значительным отклонением
от идеальности. Растворимость таких жидкостей зависит от температуры. В одних
системах взаимная растворимость жидкостей с ростом температуры увеличивается
(системы с верхней критической температурой растворения), в других уменьшается
(системы с нижней критической температурой растворения). Под критической
температурой растворения понимают ту температуру, при которой составы двух
равновесных жидких фаз одинаковы. Для изображения зависимости взаимной
растворимости жидкостей от температуры при постоянном давлении строят диаграммы
состояния в координатах температура-состав (диаграммы растворимости). При
критической температуре растворения оба жидких раствора по составу
тождественны, и является условно инвариантной (С = 2 - 2 = 0).

Рис. 1. Диаграмма растворимости системы вода-
фенол с верхней критической температурой при Р= const.
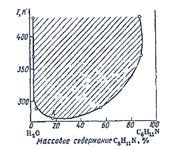
Рис. 2. Диаграмма растворимости системы вода- 2,
4, 6- триметилпиридин с нижней критической температурой при Р= const.
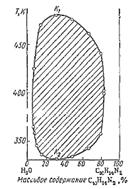
Рис. 3. Диаграмма растворимости системы вода-
никотин с верхней и нижней критической температурами при Р= const.
Иногда взаимная растворимость жидкостей
увеличивается как с повышением, так и с понижением температуры (системы с
верхней и нижней критическими температурами растворения). В некоторых системах
критические температуры растворения не достигаются, так как при повышении
температуры одна из жидкостей превращается в пар, а при понижении температуры
одна из жидкостей кристаллизуется.
3. Равновесие пар-жидкий раствор в
двухкомпонентных системах
.1 Равновесие пар-жидкий раствор в системах с
неограниченной взаимной растворимостью жидкостей
Если раствор образован из двух летучих, неограниченно
растворимых друг в друге жидкостей, то пар, находящийся в равновесии с жидким
раствором, будет содержать оба компонента. В общем случае состав пара
отличается от состава жидкого раствора, из которого он получен. При невысоких
давлениях пар можно рассматривать как смесь идеальных газов. Если пар
подчиняется законам идеальных газов и находится в равновесии с идеальным
раствором, то состав паровой фазы легко найти, зная состав жидкой фазы.
Согласно закону Дальтона общее давление пара над идеальным раствором равно
сумме парциальных давлений пара компонентов:
Робщ = ∑Рi
(Рi
=
Робщ,Xi(пар))
(3)
Во всем интервале концентраций идеального
жидкого раствора растворитель и растворенное вещество подчиняются закону Рауля:
Рi
= Рi0
Xi(ж)
(4)
Для бинарного раствора, исходя из (3) и (4),
Робщ = Р1 + Р2
= Р20 + (Р10- Р20)Х1(ж)
=Р10Х1(ж)/ Х1(п) (5)
отсюда после некоторых преобразований имеем
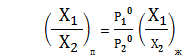
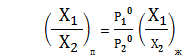 (6)
(6)
Из уравнения (6) следует, что только
при равенстве давлений пара над чистыми компонентами (Р10 =
Р20) состав пара одинаков с составом жидкого раствора, из
которого он получен. Во всех остальных случаях, даже для идеальных растворов,
состав пара отличается от состава исходного раствора.
На практике чаще приходится
встречаться с неидеальными растворами, которые не подчиняются закону Рауля. В
этих случаях состав пара определяется опытным путем. Для изучения равновесия
пар- жидкий раствор применяют два типа диаграмм состояния:
диаграммы давление пара - состав (Т
- const)
диаграммы температура кипения -
состав (Р - const)
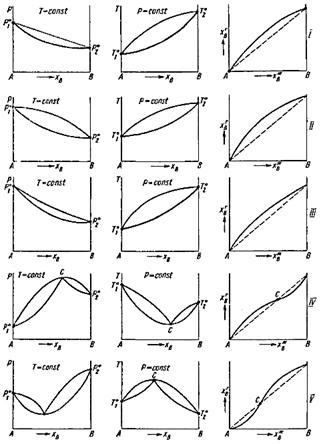
Рис.4 Различные типы диаграмм
равновесия пар- жидкий раствор
На практике для изучения равновесия
пар - жидкий раствор, чаще используются диаграммы температура-состав (диаграммы
кипения). Реальные растворы со значительным положительным или отрицательным
отклонением от идеальности способны образовывать азеотропные смеси (азеотропы),
которые на диаграммах состояния. Азеотропные смеси - это растворы, при
испарении которых получается пар того же состава, что и исходная жидкая смесь
(Х(п)=Х(ж)). Азеотропные смеси-условно инвариантные
системы (С =2-2 = 0). В реальных растворах азеотропная смесь имеет
самую низкую или самую высокую температуру кипения. При изменении внешнего
давления изменяется не только температура кипения, но и состав азеотропного
раствора. Это указывает на то, что азеотропная смесь не является химическим
соединением.
В этом случае на диаграмме состояния
появляется экстремум, лежащий в средней части диаграммы. Чем больше различие
между и, тем больше положение экстремума сдвинуто в сторону одного из
компонентов системы: при максимуме на кривой давления пара в сторону более
летучего компонента, при минимуме - в сторону менее летучего компонента.
.2 Равновесие пар - жидкий раствор в
системах с ограниченной взаимной растворимостью жидкостей
Если система образована из двух
летучих ограниченно смешивающихся жидкостей, то при испарении такой системы пар
будет содержать оба компонента и находиться в равновесии с каждой из жидких
фаз. Согласно правилу сосуществования фаз в гетерогенной системе две фазы,
порознь находящиеся в равновесии с третьей фазой, равновесны и между собой.
Следовательно, оба жидких раствора равновесны не только с паром, но и между
собой. При равновесии химический потенциал каждого из компонентов гетерогенной
системы во всех равновесных фазах одинаков:
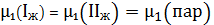
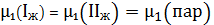 (7)
(7)
 (8)
(8)
При невысоких давлениях пар можно
рассматривать как смесь идеальных газов. Тогда

 (9)
(9)
Поскольку при заданной температуре 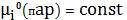
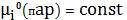 , то парциальное давление пара Рi
одного и того же компонента над обеими равновесными жидкими фазами одинаково.
Так как общее давление пара над раствором равно сумме парциальных давлений
компонентов, то при равновесии над обоими жидкими слоями общее давление пара
также одинаково. В расслаивающихся равновесных системах с изменением состава
системы составы равновесных жидких фаз не изменяются.
, то парциальное давление пара Рi
одного и того же компонента над обеими равновесными жидкими фазами одинаково.
Так как общее давление пара над раствором равно сумме парциальных давлений
компонентов, то при равновесии над обоими жидкими слоями общее давление пара
также одинаково. В расслаивающихся равновесных системах с изменением состава
системы составы равновесных жидких фаз не изменяются.
Известны два типа систем, состоящих
из ограниченно растворимых жидкостей. В системах первого типа общее давление
пара над растворами любого состава больше давлений паров чистых компонентов при
той же температуре (Р10 < Р >Р20).
В системах второго типа общее
давление пара над растворами любого состава лежит между давлениями паров чистых
компонентов при той же температуре (Р10 < Р < Р20).
Для изучения равновесия пар - жидкий
раствор в системах с ограниченной взаимной растворимостью жидкостей, пользуются
диаграммами состояния давление - состав и температура кипения - состав.
.3 Равновесие пар-жидкий раствор в
системах с взаимно нерастворимыми жидкостями
Совершенно несмешивающихся жидкостей
не существует, так как любые жидкости в какой-то степени растворимы друг в
друге. Однако если взаимная растворимость жидкостей ничтожно мала, то эти
жидкости можно рассматривать как взаимно нерастворимые. В системах, состоящих
из взаимно нерастворимых жидкостей, испарение каждой жидкости происходит
независимо от присутствия другой, и давление пара каждого компонента при данной
температуре сохраняется постоянным для любых соотношениях жидкостей.
Температура кипения смеси из двух взаимно нерастворимых жидкостей ниже
температур кипения чистых компонентов, так как общее давление паров (Р) над
системой выше давления пара каждого из компонентов в отдельности (Р10
и Р20) и равно Р = Р10 + Р20
= const(Т)
Если паровую фазу рассматривать как
смесь идеальных газов, то в соответствии с законом Дальтона состав пара можно
определить по уравнению:
Xi(пар)= 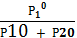
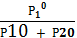 , Xi(пар)=
, Xi(пар)= 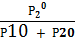
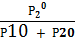 . (10)
. (10)
При заданной температуре пар такого
состава изображается фигуративной точкой. Если составы исходной жидкой смеси и
пара совпадают, то при изобарном испарении вся жидкость превращается в пар того
же состава, а при конденсации такого пара образуются два жидких слоя, суммарный
состав которых совпадает с составом исходной смеси. Если составы исходной смеси
и пара различны, например жидкая смесь, то при давлении будут испаряться обе
жидкости и образуется пар определенного состава. Дальнейшее испарение жидкого компонента
приведет к изменению состава пара и к понижению давления над жидкостью. Во всем
интервале давлений пар насыщен относительно одного компонента. После
исчезновения жидкой фазы пар становится ненасыщенным относительно обоих
компонентов и при неизменном составе будет перегреваться. При изотермическом
сжатии пара рассмотренные стадии будут происходить в обратной
последовательности. Таким образом, испарение и конденсация аналогичных смесей
характеризуются наличием некоторого интервала давлений, в котором сосуществуют
чистый жидкий компонент и паровая смесь.
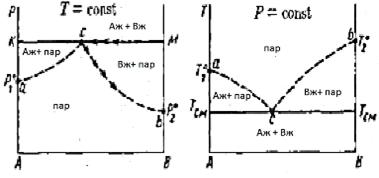
Рис. 5 Диаграмма испарения двух
несмешивающихся жидкостей.
4. Равновесие кристаллы-жидкий
раствор в двухкомпонентных системах
Растворимость твердых тел в
жидкостях зависит от природы растворяемого вещества и растворителя,
температуры, давления и присутствия в растворе посторонних веществ.
Растворимость твердых тел в
жидкостях часто резко изменяется при переходе от неорганических к органическим
растворителям. Причина различной растворимости твердых тел в различных растворителях
еще недостаточно выяснена [1]. Как показывает опыт, полярные вещества большей
частью плохо растворимы в неполярных растворителях, но хорошо растворимы в
полярных растворителях.
Количественную зависимость
растворимости твердых тел в жидкостях от температуры можно найти из условий
равновесия между насыщенным раствором и твердым растворяемым веществом. Эта
зависимость выражается уравнением:
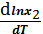
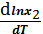 =
= 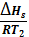
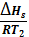 (11)
(11)
где ΔHs -изменение
энтальпии в процессе перехода 1 моль газа из газообразного состояния в
состояние насыщенного раствора или последняя теплота растворения.
ΔHs > 0,
растворимость твердых тел в жидкостях увеличивается с ростом температуры.
ΔHs < 0,
растворимость твердых тел в жидкостях уменьшается с ростом температуры.
При небольших давлениях
растворимость твердых тел в жидкостях практически не зависит от давления.
Влияние давления на растворимость проявляется при высоких давлениях(порядка 108
Па)
.1 Диаграммы плавкости
двухкомпонентных систем
Для изучения равновесия кристаллы -
жидкий раствор широко применяются диаграммы плавкости, выражающие зависимость
температур плавления смесей от их состава.
Частным случаем диаграмм плавкости
являются диаграммы растворимости, характеризующие зависимость растворимости
твердых веществ в жидкостях от температуры.
.1.1 Системы без образования
химических соединений
В системах, не образующих химических
соединений, при охлаждении расплава любого состава всегда кристаллизуются
чистые компоненты.
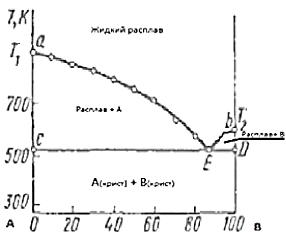
Рис. 6 Диаграмма плавкости системы
А-В
Фигуративные точки а и b изображают
температуры плавления(кристаллизации)чистых компонентов А и В(Т1 и Т2).
При этих температурах системы условно инвариантны. При температурах выше Т1
или Т2 соответствующие чистые компоненты находятся в расплаве, при
температурах ниже Т1 или Т2 - в твердом состоянии.
Фигуративные точки, лежащие на кривых аЕ и bE(линии
ликвидуса), характеризуют температуры, при которых из жидких расплавов
начинается кристаллизация компонента А или В.
В отличие от чистых компонентов
кристаллизация(плавление)большинства двухкомпонентных систем происходит не при
постоянной температуре, а в определенном температурном интервале, которое
определяется составом системы. Минимальная температура при которой
заканчивается кристаллизация расплава любого состава(или начинается плавление
твердой двухкомпонентной системы), называется эвтектической температурой(Тэ).
Линия сD, отвечающая
Тэ, ниже которой не может существовать жидкая фаза, называется линия
солидуса. Фигуративная точка Е(точка пересечения линий ликвидуса с линией
солидуса), характеризует состав расплава, который находится в равновесии
одновременно с кристаллами компонентов А и В. Смесь кристаллов компонентов А и
В, выпадающая из этого расплава при Тэ называется эвтектической
смесью(эвтектика). Система условно инвариантна в точке Тэ = cоnst.
.1.2 Системы с образованием
химических соединений, плавящихся конгруэнтно (совпадающий) [1]
Плавление называется конгруэнтным,
если состав жидкости совпадает с составом твердого химического соединения, из
которого жидкость образовалось. Такие химические соединения являются
устойчивыми и плавятся без разложения. Диаграмма плавкости двухкомпонентной
системы с образованием одного химического соединения, плавящегося конгруэнтно,
приведена на рисунке 7 на которой указаны области и равновесные фазы.
Так как в рассматриваемой системе Мg- Pb образуется
одно химическое соединение, то из расплава могут кристаллизоваться три твердые
фазы: компонент А(Мg), компонент В(Pb), и
химическое соединение- PbМg2.
Прибавление Мg или Pb к
химическому соединению приводит к понижению температуры начала кристаллизации
из расплава химического соединения.
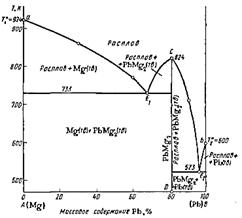
Рис. 7 Диаграмма плавкости системы Мg- Pb при Р=const.[1]
Линия ликвидуса Е1СE2 конгруэнтно
плавящегося химического соединения имеет максимум в фигуративной точке С,
отвечающей температуре плавления(кристаллизации) химического соединения.
Положение этого максимума строго соответствует составу образующегося
химического соединения. Фигуративные точки, лежащии на линии СD,
соответствуют твердому химическому соединению при разных температурах.
.1.3 Системы с образованием
химических соединений, плавящихся инконгруэнтно
Плавление называется инконгруэнтным
(несовпадающий), если состав жидкости не совпадает с составом твердого
химического соединения, из которого жидкость образовалась. Такие химические
соединения являются неустойчивыми и разлагаются при более низких температурах,
чем их температура плавления. Диаграмма плавкости двухкомпонентной системы с
образованием одного химического соединения, плавящегося инконгруэнтно, на
которой указаны области и равновесные фазы в системе, приведена на рисунке 8.
При образовании химического
соединения, плавящегося инконгруэнтно, максимум, отвечающий температуре
плавления этого соединения (фигуративная точка F), не
реализуется и попадает в область, находящуюся под линией ликвидуса одного из
компонентов ( в системе CuCl-KCl компонента
В).
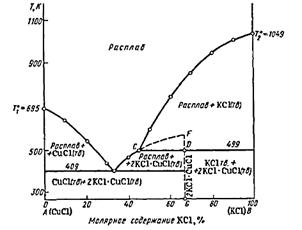
Рис. 8 Диаграмма плавкости системы CuCl-KCl при Р= cоnst[1]
Такой максимум называется скрытым.
Это связано с тем, что химическое соединение устойчиво только до температуры,
отвечающей фигуративной точке D. При этой температуре химическое
соединение распадается на жидкий расплав (фигуративная точка С) и кристаллы
компонента В. Точка С называется переходной или перитектической точкой. В
процессе распада химического соединения расплав находится в равновесии с двумя
твердыми фазами (химическое соединение и компонент В), поэтому система условно
инвариантна. При исчезновении кристаллов химического соединения система
становится условно моновариантной. Линия DG-линия
твердого химического соединения.
.1.4 Системы с неограниченной
растворимостью компонентов в жидком и ограниченной взаимной растворимостью в
твердом состояниях
В системах с ограниченной взаимной
растворимостью компонентов в твердом состоянии из расплавов кристаллизуются не
чистые компоненты, а твердые растворы. Диаграммы плавкости таких систем могут
быть двух типов, на которых указаны области и равновесные фазы в обеих
системах. В системах первого типа состав эвтектического расплава (фигуративная
точкаE) является промежуточным
между составами равновесных с ним твердых растворов В в А и А в В (фигуративные
точки С и D). В
системах второго типа перитектический расплав (фигуративная точка E) более
богат компонентом В по сравнению с равновесными с ним твердыми растворами
(фигуративные точки С и D). Характерной особенностью системы,
в которых из расплавов кристаллизуются твердые растворы, является то, что при
увеличении содержания в системе одного из компонентов температуры начала
кристаллизации твердых растворов могут повышаться (линия bE). При
кристаллизации из расплавов твердых растворов изменяется как состав сплава, так
и состав твердого раствора.
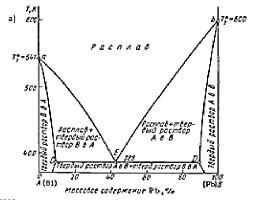
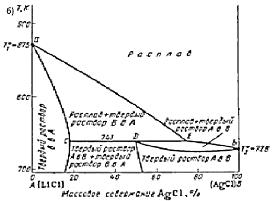
Рис. 9 Диаграмма плавкости системы
при Р= cоnst а) Bi- Pb; б)LiCl- AgCl
Экспериментальная часть[5]:
Построение диаграммы плавкости
двухкомпонентной системы легкоплавких веществ (нафталин- дифениламин)
Задача: построить диаграмму
плавкости двухкомпонентной системы.
Поместили в восемь пробирок
диаметром 2,5- 3 см 5 г смеси следующего состава таблица 1.
Закрыли пробирки пробками, в отверстия которых
вставлены термометры со шкалой 150-200 °С и латунные мешалки. Пробирки
поочередно опускали в водяную баню, нагретую на 10-15 °С выше температуры
плавления нафталина(80°С). Когда содержимое пробирки расплавилось и несколько
перегрелось, пробирку вытерли насухо и перенесли в более широкую пробирку.
Через каждые 30 секунд по секундомеру отмечали температуру, непрерывно
помешивая смесь.
Таблица 1. Таблица состава смеси нафталин-
дифениламин.
|
Нафталин,
%
|
0
|
15
|
45
|
60
|
75
|
90
|
100
|
|
Дифениламин,
%
|
100
|
85
|
55
|
25
|
10
|
0
|
|
Нафталин,
г
|
0
|
0,75
|
2,25
|
3
|
3,75
|
4,5
|
5
|
|
Дифениламин,
г
|
5
|
4,25
|
2,75
|
2
|
1,25
|
0,5
|
0
|
При появлении первых кристаллов помешивание
прекращали и отмечали температуру. Для индивидуальных веществ и сплавов
эвтектического состава наблюдения прекращали после температурной остановки,
сделав после этого еще 3-4 отсчета.
Таблица 2. Результаты эксперимента.
|
Нафталин,
%
|
0
|
15
|
45
|
60
|
75
|
90
|
100
|
|
Дифениламин,
%
|
100
|
85
|
55
|
40
|
25
|
10
|
0
|
|
Т(смеси),
°С
|
78
|
70
|
28
|
38
|
44
|
49
|
52
|
В данной системе, при охлаждении расплава любого
состава всегда кристаллизуются чистые компоненты. Т1 и Т2 изображают
температуры плавления(кристаллизации)чистых компонентов А и В. При этих
температурах система условно инвариантна. При температурах выше Т1
или Т2 соответствующие чистые компоненты находятся в расплаве, при
температурах ниже Т1 или Т2 - в твердом состоянии.
Фигуративные точки, лежащие на кривых Т1Е и Т2E(линии
ликвидуса), характеризуют температуры, при которых из жидких расплавов
начинается кристаллизация компонента А или В. Минимальная температура при
которой заканчивается кристаллизация расплава любого состава(или начинается
плавление твердой двухкомпонентной системы), называется эвтектической температурой(Тэ).
Линия ab, отвечающая
Тэ, ниже которой не может существовать жидкая фаза, называется линия
солидуса. Фигуративная точка Е(точка пересечения линий ликвидуса с линией
солидуса), характеризует состав расплава, который находится в равновесии
одновременно с кристаллами компонентов А и В. Смесь кристаллов компонентов А и
В, выпадающая из этого расплава при Тэ называется эвтектической
смесью(эвтектика). Система условно инвариантна в точке Тэ = cоnst.
Заключение
Препаративные методы уходят в прошлое и на смену
им приходят новые методы. Люди стараются предугадать результаты своих
экспериментов и в этом им помогают фазовые диаграммы. Диаграммы состояния
используют в материаловедении, металлургии, нефтепереработке, химической
технологии (в частности, при разработке методов разделения веществ),
производствах электронной техники и микроэлектроники. С ее помощью определяют
направленность процессов, связанных с фазовыми переходами, осуществляют выбор
режимов термообработки, отыскивают оптимальные составы сплавов. Анализ таких
диаграмм позволяет установить протекающие в системе качественные изменения,
характер взаимодействия между компонентами, области существования и составы
равновесных фаз. Диаграммы состояния системы позволяют описывать ее свойства
при различных температурах.
Список используемой литературы
1. К.С. Краснов «Физическая химия»
том I, Москва «Высшая школа» 2001г
. Д.Г. Кнорре «Физическая химия», Л.
Ф. Крылова, В. С. Музыкантов; Москва «Высшая школа» 1990 г
. А.М. Захаров «Диаграммы состояния
двойных и тройных систем», Москва, «Металлургия» 1990 г
. В.В. Еремин «Основы физической
химии. Теория и задачи» Учебное пособие для вузов, Москва, «Экзамен» 2005 г
. Р.А. Дулицкая «Практикум по
физической и коллоидной химии», Москва, «Высшая школа», 1978