|
Вітамін C
<#"821021.files/image001.jpg">
В молекулі вітаміну В12 розрізняють:
. Порфіринове, хромотофорне,
або коринок кільце, що пов’язане з атомом кобальту чотирма координаційними
зв’язками через атоми азоту.
. Верхнім координаційним
лігандом кобальта у вітаміні В12 являється ціаногрупа. Її місце можуть займати
інші неорганічні або органічні замісники, наприклад NO22-,
SO22-, OH-,
H2O,
CH3+, аденозин;
замісники визначають назви похідних вітаміну.
. шоста позиція кобальту
зайнята нуклеотидним ядром (нижнім лігандом кобальту), що складається з азотної
основи та залишку фосфорної кислоти. Нуклеотидне ядро пов’язане з кобальтом
через азот основи, а з кориновим кільцем через амінопропаноловий місток.
У складі вітаміну В12 або
ціанокобаламіну азотиста основа представлена 5,6-диметилбензімідазолом
(5,6-ДМБ). Наявність 5,6-ДМБ визначає активність молекули корриноїдів для вищих
тварин. Замість 5,6-ДМБ мікроорганізми можуть включати в молекулу інші
бензімідазольні та пуринові основи. Нуклеотидне ядро може бути відсутнім, як у
випадку фактору В [5].
2.1.1
Продуценти вітаміну В12
У природі вітамін B12 і корриноїдні
сполуки знаходять місце в клітинах мікроорганізмів, в тканинах тварин і деяких
вищих рослинах (горох, лотос, пагони бамбука, листя і стручки квасолі). Проте
походження вітаміну B12 у вищих рослинах остаточно не встановлено. Такі нижчі
еукаріоти, як дріжджі і міцеліальні гриби, корриноїди, напевно, не утворюють.
Організм тварин не здатний до самостійного синтезу вітаміну. Серед прокаріотів
здатність до біосинтезу корриноїдів широко поширена. Активно продукують вітамін
В12 представники роду Propionibacterium [1, 4, 5]. Природні штами
пропіоновокислих бактерій утворюють 1,0-8,5 мг/л корриноїдів, але отримано
мутант Р. shermanii М-82, за допомогою якого отримують до 58 мг/л
вітаміну [1,5]. У сімействі Propioni bacberiaceae є й інші представники,
здатні до високого накопичення вітаміну B12 в клітинах. Це, перш за все, Eubacterium
limosum, Butyribacterium rettgerii. Як продуценти вітаміну практичний
інтерес мають багато представників актиноміцетів і споріднених мікроорганізмів
[1, 4]. Істинний вітамін B12 в значних кількостях синтезує Nocardia rugosa.
Шляхом мутацій і відбору отримано штам N. rugosa, що накопичує до 18
мг/л вітаміну B12. Активні продуценти вітаміну виявлено серед представників
роду Micromonospora: M.purpureae, M.echinospora, M.halophitica, M.fusса,
M.chalceae. Високою кобаламінсинтезуючою активністю володіють метаногенні
бактерії, наприклад Methanosarcina barkeri, M.vacuolataі окремі штами
галофільних видів Methanococcus halophilus [1, 4]. Останній організм
синтезує більше 16 мг корриноїдів на грам біомаси. Настільки високого вмісту
корзиноїдів не відзначено в жодного іншого з вивчених мікроорганізмів. Причина
високого вмісту корриноїдів у метаногенних бактерій не встановлена. Корриноїди
синтезують строго анаеробні бактерії з роду клостридій. У Clostridlum
tetanomorphum і Cl. sticklandil аденозилкобаламін входить до складу
ферментних систем, що каталізують специфічні реакції ізомеризації таких
амінокислот, як глютамінова кислота, лізин і орнітин. У значних кількостях
утворюють вітамін B12 ацетогенні клостридії Cl.thermoaceticum,
Cl.formicoaceticum і Acetobacter woodi, що синтезують ацетат з СО2. Відомі
активні продуценти вітаміну B12 у псевдомонад, серед яких краще за інших
вивчений штам Pseudomonas denitrificans MB-2436 - мутант, який дає на
оптимальному середовищі до 59 мг/л корриноїдів. Інтерес представляють
термофільні бацили, а саме Bacillus circulans і Вас.stearothermophilus,
які ростуть відповідно при 60 і 75 °С і за 18 год культивування без дотримання
стерильних умов дають високі (2,0-6,0 мг/л) виходи вітаміну. Корриноїди
синтезують Rhodopseudomonas palustris, фототрофні пурпурні бактерії Rhodobactersphericus,
Rh.capsulatus, Rhodospirillumrubrum, Chromatiumuinosumі та ряд інших видів.
Значні кількості вітаміну B12 утворюють ціанобактерії Anabaena cylindrica,
одноклітинні зелені водорості Chlorella pyrenoidosae і червоні водорості
Rhodosorus marinus [6].
Продуценти вітаміну B12 культивують
в середовищах, приготованих на основі харчової сировини: соєвого борошна,
рибного борошна, м'ясного і кукурудзяного екстракту. В останні роки виявлені
мікроорганізми, що утворюють якісні корриноїди при утилізації нехарчової
сировини. Achromobacter sp., використовуючи ізопропіловий спирт як
джерело вуглецю та енергії, накопичує до 1,1 мг/л провітаміну, Pseudomonas
sp. синтезує вітамін B12 в середовищі з метанолом або пропандіолом (до 160
мкг/л), факультативний метилотроф утворює в середовищі з метанолом до 2,6 мг/
вітаміну. Виділено штам Klebsiella 101, який утворює велику кількість
корриноїдів в клітинах тільки при зростанні на середовищі з метанолом як
єдиному джерелі вуглецю та енергії [5].
2.1.2
Біосинтез вітаміну В12
Кожна структура в молекулі вітаміну:
корриноїдне кільце, нуклеотидне ядро і амінопропіленовий місток - мають своє
походження. Механізм їх виникнення - предмет інтенсивних, але ще не завершених
досліджень. Перші етапи біогенезу корриноїдів ті ж, що і перші етапи синтезу
інших тетрапірольних сполук (рис.2.2). Загальним інтермедіатом тетрапіролів є δ-амінолевулінова
кислота (δ-АЛК),
що утворюється у більшості організмів в результаті конденсації гліцину та сукциніл-КоА.
Однак Е.limosum
i C.tetanomorphum
не включають 2-14С-гліцин в коринове кільце, що
слід було очікувати, якщо б гліцин був попередником δ-АЛК.
Отже, вже на цьому етапі шлях синтезу вітаміну у бактерій може відрізнятися.
Потім утворюється порфобіліноген,
який виникає при конденсації двох молекул δ-АЛК,
а при конденсації чотирьох молекул порфобіліногену - уропорфіриноген ІІІ (УПГ
ІІІ). Послідовність реакцій між між УПГ ІІІ і кобіриновою кислотою отримала
експериментальне підтвердження лише останні роки. Показано, що при порушенні
процесу амідування клітини Propionibacterium
shermanii
виділяють в середовище сполуки, які названі коррифіринами - метильовані
відновлені похідні уропорфірину ІІІ. До теперішнього часу виділено і
охарактеризовано три сполуки: коррифірин-1 (метилкоррифірин), коррифірин-2 або
сірогідрохлорин (диметилкоррифірин) та коррифірин-3 або ізобактеріохлорин
(триметилкоррифірин). Мічена δ-АЛК
і метіонін включаються в коррифірини, а останні - у вітамін В12.

Рисунок 2.2 - Шлях біосинтезу
корзинової структури вітаміну В12 [7]
Метилювання УПГ ІІІ з одночасним
декарбоксилуванням бокового ланцюга оцтової кислоти при С12 кільця С призводить
до розходження шляхів біогенезу вітаміну В12 та інших тетрапіролів. В
результаті подальшого метилування та утворення С-С зв’язку між кільцями А і Д
синтезується кобіринова кислота.
Донором семи метальних груп, які
включаються в УПГ ІІІ, є S-аденозилметіонін. Характер включення Со і утворення
безпосереднього зв'язку між кільцями А і Д невідомий. На наступному етапі
біосинтетичного шляху кобіринова кислота перетворюється в кобінамід (фактор В),
при цьому залишки карбонових кислот кобіринової кислоти амідуються, а до
залишку пропіонової кислоти кільця Д приєднується амінопропанол. На цій же
стадії відбувається приєднання до корзинового кільця
5-дезоксиаденозилкобінамідом (кофермент на форма фактора В). Амінопропанол,
напевно, утворюється при декарбоксилуванні L-треоніну.
Далі кобаламід фосфорилюється з
утворенням кобінамідфосфату і, реагуючи з гуанозинтрифосфатом (ГТФ), дає
кобінамідгуанозиндифосфот. До коферментної форми кобінамідгуанозиндифосфоту
включається нуклеотид і утворюється кобаломін-5’-фосфат.
Вітамін В12, як уже відмічалось
вище, містить специфічну азотисту основу - 5,6-ДМБ, яка в природі зустрічається
лише в одній сполуці. Безпосереднім попередником 5,6-ДМБ служить рибофлавін. В
молекулу вітаміну В12 5,6-ДМБ включається у вигляді α-рибазол-5’-фосфату.
При ферментативному дефосфорилюванні кобаломін-5’-фосфату утворюється
кобаломін. Послідовність реакцій при синтезі кобаломіну із кобаламіду така:
1) кобінамід + АТФ = кобінамід-Ф +
АДФ;
) кобінамід-Ф + ГТФ = ГДФ-кобінамід
+ФФн;
) ГДФ-кобінамід + α-рибазол-5’-фосфат
= кобаломін-5’-фосфат + ГМФ;
) кобаломін-5’-фосфат = кобаломін +
Фн.
Відомі дві коферментні форми
вітаміну В12: аденозилкобаламін (І) і метилкобаламін (ІІ). Понад 80 % всіх
синтезовани пропіоновокислими бактеріями корриноїдів знаходиться в коферментній
формі І, яка в якості ліганда містить 5-дезоксиаденозил.
Джерелом аденозину служить АТФ.
Коферментна форма містить Со-С-зв’язок і є першою кобальт органічною сполукою,
що знайдена в живих системах. Метилкобаламін зазвичай міститься в клітинах у
незначних кількостях, але у M.barkeri
метил-фактор ІІІ, який містить в нуклеотидній частині 5-оксибензімідазол,
складає 80 % від суми усіх корриноїдів.
Регуляція біосинтезу вітаміну В12
здійснюється за принципом репресії. Вітамін В12 пригнічує лише свій особистий
синтез, не впливаючи на утворення іншиз тетрапіролів і діє на стадії
метилування УПГ ІІІ. В якості регулятора виступає лише повна нуклеотидвмісна
молекула вітаміну. Гем здійснює координовану репресію синтезу ферментів
початкових стадій біогенезу тетрапіролів.
Функціональною формою вітаміну є
аденозилкобаламін (α-(5,6-диметилбензімідазоліл)-Со-5-дезоксиаденозилкобамід)
і метилкобаламін (α-(5,6-диметилбензімідазоліл)-Со-5-метилкобамід)
[5].
2.2 Вітамін
В2 (рибофлавін)
Рибофлавін, також вітамін В2, або
лактофлавін (рис.2.3) - вітамін, що бере участь в процесах росту, пластичному
обміні; регуляторно впливає на стан центральної нервової системи, процеси в
рогівці, кришталику ока, забезпечує світловий і кольоровий зір.; входить до
складу ферментів, які регулюють важливі етапи обміну речовин, позитивно впливає
на стан шкіри та слизових оболонок, функцію печінки та кровотворення.
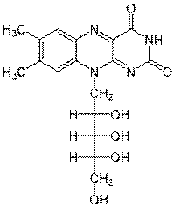
Рисунок 2.3 - Структура рибофлавіну
[8]
Рибофлавін (вітамін
В2,7,8-диметил-10-(1’-D-рибітил-ізоалоксазин)
був виділений в кристалічному вигляді у 1993 році. В основі будови флавінів, до
яких відноситься рибофлавін, лежить гетероциклічна ізоалоксозанова система, яка
представлена трьома конденсованими циклами: ароматичним (А), піразиновим (В) і
піримідиновим (С). До азоту піразонового кільця приєднаний спирт рибіт
(рис.2.4).
Рибофлавін функціонує в коензимних
формах, що представляють собою його фосфорні ефіри: флавіномононуклеотид (ФМН)
і флавінаденіндинуклеотид (ФАД). В останні десятиліття відкриті нові
біокаталітичні чинники ізоалоксозанові структури, функціональні групи яких
представлені модифікованими молекулами РФ, ФМН, ФАД.
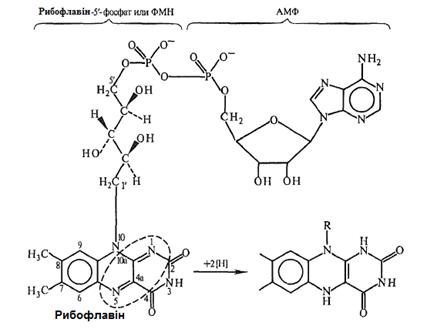
Рисунок 2.4 - Структура флавінів [7]
2.2.1
Продуценти рибофлавіну
Продуцентами рибофлавіну в природі є
вищі рослини, дріжджі, міцеліальні гриби і бактерії. Більшість мікроорганізмів
утворює вільний рибофлавін і дві його коферментні форми - ФМН і ФАД. З багатьох
бактерій і цвілевих грибів виділені аналоги РФ і їх коферментні форми. Вивчення
особливостей біосинтезу РФ різними групами мікроорганізмів показало, що він, як
правило, утворюється у більших кількостях, ніж потрібно для задоволення потреби
клітини в цьому вітаміні. Серед прокаріотів флавіногенною групою вважають
мікобактерії і ацетонобутилові бактерії. З актиноміцетів значні кількості РФ
синтезують Nocardiae ritropolis. Серед цвілевих грибів найбільш активні
продуценти рибофлавіну - гриби роду Aspergillus (Asp. Niger). Активні
продуценти рибофлавіну Eremothecium ashbyii, Ashbyii gossypii [1, 4, 5].
2.2.2
Біосинтез рибофлавіну
Шлях синтезу рибофлавіну (рис.2.5)
встановлений в результаті досліджень, виконаних з грибом Eremothecium
ashbyii, на мутантах Saccharomyces cerevisiae, Pichiaguillier mondii
і мутантах бактерій Вас. subtilis. Розшифровці шляху сприяли дослідження
з міченими сполуками і здійснення ранніх реакцій біосинтезу in vitro.
Попередником РФ служить гуанозинтрифосфат (ГТФ). Пуриновое кільце ГТФ
локалізується в гетероциклічному ядрі РФ, а рибозне ядро включається в
рибітильний ланцюг РФ.
На 1-му ступені під дією ферменту
ГТФ-циклогідролази ІІ з імідазольного кільця ГТФ видаляється С-8. Продуктами
першого ступеню є форміат, пірофосфат і
2,5-диаміно-4-гідрокси-6-рибозиламінопіримідин-5’-фосфат. Рибозне ядро ГТФ
відновлюється. На 2-му етапі біогенезу за участю відповідної редуктази відбувається
відновлення рибози останньої сполуки (ІІ) з утворенням
2,5-диаміно-4-гідрокси-6-рибітиламінопіримідмн-5’-фосфату (ІІІ), яка при
дезамінуванні дає 2,4-дигідрокси-5-аміно-6-рибітиламінопіримідин-5’-фосфат (ІV).
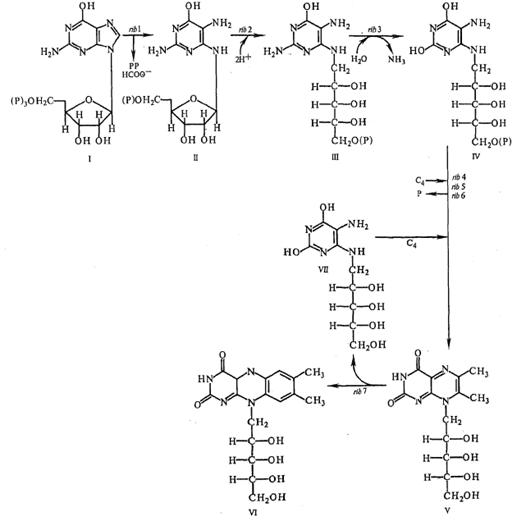
І - ГТФ; ІІ - 2,5-диаміно-4-гідрокси-6-рибозиламінопіримідин-5’-фосфат;
ІІІ - 2,5-диаміно-4-гідрокси-6-рибітиламінопіримідмн-5’-фосфату; ІV
- 2,4-дигідрокси-5-аміно-6-рибітиламінопіримідин-5’-фосфат; V
- 6,7-диметил-8-рибітиллюмазину;
VІ - рибофлавін; VІІ
- 2,4-дигідрокси-5-аміно-6-рибітиламінопіримідин
Рисунок 2.5 - Шлях біосинтезу рибофлавіну у
дріжджів [7]
На наступному ступені відбувається включення
чотирьох вуглецевих атомів з утворенням птеридину -
6,7-диметил-8-рибітиллюмазину (V).
Ця сполука виділена з E.ashbyii,
A.gossypii,
Cl.acetobutylicum,
представників видів Candida.
Показано, що донором чотирьох вуглецевих атомів може бути рибозо-5-фосфат або
його метаболіт. Перед включенням в птеридин (V)
піримідиновий інтермедіат (ІV)
піддається дефосфорилюванню. На останньому етапі дві молекули
6,7-диметил-8-рибітиламінопіримідину (VІІ).
Остання сполука (VІІ)
знову включається у реакцію синтезу 6,7-диметил-8-рибітиллюмазину.
Згідно з ступенями біосинтезу РФ, що
розглядалися, є 5 груп біохімічних мутантів. Перша група мутантів не
накопичувала в середовищі піримідинів і птеридинів, внаслідок блокування 1-ї
реакції флавіногенезу. Мутанти другої групи накопичували
2,5,6-триаміно-4-гідроксипіримідин або його рибозильоване похідне. Після
взаємодії з диацетилом ці сполуки перетворюються в 6,7-диметилптерин.
Мутанти третьої групи акумулювали
2,5-диаміно-4-гідрокси-6-рибітиламінопіримідин, що дає в результаті взаємодії з
диацетилом 6,7-диметил-8-рибітиллюмазин, що флюорисценціює зеленим кольором.
Мутанти четвертої групи накопичували
2,4-дигідрокси-5-аміно-6-рибітиламінопіримідин, так як не синтезували
люмазиновий інтермедіат (V),
а мутанти п’ятої групи виділяли в середовище 6,7-диметил-8-рибітиллюмазин [8].
2.3
Ергостерин (вітамін D)
Ергостерин (ергоста-5,7,22-трієн-3β-ол)
- це стерол, знайдений у грибах, назва якого походить від "ergot"
(ріжки), грибу із роду Claviceps, із якого ергостерин був вперше
виділений. Ергостерин не зустрічається в рослинних або тваринних клітинах. Він
є компонентом клітинних мембран дріжджів та грибів, виконуючи ту ж саму
функцію, що холестерин виконує у тваринних клітинах.
Оскільки ергостерин - це провітамін
вітаміну D2, ультрафіолетове опромінювання трав'яного матеріалу, що містить
гриби, може привести до вироблення вітаміну D2 [5] але треба відзначити, що це
не є справжнє вироблення D вітаміну рослиною, а перетворення ергостерину
грибного походження у активну форму під дією УФ-випромінювання.
Ергостерин - вихідний продукт
виробництва жиророзчинного вітаміну D2 і кормових препаратів, збагачених вітаміном
D2. В групу вітамінів D об'єднують споріднені сполуки, найважливішими з яких є
вітаміни D2 і D3, що володіють антирахітичною дією. Вітамін D2
(ергокальциферол) утворюється при опроміненні ультрафіолетовим випромінюванням
ергостерину, вітамін D3 (холекальциферол) утворюється з 7-дегідрохолестерину. В
організмі людини і тварин ці сполуки регулюють засвоєння кальцію і фосфору з
їжі і відкладення їх в кістковій тканині.
В основі структури ергостерину і
вітаміну D лежить чотири вуглецевих цикли (А, В, С, D). У разі вітаміну D
кільце В розімкнуте. Вуглеводнева структура ергостерину і вітаміну D визначає
їх ліпофільні властивості.
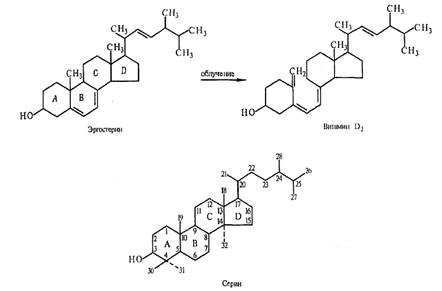
Рисунок 2.7 - Реакція переходу
ергостерину у ергокальциферол [7]
2.3.1
Продуценти ергостерину
Джерелом ергостерину є фітопланктон,
бурі і зелені водорості, але особливо багаті на ергостерин дріжджі і цвілеві
гриби, які і служать сировиною для його промислового отримання [1,4,5].
Відносно ергостерол синтезуючої здатності (% ергостеролу в абсолютно сухих
дріжджах) дріжджі при поверхневому культивуванні розташовуються в наступному
порядку: Saccharomyces. carlsbergensis (0,49-4,3), S. ellipsoidetis
(1,2-1,5), Rhodotorula glutinis (0,7-0,9), Candidautilis
(0,4-0,6), С. tropicalis (0,2-0,3). В міцелії грибів Aspergillus
і Penicillium вміст стеринів може досягати 1,2-1,4%; (Р. westlingii близько
2,2%) у розрахунку на сухий міцелій [1, 5]. Бактерії, як правило, синтезують
незначні кількості стеринів. Зазвичай вміст стеринів в їхніх клітинах складає
0,001-0,1 мг/г сухої біомаси. Стерини виявлені у Lactobacillus arabinosus,
L. pentosus, Escherichia coli, Azotobacter chroococcum, Micromonosporasp.,
Streptomyces griseus, Sphaerotillis natans, Rhodospirillum rubrum.
2.3.2
Біосинтез ергостерину
Стерини відносяться до терпенів і
мають шлях біосинтезу, що підкоряється «изопреновому правилу». Відповідно до
цього правила, стерини (тритерпени) синтезуються з ізопренових одиниць в
результаті проходження чотирьох стадій:
) утворення мевалоната з ацетил-КоА
або лейцину;
) дегідратація і декарбоксилювання
мевалонілпірофосфата з утворенням «активного ізопрену» - ізопентенілпірофосфату
і конденсація ізопренових ланок з утворенням ациклічних терпенів різної
довжини;
) циклізація ациклічних структур;
) подальша модифікація циклічної
структури. Інтермедіатами синтезу стеринів є ацетат, мевалонової кислоти,
сквален, ланостерин.
Сквален - загальний попередник
стеринів рослинного і тваринного походження, накопичується в дріжджах і при
аерації перетворюється на стерин. Розбіжність шляхів відбувається на рівні
фарнезилпірофосфату:
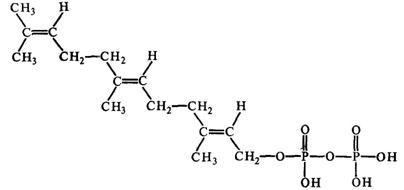
У разі стеринів він димеризуется з
утворенням сквалену:
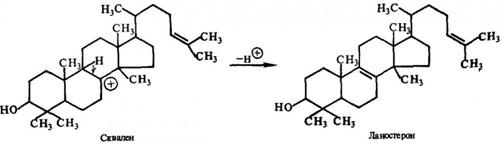
Перетворення лангостерину в
ергостерин відбувається в результаті наступни стадій:
) диметилювання лангостерину;
) транс алкілування з утворенням
24(28)-метиленової групи і одночасним відновленням С-24(25) подвійного зв’язку;
) десатурації бокового ланцюга з
утворенням С-22(23) подвійного зв’язку;
) ізомеризації Δ8
Δ7;
5) дегідрування з утворенням Δ5;
Послідовність реакцій точно не
встановлена, але виділений ряд речовин, які розглядають як інтермедіати на
шляху до ланостерину та ергостерину. Вважають, що ферменти, які беруть участь
на пізніх стадіях ергостерину, локалізуються в мікротомах дріжджів.
2.3.3 Умови
утворення ергостерину дріжджами
Найбільш високі кількості стеринів
синтезують штами Saccharomyces
carlsbergensis
ІНМІ-101 і Sacch.
carlsbergensis.
Біомаса Sacch.
carlsbergensis
може містити більше 10% ергостерину. Важлива умова синтезу ергостерину
дріжджами - хороша аерація. В анаеробних умовах в клітинах
дріжджів накопичується попередник ергостерину - сквален. Показано, що кисень
індукує синтез стеринів, надаючи активуючий вплив на епоксідазу сквалена -
першого ферменту біосинтетичного
шляху. Індукція синтезу ергостерину починається при 0,03% -ому вмісті О2 в
газовій фазі і досягає максимуму при 2% -вій концентрації.
Для біосинтезу стеринів дріжджами важливо, щоб середовище
містило великий надлишок вуглеводів і мало азоту. Дріжджі, багаті білком, як
правило, містять мало стеринів. Ці дані стосуються головним чином пекарських
дріжджів. У разі дріжджів роду Candida високое C/N в середовищі
призводить до накопичення ліпідів, а не ергостерину. Для дріжджів, що
використовують н-алкани, останні є кращим джерелом вуглецю для синтезу
ергостерину, ніж вуглеводи. Стимулюючу дію на утворення стеринів дріжджами
надають інгібітори гліколізу та роз'єднувачі окисного фосфорилювання і дихання,
а також забезпеченість дріжджів вітамінами, і перш за все пантотеновою
кислотою, яка у складі КоА бере участь у побудові молекули ергостерину. При дії
на дріжджі рентгенівського випромінювання вміст ергостерину збільшується в 2-3
рази, що пояснюють пригніченням процесу амінування, що супроводжується
підвищенням синтезу ліпідів. Синтез стеринів не пов'язаний з ростом дріжджів.
Вміст стеринів підвищується в міру старіння культури і стериноутворення триває
після зупинки росту дріжджів [8].
2.4 Каротиноїди
і вітаміну А (ретинол)
Вітамін А (рис.2.7) - група близьких
за хімічною будовою речовин, яка включає ретиноїди: ретинол (вітамін A1,
аксерофтол), дегідроретинол (вітамін А2), ретиналь (ретинен, альдегід вітаміну
A1), ретиноєву кислоту і кілька провітамінів - каротиноїдів, серед яких
найважливішим є β-каротин.
Ретиноїди містяться в продуктах тваринного походження, а каротиноїди - у
рослинних продуктах. Усі ці речовини добре розчиняються в неполярних органічних
розчинниках і погано розчиняються у воді. Депонуються в печінці, здатні
накопичуватися в тканинах. У разі передозування вітамін виявляє токсичність [9].
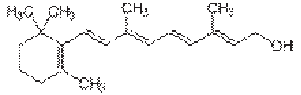
Рисунок 2.7 - Структурна формула
вітаміну А [9]
Вітамін було відкрито 1913 року.
1931 року було описано його структуру, а 1937 року його вдалося кристалізувати
[2].
Попередником вітаміну А при його
біосинтезі є каротиноїди, а саме - β-каротин.
Каротиноїди - найбільш багато
чисельна і широко розповсюджена група природних пігментів. Їх утворюють вищі
рослини, водорості, фототрофні бактерії та ряд хемотрофних бактерій. Крім того,
каротиноїди синтезують деякі міцелі альні гриби і дріжджі.
Присутні каротиноїди також в
організмі деяких членистоногих, риб, птахів та ссавців, а надходять з їжею і
слугують джерелом збагачення організму вітаміном А.
Каротиноїди знаходяться у рослин та
мікроорганізмів у вільній формі, можуть утворювати глікозиди, каротино-білкові
комплекси, але значно частіше зустрічаються у вигляді ефірів довго ланцюгових
жирних кислот.
Зазвичай каротиноїди складаються з
вісьми ізопренових залишків, які з’єднані таким чином, що дві найближчі до
центру молекули метальні групи знаходяться в положенні 1:6, а інші метильні
групи - в положенні 1:5. Усі каротиноїди можна представити, як утворені із
структури, яка має довгий центральний ланцюг кон’югованих подвійних зв’язків
(рис.2.8).
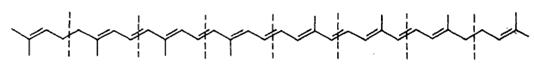
Рисунок 2.8 - Поліен, з якого шляхом
гідрування, дегідрування, окиснення, циклізації та інших реакцій можливий
синтез різних каротиноїдів
Одна з відмінностей каротиноїдів від
інших природних сполук - наявність хромофору, який містить спряжені подвійні
зв’язки, число яких у найбільш розповсюджених каротиноїдів (β-каротин,
γ-каротин
та ін.) складає 10 - 11, а може досягати п’ятнадцяти. Від числа спряжених
подвійних зв'язків в молекулі поліенів залежать наявність забарвлення і її
інтенсивність. Аліфатичні поліени, що містять до п'яти пов'язаних подвійних
зв'язків, -сполуки незабарвлені. Серед них найбільший інтерес представляють
попередники каротиноїдів - фітон і фітовлуїн. Ці сполуки являють собою масла,
що містять відповідно три і п'ять пов'язаних подвійних зв'язків. В нейроспорині
присутні дев'ять пов'язаних подвійних зв'язків, і він вже має виражене жовте
забарвлення. Зі збільшенням числа подвійних зв'язків у молекулі каротиноїдів
відбувається поглиблення забарвлення від жовтого до оранжевого, червоного і
фіолетового.
В останнє десятиліття з різних
природних джерел виділено ряд каротиноїдів, які за хімічною структурою
відрізняються від описаних раніше. Це так звані вищі каротиноїди, що
складаються з 45 або 50 атомів вуглецю. В їх молекулі містяться додаткові
С5-одиниці, що займають 2- або 2,2'- положення. С50-каротиноїди широко поширені
у мікроорганізмів, в основному у нефотосинтезуючих; до таких каротиноїдів
відноситься, наприклад, сарцинаксантин (рис.2.9, А), утворений Sаrcina
lutea.
Іншим прикладом каротиноїдів, що
мають
незвичайну структуру, є пігменти, які
містять термінальну метиленову групу, наприклад алеуреаксантин гриба Aleuria
aurantia
(рис.2.9,
Б). Виділено також α-гідроксикаротиноїди,
серед яких найбільш поширений α-гідроксифлеїксантин
(рис.2.9, В). Виявлені каротиноїди, що мають у своїй молекулі п’ятичленне
кільце і кетогрупи, наприклад актиноеритрин (рис.2.9, Г), а також арилкаротиноїди,
що містять триметилфенильні кінцеві групи, і каротиноїди глікозиди (рис2.9, Д).
Нещодавно відкрита ще одна група
каротиноїдів - це ω-фе-
нілзаміщені поліенові карбоксилової кислоти, етерифіковані 2,5-диалкілованим
резорцином (флексірубін, хлорофлексірубін), що утворюються Flexibacter
elegans
та Cytophaga
johnsonae.
У природі зустрічаються також
каротиноїди, що містять менше 40 атомів вуглецю. Вони отримали назву
апокаротиноїдів - це, наприклад, β-цитраурин
(З-гідроокси-8-апо-каротин-8'-ал), властивий деяким рослинам, триспорові
кислоти грибів, вітамін А та ін.
В даний час вивчено хімічну будову
більш 500 каротиноїдів. Завдяки вдосконаленню фізико-хімічних методів
дослідження число відомих нам пігментів, постійно збільшується.
вітамін біосинтез
ретинол рибофлавін
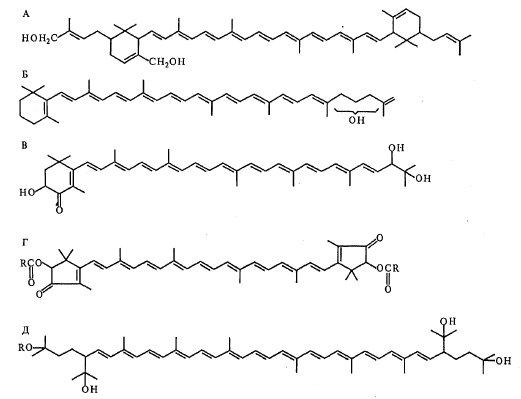
А- сарцинаксантин; Б-
алеуреаксантин; В- α-гідроксифлеїксантин;
Г- актиноеритрин; Д-бактеріоруберин моноглікозид
Рисунок 2.9 - Структурні формули
деяких каротиноїдів [7]
2.4.1
Біосинтез каротиноїдів
Дослідження, в яких застосовувалася
радіоактивна мітка (14С), а також вивчалося утворення каротиноїдів в
присутності специфічних інгібіторів і мутантами мікроорганізмів, дозволили
встановити, що біосинтез цих пігментів проходить у декілька етапів.
1. Утворення первинного С5-попередника.
Стартовою сполукою в біосинтезі каротиноїдів є ацетат. Дві молекули ацетил-КоА
конденсуються з утворенням ацетоаце-тил-КоА, який в свою чергу конденсується ще
з однією молекулою ацетил-КоА, утворюючи 3-гидрокси-3-метилглутарил- КоА. При
відновленні цієї сполуки утворюється мевалонова кислота (МВК), остання в
присутності АТФ фосфорилюється з утворенням пірофосфату МВК. У присутності АТФ
шляхом декарбоксилювання і дегідрування пірофосфат МВК перетворюється в
5-вуглецеву изопренову одиницю - ізопен- тенілпірофосфат (рис.2.10).
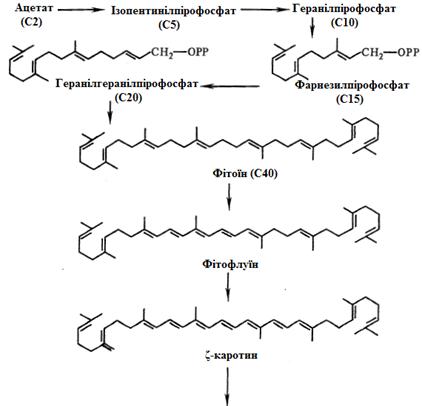
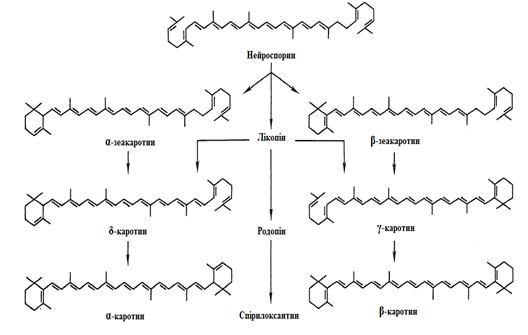
Рисунок 2.10 - Біосинтез
каротиноїдів мікроорганізмами [7]
2. Біосинтез безбарвних
С40-поліенів з С5-попередника.
Ізопентенілпірофосфат (ІПФ) ізомеризується до стадії диметилалілпірофосфата
(ДМАПФ). Потім відбувається конденсація ІПФ і ДМАПФ з утворенням
геранілпірофосфата. Ці сполуки, що містять 10 атомів вуглецю, конденсуються з
ІПФ і утворюють фарнезилпірофосфат, з якого шляхом подальшої конденсації виникає
20-вуглецева одиниця - геранілгеранілпірофосфат. Останній димеризуется,
утворюючи фітоін (7,8,11,12,7 ', 8', 11’, 12’ -октагідро-ψ-ψ-каротин)
- перший С40-попередник каротиноїдів.
Центральний хромофор фітоїну, що
складається з трьох спряжених подвійних зв'язків, передбачає існування кількох
стереохімічних ізомерів. В природних об'єктах фітоїн представлений двома
ізомерами: 15-цис-. і 15-транс-фітоїн. Як правило, перший ізомер переважаючий,
другий - зустрічається у вигляді слідів. Однак у деяких мікроорганізмів весь
фітоїн може бути представлений 15-транс-ізомером. Характер ізомеру фітоїну
визначає конфігурацію наступних попередників біосинтезу каротиноїдів, зокрема
фітофлуїну
3. Кінцеві стадії синтезу
каротиноїдів (дегідрування, циклізація, введення кисневмісних груп і
С5-одиниць). Утворення каротиноїдів з
фітоїну відбувається при послідовному дугідруванні останнього. Першим продуктом
цієї реакції є С40-поліен-фітофлуїн. При подальшому дегідруванні фітофлуїну
утворюються вже забарвлені каротиноїди - нейроспорин і лікопін (рис.2.10). Ці
сполуки піддаються потім послідовній циклізації з утворенням поліенів, що
містять α-
або β-іононові кільця
(наприклад, α-
або β-каротинів).
Використання нейроспорину або лікопіну як проміжного продукту при біосинтезі
каротиноїдів залежить від умов вирощування та особливостей ферментної системи
організму.
Встановлено, що α-
і β-іононового кільця
каротиноїдів утворюються із загального ациклічного попередника (рис.2.11),
механізм циклізації якого відрізняється в разі синтезу α-
і β-іононового кілець.
Із нейроспорину (або L-каротину)
виникають α-
і β-зеакаротини -
попередники α-
і β-каротинів
відповідно. Введення кисневмісних груп в молекулу каротиноїдів відбувається
зазвичай після закінчення процесу циклізації, тобто синтез ксантофілів
здійснюється після утворення каротинів.
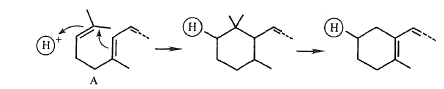
Рисунок 2.11 - Механізм
реакції
циклізації
при
утворенні
β-іононового
кільця. А - загальний ациклічний попередник при утворенні α-
і
β-іононового
кілець
[7]
Утворення С50-каротиноїдів також
відбувається після синтезу С40-каротиноїдів (каротинів). Встановлено, що
С50-бактеріоруберін утворюється шляхом приєднання С5-ізопренових одиниць до
кінцевих частин молекули лікопіну з наступним введенням гідроксильних груп
після етапу циклізації. Вважвють, що в даному випадку додаткові С5-одиниці
можуть ініціювати циклізацію каротиноїдів (етапи циклізації і приєднання
С5-одиниць можуть відбуватися одночасно). Нециклічним попередником
С50-каротиноїдів є лікопін. Отже, при циклізації цих поліенів не відбувається
інтерконверсії β-, ε-
і -γ-кілець. Для
утворення деяких С50-каротиноїдів, наприклад дегідрогенанса-Р434 Flavobacterium
denydrogenans,
необхідною умовою є наявність світла [10].
2.4.2
Біосинтез вітаміну А (ретинолу)
Природний вітамін А1-спирт (ретинол)
включає β-іононове
кільце і бічний ізопреноїдний ланцюг, що складається з двох залишків
метилбутадієну. Попередником вітаміну А є β-каротин.
Окислювання цього поліену при утворенні вітаміну А відбувається в організмі
тварин двома шляхами.
1. β-каротин
розщеплюється по центральному подвійного зв'язку та за участю
каротиндиоксигенази утворюються дві молекули ретиналю (альдегідна форма
вітаміну А). Останній відновлюється НАДН2 в ретинол під дією
алкогольдегідрогенази. Далі ретинол ферментативно етерифікується в
ретинілпальмітат, що депонується в печінці.
. У кишечнику β-каротин
розщеплюється по центральному подвійному зв'язку за участю НАДФН2-залежної
каротиноксигенази. При цьому утворюються апокаротиналі і низькомолекулярні
продукти окислення. Апокаротиналі далі за участі ферменту, локалізованого в
мітохондріях і мікросомах, перетворюються в апокаротинові кислоти, що володіють
біологічною активністю вітаміну А в функції росту.
Засвоєння вітаміну А відбувається в
кишечнику ссавців, де протікають процеси емульгування і міцелоутворення, а
також ряд біохімічних реакцій (гідроліз, етерифікация, утворення білкових
комплексів).
Субстратами при утворенні вітаміну А
можуть бути також інші каротиноїди, наприклад α-каротин
і ксантофіли. Однак при цьому вітаміну А утворюється значно менше порівняно з β-каротином.
Вітамін А в організмі людини і
тварин виконує ряд дуже важливих функцій. Перш за все він бере участь в процесі
зору. При нестачі в організмі вітаміну А не відбувається утворення світлочутливого
пігменту родопсину в паличках сітківки ока. У сприйнятті світла беруть участь
також такі пігменти, як йодопсин і порфіропсин, до складу яких входить ретинен1
і ретінен2 відповідно. Родопсин складається з ліпопротеїну опсину і ізомеру
вітаміну А альдегіду 11-цис-ретиналю.
Крім участі в процесі сутінкового
зору і адаптації ока в темряві, вітамін А необхідний для нормального росту,
розвитку і диференціювання тканин, виконує роль радіопротектора при
рентгенівському опроміненні, регулює процеси розмноження, володіє
антиінфекційним властивостями, посилює антивірусну резистентність. Відсутність
вітаміну А являєтся причиною керотинізації епітелію клітин слизових оболонок,
залоз, шкіри. Одна з основних функцій вітаміну А - регуляція проходження
метаболітів через мембрани [9, 10].
2.5 Вітамін
С (аскорбінова кислота)
Аскорбíнова
кислотá (гамма-лактон
2,3-дегідро-L-гулонової кислоти, вітамін C) C6H8O6, відносно проста органічна
кислота, яка міститься у свіжих фруктах (яблука, сливи, персики і т.д.) та
овочах (морква, капуста, буряк, картопля та ін.).
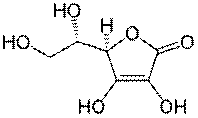
Рисунок 2.12 - Структурна формула
вітаміну С [11]
Не синтезується у організмі людини і
надходить лише з продуктами харчування. Розчиняється у воді і руйнується при
тривалому кип'ятінні, тому вимочування або переробка овочів знижує вміст у них
вітаміну С. Велика кількість вітаміну C міститься в лимонах, плодах шипшини,
червоного перцю, смородини, зеленої цибулі. Добова потреба людини в
аскорбіновій кислоті досить велика - 63-105 мг. Нестача аскорбінової кислоти
може привести до цинги. Отримана 1934 Тадеушем Рейхштейном, швейцарським
хіміком, нобелянтом.
Вітамін С виконує в організмі два
основні завдання: забезпечення імунного захисту і стабілізації психіки. Вітамін
С найкращий засіб для збереження життєвої сили. Коли бракує С в людей
кровоточать ясна, часті простуди, загроза запалення слизових оболонок, зайва
вага, підвищувана втомлюваність, слабкі нерви, погана концетрація уваги,
депресивний стан, безсоння, раннє утворення зморшок [1].
2.5.1
Біосинтез вітаміну С
Аскорбінова кислота, або вітамін С -
це протицинготний вітамін, наявний у всіх вищих рослин і тварин; тільки людина
і мікроорганізми не синтезують її, але людям вона невідкладно необхідна, а
мікроби не потребують її. І, тим не менше, певні види оцтовокислих бактерій
причетні до біосинтезу напівпродукту цієї кислоти - L-сорбози. Таким чином,
весь процес отримання аскорбінової кислоти є змішаним, тобто
хіміко-ферментативним.
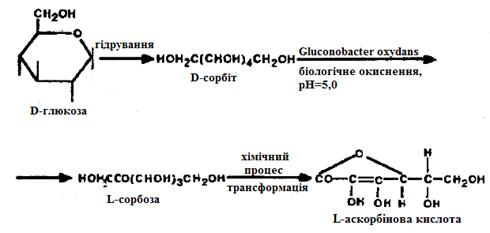
Рисунок 2.13 - Шлях біосинтезу
аскорбінової кислоти [12]
Біологічна стадія процесу
каталізується мембранозв'язаною поліолдегідрогеназою, а остання (хімічна)
включає послідовно наступні етапи: конденсація сорбози з діацетоном та
отримання діацетон-L-сорбози, окислення діацетон-L-сорбози до
діацетон-2-кето-L-гулонової кислоти, яку піддають потім гідролізу з отриманням
2-кето-L-гулонової кислоти; останню піддають енолізації з
подальшою трансформацією в L-аскорбінову кислоту. Ферментацію G.oxydans
проводят на середовищах, що містять сорбіт (20%), кукурудзяний або дріжджовий
екстракт, при інтенсивній аерації (8-10 г О2/л/год). Вихід L-сорбози може
досягти 98% за одну-дві доби. При досягненні культурою log-фази можна додатково
внести в середовище сорбіт, доводячи його концентрацію до 25%. Також
встановлено, що G.oxydans може окисляти і більш високі концентрації
поліспиртів (30-50%), що утворюються на останніх стадіях процесу. Це
відбувається завдяки поліолдегідрогеназі, що міститься в клітинній біомасі.
Ферментацію бактерій проводять в періодичному або безперервному режимі.
Принципово доведена можливість отримання L-сорбози з сорбіту за допомогою
іммобілізованих клітин в ПААГ [5]. Аскорбінову кислоту використовують як
антиоксидант в охороні здоров'я та харчовій промисловості.
ВИСНОВКИ
Отже, вітаміни необхідні будь-якому
організму: починаючи з мікроорганізмів і закінчуючи макроорганізмами.
Вважається що для нормального функціонування людини достатньо тих вітамінів,
які або синтезуються мікроорганізмами у нього в організмі, або надходять в
організм з їжею. Може раніше цього й вистачало, але зараз з нашою екологією,
неправильним харчуванням, з вживанням різних консервантів, з величезною
кількістю шкідливих звичок і т.д. люди все частіше стали стикатися з проблемою
браку в організмі вітамінів (гіпо-та авітаміноз). І доводиться вживати вітаміни
у вигляді лікарських препаратів, що продаються в аптеці. І якщо раніше вітаміни
виробляли хімічним шляхом (він і зараз превалює), то зараз більша перевага
віддається вітамінам, виробленим мікробіологічним шляхом. По-перше це все-таки
не хімічні реактив, а вітаміни, вироблені живими організмами і по-друге вони
краще засвоюються в організмі і менше виводяться з нього не приносячи користі.
Але все ж залишаються вітаміни, вироблені за змішаною технологією: вітамін С, і
ще не багато виробляються мікробіологічними шляхом: B2, B12, D, β-каротин,
налагоджується виробництво біотину.
Загалом можна зробити висновок:
майбутній розвиток вітамінного виробництва за біотехнологами. І це є важливим
завданням для них, яке ще потрібно вирішити.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
1. Промышленная микробиология: Учеб.
пособие для вузов П 81 по спец. “Микробиология” и “Биология” / З.А. Аркадьева,
А.М. Безбородов, И.Н. Блохина и др.; Под ред..
<http://cityadspix.com/tsclick-GQB3V9J0-VRMIQUYF?url=http%3A%2F%2Fwww.enter.ru%2Freg%2F13242%2Fproduct%2Ffurniture%2Fuglovoy-divan-krovat-versal-atlanta-2050600011249&sa=&bt=20&pt=9<=1&tl=3&im=Mjc3NS0wLTE0MTQwOTkxMTUtMTUyMjcwODc%3D&prdct=0234013604340d3706&kw=%D0%9F%D0%BE%D0%B4%20%D1%80%D0%B5%D0%B4..>
Н.С. Егорова. - М.:Высш. шк., 1989. - 688с.
2. Мюллер Э., Лёффлер В.
Микология: Пер. с нем. - М.: Мир, 1995. - 343 с.
. Куликов П.И.
Производство муки, жира, и белково-витаминных препаратов в рыбной
промышленности. / - Москва: Пищевая промышленность, 1991.
. Шнайдман Л.О.
Производство витаминов. / - Москва: Пищевая промышленность, 1973. - 443с.
. Mantzouridoua F.,
Tsimidou M.Z. On the monitoring of carotenogenesis by Blakeslea trispora using
HPLC // Food Chemistry. - 2007. - Vol.104. - № 1. - P.439-444.
6. Никтин Г.А. Биохимические
основы микробиологических производств: Учеб. пособие. - Киев: Вища школа.
Головное изд-во, 1981. - 312 с.
7. Елинов
Н.П.
Основы биотехнологии. - СПб.: Наука, 1995. - 600 с.
. Н.А. Шмалько, И.И. Уварова,
Ю.Ф. Осляков. Амарантовая мука - антиоксидантная добавка для макаронных
изделий, обогащенных β-каротином //
Пищевая технология. - 2004г. - №5-6. - стр. 39-41.
. К.К. Полянский, Л.В.
Голубева, О.И. Долматова, Д.В. Дорохина. Изучение реологических свойств видов
молочных консервов с β-каротином //
Пищевая технология. - 2001г. - №1. - стр. 28-29.
11. Назаров И.Н. Химия
витаминов - ПИЩЕПРОМИЗДАТ, 1959. - 98 c.
. Дмитровский А. А. Экспериментальная
витаминология/ Под ред. Островскго Ю. М. - Минск: Наука и техника, 1979.
Похожие работы на - Біосинтез вітамінів
|