Методы микробиологической диагностики заболеваний, вызванных патогенными кокками
ГОСУДАРСТВЕННОЕ АВТОНОМНОЕ
ОБЩЕОБРАЗОВАТЕЛЬНОЕ
УЧРЕЖДЕНИЕ СРЕДНЕГО ПРОФЕССИОНАЛЬНОГО
ОБРАЗОВАНИЯ РЕСПУБЛИКИ БАШКОРТОСТАН
БАШКИРСКИЙ МЕДИЦИНСКИЙ КОЛЛЕДЖ
Допускается к
защите
Зам.
директора по УР
И.Н.
Цирульникова
__________________
(подпись)
«»________20__
г.
ВЫПУСКНАЯ КВАЛИФИКАЦИОННАЯ РАБОТА
ТЕМА: Методы микробиологической
диагностики заболеваний, вызванных патогенными кокками
Выполнила
Юмагужина Гульнара Камилевна
студентка
группы 302л
специальность
060604 Лабораторная диагностика базовый уровень
Руководитель
ВКР Фаттахова Айгуль Наильевна
Уфа, 2014 г.
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
Глава 1.Обзор литературы.
.1 Стрептококки
.2 Методы исследования стрептококков
.3 Стафилококки
.4 Методы исследования стафилококков
.5 Пневмококки
.6 Методы исследования пневмококков
.7 Менингококки
.8 Методы исследования менингококков
Глава 2. Практическое применение методов микробиологической
диагностики заболеваний, вызванных патогенными кокками.
2.1 Описание и устройство лаборатории
.2 Виды исследований в данной лаборатории
.3 Описание исследования
Глава 3 . Результаты собственных исследований
ЗАКЛЮЧЕНИЕ
ВЫВОДЫ
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
Перечень сокращений, условных обозначений,
символов и специфических терминов
ДНК - дезоксирибонуклеиновая кислота
ЖСА - желточно-солевой агар
ИФА - иммуноферментный анализ
МЖСА - молочно-желточно-солевой агар
МПА - мясо-пептонный агар
ПЦР - полимеразная цепная реакция
РБ - Республика Башкорстан
РНГА - реакция непрямой гемагглютинации
РПГА - реакция прямой гемагглютинации
Neisseria meningitidis -
менингококки
pH -
реакция среды
P -
пили
S. -
стафилококки, стрептококки
S.areus - золотистый стафилококк
S.agalactiae - стрептококк группы B
S.bovis - стрептококки группы D
S.epidermidis - эпидермальный стафилококк
S.pyogenes - пиогенный стрептококк
S.pneumoniae - пневмококк
S.saprophyticus - сапрофитический стафилококк
ВВЕДЕНИЕ
Прогресс в области клинической микробиологии и инфектологии в последние
десятилетия расширил наши представления об известных возбудителях инфекционных болезней
и позволил выявить ряд ранее неизвестных инфекций человека.
В связи с существенным расширением спектра возбудителей и нередко
пересмотром роли некоторых из них в возникновении, развитии и распространении
инфекций для практики все более актуальным становится вопрос о применении
адекватных методов и средств выделения и точной идентификации возбудителя
конкретного заболевания, а также адекватных средств этиотропной терапии и
профилактики.
Успех классических методов обнаружения возбудителя инфекции зависит от
правильного выбора вида и количества исследуемого материала, времени и техники
его отбора, условий транспортирования, обработки, подбора методов и средств
выделения и идентификации возбудителя. В каждом конкретном случае они
определяются свойствами возбудителя, характером и стадией инфекции.
Следует подчеркнуть, что конечный результат исследования зависит не
только (а иногда и не столько) от компетентности и адекватных действий
микробиолога, но и от грамотности действий тех специалистов, которые имеют
отношение к исследуемому материалу на долабораторном этапе.
Не менее важное значение имеет правильная интерпретация результатов
микробиологического анализа, что так же требует достаточных знаний о свойствах
возбудителей инфекций человека. Многообразие возбудителей бактериальных
инфекций не должно быть препятствием на пути рационального контроля за
болезнями этой группы.[1]
Заболевания, обусловленные патогенными кокками, достаточно широко
распространены среди населения. Стафилококки принадлежат к числу наиболее легко
обнаруживаемых и распознаваемых микроорганизмов, не требующих сложных
диагностических приемов для их выявления, в практической работе микробиологи до
сих пор испытывают определенные трудности при установлении их причинной роли в
ряде различных заболеваний. В последние годы увеличиваются случаи заболевания
эпидемическим менингитом (особенно среди детей), а гонококковая инфекция
сопровождает человечество в течение всей его истории. Поэтому знания о природе
этих заболеваний, их выявлении и диагностики крайне необходимы.
Цель исследования: изучить свойства патогенных кокков и основы патогенеза
стафилококковых, менингококковых, пневмококковых, стрептококковых инфекций и
микробиологическую диагностику инфекционных заболеваний, обусловленных
патогенными кокками.
Задачи исследования
. Изучить биологические, морфологические свойства видов Streptococcus, Staphylococcus, Neisseria meningitidis, Streptococcus pneumoniae.
. Овладеть различными методиками лабораторной диагностики
заболеваний, вызванных патогенными кокками.
. Провести анализ собственных исследований, с выявлением
наилучшего метода микробиологической диагностики заболеваний, вызванных
патогенными кокками.
Глава 1. Морфология, культуральные свойства и
методы исследования патогенных кокков
Стрептококки - бактерии рода Streptococcus (сем.- Streptococcaceae), шаровидные или овальные клетки размером 0,6-1,0 мкм,
образующие цепи различной длины, грамположительные, факультативные анаэробы.
Различают β - гемолитические,α -гемолитические и гамма -
негемолитические стрептококки.Впервые стрептококки обнаружены
Т. Бильротом в 1874 году при роже и раневых инфекциях. Наибольшее
значение в патологии человека имеют β- гемолитические стрептококки,
отнесенные в 1958 году по предложению В.Д Белякова, к экологической группе
облигатных паразитов человека. По антигенным различиям полисахаридов
стрептококки разделена группы. Известно 20 групп стафилококков, которые
обозначают прописными латинскими буквами (от А до V) . Ряд альфа и гамма- стрептококков не вошли не в одну
группу. Для человека патогенны в основном β-гемолитические стрептококки группы А(Str. pyogenes)- возбудители ангин, хронического
тонзиллита, скарлатины, сепсиса, раневых инфекций кожи и других тканей, острого
гломерулонефрита, ревматизма, рожи.
Стрептококки группы B (Str.agalactiae) вызывают мастит, урогенитальные
инфекции у женщин, сепсис и менингит. Стрептококки групп C,G,H,Fчасто обнаруживаются в слизистой
оболочке зева человека, в том числе при острых респираторных заболеваниях. Стрептококки
группы D, или фекальные стрептококки -
сапрофиты толстой кишки человека - известны также как возбудители подострого
бактериального эндокардита, инфекций мочевого тракта. Стрептококки групп H,N,F,K,O и зеленящие стрептококки, лишенные группового антигена,
иногда обнаруживают в крови при септическом эндокардите. Вирулентные
стрептококки группы А имеют на поверхности капсулу, препятствующую фагоцитозу.
Гиалоурановая кислота, входящая в состав капсулы, не антигенна. Клеточная
стенка стрептококков состоит из трех слоев. Цитоплазматическая мембрана
стрептококков, состоит из белков и липидов, протоплазма - из ряда белков и
нуклеопротеинов. Вакцины из целых микробных клеток для профилактики и лечения
не применяютсяв связи с тяжелыми реакциями и сенсибилизирующим действием.
Стрептококки разных групп, за исключением группы D, погибают при нагревании до температуры 56̊ С в течении
30 минут. Сулема(1% р-р) и фенол (5% р-р) убивают их в течение 15 минут.
Культуры стрептококков выдерживают высушивание, особенно в белковой среде,
сохраняя при этом жизнеспособность. Стрептококки группы А высокочувствительны к
антибиотикам пенициллинового ряда и не приобретают к ним устойчивость. Эти
антибиотики действуют бактерицидно на стрептококки группы А и др. групп, за
исключением группы D.Для обнаружения
стрептококков на слизистых оболочках зева, носа и в гное, материал, взятый
тампоном, погружают в полужидкий агар на дно пробирки, где содержится капли
крови барана. После инкубации в течение 3-4 часов при температуре 37̊ С
производят посев на агар с кровью барана. Идентификация β- гемолитических стрептококков
производится на основании обнаружения на агаре характерных колоний, окруженных
зоной гемолиза, и микроскопии мазков, окрашенных по Граму.
Культуральные свойства
S. pyogenes - факультативные анаэробы.
Культивируются на питательных средах с добавлением глюкозы, сыворотки, крови
при pH 7,2-7,6. На плотных питательных
средах образует мелкие полупрозрачные колонии, в диких средах - придонный рост.
На кровяномагаре дают зону гемолиза. S. pyogenes ферментируют с образованием кислоты
без газа глюкозу, мальтозу, лактозу, сахарозу, манит, расщепляют салицин,
трегалазу, не разжижают желатин, свертывают молоко ,не восстанавливают нитраты
в нитриты.S.pyogenes выделяют экзотоксины, обуславливающие
общую интоксикацию и специфическое действие. Токсины общего действия
(эритрогенный, пирогенный, скарлатинозный) являются основными токсическими
компонентами стрептококков. Токсины местного действия относят O и S стрептолизин, гиалуронидазу, стрептокиназу, протеиназу.
1.2 Методы исследования стрептококков
Бактериологическое исследование
Для установления диагноза при острых стрептококковых инфекциях (за
исключением скарлатины с типичной клинической картиной) нужно проводить
бактериологическое исследование. При подозрении на сепсис сеют у постели
больного 10-15 мл крови во флакон, содержащий 100-150 мл сахарного бульона
(соотношение крови и среды1:10). Лучшие и надежные результаты дают посевы крови
в среду Китта-Тароцци с полужидким агаром. В нем будут расти и анаэробные
стрептококки. Посевы крови инкубируют в термостате при 37̊. При росте
стрептококков на дне среды появляется осадок. В среде может и образоваться газ.
В мазках из осадка обнаруживают грамположительные стрептококки в виде длинных
цепочек. Пневмококки располагаются короткими цепочками или парно в виде
ланцетовидных клеток, возвращенных друг друга утолщенными концами. При
отсутствии роста посевы выдерживают в термостате в течение3-4 недель,
периодически проводя бактериоскопию. Культуру, выросшую после бактериоскопии
пересевают в чашку с кровяным агаром для определения типа гемолиза. Через 18-20
часов вырастают типичные колонии, окруженной зоной гемолиза. Чтобы лучше и
точнее идентифицировать выделенные гемокультуры стрептококков, колонии с кровяного
агара рекомендуют отсеивать на МПА, молоко с метиленовым синим, желчный бульон.
Далее различные виды стрептококков можно дифференцировать по биохимическим
свойствам. Раневое содержание, мокроту, слизь из зева и носа, собранные ватным
тампоном сеют на кровяной агар. Материал наносят на среду в небольшом
количестве, а затем петлей или шпателем рассеивают его легкими штрихами по всей
поверхности. Не рекомендуется втирать изучаемый материал в агар. Для повышения
частоты посева, тампоны погружают в пробирку со средой Китта-Тароцци, к
которому добавляют полужидкий агар и 2-3 капли крови кролика. Посевы инкубируют
3-4 часа при температуре 37̊ С градусах, а затем высевают на чашки с
кровяным агаром.
CAMP-тест.
Большая часть стрептококков группы В продуцирует CAMPфактор, который при взаимодействии с β-лизином золотистого стафилококка
вызывает синергическое усиление лизиса эритроцитов. Для постановки теста через
центр чашки с кровяным агаром сплошной линией наносят суточную бульонную
культуру продуцирующего β-лизин S.aureus. Испытуемые штаммы стрептококков
наносят перпендикулярно к линии посева стафилококка. В качестве контрольных
используют штаммы S.agalactiae (положительный контроль) и S.pyogenes (отрицательный контроль). При
обнаружении в месте пересечения посевов стрептококка и стафилококка спустя 18
часов инкубации при температуре 37̊ C зоны синергического увеличения гемолиза в виде «крыла
бабочки» делают вывод о наличии в пробе S.agalactiae.
Серологическое исследование
При хронических стрептококковых инфекциях выделить возбудителя, как
правило, не удается, особенно при длительном лечении больных антибиотиками и
другими противомикробными препаратами. В таком случае проводят серологические
исследования: определение стрептококкового антигена в сыворотке крови и моче,
титрования антител к О-стрептолизин, гиалуронидазы и ДНК-азы. Антиген
стрептококков определяют в РСК. Необходимые для этого антистрептококковые
сыворотки получают путем гиперимунизации кроликов убитой культурой β-гемолитических стрептококков серогруппы
А. Титром антигена считают то наибольшее разведение сыворотки, которое
задерживает гемолиз. Лучшие результаты получают при постановке РСК на холоде. В
последнее время для выявления стрептококковых антигенов в сыворотке крови
довольно успешно используют метод ИФА. При определении стрептококковых
антигенов в моче больных используют реакцию преципитации. Осадок утренней
порции мочи после центрифугирования обрабатывают противострептококковых
преципитирующие сывороткой. Результат учитывают через час при комнатной
температуре. Стрептококковые антигены в сыворотке крови и моче часто
обнаруживают при скарлатине, ангине, ревматизме. Определение антител против
О-стрептолизин (антистрептолизина-О) проводят внесением рабочей дозы
стандартного препарата О-стрептолизин в ряд пробирок с кратными разведениями
сывороток (1:25, 1:50, 1:100 и т.д.). Смесь инкубируют в термостате в течение
15 мин, затем во все пробирки вносят по 0,2 мл 5% взвеси эритроцитов кролика и
снова помещают в термостат на 60 мин. При наличии антистрептолизина в крови
больных гемолиза не наступает. Пробирка с наибольшим разведением сыворотки, в
которой есть выраженная задержка гемолиза, содержит 0,5 AO
(антистрептолизина-О) . Для определения антител против гиалуронидазы
(антигиалуронидазы) в сыворотке больных в разных разведениях вносят стандартную
дозу гиалуронидазы и рабочую дозу гиалуроновой кислоты, которую готовят из
пупочных канатиков новорожденных. При наличии антигиалуронидазы в пробирках
образуется сгусток после добавления уксусной кислоты. Пробирка с наименьшим
количеством сыворотки, в которой есть сгусток, содержащий 1 AO (антитоксическое
единицу) антигиалуронидазы. При ревматизме и стрептококковом гломерулонефрите в
сыворотке крови обнаруживают >500 AO антистрептолизина и >800-1000 AO
антистрептогиалуронидазы уже с первых дней болезни. Именно при этих
заболеваниях чаще всего проводят обе серологические реакции. Во многих странах
используют коммерческие тест-системы для определения антител лострептолизин,
гиалуронидазы, стрептокиназы, ДНК-азы и других экзоферментов стрептококков.[2]
1.3 Стафилококки
Стафилококки - неподвижные грамположительные бактерии семейства Micrococcaceae рода Staphylococcus. Международным подкомитетом по
таксономии стафилококков и микрококков, ряд Staphylococcusвключает 3 вида: S.aureus, S.epidermidis, S.saprophyticus; наибольший интерес
для медицины представляет первый вид. Стафилококки - условно патогенные
бактерии, вызывающие заболевания у лиц со сниженным иммунитетом. Стафилококки
были открыты в 1880 году независимо друг друга Л. Пастером и Огстоном. Родовое
название Staphylococcus было дано Огстоном, а более
подробное описание представителей рода сделано в 1884 году Розенбахом. Клетки
стафилококков имеют правильную шаровидную форму диаметром 0,5 - 1,5 мкм,
делятся в нескольких плоскостях, образуя скопления, напоминающие гроздья.
Основные компоненты клеточной стенки стафилококков - пептидогликан и рибит- или
глицеринтейховые кислоты. Содержание гуанин + цитозин в ДНК составляет 30-40
моль %.[3]
Культуральные свойства.
Стафилококки - факультивные анаэробы, но более быстро и обильно растут
при наличии кислорода. При выращивании в аэробных условиях стафилококков
нуждаются в аминокислотах и витаминах, в анаэробных условиях - требуют
дополнительно урацил и ферментируемые источники углерода. Температурный оптимум
роста 35-45̊ С, но могут расти в интервале 6,5-46̊ С; оптимум ph 7,0-7,5 , возможен рост в пределах ph4,2-9,3. Стафилококки ферментируют
глюкозу в анаэробных условиях с образованием молочной кислоты. Большинство штаммов
S.aureus обладает выраженной устойчивостью к антибиотикам. Он
может поражать любой орган человека, в связи с чем и вызывает многие
заболевания. Для маркирования штаммов S.aureus, при проведение эпидемиологического
анализа, применяется метод фаготипирования. Он основан на использовании 22
фагов международного набора с узким спектром литической активности. Во второй
половине 70-х годов было описано 10 новых видов стафилококков, выделенных от
человека и животных. На плотных питательных средах стафилококки образуют
пигментированные колонии диаметром 1-5 мм, грубозернистой структуры с
уплотненным центром. Цвет пигмента колоний может быть различен у разных штаммов
одного и того же вида, в связи с чем не является дифференциальным признаком.
Патогенные штаммы стафилококка на кровяном агаре образуют вокруг колоний зону
гемолиза. На желточно-солевом агаре большая часть патогенных стафилококков
вызывает лецитовителлазную реакцию, проявляющуюся в образовании вокруг колоний
зоны помутнения с радужным венчиком по периферии. При росте на жидких
питательных средах стафилококки вызывают диффузное помутнение с последующим
выпадением осадка.
Кровяной агар: к расплавленному и охлажденному до 45̊-50̊ С
питательному агару прибавляют 5- 10% дефибринированной или цельной свежевзятой
крови животного.
Желточно-солевой агар: в расплавленный и остуженный до температуры 60̊
С мясопептонный агар pH
7,2-7,4 с 10% хлорида натрия прибавляют 10-20% желточной взвеси куриного
яйца.[4]
.4 Методы исследования
стафилококков
Бактериоскопическое исследование
При
бактериоскопическом исследовании почти со всех исследуемых материалов (раневой
содержание, экссудат, мокроты, осадок мочи и т.д.) с помощью бактериологической
петли изготавливают мазки, окрашивают по Граму и микроскопируют. Только из крови
и смывов мазки не делают так в них малое количество микроорганизмов. В типичных
случаях стафилококки имеют шарообразную форму, фиолетовый цвет, располагаются
несимметричными гроздьями, но встречаются и одинокие клетки, пары или тетради.
В последнее
время в связи с широким использованием антибиотиков морфология стафилококков
изменилась и типового их расположения в мазках из гноя часто не наблюдают. В
связи с этим отличить стафилококки от стрептококков по их морфологии и взаимным
расположением часто практически невозможно. Поэтому нужно делать посев,
выделять чистую культуру и идентифицировать ее.
Материал от
больных и бактерионосителей засевают немедленно или не позднее 3-4 ч после
взятия при условии хранения его на холоде. В первый день петлей, шпателем или
непосредственно тампоном делают посевы на кровяной агар и элективные для
стафилококков среды (желточно-солевой (ЖСА) или молочно-желточно-солевой агар
(МЖСА)). Чашки с посевами инкубируют при температуре 37°С в течение 48 часов,
или сутки в термостате и дополнительно 24 часа при комнатной температуре при
хорошем освещении. Если в исследуемом материале бактерий мало (данные
микроскопии) - то для обогащения делают еще в тиогликолевой среду. На второй
день производят высев из сахарного бульона на указанные элективные среды,
исследуют массивность роста и характер колоний после посевов других материалов.
На кровяном агаре стафилококки образуют непрозрачные, слегка выпуклые колонии
средних размеров с гладкой, блестящей, словно полированной поверхностью, четко очерченным
краем, маслянистой консистенции. Патогенные штаммы образуют вокруг колоний
прозрачные зоны гемолиза. На элективно-дифференциальных средах, как правило,
вырастают только колонии стафилококков. В частности, на желточно-солевом агаре
они образуют колонии с зоной помутнения вокруг них и характерным радужным
венчиком по периферии. На молочно-желточно-солевом агаре выявляют наличие
пигмента, который может быть золотистым, палевым, белым, желтым, оранжевым и
другим. Из всех типов колоний изготовляют мазки, окрашивают по Граму и
микроскопируют, проявляя типичные грамположительные стафилококки. Не менее
двухтипичных или подозрительных в отношении стафилококков колоний пересевают на
скошенный агар. В первую очередь отсеивают колонии с гемолизом и те, которые дали
положительную лецитовителазную реакцию. Пробирки с посевами помещают в
термостат при температуре 37̊ С на 18-20 часов. В последующие дни проводят
идентификацию выделенных чистых культур, для чего проверяют их морфологические
и тинкториальные свойства (окраска по Граму).
Биологическое
исследование
Патогенные
стафилококки, вызывающие пищевые токсикоинфекции выделяют и идентифицируют так
же, как и стафилококки вообще. Они отличаются способностью продуцировать
энтеротоксины, характеризующие термостабильностью и антигенной специфичностью.
Наиболее часто встречаются типы A и D. Указанные токсины получают путем
посева культуры в специальную полужидкую среду и инкубируют 3-4 суток при 37̊
в эксикаторе с 20% CO2. Среды
пропускают через мембранные фильтры. Полученные фильтрат прогревают при 100̊C 30 мин и вводят поросятам
внутрибрюшинно или через зонд в желудок. Через 30-60 минут возникает рвота,
позже понос и общее прострация. Чтобы выявить энтеротоксин в пищевых продуктах,
которые повлекли токсикоинфекцию, ими кормят поросят. В последнее время
идентификации и типирования энтеротоксинов проводят с помошью реакции
имунопреципитации в агаровом геле. Это самый простой и чувствительный метод.
Серологическое
исследование
Проводится
исследование тогда, когда возбудителя не удается выявить, например, при
хронических процессах (остеомиелит, септикопиемия) особенно если они долго
лечатся антибиотиками. Среди современных серологических реакций часто
используют РПГА, ИФА. [5]
1.5 Пневмококки
Пневмококки - парные кокки, относящиеся к семейству Streptococcaceae, к роду Streptococcus, обнаруживаемые в верхних
дыхательных путях здоровых и больных людей. Пневмококки одни из возбудителей
острой пневмонии. Бактерии вида Streptococcus pneumonia
обычно бывают овальной или сферической формы, размером 0,5-1,25 мкм, чаще
парные, иногда одиночные или в виде коротких цепочек. Дистальный конец каждой
пары бактерий заострен и имеет форму ланцета. При первичном выделении обладают
четко выраженной полисахаридной капсулой, которая отграничена от оболочки,
содержащий М- протеиновый антиген. Молодые культуры пневмококков
грамположительны, но старые культуры могут становиться грамотрицательными.
Полимерные компоненты клеточной стенки состоят в основном из пептидогликана и
кислотного комплекса, составляющих видоспецифическую субстанцию.[6]
Культуральные свойства.
Пневмококки - факультативные анаэробы, но хорошо растут и в аэробных
условиях при температуре 37 °С. На простых средах не культивируются. Их
выращивают на средах с добавлением крови или сыворотки. На кровяном агаре
образуют мелкие прозрачные росинки колоний, окруженные зоной позеленения.
На жидких средах вызывают слабое помутнение с осадком. Биохимически
активные, раскладывают ряд углеводов до кислоты, желатин не разреживают.
Вирулентные пневмококки раскладывают инсулин и растворяются в желчи, что
используют для их идентификации. Они продуцируют гемотоксин, лейкоцидин,
гиалуронидазу, а также имеют эндотоксин. Вирулентные свойства пневмококков, в
основном, определяют капсулы, которые подавляют фагоцитоз.
1.6 Исследование пневмококка
Бактериоскопическое исследование
Бактериоскопическое исследование материала (кроме крови) сводится к
изготовлению двух мазков. Один из них окрашивают по Граму, второй по
Бурри-Гинс, что позволяет выявить капсулу. Пневмококки располагаются в виде
ланцетовидными диплококков, окруженных общей капсулой. Если в поле зрения
выявляют 10 и более типичных диплококков, можно с большой вероятностью сделать
вывод о наличии S.pneumoniae. Однако, первичная микроскопия не дает права
поставить окончательный диагноз, поскольку в мазках могут быть капсульные
непатогенные диплококки - представители нормальной микрофлоры. Поэтому нужно
проводить посев клинического материала и выделять чистую культуру.
Бактериологическое исследование
При бактериологическом исследовании, при сепсисе сеют 10 мл крови во
флакон, содержащий 100 мл сывороточного или сахарного бульона, инкубируют 18-20
часов при температуре 37 ° С, затем высевают на кровяной агар, выделяют и
идентифицируют чистую культуру. При менингите ликвор центрифугируют и из осадка
делают посев на кровяной агар. На нем пневмококки растут в виде маленьких
круглых колоний, окруженных зеленой зоной, в центре колонии видно характерное
вдавление. Посев мокроты или гноя на питательные среды делать нецелесообразно,
поскольку присутствует сапрофитная микрофлора подавляет рост S.pneumoniae.
Лучше исследуемый материал ввести в брюшную полость белых мышей. Постановка
биопробы - быстрый, надежный и точный метод выделения чистой культуры
пневмококков. Белые мыши очень чувствительны к этим бактериям и уже через 10-12
ч после заражения пневмококки проникают в кровь и паренхиматозные органы,
вызывая сепсис. Посев крови из сердца или кусочков внутренних органов во время
вскрытия животных позволяет выделить чистую культуру возбудителя. Для
идентификации пневмококков используют такие их свойства. В отличие от других
видов стрептококков, S.pneumoniae не растет на среде с оптохином, ферментирует
инулин и очень чувствителен к действию желчи. Быстрый лизис пневмококков под
действием желчи можно обнаружить, если к 1 мл бульонной культуры добавить 0,5
мл желчи. Через 15-20 минут пребывания в термостате наступает полный лизис
бактериальных клеток. Для определения сероваров пневмококков (сейчас их
насчитывается 85) используют реакцию агглютинации на стекле с типовыми
сыворотками или феномен "набухания капсул". В присутствии
гомологичной сыворотки капсула пневмококков сильно отекает. Еще лучше проводить
серотипирования с помощью коммерческих реагентов в реакциях латекс-агглютинации
или коаглютинации, благодаря которым проявляют капсульные антигены. [5 ]
1.7 Менигококки
Менингококки - возбудитель менингита,менингококк - Neisseria meningitidis (AlbertetGhon 1903,Murray 1929) диплококк, имеет почти правильную круглую
форму; его размеры от 0,6 - 1,0 мкм. Хорошо окрашивается анилиновыми
красителями, грамотрицателен. Клетки располагаются парно; их обращенные друг к
другу поверхности слегка уплощены; снаружи заметна капсула. При культивировании
на питательных средах капсула утрачивается. Капсулы и реснички играют роль
факторов вирулентности: первые способствуют устойчивости менингококков к
фагоцитозу, вторые - их прикреплению к эпителию. Трехслойная клеточная стенка
микроба состоит из белков, гликопротеинов, липидов и липополисахарида.
Менингококк неподвижен, спор не образует, мало устойчив к внешним воздействиям,
однако повышенная влажность воздуха (80-90%), наличие защитных коллоидов
способствует сохранению его жизнеспособности. Под воздействием дезинфектантов в
виде растворов фенола (1%), хлорамина (0,01 %), перекиси водорода (0,1%)
менингококк погибает за 2-3 минуты; он чувствителен к пенициллину и его
производным, левомицетину, эритромицину; чувствительность его к тетрациклину и
сульфаниламидам значительно снизилась. [7]
Культуральные свойства.
Менингококк - факультативный анаэроб, оптимальная температура размножения
37̊, pH среды 7.2-7.6. Культивируется на
питательных средах с добавлением нативных белков - крови или сыворотки человека
и других млекопитающих. В качестве углерода и азота менингококки используют
аминокислоты (глутами, таурин, аспаргин, L-аргини, глицин тирозин), которые необходимо включать в среду
культивирования. Среда Мюллера-Хинтона является безсывороточной средой, где
содержится полный набор аминокислот и мясной экстракт. Для получения большой
массы микроорганизмов менингококк культивируют при повышенном содержании
углекислого газа (7-10%). На плотных питательных средах менингококк формирует
бесцветные, опалесцирующие, плоские, круглые колонии 0,5-1,5 мкм с ровным
краем. В сывороточном бульоне растет, образуя равномерную муть, через 3-4 дня
на поверхности среды появляется нежная пленка. Ферментирует глюкозу, мальтозу с
образованием кислоты без газа, не разжижает желатин, обладает оксидазной
активностью. Не способны синтезировать полисахариды из сахарозы. При гибели
микробной клетки высвобождается эндотоксин липополисахаридной природы.
Антигенная структура достаточно сложная и классификация менингококков основана
на различиях в строении полисахаридов капсулы. Выделяют серогруппы: A,B,C,D,X,Y,Z,W-135,H,J,Kи L. [4]
1.7 Методы исследования менингококков
Бактериоскопическое исследование
При бактериоскопическом исследовании, если спинномозговая жидкость
гнойная (мутная), мазки из нее изготавливают без какой-либо обработки, когда же
она прозрачна - мазки готовят из осадка после центрифугирования. Препараты
окрашивают метиленовой синькой, по Романовскому-Гимзе и Граму. Последний метод
дает менее четкие результаты, поскольку клетки ликвора очень меняются,
появляются многочисленные артефакты, имитирующие присутствие менингококков. В
типичных случаях бактерии в мазках выглядят как грамотрицательные диплококки,
имеющие вид кофейных зерен, которые располагаются парами, тетрадами, или
хаотично, часто внутри лейкоцитов (незавершенный фагоцитоз). В таком случае,
при тичной клинической картине, первичная микроскопия ликвора приобретает
важное значение для установления менингококковой этиологии заболевания.
Микроскопическое исследование крови при меньшей кокемии сводится к изготовлению
и окраски толстой капли. Обнаружение многочисленных темно-синих диплококков,
расположенных парами или в виде скоплений, позволяет быстро поставить диагноз.
Однако, положительные результаты бактериоскопии мазков крови бывают не всегда,
даже при типичной форме генерализованной менингококковой инфекции. Почти
постоянно и очень быстро N. meningitidis можно обнаружить микроскопически в
мазках из метастатических очагов инфекции, которыми являются элементы сыпи
(экзантемы, петехии, розеолы, папулы). Аспирированных с помощью иглы со шприцем
маленькие капельки крови из петехий размазывают на предметном стекле и
окрашивают по Романовскому-Гимзе. Мазки по содержанию петехий можно изготовить
в виде отпечатков. Для этого стерильной петлей осторожно соскабливают поверхность
петехии, затем к ней прикладывают стерильные предметное стекло, фиксируют в
пламени горелки и окрашивают. На основе данных микроскопии можно представить
предварительный ответ. Таким способом менингококки можно обнаружить даже тогда,
когда гемокультура не выделяется. При микроскопии отделяемого из носоглотки,
взятых тампоном из глубоких отделов слизистой позади мягкого неба, выявление
грамотрицательных диплококков имеет ограниченное значение, поскольку там могут
быть сходны по морфологии непатогенные виды нейссерий.
Другие экспресс-методы диагностики сводятся к постановке серологических
реакций для определения менингококкового антигенов в крови, спинномозговой и
синовиальной жидкостях. С этой целью используют реакции коаглютинации,
латекс-агглютинации, встречного имуноэлектрофорезу, ИФА, употребляя
специфические групповые антименингококовые сыворотки.
Бактериологическое исследование
При бактериологическом исследовании у больного эпидемическим гнойным
менингитом сразу при госпитализации берут 2-5 мл спинномозговой жидкости.
Стерильной пастеровской пипеткой со дна пробирки (лучше после
центрифугирования) набирают 0,3-0,5 мл и по 2-3 капли засевают на поверхность
подогретых сред в двух чашках Петри, растирая материал шпателем. В одной чашке
содержится сывороточный агар (до растопленного и охлажденного до температуры 45
° С МПА добавляют 20% лошадиной или бычьей сыворотки), во второй -
"шоколадный" агар (до растопленного и охлажденного МПА добавляют 10%
дефибринированной крови, трижды подогревают, не доводя до кипения). Остатки
ликвора используют для посева на среду обогащения (полужидкий сывороточный
агар) и одновременно для проведения указанных выше экспресс-методов
диагностики. Остаток материала в Пастеровском пипетке используют для
изготовления мазка. Посевы помещают в эксикатор, где создают повышенную
концентрацию углекислоты, поставив в него зажженную свечу и герметично закрыв
крышкой. Когда свеча погаснет, в эксикаторе будет атмосфера с 7-10% С02. После
этого сосуд с засеянными средами ставят в термостат при температуре 37 ° С.
Через 24 часа инкубации исследуют культуральные свойства. Колонии менингококков
на сывороточном агаре нежные, гладкие, бесцветные, вязкой консистенции,
размером 2-3 мм. Менингококков колонии на "шоколадном" агаре имеют сероватый
цвет, блестящую поверхность, ровный край, маслянистую консистенцию, размеры 1-3
мм. Цвет среды вокруг колоний не меняется. Если в мазках из таких колоний
обнаруживают грамотрицательные кокки, которые дают положительные пробы на
оксидазу и каталазу, это дает право отнести культуры к роду нейссерий и
провести дифференциацию видов. С этой целью отсеивают колонию на скошенный
сывороточный агар для выделения чистой культуры. В случае отсутствия роста на
обеих чашках, исследуют рост в среде обогащения. На третий день исследования
определяют серогруппы выделенной культуры в реакции агглютинации на стекле с
менингококковой сыворотками. Лиофильно высушенные сыворотки растворяют, внося в
ампулу 1 мл стерильного 0,85% раствора хлорида натрия. На предметные стекла
наносят отдельными пипетками капли диагностических сывороток различных
серогрупп (А, В, С, D и т.д.) и каплю физиологического раствора (для контроля
культуры на спонтанную агглютинацию). Бактериологической петлей выделенную
культуру эмульгируют в капле каждой сыворотки и капли физиологического
раствора. Через 2-3 мин учитывают результат реакции. Вывод о принадлежности
культуры к определенной серогруппы делают на основе реакции агглютинации с
соответствующей сывороткой. При появлении спонтанной агглютинации в капле физиологического
раствора реакцию не учитывают. Определяют дискодифузным методом
чувствительность выделенной культуры к антибиотикам и сульфаниламидным
препаратам и проводят другие тесты для дифференциации менингококков от других
патогенных и непатогенных нейссерий. При генерализованной менингококковой
инфекции для выделения возбудителя из кровяного русла с помощью стерильного
шприца берут 10 мл крови и засевают во флакон с 100 мл полужидкого среды. Через
24 часа делают высев из флакона в чашку с сывороточным (или
"шоколадным") агаром. Получив изолированные колонии, выделяют и
идентифицируют чистую культуру так; амо, как из спинномозговой жидкости. Чтобы
посеять экссудат из петехий кожу вокруг них обтирают 70% спиртом. При некрозе
петехий экссудат для посева можно взять стерильной бакгериологической петлей из
некротизированной участка. При неповрежденной коже экссудат берут тонкой иглой,
соединенной со шприцем, в котором содержится 0,2 мл 0,85% раствора хлорида
натрия. Физиологический раствор вводят в толщу петехии и отсасывают назад.
Взятый экссудат сеют на сывороточный агар с ристомицин или линкомицином,
которые подавляют микрофлору кожи. Выделение и идентификацию культур проводят
по описанной выше схеме. При диагностике назофарингита или менингококкового носительства
слизь из носоглотки берут натощак или через 3-4 часа после еды специальным
стерильным ватным тампоном, закрепленным на согнутом под углом 45 ° проволоке.
Конец тампона направляют вверх и вводят за мягкое небо, при этом корень языка
придавливают шпателем. При извлечении тампона взят материал не должен касаться
зубов, языка и слизистой щек. Материал немедленно засевают на сывороточный агар
с ристомицин или линкомицином, которые подавляют рост грамположительных кокков,
или тампон погружают в пробирку со средой обогащения. При посеве материала на
чашки его сначала втирают на небольшом участке среды (1x2 см), переворачивая
тампон всеми сторонами, потом тем же тампоном сеют штрихами на расстоянии на
всей площади агара. Теперь созданы тест-системы на основе полимеразной цепной
реакции для более надежного выявления Neisseria meningitidis.[ 5]
Таким образом, мы видим, что существует большое разнообразие патогенных
кокков со своей структурой, культуральными свойствами и различными методами
исследования. Теперь рассмотрим методы микробиологической диагностики этапов
заболеваний, вызванных патогенными кокками на практике.
Глава 2. Практическое применение методов
микробиологической диагностики заболеваний, вызванных патогенными кокками
В данной главе я хочу рассказать о методах микробиологической диагностики
в конкретной бактериологической лаборатории, видах исследований, проводимых в
ней, а также о результатах таких исследований.
.1 Описание и устройство
лаборатории
Я проходила практику на базе бактериологической лаборатории Больницы
скорой медицинской помощи г. Уфы, Республики Башкртостан, расположенной по
адресу: г. Уфа, ул. Батырская 39/2 , 450106.
Бак.лаборатория занимает II
этаж и часть III этажа отдельно стоящего 3-х этажного
здания. На I этаже здания расположен гараж
больницы. На II этаже здания находится
бак.лаборатория, на III этаже
расположены: комната для врачей, кабинет заведующей бак.лаборатории, учебная
комната кафедры лабораторной диагностики ИПО БГМУ, комната приема пищи. С
отдельным входом на III этаже
расположен спортивный зал.
Лаборатория разделена на «чистую» и «грязную» половины и имеет 2 входа:
1- для персонала, вход на «чистую» половину лаборатории; 2- для приема
анализов- с «грязной» половины. Общая площадь лаборатории -404 кв. м.
В «чистой» половине расположены: средоварочная со стерильным боксом для
разлива питательных сред, автоклавная для стерилизации питательных сред,
моечная, препараторская, стерилизационная для стерилизации посуды, материальная
комната, гардероб для персонала. А также комнаты, расположенные на III этаже, кабинет заведующей, комната
врачей, комната приема пищи, кладовая и учебная комната кафедры - находятся в
«чистой» зоне.
В «грязной» половине расположены: регистратура, посевная комната, комната
для воздушно- капельных инфекций с боксом, комната для иммунологических
исследований, комната для гнойно-септических инфекций, комната для кишечных
инфекций, материальная, комната для уборочного инвентаря, автоклавная для
уничтожения отработанного материала.
Бак.лаборатория обеспечена центральным отоплением, центральным
водоснабжением холодной и горячей воды, центральной канализацией, вытяжной
вентиляцией с механическим побуждением, искусственным и естественным
освещением, электричеством; телефонизирована городской и внутренней связью.
Поточность прохождения патогенного материала сохраняется. Поступает
материал на исследование через второй вход в холл. Холл оборудован столом,
стулом, доской объявлений, а также звонком для вызова сотрудника лаборатории.
Через окошко передается материал в регистрационную комнату. Лаборантом
проверяется целостность посуды, в которые забраны материалы на
бак.исследования, правильность забора материала, своевременная доставка ее и
правильность оформления направления. Материал доставляется работниками
отделений в биксах. В данной же комнате регистрируются анализы и переносятся в
посевную комнату. В посевной комнате посевы производятся в специально
установленных столах: для капельных инфекций, для кишечной группы и
гнойно-септических инфекций. Далее посеянные чашки, флаконы, пробирки
переносятся в соответствующие рабочие комнаты и термостатируются. Отработанный
материал собирается в рабочих комнатах в биксы и передаются на
автоклавирование. Автоклавная оборудована двумя паровыми стерилизаторами, которые
предназначены только для уничтожения отработанного материала. После
автоклавирования отработанный и убитый материал поступает в моечную, где вся
посуда моется, подвергается сушке. После этого посуда стерилизуется в сушильных
шкафах в стерилизационной комнате. Материал для забора проб подготавливается в
препараторской, в средоварке готовятся питательные среды и все стерилизуется в
автоклавах. Стерильная посуда ставится в шкаф для стерильной посуды,
подписывается дата стерилизации, а готовые питательные среды ставятся в
холодильники.
2.2 Виды исследований в данной лаборатории
.Санитарно - бактериологические исследования.
. Воздух помещений аспирационным методом.
2. Смывы на бактерии группы кишечных палочек, стафилококк,
синегнойную палочку, другие условно- патогенные бактерии, иерсинии, патогенные
микроорганизмы.
3. Контроль стерильности перевязочного материала, инструментария,
шовного материала, дистиллированной воды, инъекционных растворов в аптеках; рук
хирургов, кожи операционного поля.
. Контроль работы автоклавов, сушильных шкафов, дезкамер.
II.Исследования
при инфекционных заболеваниях.
1. На возбудителей дифтерии.
2. На возбудителей коклюша, паракоклюша.
. На менингококк - носоглоточную слизь, ликвор.
. На возбудителей дизентерии.
. На сальмонеллы (испражнения, кровь, моча, желчь).
. На энтеропатогенныеэшерихии.
. На иерсинии.
. На кампилобактерии.
. На гонококки.
2.3 Описание этапов исследований
С целью обнаружения стафилококков исследуют гной, кровь при сепсисе,
слизь из зева, носа, мокроту, мочу. В данной практике исследовала мазки из зева
и носа, а также кровь.
-й этап исследования. Через сутки просматривают наличие роста. Если
образовались колонии, обычно они бывают непрозрачными окрашенными в золотистый
до белого цвета. Для дифференцировки стафилококка колонии пересевают в молоко с
метиленовой синькой и на скошенный агар. Ставят в термостат на сутки. Их
подозрительных колоний делают мазок. Также проводят предварительный учет
чувствительности к антибиотикам.
-й этап исследования. Мазки окрашивают по Граму, изучают морфологию
бактерий.
Кровь засевают на кровяной агар бактериологической петлей штрихами.
Ставят в термостат на 24 часа. При наличии роста на кровяном агаре, характерных
для стафилококков колоний из них делают мазок, окрашивают по Граму и делают
посев на скошенный агар. После инкубации в термостате выросшую культуру
идентифицируют.
Для обнаружения стрептококков используют бактериологический и
микроскопический метод. В данной практике исследовала слизь, гной , мочу и
кровь.
-й этап исследования. Слизь сеют на 5% кровяной агар, вращая тампон по
поверхности питательной среды. После посева на плотную питательную среду
засевают на бульон с глюкозой. Инкубируют в термостате 24 часа.
Каплю гноя наносят на 5% кровяной агар и стеклянным шпателем втирают в
среду. Инкубируют в термостате сутки. Из этого же материала делают мазок,
окрашивают по Граму и микроскопируют.
Кровь засевают в бульон с 0,2% глюкозой в соотношении 1:10.Инкубируем в
термостате сутки.
-й этап исследования. Вынимают чашки из термостата и просматривают. При
обнаружении в мазке стрептококков часть оставшейся колонии пересевают в
пробирки на агар с сывороткой для выделения чистой культуры и на бульон с
кровью в пробирках.
Инкубируют в термостате.
-й этап исследования. Вынимают посевы из термостата, проверяют чистоту
культуры на скошенном агаре, делают мазки, окрашивают по Граму и
микроскопируют. При наличии чистой культуры стрептококка производят посев на
среды Гисса (лактозу, глюкозу, мальтозу, сахарозу и маннит), молоко, желатин,
40% желчь и ставят в термостат.
-й этап исследования. Производят учет результатов.
|
Вид микроба
|
Тест
|
|
лактоза
|
Глюкоза
|
сахароза
|
маннит
|
мальтоза
|
Рост на 40% желчи
|
молоко
|
желатин
|
|
Str.pyogenes
|
к
|
к
|
к
|
к
|
к
|
-
|
Сверты-вание
|
Не разжижает
|
стрептококк стафилококк микробиологический исследование
Диагностика менингококковой инфекции осуществляется бактериологическим
методом, а также серологическим.
-й этап исследования. Для исследования используют СМЖ в количестве 2-3
мл. Первую порцию для общего ликворологического исследования, вторую порцию
используют для бактериологического исследования. Первичный посев при проведении
диагностического исследования производят шпателем на 3 чашки: сывороточный
агар, кровяной агар и «шоколадный» агар. Инкубируем во влажной атмосфере с 5% CO2 при температуре 37̊. Так же
сеем на среду обогащения (полужидкий сывороточный агар). Делают мазки из
оставшегося материала и окрашивают метиленовым синим.
-й этап исследования. Ведется осмотр чашек с посевами и из колонии
готовят мазки, окрашивают, ставят тесты на оксидазу, каталазу, уреазу. На
«шоколадном» агаре колонии выглядят нежными, сероватого цвета, с блестящей
поверхностью и ровными краями, имеют масляную консистенцию.
-й этап исследования. Культуры исследуются под микроскопом и ставят пробу
с 3% раствором KOH. Для оценки
чистоты выросшей культуры готовят мазки и просматривают. На этом этапе возможна
выдача положительных результатов. Так же проводят лекарственную
чувствительность к антибиотикам.
-й этап исследования. Учитывают результаты дифференциальных посевов, а
так же чувствительность к антибиотикам. После учета результата проб на лекарственную
чувствительность и свойства других возбудителей , выдают окончательный ответ.
Бактериологическое исследование крови
Кровь, взятую из вены стерильно засевают на чашки с питательными средами,
а затем на 0,1%-ный полужидкий агар в отношении 1:10, то есть 1-2 мл крови
можно сеять в пробирку с 7-10 мл полужидкого агара или 5-10 мл крови засеять во
флаконы с 50 мл среды. После суточной инкубации материал высевают на
сывороточный и «шоколадный» агары чашки Петри. При отрицательном результате
рекомендуется инкубировать в
течение недели с ежедневными высевами.
Глава 3. Результаты собственных исследований
В данной главе я хочу показать результаты собственных исследований в виде
диаграмм, для наглядного изображения тех самых результатов и для проведения анализа
собственных исследований.
В первую очередь, хочу исследовать пробы на носительство стафилококков.
|
Нос. - ство на стафилококк
|
Пробы
|
Исследование
|
Положительный результат
|
|
Без отбора колоний
|
103
|
1098
|
82
|
|
С идент. -цией
|
995
|
|
|
|
Всего
|
1098
|
1098
|
82
|
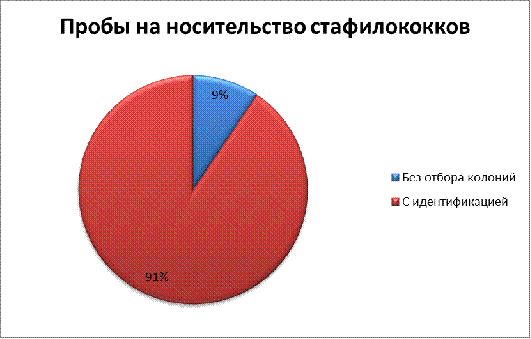
Таким
образом, видно, что без отбора колоний 9 %, с идентификацией 91% , то есть в
пробах выявлен положительный результат на ряд стафилококков.
Теперь
рассмотрим исследование на носительство на золотистый стафилококк, также с
помощью таблицы.
|
S. aureus
|
Положительный результат
|
Отрицательный результат
|
|
Количество проб
|
82
|
918
|
|
Всего
|
1000
|
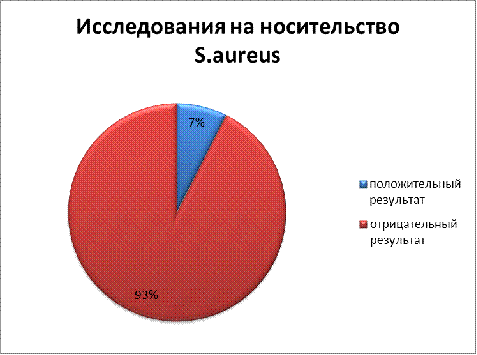
Как
видно из диаграммы из 1000 проб, положительный результат 82 пробы (7%),
отрицательный 918 (93%).
И
напоследок рассмотрим исследование на менингококк. Возьмем статистические
данные и составим из них таблицу и к ней диаграмму.
Пробы
|
Исследование
|
Положительный результат
|
|
Без отбора колоний
|
2
|
2
|
|
|
С идент.-цией
|
1
|
|
0
|
|
Всего
|
4
|
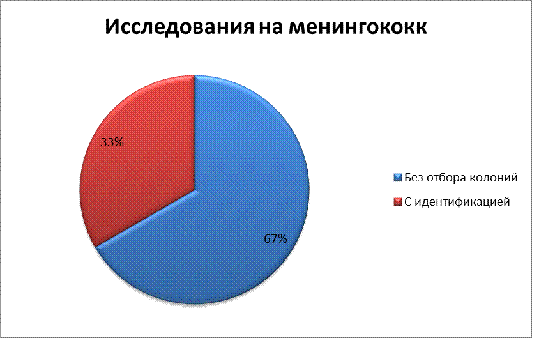
Как
видно из диаграммы из трех проб, две были без отбора колоний (67%), а одна с
идентификацией (33%). Положительные результаты отсутствуют.
ЗАКЛЮЧЕНИЕ
Мой
диплом был посвящен методам микробиологической диагностики этапов заболеваний,
вызванных патогенными кокками. В результате изучения морфологии, культуральных
свойств патогенных кокков было рассмотрено использование бактериоскопического,
бактериологического, биологического методов для обнаружения возбудителя в исследуемом
материале.
Достоинствами
бактериоскопического метода являются простота, быстрота, экономичность. Однако
он находит ограниченное применение, так как может быть использован лишь при
наличии каких-либо морфологических или тинкториальных особенностей возбудителя
и достаточном его содержании в исследуемом материале. Данный метод является
ориентировочным.
Основной
и самый точный метод диагностики бактериальных инфекций бактериологический,
который используют почти при всех заболеваниях, несмотря на его недостатки:
длительность исследования (от 4-5 дней до 2 мес), опасность (так как
накапливается чистая культура возбудителя), сравнительную дороговизну. В том
случае, если в исследуемом материале предполагается содержание возбудителя в
достаточном количестве, посев материала производят на плотные питательные среды
для получения изолированных колоний. При незначительном содержании микробов
исследуемый материал прежде засевают на жидкие питательные среды - среды
обогащения. Идентификацию выделенной чистой культуры производят по
морфологическим, тинкториальным, культуральным, биохимическим, антигенным и
токсигенным свойствам (в зависимости от вида возбудителя). Определение
перечисленных свойств позволяет установить вид возбудителя. С целью
эпидемиологического маркирования производят внутривидовую идентификацию
выделенной культуры: определяют ее фаговар, биовар и др. Кроме того, для
назначения рационального лечения, как правило, определяют чувствительность
выделенной культуры к антибиотикам.
При
микробиологической диагностике заболеваний, вызванных условно-патогенными
микробами, представителями нормальной микрофлоры, обязательным является
определение количества возбудителей в исследуемом материале.
Биологический
метод неэкономичен, негуманен, поэтому находит ограниченное применение. В
качестве экспериментальных животных используют белых мышей, морских свинок,
кроликов, обезьян и других животных.
Также
с помощью серологического метода возможно обнаружить либо специфические
антитела в сыворотке больного, либо специфические антигены непосредственно в
исследуемом материале. Антитела к возбудителю заболевания появляются, как
правило, к концу первой недели болезни. Невозможность обнаружить их в первые
дни заболевания является серьезным недостатком метода, особенно в тех случаях,
когда заболевание протекает остро. Кроме того, при многих болезнях требуются
изучение антителообразования в динамике и выявление увеличения количества
антител, что также не позволяет быстро поставить диагноз. Недостатком метода
является и то, что с его помощью нельзя точно идентифицировать возбудителя и
определить его антибиотикограмму. Но в то же время это совершенно безопасный,
относительно недорогой метод, позволяющий за короткое время поставить диагноз.
В настоящее время при ряде болезней определяют не только количество, но и
классы иммуноглобулинов.
При
некоторых заболеваниях серологический метод применяют для выявления
специфических антигенов в исследуемом материале. Поскольку специфические
антигены, входящие в состав возбудителя, находятся в патологическом материале с
первых минут болезни, этот вариант серологического метода применяют для
ускоренной (в течение первого дня болезни) или даже экспресс диагностики (в
течение нескольких часов) инфекционных заболеваний.
.
От выбора метода диагностики, в свою очередь, зависит правильность и точность
результата исследования, что является очень важным для выявления заболевания,
его лечения и в целом, для здоровья нации.
ВЫВОДЫ
Рассмотрев
все методы, можно сделать вывод, что их диагностическая ценность неравнозначна.
Ведущим методом микробиологической диагностики является бактериологический
метод, так как он позволяет выделять и идентифицировать микроб-возбудитель,
т.е. первопричину болезни. Остальные методы менее информативны, так как они
позволяют обнаружить в организме изменения, обусловленные наличием в нем
микроба. Второе место по значимости занимает серологический метод, поскольку
взаимодействие антигена и антитела характеризуется высокой степенью
специфичности. Информативность остальных методов невысокая, и они обычно служат
дополнением к бактериологическому и серологическому методам. Так, микроскопия
исследуемого материала далеко не всегда позволяет увидеть и идентифицировать
микробы под микроскопом. Их удается обнаружить только при высокой обсемененности
ими материала. Даже обнаружив бактерии под микроскопом, идентифицировать их до
вида морфологически нельзя. Как известно, все видовое многообразие бактерий
сводится к 4 основным морфологическим формам: кокки, палочки, извитые и
ветвящиеся формы. Поэтому по микро-
скопической
картине можно весьма ориентировочно отнести увиденные бактерии к крупному
таксону, например грамположительным коккам. Только в единичных случаях, когда
бактерии имеют уникальную морфологию, микроскопически можно определить их
родовую принадлежность.
Диагностические
возможности биологического метода ограничены тем, что к большинству
возбудителей антропонозных инфекций человека лабораторные животные
невосприимчивы, поэтому вызвать у них экспериментальную инфекцию не
представляется возможным.
Наряду
с рассмотренными методами особое значение приобретают методы
экспресс-диагностики, которые позволяют поставить микробиологический диагноз в
течение короткого промежутка времени (от нескольких минут до нескольких часов)
с момента доставки исследуемого материала в лабораторию. К числу
экспресс-методов относятся РИФ, ИФА, РИА, ПЦР, использование биочипов,
хроматография и др. Особенности диагностики анаэробных инфекций изложены в
материалах диска. Также в последние годы все большее значение приобретают
молекулярно-биологические методы диагностики (ДНК-зонды, ПЦР, лигазная цепная
реакция - ЛЦР, хроматография, электрофорез, иммуноблот, биочипы и
др.).Молекулярно-биологические методы диагностики основаны на идентификации ДНК
и РНК, специфичных для данного вида микробов, и включают гибридизацию на основе
ДНК-зондов и диагностику на основе ПЦР. Однако наиболее точными методами
микробиологической диагностики все же являются рутинные методы(
бактериологические, бактериоскопические, микроскопические),так как они являются
более доступными, быстрыми и не требуют больших затрат.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. WWW.erbalachema.ru
<http://erbalachema.ru/upload/file/articles/Vozb_bact_inf.pdf>
. Микробиология с
основами эпидемиологии и методами микробиологических исследований: учебник для
средних медицинских учебных заведений/ В.Б. Сбойчаков. - 2-е изд., испр.и доп.
- Спб.: СпецЛит,2011. - 608с.
. Большая медицинская
энциклопедия. Б.Н. Богомолов - издательство: АСТ, 2007 г.
. Микробиологическая
диагностика инфекционных заболеваний/ Е.П. Красноженов, М.Р. Карпова, И.Н.
Ильинских, Ю.Н. Одинцов, В.Г. Пехенько, Л.С. Муштоватова, Т.Л.Мирютова, О.П.
Бочкарева. - Ростов на Дону:Феникс, 2006. - 304 с. -(Медицина для вас)
. www.vse-zabolevaniya.ru
<http://www.vse-zabolevaniya.ru>
. Большая медицинская
энциклопедия . А.Н. Светлакова - издательство:АРТ, Хранитель, 2008 . - 904 с.
. Большая медицинская
энциклопедия. Издательство: Эксмо,2007 г., 864 с.