Основні принципи нормування радіаційного впливу
РЕФЕРАТ
Мета роботи: За літературними
джерелами визначити основні принципи нормування радіаційного впливу.
Завдання роботи: проаналізувати
джерела іонізуючого опромінення, вплив радіації на здоров’я людини, дослідити
норми радіаційної безпеки.
Об’єкт дослідження: нормативні
документи по нормам радіаційної безпеки.
В роботі системно розглянуто
біологічна дія радіаційного опромінення і встановлення лімітних доз.
ВСТУП
Атомна енергетика в даний час є
екологічно чистіша і дешевша, ніж теплова. У розвинених країнах вона забезпечує
від 15 до 70% усієї електроенергії, що виробляється (Франція - 70%, США - 17%,
Швеція - 50%, Канада - 15%). Однак у разі аварії атомні станції становлять дуе
серйозну небезпеку для людей і оточуючого середовища. За час експлуатації АЕС у
світі сталося 3 основні аварії: 1961 р. - в Айдахо-Фолс (США), 1979 р. - на АЕС
«Примайл-Айленд» у Гарисберзі (США), 1986 р. - на Чорнобильській АЕС.
Аварії на АЕС мають значні
відмінності від ядерних вибухів. Вони відрізняються від ядерних вибухів більшою
тривалістю викидів, що змінює напрямок потоків повітряних мас, тому практично
немає можливості прогнозувати розміри зон ураженості. На чорнобильській
техногенній аварії, яка стала аварією глобального масштабу, необхідно
акцентувати дещо більшу увагу. Як сьогодні стало відомо з численних фактів
вченим, ще жодна катастрофа XX століття не мала таких тяжких екологічних
наслідків, як Чорнобильська. Ця трагедія не регіонального, не національного, а
глобального масштабу.
Випадання радіоактивних речовин простежувалось
і у державах Західної Європи, підвищився радіаційний фон у Скандинавії, Японії
та США. Навіть через 15 місяців після катастрофи у Чорнобилі у Великій Британії
було виявлено надзвичайно велике забруднення рослинності радіоактивними
опадами, а також великий вміст цезію у м'ясі овець. В результаті катастрофи вже
загинуло багато тисяч чоловік (понад 50 тис з 100 тис тих, які брали участь у
ліквідації аварії). Внаслідок Чорнобильської катастрофи на території України
забруднено 12 областей, 86 адміністративних районів, 2311 населених пунктів, де
загалом мешкає близько 2 млн 600 тис жителів, у тому числі - 600 тис дітей.
Забруднено радіонуклідами понад 7 млн гектарів землі, серед яких 3 млн га
сільськогосподарських угідь та 2 млн лісових масивів. Ще близько 1.5 млн
чоловік проживає на території, де радіоактивний фон у десятки разів перевищує
допустимі норми (Київська, Житомирська, Чернівецька, Рівненська, Черкаська,
Вінницька, Чернігівська, Кіровоградська, Івано-Франківська області).
Дезактиваційні роботи, на які в 1986-1989 роках було витрачено мільйони,
бажаних результатів не дали.
У водах Дніпра, Прип'яті, Київського
водосховища концентрація радіонуклідів і через 10 років після аварії була в
10-100 разів вищою, ніж до аварії, а в донних відкладах, особливо мулових,
збагачених органікою, накопичилася велика кількість радіоактивного бруду.
Вважається, що в грунті заплав і дна водойм 30-кілометрової зони накопичилося
близько 14400 Кі цезію-137, 7360 Кі стронцію-90, 250 Кі плутонію, а в
Київському водосховищі назбиралося вже більше 60 млн тонн радіоактивного мулу
(більше 2000 Кі цезію-137)
Велику небезпеку довкіллю завдають
близько 1000 тимчасових могильників навколо ЧАЕС, у яких знаходиться 40 млн
куб. м твердих відходів з сумарною радіоактивністю понад 200 тис Кі (одиниці
радіоактивності, що визначається як кількість будь-яких радіоактивних ядер, де
проходить 37 млрд. розпаді за секунду), і саркофаг над четвертим блоком, який
вибухнув. Там ще зосталася велика кількість радіоактивного бруду потужністю в
багато сотень тисяч кюрі, надійність нерозповсюдження якого зовсім не
гарантована. Могильники вже сьогодні протікають, саркофаг з роками стає все
більше радіоактивним, конструкції його просідають, деформуються.
1.
АНАЛІТИЧНИЙ ОГЛЯД ЛІТЕРАТУРИ
.1
Встановлення категорії небезпечності підприємств та уточнення розмірів
санітарно-захисної зони
Розрахувати КНП, розміри нормативної
та уточненої СЗЗ. Дані наведені в таблицях 1.1, 1.2.
Таблиця 1.1 - Вихідні дані для
курсової роботи
|
Назва речовин, які виділяються
|
ГДКс.д. , мг/м3
|
Клас небезпечності
|
Викид, т/рік
|
|
Толуол
|
0,03
|
2
|
1,567
|
|
Анилин
|
0,06
|
3
|
0,346
|
|
Ванадію (5)оксид
|
0,001
|
2
|
0,984
|
|
Діоксид азоту
|
0,05
|
3
|
1,678
|
|
Бутанол
|
0,003
|
4
|
23,865
|
|
Формальдегид
|
0,0003
|
1
|
0,045
|
Розраховуємо категорію небезпечності
підприємства (КНП) :
КНП = ∑ ( Мі / ГДК с.д.) aі (1.1)
де Мі - маса викиду і-тої речовини,
т/рік;
ГДКсд- середньодобова гранично
допустима концентрація і-тої речовини, мг/м3;- безрозмірна константа, яка
дозволяє порівняти ступінь шкідливості і-тої речовини зі шкідливістю сірчистого
газу.
КНП = (1,567/0,03)1,7 +
(0,346/0,06)1 + (0,984/0,01)1,3 + (1,678/0,5)1 + +
(23,865/0,003)0,9+(0,045/0,003)1,7= 832,6 +5,76 + 7778,4 + 33,56 + 3240,2 +
5004,4 = 16894,92
Отже, дане підприємство відноситься
до II класу небезпеки і повинно мати санітарно-захисну зону в розмірі 500 м.
Уточнюємо розміри санітарно-захисної
зони з врахуванням рози
вітрів (lСЗЗ) за формулою:
уточнене = L ∙ Р / Р0 (1.2)
де Р - повторюваність вітру у
конкретному напрямі, %;
Р0- середня повторюваність вітру при
коловій розі вітрів, 12,5%;нормативна ширина СЗЗ, м.
Уточнені розміри СЗЗ надано в
таблиці 1.2.
Таблиця 1.2 - Повторюваність
напрямків вітру
|
Румби
|
Пн
|
ПнСх
|
Сх
|
ПдСх
|
Пд
|
ПдЗ
|
3
|
ПнЗ
|
|
Р, %
|
15
|
6
|
7
|
10
|
12
|
6
|
8
|
9
|
|
L уточнене
|
600
|
240
|
280
|
400
|
480
|
240
|
320
|
360
|
За отриманих даних видно, що розміри
санітарно-захисної зони не витримані в Західному, Північному і
Північно-Західному напрямках.
.2
Розрахунок гранично допустимих викидів шкідливих газів в атмосферу від
одиночних джерел
Розрахувати ГДВ для бензапірену, що
викидаються заводами з різних виробництв для Черкаської області (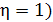 ,
А=180. Дані наведені в таблиці 1.3.
,
А=180. Дані наведені в таблиці 1.3.
Таблиця 1.3 - Вихідні дані для
курсової роботи
|
Назва шкідливих речовин
|
Висота джерела викиду Н, м
|
Діаметр гирла труби, D,м
|
Швидкість виходу газів,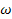 0,
м/с 0,
м/с
|
Температура викиду газів
|
Температура навколишнього повітря
|
ГДКмр, мг/м3
|
Фонова концентрація, мг/м3
|
|
Етиловий спирт
|
55
|
5,0
|
9,0
|
60
|
25
|
5,0
|
0,05
|
1. Визначаємо об’єм газоповітряної
суміші:
= 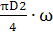 0
= (3,14
0
= (3,14 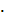 5,02/4)
∙ 9,0 =176,6 м3/с
5,02/4)
∙ 9,0 =176,6 м3/с
. Визначаємо коефіцієнт m:
= 103· 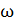 02·D/
Н2·
02·D/
Н2·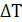 =1000·9,02·5,0/552·35 = 3,82< 100= 1/ (0,67 + 0,1
=1000·9,02·5,0/552·35 = 3,82< 100= 1/ (0,67 + 0,1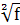 + 0,34
+ 0,34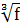 )=
1/ (0,67 + 0,1
)=
1/ (0,67 + 0,1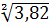 + 0,34
+ 0,34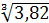 ) = 0,63
) = 0,63
. Визначаємо коефіцієнт n:
м = 0,65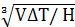 = 0,65
= 0,65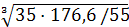 = 14,49
= 14,49
Оскільки Vм< 2, то n = 1
. Безрозмірний коефіцієнт F = 3.
.Визначаємо ГДВ:
ГДВ = (ГДК - Сф) ·Н2 ·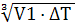 /
А· F· m·n·
/
А· F· m·n· 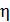 =(5,0 - 0,05)·
552··
=(5,0 - 0,05)·
552··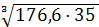 /
180 ·3 · 0,63 ·1·1= 3749,15 г/с.
/
180 ·3 · 0,63 ·1·1= 3749,15 г/с.
Висновок: ГДВ для етилового спирту,
що викидаються заводом на виробництві для Черкаської області становить 3749,15
г/с.
.3
Розрахунок оптимальної висоти труби, яка забезпечує дотримання гранично
допустимого викиду
Визначити мінімальні висоти труб для
викидів етилового спирту, що викидаються заводами з різних виробництв в
Черкаської області (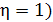 , А=180. Дані
наведені в таблиці 1.4.
, А=180. Дані
наведені в таблиці 1.4.
Таблиця 1.4 - Вихідні дані для
курсової роботи
|
Назва шкідливих речовин
|
ГДВ, г/с
|
Діаметр гирла труби, D,м
|
Швидкість виходу газів,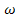 0,
м/с 0,
м/с
|
Температура викиду газів
|
Температура навколишнього повітря
|
ГДКмр, мг/м3
|
Фонова концентрація, мг/м3
|
|
Етиловий спирт
|
0,56
|
5,0
|
9,0
|
60
|
25
|
5,0
|
0,05
|
Розв’язок
. Визначаємо об’єм газоповітряної
суміші:
= 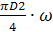 0
= (3,14
0
= (3,14 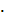 52/4)
∙ 9,0 = 176,6 м3/с.
52/4)
∙ 9,0 = 176,6 м3/с.
. Визначаємо значення Н за формулою:
Н = [ А·М·F·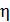 ·D
/ 8V1· (ГДК - Сф)]3/4 =(180·0,56·3·1·5,0/8·176,6·4.95)3/4 = 0,31м
·D
/ 8V1· (ГДК - Сф)]3/4 =(180·0,56·3·1·5,0/8·176,6·4.95)3/4 = 0,31м
. Визначаємо значення Vм :
:
м =
1,3·
=
1,3·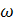 0·
D / Н = 1,3·9,0·5,0/0,31 = 188,7
0·
D / Н = 1,3·9,0·5,0/0,31 = 188,7
. Так як викид гарячий(∆T>
0), то обраховуємо 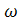 0
0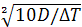 :
:
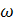 0
0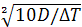 = 9,0·
= 9,0·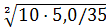 =10,71
=10,71
. Оскільки H>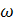 0
0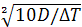 ,
то H=0,31м
,
то H=0,31м
Висновок: Так як можна вважати, що
оптимальна висота труби складає 0,31м.
1.4
Розрахунковий метод визначення класу небезпеки промислових відходів
Розрахувати клас небезпеки
промислових відходів за даними наведеними в таблиці 1.5.
Визначаємо індекси токсичності
кожного хімічного інгредієнта:
К1 = lg(LD50 )/ (S + 0,1F + Св) (1.3)
Таблиця 1.5 - Вихідні дані для
курсової роботи
|
Назва інгредієнта
|
Хімічна формула
|
Вміст інгредієнта, %
|
LD50
|
Розчинність у воді,/100 г, S
|
Коефіцієнт леткості, F
|
|
Оксид ванадію
|
V2O5
|
30
|
23,4
|
0,07
|
0
|
|
Хлорид ртуті
|
HgCl2
|
40
|
175
|
6,6
|
0,0013
|
|
Сульфат кадмію
|
CdSO4
|
30
|
47
|
76,4
|
0
|
[V2O5] =
lg23,4 / (0,07+0,1×0+0,3) = 2,9[HgCl2] = lg175 /
(6,6+0,1×0,0013+0,4) = 0,32[CdSO2] = lg47 / (76,4+0,1×0+0,3) = 0,02
Перевіряємо умову 2K1 >K3: 2 •
2,4 = 4,8
Оскільки умова виконується, то для
розрахунку береться два індекса K для інгредієнтів.
Визначаємо сумарний індекс
небезпеки:
К∑ = ( 1/n2) ∙ ∑Кі=
(1/22)∙ (0,32+0,02) = 0,085
Висновок: У цьому разі К∑ =
0,085 тому відходи з хімічного підприємства належать до I класу небезпеки . Для
зниження небезпечності потрібно проводити заходи, які спрямовані на поліпшення
умов на виробництві.
1.5
Загальний принцип встановлення гранично допустимого скиду для водотоків
Розрахувати ГДС (г/с) і допустимі
концентрації керосину у стічних водах, які скидаються в бистрі ріки. Вихідні
дані для розрахунків надано в таблиці 1.6.
Таблиця 1.6 - Вихідні дані для
розрахунку ГДС
|
Забруднююча речовина
|
Витрата річкової води, м3/с
|
Швидкість течії,м/с
|
Глибинарічки, М
|
Фонова концентрація, мг/л
|
Витрата стічних вод, м3/с
|
Відстань до створу, км
|
ГДК мг/л
|
Коефіцієнт покрученості річки
|
|
сульфат
|
450
|
1,5
|
2,5
|
128,5
|
37,8
|
3
|
300
|
2,0
|
. Визначаємо коефіцієнт турбулентної
дифузії D:
= VсрНср / 200 = 1,5∙ 2,5/200
= 0,018
. Визначаємо коефіцієнт, що враховує
гідравлічні умови змішуванняα:
α = εφ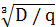 =
1,5 ∙ 3 = 0,117
=
1,5 ∙ 3 = 0,117
. Розраховуємо проміжний коефіцієнт β:
β=e-a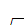 -
= e-0,117
-
= e-0,117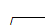 = 0,17
= 0,17
. Розраховуємо коефіцієнт змішування
γ:
γ = (1 - β) / [1 + β ∙Q
/q]= (1 - 0,17) / (1+0,17∙450/37,8) = 0,4
. Визначаємо кратність розбавлення
n:
n = (γQ + q) /q= (0,4∙450+37,8)
/ 37,8 = 5,76
. Визначаємо допустиму концентрацію
сульфату у стічних водах ( Сст):
Сст = n∙(ГДК - Св) + Св= 5,76 ∙
(300 - 128,5) + 128,5 = 1116 мг/л
. Розраховуємо гранично - допустимий
скид:
ГДС = Сст∙q= 1116∙37,8=
42184,8 г/с
Висновок: Допустима концентрація
сульфату у стічних водах складає 1116мг/м3, а ГДС дорівнює 42184,8 г/с.
2 . ОЦІНКА ТА НОРМИ РАДІАЦІЙНОГО
ВПЛИВУ НА БІОТУ
2.1
Загальні положення
Державні санітарні норми і правила
при роботі з джерелами електромагнітних полів (далі - санітарні норми і
правила) встановлюють вимоги до умов праці працівників, що займаються
виготовленням, експлуатацією, обслуговуванням та ремонтом обладнання, при
роботі якого виникають постійні магнітні поля (далі-ЕМП) та електромагнітні
випромінювання (далі - ЕМВ) у діапазоні частот від 50,0 Гц до 300,0 ГГц.
Робоча зона - простір заввишки до 2
м над рівнем підлоги або площини, на яких розташовані місця постійного або
тимчасового перебування працівників.
Постійні магнітні поля, а також
змінні ЕМП на частоті 50 Гц нормуються за магнітною (Н) та електричною (Е)
складовими ЕМП. Одиницею напруженості магнітного поля є ампер на метр (А/м),
електричного поля - вольт на метр (В/м).
Граничнодопустимі рівні
електромагнітних полів: ГДР електромагнітних полів промислової частоти (50 Гц)
ГДР електричних полів частотою 50 Гц визначаються залежно від часу дії цього
фактора на організм людини за робочу зміну. Перебування в електричному полі
напруженістю до 5 кВ/м включно допускається протягом 8 годин робочого дня.
У зв’язку з тім, що напруга, яка
використовується в електрозварювальних установках,не перевищує 660 В, рівень
електричного поля на робочих місцях зварників не перевищує граничнодопустимих
значень. Рівні напруженості магнітного поля частотою 50 Гц при постійному
впливі не повинні перевищувати 1,4 кА/м протягом робочого дня (8 год).
радіація людина генетичний доза
Таблиця 2.1 - Час перебування людини
в магнітному полі напруженістю понад 1,4 кА/м регламентується
|
Час перебування персоналу, рік
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
|
Напруженість магнітного поля, А/м
|
6,0
|
4,9
|
4,0
|
3,2
|
2,5
|
2,0
|
1,6
|
1,4
|
|
Магнітна індукція, мТл
|
7,5
|
6,13
|
5,0
|
4,0
|
3,13
|
2,5
|
2,0
|
1,75
|
ГДР для змінного магнітного поля
частотою 50 Гц при локальному впливі на кисті рук визначається за формулою:
Нгд лок=Нгд заг×5
де Нгд лок - ГДР змінного магнітного
поля частотою 50 Гц при локальному впливі (кисті рук), А/м;
НГДЗАГ - ГДР змінного магнітного
поля частотою 50 Гц при загальному впливі (табл.1), А/м.
2.1.1
3агальні вимоги до проведення вимірювань та гігієнічна оцінка результатів
досліджень
Оцінка рівнів дії постійних
магнітних полів, а також змінних ЕМП у діапазонах частот 50 Гц, 1 кГц-300 МГц
здійснюється шляхом вимірювання напруженості електричної і магнітної складових
Ем. Якщо установка має декілька робочих режимів, що відрізняються параметрами
генерації, видом і розміщенням робочих елементів або випромінювальних систем та
ін., вимірювання проводиться в кожному режимі при максимально використаній
потужності. Якщо на робочому місці працюючого можливе опромінювання від декількох
установок, що працюють одночасно, інтенсивність його має бути оцінена для
кожного з вимірюваних джерел. Апаратура, яка використовується для
санітарно-гігієнічних досліджень рівнів ЕМП повинна мати свідоцтво про
метрологічну повірку.
Приміщення у яких розміщуються
установки, які є джерелами ЕМП, повинні відповідати вимогам, діючих санітарних
норм щодо проектування промислових підприємств і за своїм планувальним рішенням
відповідати характеру виконуваних у них технологічних процесів. Рівні освітлення,
опалення і вентиляції приміщень повинні відповідати вимогам будівельних норм і
правил.
Метеорологічні умови в приміщеннях,
наявність у повітрі робочої зони шкідливих речовин, рівень шуму, а також інших
несприятливих факторів виробничого середовища повинні відповідати вимогам,
указаним у відповідних нормативних документах, затверджених Міністерством
охорони здоров'я України.
устаткування, яке є джерелами ЕМП,
залежно від конструкції, призначення, потужності й умов використання, можуть
розміщуватись як в окремих, спеціально призначених приміщеннях, так і в
загальних приміщеннях, включаючи розміщення в поточних лініях, при дотриманні
вимог розділу 4 санітарних норм і правил. При розміщенні устаткування і
організації робіт щодо його обслуговування слід, крім цих санітарних норм та
правил, також керуватись: будівельними нормами і правилами;правилами
влаштування електроустановок; правилами технічної експлуатації електроустановок
споживачів і правилами техніки безпеки при експлуатації електроустановок
споживачів.
Захисні засоби повинні відповідати
вимогам правил використання і випробування захисних засобів, які
використовуються в електроустановках. Допускається при погодженні з органами
державного санітарно-епідеміологічного нагляду проведення робіт щодо настроювання
і регулювання апаратури, яка є джерелом ЕМП, в екранованих приміщеннях. Робочі
площі та об'єми екранованих приміщень повинні встановлюватись, виходячи з
габаритів оброблюваних виробів, з урахуванням вимог безпеки при роботі з
високою напругою і санітарних норм проектування промислових підприємств. Для
унеможливленім перевищення ГДР за рахунок відбитого випромінювання стіни, стелю
і підлогу екранованих приміщень необхідно покривати матеріалами, що поглинають
ЕМВ до допустимих рівнів.
Засоби захисту слід використовувати
при всіх видах робіт, якщо умови останніх не відповідають вимогам розділу 4 цих
санітарних норм і правил. Захист персоналу від дії ЕМП досягається шляхом
проведення організаційних, інженерно-технічних заходів, а також використання
засобів індивідуального захисту. До організаційних заходів належать: вибір
раціональних режимів праці установок, обмеження місця і часу перебування
персоналу в зоні опромінювання і т. ін.
Інженерно-технічні заходи включають
раціональне розміщення обладнання, використання засобів, які обмежують
надходження електромагнітної енергії на робочі місця персоналу (поглинальні
матеріали, екранування).
До засобів індивідуального захисту
належать захисні окуляри, щитки, шоломи, захисний одяг (комбінезони, халати з
металовмісної тканини; окуляри з металовмісним склом).
Засіб захисту в кожному конкретному
випадку повинен визначатись з урахуванням робочого діапазону частот, характеру
робіт, необхідної ефективності захисту. Особи (фахівці), які проводять
дослідження електромагнітних випромінювань, повинні мати засоби індивідуального
захисту від впливу ЕМВ. На кожний засіб захисту повинна бути складена технічна
документація з відміткою про призначення та діапазон частот, у яких цей засіб
захисту може бути використаний, допустимої потужності розсіювання, забезпеченої
ефективності захисту за всім діапазоном частот, на який розраховано
використання даного засобу. У діапазонах частот 50 Гц, 1 кГц - 300 МГц
(розробка, використання, випробування, експлуатація установок для термообробки
матеріалів, засобів зв'язку, фізіотерапевтичної апаратури) захист.
Службові приміщення на території
об'єкта слід розміщувати переважно в місцях, захищених від ЕМП
("радіотінь", "мертва зона"), орієнтувати так, щоб було
унеможливлене опромінювання вікон і дверей, у разі необхідності - екранувати.
Маршрути руху персоналу на території об'єкта слід установлювати таким чином,
щоб унеможливити опромінювання при рівнях, що перевищують граничнодопустимі.
Зони випромінювання з ЩПЕ вище 10 Вт/м2 (1000 мкВт/см2) повинні бути позначені
спеціальними попереджувальними знаками.
.1.2
Правовий статус
НРБУ-97 є основним державним
документом, що встановлює систему радіаційно-гігієнічних регламентів для
забезпечення прийнятих рівнів опромінення як для окремої людини, так і для
суспільства взагалі і є обов'язковими для виконання всіма юридичними та
фізичними особами, які проводять практичну діяльність з джерелами іонізуючого
випромінювання.
НРБУ-97 поширюються на ситуації
опромінення людини джерелами іонізуючого випромінювання в умовах:
нормальної експлуатації
індустріальних джерел іонізуючого випромінювання;
медичної практики;
радіаційних аварій;
опромінення техногенно-підсиленими
джерелами природного походження.
Відповідальність за виконання
НРБУ-97 покладається на:
фізичні та юридичні особи, незалежно
від форм власності та підпорядкованості які виробляють, переробляють,
застосовують,зберігають, транспортують, здійснюють поховання, знищення
чиутилізацію джерел іонізуючого випромінювання, а також проектують роботи з
ними;
керівників та посадових осіб органів
Державної виконавчої влади і організацій, які планують та реалізують
контрзаходи вчастині Норм, що стосується обмеження опромінення при радіаційних
аваріях та опромінення від техногенно-підсилених джерел природного походження.
Особи, які допустили протиправні дії
з джерелами іонізуючих випромінювань, чи не планують або не реалізують
контрзаходи по зменшенню рівнів опромінення до регламентованихНРБУ-97 величин,
притягуються до відповідальності відповідно до чинного законодавства України.
2-5 З моменту офіційного опублікування Норм радіаційної безпеки України, дія
НРБ-76/87 відміняється.
За виключенням випадків, окремо
розглянутих і узгоджених з державними регулюючими органами. Будь-які діючі
відомчі та галузеві норми, правила,інструкції та інші нормативно-правові акти,
які прямо або опосередковано пов'язані з протирадіаційним захистом людини
повинні бути приведені у відповідність до вимог НРБУ-97 у строки,узгоджені з
органами Державного санітарно-епідеміологічного нагляду, а ті, що створюються -
не повинні їм суперечити.
Норми радіаційної безпеки України
(НРБУ-97) охоплюють систем принципів, критеріїв, нормативів та правил,
виконання яких є обов'язковим в політиці держави щодо забезпечення
протирадіаційного захисту людини та радіаційної безпеки.
Підстава для розробки
нормативно-правового акта відносно захоронення радіаційних відходів.
Згідно із чинним законодавством
України прийняття рішень щодо можливості/неможливості захоронення радіоактивних
відходів (далі - РАВ) з певними характеристиками у поверхневих (при
поверхневих) сховищах базується на концепції обмеження рівнів поточного та
потенційного опромінення населення, в тому числі майбутніх поколінь, та
відповідній системі критеріїв (регламентів). При цьому можуть розглядатися
варіанти захоронення РАВ з наданням через 300 років після припинення
експлуатації сховища повного або обмеженого звільнення РАВ у системі
захоронення від регулюючого контролю.
Вимоги, пов’язані з прийняттям таких
рішень, в тому числі рішень з боку органів державного регулювання ядерної та
радіаційної безпеки (далі - органи державного регулювання ЯРБ), встановлені в
НРБУ-97, НРБУ-97/Д-2000 та ОСПЗРБУ. Досвід застосування цих нормативно-правових
актів (далі НПА) на практиці виявив нагальну необхідність створення додаткового
НПА, який у більш детальній і прозорій формі встановлює процедури, що потрібно
виконати крок за кроком, для обґрунтування можливості прийняття певного
рішення.
Правила та умови звільнення
радіоактивних відходів, розміщених в при поверхневих сховищах, від регулюючого
контролю деталізують вимоги законодавства України, в тому числі НРБУ-97,
НРБУ-97/Д-2000, ОСПЗРБУ, що стосуються можливості/неможливості захоронення
радіоактивних відходах (далі - РАВ) у поверхневих (при поверхневих) сховищах
РАВ (далі при поверхневі сховища).
Крім цього, підставою для розробки
НПА є:
) Закони України:
«Про використання ядерної енергії та
радіаційну безпеку»;
«Про поводження з радіоактивними
відходами»;
) Комплексна програма (у редакції
постанови Кабінету Міністрів України від 25 грудня 2002 р. № 2015);
) Пункт 1.7Н Змін до Плану
прикладних досліджень у сфері ядерного регулювання на 2006 рік, затверджених
наказом від 01.09.06 № 135,
) Рішення Колегії України від 5
жовтня 2006 року № 15;
) Результати наради, що відбулась в
МОЗ 12.09.06 за участю представників МОЗ, МНС, України, установ та організацій,
що здійснюють діяльність у сфері поводження з РАВ.
Крім цього при розробці правил умов
був використаний рекомендаційний документ «Рекомендації щодо встановлення
критеріїв приймання кондиційованих радіоактивних відходів на захоронення у при
поверхневих сховищах» (РД 306.4.098-2004).
Розробка правил та умов виконана
Науковим центром радіаційної медицини Академії медичних наук України у
співпраці з експертами Державного науково-технічного центру з ядерної та
радіаційної безпеки (ДНТЦ ЯРБ) згідно технічного завдання на виконання роботи,
затвердженого 25 вересня 2006 року.
Правила та умови:
тлумачать та конкретизують
застосування основних термінів в сфері радіаційної безпеки стосовно діяльності
щодо захоронення РАВ;
визначають завдання, які потрібно
послідовно виконати під час обґрунтування можливості захоронення РАВ з певними
характеристиками у конкретних при поверхневих сховищах;
встановлюють процедури виконання цих
завдань в залежності від варіанту звільнення РАВ (повне, обмежене, обмежене зі
спеціальними вимогами) по завершенні періоду 300 років після припинення
експлуатації (початку закриття) сховища (далі - період 300 років).
Вимоги не поширюються на РАВ, що
утворюються в процесі видобутку та переробки уранових руд. Галуззю застосування
правил і умов є сфера поводження з РАВ в частині захоронення РАВ з певними
характеристиками у конкретних при поверхневих сховищах та регулювання безпеки
діяльності в цій сфері.
Розробка правил та умов здійснюється
з метою:
вдосконалення нормативно-правової
бази у сфері поводження з РАВ;
забезпечення належного рівня захисту
людини та навколишнього природного середовища від впливу іонізуючого
випромінювання;
визначення кількісних характеристик
РАВ (зокрема, активності по кожному радіонукліду) для усіх типів звільнення
РАВ, у при поверхневих сходах.
Головною метою є, в першу чергу,
детальні роз’яснення та тлумачення тих норм, правил та вимог НРБУ-97 (Розділ
9), НРБУ-97/Д-2000 (Розділ 4) та ОСЗРБУ (Розділ 15), що містять такі поняття,
як «повне звільнення», «обмежене звільнення» та «обмежене звільнення із
спеціальними вимогами», а також співвідношення між цими поняттями та поняттям
«рівні вилучення».
НРБУ-97 поширюються на ситуації
опромінення людини джерелами іонізуючого випромінювання в умовах:
нормальної експлуатації
індустріальних джерел іонізуючого випромінювання;
медичної практики;
радіаційних аварій;
опромінення техногенно-підсиленими
джерелами природного походження.
НРБУ-97 включають чотири групи радіаційно-гігієнічних
регламентованих величин:
Перша група - регламенти для
контролю за практичною діяльністю, метою яких є додержання опромінення
персоналу та населення на прийнятному для індивідууму та суспільства рівні, а
також підтримання радіаційно-прийнятного стану навколишнього середовища та
технологій радіаційно-ядерних об'єктів як з позицій обмеження опромінення
персоналу та населення, так і з позицій зниження імовірності виникнення аварій
на них. До цієї групи входять:
ліміти доз;
похідні рівні:
допустимі рівні;
контрольні рівні.
Друга група - регламенти, що мають
за мету обмеження опромінення людини від медичних джерел. До цієї групи
входять:
рекомендовані рівні.
Третя група - регламенти щодо
відвернутої внаслідок втручання дози опромінення населення в умовах радіаційної
аварії. До цієї групи входять:
рівні втручання;
рівні дії.
Четверта група - регламенти щодо
відвернутої внаслідок втручання дози опромінення населення від
техногенно-підсилених джерел природного походження. До цієї групи входять:
рівні втручання;
рівні дії.
Нормами радіаційної безпеки
встановлюються такі категорії осіб які зазнають опромінювання:
Категорія А (персонал) - особи, які
постійно чи тимчасово працюють безпосередньо з джерелами іонізуючих
випромінювань.
Категорія Б (персонал) - особи, які
безпосередньо не зайняті роботою з джерелами іонізуючих випромінювань, але у
зв'язку з розташуванням робочих місць в приміщеннях та на промислових
майданчиках об'єктів з радіаційно-ядерними технологіями можуть отримувати
додаткове опромінення.
Категорія В - все населення.
Ліміти доз та допустимі рівні.
Числові значення лімітів доз
встановлюються на рівнях, що виключають можливість виникнення детерміністичних
ефектів опромінення і, одночасно, гарантують настільки низьку імовірність
виникнення стохастичних ефектів опромінення, що вона є прийнятною як для
окремих осіб, так і для суспільства в цілому.
Для осіб категорій А і Б ліміти доз
встановлюються в термінах індивідуальної річної ефективної та еквівалентних доз
зовнішнього опромінення (ліміти річної ефективної та еквівалентної доз).
Обмеження опромінення осіб категорії В (населення) здійснюється введенням
лімітів річної ефективної та еквівалентної доз для критичних груп осіб
категорії В. Останнє означає, що значення річної дози опромінення осіб, які
входять в критичну групу, не повинно перевищувати ліміту дози, встановленого
для категорії В.
З лімітом дози порівнюється сума
ефективних доз опромінення від усіх індустріальних джерел випромінювання. До
цієї суми не включають:
дозу, яку одержують при медичному
обстеженні або лікуванні;
дозу опромінення від природних
джерел випромінювання;
дозу, що пов'язана з аварійним
опроміненням населення;
дозу опромінення від
техногенно-підсилених джерел природного походження.
Додатково до ліміту річної ефективної
дози встановлюються ліміти річної еквівалентної дози зовнішнього опромінення
окремих органів і тканин:
кришталика ока;
шкіри;
Таблиця 2.2 - Ліміти дози
опромінення (мЗв.рік в ступені -1)
|
Категорія осіб, які зазнають опромінювання
|
|
А а)б)
|
Б а)
|
В а)
|
|
ЛД E (ліміт ефективної дози) Ліміти
еквівалентної дози зовнішнього опромінення: - ЛДlens (для кришталика ока) -
ЛДskin (для шкіри) - ЛДextrim (для кистей та стіп)
|
20 в) 150 500 500
|
2 15 50 50
|
1 15 50 -
|
Примітки: а) - розподіл дози
опромінення протягом календарного року не регламентується; б) - для жінок
дітородного віку (до 45 років), та для вагітних жінок діють обмеження пункту
5.6; в) - в середньому за будь-які послідовні 5 років, але не більше 50 мЗв за
окремий рік (ЛДmax)
Встановлюється такий перелік
допустимих рівнів (ДР), які відносяться до радіаційно-гігієнічних регламентів
першої групи.
Для категорії А:
допустиме надходження (ДНinhal А)
радіонукліду через органи дихання;
допустима концентрація (ДКinhal А)
радіонукліду в повітрі робочої зони;
допустима потужність дози
зовнішнього опромінення (ДПД А);
допустиме радіоактивне забруднення
(ДЗ А) шкіри, спецодягу та робочих поверхонь.
Для категорії Б:
допустиме надходження (ДНinhal Б)
радіонукліда через органи дихання:
концентрація (ДКinhal Б)
радіонукліда в повітрі робочої зони;
Для категорії В:
допустиме надходження радіонукліда
через органи дихання (ДНinhal В) і травлення (ДНingest);
допустимі концентрації радіонукліда
в повітрі (ДНinhal В) та питній воді (ДНingest);
допустимий скид та викид у довкілля.
Числові значення допустимих рівнів
(ДН, ДК) розраховані для умов впливу одного радіонукліду та одного шляху
надходження при референтних умовах опромінення подані у Додатку 2. Ці числові
значення є радіаційно-гігієнічними регламентами.
Величини допустимих рівнів
розраховані з умов надходження одного батьківського радіонукліду і відсутності
в момент надходження дочірніх продуктів розпаду. Акумуляція в організмі
дочірніх продуктів розпаду, що виникли після надходження в організм, врахована
у величинах ДР. Дочірні радіонукліди, що надходять в організм разом з
батьківськими, розглядаються в умовах, як самостійні радіонукліди.
Якщо є дані про фактичні умови
опромінення, що суттєво відрізняються від референтних, допускається перегляд ДР
для окремого підприємства, технології, робочого місця тощо. Розробка і
затвердження таких ДР проводиться у порядку, встановленому Міністерством
охорони здоров'я України.
2.2
Дозиметрія радіації
.2.1
Формування дози опромінення в біологічному середовищи
При формуванні дози опромінення в
біологічному середовищі розрізняються безпосередньо іонізуючі частки і побічно
іонізуючі частки. Безпосередньо іонізуючі частки - це заряджені частки:
альфа-частки (ядра гелію), бета-частки (електрони, позитрони) і ін. а побічно
іонізуючі частки - це незаряджені частки: нейтрони, гамма-кванти.
При опроміненні біологічних
індивідуумів розрізняють гостре (що виявляється ранніми ефектами опромінення) і
пролонговане (тривале), однократне і багатократне (фракціоноване) опромінення.
Як гостре, так і пролонговане опромінення може бути однократним або
фракціонованим. Крім того, можливе хронічне опромінення, яке можна розглядати
як різновид фракціонованого, але такого, що здійснюється тривалий час при дуже
малих потужностях дози. Дозу, що формується випромінюванням в речовині можна
оцінити, вимірюючи, наприклад, викликане ним підвищення температури. Проте,
навіть при дозах небезпечних для життя людини, енергії, що виділяється,
виявляється недостатньо для нагріву опромінюваного організму на тисячні долі
градуса. Тому при вивченні дії випромінювання на біологічні об'єкти, дози
оцінюють із застосуванням чутливіших методів дозиметрії. Розподіл дози в часі
для різних по лінійній передачі енергії (ЛПЕ) випромінювань може значно
розрізнятися і по-різному позначатися на радіобіологічних ефектах опромінення.
Це виявляється особливо на віддалених наслідках біологічної дії випромінювань
різних ЛПЕ, у зв'язку з чим, визначенню тимчасового розподілу дози в
радіобіології приділяється серйозна увага. Іонізуюче випромінювання,
взаємодіючи з речовиною, передає йому енергію малими, кінцевими порціями.
Передача енергії є процесом випадковим. Випадковою є і енергія, передавань
речовині в кожному акті взаємодії. Тому поглинена в деякому об'ємі речовини
енергія при багатократному опроміненні його в тотожних умовах однією і тією ж
дозою іонізуючого випромінювання одного вигляду, строго кажучи, є дещо різною.
Необхідно пам'ятати про принципово завжди присутні, але не завжди істотні флуктуації
(розкиди) енергії, що поглинається (і, відповідно, поглиненої дози).У випадку
малих опромінюваних об'ємів, порівняних по величині з об'ємом окремих клітин,
або субклітинних структур, можлива ситуація, при якій флуктуації поглиненої
дози виявляються порівняними і навіть перевершують величину дози. У таких
умовах зіставлення виходу радіаційно-індукованих ефектів з поглиненою дозою
стає неоднозначним і виникає необхідність враховувати ці флуктуації. Флуктуації
тим значніше, чим менше об'єм, в якому оцінюється величина поглиненої дози, і
чим більше величина ЛПЕ випромінювання, що формує цю дозу. В випадку формування
так званих "малих доз" опромінення (у мікродози метричному розумінні
даного терміну, яке не завжди збігається з його біологічним розумінням), кількість
пронизуватих треками іонізуючого випромінювання чутливих мікрооб'ємів в
опромінюваному об'єкті істотно менше їх загального числа. В цьому випадку
спостережувана, в середньому, лінійна зміна ступені прояву того або іншого
радіобіологічного ефекту від дози випромінювання пов'язана просто із зростанням
числа чутливих мікрооб'ємів, що пронизуються треками випромінювання, а не з
власне лінійним характером дозової залежності виходу цього ефекту. Подібна
ситуація найчастіше реалізується в штатних умовах професійного опромінення і
при дії на людину випромінювання радіаційного фону Землі, що формує, як відомо,
поглинені дози облучення на рівні сотень міллігрей в рік (мГр/рік). Це означає,
що протягом року через чутливі об'єми окремих кліток організму людини дуже
рідко проходить більше одного трека, а через іншу їх частину за цей же час
треки взагалі не проходять. Кількісна радіобіологія, навпаки, найчастіше вивчає
дію випромінювання в таких умовах, коли кожен чутливий мікрооб'єм в
опромінюваному біологічному об'єкті пронизується великим числом треків і
збільшення дози опромінення відповідає умові збільшення числа треків через
кожен з його чутливих мікрооб'ємів.
.2.2
Основні фізичні велечини дозометрії
Першопричиною радіаційних ефектів є
поглинання енергії випромінювання опромінюваним об'єктом, і доза, як міра
поглиненої енергії, є основною дозиметричною величиною. Тому, основною фізичною
дозиметричною величиною, що використовується для оцінки міри дії випромінювання
на середовище, є поглинена доза випромінювання. Поглинена доза випромінювання
(D) - це величина що визначається енергією випромінювання (Дж) поглинаємою
одиницею маси (кг) опромінюваної речовини. За одиницю дози в системі СІ
прийнятий грей (Гр):D = 1Дж/1кг=1 Гр.Грей це така доза іонізуючого випромінювання,
при якій ділянці речовини масою 1 кг передається енергія 1 Дж. Позасистемною
одиницею є "рад". 1 рад = 0,01 Гр.
Поглинена доза характеризує не саме
випромінювання, а міру його дії на середовище. В принципі один і той же потік
випромінювання в різних середовищах і навіть в різних ділянках одного
середовища може сформувати різну величину поглиненої дози. Тому, коли говорять
про поглинену дозу, необхідно вказувати, в якому середовищі вона сформована: в
повітрі, воді або м'якій біологічній тканині.Для характеристики розподілу дози
опромінення в часі використовують величину потужності поглиненої дози, або
інтенсивності опромінення. Під цим розуміють кількість енергії випромінювання,
що поглинається в одиницю часу одиницею маси опромінюваної речовини (Гр/година;
Гр/рік).При практичному використанні випромінювань людина, виключаючи
спеціальні випадки медичних дій і радіаційні аварії, піддається дії малих доз
опромінення. Умови роботи професіоналів в даний час найчастіше відповідають
ситуації, коли чутливі мішені кліток їх організму одиничних треків іонізуючих
часток, що формують дозу опромінення, істотно більше того часу, впродовж якого
працюють репаративні (відновні) системи кліток, що усувають порушення,
викликані частинкою що пройшла.
В цих умовах індуковані біологічні
ефекти не залежать від таких чинників, як потужність дози, її розподіл, умови і
ритм опромінення. Вихід ефектів визначається лише сумарною накопиченою дозою
(незалежно від часу опромінення), тобто наслідки опромінення будуть однаковими
при однократному опроміненні даною дозою, або при її здобутті протягом
декількох днів, місяців і навіть року. На міру вираженості ефекту впливатиме
лише просторовий розподіл актів іонізації і збудження, що створюються в треках,
тобто лінійного передавання енергії (ЛПЕ) іонізуючого випромінювання. Тому, для
таких умов введена спеціальна величина дози, що враховує обидва цих чинника, -
еквівалентна доза. Цією величиною можна однозначно пов'язати вихід радіаційних
наслідків опромінення з дозою опромінення.
Еквівалентна доза (Н) визначається
як добуток поглиненої дози (D) даного виду випромінювання на середнє значення
звужуючого фактору (коефіцієнта якості) іонізуючого випромінювання (WR), в
даному елементі - об'єму біологічної тканини. Значення WR для різних видів випромінювань
представлені в таблиці 1. Ця доза є міра виваженості стохастичних ефектів
опромінення. Вона застосовна для оцінки радіаційної небезпеки хронічного
опромінення випромінюванням довільного складу (і гострого опромінення дозою
менше 0,25 зіверт) і визначається за формулою:
Н = D • WR
За одиницю еквівалентної дози в
системі СІ прийнятий зіверт (Зв). Зіверт дорівнює такій еквівалентній дозі, при
якій, величина добутку поглиненої в біологічній тканині дози іонізуючого
випромінювання на середнє значення зважуючого фактору, для цього випромінювання
дорівнює 1 Дж/кг. Позасистемною одиницею є "бер" (біологічний
еквівалент рентгена). 1 бер = 0,01 Зв.
З визначення виходить, що для
випромінювання з WR = 1, еквівалентна доза 1 Зв реалізується при поглиненій дозі
1 Гр, тобто для цього випадку 1 Зв = 1 Гр. Якщо ж WR відмінно від 1, то
еквівалентна доза 1 Зв буде сформована в біологічній тканині при величині
поглиненої дози в ній рівною (1/WR) Гр. Допускається підсумовування
еквівалентних доз для оцінки загального рівня опромінення за тривалий проміжок
часу, якщо кожна разова доза, що мала місце при фракціонованому гострому
опромінення за цей час не перевищувала 0,25 Зв.
Таблиця 1 - Значення радіаційних
зважуючих факторів (WR)
|
Вид випромінювання і діапазон енергії
|
WR
|
|
|
Фотони, всі енергії (включаючи гама- і
рентгенівське випромінювання)
|
1
|
|
|
Електрони (позитрони) і мюони, всі енергії
|
1
|
|
Протони з енергією > 2 МеВ
|
5
|
|
Нейтрони з енергією < 10 кеВ
|
5
|
|
Нейтрони з енергією від 10 кеВ до 100 кеВ
|
10
|
|
Нейтрони з енергією від 100 кеВ до 2 МеВ
|
20
|
|
Нейтрони з енергією від 2 МеВ до 20 МеВ
|
10
|
При заданій еквівалентній дозі
опромінення вірогідність виходу стохастичних наслідків залежить від
опромінюваної їм тканини або органу. Тому, був введений ще один коефіцієнт, що
враховує специфіку різних тканин з точки зору вірогідності індукції в них
стохастичних наслідків опромінення, - тканинний звужуючий фактор (WT). Прийняті
в теперішній час значення WT представлені в таблиці 2 і використовуються
виключно для розрахунку ефективної дози. Звужуючі тканинні фактори введені,
виходячи з концепції безпорогової дії випромінювань, а їх величини відповідають
виходу стохастичних наслідків для різних органів і тканин, отриманому на основі
лінійної екстраполяції наявних даних з області великих доз опромінення
(оскільки реальний вихід стохастичних наслідків в області малих доз невідомий).
Абсолютні значення факторів
підібрані так, щоб їх сумарна величина дорівнювала одиниці. Це дозволяє
трактувати тканинні зважуючі фактори, як набір коефіцієнтів, що визначають
відносні вклади відповідних органів в сумарний вихід стохастичних наслідків, що
виникають при рівномірному опроміненні всього організму. Самим радіо чутливим
органом по критерію виходу цих наслідків є статеві залози, повністю
відповідальні за генетичні ефекти і частину соматичних стохастичних наслідків
опромінення.
Таблиця 2 - Значення тканинних
зважуючих факторів (WT)
|
Тканина або орган
|
WT
|
|
|
Гонади (статеві залози)
|
0.20
|
|
|
Червоний кістяний мозок
|
0.12
|
|
Товста кишка
|
0.12
|
|
Легені
|
0.12
|
|
Шлунок
|
0.12
|
|
Сечовий міхур
|
0.05
|
|
Молочна залоза
|
0.05
|
|
Печінка
|
0.05
|
|
Стравохід
|
0.05
|
|
Щитовидна залоза
|
0.05
|
|
Шкіра
|
0.01
|
|
Кісткова поверхня
|
0.01
|
|
Інші тканини і органи (наднирки, нирки,
головний мозок, дихальні шляхи позагрудної області, мишці, матка, селезінка,
тонка кишка, підшлункова і вилочкова залоза)
|
0.05
|
|
Все тіло
|
1.00
|
Абсолютні значення факторів
підібрані так, щоб їх сумарна величина дорівнювала одиниці. Це дозволяє
трактувати тканинні зважуючі фактори, як набір коефіцієнтів, що визначають
відносні вклади відповідних органів в сумарний вихід стохастичних наслідків, що
виникають при рівномірному опроміненні всього організму. Самим радіо чутливим
органом по критерію виходу цих наслідків є статеві залози, повністю
відповідальні за генетичні ефекти і частину соматичних стохастичних наслідків
опромінення.
Фізичний сенс поняття ефективної
дози наступний: значення ефективної дози (Е) відповідає такому рівню
рівномірного опромінення всього організму, при якому сумарний вихід
стохастичних наслідків опромінення у нього буде таким же, як і в разі
локального опромінення органу (Т) еквівалентною дозою величиною (Н):
Е = Н • WT
За одиницю ефективної дози в системі
СІ теж був прийнятий зіверт (Зв). При рівномірному опроміненні - ефективна доза
дорівнює еквівалентній дозі. При нерівномірному опроміненні - ефективна доза
дорівнює добутку еквівалентної дози на тканинний зважуючий фактор, або дорівнює
такій еквівалентній дозі (при рівномірному опроміненні), яка створює такий же
ризик небажаних наслідків. Виміряти ефективну дозу опромінення організму
неможливо. Її розраховують як суму добутків еквівалентних доз (Н) в окремих
органах і тканинах на відповідні значення зважуючих факторів (WT), що зважують,
вказаних в таблиці 2.Ефективна доза є мірою виходу стохастичних наслідків
біологічної дії малих доз опромінення на даного індивіда, тобто вона є міра
індивідуальної небезпеки, обумовленої дією на організм малих доз іонізуючих
випромінювань.
Для фотонного випромінювання введена
специфічна величина в дозиметрії - експозиційна доза. Чисельно вона дорівнює
абсолютному значенню повного заряду іонів одного знаку, утворених в одиниці
маси повітря при повному гальмуванні електронів і позитронів, звільнених
фотонами (рентгенівським випромінюванням). Тобто, це повітряне еквівалентна
одиниця дози, яка не призначена для дозиметрії в речовині. Одиницею виміру
експозиційної дози в системі СІ є кулон/кг (Кл/кг), позасистемною одиницею є
рентген (Р).1 Р = 2,58 • 10-4 Кл/кг.
Експозиційну дозу можна
використовувати для наближеної оцінки поглиненої і експозиційної доз в речовині
(табл. 4).
Таблиця 4 - Перерахунок доз для
гама-випромінювання (мишці)
|
Величина
|
Система
|
Одиниця
|
Перерахунок в:
|
|
Експозиційна доза
|
СИ
|
Кл/кг
|
Поглинену 1 P ~ 0,0091 Гр ~0,96 рад
|
|
Позасистемна
|
Р
|
Еквівалент
|
2.3.1 Вплив
радіації на організм людини
Вплив радіації на організм людини
може бути різним, але майже завжди він негативний. У малих дозах радіаційне
випромінювання може стати каталізатором процесів, що приводять до раку, чи до
генетичних порушень, а у великих дозах часто приводить до повної чи часткової
загибелі організму внаслідок руйнування кліток тканин. Складність у відстеженні
послідовності процесів, викликаних опроміненням, зумовлена тим, що наслідки
опромінення, особливо при невеликих дозах, можуть проявитися не відразу, і найчастіше
для розвитку хвороби вимагаються роки чи навіть десятиліття. Крім того,
внаслідок різної проникаючої здатності різних видів радіоактивних випромінювань
вони впливають на організм: - частки найбільш небезпечні, однак для -
випромінювання навіть лист паперу є нездоланною перешкодою; - випромінювання
здатне проходити в тканині організму на глибину один-два сантиметра; найбільш
нешкідливе - випромінювання характеризується найбільшою проникаючою здатністю:
його може затримати лише товста плита з матеріалів, що мають високий коефіцієнт
поглинання, наприклад, з бетону чи свинцю. Також розрізняється чутливість
окремих органів до радіоактивного випромінювання. Тому, щоб одержати найбільше
достовірну інформацію про ступінь ризику, необхідно враховувати відповідні
коефіцієнти чутливості тканин при розрахунку еквівалентної дози опромінення:
,03 - кісткова тканина
,03 - щитовидна залоза
,12 - червоний кістковий мозок
,12 - легені
,15 - молочна залоза
,25 яєчники чи насінники
,30 - інші тканини
,00 - організм в цілому.
Імовірність ушкодження тканин
залежить від сумарної дози і від величини отриманої дози, тому що завдяки
репараційним здібностям більшість органів мають можливість відновитися після
серії дрібних доз. Проте, існують дози, при яких летальний результат практично
неминучий. Так, наприклад, дози порядку 100 г приводять до смерті через кілька
днів чи навіть годин внаслідок ушкодження центральної нервової системи, від
крововиливу, в результаті дози опромінення в 10-50 г смерть настає через
один-два тижня, а доза в 3-5 грам грозить обернутися летальним результатом
приблизно половині опромінених. Знання конкретної реакції організму на ті чи
інші дози необхідні для оцінки наслідків дії великих доз опромінення при
аваріях ядерних установок чи пристроїв або небезпеки опромінення при тривалому
перебуванні в районах підвищеного радіаційного випромінювання, як від природних
джерел, так і у випадку радіоактивного забруднення. Однак навіть малі дози
радіації небезпечні і їхній вплив на організм і здоров'я майбутніх поколінь до
кінця не вивчено. Серед найбільш розповсюджених ракових захворювань, викликаних
опроміненням, виділяються лейкози. Оцінка ймовірності летального результату при
лейкозі більш вірогідна, чим аналогічні оцінки для інших видів ракових
захворювань. Це можна пояснити тим, що лейкози першими виявляють себе,
викликаючи смерть у середньому через 10 років після моменту опромінення. За
лейкозами “по популярності” випливають: рак молочної залози, рак щитовидної
залози і рак легень. Менш чуттєві шлунок, печінка, кишечник і інші органи і
тканини. Вплив радіологічного випромінювання різко підсилюється іншими
несприятливими екологічними факторами (явище синергізма). Так, смертність від
радіації в курців помітно вище.
Що стосується генетичних наслідків
радіації, то вони виявляються у виді хромосомних аберацій (у тому числі зміни
числа структури хромосом) і генних мутацій. Генні мутації виявляються відразу в
першому поколінні (домінантні мутації) чи тільки за умови, якщо в обох батьків
мутантним є той самий ген (рецесивні мутації), що є малоймовірним. Вивчення
генетичних наслідків опромінення ще більш утруднено, чим у випадку раку.
Невідомо, які генетичні ушкодження при опроміненні, виявлятися вони можуть
протягом багатьох поколінь, неможливо відрізнити їх від тих, що викликано
іншими причинами. Приходиться оцінювати появу спадкоємних дефектів у людини за
результатами експериментів на тваринах. При оцінці ризику НКДАР використовує
два підходи: при одному визначають безпосередній ефект даної дози, при іншому -
дозу, при якій подвоюється частота появи нащадків з тією чи іншою аномалією в
порівнянні з нормальними радіаційними умовами.Так, при першому підході
встановлено, що доза в 1 г, отримана при низькому радіаційному фоні особами
чоловічої статі (для жінок оцінки менш певні), викликає появу від 1000 до 2000
мутацій, що приводять до серйозних наслідків, і від 30 до 1000 хромосомних
аберацій на кожен мільйон живих немовлят.
При другому підході отримано
наступні результати: хронічне опромінення при потужності дози в 1 г на одне
покоління приведе до появи близько 2000 серйозних генетичних захворювань на
кожен мільйон живих немовлят серед дітей тих, хто піддався такому опроміненню.
Оцінки ці ненадійні, але необхідні. Генетичні наслідки опромінення виражаються
такими кількісними параметрами, як скорочення тривалості життя і періоду
непрацездатності, хоча при цьому визнається, що ці оцінки не більш ніж перша
груба прикидка. Так, хронічне опромінення населення з потужністю дози в 1 г на
покоління скорочує період працездатності на 50000 років, а тривалість життя -
також на 50000 років на кожен мільйон живих немовлят серед дітей першого
опроміненого покоління; при постійному опроміненні багатьох поколінь виходять
на наступні оцінки: відповідно 340000 років і 286000 років.
Існує три шляхи надходження
радіоактивних речовин в організм: при вдиханні повітря, забрудненого
радіоактивними речовинами, через заражену їжу чи воду, через шкіру, а також при
зараженні відкритих ран. Найбільш небезпечний перший шлях, оскільки:
· обсяг легеневої вентиляції дуже
великий
· значення коефіцієнта засвоєння в
легенях більш високі.
Пилові частки, на яких
сконцентровані радіоактивні ізотопи, при вдиханні повітря через верхні дихальні
шляхи частково осідають у порожнині рота і носоглотці. Звідси пил надходить у травний
тракт. Інші частки надходять у легені. Ступінь затримки аерозолів у легенях
залежить від дисперсіонності. У легенях затримується близько 20% усіх часток;
при зменшенні розмірів аерозолів величина затримки збільшується до 70%.
При всмоктуванні радіоактивних
речовин зі шлунково-кишкового тракту має значення коефіцієнт резорбції, що
характеризує частку речовини, що попадає зі шлунково-кишкового тракту в кров. У
залежності від природи ізотопу коефіцієнт змінюється в широких межах: від сотих
часток відсотка (для цирконію, ніобію), до декількох десятків відсотків
(водень, лужноземельні елементи). Резорбція через неушкоджену шкіру в 200-300
разів менше, ніж через шлунково-кишковий тракт, і, як правило, не грає істотної
ролі.
При влученні радіоактивних речовин в
організм будь-яким шляхом вони вже через кілька хвилин виявляються в крові.
Якщо надходження радіоактивних речовин було однократним, то концентрація їх у
крові спочатку зростає до максимуму, а потім протягом 15-20 доби знижується.
Концентрації в крові довго живучих
ізотопів надалі можуть утримуватися практично на одному рівні протягом
тривалого часу внаслідок зворотного вимивання речовин, що відклалися. Кінцевий
ефект опромінення є результатом не тільки первинного ушкодження кліток, але і
наступних процесів відновлення. Передбачається, що значна частина первинних
ушкоджень у клітці виникає у виді так званих потенційних ушкоджень, що можуть
реалізовуватися у випадку відсутності відбудовних процесів. Реалізації цих
процесів сприяють процеси біосинтезу білків і нуклеїнових кислот. Поки
реалізація потенційних ушкоджень не відбулася, клітка може в них
"відновитися". Це, як передбачається, зв'язано з ферментативними
реакціями й обумовлено енергетичним обміном. Вважається, що в основі цього
явища лежить діяльність систем, що у звичайних умовах регулюють інтенсивність
природного мутаційного процесу.
Іонізуючі випромінювання здатні
викликати усі види спадкоємних змін. Спектр мутацій, індукованих опроміненням,
не відрізняється від спектра спонтанних мутацій. Останні дослідження Київського
інституту нейрохірургії показали, що радіація навіть у малих кількостях, при
дозах у десятки берів, найсильнішим чином впливає на нервові клітки - нейрони.
Але нейрони гинуть не від прямого впливу радіації. Як з'ясувалося, у результаті
впливу радіації в більшості ліквідаторів ЧАЕС спостерігається
"післярадіаційна енцефлопатія". Загальні порушення в організмі під
дією радіації приводить до зміни обміну речовин, що спричиняють патологічні
зміни головного мозку.
Радіоактивні речовини характеризуються
іонізуючим випромінюванням, енергії якого достатньо для відділення електронів
від атомів (в результаті чого утворюються заряджені іони) і розриву хімічних
зв'язків. Іонізуюча радіація може зашкодити будь-якому типу тканини людського
організму, причому в більшості випадків пошкодження від іонізуючого
випромінювання не піддаються відновленню. Більше того - будь-яке порушення
природного механізму відновлення організму призводить до утворення ракових
клітин. У загальному випадку ступінь ушкоджень організму залежить від
інтенсивності і тривалості впливу радіації на нього. Наслідки для здоров'я в
результаті радіаційного опромінення прийнято поділяти на дві основні категорії:
стохастичні і не стохастичні.
Стохастичні наслідки опромінення
пов'язані з довгостроковим опроміненням при мінімальному рівні радіації (сама
назва «стохастичний» означає ймовірність чого-небудь). Чим вищий рівень
радіації, тим імовірніші наслідки для здоров'я, проте рівень радіації не
впливає на їх вигляд.
Більшість вважає рак ключовим
наслідком для здоров'я людини внаслідок опромінення. Рак - це неконтрольований
ріст клітин. Зазвичай організм контролює механізм росту та розвитку клітин, а
також відновлення пошкоджених тканин. У результаті пошкоджень на клітинному або
молекулярному рівні цей механізм порушується, приводячи до неконтрольованого
росту клітин. Ось чому здатність радіації розривати хімічні зв'язки в атомах і
молекулах робить її потужним канцерогеном. Крім того, до групи стохастичних,
або випадкових наслідків опромінення входять зміни в ДНК, викликані радіацією -
так звані клітинні мутації. У деяких випадках організм не справляється із
завданням відновлення таких утворень, що призводить до появи нових мутацій.
Мутації можуть бути тератогенними або генетичними. Тератогенні мутації
викликані опроміненням плоду і впливають тільки на людей, що постраждали від
опромінення. Генетичні ж мутації передаються наступним поколінням.
Не стохастичні наслідки для здоров'я
людини пов'язані з опроміненням високої інтенсивності - чим інтенсивніший вплив
радіації на організм людини, тим серйозніші наслідки для здоров'я.
Короткострокове інтенсивне опромінення називають гострим опроміненням. На
відміну від раку, наслідки короткострокового опромінення зазвичай виникають
досить швидко. У числі найбільш поширених наслідків гострого опромінення -
опіки і так звана променева хвороба, або радіаційне ураження, що викликає
передчасне старіння і часто призводить до летального результату. При
опроміненні дозами значної потужності летальний результат наступає протягом
двох місяців. У число основних симптомів променевої хвороби входять нудота,
слабкість, втрата волосся, опіки шкіри, порушення роботи різних органів. Від
деяких наслідків для здоров'я, що зазвичай спостерігаються при гострому
опроміненні, страждають і пацієнти, що проходять курс радіотерапії.
2.3.2 Вплив
радіонуклідів на популяції рослин
Таким чином, можна обґрунтовано
вважати, що поверхнева активність Радіонуклідів території приблизно до рівня
3,7 • 103 Бк/км2 (103 Кі/км2) ніяк не впливатиме на проживання на ній
мікроорганізмів і рослинність. Це нижня межа радіорезистентності цих
організмів. Насправді їхня Радіорезистентність є ще вищою. По-перше, ефект
хронічного опромінення набагато менший, ніж гострого (а наведений вище матеріал
стосується в основному гострого опромінення). По-друге, при використанні даних
про радіонуклідне забруднення ми враховували лише і зовнішнє опромінення від
радіонуклідів, внесених у ґрунт чи воду, а не і додаткове внутрішнє опромінення
за рахунок інкорпорованих радіо-1 нуклідів. Як відомо, коефіцієнти переходу і
накопичення можуть бути! дуже значними, і дози, отримані рослинами внаслідок
дії радіонуклідів, І мають бути істотно більшими, ніж було враховано нами під
час розгляду впливу радіонуклідів на рослини (як і на тварин, що живуть на і
забруднених ними територіях).
Фактично людину
цікавить не стільки характер змін у стані здоров'я окремих представників біоти,
що живуть на забруднених територіях, скільки те, яку шкоду може заподіяти таке
забруднення популяціям І цих організмів, тобто як уплине їх опромінення на
здатність давати повноцінне и потомство. Таких даних уже накопичено досить, щоб
вважати, І що популяції мікроорганізмів і вищих рослин значно стійкіші
(особливо хронічного), ніж їх окремі особини. З огляду на такий § популяційний
аспект радіоекологічних досліджень можна цілком обґрунтованим вважати рівень
потужності поглиненої дози випромінювання 10 Гр/рік чи поверхневої активності
радіонуклідів 3,7 • 1013 Бк/км2 (103 Кі/км2) як нижню межу біологічно нешкідливого
опромінення не тільки мікроорганізмів, а й рослин. Інакше кажучи, при дозах, що
не перевищують наведених значень, ніяких несприятливих наслідків для І рослин
очікувати не слід. Незалежно від такого опромінення рослини І і мікроорганізми
будуть нормально виконувати свої трофічні функції, мати таку саму
продуктивність і кондицію вальну здатність, як і без І опромінення, і, отже,
відігравати ту саму роль концентраторів і радіонуклідів у міцно зв'язані з
детритом форми захворювання.
Нагадаємо, що таке
кондиціювання навколишнього середовища від радіонуклідів, які потрапили до
нього, більш ніж на 99 % виконують саме вищі рослини і мікроорганізми, і тільки
близько 1 % припадає нш| тварин.
.3.2.1
Генетичні наслідки опромінення рослин
Генетичні наслідки
опромінення мікроорганізмів не було описано у відповідному підрозділі, тому що
вони у загальному розумінні мають І універсальний характер для всієї біоти і їх
зручніше розглянути в розділі, і присвяченому вищим рослинам, для яких ці
наслідки різноманітніші.
Щодо генетичних
наслідків опромінення, то маються на увазі головним чином мутації генів, адже
досить значні мутації хромосом, як правило, летальні для клітин, і
закономірності їх виникнення внаслідок опромінення такі самі, як і
закономірності його летальної дії.
Проте не можна
вважати мутації генів однотипними. Крім уже зазначеної вище різноманітності
їхньої структурної основи - від точкових мутацій, зумовлених ураженням малої
кількості основ, до структурних, які захоплюють багато тисяч основ, потрібно
враховувати, що подібні фенотипічні наслідки можуть мати зміни генів унаслідок
внутрішніх рекомбінацій; частота ж рекомбінацій може у 10 - 30 разів
перевищувати частоту справжніх мутацій генів. Таким чином, під генетичними
наслідками опромінення розуміють інтегральний підсумок, що виявляється в зміні
потомства опромінених особин незалежно від того, зумовлене це мутацією генів
(точковою чи структурною) чи хромосом.
Розглянемо два
аспекти мутагенної дії випромінювання: залежність її від потужності дози і ЛПЕ
випромінювання, а також від рівнів інтегральної поглиненої дози випромінювання.
На підставі різних даних, отриманих як на мікроорганізмах, так і на вищих
рослинах, встановлено, що мутагенний ефект опромінення, віднесений до одиниці
поглиненої дози випромінювання (наприклад, частота мутацій на 1 Гр), зі
збільшенням потужності поглиненої дози спочатку дещо зменшується, а потім
починає зростати. Механізм такої закономірності й локалізація «точки перегину»
на осі потужності дози остаточно не з'ясовані. З цього приводу існує лише одна
гіпотеза, що пов'язує характер змін мутагенного ефекту опромінення з індукцією
в об'єктах системи відновлення (SOS-системи), які зазнали опромінення, і
зумовленим із цим відновленням клітин від передмутаційиих змін ДНК.
У такий самий
спосіб, тобто на підставі загальних понять, зазвичай пояснюють емпірично
встановлений факт збільшення генетичного ефекту опромінення зі збільшенням ЛПЕ
випромінювання. Проте, як уже зазначалось, механізм цього феномену ще не
з'ясовано.
Щодо кількісної
залежності частоти індукції мутацій від поглиненої Дози випромінювання є дані в
основному для одноразового гострого опромінення в досить великих дозах - 1 Гр
(100 рад) і більше. У разі хронічного впливу також звичайно експериментують із
поглиненими Дозами 1 Гр (100 рад) і більше на покоління, тому що зменшення дози
нижче цього рівня зумовлює необхідність настільки збільшувати обсяг вибірки
(для отримання вірогідних даних), що це робить неможливим Дослідження.
Можна вважати, за
потужності поглиненої дози 0,1 - 1 Гр/рік у разі хронічного опромінювання
рівень реєстрованих генетичних змін статистично не відрізнятиметься від
контролю. Це твердження стосується 1 мікроорганізмів, і вищих рослин, і,
очевидно, переважної більшості Тварин.
Тому таку
потужність поглиненої дози у разі хронічного опромінювання 0,1 - 1 Гр/рік
можна, мабуть, вважати щодо генетичних наслідків безпечною для будь-яких
представників біоти. Непрямим підтвердженням цього є те, що у випадку
виникнення при такому опроміненні і з низькою частотою мутантних особин
(додатково до спонтанного фону) вони, як правило, будуть швидко елімінуватися з
популяції внаслідок добору, адже давно відомо, що переважна більшість
спонтанних та індукованих мутантів відрізняються від особин дикого типу (що і
виділені з природних умов без добору) дещо зниженою життєздатністю. Мутанти із
підвищеною життєздатністю, що піддаються добору, будуть залучатися до участі в
житті популяції, не завдаючи їй ніякої шкоди.
2.3.3 Вплив
іонізуючого опромінення на тварин - мутації під впливом радіації
Іонізуюче випромінення - невидимі
оком випромінення високої енергії, що уявляють з себе потоки елементарних
часток ( електронів , позитронів , мезонів , протонів та нейтронів ) , а також
більш важких багатозарядних іонів ( альфа-частки , ядра більш важких елементів
, або мають електромагнітну природу ( гамма- та рентгенівські промені ). Всіх
їх об’єднує схожість фізичних властивостей та , перш за все - аналогічний
характер взаємодії з речовиною. Так , наприклад , кванти гамма та
рентгенівських променів при зустрічі з атомами речовини віддають їм частку
своєї енергії , при цьому електрино нейтральний атом речовини перестає існувати
перетворюючись у пару протилежно заряджених іонів . Частка або квант високої
енергії вибиває один з електронів , що уносить з собою з атома один від ємний
заряд , тому атом стає позитивно зарядженим , а електрон приєднується до
сусіднього атому утворюючи від’ємний іон. Інша назва «проникаюча» радіація
свідчить про здатність проникати в глибину речовини. Окрім гамма - та рентгенівських
променів іонізуючими властивостями володіють ультрафіолетові промені , в
особливості короткохвильові
Біологічний ефект випромінення
високих енергій може бути дуже значним при загальному несуттєвому рівні
переносу енергії . Так , наприклад летальна доза гамм - чи рентгенівських
променів для людини, якщо її перетворити на теплову енергію не вистачить навіть
на те , щоб вскіпятити стакан води для чаю . У той же час тварини можуть
переносити куди більший рівень інфра-червоного випромінення , це пояснюється
тим , що іонізуюче опромінення викликає якісно інші зміни у організмі.
Справа в тому, що ті іони що
утворюються мають дуже велику хімічну активність, та можуть породити ланцюг
подій, кінцевими стадіями якого може бути променева хвороба, мутації та пухлини.
Іонізуюче опромінення надходить до
до нас з усіх боків : вони надходять до нас з всесвітнього простору ( так звані
«космічні промені» ) постійно з однаковою інтенсивністю вже мільйони років .
вони випромінюються природно радіоактивним елементами , що входять у склад
земної кори , а звідти у вигляді пилу попадають у повітря , або вимиваються
водою у гідросферу. Взагалі будь-яке небесне тіло більш-менш «пристойних»
розмірів має в своєму складі радіоактивний елемент , звичайно і в живих істотах
існують радіоактивні елементи.
Можна дійти висновку , що а ні на
Землі , а ні у всесвіті немає місць вільних від іонізуючої радіації . Можна
сказати , що поверхня Землі , а також водойми та шар повітря , тобто вся
біосфера постійно знаходиться під впливом іонізуючого.
Таким чином світ в якому ми живемо є
радіоактивним , але це не є реалією тільки сьогодення , так було на Землі
завжди з моменту утворення Сонячної системи . Відповідно даним життя зародилося
на Землі 3.5 млрд. років тому . Процес еволюції , розвитку та формування
екосистем проходив на тлі постійного.
Звичайно , що за такий час не
обійшлося без впливу опромінення на життя. З одного боку, кванти та частки
іонізуючого опромінення природного фону мають велику енергію , так що при
взаємодії з речовиною біологічної системи , особливо з хромосомами клітинного
ядра викликає розрив зв’язків між атомами та їх перегрупування. Більшість з цих
порушень потім самоліквідується , однак деяка частина не встигає відновитися до
моменту дуплікації молекули ДНК , тоді передаються-клітинам-нащадкам.
Для організму загибель однієї
клітини суттєвого значення не відіграє , тому що клітини, що вижили в процесі
розмноження заповнюють цей дефект. Те ж саме можна сказати і про окремі
одноклітинні,популяції.
Якщо ж клітина не помирає , то вона
може набути нових властивостей , котрих раніш не було , або навпаки загублює
раніш властиві властивості . Так, наприклад , на 1 мільйон клітин одна є
мутантною внаслідок природного радіаційного фону.
При отриманні чи втраті ознаки
організм може або отримати пріоритет, або навпаки стати аутсайдером або не
отримати ні того не іншого у своїй боротьбі за виживання та продовження роду .
Якщо признак корисний - організм залишає більше нащадків , якщо навпаки -
залишає менше чи не залишає взагалі . Таким чином нова корисна мутація через
деякий час стає набуттям всього роду , або його нової гілки шкідлива, мутація
зникає.
І так іонізоване опромінення це
природний мутагенний агент , якій має важливе місце у постачанні мутацій у
природу , які є «сировиною» для природного відбору . Тобто природній
радіоактивний фон використовується життям в своїх інтересах , в якості
постійних мутагенних чинників , до яких життя адоптувалося і має досить
непогане процентне співвідношення корисних мутацій . Якщо ж іонізоване опромінення
буде вище норми то мутації будуть про індуковані , але клітини при цьому будуть
мати майже одні «негативні» мутації
Зрозуміле, що кількість шкідливих
мутацій набагато більша ніж корисних, тому кожний шаг вперед супроводжується
загибеллю великої кількості менш пристосованих особин. Причому при руху від
менш складних організмів до більш складних відсоток шкідливих мутацій
збільшується , в цьому немає нічого дивного, бо чим складніша система , тим
простіше її зламати та тим складній удосконалити. У високоорганізованої тварини
, в тому числі у людини, позитивні мутації - дуже рідкісний випадок . Більша
частина мутацій шкідливі , або нейтральні , багато з них стають причиною
спадкових хвороб. Звичайно, що іонізуюча радіація теж вносить вклад в цей процес.
Друга важлива риса , на якій би я
хотів наголосити це необхідність захисту від через мірної мутагенної небезпеки.
Тому живі організми виробили спеціальний механізм , який з одного боку зберігає
набуту мутацію , а з іншого зводить до мінімуму вірогідність утворення нових
мутацій . це система репарації ДНК. Всі інші органели та компоненти клітини не
мають таких систем , бо не відіграють такого суттєвого значення. На мою думку
саме іонізуюче опромінення примусило створити цю систему , бо під час
зародження життя на Землі природний фон був вище. І , нарешті , третя риса .
Якщо доза опромінення на стільки сильна , що репаративні ферменти не можуть
своєчасно «відремонтувати» ДНК , то може виникнути стійка мутація , що може
призвести до утворення пухлини в організмі. Саме тому була створена ще одна
система захисту - імунну систему , що не тільки захищає організм від бактерій,
хвороб них грибків та вірусів , а й відшукують у організмі трансформовані
клітини з хибною інформацією та вбивають їх.
Одже іонізуюче випромінення має
такий вплив : стимулювання мутацій організмів , в результаті чого постачається
новий матеріал для еволюції. пряма дія на організм , в результаті якої може
виникнути пухлина.
2.4
Системні радіобіологічні ефекти
.4.1
Індукована опроміненням генетична нестабільність
Під впливом
опромінення спостерігається зростання генетичної нестабільності, під якою
розуміють стійкі, тривалі, поширені на багато поколінь порушення функціонування
генетичних керуючих систем клітин. Прояви генетичної нестабільності, як
правило, мають характер системної відповіді на опромінення. Генетична
нестабільність тенденції до підвищення мінливості спадкових ознак зумовлена
структурно-функціональною непостійністю геному - сукупності ядерних елементів
генетичної конституції особини.
Індукована
опроміненням генетична нестабільність клітин проявляється в багатьох
порушеннях, зокрема, в зростанні частоти генних мутацій, хромосомних аберацій,
ампліфікації генів, збільшенні клонової гетерогенності, частоти трансформації
клітин. Зростає також частота реалізації віддалених наслідків опромінення у
формі проліферативної загибелі клітин, яка спостерігається в наступних
поколіннях опромінених клітин. Може також істотно відхилятися від норми
експресія окремих генів. Клони, одержані з однієї родоначальної клітини, під
впливом опромінення демонструють дестабілізацію хромосом, яка проявляється в
багатьох клітинних поколіннях.
Генетична
нестабільність проявляється в зростанні темпів генетичних змін. У клітинній
лінії, яка виникла з однієї опроміненої клітини, протягом багатьох поколінь
можуть спостерігатися цитоге-нетичні зміни. Наступні покоління клітин, що
ушкоджені іонізуючим випромінюванням, але зберегли здатність до поділу,
виявляють схильність до формування нових хромосомних аберацій або точкових
мутацій.
Мішень, що
відповідає за індукцію генетичної нестабільності, має порівняно великі розміри:
вона складається з багатьох структурних і регуляторних генів, у генотипічному
прояві яких і виражається генетична нестабільність. Увічнення цитогенетичної
мінливості, зумовленої генетичною нестабільністю, пояснюють хромосомною
рекомбінацією, нестабільністю сателітів, циклом утворення мостів - розривів і
злиттям у дицентриках, що свідчить про хромосомну дестабілізацію.
Генетична
нестабільність, індукована дією іонізуючої радіації, характеризується локусною
специфічністю, тобто зумовлене опроміненням збільшення ймовірності виникнення
мутації в різних локусах неоднакове. Зазначимо, що спонтанна мутабільність
окремих генів також неоднакова. Трапляються гени як дуже стабільні, так і
лабільні, й, крім того, є багато проміжних за мутабільністю форм.
Припускають, що
геномна нестабільність зумовлюється змінами в повторюваних послідовностях ДНК,
а також у теломерних ділянках хромосом, у генах, що контролюють репарацію,
транскрипцію, реплікацію ДНК і рекомбінаційні процеси з хромосомах.
Гіперваріабельні
ділянки ДНК, або мінісателіти, характеризуються виразним популяційним
поліморфізмом, який підтримується високими частотами мутацій, що виникають в
їхніх межах.
Геномна нестабільність
проявляється навіть за опромінення в незначних дозах, про що свідчать
результати вивчення медико-біологічних наслідків проживання на забруднених
радіацією територіях.
Опромінення
альфа-частинками в однотрековій дозі набагато ефективніше щодо генетичної
нестабільності, ніж опромінення гамма - або рентгенівським випромінюванням.
Генетична
нестабільність, індукована опроміненням, причетна до канцерогенезу. Відомі
гени, мутації яких істотно впливають на частоту трансформацій клітин.
Індукована опроміненням
геномна нестабільність проявляється в тому, що в клітинній лінії, яка виникла з
опроміненої клітини, зростає частота мутацій після багатьох поділів, а геномна
нестабільність стовбурних клітин зберігається після їх трансплантації в
неопромінений організм.
Відтермінована
хромосомна нестабільність. Деякі клітини, що зазнали опромінення, протягом
тривалого часу зберігають стан латентної хромосомної нестабільності: в
потомстві клітини після низки поділів виникають хромосомні аберації. Хромосомну
нестабільність виявлено в лімфоцитів, фібробластів, стовбурних клітин системи
кровотворення. Проте деякі з клонів клітин не схильні до хромосомної
нестабільності. Це є однією з причин геномної нестабільності, яка зумовлює
пізню проліферативну загибель клітини, появу мутантних форм. Хромосомна
нестабільність причетна до радіаційної індукції пухлин, коли цей процес має
досить тривалий латентнийперіод.
Вважають, що
хромосомна нестабільність спричиняється скороченням природної кінцевої частини
хромосоми (теломери). Зростання частоти хромосомних аберацій унаслідок старіння
клітинного клону також пов'язане зі скороченням теломери.
Крім того, як
причину розглядають мутаційні зміни генів, що контролюють проходження клітиною
мітотичного циклу, забезпечуючи зупинку у відповідних його пунктах, й через це
клітини швидше досягають старіння, для якого характерна хромосомна
нестабільність. Не виключено також, що хромосомна нестабільність може
зумовлюватися не ушкодженням мішені, а індукцією помилкової репарації або
епігенетичною зміною ензиматичного контролю стабільності геному невої патології
органів, які не зазнали прямої дії радіації. Це дає підстави вважати, що є
дистанційні ефекти опромінення, які реалізуються опосередковано передаванням
певних хімічних факторів з опромінених органів у неопромінені. Особливо
показовими щодо цього є досліди з парабіонтами - тваринами, штучно з'єднаними
через кровоносні системи або зрощуванням тканин. Якщо опромінювати одну з цих
тварин, то ознаки променевого ураження проявляються не лише в неї,неопроміненого
парабіонта.
Передавання агента
хімічної природи, який спричиняє ефекти радіаційного ураження, від
безпосередньо опромінених органів до неопромінених відбувається й у межах
одного організму.
Речовини, що
індукують процеси, подібні до променевого ураження, є радіоміметиками. Отже, з
опромінених органів або тканин транспортуються речовини радіоміметичної дії,
які названо радіо -токсинами.
Утворюючися в
опромінених тканинах, радіотоксини переносяться з міжклітинною рідиною - лімфою
- до неопромінених частин організму, де й проявляється їхня дія. Можливими
носіями токсичних властивостей міжклітинної рідини в опромінених тварин є
продукти розпаду білків, низка похідних фенолів та деякі інші речовини. їх
поява зумовлена порушенням метаболізму під час опромінення.
Кров тварин, які
зазнали дії іонізуючого випромінювання, має радіотоксині властивості. Під
впливом такої крові істотно зменшується активність відповідної АТФ-ази
плазматичних мембран тимоцитів.
Соматичний і
мультигенеративний канцерогенез. Серед віддалених наслідків опромінення
особливо небезпечним явищем є радіаційний канцерогенез. Розрізняють соматичний
і мультигенеративний канцерогенез.
У разі соматичного
канцерогенезу трансформується соматична клітина, яка в клоні клітин, що
розмножуються мітотичним поділом, зазнала кількох мутаційних змін. Пухлини
виникають в опроміненому організмі.
Мультигенеративний
канцерогенез полягає в тому, що в кількох поколіннях у нащадків батьків,
опромінених ще до зачаття першого покоління, виникають специфічні й неспецифічні
пухлини. Вважають, що цей ефект ґрунтується на трансзиготному передаванні
специфічних мутацій, з якими пов'язаний багатостадійний канцерогенез. Ці
мутації визначають спадкову схильність клітин до трансформації. Мутантним
клітинам властива підвищена чутливість до дії мутагенних факторів.
Мутації, що
зумовлюють мультигенеративний канцерогенез, мають особливу природу: вони не
належать ні до точкових мутацій, ні до великих хромосомних перебудов. Для
прояву ефекту не потрібна гомозиготність клітин за генами, які зазнали
мутаційних змін.
В розвитку
променевого ураження організму водночас з ушкодженням окремих органів і тканин,
що зазнали безпосереднього опромінення, виявляються ознаки невої патології
органів, які не зазнали прямої дії радіації. Це дає підстави вважати, що є
дистанційні ефекти опромінення, які реалізуються опосередковано передаванням
певних хімічних факторів з опромінених органів у неопромінені. Особливо
показовими щодо цього є досліди з парабіонтами - тваринами, штучно з'єднаними
через кровоносні системи або зрощуванням тканин. Якщо опромінювати одну з цих
тварин, то ознаки променевого ураження проявляються не лише в неї, а й у
неопроміненого парабіонта.
Передавання агента
хімічної природи, який спричиняє ефекти радіаційного ураження, від
безпосередньо опромінених органів до неопромінених відбувається й у межах
одного організму.
Речовини, що
індукують процеси, подібні до променевого ураження, є радіоміметиками. Отже, з
опромінених органів або тканин транспортуються речовини радіоміметичної дії,
які названо радіо -токсинами.
Утворюючися в
опромінених тканинах, радіотоксини переносяться з міжклітинною рідиною - лімфою
- до неопромінених частин організму, де й проявляється їхня дія. Можливими
носіями токсичних властивостей міжклітинної рідини в опромінених тварин є
продукти розпаду білків, низка похідних фенолів та деякі інші речовини. їх
поява зумовлена порушенням метаболізму під час опромінення.
Кров тварин, які
зазнали дії іонізуючого випромінювання, має радіотоксині властивості. Під впливом
такої крові істотно зменшується активність відповідної АТФ-ази плазматичних
мембран тимоцитів.
Соматичний і
мультигенеративний канцерогенез. Серед віддалених наслідків опромінення
особливо небезпечним явищем є радіаційний канцерогенез. Розрізняють соматичний
і мультигенеративний канцерогенез.
У разі соматичного
канцерогенезу трансформується соматична клітина, яка в клоні клітин, що
розмножуються мітотичним поділом, зазнала кількох мутаційних змін. Пухлини
виникають в опроміненому організмі.
Мультигенеративний
канцерогенез полягає в тому, що в кількох поколіннях у нащадків батьків,
опромінених ще до зачаття першого покоління, виникають специфічні й
неспецифічні пухлини. Вважають, що цей ефект ґрунтується на трансзиготному
передаванні специфічних мутацій, з якими пов'язаний багатостадійний
канцерогенез. Ці мутації визначають спадкову схильність клітин до
трансформації. Мутантним клітинам властива підвищена чутливість до дії
мутагенних факторів.
Мутації, що
зумовлюють мультигенеративний канцерогенез, мають особливу природу: вони не
належать ні до точкових мутацій, ні до великих хромосомних перебудов. Для
прояву ефекту не потрібна гомозиготність клітин за генами, які зазнали
мутаційних змін.
2.4.2
Радіоадаптація
Радіоадаптація
полягає в підвищенні радіостійкості організму після його опромінення в малій
дозі. Вперше це явище було виявлено на лімфоцитах людини й дістало назву
феномена адаптивної відповіді лімфоцитів людини на дію іонізуючої радіації.
Феномен адаптивної радіорезистентності виявлено в бактерій, лімфоцитів (у
культурі) людини, кролика, клітин кісткового мозку in vivo й in vitro,
сперматозоїдів, клітин китайського хом'ячка, фібробластів, диплоїдних і
гаплоїдних дріжджів, у рослин та деяких інших біологічних об'єктів.
Найчастіше про
адаптивну відповідь судять за виходом хромосомних аберацій або за утворенням
мікроядер. Проте й за іншими Критеріями радіаційного ураження чітко виявляється
адаптивна відповідь організму на попереднє опромінення в малій дозі.
Прояв
радіоадаптації властивий біологічним системам різного рівня: від клітин до
цілісних організмів вищих тварин. Наприклад, унаслідок опромінення щурів у дозі
5 сГр їхня радіостійкість збільшується, що виявлялося через місяць після
передавання малої дози в дослідах із гострим опроміненням у високих дозах.
Малу дозу називають
адаптувальною, високу - тестувальною. Змінюючи інтервал часу At між
опроміненнями в цих дозах, визначають час, протягом якого формується підвищена
радіостійкість (адаптивна відповідь, або радіоадаптаційний синдром), а також
час, протягом якого зберігається індукована радіостійкість. Інтенсивність
радіоадаптаційного синдрому оцінюють фактором підвищення дози (ФПД) -
коефіцієнтом, чисельне значення якого показує, в скільки разів слід збільшити
дозу після розвитку радіоадаптації, щоб ефект був такий самий, як у разі
опромінення біологічного об'єкта, котрий не зазнав впливу адпатувальної дози.
Радіоадаптація
проявляється в підвищенні радіостійкості, яку оцінюють за різними критеріями -
виживаністю організмів або клітин, виходом хромосомних аберацій, частотою
виникнення точкових мутацій, утворення мікроядер, здатністю до утворення
колоній клітин у культурі, клоногенною здатністю клітин, інтенсивністю
репарації ДНК від одно - або двониткових розривів. Наприклад, адаптивну
відповідь стовбурних клітин кісткового мозку оцінюють за утворенням
макроколоній у селезінці.
ВИСНОВКИ
НРБУ-97 є основним державним
документом, що встановлює систему радіаційно-гігієнічних регламентів для
забезпечення прийнятих рівнів опромінення як для окремої людини, так і для
суспільства взагалі і є обов'язковими для виконання всіма юридичними та
фізичними особами, які проводять практичну діяльність з джерелами іонізуючого
випромінювання.
НРБУ-97 поширюються на ситуації
опромінення людини джерелами іонізуючого випромінювання в умовах:
нормальної експлуатації
індустріальних джерел іонізуючого випромінювання;
медичної практики;
радіаційних аварій;
опромінення техногенно-підсиленими
джерелами природного походження.
Відповідальність за виконання
НРБУ-97 покладається на:
фізичні та юридичні особи, незалежно
від форм власності та підпорядкованості які виробляють, переробляють,
застосовують,зберігають, транспортують, здійснюють поховання, знищення чи
утилізацію джерел іонізуючого випромінювання, а також проектують роботи з ними;
керівників та посадових осіб органів
Державної виконавчої влади і організацій, які планують та реалізують
контрзаходи в частині Норм, що стосується обмеження опромінення при радіаційних
аваріях та опромінення від техногенно-підсилених джерел природного походження.
Особи, які допустили протиправні дії
з джерелами іонізуючих випромінювань, чи не планують або не реалізують
контрзаходи по зменшенню рівнів опромінення до регламентованихНРБУ-97 величин,
притягуються до відповідальності відповідно до чинного законодавства України.
2-5 З моменту офіційного опублікування Норм радіаційної безпеки України, дія
НРБ-76/87 відміняється.
Першопричиною радіаційних ефектів є
поглинання енергії випромінювання опромінюваним об'єктом, і доза, як міра
поглиненої енергії, є основною дозиметричною величиною. Тому, основною фізичною
дозиметричною величиною, що використовується для оцінки міри дії випромінювання
на середовище, є поглинена доза випромінювання. Поглинена доза випромінювання
(D) - це величина що визначається енергією випромінювання (Дж) поглинаємо
одиницею маси (кг) опромінюваної речовини. За одиницю дози в системі СІ
прийнятий грей (Гр): D = 1Дж/1кг=1 Гр.Грей це така доза іонізуючого
випромінювання, при якій ділянці речовини масою 1 кг передається енергія 1 Дж.
Позасистемною одиницею є "рад". 1 рад = 0,01 Гр.
ПЕРЕЛІК ПОСИЛАНЬ
1. В.М. Лапін. Безпека
життєдіяльності людини. - Київ - Львів, 2009 р.
. Допризовна підготовка (за ред. М.
І. Томчука). - Киів, 2011 р.
. Авсеєнко В.Ф. Дозиметричні и
радиометричні прилади та вимірювання. Київ, 2010 р.
. Г.О. Біляшевський, Р.С. Фурдуй.
Основи екологічних знань. - Київ, 2007 р.
. Закон України «Про статус та
соціальний захист громадян, які постраждали внаслідок Чорнобильської
катастрофи».