Химические реагенты для очистки природного газа от сероводорода и других сернистых соединений
ФЕДЕРАЛЬНОЕ
АГЕНСТВО ПО ОБРАЗОВАНИЮ РОССИЙСКОЙ ФЕДЕРАЦИИ
РОССИЙСКИЙ
ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ НЕФТИ И ГАЗА ИМЕНИ И.М. ГУБКИНА
ФАКУЛЬТЕТ
ХИМИЧЕСКОЙ ТЕХНОЛОГИИ И ЭКОЛОГИИ
Кафедра
технологии химических веществ для нефтяной и газовой промышленности
Реферат на
тему:
"Химические
реагенты для очистки природного газа от сероводорода и других сернистых
соединений"
Выполнила:
ст.гр. ХТМ-13-01
Балтаева М.Б.
Проверила:
доц. Смирнова Т.С.
Москва 2014
Оглавление
Введение
. Характеристика сернистых примесей
. Классификация способов очистки от примесей
сероводорода и других сернистых соединений
. Абсорбционные методы очистки
.1 Сорбционные методы очистки газов от сероводорода
растворами алканоламинов
.1.1 Технология аминовой очистки
.1.2 Влияние параметров на процесс аминовой очистки
.1.3 Пенообразование в аминовых растворах и борьба с ним
.2 Процессы очистки растворами солей щелочных металлов
.3 Основы технологии очистки газа физическими
абсорбентами
.4 Абсорбция комбинированными поглотителями
4. Адсорбционные методы очистки
.1 Физическая адсорбция
.2 Химическая адсорбция
5. Окислительные методы
Заключение
Список литературы
Введение
сернистый очистка сорбционный окислительный
Многие природные газы в своем составе содержат сернистые компоненты и
диоксид углерода. Среди сернистых компонентов чаще всего встречаются
сероводород, меркаптаны, серооксид углерода, сероуглерод и сульфиды. В
настоящее время добыча сероводородсодержащего природного газа в странах СНГ
составляет около 10 % всего объема потребляемого газа [14], при этом содержание
сероводорода в газах колеблется в широких пределах - от нескольких долей до
нескольких десятков процентов (26% - на Астраханском газоконденсатном
месторождении). За рубежом эксплуатируются месторождения и с более высокой концентрацией
сероводорода в газе - до 87-98 % (Канада).
Сернистые соединения отравляют катализаторы в процессах переработки газа,
при сгорании образуют оксиды серы, содержание которых в воздушном бассейне
опасно для человека и окружающей среды, вызывает коррозию газопроводов и
аппаратуры, весьма ядовиты для человека и животных. Поэтому в газе, подаваемом
потребителям, должно содержаться сероводорода не более 5,7 мг/м3
газа и общей серы - не более 50 мг/м3 газа.
В настоящее время разработаны и эксплуатируются в промышленности
различные методы очистки природного газа от сернистых соединений, в связи с чем
целью данной работы является рассмотрение и анализ данных методов.
Выбор процесса очистки газа от сернистых соединений определяется
экономикой и зависит от многих факторов, основными из которых являются: состав
и параметры сырьевого газа, требуемая степень очистки и область использования
товарного газа, наличие и параметры энергоресурсов, отходы производства и др.
. Характеристика сернистых примесей
Сероводоро́д (серни́стый водоро́д, сульфид водорода, дигидросульфид)
- бесцветный газ с запахом протухших яиц и сладковатым вкусом. Химическая
формула - H2S.
Запах сероводорода ощутим даже при незначительных концентрациях 1:100000.
Плотность сероводорода по отношению к воздуху составляет 1,1912. Сероводород
хорошо растворяется в воде и легко переходит из растворённого состояния в
свободное.
Сероводород - сильный восстановитель. На воздухе постепенно окисляется,
при ~ 250 °С воспламеняется. Горит, при избытке кислорода образует диоксид серы
и воду, при недостатке - серу и воду (промышленный способ получения серы).
Сероводород легко окисляется в водном растворе кислородом, галогенами. Сильные
окислители (HNO3, Cl2) окисляют сероводород до серной
кислоты.
Сероводород применяют в основном для производства серы и серной кислоты.
Его используют также для получения различных сульфидов (в частности, сульфидов
и гидросульфидов натрия, аммония), сераорганических соединений (тиофены, тиолы
и т. п.), тяжелой воды, для приготовления лечебных сероводородных ванн, в
аналитической химии для осаждения сульфидов металлов.
Сероводород оказывает вредное воздействие на процессы химической
переработки углеводородов: отравляет катализаторы, резко снижая срок действия
или выводя их из строя. Сероводород - сильно коррозионно-активное вещество. Он
разъедает технологическое оборудование, трубопроводы и арматуру. Техническими
условиями на углеводородное сырьё для нефтехимического производства содержание
сернистых соединений, в том числе сероводорода, также строго ограничивается,
оно должно быть в пределах 0,002-0,005 мас.%..
Сероводород очень токсичен, имеет 2-ой класс опасности. Является сильным
нервным ядом, вызывающим смерть от остановки дыхания. Сероводород действует
раздражающе на дыхательные пути и глаза. ПДК в воздухе рабочей зоны 10 мг/м3, в атмосферном воздухе 0,008 мг/м3. При высокой концентрации
однократное вдыхание может вызвать мгновенную смерть. Главное токсикологическое
свойство сероводорода заключается в общем воздействии на организм - центральную
нервную систему, окислительные процессы и кровь. Сероводород отравляет
окружающую среду.
Токсичность сероводорода возрастает в составе нефтяных газов (ПДКрз - 10 мг/м3, в смеси углеводородами (С1-С5)
- 3 мг/м3, что соответствует
1-му классу опасности). Известно большое число тяжелых и молниеносных
отравлений этими газовыми смесями.
Тиолы (меркаптаны, тиоспирты) - сернистые аналоги спиртов общей формулы
R-SH, где R - углеводородный радикал, например, метантиол (метилмеркаптан) (CH3SH), этантиол (этилмеркаптан) (C2H5SH) и т. д. В терминологии IUPAC название
"меркаптаны" признано устаревшим и не рекомендуется к использованию.
Тиолы, являющиеся ловушками для радикалов, используют для защиты от
радиации и как антиокислители, например додекантиол - стабилизирующая добавка
для каучуков. Меркаптаны и их производные (соли, сульфиды, дисульфиды)
используют как ускорители вулканизации натурального и синтетического каучуков
(например, 2-меркаптобензтиазол-каптакс), как ускорители пластикации каучуков,
в синтезе некоторых лекарственных препаратов.
Метилмеркаптан и этилмеркаптан - органические серосодеражащие газы,
обладающие высокой токсичностью и наркотическим действием. Меркаптаны - сильные
яды нервно-паралитического действия, они вызывают паралич мышечной ткани, при
низких концентрациях провоцируют тошноту, головную боль. ПДКрз для метилмеркаптана - 0,8 мг/м3, для этилмеркаптана - 1,0 мг/м3.
Тиолы в очень низкой концентрации вводят в природный гaз для того, чтобы
по их запаху можно было определить утечки газа в помещении.
Тиофен (C4H4S) - гетероциклическое соединение,
ароматический пятичленный гетероцикл, содержащий один атом серы в цикле.
Бесцветная жидкость, температура плавления -38,3 °С, кипения - 84,1 °С. Хорошо
растворим в органических средах, и плохо растворим в воде. По физическим и
химическим свойствам сходен с бензолом.
Сероуглерод (CS) - бесцветная жидкость с запахом эфира. На свету
разлагается с образованием продуктов, обладающих запахом гнилых овощей. При
этом отщепляется элементарная сера. Пары чрезвычайно легко воспламеняются, в
смеси с воздухом взрывоопасен. Сероуглерод - сильный нервный яд, угнетающе
действующий на центральную нервную систему. Класс опасности 1. ПДК сероуглерода
в воздухе рабочей зоны - 1 мг/м3.
Сероуглерод применяют при производстве вискозного волокна, как
растворитель фосфора, жиров, масел, резины и восков, в производстве
четырёххлористого углерода, карбанилида, NH4SCN, при изготовлении оптического стекла; в борьбе с
врелителями сельского хозяйства; используется как исходное вещество в синтезе
ускорителей вулканизации каучука, флотирующих агентов и др.
Сероокись углерода (COS) - бесцветный газ почти без запаха (в чистом
состоянии). Растворяется в воде, спирте, толуоле. Легко воспламеняется и горит
синеватым пламенем. В воде, даже во влажном воздухе, и при действии щелочей
распадается на CO2 и H2S. С воздухом образует взрывчатую
смесь. При отравлении действует главным образом на центральную нервную систему.
Раздражающее действие слабое.
. Классификация способов очистки от примесей сероводорода и других
сернистых соединений
Для выделения сероводорода при очистке природного газа применяют методы,
которые можно разделить на две группы:
. Сероводород абсорбируют из газовой смеси веществом, которое
затем регенерируют в процессе десорбции
. Сероводород одновременно адсорбируют и окисляют до конечного
продукта - серы.
Абсорбционные методы выделения кислых компонентов подразделяют на две
группы:
. Сухие - с применением очистной массы в твёрдом виде
. Мокрые - с применением жидких растворов
На заводских промышленных установках газы очищают комбинированным
способом, т.е. с применением твёрдых и жидких поглотителей.
При сухих способах используют твёрдые поглотители (адсорбенты) - окись
цинка, шлам алюминиевого производства, губчатое железо (окись железа),
активированный уголь. В последнее время всё большее распространение в процессах
адсорбционной очистки получают молекулярные сита, с использованием которых
одновременно осушают газы от сероводорода и очищают их.
Твёрдые поглотители (кроме молекулярных сит) применяют для очистки
относительно небольших количеств газа и при низком давлении. Все твёрдые
поглотители используют для очистки газов с низким содержанием сероводорода.
Мокрые способы применяют для очистки больших количеств газа со значительным
содержанием в нём сероводорода и углекислоты и при высоком давлении. Мокрые
способы выделения кислых компонентов подразделяются на несколько видов:
. Процессы, в которых происходит химическое взаимодействие
сероводорода с активной частью абсорбента
. Процессы, в которых поглощение сероводорода осуществляется за
счёт физического растворения
. Процессы, в которых применяют абсорбенты смешанного типа;
поглощение H2S происходит
одновременно за счёт физической абсорбции и химической реакции.
Выбор того или иного метода очистки газа зависит от многих факторов (это
начальные и конечные допустимые концентрации сероводорода, область применения
очищенного газа - в быту, в химии или в двигателях, а также возможность
использования определенного поглотителя и экономические факторы), но основными
из них являются концентрации сероводорода и сероорганических соединений в
исходном газе. Очень важное значение в любом методе очистки имеет правильный
выбор поглотителей, которые должны удовлетворять следующим общим требованиям:
§ поглотитель должен иметь низкое давление насыщенного пара при
температурах сорбции, чтобы потери его с очищаемым газом были минимальны;
§ поглотитель должен обладать высокой способностью поглощать кислые
соединения из газа в широком интервале их парциальных давлений;
§ поглотитель должен иметь невысокую вязкость, обеспечивающую хороший
межфазный контакт с газом, малую растворяющую способность в отношении
углеводородов;
. Абсорбционные методы очистки
3.1 Сорбционные методы очистки газов от сероводорода растворами
алканоламинов
.1.1 Технология аминовой очистки
Алканоламины, будучи щелочами, легко вступают в реакцию с H2S,
образуя водорастворимые соли. Процесс взаимодействия H2S с алканоламинами
описывается следующими суммарными реакциями (на примере моноэтаноламина).
2RNH2 + H2S ↔ (RNH3)2S
(RNH3)2S + H2S ↔ 2RNH3HS
где R - группа OHCH2CH2.
Процесс поглощения сероводорода сопровождается выделением теплоты
(таблица 1), а процесс регенерации раствора абсорбента - поглощением теплоты.
Меркаптаны обратимо реагируют с алканоламинами с образованием
водорастворимых меркаптидов, разрушающихся при регенерации раствора абсорбента.
Серооксид углерода в водных растворах аминов гидролизуется:
СОS + H2O → СО2
+ H2S
Образовавшиеся H2S и СО2 реагируют с аминами по
основным реакциям, но эти реакции из-за малого содержания СОS в исходном газе
никогда не доходят до конца.
В насыщенном растворе абсорбента сероводород и другие извлекаемые
компоненты газа находятся не только в связанном виде за счет химических
реакций, но и в свободном, растворенном виде.
Согласно принципу Ле-Шателье понижение температуры и повышение давления
способствует протеканию реакций в прямом направлении, а повышение температуры и
понижение давления - в обратном направлении. Это положение является
определяющим при выборе режимов очистки газа и регенерации насыщенного
абсорбента.
Таблица 1 - Основные физико-химические свойства алканоламинов
|
Показатели
|
МЭА
|
ДЭА
|
МДЭА
|
|
Формула
|
HOC2H4NH2
|
(HOC2H4)2NH
|
(HOC2H4)2
CH3N
|
|
Молекулярная масса
|
61,1
|
105,1
|
119,2
|
|
Плотность при 20 0С,
кг/м3
|
1,015
|
1,094
|
1,018
|
|
Температура, 0С:
|
|
|
|
|
кипения при атмосферном
давлении
|
170
|
268
|
247
|
|
замерзания
|
10,5
|
27,5
|
-21,0
|
|
Давление насыщенных паров
при 60 0С, Па
|
660
|
4,5
|
24
|
|
Динамическая вязкость при
20 0С, 103 Пас
|
19
|
300
|
80
|
|
Удельная теплоемкость при
20 0С, кДж/кг град
|
2,72
|
2,47
|
2,32
|
|
Массовая доля амина в
рабочем растворе, %
|
10-20
|
20-30
|
30-50
|
|
Теплота реакции, кДж/кг:
|
|
|
|
|
с H2S
|
1511
|
1173
|
1047
|
|
Содержание основного вещества,
% мас., не менее
|
99,0
|
99,0
|
99,0
|
Принципиальная технологическая схема однопоточной абсорбционной очистки
газа растворами этаноламинов приведена на рисунке 1. Поступающий на очистку газ
I проходит восходящим потоком через абсорбер 1 навстречу потоку
регенерированного абсорбента V. Насыщенный кислыми газами раствор абсорбента
VI, выходящий с низа абсорбера, подогревается в теплообменнике 5
регенерированным раствором из десорбера 6 и подается на верх его. После
частичного охлаждения в теплообменнике 5 регенерированный раствор дополнительно
охлаждается в холодильнике 3 и подается наверх абсорбера 1.
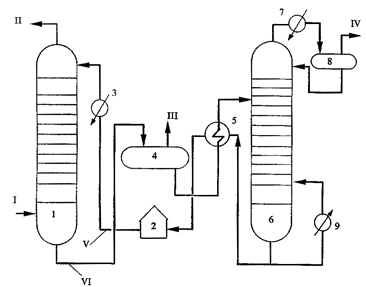
Рисунок 1. Технологическая схема однопоточной аминовой очистки газа:
|
1 - абсорбер; 2 - емкость
регенерированного абсорбента; 3 - холодильник; 4 - экспанзер; 5 -
теплообменник; 6 - десорбер; 7 - конденсатор-холодильник; 8 - сеператор; 9 -
рибойлер; I - исходный газ; II - очищенный
газ; III - экспанзерный газ; IV - кислые
газы; V, VI - соответственно регенерированный и насыщенный
растворы амина
|
Тепло, необходимое для регенерации насыщенного раствора, сообщается
последнему в рибойлерах, обогреваемых водяным паром. Кислый газ из десорбера
охлаждается для конденсации содержащихся в нем водяных паров. Конденсат этих
паров из сепаратора 8 возвращают в десорбер 6 несколько выше входа насыщенного
раствора амина.
В схеме предусмотрен экспанзер (выветриватель) 4, в котором за счет
снижения давления насыщенного раствора выделяются физически растворенные в
абсорбенте углеводороды и частично сероводород и диоксид углерода. Экспанзерный
газ III после очистки используется в качестве топливного газа или
компримируется и подается в исходный газ I.
В случае большого содержания в очищаемом газе кислых компонентов также
целесообразно применение двухпоточного ввода абсорбента, но разной степени
регенерации. Частично регенерированный абсорбент подается в среднюю часть
абсорбера, а на верхнюю тарелку подается глубокорегенерированный абсорбент для
тонкой очистки газа. Такая схема по сравнению с обычной однопоточной схемой
(рисунок.1) позволяет на 10-15 % снизить расход водяного пара на регенерацию.
Кроме того, при очистке высококислых газов необходимо осуществлять двойное
выветривание насыщенного раствора абсорбента при разных давлениях:
первоначально при давлении 1,5-2,0 МПа для выделения основного количества
растворенных углеводородов, а на второй ступени при давлении, близким к
атмосферному, без подвода тепла выделяется часть кислых газов, которая
направляется непосредственно на производство серы. За счет двухступенчатого
выветривания дополнительно экономится до 10 % водяного пара, подаваемого в
рибойлеры десорбера, но при этом устанавливается насос для подачи насыщенного
раствора абсорбента из второго выветривателя в десорбер, который работает в
неблагоприятных условиях при высокой степени насыщения раствора абсорбента
кислыми компонентами и высокой температуре раствора (до 65-75 0С).
При очистке газа, содержащего СОS наряду с H2S и СО2 в
абсорбере может быть предусмотрена зона поглощения и гидролиза СОS, состоящая
из 5-8 тарелок, куда подается регенерированный раствор амина в количестве 10-15
% от общего объема с температурой до 70-80 0С.
В промышленных схемах аминовой очистки газа предусматриваются также
системы фильтрации раствора и ввода антивспенивателя.
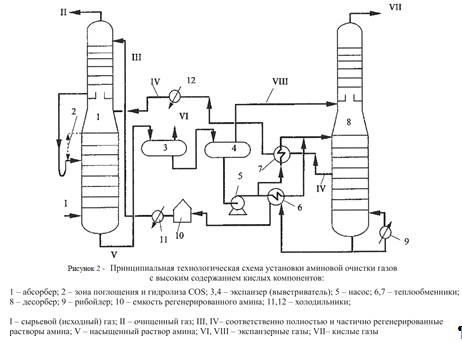
На рисунке 2 приведена принципиальная технологическая схема установок
аминовой очистки газов с высоким содержанием кислых компонентов,
эксплуатируемых в Канаде, Франции, США и на Астраханском ГПЗ. В ней
предусмотрены и раздельный ввод в абсорбер частично и полностью
регенерированного раствора амина, и двухступенчатое выветривание насыщенного
раствора амина, и зона поглощения и гидролиза СОS в абсорбере.
При МЭА-очистке общая степень насыщения раствора абсорбента кислыми
газами составляет от 0,3-0,4 до 0,6-0,7 моль/моль МЭА.
Технологический режим в абсорбере следующий: температура исходного газа -
30-35 0С, регенерированного МЭА - 35-45 0С; давление 3
МПа. Десорбер работает при следующих параметрах: температура насыщенного амина
на входе в десорбер - 85-95 0С, регенерированного амина в кубе
десорбера - 110-120 0С (не более 125 0С); давление
0,3-0,8 МПа. Количество тарелок в абсорбере и десорбере составляет 20-25 штук,
тип тарелок - клапанные, ситчатые или решетчатые, коэффициент полезного
действия - 0,25-0,40.
ДЭА-процесс существует в двух разновидностях - обычный ДЭА-процесс
(концентрация ДЭА в растворе 20-25 % мас., поглотительная способность по кислым
компонентам - 0,5-0,8 моль/моль ДЭА) и ДЭА-SNPA-процесс (концентрация ДЭА в
растворе 25-30 % мас., поглотительная способность по кислым компонентам -
1,0-1,3 моль/моль ДЭА). Первая разновидность используется при наличии в
исходном газе COS и СS2 и парциальном давлении кислых компонентов в
нем от 0,2 МПа и выше, вторая - при парциальном давлении кислого газа выше 0,4
МПа. Технологический режим в абсорбере при ДЭА - очистке следующий: температура
верхнего потока абсорбера - 35-40 0С; среднего потока - 70-80 0С;
насыщенного абсорбента - 65-75 0С; давление - 6,0-7,0 МПа; общий
расход раствора абсорбента - 1,0-1,5 л/м3 газа. Параметры
технологического режима десорбера следующие: температура верха - 50-55 0С;
питания - 105-115 0С; низа - 120-125 0С; давление -
0,18-0,25 МПа. Количество тарелок в абсорбере и десорбере, их тип и к.п.д.
такие же, как и при МЭА-очистке.
.1.2 Влияние параметров на процесс аминовой очистки
Основное влияние на процесс аминовой очистки сернистых природных газов
оказывают давление, температура, кратность циркуляции (расход) раствора
абсорбента и концентрация этаноламина в растворе абсорбента.
С повышением давления в абсорбере глубина очистки газа от кислых
компонентов увеличивается, однако, процесс обычно проводят при давлении исходного
газа (не выше 6,0-7,0 МПа) во избежание дополнительных энергозатрат на сжатие
газа.
Понижение температуры оказывает благоприятное влияние на процесс, но при
этом следует иметь в виду, что слишком низкие температуры увеличивают вязкость
раствора абсорбента и затраты на его перекачку, а также растут затраты на отвод
тепла из абсорбера.
Кратность циркуляции абсорбента должна быть оптимальной, так как избыток
абсорбента не приводит к заметному увеличению степени очистки газа, но резко
растут эксплуатационные затраты, а его недостаток не позволяет обеспечить
требуемую глубину очистки. Кратность циркуляции раствора абсорбента Vа
можно определить по формуле:
а
= 6,3·(V· у·М)/С·Х, м3/ч,
где V - расход исходного газа, м3/ч;
у - мольная доля кислых компонентов в исходном газе;
М - молекулярная масса алканоламина;
С - отношение количеств кислых компонентов и алканоламина,
моль/моль;
Х - концентрация раствора абсорбента, % мас.
Как уже показано выше, по опыту эксплуатации установок аминовой очистки
газов растворы, в которых массовая доля МЭА составляет 15-20 %, а ДЭА - 20-30
%, являются оптимальными как с точки зрения кратности циркуляции, так и
величины эксплуатационных расходов, которые возрастают при применении более
концентрированных растворов.
Давление при десорбции выбирается таким, чтобы обеспечить применением
обычных хладоагентов (воды или воздуха) конденсацию водяных паров из кислых
газов, хотя понижение давления способствует глубине регенерации раствора
абсорбента. Температура десорбции не должна превышать 120-125 0С во
избежание потерь амина с кислыми газами и его термодеструкции.
3.1.3 Пенообразование в аминовых растворах и борьба с ним
Вспенивание растворов аминов - одна из серьезных проблем при эксплуатации
установок очистки газа. Вспенивание приводит к нарушению режима работы
установок, ухудшению качества очищенного газа и, как следствие этого, к
необходимости снижения производительности установок по газу. При вспенивании
возрастают потери аминов в результате уноса с газом
Вспенивание возникает, как правило, в абсорберах, но бывают случаи, когда
начавшееся вспенивание раствора переносится и в десорбер. Признаками
вспенивания являются увеличение объема пены на тарелках, резкое увеличение
перепада давления в аппарате, появление значительного уровня жидкости в
сепараторах очищенного (после абсорбера) и кислого (после десорбера) газов.
Основная причина вспенивания - это примеси, поступающие в систему
установки вместе с очищаемым газом и постепенно накапливающиеся в растворе
абсорбента (жидкие углеводороды, пластовая вода, механические примеси,
ингибиторы коррозии, поверхностно-активные и смолистые вещества и др.).
Пенообразователями являются также смазочные масла (попадают в амин, например,
через систему смазки насосов), продукты коррозии и деградации амина.
Для предотвращения вспенивания на промышленных установках используют
следующие способы:
глубоко очищают исходный газ от механических примесей и др. в сепараторах
и каплеотбойниках;
регенерированный раствор абсорбента подают на верхнюю тарелку абсорбера с
температурой на 2-5 0С выше температуры уходящего из абсорбера газа
для предупреждения конденсации из него углеводородов;
проводят регулярную очистку и промывку аппаратов установки от
накопившегося при эксплуатации шлама;
постоянно фильтруют раствора амина;
применяют антивспениватели (силиконовые композиции, высококипящие спирты
и др.).
Фильтрации подвергается часть раствора абсорбента, при этом может
подвергаться фильтрации как регенерированный раствор (более часто), так и
насыщенный. Вначале раствор проходит механический фильтр (целлюлозный,
сетчатый, дисковый и др.) для удаления механических примесей, а затем поступает
в адсорбер с активированным углем для улавливания углеводородов, продуктов
деградации амина и других адсорбируемых примесей. После угольного адсорбера на
установке обычно устанавливают фильтр для улавливания частиц угля, выносимого с
потоком абсорбента из адсорбера. Фильтрации на угольных адсорберах подвергается
5-20 % раствора от его общего количества в системе установки, а на механических
фильтрах - его большее количество, вплоть до 100%. Скорость прохождения
раствора через угольный адсорбер составляет около 10 л/(мин*м2), но
в ряде случаев она может достигать 20-60 л/(мин*м2). Высота
фильтрующего слоя в одном адсорбере находится на уровне 3-4 м. Из опыта
эксплуатации установок аминовой очистки газов содержание примесей в растворе
абсорбента не должно превышать 2 г/л во избежание его вспенивания. Концентрация
пеногасителя в растворе абсорбента не должна превышать 0,01-0,001 % мас., так
как его большее количество может привести к обратному явлению - стабилизации
пены. Пеногасители вводят в систему установки постоянно небольшими порциями,
либо кратковременно непосредственно в момент вспенивания раствора абсорбента.
Пеногасители перед вводом в систему растворяют в аминах или других
растворителях, не содержащих углеводороды, вызывающие вспенивание раствора
абсорбента.
3.2 Процессы очистки растворами солей щелочных металлов
Эти процессы основаны на хемосорбционной активности водных растворов карбонатов
натрия и калия по отношению к основным серосодержащим соединениям газа (кроме
меркаптанов). Процесс совершенствуют путем добавок к поглотителю различных
активирующих добавок, повышающих его поглотительную способность и снижающих его
коррозионную активность и пенообразование.
Химизм процесса карбонатной очистки описывается следующими уравнениями:
Nа2СО3
+ H2S → NaHCO3 + NaHS;
Na2CО3 + Н2О →
2NaHCО3;
Na2CО 3 + H2S → КНСО3 + KHS;
COS +
Н2О → СО2 + Н2S.
Процесс проводится при сравнительно высоких температурах (90-120 0С)
и давлениях выше 2,0 МПа. В отношении технологической схемы и оборудования
карбонатная очистка аналогична аминовой.
В процессе "горячий поташ" используется 25-35 % -ный водный
раствор К2СО3, удаляющий из газа Н2S, СО2,
СОS и СS2, но не удаляющий меркаптаны. Процессы абсорбции и
десорбции проходят при температуре 105-115 0С, но давление в
абсорбере составляет 2-14 МПа, а в десорбере - 0,2-0,8 МПа. Процесс
"горячий поташ" целесообразно применять для очистки больших потоков
газа с концентрацией кислых компонентов более 5-8 %. К недостаткам процесса
можно отнести: трудность удаления меркаптанов, коррозию оборудования и
необходимость иметь низкое соотношение количеств сероводорода и диоксида
углерода в исходном газе.
3.3 Основы технологии очистки газа физическими абсорбентами
Процессы физической абсорбции основаны на растворении компонентов газа в
жидкости, происходящем по закону Генри (объем поглощаемого компонента
пропорционален его парциальному давлению в газовой смеси).
Растворимость кислых компонентов в физических абсорбентах при различных
температурах описывается уравнением:
К = D1 + D2Т + D3/Т + D4lnТ,
где К - константа Генри;
D1-D4 - коэффициенты, определяемые по справочным данным;
Т- температура контакта, К.
В качестве абсорбентов используют моно-, ди- и триэтиленгликоли, их
диметиловые эфиры, сульфолан (тетрагидротиофендиоксид), N-метилпирролидон, трибутилфосфат,
пропиленкарбонат и др. Перечень и характеристика наиболее распространенных
абсорбентов, используемых в процессах очистки газов физической абсорбцией,
приведены в таблице 2
Достоинством этих методов являются более низкие энергозатраты на
регенерацию поглотителей.
Различными фирмами разработаны промышленные процессы очистки газа с
использованием этих растворителей, рассчитанные на различные параметры как
исходного газа (содержание и состав вредных примесей, количество выносимого
конденсата и др.), так и
очищенного газа (требования по глубине очистки, селективность по компонентам
вредных примесей и др.).
К процессам физической абсорбции относятся такие, как
"Селексол", "Флуор сольвент", "Пурисол" и др. В
процессе "Селексол" абсорбентом служит смесь полиэтиленгликолей (от
три- до наноэтиленгликолей) с диметиловым эфиром. В процессе "Флуор
сольвент" используют пропиленкарбонат, "Пурисол" -
n-метил-2-кетопиролидин (НМП), предназначенный для грубой очистки газов с
высоким содержанием кислых компонентов.
Таблица 2 - Характеристики некоторых физических абсорбентов
|
Абсорбент
|
Формула
|
Молекулярная масса
|
Плотность ρ204
|
Температура кипения, ˚С
|
|
Этиленгликоль
|
C6H6O2
|
62
|
1,116
|
197
|
|
Диэтиленгликоль
|
C4H10O3
|
106
|
1,118
|
245
|
|
Триэтиленгликоль
|
150
|
1,126
|
287
|
|
Сульфолан
(тетрагидротиофендиоксид)
|
C4H12O2
|
124
|
1,260
|
286
|
|
N- метилпирролидон (N-МП)
|
C5H11N
|
85
|
1,030
|
206
|
|
Трибутилфосфат (ТБФ)
|
(C4H9O)3PO
|
266
|
0,970
|
289
|
Очистка гликолями (ДЭГ, ТЭГ) применяется обычно на промыслах в тех
случаях, когда газ содержит большое количество Н2S и СО2 и не нужно очищать
газ от этих примесей до требований отраслевого стандарта (ОСТ 51.40-83). Его
используют для нужд самого промысла (закачка в пласт для поддержания пластового
давления, применение в качестве топливного газа). Применение гликолей упрощает
технологию очистки, поскольку для очистки и осушки газа от паров воды
используется один абсорбент. Кроме того, основное количество абсорбированных
компонентов выделяется из насыщенного абсорбента простой дегазацией, без затрат
тепла. Наибольшее распространение в таких процессах очистки получил ДЭГ.
Принципиальная схема очистки газа диэтиленгликолем показана на рисунке 3.
Основной поток газа с температурой до 40°С направляется в абсорбер 2 (давление
7-8 МПа), где он осушается от влаги. Другая часть сырого газа поступает в
колонну 1 (давление на 0,2-0,3 МПа выше, чем в абсорбере) для глубокой очистки oт H2S
абсорбцией регенерированным высококонцентрированным раствором ДЭГ, который
после насыщения направляется как осушающий агент в абсорбер 2. Осушенный газ с
верха абсорбера 2 используется как топочное топливо, а насыщенный ДЭГ через
дегазаторы 4 направляется в отдувочную колонну 3 (давление в ней также на 0,2
МПа выше, чем в абсорбере 2). Очищенный от H2S газ
III сверху колонны частью выводится как топливо или для других технологических
нужд, а другая часть, нагретая до 120°С, подается в низ колонны 3 как
отдувочный газ, который "отдувает" от раствора ДЭГ сероводород и с
концентрацией его в отдувочном газе до 7% последний направляется в смеси с
сырым газом в абсорбер 2.
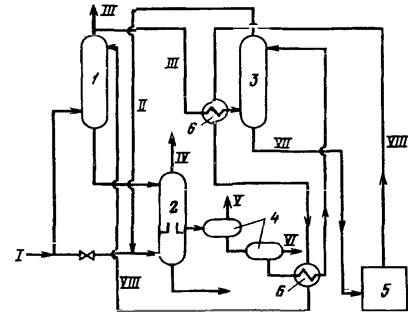
Рисунок 3- Принципиальная схема очистки и осушки газа раствором ДЭГ: 1 -
абсорбер очистки от сероводорода; 2 - абсорбер осушки; 3 -
колонна отдувки; 4 -дегазаторы; 5 - блок регенерации ДЭГ; 6 -
теплообменник; I, II и III - исходный, отдувочный и очищенный от сероводорода газы; IV -
осушенный газ, V - газ дегазации; VI - жидкие углеводороды; VII -
раствор ДЭГ, насыщенный сероводородом и водой, VIII - регенерированный
раствор ДЭГ
Из дегазаторов выводят десорбированный газ V и жидкие углеводороды VI, поглощенные в абсорбере потоком абсорбента.
Процесс "Пуризол". В качестве абсорбента использует N-метилпирролидон (N-МП) -
тяжелый малотоксичный растворитель, смешивающийся с водой в любых соотношениях.
В N-МП хорошо растворяются сероводород и меркаптаны, а также
диоксид углерода (при достаточно высоких парциальных давлениях). Растворимость
Н2S в N-МП в 10-12 раз больше,
чем СО2 и поэтому процесс можно использовать для селективного
извлечения Н2S.
Схема процесса "Пуризол" может быть одно- и двухступенчатой.
Первая применяется в случаях, когда содержание СО2 в газе мало или
существенно меньше, чем содержание H2S. Двухступенчатая схема используется
для очистки газов с большим содержанием СО2 (равным или выше, чем
содержание Н2S); на
первой ступени в этом случае удаляется Н2S, а на второй - СО2.
Регенерация поглощенных раствором N-МП примесей производится при
пониженном (близком к атмосферному) давлении и температуре от 100 до 120 °С.
Поскольку в режиме абсорбции (при высоком давлении) в растворе N-МП,
кроме вредных примесей, растворяются углеводороды, то абсорбент до регенерации проходит
ступень выветривания (отдува) из него углеводородов, а отдувочный газ
возвращается в поток сырого газа перед абсорбером.
В процессе "Селексол" в качестве абсорбента используется
концентрированный (содержание воды - 0-5 % мас.) диметиловый эфир полиэтиленгликоля,
который хорошо поглощает все сернистые соединения, диоксид углерода и воду.
Этот абсорбент используется для селективной очистки природного газа от
сероводорода в присутствии диоксида углерода, так как растворимость Н2S
в нем в 7-10 раз выше растворимости СО2. Одновременно процесс
используется и для осушки газа. По поглотительной способности селексола
различные компоненты газа располагаются в следующем ряду:
Н2О> СS2>СН3SН> Н2S>
С5Н12> С4Н10> С3Н8>СО2>
С2Н6
Селективное выделение сероводорода из природного газа позволяет получить
кислый газ - сырье производства элементной серы с малым содержанием других
компонентов, что значительно улучшает показатели процесса Клауса.
В технологическую схему процесса "Селексол" входят абсорбер,
регенератор, выветриватели, теплообменники и насосы.
Принципиальная схема процесса приведена на рисунке 4. Давление абсорбции
- 7,0-7,5 МПа, температура - 25-35 0С, кратность подачи абсорбента -
1,5-2,5 л/м3 газа.
Регенерация абсорбента осуществляется понижением давления в
выветривателях и десорбере и отдувкой топливным или инертным газом, а также
подводом тепла в куб десорбера.
Другой разновидностью абсорбента на основе диалкиловых эфиров
полиэтиленгликолей является смесь метилизопропиловых эфиров ПЭГ - "Сепасолв-МПЕ".
По растворимости Н2S и СО2 абсорбенты
"Селексол" и "Сепасолв-МПЕ" практически идентичны.
"Сепасолв-МПЕ" обладает меньшей вязкостью и меньшим давлением
насыщенных паров. Регенерация абсорбента осуществляется при температуре около
140 0С с подачей или без подачи отдувочного газа (во втором случае
абсорбент содержит 3-5 % мас. воды).
Метанол используется в процессе "Ректизол" - одном из
первых абсорбционных процессов для очистки природного газа. Абсорбция проходит
при давлении 2,0-7,5 МПа, температуре - минус 35 - минус 70 0С,
кратность подачи метанола - 0,3-0,5 л/м3 газа. Десорбция
осуществляется ступенчатым понижением давления, а на последней ступени может
применяться тепловая регенерация.
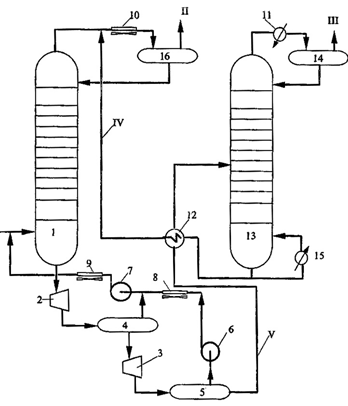
Рисунок 4 - Принципиальная технологическая схема процесса Селексол: 1 -
абсорбер; 2,3 - гидравлические турбины; 4,5 - выветриватели; 6,7 - компрессоры;
8,9,10,11 - конденсаторы-холодильники; 12 - теплообменники; 13 - десорбер;
14,16 - сепараторы; 15 - рибойлер; I - сырьевой газ; II -
очищенный газ; III - кислый газ; IV - регенерированный абсорбент; V - частично разгазированный абсорбент
3.4 Абсорбция комбинированными поглотителями
Для выделения сероводорода можно использовать смеси алканоламинов с
физическими абсорбентами (метанолом, бензиловым спиртом, сульфоланом). Таким
образом один из компонентов, например, сульфолан, осуществляет физическую
абсорбцию, а другой-алканоламин-хемосорбцию (Сульфинол - процесс).
Процесс "Сульфинол" разработан в начале 1960-х гг.
фирмой "Шелл Ойл Компани" и нашел широкое применение, благодаря своим
преимуществам. В процессе используют комплексный поглотитель, состоящий из 60 -
65% сульфолана, являющегося физическим абсорбентом кислых компонентов газа, 28
- 32% диизопропаноламина (ДИПА, хемосорбент) и около 6% воды, добавляемой в
качестве депрессатора, снижающего на 10 - 12°С температуру застывания смеси.
Наличие в составе поглотителя компонента, физически растворяющего вредные
примеси (сульфолан), и хемосорбента (ДИПА) позволяет придать процессу
универсальность по составу исходного газа, т.е. глубина очистки при
использовании такого поглотителя мало зависит от начальной концентрации
примесей. При высоком содержании сероводорода значительная часть его (за счет
высокого парциального давления) растворяется сульфоланом, а остаточные
небольшие его количества (при малых парциальных давлениях) хемосорбирует ДИПА.
Поглотительная ёмкость такого смешанного абсорбента составляет от 30 до
120 мг/м3 в зависимости от состава исходного газа и условий процесса
(для сравнения, при использовании МЭА - 25 - 30 мг/м3). Более
высокая поглотительная способность абсорбента в процессе "Сульфинол"
обусловливает меньшую кратность его циркуляции и меньшие габариты аппаратов.
Значительно ниже (на 30 -80%) также энергозатраты на регенерацию абсорбента,
поскольку десорбция основного количества растворенных в сульфолане компонентов
осуществляется при снижении давления в десорбере. Еще одним несомненным
преимуществом процесса "Сульфинол" является то, что смесь сульфолана
с ДИПА очищает газ как от H2S и CO2, так и достаточно глубоко от других серосодержащих
соединений (COS, CS2 и тиолы).
Принципиальныя схема очистки газа от кислых компонентов в процессе
"Сульфинол" приведена на рисунке 5.
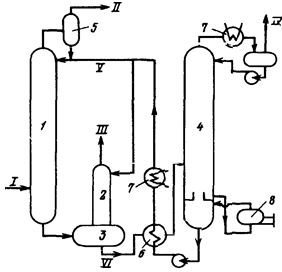
Рисунок 5 -. Принципиальная схема очистки газа в процессе
"Сульфинол" 1,2 -абсорберы, 3 - дегазатор, 4 -
десорбер, 5 - сепаратор, 6 - теплообменник, 7 - холодильники, 8
- ребойлер, I и II - исходный и очищенный газы, III - очищенный газ
дегазации, IV- кислые газы, V, VI- регенерированный и насыщенный
абсорбент.
Важно также отметить, что оба поглотителя имеют низкое давление
насыщенных паров в условиях очистки и поэтому очень мало теряются с очищенным
газом.
В последнее время той же фирмой разработан комбинированный процесс
"Сульфинол-СКОТ," с помощью которого единой системой поглотителя
(сульфолан - ДИПА) решаются две разные задачи: из углеводородного газа
выделяется концентрат кислых газов, направляемых на производство серы процессом
Клауса, и улавливается значительное количество оксидов серы из отходящих
дымовых газов процесса Клауса.
4. Адсорбционные методы очистки
Методы очистки газов от сероводорода с использованием твердых сорбентов
могут быть классифицированы на основании физико-химических процессов,
происходящих при сорбции сернистых соединений:
· адсорбционные методы (физическая адсорбция);
· хемосорбционные методы (образование устойчивых химических
соединений сероводорода с сорбентом).
.1.
Физическая адсорбция
Очистка газа на активированном угле является наиболее распространенным
методом. Сущность способа: серосодержащий газ смешивают с 3-4% воздуха и
пропускают через фильтр, заполненный активированным углем. Сероводород
окисляется на фильтре по реакции:

Температура реакции 40оС, она ускоряется в присутствии аммиака
Роль активированного угля двояка: он является катализатором окисления
сероводорода и адсорбентом серы, образующейся в процессе окисления. Во время
регенерации фильтра его обрабатывают раствором сернистого аммония, который
растворяет серу с образованием многосернистого аммония:
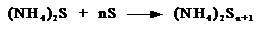
Насыщенный раствор многосернистого аммония поступает в кипятильник, где
разлагается на NH3, H2S и S при температуре 130оС:

Элементарная сера является товарным продуктом хорошего качества (99%-ной
чистоты). Длительность работы угля до регенерации - 1-3 недели, а общий срок
службы - около двух лет. Для регенерации угля может применяться продувка
фильтра потоком горячего (300-330оС) регенерированного газа.
Степень очистки газа от сероводорода достигает 99%. Недостатки -
цикличность процесса и сложность технологической схемы, трудности утилизации
образующегося аммиака и сероводорода (в цикле регенерации), зауглероживание
катализатора-адсорбента.
Возможна очистка газа от сероводорода на активированном угле в кипящем
слое. В процессе используются активированные угли с основными центрами типа
СКТ-3, СКТ-26, АГ-3. Метод целесообразно использовать при обработке больших
объемов газа (до 200 000 м3/ч.) с низким содержанием сероводорода.
Очистка с помощью синтетических цеолитов
Молекулярные сита (цеолиты) - это синтетические или природные
кристаллические алюмосиликаты, в каркасе которых кремний и алюминий находятся в
тетраэдрической конфигурации, содержащие щелочные металлы. В промышленности
применяют, в основном, синтетические цеолиты. По строению цеолиты представляют
систему регулярных каналов и сообщающихся плоскостей с размером пор от 0,3 до
1,0 нм в зависимости от типа цеолита. В ходе адсорбции примеси, присутствующие
в газе, диффундируют через поры и поверхности внутренних плоскостей. В
промышленности применяются цеолиты, сформованные в виде таблеток или шариков
размером около 3 мм.
По сравнению с другими адсорбентами молекулярные сита имеют большую
поглотительную способность, менее подвержены загрязнению и закоксовыванию и,
благодаря наличию пор регулируемого размера, обладают уникальной селективностью
в адсорбции, зависящей от размеров молекул. Их использование позволяет снизить
удельный объем адсорбента, работать при более низком перепаде давлений в слое
адсорбента, исключить потери газа из-за адсорбции ряда его компонентов,
обеспечить более длительную и надежную работу установки.
Для проведения очистки используются цеолиты типа СаА. При этом происходит
одновременно и осушка газа. Процесс идет под давлением 1,7-5 МПа. Остаточное
содержание сероводорода 1мг/м3. При наличии в системе сероводорода,
паров воды и диоксида углерода вначале адсорбируется вода и сероводород, и
только после них - диоксид углерода.
Процесс очистки природного газа на цеолитах, как всякий адсорбционный
процесс, является циклическим. После появления за слоем цеолита сернистых
соединений в количестве, определяемом требованиями потребителя к очищенному
газу, сорбент подвергают регенерации. Очистку от сернистых соединений в этот
период проводят в другом адсорбере с регенерированным и охлажденным слоем
цеолита.
Регенерацию цеолитов осуществляют путем продувки очищенным газом,
нагретым до температуры 300-350° С.
Температурный режим регенерации выбирается по наиболее трудно
десорбируемому компоненту. Таким компонентом являются пары воды, сорбируемые
легче сернистых соединений и требующие применения более высоких температур на
стадии регенерации. Удаление остаточной воды на стадии регенерации является
непременным условием для последующего проведения процесса очистки на этом же
слое без снижения адсорбционной емкости. Проведение регенерации противотоком
также позволяет уменьшить воздействие остаточной воды.
К недостаткам процесса следует отнести: значительный расход газа на
регенерацию адсорбента (до 10% объема обрабатываемого газа), причем газы
регенерации обычно сжигаются, что приводит к безвозвратным потерям газа и серы
и загрязнению атмосферы. Таким образом, очистка на цеолитах целесообразна
только на крупных ГПЗ, где возможна утилизация газов регенерации. В последнее
время предложена регенерация цеолитных адсорбентов методом экстракции
углеродистых отложений органическими растворителями: метанолом, уксусным
ангидридом, дихлорэтаном, бензолом, н-гексаном и широкой фракцией легких
углеводородов (ШФЛУ) С3-С5.
4.2 Химическая адсорбция
Оксиды цинка, железа, меди относятся к наиболее распространенным твердым
хемосорбентам При использовании оксидов железа (наиболее старый способ)
протекают реакции:

Регенерация сорбента проводится воздухом по реакциям:
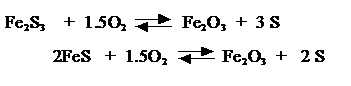
В зависимости от количества подаваемого на регенерацию воздуха можно
получать как элементарную серу, так и оксиды серы. Метод характеризуется
дешевизной, возможностью регенерации хемосорбента, но существенным его недостатком
является низкая степень очистки от сероводорода (до 10 мг/м3) и
невозможность использования образующейся серы.
При очистке с помощью оксидов цинка протекают реакции не только с
сероводородом, но и с другими сернистыми соединениями:
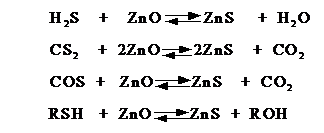
Температура процесса 350-400 0C, а сероемкость сорбента достигает 30%. Остаточное содержание
серы в газе до 1мг/м3. Процесс достаточно универсальный, широко
используется в промышленности, однако при этом сам хемосорбент не подлежит регенерации.
При очистке с помощью оксидов меди процесс протекает с большой скоростью, но
хемосорбент также не подлежит регенерации.
Широкое распространение получила хемосорбционно-каталитическая система.
На первой стадии проводят каталитическое гидрирование сероорганических
соединений до углеводородов и сероводорода, а далее-хемосорбцию сероводорода
поглотителями (оксидами цинка, железа или меди). В России разработан
низкотемпературный хемосорбент ГИАП-10-2 на основе оксида цинка с активирующей
добавкой оксида меди.
Близкий к этому - железо-содовый метод. Основан на использовании в
качестве поглотительного раствора взвеси гидрооксида двух- и трехвалентного
железа
H2S+Na2CO3 NaHS + NaHCO3
NaHS+2Fe(OH)3 Fe2S3+3NaOH+3H2O+2Fe(OH)3 2FeS +S +
3NaOH+3H20
Регенерацию поглотительного раствора осуществляют пропусканием через него
воздуха. При этом около 70% сероводорода переводится в элементную серу, а 30%
-окисляется до тиосульфата натрия.
Основным достоинством всех процессов очистки природного газа от
сероводорода твердыми сорбентами является простота аппаратурного оформления и
легкость проведения технологического процесса собственно очистки газа,
особенно, в случае использования дешевых нерегенерируемых сорбентов на основе
оксида железа.
Общим недостатком таких процессов является низкая линейная скорость газов
в аппаратах газоочистки (на порядок ниже, чем при абсорбционных процессах). То
есть для очистки газов твердыми сорбентами требуются газоочистные аппараты с
площадью сечения в 10 раз большей, чем при абсорбционной очистке.
5. Окислительные методы
Эти процессы совмещают очистку газов от сероводорода с одновременным
окислением его до элементарной серы. В настоящее время существует множество
окислительных процессов очистки, но применяются они в основном для очистки
газов от H2S и для очистки
жидких продуктов от R-SH. Среди них такие как "Феррокс",
"Тилокс", "Стретфорд", "Сульфолин",
"Ло-Кэт" применяются для очистки газов от сероводорода.
Жидкофазно-окислительные процессы обычно применяются для очистки малосернистых
газов и газов малых месторождений с небольшим количеством получаемой серы (до
5-10 т в сутки). Эти методы основаны на поглощении сероводорода раствором
какого-либо окислителя с образованием элементарной серы и последующей
регенерацией раствора кислородом воздуха.
Наибольшее распространение за рубежом среди промышленных процессов
получили следующие: мышьяково-содовый, "Стретфорд", поташный метод с
использованием хелатных комплексов железа. Имеются и другие подобные системы:
процесс "Tahanakx" (Япония) - с использованием
окислительно-восстановительных (ОВС) систем на основе хинолина или антрахинона,
"Xiperion" - с использованием OBC Fe-нафто-хинон, с использованием
OBC на основе фталоцианинов. В России и странах СНГ в настоящее время
используются, в основном, процессы на базе комплексных соединений железа и
фталоцианинов кобальта. Степень извлечения и утилизации сероводорода во всех
окислительных процессах составляет более 98 %. Сера, получаемая в процессах
окислительной очистки, получается в мелкодисперсной форме со средним размером
частиц 5-10 мкм. Для выделения дисперсной серы из раствора применяют
гравитационное осаждение, фильтрацию на фильтре или центрифуге. Для получения
товарного продукта применяют также автоклавную плавку дисперсной серы. Дисперсная
сера также пригодна в качестве сырья для приготовления коллоидной серы
Феррокс-процесс. По этому способу сероводород абсорбируется суспензией
3%-ого карбоната натрия и 0,4 %-ого оксида железа (III). Первоначально
сероводород конвертируется в бисульфид натрия под действием карбоната натрия.
Затем он реагирует с оксидом железа. Раствор обрабатывают кислородом воздуха, в
результате выделяется элементарная сера, а регенерированный оксид железа
возвращается в абсорбер. Процесс осложнён протеканием побочных реакций
образования тиоцианатов и тиосульфатов металлов. Остаточное содержание
сероводорода составляет около 5 ppm.
Тилокс-процесс. Этот метод применяют при очистке газов с высоким
содержанием сероводорода. Поглощение осуществляют нейтральным раствором тиоарсената
натрия. Насыщенный абсорбционный раствор регенерируют барботажем воздуха. В
результате образуется мелкодисперсная сера, которая удаляется с поверхности
раствора. Процесс отличает высокая эффективность. Недостаток заключается в
загрязнении серы соединениями мышьяка.
Стретфорд-процесс. Сероводород выделяют из смеси газов посредством
поглощения его раствором, содержащим щелочной органический реагент и ванадат
аммония, с одновременным получением высококачественной серы. Процесс
непрерывный. Гидросульфид окисляется с образованием серы, выделяющейся в виде
тонкодисперсной суспензии. Суспензию концентрируют, а затем серу
отфильтровывают и очищают промывкой. Процесс, разработанный фирмой Бритиш Газ,
включает кроме традиционных блоков абсорбции - регенерации и фильтрации серы,
еще и установку по выведению солей из поглотительного раствора, что позволяет
применять технологию для извлечения сравнительно больших объемов серы.
Технология применяется как для очистки природного газа, так и других
технологических газов - отходящих газов многих производств - получения
вискозного волокна, коксового и природного газов. В мировой зарубежной практике
работает около 30 установок. Капитальные затраты составляют ориентировочно -0,8
млн. дол. на тонну серы, а эксплуатационные ориентировочно - 80 дол. на тонну.
Клаус-процесс - процесс каталитической окислительной конверсии
сероводорода. Процесс применяется для переработки газов с высоким содержанием
сероводорода. Оборудование включает цилиндрический реактор диаметром 10 м и
высотой 5-6 м, в котором на решётку помещён катализатор (боксит) слоем толщиной
2 м. Очищаемый газ проходит сверху вниз. При этом сероводород окисляется
кислородом в соответствии с реакцией:
H2S + O2 = 2H2O + 2S
Усовершенствованная система процесса предусматривает сжигание части
сероводорода до оксида серы (IV) в начале процесса перед подачей газа в печь
Клауса. Остаточное количество сероводорода окисляется оксидом серы (IV) до
элементарной серы. Процесс контролируют таким образом, чтобы состав смеси
соответствовал стехиометрии реакций:
2H2S + 3O2 = 2H2O + 2SO22 +
2 H2S = 2H2O + 3S
Контактная масса состоит из смеси оксида кремния (IV), гидроксида
алюминия и оксида железа (III). Получаемая в печи сера разливается по формам и
застывает. Степень выделения сероводорода из газовой смеси составляет 95 %.
Метод Клауса получил наибольшее распространение.
Клаус-процесс активно применяется на нефтеперерабатывающих предприятиях,
для переработки сероводорода с установок гидрогенизации и установок аминовой
очистки газов. Основная задача - достижение 99,5 % извлечения серы без
дополнительной очистки отходящих газов. Однако остаточные газы при процессе
Клауса обычно содержат (в зависимости от эффективности работы и качества
исходного газа) 1-2 % сероводорода, до 1 % диоксида серы, до 0,4 % сероокиси
углерода, до 0,3 % сероуглерода, 1-8 г/м3 капельной и паровой серы, по 1-1,5 % водорода и оксида
углерода, до 15 % углекислоты, около 30 % водяных паров и азот. Экологические
требования диктуют необходимость доочистки отходящих газов.
Заключение
Ужесточение экологических требований и дефицит разведанных месторождений
природных газов с отсутствием сернистых примесей ставит в ряд важнейших задач
очистку от кислых примесей (в частности, от сероводорода), делающих невозможным
использование таких газов в качестве топлива, а также вызывающих загрязнение
окружающей среды, коррозию технологического оборудования и разрушение
строительных конструкций.
В тоже время на территории Росси разведано и законсервировано много
газовых, нефтегазовых, газоконденсатных серосодержащих месторождений. Однако
разработка данных месторождений без обеспечения их эффективным сероочистным
оборудованием может стать источником серьезных экологических осложнений.
Экологическую опасность сероводорода в большей мере определяет продукт его
сжигания (сернистый ангидрид), который оказывает активное техногенное
воздействие на окружающую среду, народохозяйственные и природные объекты.
Наиболее эффективным направлением решения данной проблемы является обеспечение
предварительной очистки природного газового топлива и перевод на него всех
крупных потребителей энергии.
При огромных масштабах использования газа в народном хозяйстве
первоочередной задачей является явственное улучшение процессов подготовки,
всесторонняя интенсификация производства, расширение ассортимента продукции и
повышение ее качества.
В настоящее время разработаны и эксплуатируются в промышленности
различные методы извлечения сернистых соединений, которые отличаются
необходимыми затратами и степенями очистки. Наиболее распространенным методом
является абсорбция аминами.
Список литературы
1. Голдобин В. Природный газ - добро или зло // Нефть России,
№11, 2007.
. Хисамутдинов Н.И. Разработка газовых месторождений в
поздней стадии. М.: ВНИИОЭНГ, 2004. - 252 с.
3. Ганз С.Н., Кузнецов И.Е. Очистка природных газов. Киев,
1967
.Кемпбел Д.М. Очистка и переработка природных газов: Пер. с
англ. Под ред. Гудкова С.Ф. - М.: Недра, 1977. - 349 с.: ил.
.Мановян А.К. Технология первичной переработки нефти и
природного газа: Учебное пособие для вузов. - М.: Химия, 1999. - 568 с.: ил.
.Технология переработки сернистого природного газа:
Справочник / А.И. Афанасьев, В.М. Стрючков, Н.И. Подлегаев, Н.Н. Кисленко и
др.: Под ред. А.И. Афанасьева. - М.: Недра, 1993. - 152 с.: ил.
.Агаев Г.А., Настека В.И., Сеидов З.Д. Окислительные процессы
очистки сернистых природных газов и углеводородных конденсатов. - М.: Недра,
1996. - 301 с.: ил.
. http://neftegaz.ru/tech_library/view/4296
9.Ахмадуллина А.Г., Ахмадуллин Р.М. О новых разработках и
внедрениях в области сероочистки углеводородного сырья, стр.3-8// Химия и
технология топлив и масел. - 2008 г., т44. №6, с. 3-8.
10.А. В. Анисимов, А. В. Тараканова, Окислительное
обессеривание углеводородного сырья // Рос. хим. ж. (Ж. Рос. хим. об-ва им.
Д.И. Менделеева) - 2008, т. LII,
№ 4, с. 32-40.