Получение MQ-смол
Содержание
Введение
Литературный обзор
Экспериментальная часть
Выводы
Список используемой литературы
Введение
Для модификации кремнийорганических эластомерных
композиционных материалов в последнее время широкое применение находят так
называемые MQ - смолы [1,2]. Эти соединения встречаются в литературе также под
другими названиями: олиготриметилсилоксисилоксаны, триметилсилоксисиликаты или
сополимерные MQ - силоксаны. MQ - смолы известны уже на протяжении более
полувека. Области применения MQ смол, а также их свойства и методы получения
были подробно описаны в обзорах Молчанова в 80-х годах прошлого столетия [1,3].
За прошедшие годы бурного развития науки и техники, интерес к
MQ - смолам не только не снизился, а наоборот - заметно возрос. За рубежом MQ -
смолы как отдельный класс кремнийорганических смол стали включать в специальные
энциклопедические издания, а также в монографии по химии и технологии
кремнийорганических соединений [4 - 6]. Первые упоминания о MQ - смолах
появились и в отечественных изданиях [7,8].
смола олигомерное кремнийорганическое соединение
Литературный
обзор
MQ - смолы и способы их получения.
MQ - смолы - это олигомерные кремнийорганические соединения,
молекулы которых содержат в основной цепи структурные фрагменты диоксида
кремния [SiO2] (Q), а в обрамлении - триметилсилокси [ (CH3)
3 SiO1/2] (М) группы. Для наиболее распространенных MQ -
смол элементарное звено цепей молекул изображается формулой [MxQOHyQz]
n, где x = 0,62 - 0,65; y = 0,15 - 0,17; z = 0,82 - 0,85; n = 30 -
32. Приведенная формула соответствует пространственной сильноразветвленной
структуре смолы со средней молекулярной массой (Мn), приблизительно
равной 3500 г/моль. MQ - смолы содержат также большое количество (обычно ~2% от
массы смолы) гидроксильных групп, которые расположены на не полностью
сконденсированных фрагментах диоксида кремния Q.
Структуры MQ - смол до сих пор окончательно не описаны. По -
видимому, это связано с возможным их многообразием и большой сложностью.
Вероятно, о структуре MQ - смол можно говорить с какой - то долей уверенности
только применительно к конкретному методу получения. Так считают, что MQ -
смолы, полученные из силиката натрия, построены из силикатных кластеров
различного размера, окруженных по периферии (или капсулированных) группами [
(CH3) 3 SiO1/2]. Исходя из подобного
представления, возможно оценить размеры подобных образований, которые
оказываются на уровне единиц нанометров [9,10].
По внешнему виду MQ - смолы, не содержащие растворителя,
представляют собой бесцветные или светло - желтые твердые продукты от
смолообразных до хрупких в зависимости от соотношения звеньев M и Q. Чем меньше
M, тем более хрупкой становится смола [11]. При соотношении M: Q менее 0,7
смолы перестают размягчаться (до 200 оС), сохраняя при этом
растворимость в органических растворителях.
Уникальным свойством MQ - смол является их хорошая, несмотря
на пространственную структуру, растворимость в органических растворителях
(толуол, спирт, бензин, ацетон) и совместимость с полидиметилсилоксанами.-
силоксаны по термической и термоокислительной стабильности превосходят линейные
полидиметилсилоксаны. При этом скорость разложения не зависит от наличия
кислорода. Введение MQ - силоксанов в полидиметилсилоксаны подавляет
циклодеполимеризацию полидиметилсилоксанов при нагреве как в инертной
атмосфере, так и на воздухе. Термодеструкция MQ - смол начинается при
температуре выше 300 оС и протекает в направлении отрыва
триметилсилокси радикалов и образования кремнеземного остатка (неорганического
"кокса") в виде неспекшегося порошка [12].
Специфические физико-механические свойства MQ - смол
позволяют широко использовать их для улучшения эксплуатационных и, прежде
всего, физико - механических свойств эластомеров. MQ - силоксаны входят в
состав высокопрочных заливочных, формовочных и пропиточных составов,
отверждаемых по разным механизмам. Прочность вулканизатов с участием MQ - смол
на основе жидких каучуков достигает 5 МПа, а на основе высокомолекулярных
каучуков - 10 МПа и выше. Обычно это эластомерные материалы специального назначения:
электроизоляционные, стойкие к действию растворителей; огне - и
абляционностойкие резины. MQ - силоксаны незаменимы при создании высокопрочных
прозрачных силиконовых материалов и изделий (например, глазных имплантатов).
Эластомеры с участием MQ - смол широко используют в оптоволоконной технике
[13].
Другие эластомерные композиционные материалы с участием MQ -
смол включают пеноматериалы, покрытия, адгезивы [14,15]. Без MQ - смол было бы
невозможно создание таких важных для техники материалов, как кремнийорганические
адгезивы, чувствительные к давлению и сохраняющие эластичность в диапазоне - 73
÷ 260 оС [16].
Среди неотверждаемых составов с участием MQ - смол следует
выделить пеногасители, эксплуатируемые в жестких условиях (интенсивное
перемешивание и щелочная среда) [17,18], косметические препараты [19].
Немалую роль MQ - смолы играют в антиадгезионных и
гидрофобизирующих композициях [20].
Известны примеры использования MQ - смол в керамифицирующихся
силиконовых композициях, а также при получении кварцевого стекла [21].- смолы
обладают уникальным свойством окислять карбонилы металлов (Cr, Mo, Co, Ni, Fe)
с образованием органорастворимых металлокремнийорганических комплексов [22].
Неослабевающее внимание к MQ - смолам в мировой научной
литературе и постоянное расширение областей их применения приводит в свою
очередь к большому разнообразию методов их синтеза. Известные в настоящее время
методы получения MQ - силоксанов можно разделить на несколько типов:
· Гидролитическая поликонденсация
кремнийорганических мономеров (в том числе тетрафункциональных хлор и
алкоксисиланов).
· Гетерофункциональная поликонденсация
органо-разно функциональных силанов.
· Триметилсилилирование кремневых кислот и
силикатов.
Гидролитическая поликонденсация
кремнийорганических мономеров.
Метод гидролитической поликонденсации широко используется для
синтеза силоксанов с Q - звеньями. Закономерности процессов, протекающих при
осуществлении этого метода, отражены в многочисленных публикациях.
Чтобы направить процесс в сторону образования
органорастворимых соединений, содержащих Q - звенья, приходиться прибегать к
таким приемам, как использование больших избытков воды, а также использование
растворителей, смешивающихся с водой.
Избежать гелеобразования при гидролитической поликонденсации
можно путем использования в качестве исходных мономеров вместо хлорсиланов -
алкоксисиланы [23].
Однако в последнее время появились работы по синтезу MQ -
смол ацидолизом алкоксисиланов в неводных средах [24]. В основе этого метода
лежит конденсация тетраэтоксисилана (или этилсиликата) с органоалкоксисиланами
в среде ледяной уксусной кислоты в присутствии кислотного катализатора [25]:
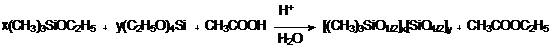
Гетерофункциональная поликонденсация кремнийорганических
мономеров.
Работы по получению MQ - силоксанов методом гетерофункциональной
конденсации начаты в США в конце 40 - х годов, а затем уже были продолжены в
других странах [1]. Так взаимодействием органосиланолятов натрия с
четыреххлористым кремнием по схеме 1 получены соответствующие тетракис
(триорганосилокси) силаны:
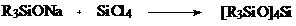
или

и далее
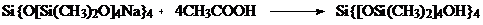
Схема 1.
с образованием регулярных олигомеров пространственного строения,
которые структурируются при нагревании свыше 230 оС.
В работе [26] соконденсацией триметилацетоксисилана с
тетраэтоксисиланом в присутствии соляной кислоты был получен тетракис
(триметилсилокси) силан с выходом 80%.

Данное соединение может быть получено и по реакции
четыреххлористого кремния и триметилсиланолята натрия, но выход его составляет
всего лишь 18% [26].
В патенте [27] предложен способ получения кремнийорганических MQ -
смол на основе гексаорганодисилоксана общей формулы [R1R2Si]
2O, где R = - CH3; R1 = - CH3; - C6H5;
- CH=CH2 или его смеси с органоалкоксисиланами общей формулы RnSi
(OR1) 4-n, где R1 = - CH3; - C2H5;
n = 1, 2, 3 и продукта частичного гидролиза тетраэтоксисилана. Ацидолиз ведут в
присутствии каталитических количеств триметилхлорсилана. Данный способ, по
мнению авторов, исключает или значительно сокращает использование
алифатического спирта и расход уксусной кислоты, а также снижает образование
побочных продуктов.
В работе [28] были синтезированы MQ - смолы гидролитической
конденсацией смеси тетраэтоксисилана и триметилхлорсилана. Реакция представлена
на схеме 2:
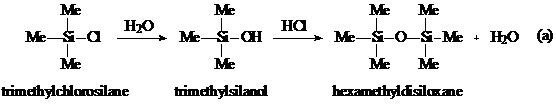
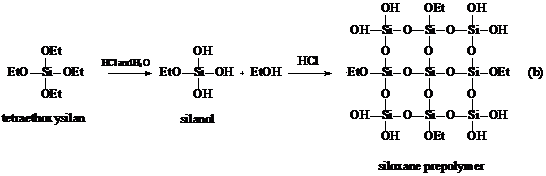

Схема 2.
Тетраэтоксисилан служит заготовкой Q - звеньев, а
триметилхлорсилан соответственно M - звеньев. Во время гидролиза
триметилхлорсилана образуется триметилсиланол, который реагирует с силоксановым
преполимером, но и конденсируется, образуя гексаметилдисилоксан. А полученный
гексаметилдисилоксан, в свою очередь, реагируя с соляной кислотой образует
триметилсиланол и триметилхлорсилан (схема 2 (а)). Силоксановая цепь образуется
после гидролиза тетраэтоксисилана (схема 2 (б)). Силоксановая смола с высокой
степью сшивки образуется в ходе конденсации силоксанового преполимера с
триметилсиланолом, конечная структура которой показана на схеме 2 (с).
Полученные этим способом MQ - смолы были использованы как составляющие клеев
чувствительных к давлению.
Триметилсилилирование силикатов и кремниевых кислот.
Методы триметилсилилирования (ТМС) силикатных материалов широко
известны, поскольку они используются не только для синтеза силоксанов, но также
для изучения структуры силикатов [29]. Особый интерес силоксанов представляют
многочисленные работы по триметилсилилированию кремневых кислот и растворимого
стекла [30].
Существует два метода триметилсилилирования силикатов: Метод Ленца
[31] и "Прямой" метод [32].
Метод Ленца заключается в следующем:
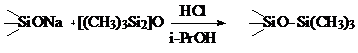
Схема 3.
Силикат суспензируют в воде в течении 1 часа, затем к 2 - х фазной
системе добавляют смесь льда, концентрированной соляной кислоты, пропан - 2 -
ола и гексаметилдисилоксана. Смесь перемешивают в течение 48 часов при
комнатной температуре и затем фильтруют. Фаза кислота - вода выщелачивает
катионы из силиката и образует кремниевую кислоту. Выход кремниевой кислоты
определяется количеством триметилсилилирующего агента, который образуется в
результате разложения гексаметилдисилоксана в присутствии соляной кислоты.
Пропан - 2 - ол используется для увеличения растворимости силилирующего агента
в воде.
Было обнаружено, что триметилсилилирование не всегда проходит до
конца, поэтому, в конечном продукте могут оставаться непрореагировавшие
силанольные группы. После дериватизации группы Si - OH были заблокированы путем
обработки исходного продукта ионообменной смолой Amberlyst 15 в присутствии
гексаметилдисилоксана. Метод триметилсилилирования позволяет определять
молекулярный размер силикатных анионов, при условии, что значение n не меняется
в ходе реакции. К сожалению, поликремниевая кислота в кислых растворах
подвержена равновесию: полимеризация / деполимеризация.
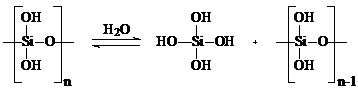
"Прямой" метод:
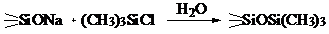
Схема 4.
В "прямом" методе Гоца и Мэйсона была осуществлена
попытка подавления побочных реакций. Для этого вместо соляной кислоты, воды и
гексаметилдисилоксана использовался триметилхлорсилан (схема 4). Этот метод
особенно применим к тем силикатам, которые содержат значительные количества
кристаллизационной воды. Этот метод метод Гоц и Мэйсон применили ранее на
[32,33,34] оливине и гемиморфите. Из оливина с 88% -ым выходом был получен QM4
- силоксан, из гемиморфита с 94% - ым выходом Q2M6 -
силоксан как и у оригинальных силикатных структур. Дент Глассер и Шарма [35,36]
применяли триметилсилилирование для исследований силиката натрия и пришли к
выводу, что метод Ленца является более подходящим, вероятно потому что большое количество
используемой соляной кислоты быстро снижает pH до точки где равновесные
процессы полимеризации - деполимеризации проходят относительно медленно.
Перечисленные процессы могут быть модифицированы частичной или
полной заменой триметилхлорсилана органофункциональными хлорсиланами
содержащими Si-H или Si-Vin группы с получением реакционноспособных MQ - смол.
Экспериментальная
часть
Исходные материалы и методы их очистки.
Очистку исходных материалов проводили по
известным методикам [37]
Толуол, технический продукт, очищали перегонкой при
атмосферном давлении, использовали фракцию с температурой кипения 110 0С
Пиридин сушили длительное время над КОН, а затем перегнали.
Использовали фракцию с температурой кипения 115 0С.
Триметилхлорсилан, технический продукт, очищали перегонкой,
использовали фракцию с температурой кипения 57 0С.
Пропионовый ангидрид, фирма FLUKA ANALYTICAL, чистота (≥
96,0%). Использовали без дополнительной очистки.
Уксусная кислота, технический продукт, очищали вымораживанием
(tпл. = 16 оС).
Этилацетат, технический продукт, очищали перегонкой под
атмосферным давлением, использовали фракцию с температурой кипения 77 оС.
Гексаметилдисилоксан. В 2-х горлую колбу, снабженную
магнитной мешалкой, термометром и капельной воронкой, загрузили 500 г (27,7
моль) H2O. Затем прикапали 256,1 г (1,6 моль) триметилхлорсилана.
После остывания смесь разделили на делительной воронке. Продукт промыли водой
до нейтральной реакции pH и отсутствия Cl-. Продукт сушили над
безводным сульфатом натрия.
Этилсиликат - 40, технический продукт, очищали от остаточных
этанола и тетраэтоксисилана на роторном испарителе с азотной ловушкой (60 оС/
1мм. рт. ст.).
Для осушки растворов использовали прокаленный сульфат натрия.
Для приготовления водных растворов использовали
дистиллированную воду.
Синтез MQ - смолы [смола А] (соотношение M: Q =
2:
) проводили по известной методике [38].
В 3-х горлую колбу, снабженную магнитной мешалкой,
термометром, обратным холодильником и капельной воронкой с обводным краном,
загрузили 3,3 г (20 ммоль) гексаметилдисилоксана, 3,0 г (20 ммоль) этилсиликата
- 40 и 0,07 г (0,65 ммоль) триметилхлорсилана.
Далее с помощью капельной воронки прикапали 3,3 г (20 ммоль)
уксусной кислоты, постепенно повышая температуру в реакционной массе до 40 - 50
оС. После ввода всего количества уксусной кислоты реакционную смесь
кипятили 3 часа.
После охлаждения к реакционной массе добавили 15 мл толуола.
Толуольный раствор промывали 5% -ым водным раствором NaHCO3, а затем
дистиллированной водой до нейтральной реакции.
Толуольный раствор сушили над безводным сульфатом натрия.
После чего отогнали растворитель и высушили продукт до постоянного веса.
Выделено 3,24 г (72,8 %) бесцветного вязкого прозрачного
полимера.
Найдено (%): C, 30,38; Si, 37,81; H, 7,79.
Вычислено для [Si3O3C6H18]
(%): C, 32,4; Si, 37,9; H, 8,1.
Спектр ЯМР 1H (δ, м. д.): 0,18 (с, 9H, Si
(CH3) 3); 3,89 (м, 2H, - OCH2 - CH3);
1,31 (м, 3H, - OCH2 - CH3).
Спектр ЯМР 29Si (δ, м. д.): 8,54 ÷ 10,77 (M); - 103,62 ÷ - 93,86 (Q1 -
Q3); - 113,9 ÷ - 106,1 (Q4).
Триметилсилилирование смолы А.
К смеси 3,0 г (27,0 ммоль) триметилхлорсилана, 2,3 г (28,6
ммоль) пиридина и 20 мл толуоладобавили раствор 1,2 г (5,4 ммоль) смолы А в 20
мл толуола. Смесь перемешивали при температуре кипения растворителя в течении 2
часов. После охлаждения к полученной смеси добавили 15 мл дистиллированной воды
и 2,5 мл концентрированной соляной кислоты. Смесь разделили на делительной
воронке. Толуольный раствор промыли водой до отсутствия реакции на Cl-.
Толуольный раствор сушили над безводным сульфатом натрия. После чего отогнали
растворитель и высушили продукт до постоянного веса. Выделено 1,07 г (87%
выход) бесцветного прозрачного вязкого полимера.
Найдено (%): С, 31,05; Si, 37,08; H, 7,73.
Вычислено для [Si3O3C6H18]
(%): C, 32,4; Si, 37,9; H, 8,1.
Спектр ЯМР 1H (δ, м. д.): 0,19 (с, 9H, Si
(CH3) 3); 3,89 (с, 2H, - OCH2 - CH3);
1,32 (c, 3H, - OCH2 - CH3).
Спектр ЯМР 29Si (δ, м. д.): 8,55 ÷ 10,2 (M); - 104,57 ÷ - 99,34 (Q1 -
Q3); - 113,76 ÷ - 105,1 (Q4).
Синтез MQ - смолы на основе этилсиликата - 40,
гексаметилдисилоксана и проипонового ангидрида [соотношение M: Q = 2: 1 (смола
Б)].
В трехгорлую колбу, снабженную магнитной мешалкой, обратным
холодильником и капельной воронкой с обводным краном загрузили 6,5 г (40 ммоль)
гексаметилдисилоксана, 7,8 г (60 ммоль) пропионового ангидрида и 0,714 г (5,25
ммоль) хлористого цинка. Смесь кипятили 1 час.
Затем прикапали 6,0 г (40 ммоль) этилсиликата - 40, кипятили
еще 1 час. После чего к охлажденной реакционной массе добавили 1 мл
концентрированной соляной кислоты и 2 мл дистиллированной воды и кипятили еще 5
часов.
После охлаждения смесь разделили на делительной воронке,
добавили 10 мл этилацетата, и промывали 5% - м раствором NaHCO3 и
дистиллированной водой до нейтральной реакции pH и отсутствия Cl-.
Этилацетатный раствор сушили над безводным сульфатом натрия. После чего
отогнали растворитель и высушили продукт до постоянного веса. Выделено 5,34 г
(60%) бесцветного прозрачного вязкого полимера.
Найдено (%): С, 28,94; Si, 38,17; H, 7,7.
Вычислено для [Si3O3C6H18]
(%): C, 32,4; Si, 37,9; H, 8,1
Спектр ЯМР 1H (δ, м. д.): 0,16 (c, 9H, Si
(CH3) 3); 1,89 (с, 2H, - OCH2 - CH3);
1,24 (c, 3H, - OCH2 - CH3).
Спектр ЯМР 29Si (δ, м. д.): 9,79 (M); - 105 ÷ - 97,5 (Q1 - Q3); - 108,28 (Q4).
Триметилсилилирование смолы Б.
К смеси 9,1 г (0,08 моль) триметилхлорсилана, 7,0 г (0,09
моль) пиридина и 20 мл толуола добавили раствор 3,74 г (0,02 моль) смолы Б в 20
мл толуола. Смесь перемешивали при температуре кипения растворителя в течении 2
часов. После охлаждения к полученной смеси добавили 15 мо дистиллированной воды
и 2,5 мл концентрированной соляной кислоты. Смесь разделили на делительной
воронке. Толуольный раствор промыли водой до отсутствия реакции на Cl-.
Толуольный раствор сушили над безводным сульфатом натрия. После чего отогнали
растворитель и высушили продукт до постоянного веса.
Выделено 3,55 г (94,2%) бесцветного вязкого прозрачного
полимера.
Найдено (%): C, 30,24; Si, 37,9; H, 7,73
Вычислено для [Si3O3C6H18]
(%): C, 32,4; Si, 37,9; H, 8,1
Спектр ЯМР 1H (δ, м. д.): 0,19 (c, 9H, Si
(CH3) 3); 3,86 (с, 2H, - OCH2 - CH3);
1,26 (c, 3H, - OCH2 - CH3).
Спектр ЯМР 29Si (δ, м. д.): 8,55 - 10,21
(M); - 104,57 ÷ - 99,35 (Q1 - Q3);
- 110,77 ÷ - 105,16 (Q4).
Обсуждение результатов.
Как упоминалось в литературном обзоре, области применения MQ
- смол достаточно широки. Однако, что касается структуры MQ - силоксанов, то
она окончательно не выяснена. В настоящее время принято считать, что молекулы
этих соединений построены из кластеров четырехфункциональных силикатных групп
(Q), обрамленных монофункциональными триметилсилокси группами (M).
Пространственная сильно сшитая структура MQ - смол характеризуется следующими
параметрами: соотношением M и Q - звеньев, молекулярной массой и содержанием Si
- OH и Si - OR - групп. Для количественного определения этих параметров
используют стандартные методы анализа: ЯМР 29Si и 1H -
спектроскопию, гельпроникающую хроматографию (ГПХ), ИК - спектроскопию.
Соответственно группы Si - OH и Si - OR присутствуют в
составе Q - звеньев. В зависимости от количества этих функциональных групп у
одного атома кремния различают звенья: Q1, Q2, Q3,
Q4 (см. рис.1) [39].
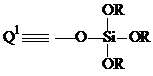
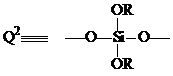
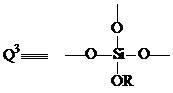
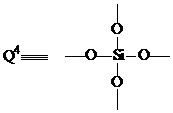
Рис. 1: Структуры звеньев Q1, Q2, Q3
и Q4, где R = H, Et
Как правило, традиционные методы синтеза MQ - смол, основанные на
гидролитической поликонденсации со - мономеров, приводят к образованию
полидисперсных продуктов с высоким содержанием этих функциональных групп.
Ввиду этого вызывает определенный интерес разработка методов
синтеза MQ - смол, обладающих меньшей дефектностью Q - звеньев и пониженной
полидисперстностью.
Для начала в нашей работе был воспроизведен синтез MQ - смолы,
приведенный в патенте [27], на основе гексаметилдисилоксана и продукта
частичного гидролиза тетраэтоксисилана (этилсиликат - 40) в среде уксусной
кислоты в присутствии каталитических количеств триметилхлорсилана. Соотношение
M: Q было выбрано 2:
. В результате был получен бесцветный вязкий прозрачный полимер
(смола А) с выходом 73%.
Данный продукт был исследован методами элементного анализа, ГПХ, а
также ЯМР 1H и 29Si спектроскопии.
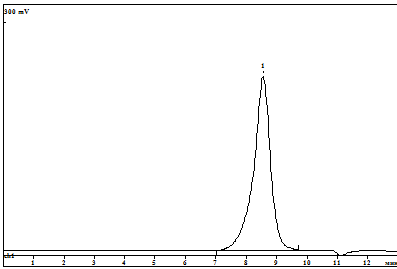
Рис. 2: Гель - хроматограмма смолы А.

Рис.3: ЯМР 1H - спектр смолы А.
Данные элементного анализа отвечают структурному звену { [SiO2]
[O0,5Si (CH3) 3] 2}. На гель -
хроматограмме (рис.2) видно унимодальное распределение со средневесовой молекулярной
массой = 1242, индекс полидисперстности = 1,2. По ЯМР 1H спектру
смолы А рассчитывали содержание остаточных этокси - групп в продукте, которое
составило 7,0%. По ЯМР 29Si - спектру оценивалось содержание
дефектных Q - звеньев (Q1, Q2, Q3).
По данным работы [39] химический сдвиг звеньев Q1, Q2,
Q3 и Q4 проявляются в областях - 89,0 ÷ - 89,2 м. д.; - 92,4 ÷ - 98,2 м. д.; - 99,2 ÷ - 106,6 м. д.; и - 106,8 ÷ - 114,0 м. д. соответственно.
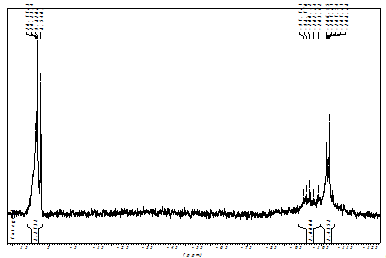
Рис.4: ЯМР 29Si - спектр смолы А.
На ЯМР 29Si смолы А присутствуют соответственно сигналы
Q2, Q3 и Q4 - звеньев. Процентное соотношение
Q2: Q3: Q4 составило соответственно: - 97,7 ÷ - 98,8 м. д.; - 100,3 ÷ - 103,6 м. д.; - 107 ÷ - 109,6 м. д. Общее количество дефектных
звеньев Q2 и Q3 в смоле 42%. Ввиду большого процента
дефектности Q - звеньев в продукте А была проведена реакция
"блокирования" силанольных групп при действии на них (CH3)
3SiCl (реакция триметилсилилирования) по известной методике [40,41]:

Реакцию проводили в среде толуола, в качестве акцептора хлористого
водорода использовали пиридин. В результате был получен бесцветный вязкий
прозрачный полимер с выходом 87%.
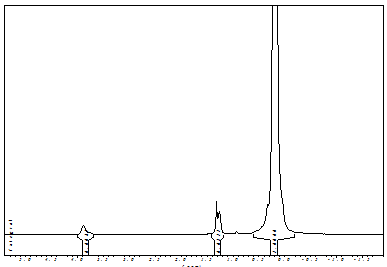
Рис. 5: ЯМР 1H - спектр триметилсилильного производного
смолы А.
Этот продукт был изучен методами элементного анализа, ГПХ, ЯМР 1H
и 29Si - спектроскопии.
Судя по спектру ЯМР 1H содержание остаточных алкокси -
групп осталось прежним 7,0% (рис. 5). На спектре ЯМР 29Si (рис.6)
триметилсилильного производного смолы А присутствуют сигналы звеньев Q3
и Q4. содержание дефектных звеньев Q3 составило 20,7%.
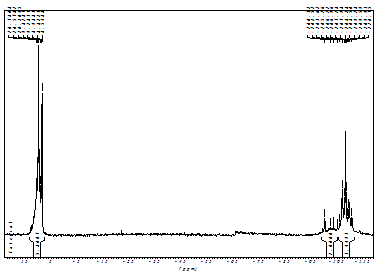
Рис.6: ЯМР 29Si - спектр триметилсилильного
производного смолы А.
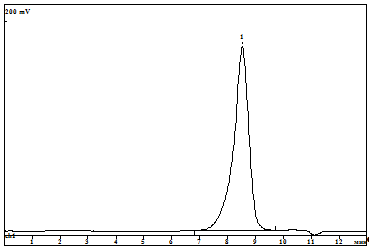
На гель - хроматограмме данного соединения так же наблюдается как
и в случае исходной смолы А унимодальное распределение. Средневесовая
молекулярная масса продукта триметилсилилирования смолы А составила 1198,
индекс полидисперстности = 1,2.
Таким образом "блокирование" функциональных групп
триметилхлорсиланом в смоле А позволило снизить содержание дефектных Q -
звеньев вдвое. Однако, степень дефектности Q - звеньев остается достаточно
большой.
Представляет интерес получать MQ - смолы с меньшим содержанием
дефектных Q - звеньев. Нами предложен иной метод получения MQ - силоксанов,
основанной на реакции гетерофункциональной поликонденсации. Известно, что алкил
(арил) алкоксисиланы в присутствии катализаторов вступают в реакцию ступенчатой
конденсации алкил (арил) ацетоксисиланами. В результате реакции образуются
низкомолекулярные продукты конденсации - органосилоксаны линейной структуры и
этилацетат [42,43,44]. В качестве катализатора реакции используется FeCl3,
AlCl3, толуолсульфокислота, соляная кислота и силонолят натрия.
Так же известно, что ангидриды карбоновых кислот в присутствии
ZnCl2, FeCl3, серной и хлорной кислот расщепляют
силоксановую связь в циклосилоксанах и гексаалкилдисилоксанах [45].
В данной работе в качестве объектов исследования были взяты
гексаметилдисилоксан, пропионовый ангидрид и хлористый цинк в качестве
катализатора.
Синтез MQ - смолы с соотношением M: Q = 2: 1 проводили следующим
образом. На первой стадии проводили расщепление гексаметилдисилоксана
пропионовым ангидридом в присутствии 5% масс. хлористого цинка (безводного) по
схеме:
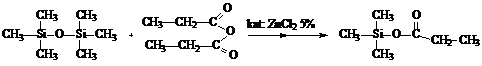
Схема №1
В результате реакции образовался триметилпропионоксисилан,
служащий "заготовкой" M - звена.
На второй стадии к полученному триметилпропионоксисилану добавляли
полиэтоксисилоксан (этилсиликат - 40) и проводили гетерофункциональную
конденсацию в течении 1 часа, в ходе которой получали форполимер.
На рис. № 8 приведен ЯМР 1H - спектр промежуточного
продукта (форполимера), полученного на второй стадии.
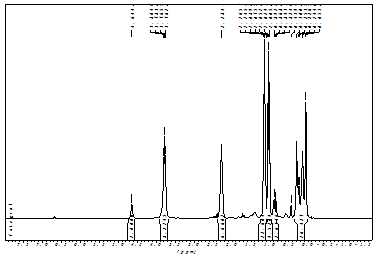
Рис. №8: ЯМР 1H - спектр промежуточного
триметилпропионоксисилана.
В пользу протекания гетерофункциональной конденсации служит
наличие сигналов протонов в области 0,05 ÷0,300 м. д., отвечающих группам - OSi (CH3)
3.
Далее к полученному форполимеру добавили 33 % - ную водный раствор
соляной кислоты и подвергали гидролитической поликонденсации в течении 5 часов.
В результате был получен бесцветный вязкий полимер (смола Б) с выходом 60%.
Продукт Б был исследован методами элементного анализа, ГПХ и ЯМР 1H
и 29Si - спектроскопии. Данные элементного анализа близки к звену {
[SiO2] [O0,5Si (CH3) 3] 2}:38,17
1,36 328,94 2,41 5,37,68 7,41 16,8
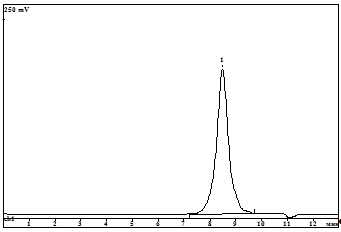
Рис.9: Гель - хроматограмма смолы Б.
На ГПХ продукта реакции наблюдается унимодальное распределение. Mw
= 1303,5. Mn/Mw = 1,16.
По данным ЯМР 1H - спектроскопии (рис.9) продукта Б
оказалось невозможным рассчитать количество остаточных этокси - групп.
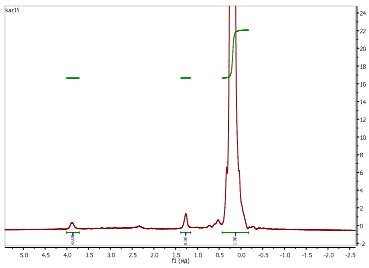
Рис.10: ЯМР 1H - спектр смолы Б.
На ЯМР 29Si - спектре присутствуют сигналы звеньев Q2,
Q3,Q4. соотношение их составило: Q2 = - 98,8 ÷ - 99,4; Q3 = - 100,3 ÷ - 104,6; Q4 = - 105,2 ÷ - 110,8. Общее количество дефектных
звеньев в продукте Б составило 24,7%.
По аналогии с продуктом А было проведено "блокирование"
дефектных звеньев QOH триметилхлорсиланом в среде толуола с
использованием акцептора HCl пиридина.
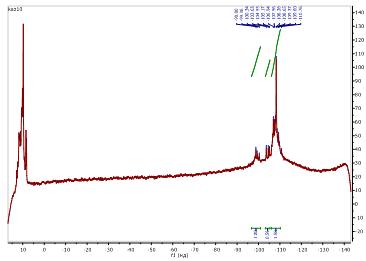
Рис.11: ЯМР 29Si - спектр смолы Б.
В результате был получен бесцветный вязкий прозрачный полимер с
выходом 94%. Триметилсилильное производное продукта Б было исследовано с
помощью элементного анализа, ГПХ и ЯМР 1H и 29Si -
спектроскопии. Содержание остаточных этокси - групп оказалось также соизмеримо
с погрешностью расчета по данным ЯМР 1H - спектроскопии.
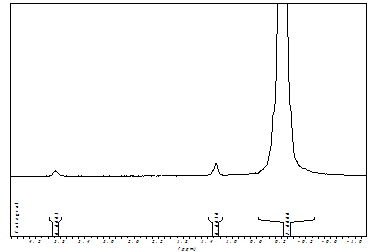
Рис.12: ЯМР 1H - спектр триметилсилильного производного
смолы Б.
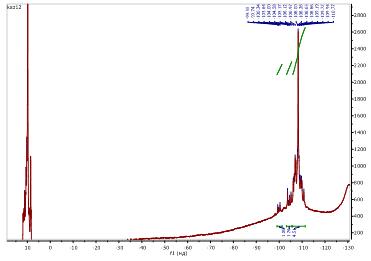
Рис.13: ЯМР 29Si - спектр триметилсилильного
производного смолы Б.
На ЯМР 29Si - спектре присутствуют сигналы звеньев Q2,
Q3,Q4. Соотношение их составило: Q2 = - 99,4 ÷ - 99,7: Q3 = - 100,1 ÷ - 104,6: Q4 = - 105,2 ÷ - 110,8. Общее количество дефектных
звеньев составило 16%.
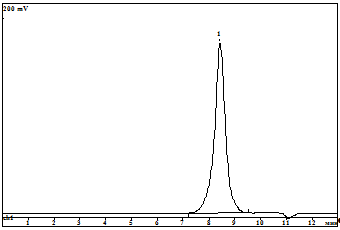
Рис.14: Гель - хроматограмма триметилсилильного производного смолы
Б.
На ГПХ триметилсилоксипроизводного продукта Б присутствует один
пик, отвечающий средневесовой молекулярной массе Mw = 1300,5 и
индексу полидисперсности Mn/Mw = 1,1.
Таким образом, по разработанной нами методике синтеза MQ - смолы
был получен продукт Б обладающий меньшим количеством дефектных Q - звеньев по
сравнению с продуктом А, полученным по методу синтеза из патента [46].
Триметилсилилированием продуктов А и Б удалось снизить содержание звеньев QOH.
Однако в случае продукта Б процент содержания дефектных Q - звеньев оказался
ниже.
Выводы
1. Впервые проведена реакция получения MQ - смол при
взаимодействии гексаметилдисилоксана, тетраэтоксисилана (этилсиликата - 40),
пропионового ангидрида и хлористого цинка.
2. Установлено, что при проведении реакции по известной
методике получается большое количество дефектных звеньев QOH, чем
при разработанной нами методике. Количество подтверждено ЯМР 29Si -
спектром.
Список
используемой литературы
1.
Молчанов Б.В., Чупрова Е.А., Чернышев Е.А. и др. Органосилоксаны, содержащие в
основной цепи структурные фрагменты двуокиси кремния // Обзорная информация:
Сер. Элементоорганические соединения и их применение. М.: НИИТЭХИМ, 1984.
.
Lewis L. N., Wengrovins J. H., Burnell T. B. et al. // Chem. Mater. 1997. N9.
P.761.
.
Молчанов Б.В., Виноградов С.В., Чупрова Е.А. Композиционные материалы на основе
олиготриорганосилоксисилоксанов // Обзорная информация: Сер.
Элементоорганические соединения и их применение. М.: НИИТЭХИМ, 1988., 37 с.
.
Encyclopedia of polymer science and engineering, vol.15, John Wiley & Sons,
New York, 1989.
.
Kirk - Othmer Encyclopedia of chemical technology, vol.22, John Wiley &
Sons, Inc.: New York, 1997.
.
Brook M. A. "Silicon in organic, organometallic, and polymer
chemistry", Wiley: New York, 2000.
.
Клеящие материалы. Герметики: Справ. /Под ред.А.П. Петровой. - СПб: НПО
"Профессионал", 2008, - 592 стр. ил.
.
Поциус А.В. /Клеи, адгезия, технология склеивания/ Пер. с англ. - СПб:
Профессия, 2007. - 376 стр. ил.
.
Айлер Р. Химия кремнезема: Пер. с англ.: В 2ч. Ч.1. М.: Мир, 1982.416 с.
.
Arkles B.commercial application of Sol - Gel - Derived Hybrid Materials // MRS
Balletin. 2001. N5. P.402.
.
Молчанов Б.В., Чупрова Е.А., Виноградов С.В., Донской А.А., Баритко Н.В. //
Модификация кремнийорганических эластомерных композиций MQ - смолами //
ВИАМ/2005 - 204337.
.
Молчанов Б.В., Ким Ван Док // Пласт. массы. 1997. №6. С.26
.
US 4535141. L. A. Kroupa // Liquid curable polyorganosiloxane compositions //
Aug.13, 1985.
.
G. Fabricius, G. Sundholm; JOURNAL OF APPLIED ELECTROCHEMISTRY 15 (1985)
797-801.
.
US 6054523. R. Braun, K. Braunsperger, H. Söllradl, S. Oberneder, R.
Braunsperger // Aqueous dispersions of organopolysiloxanes // Apr.25, 2000.
.
US 6274692. C. Herzig, O. Zoellner, F. Hockemeyer, R. Banfic // Cross -
linkable compounds, optionally containing MQ silicon resins // Aug.14,
2001.6187834. L. E. Thayer, J. S. Tonge, G. A. Vincent // Radiation curable
silicone compositions // Feb.13, 2001.
.
Kanner B. et. al. /J. Cell. Plastics 1979, N11/12, 315 - 320
.
US 5082590. C. Araud // Polydimethylsiloxane / MQ resins antifoaming
compositions // Jan.21, 1992.
.
US 3541205. W. D. Hardigan, L. F. Stebleton // Wash resistant lotion containing
organosilicon resins // Nov.17, 1970. 5496544. M. Mellul, S. Lecomte, I. Bara,
B. DeFossez // Powdered cosmetic composition containing a silicone fatty binder
// Mar.5, 1996. 5800816. H. Brieva, J. G.russ, I. M. Sandewicz // Cosmetic
composition // Sep.1, 1988.
.
Коваленко С.И. и др." Разработка и исследование свойств
кремнийорганической основы антиадгезионного разделительного средства",
Тезисы докладов ч.2, с. 200, VII Всесоюзная конференция по химии, технологии
производства и практическому применению кремнийорганических соединений,
Тбилиси, 1990 г.
.
US 6211307. Motoaki Iwabuchi, Masaaki Yamaya // Organopolysiloxane composition
for forming fired film // Apr.3, 2001.
.
Магомедов Г. К - И., Чернышев Е.А., Морозова Л.В. и др. // Металлоорганическая
химия. 1992. Т.5. №1.
.
US 2857356. John T. Goodwin // Organopolysiloxane compositions having pressure
- sensitive adhesive properties // Oct.21, 1958.6881355. M. Hafner, G.
Stockbauer, O. Pfueller, A. Stankowiak // Antifreeze // Apr. 19, 2005.
.
E. V. Egorova, N. G. Vasilenko, N. V. Demchenko, E. A. Tatarinova, A. M.
Muzafarov, 2009, published in Doklady Nauk, 2009, vol.424, No.2, pp. 200 - 204.
.
Андрианов К.А. // В кн.: Полимеры с неорганическими главными цепями. 1962.
Москва, Академия Наук СССР, с.157 - 165.
.
L. Sommer, J. Amer. Chem. Soc.71, 3253 (1949).
.ru
2384591. Чупрова Е.А., Виноградов С.В., Поливанов А.Н. // способ получения
кремний органических смол // 5.11.2005.
.
Applied Polymer; Chung - Feng J. Kuo, Jiong - Bo Chen, Chung - Yang Shin, Chao
- Yang Huang. Dec.13, 2013
.
Currell B. R., Parsonage J. R. - J. Macromol. Sci. Chem., 1981, v. A16,
№1,p.141; Calhonn H. P., Masson C. R. - Rev. Sil. Germ. Tin. Lead Compounds,
1981, v.5, №4, p.153; Hoebbel D. "Inorg.organ. Polymers”, - Eur. Water
Res. Soc., 1992, 5 (EUROGEL’91), 467; Abe Y., Misono T., - Chem. Soc. Japan,
1981, v.7.
.
Kohama Sh. - Kagaku to Kogyo (Osaka), 1981, v.55, № 9, p.326; Kajiwara M.,
Yamamoto N. - Polymer Commun., 1983, v.24, № 5, p.150.
.
C. W. Lentz, Inorganic Chemistry, 3, 574 (1964)
.
J. Gotz and C. R. Masson, J. Chem. Soc., (A), 2683 (1970)
.
F. Wu, J. Gotz, W. D. Jamieson and C. R. Masson, J. Chromatog., 48, 515 (1970)
.
S. K. Sharma, L. S. Dent Glasser and C. R. Masson, J. C. S. (Dalton), 1324
(1973)
.
L.S. Dent Glasser and S. K. Sharma, Brit. Polymer. J., 6, 283 (1974)
.
А. Гордон, Р. Форд // Спутник химика. М. МИР. 1976.
.2384591
(13) С, авторы: Чупрова Е.А., Виноградов С.В., Поливанов А. Н.
.
J. Polymer Science, 2003, p.2250, YOSHIMATO ABE et. al.
.
Н.В. Сергиенко, Н.В. Черкун, В.Д. Мякушев, Б.Г. Завин. Взаимодействие 3d
- металлоорганосилоксанов с ацетилацетоном // Изв. АН, Сер. Хим., 2010, №7,
1340
.А.С.
№ 1122748 (1966), К.А. Андрианов, Г.Л. Слонимский, В.С. Папков, С.Е. Якушкина.
.
К.А. Андрианов, Н.Н. Соколов и Е.Н. Хрусталева.Ж. Орган. Химии, 26, 1102
(1956).
.
W. J. Huggorty, L. Breed. Chem. №7, 2464 (1961)
44.
К.А. Андрианов, А.К. Дабагова и Ж.С. Сырцова. Изв. АНСССР, ОХН; 1962, №9,
с.1572.
.
М.Г. Воронков, В.П. Милешкевич, Ю.А. Южелевский. "Силоксановая
связь", НАУКА. 1976.
.2384591
(13) С1. Чупрова Елена Александровна, Виноградов Сергей
Владимирович, Поливанов Александр Николаевич;