Жидкие гетерогенные системы. Кинетическая агрегативная и конденсационная устойчивость гетерогенных систем.
РЕФЕРАТ
На
тему: Жидкие гетерогенные системы. Кинетическая агрегативная и конденсационная
устойчивость гетерогенных систем
План
Введение
. Жидкие гетерогенные
системы
1.1 Суспензии
1.2 Эмульсии
1.3 Пены
. Кинетическая, агрегативная
(конденсационная) устойчивость гетерогенных систем
2.1 Кинетическая
устойчивость
2.2 Агрегативная
устойчивость
Литература
Введение
Неоднородной,
или гетерогенной, считается система, которая состоит из двух или
нескольких фаз. Каждая фаза имеет свою поверхность раздела, которую можно
механически разделить.
Неоднородная система состоит из дисперсной
(внутренней) фазы и дисперсионной (внешней) среды, окружающей частицы
дисперсной фазы.
Системы, в которых внешней фазой являются
жидкости, называются неоднородными жидкими системами, а системы, в
которых внешней фазой являются газы, - неоднородными газовыми системами.
Гетерогенные системы часто называют дисперсными системами.
.
Жидкие гетерогенные системы
ЖГС делятся на следующие три класса:
Суспензии-системы, состоящие из жидкой
дисперсионной среды и твердых взвешенных в ней частиц.
Эмульсии-системы, состоящие из жидкой
дисперсионной среды и взвешенных в ней жидких частиц одной или нескольких
других жидкостей.
Пены-системы, состоящие из жидкой дисперсионной
среды и взвешенных в ней частиц газов.
.1 Суспензии
Суспе́нзия
(от лат. suspensio, подвешивание) - смесь веществ, где твёрдое вещество
распределено в виде мельчайших частиц в жидком веществе во взвешенном
(неосевшем) состоянии.
Из всех трех классов жидких неоднородных смесей
в технике наиболее часто встречаются суспензии. Суспензии могут различаться по
количеству дисперсной твердой фазы и по степени ее дисперсности, т. е. по
концентрации и величине взвешенных твердых частиц.
Суспензия - это грубодисперсная система с
твёрдой дисперсной фазой и жидкой дисперсионной средой. Обычно частицы
дисперсной фазы настолько велики (более 10 мкм), что оседают под действием силы
тяжести (седиментируют). Суспензии, в которых седиментация идёт очень медленно
из-за малой разницы в плотности дисперсной фазы и дисперсионной среды, иногда
называют взвесями. В концентрированных суспензиях легко возникают дисперсные
структуры. Типичные суспензии - пульпы, буровые промывочные жидкости, цементные
растворы, эмалевые краски. Широко используются в производстве керамики.
Суспензии лекарственных веществ готовят двумя
методами:
· дисперсионным (в основе метода лежит
принцип получения определенной степени дисперсности путем измельчения
порошковидного лекарственного вещества);
· конденсационным (в основе способа -
соединение молекул в большие доли - агрегаты, характерные для суспензий).
Общие правила приготовления суспензий
. Водные суспензии с концентрацией лекарственных
веществ 3% и больше, готовят по массе.
. Суспензии с гидрофильными веществами готовят,
путем растирания последних в ступке сначала в сухом состоянии, а затем по
правилу Дерягина (0,4-0,6 г жидкости на 1 г вещества).
. Если в прописи есть вязкая жидкость (сироп,
глицерин), то сухие вещества растирают с этими средствами.
. Суспензии с веществами, которые имеют большой
удельный вес (висмута нитрат основной) готовят методом взбалтывания.
. Суспензии с гидрофобными веществами готовят с
использованием стабилизаторов, количество которых зависит вот свойств веществ.
. Серу можно диспергировать с глицерином или со
спиртом этиловым в зависимости вот состава препарата.
. Из водорастворимых веществ, которые входят в
состав суспензий, сначала готовят раствор (можно использовать концентрированные
растворы), которым в дальнейшем разводят полученную по правилу Дерягина пульпу.
. Суспензии не процеживают в отличие от
эмульсий.
. Настойки, сиропы, жидкие экстракты, добавляют
к готовым суспензиям и эмульсиям.
Агрегативная устойчивость суспензии (способность
частиц сохранять свои первоначальные размеры, не слипаться) зависит от
плотности поверхностного электрического заряда частиц, их потенциала (потенциал
Штерна), толщины двойного электрического слоя, интенсивности взаимод. частиц со
средой (лиофильности суспензии). Понижение этих параметров приводит к потере
агрегативной устойчивости. Осаждение частиц из суспензии (разделение фаз) может
быть значительно ускорено путем их укрупнения в результате коагуляции
(флокуляции) при введении в суспензию электролитов (флокулянтов), под действием
электрического поля, магнитного или электромагнитного полей, жесткого
ионизирующего излучения, теплового воздействия. Осадки, образующиеся из
коагулированных суспензий, являются более рыхлыми, имеют больший
седиментационный объем, чем осадки, получаемые из агрегативно устойчивых
суспензий. Процессы разделения суспензий реализуются, напр., при очистке
сточных вод в различного типа отстойниках, фильтрах, флотаторах, гидроциклонах
и центрифугах. Суспензии широко
применяются в химической, цементной, силикатной, керамической, горной, металлургической,
бумажной, текстильной, пищевой, кожевенной и других областях промышленности.
Так, с суспензиями имеют дело при растворении солей, выщелачивании,
электрофоретическом осаждении твердой фазы при получении декоративных,
антикоррозионных и электроизоляционных покрытий, полупроводниковых пленок,
электрофоретических. дисплеев. В природных условиях образование суспензий
происходит при диспергировании почв, грунтов и скальных пород под воздействием
сил прибоя, приливно-отливных явлений, при движении ледников, в результате
выветривания и выщелачивания, при загрязнении водоемов атмосферной пылью. В
медицине суспензии используют для внутреннего и наружного применения, а также
для инъекций.
1.2 Эму́льсия
Эму́льсия
(новолат.
emulsio; от лат. emulgeo - дою, выдаиваю) - дисперсная система, состоящая из
микроскопических капель жидкости (дисперсной фазы), распределенных в другой
жидкости (дисперсионной среде).
Эмульсии могут быть образованы двумя любыми
несмешивающимися жидкостями; в большинстве случаев одной из фаз эмульсий
является вода, а другой - вещество, состоящее из слабополярных молекул
(например, жидкие углеводороды, жиры). Например, молоко - одна из первых
изученных эмульсий: в нём капли молочного жира распределены в водной среде.
Эмульсии относятся обычно к грубодисперсным
системам, поскольку капельки дисперсной фазы имеют размеры от 1 до 50 мкм.
Эмульсии низкой концентрации - неструктурированные жидкости.
Высококонцентрированные эмульсии - структурированные системы.
Тип эмульсии зависит от состава и соотношения ее
жидких фаз, от количества и химической природы эмульгатора, от способа
эмульгирования и некоторых других факторов.
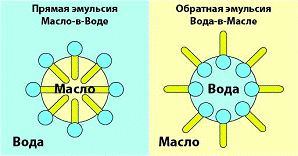
· Прямые, с каплями неполярной
жидкости в полярной среде (типа "масло в воде")
Для эмульсий типа м/в хорошими эмульгаторами
могут служить растворимые в воде мыла (натриевые и калиевые соли жирных
кислот). Молекулы этих соединений, адсорбируясь на поверхности раздела фаз, не
только снижают поверхностное натяжение на ней, но благодаря закономерной
ориентации в поверхностном слое создают в нем пленку, обладающую механической
прочностью и защищающей эмульсию от разрушения.
· Обратные, или инвертные (типа
"вода в масле")
Для эмульсии типа в/м хорошими эмульгаторами
могут быть нерастворимые в воде мыла (кальциевые, магниевые и алюминиевые соли
жирных кислот).
Изменение состава эмульсий или внешнее
воздействие могут привести к превращению прямой эмульсии в обратную или
наоборот.
Эмульсии образуются двумя путями:
· путём дробления капель.
Этот метод осуществляется путём медленного
прибавления диспергируемого вещества в дисперсную систему в присутствии
эмульгатора при непрерывном и сильном перемешивании. Главными факторами, от
которых зависит степень дисперсности частиц получаемой эмульсии и её устойчивость,
является скорость перемешивания, скорость введения диспергируемого вещества,
его количество, природа эмульгатора и его концентрация, температура и pH среды.
· путём образования плёнок и их
разрыва на мелкие капли.
Механизм образования состоит в следующем.
Жидкость, образующая дисперсную фазу (например, масло), при медленном
прибавлении к дисперсионной среде образует плёнку. Эта плёнка разрывается
пузырьками воздуха, выходящими из отверстия трубки, которые находятся на дне
сосуда. Образуются мелкие единичные капли. Одновременно пузырьки воздуха
энергично размешивают всю жидкость и этим самым способствуют
дальнейшему
эмульгированию. В настоящее время для получения концентрированной эмульсии
масла с водой её подвергают действию ультразвука.
Эмульсии широко используют в различных отраслях
промышленности:
v Пищевая промышленность (сливочное масло,
маргарин);
v Мыловарение;
v Переработка натурального каучука;
v Строительная промышленность (битумные материалы,
пропиточные композиции);
v Автомобильная промышленность (получение
смазочно-охлаждающих жидкостей);
v Сельское хозяйство (пестицидные препараты);
v Медицина. Эмульсии используют для внутреннего и
наружного применения, а также для инъекций.
v Живопись.
1.3 Пены
Пе́на
- дисперсная система с газовой дисперсной фазой и жидкой или твёрдой
дисперсионной средой.
Пены по своей природе близки к концентрированным
эмульсиям, но дисперсной фазой в них является газ, а не жидкость. Пены получают
из растворов поверхностно-активных веществ. Для повышения их устойчивости в
растворы ПАВ добавляют высокомолекулярные вещества, повышающие вязкость
растворов. В качестве характеристик пены используется комплекс свойств,
всесторонне характеризующих пену.
ü Пенообразующая способность раствора
- количество пены, выражаемое её объёмом (смі) или высотой столба (м), которое
образуется из заданного постоянного объема пенообразующего раствора при
соблюдении некоторых стандартных условий пенообразования в течение постоянного
времени.
ü Кратность пены, которая представляет
собой отношение объёма пены к объёму раствора, пошедшего на её образование.
ü Дисперсность пены, которая может
быть охарактеризована средним размером пузырьков, распределением их по размерам
или поверхностью раздела "раствор-газ" в единице объёма пены.
Для пен, особенно высокократных, характерна
ячеистая пленочно-каналовая структура, в которой заполненные газом ячейки
разделены тонкими плёнками. Три плёнки, расположенные под углом 120°, сливаются
в канал, четыре канала с углом между ними около 109° образуют узел. Наиболее
типичной формой ячейки в монодисперсной пене является пентагональный додекаэдр
(двенадцатигранник с пятиугольными гранями), часто с 1-3 дополнительными
гранями; среднее число плёнок, окружающих ячейку, обычно близко к 14. В
низкократной пене форма ячеек близка к сферической и размер плёнок мал.
В ряде случаев практического применения пен
важны такие их свойства, как вязкость, теплопроводность, электропроводность,
оптические свойства и т. д. Пены находят широкое применение во многих отраслях
промышленности и в быту:
· В быту: пенные моющие средства для
ванн, чистки ковров и мебели.
· В пожаротушении: при возгорании
ёмкостей с легко воспламеняющимися жидкостями, при тушении пожаров в закрытых
помещениях - в подвалах, на судах и в самолётах.
· В строительстве: устройство кровли,
гидроизоляция и утепление фундаментов, звукоизоляция стен.
· В горнорудной промышленности:
использование пенной флотации для обогащения полезных ископаемых;
предотвращение промерзания полигонов для добычи полезных ископаемых открытым
способом в условиях Крайнего Севера; изготовление взрывоустойчивых и
изолирующих перемычек в шахтах и рудниках.
· В отделке текстильных материалов.
· В кулинарии: кондитерские пены,
муссы, торты, бисквиты и др.
Пены с твёрдыми тонкими стенками (аэрогели,
пенопласты) широко используются для изготовления тепло- и звукоизолирующих
материалов, спасательных средств, упаковки и другие.
.
Кинетическая агрегативная и конденсационная устойчивость гетерогенных систем
суспензия устойчивость
гетерогенный кинетический
Для гетерогенных систем характерна кинетическая
(седиментационная) и агрегативная (конденсационная) устойчивость.
2.1 Кинетическая
устойчивость
Кинетическая устойчивость
- это способность дисперсной системы сохранять равномерное распределение частиц
по всему объему (или массе) лекарственной формы. Частицы под действием силы
тяжести опускаются на дно или всплывают в зависимости от относительных
плотностей дисперсионной среды и дисперсной фазы.
Кинетическая устойчивость описывается формулой
Стокса:
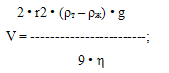
Где,- скорость оседания частиц, м/с;- радиус
частиц, м;
ρт
- плотность дисперсной фазы, г/м3;
ρж
- плотность дисперсионной среды, г/м3;
η - вязкость среды, Па
• с;- ускорение свободного падения, м/с2;
Кинетическая устойчивость прямо пропорциональна
вязкости среды. Чем больше вязкость, тем выше устойчивость гетерогенной
системы, следовательно для придания устойчивости системе необходимо вводить
вещества повышающие вязкость среды: сиропы, глицерин и др. Кинетическая
устойчивость обратно пропорциональна радиусу частиц: чем меньше радиус, тем
больше устойчивость. Малый размер частиц обуславливает их большую удельную
поверхность, что приводит к увеличению свободной поверхностной энергии.
Δ F = Δ S • δ
Где,
Δ F - изменение свободной
поверхностной энергии, Н/м;
Δ S - изменение
поверхности, м2;
δ - поверхностное
натяжение, Н/м.
Измельчать частицы до бесконечно малых размеров
невозможно, так как свободная поверхностная энергия стремится к минимуму.
Уменьшение свободной поверхностной энергии может происходить за счет агрегации
частиц, поэтому на границе раздела фаз частицы, как правило, стабилизируют.
Формула Стокса применима к идеальным системам, содержащим частицы строго
шаровидной формы, абсолютно твердые и гладкие. Реальные суспензии не
удовлетворяют этим требованиям, поэтому формула Стокса, не отражающая явления
на границе раздела фаз, носит приближенный характер, так как самопроизвольно
протекают процессы, направленные на уменьшение запаса свободной энергии. Внешне
это проявляется слиянием частиц или их слипанием.
2.2 Агрегативная
устойчивость
Агрегативная устойчивость
- это способность частиц дисперсной фазы противостоять слипанию, агрегации,
слиянию. При большом запасе свободной поверхностной энергии в суспензиях может
происходить процесс флокуляции (от лат. flocke - хлопья). Флокулы способны
оседать или всплывать, то есть нарушение агрегативной устойчивости приводит к
нарушению кинетической устойчивости. Система восстанавливает свои свойства при
взбалтывании. При образовании кристаллоподобных осадков систему нельзя
восстановить взбалтыванием, частицы не сохраняют свою индивидуальность. Процесс
образования конденсата - процесс необратимый. В эмульсиях может происходить
коалесценция, то есть слияние капелек друг с другом, образуется два слоя -
эмульсия расслаивается. Для того, чтобы эмульсия сохранила агрегативную
устойчивость, необходимо сохранить достигнутую степень дисперсности, понизив
величину поверхностного натяжения. Практически это можно осуществить с помощью
веществ, способных адсорбироваться на поверхности раздела фаз.
Агрегативная устойчивость обусловлена
способностью дисперсных систем образовывать агрегаты (т.е. укрупняться). По
отношению к агрегации дисперсные системы могут быть устойчивыми кинетически и
термодинамически. Термодинамически устойчивые системы образуются в результате
самопроизвольного диспергирования одной из фаз, т.е. самопроизвольного
образования гетерогенной свободнодисперсной системы. Дисперсные системы также
делят на:
ü лиофильные, обладающие
термодинамической устойчивостью;
ü лиофобные, которые термодинамически
неустойчивы к агрегации, но могут быть устойчивы кинетически, т.е. обладать
значительным временем жизни.
Агрегативная устойчивость и длительное существование
лиофобных дисперсных систем с сохранением их свойств обеспечивается
стабилизацией. Для высокодисперсных систем с жидкой дисперсионной средой
используют введение веществ - стабилизаторов (электролитов, ПАВ, полимеров. В
теории устойчивости Дерягина-Ландау-Фервея-Овербека (теории ДЛФО) основная роль
отводится ионно-электростатическому фактору стабилизации. Стабилизация
обеспечивается электростатическим отталкиванием диффузных частей двойного
электрического слоя, который образуется при адсорбции ионов электролита на
поверхности частиц. При некотором расстоянии между частицами отталкивание
диффузных слоев обусловливает наличие минимума на потенциальной кривой
(дальний, или вторичный, минимум; смотри рисунок). Хотя этот минимум
относительно неглубок, он может препятствовать дальнейшему сближению частиц,
притягиваемых силами межмолекулярного взаимодействия. Ближний, или первичный,
минимум соответствует прочному сцеплению частиц, при котором энергии теплового
движения недостаточно для их разъединения. Сближаясь на расстояние, отвечающее
этому минимуму, частицы объединяются в агрегаты, образование которых ведет к
потере системой агрегативной устойчивости. При этом устойчивость системы к
коагуляции определяется высотой энергетического барьера.
Агрегативная устойчивость, как и кинетическая,
является самостоятельной характеристикой лиофобных коллоидов. Разумеется, обе
характеристики устойчивости внутренне связаны между собой: агрегативная
устойчивость имеет смысл только для кинетически устойчивых систем, а кинетическая
устойчивость быстро утрачивается в агрегативно неустойчивой системе. Химические
и структурномеханические свойства адсорбционных слоев в значительной мере
определяют поведение лиофобных коллоидных систем. Эти слои могут быть
образованы или изменены небольшими количествами веществ, поэтому создаются
возможности регулирования ряда свойств лиофобных коллоидов, что широко
используется в различных практических приложениях.
Литература
. "Высококонцентрированные
дисперсные системы" Урьев Н. Б., 1980
. "Капиллярная
химия" под ред. К. Тамару, пер. с япон., М., 1983
. "Коагуляционные
контакты в дисперсных системах", 1982
. "Коллоидная химия.
Избранные труды", 1978;
. "Коллоидная
химия" Щукин Е. Д., Перцов А. В., Амелина Е. А.,1982
. "Поверхностные
явления в дисперсных системах" Ребиндер П. А.
. "Успехи химии"
Дерягин Б. В.,1979, т. 48, в. 4, с. 675-721,