Устройство для измерения скорости распространения пульсовой волны кровотока
Федеральное
агентство по образованию
Государственное
образовательное учреждение высшего профессионального образования
«Курский
государственный технический университет»
Кафедра
«Биомедицинская инженерия»
КУРСОВОЙ
ПРОЕКТ
по дисциплине
«Проектирование диагностической и терапевтической техники»
на тему
«Устройство для измерения скорости распространения пульсовой волны кровотока»
Автор работы Аунг Ко Ко У.
Биомедицинская инженерия
Группа БМ-85М
Руководитель работы Кузьмин А.А.
Курск, 2009
г.
Содержание
Введение
. Анализ проблемы
.1 Определение скорости распространения пульсовой волны
.2 Исследование особенностей сфигмограммы и скорости распространения
пульсовой волны по крупным артериальным сосудам
.3 Анализ существующих устройств для регистрации и измерения параметров
пульсовой волны
. Обоснование структурной схемы устройства
. Выбор элементной базы и расчет основных элементов и узлов
. Расчет блока питания и потребляемой мощности
Заключение
Список литературы
Введение
Одна из основных задач современной кардиологии -
снижение сердечно-сосудистой заболеваемости и смертности. Среди стратегий ее
решения - выявление групп высокого риска для проведения профилактических
медикаментозных и немедикаментозных вмешательств. В качестве инструмента для
оценки риска развития сердечно-сосудистых заболеваний (ССЗ) широко используют
различные шкалы (SCORE, Фрамингемская шкала и др.). Однако практически все они
предназначены для общей популяции и не могут быть использованы для пациентов с
уже манифестировавшими ССЗ.
Возможность предсказания развития повторных
сердечно-сосудистых осложнений (ССО) у пациентов с ишемической болезнью сердца
(ИБС) может способствовать формированию эффективной стратегии ведения этой
когорты больных. Поиск надежных способов оценки прогноза продолжается.
Роттердамское исследование показало высокую связь повышенной скорости пульсовой
волны (СПВ) - как маркера жесткости артерий - с наличием атеросклероза. Это
стало предпосылкой к изучению данного параметра как предиктора прогноза для
пациентов с ИБС.
1. Анализ проблемы
.1 Определение скорости
распространения пульсовой волны
В момент систолы некоторый объем крови поступает в
аорту, давление в начальной части ее повышается, стенки растягиваются. Затем
волна давления и сопутствующее ее растяжение сосудистой стенки распространяются
дальше к периферии и определяются как пульсовая волна. Таким образом, при
ритмическом выбрасывании крови сердцем в артериальных сосудах возникают
последовательно распространяющиеся пульсовые волны. Пульсовые волны распространяются
в сосудах с определенной скоростью, которая, однако, отнюдь не отражает
линейной скорости движения крови. Эти процессы в принципе различны. Сали (Н.
Sahli) характеризует пульс периферических артерий как «волнообразное движение,
которое происходит вследствие распространения образующейся в аорте первичной
волны по направлению к периферии».
Определение скорости распространения пульсовой волны,
по мнению многих авторов, является наиболее достоверным методом изучения
упруговязкого состояния сосудов.
Сфигмограммы периферического пульса используются для
определения скорости распространения пульсовой волны. Для этого
синхронно регистрируют сфигмограммы сонной, бедренной и лучевой артерий и
определяют время запаздывания периферического пульса по отношению к
центральному (Dt) (рис. 1).
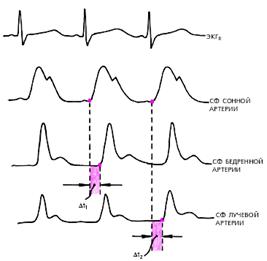
Рис.
1. Определение скорости распространения пульсовой волны на отрезках: «сонная -
бедренная артерии» и «сонная - лучевая артерии». Дельта-t1 и дельта-t2 -
запаздывание пульсовой волны соответственно на уровне бедренной и лучевой
артерий
Для
определения скорости распространения пульсовой волны производится одновременная
запись сфигмограмм с сонной, бедренной и лучевой артерий (рис. 2). Приемники
(датчики) пульса устанавливаются: на сонной артерии- на уровне верхнего края
щитовидного хряща, на бедренной артерии- в месте выхода ее из-под пупартовой
связки, на лучевой артерии- в месте пальпации пульса. Правильность наложения
датчиков пульса контролируется положением и отклонениями «зайчиков» на
визуальном экране прибора.
Если
одновременная запись всех трех пульсовых кривых по техническим причинам
невозможна, то одномоментно записывают сначала пульс сонной и бедренной
артерий, а затем сонной и лучевой артерий. Для расчета скорости распространения
пульсовой волны нужно знать длину отрезка артерии между приемниками пульса.
Измерения длины участка, по которому распространяется пульсовая волна в
эластических сосудах (Lэ) (аорта- подвздошная артерия), производятся в
следующем порядке (рис. 2):
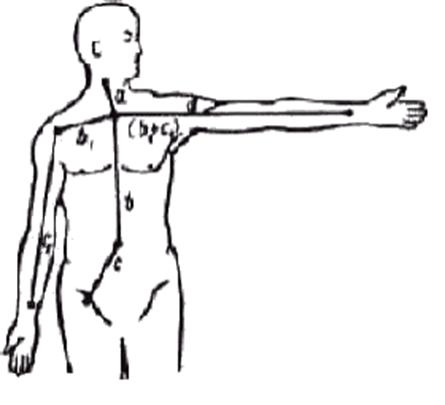
Рис.
5. Определение расстояний между приемниками пульса - «датчиками» (по В. П.
Никитину).
Обозначения
в тексте:
а-
расстояние от верхнего края щитовидного хряща (местоположение приемника пульса
на сонной артерии) до яремной вырезки, где проецируется верхний край дуги
аорты;расстояние от яремной вырезки до середины линии, соединяющей обе spina
iliaca anterior (проекция деления аорты на подвздошные артерии, которая при
нормальных размерах и правильной форме живота точно совпадает с пупком);
с-
расстояние от пупка до местоположения приемника пульса на бедренной артерии.
Полученные
размеры b и с складываются и из их суммы вычитается расстояние а:
b+с-а
= LЭ.
Вычитание
расстояния а необходимо в связи с тем, что пульсовая волна в сонной артерии
распространяется в противоположном к аорте направлении. Ошибка в определении
длины отрезка эластических сосудов не превышает 2,5-5,5 см и считается
несущественной. Для определения длины пути при распространении пульсовой волны
по сосудам мышечного типа (LМ) необходимо измерить следующие расстояния:
от
середины яремной вырезки до передней поверхности головки плечевой кости (61);
от
головки плечевой кости до места наложения приемника пульса на лучевой артерии
(а. radialis)- с1.
Более
точно измерение этого расстояния производится при отведенной под прямым углом
руке - от середины яремной вырезки до местоналожения датчика пульса на лучевой
артерии- d(b1+c1).
Как
и в первом случае, из этого расстояния необходимо вычесть отрезок а. Отсюда:
+
с1 - а - Lи, но b + с1 = d
или
- а = LM
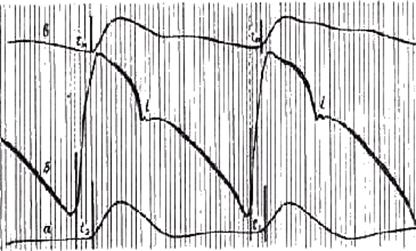
Рис.3. Определение времени
запаздывания пульсовой волны по началу подъема восходящего колена кривых (по В.
П. Никитину)
Обозначения:
а- кривая бедренной артерии;
б- кривая сонной артерии;
в- кривая лучевой артерии;э-
время запаздывания по эластическим артериям;м- время запаздывания по мышечным
артериям;инцизура
Второй величиной, которую
необходимо знать для определения скорости распространения пульсовой волны,
является время запаздывания пульса на дистальном отрезке артерии по отношению к
центральному пульсу (рис. 3). Время запаздывания (г) определяется обычно по
расстоянию между началами подъема кривых центрального и периферического пульса
или по расстоянию между местами изгиба на восходящей части сфигмограмм.
Время запаздывания от начала
подъема кривой центрального пульса (сонной артерии- а. саrоtis) до начала
подъема сфигмографической кривой бедренной артерии (а. femoralis)- время
запаздывания распространения пульсовой волны по эластическим артериям (tэ)-
Время запаздывания от начала подъема кривой а. саrоtis до начала подъема
сфигмограммы с лучевой артерии (а.radialis)- время запаздывания по сосудам
мышечного типа (tМ). Регистрация сфигмограммы для определения времени
запаздывания должна производиться при скорости движения фотобумаги- 100 мм/с.
Для большей точности в
подсчете времени запаздывания пульсовой волны регистрируется 3-5 пульсовых
колебаний и берется среднее значение из полученных при измерении величин (t)
Для вычисления скорости распространения пульсовой волны (С) теперь необходимо
путь (L), пройденный пульсовой волной (расстояние между приемниками пульса),
разделить на время запаздывания пульса (t)
С=L(cм)/t(c).
Так, для артерий
эластического типа:
Э=LЭ/TЭ,
для артерий мышечного типа:
СМ=LM/tM.
Например, расстояние между
датчиками пульса равно 40 см, а время запаздывания- 0,05 с, тогда скорость
распространения пульсовой волны:=40/0,05=800 cм/с
В норме у здоровых лиц
скорость распространения пульсовой волны по эластическим сосудам колеблется в
пределах 500-700 см/с, по сосудам мышечного типа- 500-800 см/с.
Упругое сопротивление и,
следовательно, скорость распространения пульсовой волны зависят прежде всего от
индивидуальных особенностей, морфологической структуры артерий и от возраста
обследуемых.
Многие авторы отмечают, что
скорость распространения пульсовой волны с возрастом увеличивается, при этом
несколько в большей степени по сосудам эластического типа, чем мышечного. Такое
направление возрастных изменений, возможно, зависит от понижения растяжимости
стенок сосудов мышечного типа, что в какой-то мере может компенсироваться
изменением функционального состояния ее мышечных элементов. Так, Н.Н. Савицкий
приводит по данным Людвига (Ludwig, 1936) следующие нормы скорости
распространения пульсовой волны в зависимости от возраста.
Возрастные нормы скорости
распространения пульсовой волны по сосудам эластического (Сэ) и мышечного (См)
типов:
При сопоставлении средних
значений Сэ и См, полученных В.П. Никитиным (1959) и К.А. Морозовым (1960), с
данными Людвига (Ludwig, 1936) следует отметить, что они довольно близко
совпадают.
Е.Б. Бабским и В.Л. Карпманом
предложены формулы для определения индивидуально должных величин скорости
распространения пульсовой волны в зависимости или с учетом возраста:
Сэ =0,1*B2 + 4B + 380;
См = 8*B + 425.
В этих уравнениях имеется
одно переменное В- возраст, коэффициенты представляют собой эмпирические
постоянные.
Скорость распространения
пульсовой волны по эластическим сосудам зависит также от уровня среднего
динамического давления. При повышении среднего давления скорость распространения
пульсовой волны увеличивается, характеризуя усиление «напряженности» сосуда за
счет пассивного растяжения его изнутри высоким артериальным давлением. При
изучении упругого состояния крупных сосудов постоянно возникает необходимость
определять не только скорости распространения пульсовой волны, но и уровень
среднего давления.
Несоответствие между
изменениями среднего давления и скоростью распространения пульсовой волны в
известной степени связано с изменениями тонического сокращения гладкой мускулатуры
артерий. Это несоответствие наблюдается при изучении функционального состояния
артерий преимущественно мышечного типа. Тоническое напряжение мышечных
элементов в этих сосудах меняется довольно быстро.
Для выявления «активного
фактора» тонуса мускулатуры сосудистой стенки В.П. Никитин предложил
определение соотношения между скоростью распространения пульсовой волны по
сосудам мышечного (См) и скорости по сосудам эластического (Сэ) типов. В норме
это соотношение (СМ/С9) составляет от 1,11 до 1,32. При усилении тонуса гладкой
мускулатуры оно возрастает до 1,40-2,4; при понижении- уменьшается до 0,9-0,5.
Уменьшение СМ/СЭ наблюдается при атеросклерозе, за счет увеличения скорости
распространения пульсовой волны по эластическим артериям. При гипертонической болезни
эти величины, в зависимости от стадии, различны.
Таким образом, при увеличении
упругого сопротивления скорость передачи пульсовых колебаний нарастает и иногда
достигает больших величин. Большая скорость распространения пульсовой волны
является безусловным признаком увеличения упругого сопротивления артериальных
стенок и уменьшения их растяжимости.
В норме скорость
распространения пульсовой волны, рассчитанная таким способом, составляет
450-800 см.с-1. Следует помнить, что она в несколько раз
выше скорости кровотока, т. е. скорости перемещения порции крови по
артериальной системе.
По скорости распространения
пульсовой волны можно судить об эластичности артерий и величине их мышечного
тонуса. Скорость распространения пульсовой волны увеличивается при атеросклерозе
аорты, гипертонической болезни и симптоматических гипертензиях и уменьшается
при аортальной недостаточности, открытом артериальном (боталловом) протоке, при
снижении мышечного тонуса сосудов, а также при облитерации периферических
артерий, их стенозах и уменьшении ударного объема и АД.
Скорость распространения
пульсовой волны нарастает при органическом поражении артерий (увеличение Сэ при
атеросклерозе, сифилитическом мезоаортите) или при усилении упругого
сопротивления артерий за счет повышения тонуса их гладкой мускулатуры,
растяжении стенок сосуда высоким артериальным давлением (увеличение См при
гипертонической болезни, нейроциркуляторной дистонии гипертензивного типа). При
нейроциркуляторной дистонии гипотонического типа уменьшение скорости
распространения пульсовой волны по эластическим артериям связано в основном с
низким уровнем среднего динамического давления.
На полученной
полисфигмограмме по кривой центрального пульса (а. саrotis) определяется также
время изгнания (5) - расстояние от начала подъема пульсовой кривой сонной
артерии до начала падения ее главной систолической части.
Н.Н. Савицкий для более
правильного определения времени изгнания рекомендует пользоваться следующим
приемом (рис. 4). Проводим касательную прямую через пятку инцизуры а. саrotis
вверх по катакроте, из точки отрыва ее от катакроты кривой опускаем
перпендикуляр. Расстояние от начала подъема пульсовой кривой до этого
перпендикуляра и будет временем изгнания.
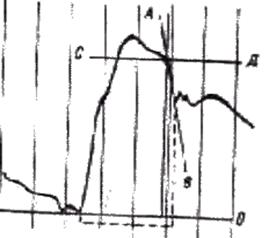
Рис.4. Прием для определения
времени изгнания (по Н.Н. Савицкому).
Проводим линию АВ,
совпадающую с нисходящим коленом катакроты У места отхождененя ее от катакроты
проводим линию СД, параллельную нулевой. Из точки пересечения опускаем
перпендикуляр на нулевую линию. Время изгнания определяется расстоянием от
начала подъема пульсовой кривой до места пересечения перпендикуляра с нулевой
линией. Пунктиром показано определение времени изгнания по месту расположения
инцизуры.
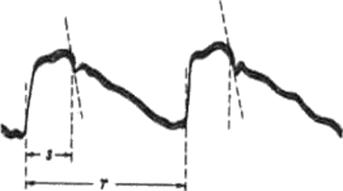
Рис.6. Определение времени
изгнания (5) и времени полной инволюции сердца (Т) по кривой центрального
пульса (по В.П. Никитину).
Время полной инволюции сердца
(длительность сердечного цикла) Т определяется по расстоянию от начала подъема
кривой центрального пульса (а. carotis) одного сердечного цикла до начала
подъема кривой следующего цикла, т.е. расстояние между восходящими коленами
двух пульсовых волн (рис. 6).
.2 Исследование
особенностей сфигмограммы и скорости распространения пульсовой волны по крупным
артериальным сосудам
Характерным и ранним
признаком субаортального стеноза является систолический шум, который
выслушивается вдоль левого края грудины, в точке Боткина, распространяется на
сосуды шеи, отделен от 1-го тона, иногда состоит из двух фаз, может сопровождаться
систолическим дрожанием грудной клетки. Часто выслушивается систолический шум
над верхушкой, который проводится в подмышечную область (шум регургитации). На
ЭКГ регистрируются признаки гипертрофии левого желудочка и предсердий,
отрицательные зубцы Т и смещение книзу интервала S - Т в левых грудных
отведениях. Иногда в классических отведениях появляются глубокие зубцы Q как
отражение гипертрофии межжелудочковой перегородки. I. Heublein с соавторами
(1971) считают, что характерным электрокардиографическим признаком
субаортального стеноза являются комплексы типа qrS в сочетании с положительным
зубцом Т в левых грудных отведениях. Рентгенологически определяется умеренное
увеличение левого желудочка и левого предсердия, усиление легочного рисунка за
счет застоя, иногда расширение восходящей аорты.
В
дифференциально-диагностическом отношении важны изменения сфигмограммы:
характерен двойной ее контур с быстрым первым спуском анакроты за счет
нарастающего сужения путей оттока. Нарастающее давление в левом желудочке
проталкивает кровь в аорту,- появляется второй подъем кривой, менее крутой, чем
первый, с последующим длительным спуском и дополнительными низкоамплитудными
колебаниями (W. H. Carter с соавт., 1971).
Сфигмографическое
исследование с синхронной записью пульса с сонной, лучевой и бедренной артерий
проведено у 88 детей. Сфигмографическое исследование осуществлялось в
горизонтальном положении ребенка с помощью того же трехканального электронного
прибора «Визокард-Мультивектор», с применением пьезоэлектрических приемников
пульса, одновременно с электрокардиограммой во II стандартном отведении. Запись
проводилась сначала с сонной и лучевой, затем с сонной и бедренной артерий
после 10-минутного отдыха одновременно с двух и более точек, что необходимо для
определения скорости пульсовой волны, а также синхронно с другими кривыми,
отражающими различные проявления сердечной деятельности (электрокардиограмма,
фонокардиограмма).
Для изучения функционального
состояния крупных артериальных сосудов пульсовые датчики устанавливались в трех
разных точках: на сонной (переднешейная борозда - на уровне верхнего края
щитовидного хряща), лучевой (в обычной точке прощупывания пульса) и на
бедренной артериях (середина пупартовой связки). Регистрацию пульсовых кривых
проводили только после соответствующего оптимального приспособления датчика, по
достижении при данном усилении максимальной амплитуды сфигмограммы.
По времени запаздывания
пульсовых кривых и по расстоянию между точками, с которых записываются
пульсовые кривые, определяется скорость распространения пульсовой волны по
сосудам мышечного (на участке сонная артерия - лучевая артерия) и по сосудам
эластического типов (на участке сонная артерия - бедренная артерия).
Запаздывание пульсовой волны измеряется по расстоянию между началом подъема
каждой из сфигмограмм.
Для определения длины пути
между сонной и лучевой артериями измеряется расстояние с помощью сантиметровой
ленты от верхнего края щитовидного хряща (местоположение первого приемника
пульса) до яремной ямки (проекция верхнего края дуги аорты). Затем на
отведенной руке, составляющей с туловищем прямой угол, измеряется расстояние от
яремной ямки до места регистрации пульса на лучевой артерии. Из общего
расстояния между датчиками вычитается удвоенное расстояние между щитовидным
хрящом и яремной ямкой (так как пульсовая волна в лучевой и сонной артериях
распространяется в противоположных направлениях).
Для определения длины участка
«сонная артерия - бедренная артерия» измеряется расстояние от верхнего края
щитовидного хряща до яремной ямки, затем - от яремной ямки до пупка (проекция
деления аорты на подвздошные артерии) и от пупка до середины пупартовой связки
(место наложения третьего датчика пульса). Все полученные размеры складываются
и из образовавшейся суммы вычитается удвоенное расстояние между щитовидным
хрящом и яремной ямкой (Н. Н. Савицкий, 1956; В. Н. Никитин, 1958, и др.).
Изучение формы пульсовых
кривых у детей с суставно-висцеральным течением ревматоидного артрита (I
группа) показало, что кривые артериального пульса, имея общие черты, отличаются
большим разнообразием индивидуальных особенностей. Обращает на себя внимание,
что у многих детей в острый период заболевания кривые артериального пульса,
особенно с сонной артерии, отличались неустойчивостью формы и амплитуды, их
изменчивостью даже в различных сердечных циклах, следующих друг за другом.
Очевидно, причина такой вариабельности - в лабильности гемодинамики, в
неодинаковой силе сердечных сокращений, меняющейся величине ударного объема
сердца, в неустойчивости сосудистого тонуса у больных ревматоидным артритом с
выраженным токсико-аллергическим синдромом.
Отмечается также более
частое, чем у здоровых детей, отсутствие на кривой каротидного пульса
пресистолического колебания, которое зарегистрировано лишь у 55% больных детей
(по данным М. К. Осколковой, у 80% здоровых). При обследовании детей, больных
ревматизмом, М. К. Осколкова (1967) также констатировала отсутствие
пресистолического колебания на кривой каротидного пульса. Эта особенность
обусловлена, с одной стороны, ослаблением сократительной функции предсердий, с
другой - изменениями систолического объема сердца и сосудистого тонуса,
учитывая, что генез пресистолического зубца связан с перечисленными факторами.
Увеличение пресистолической
волны наблюдалось всего лишь у 5 детей, у 3 из них, по данным
клинико-инструментальных методов исследования, предполагалось формирование
митрального и аортального пороков, а у 2 - преобладали симптомы миокардита.
Инцизура на кривой
каротидного пульса у 84% детей была отчетливо выражена в верхней или средней
трети нисходящей ветви сфигмограммы, у 11% детей она регистрировалась в нижней
трети кривой и у 5% - была слабо выражена или отсутствовала. Дикротическая
волна на катакроте пульса с лучевой артерии располагалась у большинства детей I
группы в нижней ее трети, в отличие от здоровых детей, у которых, она, как
правило, регистрируется в средней трети катакроты (М. К. Осколкова, 1967) и
нередко была увеличена. Подобные изменения рассматриваются как признак снижения
тонуса артериальных сосудов. В динамике наблюдения, при стихании основного
процесса, с уменьшением интоксикации, отмечалось смещение дикротической волны
ближе к вершине кривой и уменьшение ее амплитуды. Данный признак можно
объяснить увеличением напряжения (тонуса) стенок артериальных сосудов при
улучшении состояния детей (В. П. Никитин, 1950; М. К. Осколкова, 1957). Л. П.
Прессман (1964), изучая состояние сердечно-сосудистой системы при инфекционных
заболеваниях у взрослых, пришел к выводу, что величина дикротической волны у них
находится в прямой зависимости от степени интоксикации. Сопоставление форм
пульсовых кривых с характером поражения сердца не выявило достаточно типичных
изменений сфигмограммы. При явлениях кардита у некоторых детей отмечалось лишь
небольшое снижение амплитуды пульсовых кривых, иногда изменчивость их формы и
величины в различных сердечных циклах. В течение болезни форма пульсовых кривых
с центральных и периферических артерий нередко изменялась.
Характерным признаком
недостаточности аортальных клапанов на СФГ сонной артерии является крутой
подъем кривой, слабая выраженность или отсутствие инцизуры. Феномен
исчезновения или уменьшения выраженности инцизуры является важным признаком
вовлечения в патологический процесс аорты (М. Н. Абрикосова, 1963; М. К. Осколкова,
1967, и др.).
Блюмбергер (1958), М. А.
Абрикосова (1963), М. К. Осколкова (1967) полагают, что большая или меньшая
выраженность инцизуры на сфигмограмме с сонной артерии при поражении аорты
зависит от степени деформации клапанного аппарата: при меньшем поражении -
инцизура выражена, при большем - исчезает.
Кроме изучения
морфологических особенностей сфигмограммы, высчитывалась скорость
распространения пульсовых волн. Изучение скорости распространения пульсовой
волны по сосудам эластического и мышечного типов больных с
суставно-висцеральной формой ревматоидного артрита показало отчетливое
уменьшение этого показателя по сравнению с нормальными величинами как в острый
период, на фоне лечения, так и в период стихания.
Из таблицы следует, что у
детей в возрасте от 3 до 6 лет при суставно-висцеральной форме заболевания
средние данные исходных величин в острый период болезни по сосудам
эластического типа были равны 456,8±13,5 см/сек., а по сосудам мышечного типа -
484,0±24,8 см/сек., не достигая нормальных величин даже в период стихания.
У детей в возрасте от 7 до 11
лет средние показатели скорости распространения пульсовой волны по сосудам
эластического типа равнялись 470,0± ±22,0 см/сек., а по сосудам мышечного типа
- 588,0± ±15,8 см/сек., то есть эти показатели были ниже, чем данные у здоровых
детей и оставались сниженными и при стихании процесса с разницей, статистически
достоверной (Р<0,05).
Наибольшее снижение
показателей скорости распространения пульсовой волны наблюдалось у детей в
возрасте от 12 до 15 лет. Средние показатели ее по сосудам эластического типа в
острый период болезни были 504,7+10,5 см/сек., а по сосудам мышечного типа -
645,0-27,6 см/сек. Эти величины статистически достоверно снижены по сравнению с
данными здоровых детей (Р< 0,005).
В период улучшения общего
состояния наблюдалось незначительное повышение скорости распространения
пульсовой волны по сосудам эластического типа, по сосудам же мышечного типа
скорость оставалась значительно сниженной (соответственно 508,0±10,0 см/сек, и
528,7 ±10,7 см /сек.; Р<0,01). Столь стойкое нарушение функционального
состояния крупных артериальных сосудов очевидно можно объяснить высокой
степенью аллергизации, продолжающейся активностью ревматоидного артрита и
большой длительностью заболевания.
У взрослых больных В. И.
Трухляев (1968) констатировал повышение скорости распространения пульсовой
волны по крупным артериальным сосудам. Эта разница по сравнению с данными,
полученными у детей, лишний раз подчеркивает своеобразие пеактивности детского
организма. Б. А. Гайгалене (1970) у взрослых обнаруживала асимметрию тонуса
сосудов и изменение их реакции на холод.
Изучение характера кривых
центрального и периферического пульса у больных с суставной формой
ревматоидного артрита (II группа) обнаружило отсутствие пресистолической волны
на сфигмограмме каротидного пульса у 8 (из 31) детей. У этих больных
наблюдалась тахикардия, связанная, по-видимому, с токсико-аллергическим
состоянием в острый период заболевания. У остальных 23 детей пресистолическая
волна регистрировалась, варьируя лишь в амплитуде. Вершина пульсовых кривых у
20 детей имела округлые очертания, у 5 - заостренные и у 6 - форму
«систолического плато». Вершину типа «систолическое плато» М. К. Осколкова чаще
наблюдала у детей, больных ревматизмом. И. М. Руднев (1962) считает, что кривые
типа «плато» с высоким осциллометрическим индексом указывают на понижение
тонуса сосудов и на наличие сопротивления току крови на периферии. Если учесть,
что у этих детей при капилляроскопии обнаруживалось спастико-атоническое
состояние капилляров с преобладанием спастического компонента, а
рентгенологически определялись признаки снижения тонуса сердечной мышцы, то,
возможно, указанная форма сфигмограммы и отражала задержку в нарастании и
спадении давления в центральных артериальных сосудах.
Инцизура на кривой
каротидного пульса у 64,5% детей располагалась в верхней или средней трети
нисходящей ветви сфигмограммы, а у 35,5%-в нижней ее трети. Инцизура и
начальная диастолическая волна у большинства детей были хорошо выражены.
Дикротическая волна на
сфигмограмме с лучевой артерии у 36% детей располагалась в средней трети
ка-такроты. На сфигмограмме с бедренной артерии дикротическая волна чаще
регистрировалась в нижней трети катакроты, а у 8% детей она не
регистрировалась. В острый период заболевания амплитуда пульсовых кривых
лучевой и бедренной артерий у 19 детей II группы была увеличена. Этот факт,
возможно, связан с компенсаторной гиперфункцией миокарда и снижением тонуса
крупных сосудов.
Анализ полученных данных
скорости распространения пульсовой волны по сосудам эластического и мышечного
типов у детей с суставной формой ревматоидного артрита так же, как и у детей I
группы, указывал на уменьшение скорости распространения пульсовой волны во всех
возрастных группах. Однако это уменьшение было несколько менее выражено, чем
при суставно-висцеральной форме заболевания.
У детей дошкольного возраста
(от 3 до б лет) скорость распространения пульсовой волны в острый период
болезни была равна 512,0±19,9 см/сек, по сосудам эластического типа и
514,6±12,9 см/сек, по сосудам мышечного типа.
У детей младшего школьного
возраста (от 7 до 11 лет) средние показатели скорости распространения пульсовой
волны были равны для сосудов эластического типа 531,5±17,2 и мышечного типа -
611,8± 24,0 см/сек. В период стихания наблюдалось некоторое увеличение скорости
распространения пульсовой волны по сосудам эластического и мышечного типов.
У детей старшего школьного
возраста (от 12 до 15 лет) в острый период заболевания скорость распространения
пульсовой волны по сосудам эластического типа равнялась 517,7±11,0 см/сек, и по
сосудам мышечного типа - 665,7±25,7 см/сек. В период улучшения состояния
наблюдалось некоторое увеличение данных показателей как по сосудам
эластического, так и мышечного типов (соответственно 567,5±26,7 см/сек, и
776,8±50,4 см/сек.). Уменьшение скорости распространения пульсовой волны по
сосудам эластического и мышечного типов, согласно данным литературы,
свидетельствует о снижении тонуса артериальной стенки (Н. Н. Савицкий, 1963; В.
П. Никитин, 1959, и др.). У детей с ревматоидным артритом оно может быть
связано с патоморфологическими и гистохимическими изменениями сосудистой стенки
в результате хронически протекающего системного васкулита (А. И. Струков, А. Г.
Бегларян, 1963, и др.), а также с токсико-аллергическими влияниями на
нейро-эндокринный регуляторный аппарат.
Дальнейшее уменьшение
скорости распространения пульсовой волны по сосудам эластического и мышечного
типа, наблюдавшееся у части детей в фазе стихания ревматоидного процесса, в
конце лечения, возможно, обусловлено своеобразной следовой реакцией нервной и
сердечно-сосудистой системы на патологический процесс. Возможно, имело какое-то
значение применение разнообразных медикаментозных средств, в том числе и
пирамидона, который, по наблюдениям И. М. Руднева (1960), вызывает понижение
тонуса сосудов. Приведенные исследования подтверждают большую клиническую
ценность сфигмографии в оценке функционального состояния крупных артериальных
сосудов при динамическом исследовании их в разные фазы патологического
процесса.
.3 Анализ существующих
устройств для регистрации и измерения параметров пульсовой волны
Известен ряд неинвазивных
способов, устройств и систем, исследующих деятельность организма человека,
основанных на различных физических механизмах, связанных с образованием и
распространением пульсовой волны. Основные физические методы исследований
связаны с измерением изменения во времени следующих физических величин:
электрических, например тока (напряжения) с помощью электрокардиограмм (ЭКГ);
механических, например давления с помощью манометра или пьезодатчика;
оптических, например освещенности с помощью оптоэлектронных преобразователей.
Регистрация пульсовой волны с помощью ЭКГ или датчиков давления обычно требует
фиксированного подключения специальных датчиков к нескольким местам на теле
пациента, что ограничивает возможные применения данных устройств чисто
медицинскими применениями, не допуская встраивания этих устройств в другие
электронно-бытовые устройства и системы.
Известные одноэлементные
устройства и способы оптической регистрации пульсовой волны во многих случаях
позволяют регистрировать периферический пульс, например, при легком касании
пальцем пользователя оптоэлектронного преобразователя. Однако в некоторых
случаях, например, если у пользователя холодные руки или слишком слабый
(сильный) прижим пальца к фотоприемнику, то не удается устойчиво регистрировать
пульсовую волну у всех 100% пациентов.
Известны способ и устройство
регистрации пульсовой волны, позволяющие устойчиво выявлять пульс с помощью
двухканального оптоэлектронного преобразователя.
В этом способе регистрации
пульсовой волны импульсные последовательности, пропорциональные оптической
плотности рассеивания света в кровонесущей ткани, формируют двухканальным
оптоэлектронным преобразователем с длинами волн инфракрасного диапазона, при
этом импульсная последовательность центрального пульса обеспечивает жесткую
синхронизацию режимов измерения, а результат измерения на индикаторе линейно
связан с разностью фаз двух импульсных последовательностей.
Устройство содержит первый
оптоэлектронный преобразователь, выход которого соединен с входом первого
формирователя импульсной последовательности, выход которого соединен с первым
входом ключевой логической схемы И-НЕ и первым входом формирователя команд
управления. Выход второго оптоэлектронного преобразователя соединен с входом
второго формирователя импульсной последовательности, выход которого соединен со
вторым входом ключевой логической схемы И-НЕ. Первый выход формирователя команд
управления соединен с третьим входом ключевой логической схемы И-НЕ, а второй и
третий выходы подключены соответственно ко входам первого и второго
оптоэлектронных преобразователей. На четвертый вход ключевой логической схемы
И-НЕ подключен генератор измерительной частоты. Кнопка пуска подключена ко
второму и третьему входам формирователя команд управления. Выход ключевой
логической схемы И-НЕ соединен со входом счетчика частоты, выход которого
подключен на вход регистра памяти. Соответственно выход регистра памяти
подключен к индикатору.
Устройство состоит из двух
датчиков и блока обработки и управления. Датчики устанавливаются на
определенном расстоянии один от другого над исследуемой артерией, информация с
датчиков поступает в блок обработки и управления. Блок обработки состоит из
пикового детектора, фазового компаратора, задатчика расстояния между датчиками,
аналогового коммутатора, аналого-цифрового преобразователя, микроЭВМ,
репрограммируемого таймера, индикаторного устройства и цифроаналогового преобразователя.
Получая от датчиков информацию о моментах прохождения пульсовой волны и
амплитуде пульсовой волны, а также от задатчика расстояния то расстояние,
которое проходит волна между датчиками, блок обработки производит вычисление
скорости распространения пульсовой волны и артериального давления и фиксирует
полученные результаты на носителе (бумаге, магнитной пленке). Отсутствие
механизма пережатия у предлагаемого устройства позволит проводить длительные
автоматические исследования артериального дваления у пациента с автоматической
регистрацией результатов исследования. Устройство хорошо сопрягается с
радиотелеметрическими системами и обеспечит дистанционный контроль величины
артериального давления у водителей различного вида транспорта, операторов и др.,
что позволит своевременно предупреждать возникновение аварийных ситуаций.
Известен ИК-датчик, который используется при контроле
частоты пульса человека. Непосредственно на базе ручных электронных часов
реализуется схема включения ИК-датчика и обработки его электрических сигналов.
Для устойчивой работы схемы обработки сигнал с ИК-датчика усиливается
усилителем. ИК-датчик состоит из ИК-светодиода и ИК-фотоприемника, которые
конструктивно расположены рядом друг с другом, но разделены оптически непрозрачной
зоной/областью. При отсутствии отраженного от биоткани зондирующего ИК-сигнала
прямого взаимного влияния ИК-светодиода на ИК-фотодиод нет. Данное положение
является принципиальным. Поверхность такого ИК-датчика защищена от возможного
загрязнения в процессе работы защитным стеклом. Если приложить палец к
защитному стеклу, то такой ИК-датчик фиксирует степень изменения насыщения
биоткани кровью (капиллярный уровень) синфазно с работой сердца. ИК-датчик
непосредственно подключен к линейному усилителю. Дальнейшая схема пересчета
позволяет косвенно определить по сигналу такого ИК-датчика искомую частоту
пульса.
Недостатки устройства:
ИК-датчик работает достаточно неустойчиво при
значительной солнечной активности, что «ослепляет ИК-датчик»;
степень прижимания тканей пальца к контактной зоне
ИК-датчика влияют на степень отраженного сигнала, что может влиять на точность
пересчета при определении частоты пульса;
колебания (дрожание руки) также влияет на искажение
результатов ИК-датчика;
принципиально невозможно контролировать венозный
уровень кровотока из-за фонового капиллярного уровня.
Наиболее близкой к этому устройству является
конструкция ИК-датчика, которая также применяется при контроле частоты пульса
человека. ИК-датчик конструктивно (рис.7) выполнен в прямоугольном каркасе (1)
из оптически непрозрачного твердого материала, например текстолита, в котором
на одной линии под острым углом α друг к другу сформированы два
цилиндрических канала (2, 3). В первый из каналов вмонтирован ИК-светодиод (5),
а во второй - ИК-фотодиод (6). Взаимный острый угол расположения каналов а
таков, что оптически непрозрачная перегородка исключает прямое влияние
ИК-светодиода (5) на ИК-фотодиод (6). Внешняя поверхность ИК-датчика защищена
от возможного загрязнения защитной, оптически прозрачной для ИК длин волн
пластиной (4), например, из полистирола. Реализация возможностей ИК-датчика (Е)
достигается путем его подключения к линейному усилителю (А).
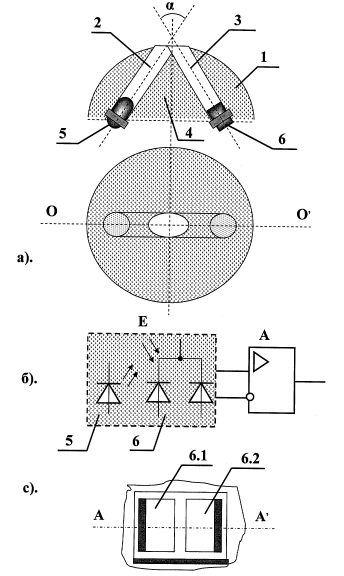
рис.7 конструкция ИК-датчика для измерения частоты
пульса.
Недостатки данного устройства (прототипа) точно такие
же, как и в аналоге.
Известны способы и устройства измерения пульсовой
волны, в которых анализ пульсовой волны производится по ее амплитудно-частотным
характеристикам, когда для целей постановки диагноза такие амплитудно-частотные
характеристики сравнивают с соответствующими характеристиками, принятыми за
норму [например: полезная модель RU 9577, опубл. 16.04.1999; патенты США: US
5381797, опубл. 17.01.1995; US 5961467, опубл. 05.10.1999; US 6767329, опубл.
27.07.2004]. Однако при таком подходе интерпретация сравниваемых характеристик
носит в большей степени эмпирический характер, что затрудняет установить
реальную связь параметров пульса с состоянием человека, например как это
установлено в китайской традиционной медицине.
Известны способы и устройства измерения пульсовой
волны для целей постановки диагноза, в которых анализ измеренной пульсовой
волны производят путем ее разложения на составляющие.
Известен способ дифференциальной диагностики
заболеваний легких путем регистрации и записи сфигмографического сигнала с
лучевой артерии пациента [патент RU 2100009, опубл. 27.12.1997]. В сигнале
выделяют характерные точки единичных колебаний, определяют амплитудные и
временные параметры этих точек пульсовой волны, формируют динамические ряды,
отражающие зависимость найденных параметров от номера периода, проводят
спектральный анализ сформированных рядов, вычисляют критерий, по значению
которого производят диагностику. Известный способ является узкоспециализированным.
Известны способ и аппарат для диагностики и
мониторинга циркуляции крови [патент US 5730138, опубл. 24.03.1998], согласно
которым измеряют форму волны кровяного давления (пульсовая волна) в артерии
пациента, анализируют частотные составляющие пульсовой волны и сравнивают
образцы каждой резонансной составляющей пульсовой волны с образцом нормальной
пульсовой волны для определения возможного дисбаланса распределения крови
пациента.
В соответствии с этим дисбалансом может быть проведен
диагноз на основе принципов китайской традиционной медицины, согласно которому
каждая гармоника в пульсовой волне соответствует определенному меридиану,
включающему определенные органы.
Аппарат включает устройство анализа амплитуды и фазы
резонансных частот на базе компьютера и датчик, прикладываемый к артерии.
Однако понятие «нормальной» пульсовой волны является относительным, поэтому
поставленный диагноз является малодостоверным. Также в данном техническом
решении не проработан способ корректного выделения составляющих пульсовой
волны.
Устройство работает следующим образом.
Устанавливаются пьезоэлектрические датчики над
исследуемой артерией на определенном расстоянии L. Пульсовая волна вызывает
поперечные колебания стенок артерии, эти колебания сжимают и отпускают пластины
датчиков.
Полученный с датчиков сигнал усиливается и фильтруется
для компенсации помех. Контактный элемент обеспечивает более плотную связь со
стенкой артерии воспринимающей пластины, что увеличивает чувствительность
датчиков к колебаниям стенки артерии.
Поскольку сигнал, принимаемый с датчиков довольно
сложен, АЦП микроконтроллера не обладает достаточной частотой дискретизации для
его обработки. Поэтому в схеме используется АЦП МАХ-1241.
Оцифрованные сигналы поступают в микроконтроллер, где
происходит их обработка в соответствии с выбранным режимом работы и вычисление
разности фаз. Разность фаз колебаний пульсовой волны в точности равна времени
распространения пульсовой волны между датчиками. Вычисленное значение скорости
распространения пульсовой волны отображается на ЖКИ.
В устройстве предусмотрена клавиатура для выбора
режима работы в зависимости от исследуемой части тела и расстояния между
датчиками.
Блок питания обеспечивает все функциональные узлы
питающими напряжениями.
Структурная схема устройства показана на рисунке 8.
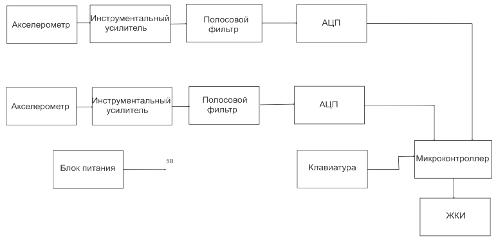
Рис.8 Структурная схема устройства
3. Выбор элементной базы и расчет
основных элементов и узлов
пульсовой волна кровоток
сфигмограмма
Усилитель
Показанная на рис. 9 схема представляет собой
простейший и самый дешевый измерительный усилитель. Резисторы R2 и R6 действуют как делитель напряжения для неинвертирующего
входа операционного усилителя (ОУ). Благодаря обратной связи через резисторы R1 и R5 и очень большому внутреннему коэффициенту усиления ОУ
напряжение на инвертирующем входе усилителя поддерживается равным напряжению на
неинвертирующем входе. Отношение Кз/МГ определяет коэффициент
передачи усилителя. Когда R1/R5=R2/R6, усиление дифференциального
сигнала намного больше усиления синфазного сигнала, и коэффициент ослабления
синфазного напряжения (КОСС) будет максимальным.
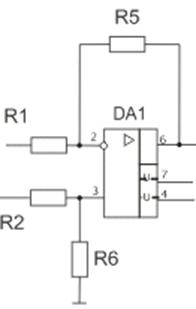
Рис. 9 схема усилителя
Дифференциальный коэффициент усиления:
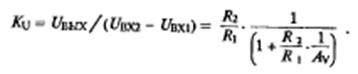
где Av -
коэффициент усиления ОУ, Av→∞
Коэффициент усиления синфазного сигнала, обусловленный
рассогласованием резисторов, равен:
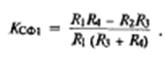
Коэффициент усиления синфазного сигнала, обусловленный
конечным значением КОСС операционного усилителя (КОССоу), равен:
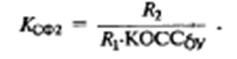
Отметим, что КОССоу выражается отношением, а не в
децибелах. Коэффициент оелаблсцил синфазного сигнала всей схемы:
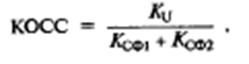
Дифференциальное входное сопротивление:
Rвхдиф = R1+R3
Входное сопротивление для синфазного сигнала (при КОСС
= ∞) составляет:
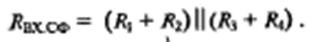
Выходное напряжение смещения (при R1=R2 и R5=R6) в нашем случае равно:
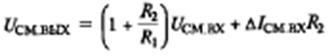
Для реализации коэффициента усиления равным 10,
выбраны следующие значения сопротивлений R1=R2=10кОм R5=R6=100кОм
Полосовой фильтр
На рисунке 10 изображен полосовой фильтр, применяемый
в устройстве
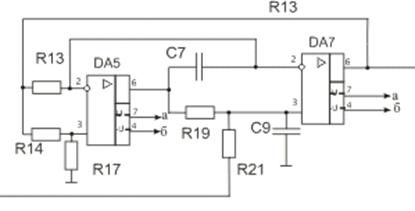
Рис.10 схема полосового фильтра
Передаточная функция
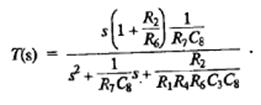
Параметры схемы
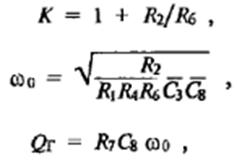
Полоса пропускания по уровню -3Дб
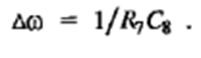
Несмотря на наличие пяти резисторов и двух
конденсаторов, расчет элементов по приведенным формулам оказывается довольно
простым. Настройка схемы сводится к операциям установки
коэффициента передачи - резистором R14,
резонансной частоты ω0 - резистором R19,
добротности Qf - резистором R21
Эта схема особенно хороша для построения фильтров с
высокой добротностью Qf,
поскольку она некритична к отклонениям значений элементов от номинальных,
проста в настройке и не требует применения элементов с большим диапазоном
номиналов. Эти преимущества достигаются за счет использования двух ОУ.
Согласно значениям сердечного ритма, полоса
пропускания данного фильтра составляет 0,5-5Гц Для реализации этого рассчитаны
следующие параметры : R13=R14=10кОм, R17= R17=100кОм,
R17=20кОм, С7=0.4 мкФ С9=0.1мкФ
Для регистрации пульсовой волны используется
акселерометр ADXL320
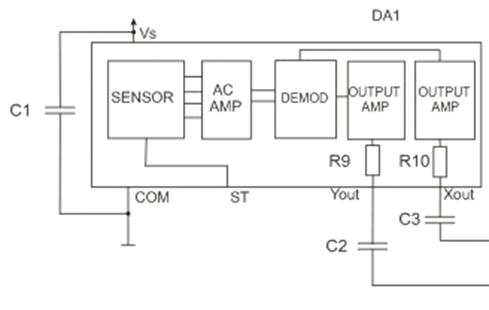
Рис.11 схема акселерометра
JCP - двухмерный датчик ускорения, с низкой ценой и
малым потреблением. Измеряет ускорение в диапазоне ± 5G, вибрацию и гравитацию.
Технические особенности:
разрешение 2 мg при 60 Гц;
напряжение питания в диапазоне 2,4 … 5,25 В;
ток потребления 350 мА при напряжении питания 2,4 В;
стабильный уровень нулевого ускорения;
высокая чувствительность;
выравнивание по осям с точностью до 0,1 градуса;
BW корректировка при помощи одного конденсатора;
однополярное функционирование;
аварийная нагрузка 10000g.
Структурная схема приведена на рисунке12.
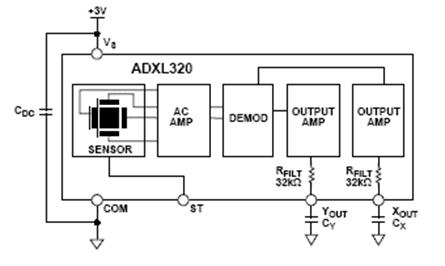
Рис.12 схема акселерометра
Области применения: схемы движения и ориентации,
интеллектуальные ручные устройства, мобильные телефоны, приборы для медицины и
спорта, устройства безопасности.
Для оцифровки сигналов используется АЦП МАХ-1241
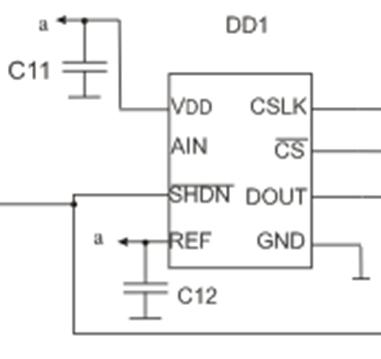
Рис.13 схема полосового фильтра
Для обработки полученной информации используется
микроконтроллер PIC16F877. Для отображения информации
используется ЖК-монитор LM016L.
5. Расчет блока питания и
потребляемой мощности
Питание самодельных радиоэлектронных устройств, как
правило, осуществляют от сети переменного тока или автономных источников
питания (гальванических элементов и аккумуляторов). Одни устройства потребляют
небольшой электрический ток и в этом случае можно обойтись батарейками, в
других случаях емкости батареек недостаточно для длительной работы и приходится
пользоваться блоками питания от сети.
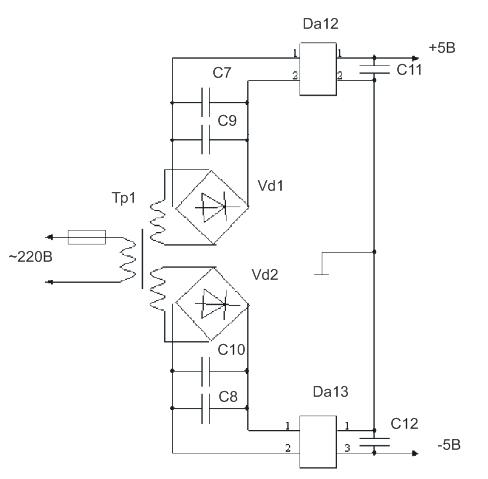
Рисунок 13 Принципиальная схема блока питания
Номинальное напряжение ОУ составляет ±5В. Ток потребления одного ОУ - 4мА.
С учетом потребления микроконтроллера и ЖКИ, ведем расчет источника питания на
ток 100 мА от каждого источника. Потребляемая мощность составит 1200 мВт.
Выбираем стандартный трансформатор ТПП248 ШЛМ20´20 мощностью 14,5Вт с двумя обмотками
с выходным напряжением 20В и допустимым током 165мА. Максимальный ток первичной
обмотки 100мА.
В качестве выпрямителя используем выпрямительный мост
КЦ422В со следующими параметрами:
Uобр=200В; Iпр max=0,5A; Iобр max= 50мкА, fmax=1кГц.
Расчет емкости конденсатора фильтра однофазного
мостового выпрямителя ведем по формуле
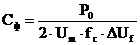 , где
, где
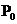 -
мощность на выходе выпрямителя,
-
мощность на выходе выпрямителя, 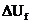 -
максимальный размах пульсаций выпрямленного напряжения,
-
максимальный размах пульсаций выпрямленного напряжения, 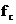 - частота сети.
- частота сети.
Получим:
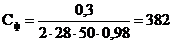 мкФ.
мкФ.
Из
стандартного ряда выбираем конденсатор К50-3Б 50В 390мкФ.
В качестве стабилизаторов используем
стабилизатор положительного напряжения ИС 7815 с выходным напряжением 5±0,45В, Uвхmax=35В, Iвхmax=1,5А и стабилизатор отрицательного напряжения ИС 7815
с выходным напряжением -5±0,3В,
-Uвхmax=35В, Iвхmax=1,5А.
Заключение
В процессе выполнения работы
разработана принципиальная схема устройства, позволяющего проводить измерение
скорости распространения пульсовой волны кровотока. Устройство может работать в
четырех режимах, в зависимости от условий измерения.
Список используемой литературы
1. Левшина Е.С.,Новицкая П.В. Электрические измерения физических
величин: (Измерительные преобразователи). Учеб. пособие для вузов. - Л.:
Энергоатомиздат. Ленинград. отделение, 1983.-320 с.
. Пейтон А. Дж., Волш В. Аналоговая электроника на операционных
усилителях. - М.: БИНОМ, 1994.
. Механцев Е.Б., Лысенко И.Е. Физические основы микросистемной
техники. Учебное пособие.- Таганрог: Изд-во ТРТУ, 2004.- 54 с.
. Протопопов А.С. Усилители с обратной связью, дифференциальные и
операционные усилители и их применение.- М.: САЙНС-ПРЕСС, 2003.- 64с.
. Дж. Фрайден Современные датчики. Справочник.- М.: Техносфера,
2005.- 592с.
. Пат. 2336810 Российская Федерация, A61B 5/024 «Оптоэлектронный
ИК-датчик пульсовой волны» [Текст]/ Ус Н.А.; заявитель и патентообладатель Ус
Н.А.- №2007112233/14; заявл. 2007.04.02 ; опубл. 2008.10.27.
. Пат. 2040207 Российская Федерация, A61B5/022 «Устройство для измерения
артериального давления и емкостной датчик» [Текст]/ Сиволапов А.А.; Бровкович
Э.Д.; заявитель и патентообладатель Сиволапов А.А.; Бровкович Э.Д.;-
№93009423/14; заявл. 1993.02.18; опубл. 1995.07.25.
.Пат. 2199943 Российская Федерация, A61B5/02, «Способ и устройство
регистрации пульсовой волны и биометрическая система» [Текст]/ Минкин В.А.;
Штам А.И.; заявитель и патентообладатель Минкин В.А.; Штам А.И. -
№2001105097/14; заявл. 2001.02.16; опубл. 2003.03.10.
.Пат. 93009423 Российская Федерация, A61B5/02 «Устройство для измерения
скорости распространения пульсовой волны и среднего артериального давления»
[Текст], Сиволапов А.А.; Бровкович Э.Д.; заявитель и патентообладатель
Сиволапов А.А.; Бровкович Э.Д.;.- №2003122269/14; заявл. 1993.02.18; опубл.
1996.04.20.
. Пат. 2281686 Российская Федерация, A61B 5/021 «Способ диагностики
состояния артериального русла при помощи компьютерной сфигмографии» [Текст],
Германов А.В.; Рябов А.Е.; Фатенков В.Н.;; заявитель и патентообладатель
Германов А.В.; Рябов А.Е.; Фатенков В.Н.;- №2004113716/14 ; заявл. 2004.05.05 ;
опубл. 2006.08.20.
.Пат. 2038039 Российская Федерация, A61B5/0205 «Датчик пульсовой волны»
[Текст], Романовская А.М.; Романовский В.Ф. ; заявитель и патентообладатель
Романовская А.М.; Романовский В.Ф. - №4784700/14; заявл. 1989.12.19 ; опубл.
1995.06.27
. М. К. Осколкова, Ю. Д. Сахарова. "Сердце и сосуды при ревматоидном
артрите у детей" Изд-во "Медицина", Ташкент, 1974 г.
. Инструментальные методы исследования сердечно-сосудистой системы:
Справочник. М.: Медицина, 1986. 416 c.
.Поединцев Г.М. О режиме движения крови по кровеносным сосудам //
Развитие новых неинвазивных методов исследования в кардиологии. Воронеж, 1983.
С. 16.
.Поединцев Г.М. Некоторые принципы математического моделирования
биологических систем и критерии оценки их адекватности // Медицинские
информационные системы: Межведомственный тематический научный сборник.
Таганрог: ТРТИ, 1988. Вып. 1(VIII). С. 113.
.Струмските О.К. Математические способы определения минутного, ударного и
фазовых объемов сердца по длительностям фаз сердечного цикла // Развитие новых
неинвазивных методов исследования в кардиологии. Воронеж, 1983. С. 16.
.Цыдыпов Ч.Ц., Бороноев В.В., Пупышев В.Н., Трубачеев Э.А. Проблемы
объективизации пульсовой диагностики тибетской медицины // Межд. семинар по
использованию компьютеров в тибетской медицине “Тибетская медицина (история,
методология изучения и перспективы использования)”. Улан-Удэ, 1989. С. 24.
.Валтнерис А.Д., Яуя Я.А. Сфигмография как метод оценки изменений
гемодинамики под влиянием физической нагрузки. Рига: Зинатне, 1988. 132 с.
.Азаргаев Л.Н., Бороноев В.В., Шабанова Е.В. Сравнительный анализ
сфигмограмм сонной и лучевой артерий // Физиология человека. 1997. Т. 23. № 5.
С. 67.
.Лищук В.А. Математическая теория кровообращения. М.: Медицина, 1991. 256
с.
.Аветикян Ш.Т. Длительность интервалов “подъем-инцизура” артериального
пульса в центральном и периферическом отделах сосудистой системы при различных
положениях человека // Физиология человека. 1984. Т. 10. № 2. С. 24.
. Бороноев В.В., Ринчинов О.С. Методы сплайн-аппроксимации в задаче
амплитудно-временного анализа пульсовой волны // Изв. ВУЗов. Радиофизика. 1998.
Т. XLI. № 8. С. 1043.
.Куликов Ю.А. Объемные параметры центральной гемодинамики по данным
анализа фазовой структуры сердечного цикла // Развитие новых неинвазивных
методов исследования в кардиологии. Воронеж, 1983. C. 49.
.Милягин В.А., Милягина И.В., Грекова М.В. и др. Новый автоматизированный
метод определения скорости распространения пульсовой волны. Функцион.
диагностика. 2004; 1: 33-9.
.Агеев Ф.Т., Орлова Я.А., Кулев Б.Д. и др. Клинические и сосудистые
эффекты бетаксолола у больных с артериальной гипертонией. Кардиология. 2006;
11: 38-43.
Приложение

