Синтез наноматериалов с применением нанореакторов
Федеральное
государственное бюджетное образовательное учреждение высшего профессионального
образования
«Пермский
национальный исследовательский политехнический университет»
Механико-технологический
факультет
Курсовая
работа по теме:
Синтез
наноматериалов с применением нанореакторов
Пермь
2013
Содержание
Введение
. Методы получения наноматериалов
. Синтез наночастиц в аморфных матрицах
. Синтез наночастиц в упорядоченных матрицах
.1 Получение наночастиц в нульмерных нанореакторах
.2 Получение наночастиц в одномерных нанореакторах
.2.1 Цеолиты структурного типа MF1
.2.2 Мезопористые молекулярные сита
.2.3 Использование мезопористого SiO, для синтеза нанокомпозитов
.2.4 Мезопористые алюмосиликаты
.3 Получение наночастиц в двумерных нанореакторах
.3.1 Слоистые двойные гидроксиды
Заключение
Список использованных источников
Введение
Нанореактор (англ. nano-reactor) -
реактор для осуществления химических реакций в ограниченном объеме, размер
которого не превышает 100 нм хотя бы по одному из измерений и ограничен
физически размерами элементов упорядоченной структуры [1].
Основная задача, решаемая при
использовании нанореакторов, - предотвращение слияния и роста твердых частиц
при синтезе и, в ряде случаев, последующей термообработке синтезируемых
материалов. В качестве нанореакторов обычно выступают поры естественного или
искусственного материала, инертного по отношению к используемым реагентам и
продуктам реакции. При синтезе нанообъектов поры инертной матрицы заполняются
одним из реагентов, после чего он приводится в контакт со вторым реагентом,
обычно в жидкой или газообразной форме, инициатором (в случае полимеризации),
или подвергается воздействию электрического тока (при электрохимическом
синтезе). Регулирование размеров пор при создании искусственного пористого
материала или выбор естественного пористого материала с узким распределением
пор по размерам в требуемом диапазоне позволяет управлять размером
синтезируемых частиц. Нанореакторы могут использоваться как для получения нанокомпозитов
синтезируемого материала с материалом инертной матрицы, так и для получения
изолированных нанообъектов, для чего материал матрицы подвергается селективному
растворению [2]. В качестве естественных нанореакторов часто используются
цеолиты и слоистые двойные гидроксиды, в качестве искусственных - искусственные
цеолиты и пористые мембраны на основе оксидов металлов, созданные
электрохимическим методом.
К нанореакторам относят
наноразмерные полости, в ряде случаев нанопоры в различных матрицах, которые могут
быть использованы в качестве нанореакторов для получения желаемых
нанопродуктов. Основное назначение нанореакторов способствовать формированию
«переходного состояния» или активированного комплекса, преобразующегося в
нанопродукт практически без затрат на энергию активации. В этом случае основное
влияние на ход и направление процесса оказывает энтропийный член уравнения
Аррениуса, связанный со статистическими суммами или с активностью стенок
нанореактора и участвующих в процессе компонентов.
Создание активных и недорогих
наноструктур, способных существенным образом изменять свойства материалов,
является актуальной проблемой. Наиболее перспективным методом получения таких
наноструктур является синтез в нанореакторах полимерных матриц.
Преимуществами данного метода
являются низкие энергетические затраты, необходимые для запуска реакций в
нанореакторах полимерной матрицы, простота используемого оборудования,
возможность организации замкнутого, экологически чистого производства.
Современные методы получения энергии
часто связаны с загрязнениями окружающей среды побочными продуктами и
сопровождаются избыточным выделением тепла. Использование нанопродуктов,
содержащих металл, открывает перспективы развития альтернативной энергетики в
направлении применения их в качестве аккумуляторов водорода или в качестве
наноразмерных химических источников электрического тока.
Потребности развития экологически
чистых производств открывают широкие перспективы применения нанореакторов в
химии и в металлургии. Однако реализовать направленные синтезы в нанореакторах
трудно без предварительного математического моделирования, прогнозирующего
поведение химических частиц и их превращения в нанореакторах.
1. Методы получения наноматериалов
К настоящему времени разработаны
многочисленные методы получения наноматериалов как в виде нанопорошков, так и в
виде включений в пористые или монолитные матрицы. При этом в качестве нанофазы
могут выступать ферро- и ферримагнетики, металлы, полупроводники, диэлектрики и
др.
Согласно Фендлеру[3], важнейшими
условиями получения наноматериалов являются:
. Неравновесность систем.
Практически все наносистемы термодинамически неустойчивы, и их получают в
условиях, далеких от равновесных, что позволяет добиться спонтанного
зародышеобразования и избежать роста и агрегации сформировавшихся наночастиц.
. Однородность наночастиц. Высокая
химическая однородность наноматериала обеспечивается, если в процессе синтеза
не происходит разделения компонентов как в пределах одной наночастицы, так и
между частицами.
. Монодисперсность наночастиц.
Свойства наночастиц чрезвычайно сильно зависят от их размера, поэтому для
получения материалов с хорошими функциональными характеристиками необходимо
использовать частицы с достаточно узким распределением по размерам.
В дальнейшем было показано, что эти
условия не всегда обязательны для выполнения. Например, растворы
поверхностно-активных веществ (мицеллярные структуры, пленки Ленгмюра -
Блоджетт, жидкокристаллические фазы) являются термодинамически стабильными, тем
не менее они служат основой для формирования разнообразных наноструктур.
Все методы получения наноматериалов
можно условно разделить на несколько больших групп. К первой группе относят так
называемые высокоэнергетические методы, основанные на быстрой конденсации паров
в условиях, исключающих агрегацию и рост образующихся частиц. Основные различия
между отдельными методами этой группы состоят в способе испарения и
стабилизации образующихся наночастиц. Испарение можно проводить с
использованием плазменного возбуждения (plasma-ark), лазерного излучения (laser
ablation), вольтовой дуги (carbon ark) или термического воздействия. Конденсацию
осуществляют либо в присутствии ПАВ, адсорбция которого на поверхности частиц
замедляет рост (vapor trapping); либо на холодной подложке, когда рост частиц
ограничен скоростью диффузии; либо в присутствии инертного компонента, что
позволяет направленно получать нано композитные материалы с различной
микроструктурой [4]. Если компоненты взаимно нерастворимы, то размер наночастиц
можно варьировать с помощью термической обработки.
Ко второй группе относятся
механохимические методы (ball-milling), позволяющие получать нанокомпозиты при
совместном помоле взаимо нерастворимых компонентов в планетарных мельницах или
при распаде твердых растворов с образованием новых фаз под действием
механических напряжений.
Третья группа методов основана на
использовании пространственно-ограниченных систем - нанореакторов (мицелл,
капель, пленок и т.д.) [1]. К их числу относится синтез в обращенных
мицеллах, в пленках Лэнгмюра - Блоджетт и в адсорбционных слоях.
Ясно, что размер образующихся при этом частиц не может превосходить размер
соответствующего нанореактора, поэтому указанные методы позволяют получать
монодисперсные системы. К этой группе можно отнести также биомиметический и
биологический методы синтеза наночастиц, в которых в качестве нанореакторов
выступают биомолекулы (белки, ДНК и др.).
В четвертую группу входят методы,
основанные на формировании в растворах ультрамикродисперсных коллоидных частиц
при поликонденсации в присутствии поверхностно-активных веществ,
предотвращающих агрегацию.
К пятой группе относятся химические
методы получения высокопористых и мелкодисперсных структур (металлы Рике,
никель Ренея), основанные на удалении одного из компонентов микрогетерогенной
системы в результате химической реакции или анодного растворения. К числу этих
методов можно отнести также традиционный способ получения нанокомпозитов путем
закалки стеклянной или солевой матрицы с растворенным веществом, в результате чего
происходит кристаллизация этого вещества в матрице (стекла, модифицированные
полупроводниковыми или металлическими наночастицами). При этом введение
вещества в матрицу может осуществляться двумя способами: добавлением его в
расплав (раствор) с последующей закалкой и непосредственным введением в твердую
матрицу с помощью ионной имплантации.
Одним из наиболее распространенных
химических методов получения нано материалов является золь-гель-синтез. С его
помощью получают гомогенные оксидные системы, химическая модификация которых
(восстановление, сульфидирование и т.д.) приводит к формированию наночастиц
соответствующего материала в матрице [5]. Следует отметить, что использование
золь-гель-метода позволяет получать наноматериалы с улучшенными функциональными
свойствами благодаря контролю состава и структуры промежуточных продуктов. Он
привлекателен также своей реализуемостью в лабораторных условиях. Однако этот
метод имеет и серьезные недостатки. Во-первых, он не обеспечивает
монодисперсности частиц. Во-вторых, он не позволяет получать двумерные и
одномерные наноструктуры, а также пространственно-упорядоченные структуры,
состоящие из наночастиц, расположенных на одинаковом расстоянии друг от друга,
или из параллельных нанопластин с прослойками инертной матрицы, которые можно
синтезировать в нано реакторах. И наконец, в ряде случаев получение требуемого
нанокомпозита невозможно из-за химического взаимодействия частиц с
гелеобразующим агентом.
Необходимо отметить, что
использование свободных наночастиц и наноструктур в качестве материалов сильно
затруднено ввиду метастабильности вещества в нанокристаллическом состоянии. Как
уже отмечалось выше, это связано с увеличением удельной поверхности частиц по
мере уменьшения их линейных размеров до нанометровых, приводящим к возрастанию
химической активности соединения и усилению процессов агрегации. Чтобы
предотвратить агрегацию наночастиц и защитить их от внешних воздействий
(например, от окисления кислородом воздуха), наночастицы заключают в химически
инертную матрицу.
Анализ литературных данных
показывает, что к настоящему времени разработаны десятки способов матричной
изоляции наноструктур, которые можно условно разделить на две группы: получение
свободных наночастиц с последующим включением в инертную матрицу и непосредственное
формирование наноструктур в объеме матрицы в процессе ее химической
модификации.
Первая группа методов отличается
простотой в реализации, однако накладывает серьезные ограничения на возможности
выбора матрицы. В качестве последней, как правило, используют органические
полимерные соединения, не отличающиеся высокой термической устойчивостью и не
всегда обладающие необходимыми физическими свойствами (например, высокой
оптической прозрачностью). Кроме того, при инкорпорировании не исключены процессы
агрегации наночастиц.
Вторая группа методов позволяет не
только избежать этих недостатков, но и непосредственно контролировать параметры
наночастиц в матрице на стадии их формирования и даже менять эти параметры в
процессе эксплуатации материала. Используемые для этих целей матрицы должны
содержать структурные пустоты, которые могут быть заполнены соединениями,
последующая модификация которых приводит к формированию наночастиц в этих
пустотах. Другими словами, эти пустоты должны ограничивать зону протекания
реакции с участием внедренных в них соединений, т.е. выступать в роли
своеобразных нанореакторов. Очевидно, что, выбирая соединения с различной
формой структурных пустот, можно осуществлять синтез наноструктур различной
морфологии и анизотропии.
В качестве примера можно привести
синтез наноматериалов с использованием пористых оксидных матриц (обычно SiO2
или Аl2Оз) [6]. Однако ввиду неупорядоченности пористой
структуры таких матриц и достаточно широкого распределения пор по размерам с их
помощью практически невозможно получить удовлетворительно сформированные
наносистемы. Обычно нанокомпозиты, полученные на основе пористых оксидных
матриц, используют в катализе, где требования к монодисперсности частиц и их
морфологии не столь высоки. Кроме того, жесткая пористая структура
таких матриц не дает возможности менять размеры и морфологию частиц во время
синтеза; последние, как правило, жестко зависят от размера и морфологии пор,
т.е. при использовании одного типа матрицы можно получить лишь очень
ограниченный круг наноструктур.
Иногда для быстрого направленного
формирования наночастиц в матрице прибегают к дополнительным физическим
воздействиям, таким как ультразвук, микроволновое и лазерное облучение.
2. Синтез наночастиц в аморфных
матрицах
Первый практический опыт получения
нано частиц в аморфных матрицах - получение окрашенных стекол - относится к
временам древнего Египта. Однако механизм возникновения окраски в таких
аморфных матрицах был установлен лишь 100 лет назад. В настоящее
время кристаллизация стекла - основной и фактически единственный метод синтеза
наночастиц в аморфных матрицах. Известно, что процессы зародышеобразования и
роста кристаллов в аморфной матрице зависят как от условий термообработки
стекла, так и от его состава. Размер кристаллов можно регулировать, например,
путем создания определенной концентрации зародышей, что достигается
термообработкой стекла при относительно низкой температуре. Дальнейший рост
кристаллов происходит при более высокой температуре отжига. При этом следует
учитывать, что в процессе кристаллизации дисперсной фазы состав матрицы
изменяется и, соответственно, изменяется диффузионная подвижность ионов,
составляющих кристаллическую фазу (уменьшение коэффициента диффузии
способствует торможению роста и образованию более мелких частиц дисперсной
фазы, а увеличение - формированию более крупных частиц).
С использованием метода
кристаллизации стекла были получены разнообразные наночастицы
полупроводниковых, магнитных и каталитически активных материалов.
В частности, допированные
наночастицами полупроводников стекла получили широкое распространение в
качестве оптических фильтров. Их привлекательность обусловлена в первую очередь
нелинейно-оптическими свойствами, такими как значительный резонансный эффект,
зависимость положения края полосы поглощения от размера частиц, эффект удвоения
частоты падающего излучения (генерация второй гармоники) и др. [7]. Рассматривалась
возможность применения стекол, содержащих наночастицы высококоэрцитивных
магнитных фаз (гексаферритов бария и стронция), в качестве среды для записи и
хранения информации.
Однако метод кристаллизации стекла
не позволяет получать наночастицы с достаточно узким распределением по
размерам, что необходимо для проявления эффектов размерного квантования или
применения таких наночастиц в технологии. Решением проблемы является
использование пористых материалов с упорядоченной структурой пор, таких как
мезопористый оксид кремния и цеолиты, имеющих одномерные каналы или двумерные
полости. В этом случае удается получить наночастицы нитевидной,
пластинчатой или сферической формы (в зависимости от типа пористой структуры) с
узким распределением по размерам.
3. Синтез наночастиц в упорядоченных матрицах
Упорядоченные матрицы (или
нанореакторы) обычно классифицируют в соответствии с размерностью
присутствующих в них пор. Рассмотрим последовательно синтез наночастиц в нуль-,
одно- и двумерных нанореакторах.
.1 Получение наночастиц в нульмерных
нанореакторах
К нульмерным нанореакторам относятся
материалы, характеризующиеся открытой пористостью с упорядоченным расположением
сферических пор. К числу таких материалов в первую очередь следует отнести
цеолиты - природные и синтетические алюмосиликаты состава
ixMiiy(Alx+2ySizO2x+4y+2z)nН2О
К настоящему моменту известно более
150 типов цеолитов, из которых около 30 - природные цеолиты. Структура цеолитов
построена из тетраэдров [Si04]4- n [АlO4]5-,
объединенных общими вершинами в трехмерный каркас, пронизанный полостями и
каналами, в которых располагаются молекулы воды и катионы щелочных (Мi)
и щелочноземельных (Мii) металлов.
В отличие от атомов каркаса,
связанных между собой ковалентными связями, катионы, находящиеся в каналах,
связаны с матрицей только электростатически и могут легко обмениваться на
другие катионы в водных растворах.
Изоморфное замещение атомов алюминия
каркаса на атомы других элементов, таких как В, Ga, Fe, Со, Ti, V, и обмен
катионов, содержащихся в порах, позволяют направленно изменять свойства
цеолитов. Существует несколько факторов, обусловливающих возможность изоструктурного
замещения [6]:
близость радиусов замещаемого и
замещающего атомов (чем больше различие в радиусах, тем энергетически менее
выгодна замена);
замещение меньшего по размеру атома
на больший возможно при условии уменьшения координации последнего, и наоборот;
близость электроотрицательностей и
потенциалов ионизации замещаемого и замещающего атомов;
достижение минимума свободной
энергии в процессе изоморфного замещения с сохранением координационного числа.
По сравнению с другими
тектосиликатами цеолиты имеют более открытую структуру. Тетраэдры ТО4
(первичные сборочные узлы) формируют кольца различных размеров, в результате
соединения которых образуются более сложные структуры (вторичные сборочные
узлы), причем различным типам цеолитов соответствуют определенные сочетания
вторичных сборочных узлов. (Следует отметить, что угол Si -О -Si может
изменяться в достаточно широких пределах (135-165°), в результате чего
становится возможным существование кремниево-кислородных колец с различным
числом атомов.) Для цеолитов с большим содержанием кремния более характерны
кольца с 5 атомами кислорода, в которых угол Si-О-Si составляет около 145°.
Цеолиты с большим содержанием алюминия, имеющие в структуре большое количество
связей Si -О-А1, в основном построены из колец, содержащих 3 или 6 атомов
кислорода. В структурах природных цеолитов наиболее часто встречаются кольца с
4 или 6 атомами кислорода.
Классификация цеолитов представляет
собой достаточно сложную задачу. Каждая индивидуальная структура описывается
структурным кодом, содержащим только три заглавные латинские буквы - так
называемый IZA-код, принятый International Zeolite Association Structure
Commission. Эта кодировка применима как к алюмосиликатам, так и к некоторым
другим соединениям, имеющим аналогичную структуру и содержащим атомы элементов
(Si, Al, Р, Ga, Ge, В, Be и др.) в тетраэдрическом окружении.
Наиболее общий подход к синтезу
цеолитов основан на совместном гидролизе соединений кремния и трехзарядного
металла (чаще всего алюминия) в присутствии щелочи и четвертичного амина
(темплат). В качестве источников атомов кремния чаще всего используют
кремнийорганические соединения, подвергающиеся гидролизу, силикат натрия или
силикагель с большой площадью поверхности (>200 м2г-1),
в качестве источников ионов М3 + - соли (сульфаты, нитраты, хлориды)
или алкоксиды (изопропилаты, бутилаты) этих металлов, а в качестве темплатов -
первичные, вторичные, третичные и четвертичные амины, спирты и некоторые эфиры.
Схемы синтеза цеолитов различного
состава и структуры фактически одинаковы. Гели, содержащие соединения кремния и
алюминия, состаривают в течение длительного времени при температуре ниже
температуры кристаллизации (нередко в гидротермальных условиях) в присутствии
тем платов. Это время необходимо для формирования цеолита с необходимой
структурой и высоким выходом. Условия состаривания и природа темплатов
оказывают решающее влияние на структуру цеолитов. Присутствие
молекул темплата повышает кристалличность алюмосиликатного каркаса и влияет на
его структуру. Цеолиты некоторых структурных типов могут формироваться и без
использования темплата. Структурный тип получаемого цеолита зависит также от
природы и концентрации источника трехзарядного металла.
В цеолитах отрицательный заряд
матрицы компенсируется ионами щелочных металлов, аммония и/или алкиламмония (в
зависимости от использованных в ходе синтеза реактивов). Катионы металлов, как
правило, удаляют промыванием или ионным обменом на NH4+,
так как присутствие катионов металлов понижает термическую стабильность получаемых
матриц. Для удаления темплата готовые цеолиты отжигают в токе кислорода при 500
- 550°С, переводя их в так называемую Н-форму. Контроль соотношения Si:А1 в
цеолитах осуществляют стандартными методами количественного анализа.
В силу открытой пористости цеолитов
и высокой скорости диффузии газов в порах химические реакции с участием
интеркалированных катионов можно проводить при повышенных температурах
(например, восстановление водородом, необходимое для получения магнитных
нанокомпозитов) практически без разрушения матрицы, ограничивающей реакционную
зону. Указанные свойства открывают широкие возможности химического дизайна
нанокомпозитных материалов на основе цеолитов.
Наибольшее распространение получили
наноматериалы на основе цеолита Y (тип FAU). Структура Y-цеолита
состоит из вторичных сборочных узлов 6-6 (гексагональная призма), 6-2
(шестиугольник и квадрат с общим ребром), 6 (шестиугольник) и 4 (квадрат) (рис.
1).
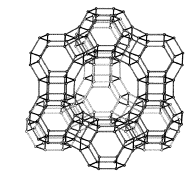
Рисунок 1 - Структура цеолита Y
Основным мотивом структуры цеолитов
FAU является усеченный кубом октаэдр - содалитовая ячейка или малая р-полость с
внутренним диаметром 0.66 нм, состоящая из четырехчленных (свободный диаметр
менее 0.1 нм) и шестичленных колец (диаметр ~0.22 нм) из Т-атомов. В вершинах
многогранника расположены 24 атома Т, а атомы кислорода находятся между ними.
При соединении таких многогранников через гексагональные призмы (диаметр
полости 0.36 нм) из Т-атомов образуется структура цеолитов (X и Y). Для них
характерна кубическая сингония с параметрами решетки а=24.345 А(рис.2).

Рисунок 2 - Усредненное изображение
кристалла NaY вдоль направления [110], полученное с помощью просвечивающей
электронной микроскопии (ПЭМ)
В структуре имеются различные типы
полостей: а-полость (а-cage, supercage) - самая крупная полость (диаметр 1.2
нм), находящаяся в окружении 8 усеченных октаэдров; р-полость (p-cage, sodalite
cage) - полость, ограниченная усеченным октаэдром; у-полость - гексагональная
призма (см. рис. 1).
Основным методом получения
нанокомпозитных материалов на основе цеолитов является обмен катионов Na+,
Н и NHJ, входящих в состав цеолитов, на катионы других металлов в водных
растворах с последующим восстановлением металла водородом. Получение
медьсодержащего цеолита ионным обменом нитрата меди с NaY-цеолитом или отжигом
смеси NaY-цеолита с хлоридом меди при 420СС. В случае твердофазного
отжига исходный цеолит NaY сначала стабилизировали, добавляя NaBr для
заполнения р-пол остей. Это позволило ввести медь в а-полости и повысить
термическую стабильность матриц. Восстановление проводили в атмосфере водорода
при температурах 300-600°С. В обоих случаях были получены частицы меди (3-7
нм), превышающие по размеру а-полости, что приводило к разрушению пористой
структуры.
Аналогичным образом получали нанокомпозиты
Au/NaY и Au-Fe/NaY. И в этом случае восстановление металлов приводило к
формированию наночастиц, значительно превышающих размеры а-полости цеолита.
Лантанидсодержащие цеолиты
(структурный тип FAU) образуются в результате ионного обмена катионов, входящих
в состав цеолитов, с хлоридами или нитратами РЗЭ. Отжиг модифицированных таким
путем цеолитов при 500°С приводит к образованию оксидов редкоземельных
элементов и частичному замещению атомов алюминия в структуре цеолита на атомы
РЗЭ, что повышает термическую стабильность цеолита. При достаточно высоких
содержаниях лантанидов наблюдается также образование оксидов лантанидов вне
цеолита. Помимо солей металлов можно применять также комплексные катионы.
В последнее время появились работы
по синтезу наночастиц интерметаллидов с использованием цеолитов.
Таким путем были получены (Pt, Pd)-за мешенные цеолиты. Аммонийные комплексы
палладия и платины внедряли в Y-цеолит ионным обменом. Термолиз комплексов
металлов в токе кислорода при температуре 300°С с последующим восстановлением в
токе водорода при 300°С приводил к формированию наночастиц сплава, содержащего
~40% платины, однако данные относительно расположения наночастиц в матрице
цеолита отсутствуют.
Для получения Au-Pd-интерметаллида в
Y-цеолите в качестве источника золота использовали комплекс [Au(en)2]3 +,
а в качестве источника палладия - Pd(NH3)4+. Ионный обмен
проводили в две стадии. Сначала вводили в матрицу цеолита комплекс палладия,
термолиз которого в кислороде сопровождался образованием атомов Pd и их
перемещением в более выгодные по координации р-полости. Затем осуществляли
ионный обмен с комплексом золота с последующим восстановлением композита.
Образование сплава проходило в ос-полости цеолита. В зависимости от соотношения
Au: Pd и состава исходного цеолита были получены частицы размером от 1 до 3 нм.
Продолжительный отжиг приводил к плавлению наночастиц с одновременным их ростом
(до 3.5-4 нм) и частичному разрушению пористой структуры цеолита.
Следует отметить, что синтез
нанокомпозитов в цеолитах не ограничивается применением матриц структурного
типа FAU. Известно немало работ, посвященных получению нанокомпозитов в
цеолитах структурного типа MFI (а также ZSM, MAS и др.), которые относятся к
одномерным нанореакторам.
Более удачный пример использования
цеолитов в качестве нанореакторов: смешанные сульфиды кобальта и молибдена в
Y-цеолите получали последовательным замещением ионов Na+ на ионы
кобальта с последующим введением в цеолит гексакарбонила молибдена в токе СО.
Согласно данным химического анализа, на каждую а-полость цеолита приходилось
около двух молекул Мо(СО)6. Общий состав образца, полученного на
этой стадии, описывается формулой Со(4мас.%)Мо(10 Mac.%)NaY. Далее образец
сульфидировали в токе H2S при разных температурах (25-400°С). Образовавшиеся
при этом частицы смешанных сульфидов имели размер 1 -2 нм.
Цеолиты активно применяют и в
качестве матрицы для получения люминесцентных наночастиц [5].
В настоящее время основной проблемой
при создании нанокомпозитов на основе цеолитов является сложность изучения
распределения наночастиц в матрице методом прямого наблюдения, таким как
просвечивающая электронная микроскопия (ПЭМ). Поэтому большее распространение в
синтезе изолированных в матрице нанокомпозитов получили матрицы, обладающие
упорядоченной пористой структурой с размером пор 2-50 нм. К числу таких матриц
относятся мезопористые молекулярные сита и пористый оксид алюминия.
.2 Получение наночастиц в одномерных
нанореакторах
Нанореактор, 1D (англ. nano-reactor,
1D) - разновидность нанореактора, размер которого в двух измерениях не
превышает 100 нм, а в третьем - существенно больше.
Одномерные нанореакторы,
обеспечивающие диффузию реагирующих компонентов лишь вдоль одного из
направлений, активно используются при получении протяженных нанообъектов -
наностержней и нановолокон [1].
В качестве твердофазных одномерных
нанореакторов могут быть использованы углеродные нанотрубки, пористый кремний,
цеолиты типа MFI, мезопористые молекулярные сита и пористые структуры на основе
оксида алюминия и титана, полученные методом анодирования.
Скол пленки пористого диоксида
титана, синтезированного методом анодного окисления металлического титана.
Может использоваться в качестве нанореактора для получения нановолокон
различных металлов методом электроосаждения, осаждения из газовой фазы и т.д.
(рис. 3).

Рисунок 3 - Скол пленки пористого
диоксида титана
Круг материалов, которые могут быть
использованы в качестве одномерных твердотельных нанореакторов, невелик. Он
включает цеолиты типа MFI, мезопористые молекулярные сита и мезопористые
структуры на основе оксида алюминия.
.2.1 Цеолиты структурного типа MF1
Цеолиты типа MFI обладают
упорядоченной системой каналов диаметром 0.54-0.56 нм с гексагональной
упаковкой (рис. 4). Наночастицы металлов в каналах MFI-цеолитов
обычно получают ионным обменом протонов (цеолит в Н+ - форме) на
катионы металлов или комплексы металлов с последующим мягким восстановлением в
токе водорода [6].
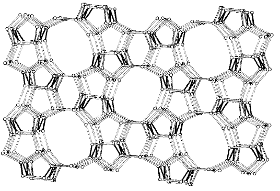
Рисунок 4 - Структура цеолита
структурного типа MFI
При восстановлении катионов металла
в матрице таких цеолитов следует ожидать формирования анизотропных наночастиц
(к сожалению, исследования распределения частиц по размерам и их анизотропии не
проводились из-за сложности, связанной с малым размером каналов).
.2.2 Мезопористые молекулярные
сита
Мезопористые молекулярные сита были
открыты исследователями американской компании Mobile Research and Development
Corporation в 1992г. Им удалось синтезировать семейство сит на основе SiO2
(МСМ-41), обладающих однородным и высокоупорядоченным распределением пор строго
контролируемого размера от 2 до 10 нм и с чрезвычайно высокой удельной
поверхностью (~ 1000 м2 г-1).
Наиболее распространенным методом
синтеза мезопористого SiO2 является темплатный метод. Темплат, или
шаблон, является центром, вокруг которого организуются основные структурные
единицы матрицы и формируется каркас. Удаление темплата приводит к образованию
полости такого же размера и формы, как темплат. Точность «отпечатка» после
удаления темплата зависит от нескольких факторов: природы взаимодействия
темплат-матрица, способности матрицы принимать очертания темплата,
относительных размеров темплата и структурных единиц матрицы. Схема темплатного
синтеза изображена на рис. 5.
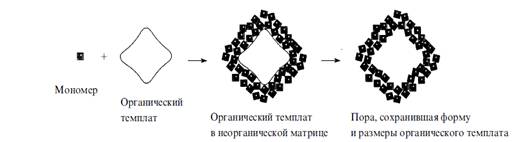
Рисунок 5 - Схема темплатного
синтеза
И хотя открытие молекулярных сит
датируется 1992 г., первое описание «темплатного синтеза» относится к 1949 г.,
когда было изучено гелеобразование тетраэтоксисилана (TEOS) в присутствии
индикатора метилоранжа (темплат). Образовавшийся в результате поликонденсации
TEOS силикагель селективно адсорбировал метилоранж. С тех пор этот довольно
простой и элегантный метод стал широко применяться для синтеза большого числа
органических и неорганических материалов.
Рассмотрим синтез молекулярных сит
на примере получения мезопористого SiO2 (МСМ-41). Образцы МСМ-41
получают поликонденсацией соединений кремния (Si(Ome)4 или Si(Oet)4)
в присутствии темплата, в качестве которого могут выступать различные молекулы,
в частности нековалентно связанные органические поверхностно-активные
вещества (ПАВ).
Бифункциональные молекулы
цетилтриметиламмоний-бромида амфифильны, т.е. содержат гидрофильную головную
группу и гидрофобный «хвост». В водном растворе такие молекулы объединяются в
мицеллы, в которых гидрофильные головные группы образуют внешнюю поверхность, а
гидрофобные «хвосты» обращены к центру. Степень мицеллизации и форма мицелл
зависят от концентрации ПАВ. При высоких концентрациях ПАВ происходит агрегация
мицелл с образованием жидкокристаллических фаз, структура которых зависит от
температуры и концентрации раствора. На рис. 6 приведена фазовая диаграмма
системы С16H33Nme3Br.
Реакционную смесь, содержащую водный
раствор ПАВ, тетраалкоксисилан и кислоту (или щелочь) термостатируют в течение
нескольких часов при температуре 80°С. При этом в результате гидролиза
тетраалкоксисилана вокруг мицелл ПАВ образуется мезопористый оксид кремния. К
числу параметров, влияющих на процесс гелеобразования, относятся pH раствора,
природа и концентрация темплата и кремнийсодержащего соединения, температура,
тип катализа и др.
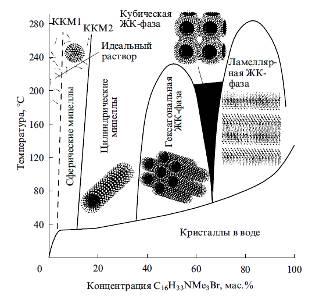
Рисунок 6 - Схематическая фазовая
диаграмма системы С16H33Nme3Br - H2O(ЖК-фаза
- жидкокристаллическая фаза) [39]
Особое значение придают pH среды, а
точнее ζ -потенциалу,
характеризующему электростатическое взаимодействие между коллоидными частицами
и определяющему структуру продуктов поликонденсации. В случае кислотного
катализа лимитирующей, по-видимому, является стадия гидролиза
тетраалкоксисилана, в то время как конденсация протекает относительно быстро.
Это приводит к формированию слаборазветвленных частиц золя.
Возможны различные виды связывания
темплат-матрица [5]. В рассматриваемом случае взаимодействие темплат-матрица
осуществляется за счет электростатических сил, водородных или
Ван-дер-Ваальсовых связей.
Иногда в качестве источников кремния
используют силикат натрия. Типы мезопористых фаз, полученных описанным методом,
приведены на рис. 7.
Альтернативным методом получения
мезопористого оксида кремния является гидротермальный синтез. Реакционную
смесь, содержащую водный раствор ПАВ и аморфный оксид кремния, подвергают
гидротермальной обработке при температуре порядка 150°С в течение продолжительного
времени. В результате такой обработки происходит растворение оксида кремния,
сопровождающееся перестройкой его структуры. Гидролизованный оксид кремния
образует мезофазы вокруг мицелл ПАВ.
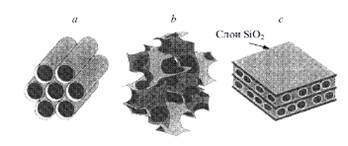
Рис. 7. Возможные структуры МСМ-фаз.
[5]
а - гексагональная, b - кубическая,
с- ламеллярная
Одной из важнейших характеристик
пленок является их ориентация относительно плоскости подложки. В случае
мезопористого оксида кремния особое внимание уделяется взаимному расположению
мезопор. Как правило, они располагаются параллельно подложке, так как энергия
взаимодействия пленка - подложка максимальна именно при такой ориентации
мицелл. Так, пленки МСМ-41 практически всегда обладают (100)-ориентацией.
Описано получение ориентированных пленок мезопористого оксида кремния на
стеклянных, полимерных, графитовых, слюдяных и кремниевых подложках.
Упорядочение пор в плоскости
подложки (т.е. формирование текстуры прокатки) наблюдается существенно реже и
возможно только в том случае, когда подложка обладает некоторым особым
направлением.
.2.3 Использование мезопористого
SiO, для синтеза нанокомпозитов
Область применения мезопористых фаз
и материалов на их основе очень обширна, что обусловлено наличием у них
уникальных свойств, таких как большая удельная поверхность, упорядоченная
система мезопор, однородное распре деление пор по размерам, высокая скорость
диффузии газов в объем материала и т.д. Мезопористые фазы находят применение в
качестве катализаторов и носителей для катализаторов; матриц для проводящих
полианилиновых и углеродных волокон; миниатюрных
реакторов для окислительно-восстановительных реакций; селективных
мембран; адсорбентов с высокой площадью поверхности; стандартов
пористости.
По структурным параметрам
наноструктуры, синтезированные внутри цилиндрических пор, подразделяют на
объемные наночастицы, нитевидные наночастицы и нанотрубки. Методы
синтеза нанокомпозитов на основе SiO2 можно разделить на две группы.
К первой группе относятся методы, основанные на пропитке пористого материала
солями металла с последующей химической модификацией композита.
Вторая группа методов основана на
модификации мезопористого диоксида кремния комплексами металлов (в частности,
комплексами, образующими химическую связь с атомами кремния или кислорода). Комплексы
можно внедрять в Si02 через газовую фазу, путем пропитки или
электрохимически.
Альтернативный метод синтеза
нитевидных наночастиц железа описан в работе. Авторы вводили неполярный
комплекс железа, способный разлагаться при низких температурах в условиях
незначительной агрегации наночастиц, в гидрофобную часть жидкокристаллической
мицеллы в матрице мезопористого диоксида кремния (рис. 8). В качестве такого
комплекса был выбран Ре(СО)5. Разложение карбонильного комплекса
проводили в вакууме под действием УФ-облучения. Образовавшиеся в результате
такого разложения частицы металлического железа (рис. 9,а), как было показано в
работах, содержали значительную долю аморфного железа, поэтому было предложено
дополнительно кристаллизовать частицы железа в объеме мезопористого диоксида
кремния путем отжига в токе водорода при невысоких температурах.
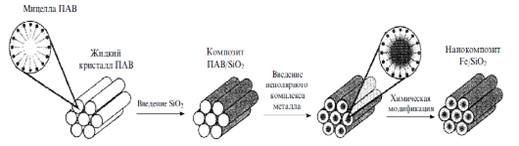
Рисунок 8 - Схема синтеза нанонитей
железа в матрице мезопористого диоксида кремния
Полученные после отжига частицы
характеризовались высоким значением параметра анизотропии, который оценивали с
использованием двух независимых методик: температурной зависимости магнитной
восприимчивости и малоуглового рассеяния поляризованных нейтронов. Оказалось,
что при разложении Fe(CO)5 при повышенной температуре происходит
более полная кристаллизация железа и, следовательно, рост нанокристаллов в
длину. Так как диаметр наночастиц при этом не изменяется, то происходит
увеличение фактора геометрической анизотропии.
Таким образом, удалось не только
получить наночастицы в порах мезопористого диоксида кремния, но и добиться их
гомогенного распределения.
Другой подход к синтезу наночастиц в
порах мезопористого SiO2, основанный на гидрофилизации внутренней
поверхности пор матрицы диоксида кремния остатками этилендиамина, был
реализован в работе.

Рисунок 9 - Микрофотографии
(просвечивающий режим) и электронная дифракция (на врезках) нанонитей железа в
матрице мезопористого диоксида кремния, полученных УФ-облучением в вакууме (а)
и дополнительной кристаллизацией при температуре 375°С (b)
наноматериал нанореактор синтез
Особый интерес представляет синтез
одномерных наночастиц с использованием пленок мезопористого диоксида кремния, в
частности магнитных нанокомпозитов для изготовления запоминающих устройств со
сверхвысокой плотностью записи информации.
В последние годы в связи с бурным
развитием информационных технологий появилась необходимость хранения и
обработки огромных объемов информации, что потребовало создания новых устройств
со сверхвысокой плотностью записи. Для этих целей были разработаны
принципиально новые магнитные материалы с прецизионными свойствами и
нелинейными магнитными характеристиками.
Согласно литературным данным,
наиболее перспективными магнитными материалами для создания устройств хранения
информации являются ферромагнитные одноразмерные структуры. Однако материалы,
полученные на основе наночастиц сферической формы, обладают малыми значениями
температур блокировки и практически нулевой коэрцитивной силой при комнатной
температуре, поэтому было предложено использовать анизотропные наночастицы.
Другим важным требованием к
магнитным материалам на основе наночастиц является условие жесткого
«закрепления» намагниченных наночастиц в некоторой матрице для предотвращения
их перемещения, агрегации и химического взаимодействия. Этого можно добиться,
синтезируя магнитные наночастицы в нанореакторах. Использование таких частиц
вместо металлических сплавов позволяет обойтись без защитного слоя на магнитном
носителе информации и тем самым повысить разрешающую способность считывающей
головки.
Перспективы использования магнитных
нанокомпозитов, полученных на основе эпитаксиальных пленок мезопористого SiO2,
в качестве запоминающих устройств со сверхвысокой плотностью записи. Известно,
что мезопористый SiO2 образует эпитаксиальные пленки на ряде
подложек. Оказалось, что при введении магнитного материала (например, железа) в
объем пор образуется упорядоченная система магнитных наночастиц диаметром в
несколько нанометров и длиной порядка сотен нанометров (рис. 10).
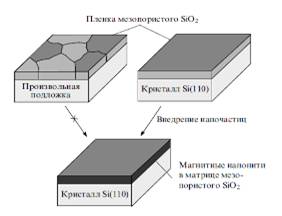
Рисунок 10 - Схема формирования
эпитаксиальных пленок нанокомпозитов Fe/SiO2 для использования в
качестве устройств со сверхвысокой плотностью записи
.2.4 Мезопористые алюмосиликаты
Перспективными матрицами для
получения нанокомпозитов являются мезопористые материалы на основе диоксида
кремния с упорядоченным расположением пор, в структуре которых часть атомов
кремния замещена атомами алюминия. Частичное замещение атомов Si на атомы А1 в
структуре диоксида кремния создает отрицательный заряд на матрице,
пропорциональный количеству введенного алюминия. В качестве положительно
заряженных противоионов, расположенных внутри пор, могут выступать катионы
переходных металлов, количество которых можно контролировать, изменяя
содержание алюминия в матрице. Восстановление катионов переходных металлов
позволяет получать нанокомпозиты с заданным содержанием металлической фазы в
алюмосиликатной матрице.
Дальнейшее применение алюмосиликатов
для получения нитевидных наночастиц переходных металлов показало, что
морфология наночастиц в образцах зависит от соотношения Si: Аl в
алюмосиликатных матрицах. При использовании алюмосиликатных матриц с небольшим
количеством алюминия (<10 мол.%) удалось получить нанокомпозиты, содержащие
нитевидные частицы. В матрицах с большим содержанием алюминия формировались не
только нанонити, но и сферические частицы размером 3-10 нм, при этом общее
количество переходного металла в нанокомпозите уменьшалось. По мнению авторов,
это объясняется формированием полигидроксокомплексов алюминия, которые
блокируют поры и препятствуют внедрению ионов металлов.
.3 Получение наночастиц в двумерных
нанореакторах
Нанореактор, 2D (англ. nano-reactor,
2D) - разновидность нанореактора, размеры которого по одному из измерений не
превышают 100 нм, а по двум другим - существенно больше.
Наиболее известными классами
веществ, используемых в качестве 2D-нанореакторов, являются слоистые двойные
гидроксиды и различные производные графита. В отличие от 1D- и
3D-нанореакторов, 2D-нанореакторы обычно используются для получения плоских
(условно-двумерных) наночастиц матричной фазы, в том числе графена, путем
интеркаляции реагентов в межслоевое пространство и последующей термической или
химической обработки материала, приводящей к увеличению объема
интеркалированного реагента, эксфолиации и расслаиванию матрицы [5].
В качестве двумерных нанореакторов
целесообразней всего использовать слоистые структуры с переменным размером
структурных полостей. В таких соединениях слои связаны между собой слабыми
ван-дер-ваальсовыми силами, что позволяет легко изменять размер межслоевого
пространства. Кроме того, слоистая структура позволяет значительно ускорить
диффузию газов в межслоевом пространстве и тем самым облегчить химическую
модификацию слоистых соединений.
Опубликовано несколько десятков
работ, посвященных синтезу нанокомпозитов с использованием слоистых матриц.
Наиболее широко применяются соединения с отрицательно заряженными слоями и
катионами в межслоевом пространстве - алюмосиликаты. Однако такие соединения,
как правило, нестехиометричны, сильно гидратированы и имеют сшивки между
слоями, что существенно усложняет синтез наноматериалов с их использованием и
негативно сказывается на воспроизводимости результатов. Естественно,
все это препятствует систематическому изучению механизмов формирования
наноструктур в слоистой матрице.
.3.1 Слоистые двойные гидроксиды
Наиболее распространенными
двумерными нанореакторами являются слоистые двойные гидроксиды (СДГ) состава M2+1-xM3+x
(OH)2[Xn-x/n · mН20] (X -
анион). К настоящему времени получены соединения с М2+ = Mg2+,
Zn2+, Fe2+, Со2+, Ni2 +, Cu2+,
Cd2 +, Sn2 +, Mn2+, Pd2+, Pt2+
и M3 + = Al3+, Fe3 +, Cr3+, Mn3
+, Ga3+, In3+, Bi3 +, Y3+, La3+,
V3+, Rh3 +, Ir3+, Ru3+ (см.
работы). Как правило, радиусы катионов М2+ и М3+,
участвующих в формировании слоистой структуры, не должны отличаться больше, чем
в полтора раза. В качестве аниона X- может выступать практически
любой анион или анионный комплекс. Структура СДГ представляет собой систему из
положительно заряженных гидроксидных слоев [М2+1-xМ3+x(ОН)2]x+
и анионов, находящихся в межслоевом пространстве (рис. 11). Помимо анионов в
межслоевом пространстве часто присутствуют лабильные молекулы воды. Структура
СДГ в целом стабильна за счет электростатического взаимодействия между
положительно заряженными гидроксидными слоями и межслоевыми анионами, несущими
отрицательный заряд.

Рис. 11. Структура слоистых двойных
гидроксидов
Заключение
В данной курсовой работе мной были
рассмотрены способы синтеза наночастиц в нанореакторах (синтез наночастиц в
аморфных матрицах и синтез наночастиц в упорядоченных матрицах). Были затронуты
перспективность и актуальность данного метода, а также области применения
нанореакторов (которые достаточно обширны), основное назначение нанореакторов,
которое заключается в том, чтобы способствовать формированию «переходного
состояния» или активированного комплекса, преобразующегося в нанопродукт
практически без затрат на энергию активации. Изучив множество статей и
публикаций, я пришла к выводу, что нанореакторы могут использоваться, как для
получения нанокомпозитов синтезируемого материала с материалом инертной
матрицы, так и для получения изолированных нанообъектов.
В процессе работы над данным
курсовым проектом мной были усвоены преимущества синтеза наночастиц в нанореакторах,
это создание активных и недорогих наноструктур, способных существенным образом
изменять свойства материалов, при низких энергетических затратах, необходимых
для запуска реакций в нанореакторах полимерной матрицы, простоте используемого
оборудования, и возможности организации замкнутого, экологически чистого
производства. В свою очередь, потребности развития экологически чистых
производств открывают широкие перспективы применения нанореакторов в химии и в
металлургии.
В заключение хотелось бы отметить,
что использование нанореакторов открывает широкие возможности для дизайна
функциональных наноматериалов с заданными физико-химическими характеристиками,
которые могут найти применение в самых разных областях науки и технологии
(например, в магнитных устройствах хранения информации, электронных
устройствах, сенсорах, катализаторах, мембранных материалах и т.д.).
Твердотельная матрица позволяет избежать агрегации наночастиц и защитить их от
внешних воздействий, что существенно облегчает практическое применение таких
материалов.
Список использованных источников
1. Лукашин А.В. Создание функциональных нанокомпозитов на
основе оксидных матриц с упорядоченной пористой структурой.// Автореферат
диссертации на соискание ученой степени доктора химических наук. 2009.
. Лукашин А.В., Калинин С.В., Никифоров М.П., Привалов
В.И., Елисеев А.А., Вертегел А.А., Третьяков Ю.Д. Влияние условий синтеза на
структуру слоистых двойных гидроксидов // ДАН. 1999. Т.364. №1. С.77-79.
. Бакеева И.В. Наноструктуры: основные понятия,
классификация, способы получения // Учебное пособие. второе издание. 2008. 68C.
. Напольский К.С., Колесник И.В., Елисеев А.А., Лукашин
А.В., Вертегел А.А., Третьяков Ю.Д. Синтез нитевидных наночастиц железа в
матрице мезопористого диоксида кремния // ДАН. 2002. Т.386. №2. С.207-210.
. Третьяков Ю.Д., Лукашин А.В., Елисеев А.А. Синтез
функциональных нанокомпозитов на основе твердофазных нанореакторов // Успехи
химии. 2004. Т.73. №9. С.974-998.
. Колесник И.В., Елисеев А.А., Гаршев А.В., Лукашин А.В., Третьяков
Ю.Д. Синтез наночастиц серебра в матрицах мезопористых алюмосиликатов с высоким
содержанием алюминия // Изв. РАН Сер. хим. 2004. Т.53. №11. C.2391-2393.
. Харламова М.В., Саполетова Н.А., Елисеев А.А., Лукашин
А.В. Магнитные свойства наночастиц γ-оксида железа в матрице мезопористого оксида кремния // Письма в
ЖЭТФ. 2007. Т.85. №9. С.538-543.