Биохимическая и физиологическая сущность ферментов
Содержание
Введение
. Ферменты: биохимическое
строение и физиологическая роль
. Методика определения
активности ферментов и ферментативного спектра в жидкостях организма
. Основные ферменты в моче в
норме и при патологии
. Ферментный спектр мочи при
заболеваниях почек
Заключение
Список использованной
литературы
Введение
На сегодняшний день остро стоит проблема совершенствования методов
диагностики различных заболеваний человека. В медицине достаточно давно
применяются в качестве диагностических инструментов анализы крови и анализы
мочи. При этом чаще используется именно биохимический анализ крови. Однако, как
свидетельствует практика, для выявления некоторых видов заболеваний, например
патологий почек и мочевыводящих путей большей диагностической ценностью
обладает не биохимический анализ сыворотки крови, а биохимический анализ мочи.
Все это определяет актуальность выбора темы работы.
И если раньше лечащие врачи в основном обращали внимание на уровень
глюкозы, общего белка, мочевины, креатинина в моче, а из ферментов - на уровень
амилазы (диастазы), то за последнее десятилетие значительную популярность
приобрели тесты на ферментный спектр мочи. Подобная методика очень востребована
не только в диагностике нефропатологий, но и при раннем выявлении тяжёлых заболеваний
у новорождённых, при комплексной диагностике заболеваний.
Энзимодиагностика - один из важнейших разделов клинической биохимии,
который имеет свои задачи, направления и специфические исследовательские
приёмы. В этой области достигнуты значительные успехи: открыт и выделен ряд
новых ферментов; изучена их роль в разных звеньях метаболизма; создана
концепция науки о ферментах, которая рассматривает заболевание как
последовательные нарушения в структуре и функциях энзимов. Благодаря этим
достижением стало возможным раскрытие патогенеза многих заболеваний на
молекулярном уровне, создание не только эффективных методов диагностики, но
профилактики, лечение больных. Поэтому в докладе мы рассмотрим биохимическую и
физиологическую сущность ферментов и набор основных энзимов в моче человека.
. Ферменты: биохимическое строение и физиологическая роль
Ферменты (энзимы) - это специфические белки, которые выполняют в
организме роль биологических катализаторов.
Являясь белками, ферменты имеют первичную, вторичную, третичную и многие
из них - четвертичную структуру.
При гидролизе ферментов образовывается смесь аминокислот. Известно свыше
20 различных аминокислот, входящих в состав белков.
Ферменты имеют общие с белками физико-химические свойства:
при гидролизе расщепляются на аминокислоты;
имеют высокую молекулярную массу;
создают коллоидные растворы;
плохо кристаллизуются;
очень неустойчивы к высоким температурам солей, тяжелых металлов, кислот,
щелочей и т.п;
имеют антигенные свойства.
Молекулярная масса ферментов характеризуется широкой вариацией - от
нескольких десятков тысяч до несколько миллионов.
Ферменты отличаются по своей структуре. Их разделяют на 2 группы -
простые и сложные. Простые, или однокомпонентные ферменты составляются только
из аминокислот. К ним относятся небольшое количество ферментов (рибонуклеаза,
амилаза, альдолаза, уреаза, пепсин и др.). Но большинство ферментов состоит из
двух компонентов: небелковой части или простетической группы и белковой части -
апофермента (рис. 1). Эти две части фермента отдельно не имеют силы, но только
в комплексе друг с другом они проявляют каталитическую способность.
Небелковый компонент распада ферментов называется коферментом.
Многие коферменты являются витаминами или их производными. В данное время
биохимии известно свыше 300 отдельных ферментов (а, возможно в ближайшее время
их станет больше, так как наука не стоит на месте), в состав которых входят в
качестве коферментов витамины или их производные. Как следствие, при
авитаминозах в организме наблюдается нарушение деятельности всех ферментных
систем.

Рисунок 1 Схема строения ферментов
Для определения механизма действия ферментов было предложено немало
теорий. Оказалось, что катализаторы лишь сокращают время, необходимое для
достижения равновесия химической реакции. Большинство химических реакций в
живых организмах нуждается в «запуске», что и выполняют ферменты (рис. 2).
В основе жизнедеятельности организма лежат химические преобразования
разных веществ, скорость которых определяют ферменты - биологические
катализаторы. Пищеварение, использование всех полезных веществ, которые
поступили в организм, рост, свертывание крови, мышечные сокращения и много
других физиологических процессов - все это построено на четкой, последовательной
работе ферментных систем.
Важнейшим признаком ферментов является не только их свойство ускорять
протекание химических реакций, но выборочно катализировать лишь определенный
путь преобразования данного субстрата. Это одна из основных функций ферментов
по сравнению с небиологическими катализаторами.
Возвратность ферментативных реакций заключается в способности ферментов
катализировать прямую и обратную реакцию. Так, например, липаза может при
определенных условиях расцепить жир до глицерина и жирных кислот, а также
катализировать его синтез из продуктов распада. Способность ферментов ускорять
химические процессы, как в сторону синтеза, так и распада, имеет большое
значение, так как создает возможность переключения этих процессов с одного на
другой, чем обеспечивает тесную взаимосвязь катаболизма и анаболизма, гибкость
и приспособленность обмена веществ к влиянию внешних и внутренних факторов.
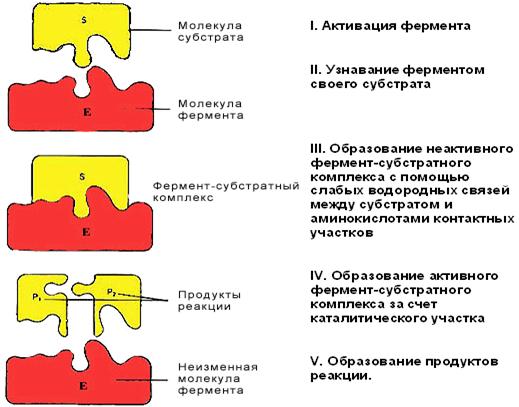
Рисунок 2 Схема механизма действия ферментов
Ферменты очень чувствительные к изменению ph среды (то есть к степени
кислотности и щёлочности), в которой они действуют. Каждый фермент имеет
оптимум ph, при котором он наиболее активен.
Для большинства ферментов оптимальная среда близка к нейтральному уровню
кислотно-щелочной среды (ph около 7,0), так как максимальная активность
ферментов проявляется при физиологических значениях ph, а в кислой или щелочной
среде их активность снижается. Но и из этого правила есть исключения, и их
немало. Например, пепсин, который находится в желудочном соке, активируется
лишь в очень кислой среде (ph 1,5 - 2,5). Ферменты очень чувствительные и к
температуре, как мы убедились. При повышении температуры до 40-500 ̊С
повышается активность большинства ферментов, что отвечает общеизвестному закону
ускорения химических реакций с повышением температуры. Установлено, что
повышение температуры на каждых 100 ̊С увеличивает скорость ферментативной
реакции в 1,5 - 2 раза. И потому необходимо придерживаться температурного
режима при проведении проб на ферменты.
Преобразование ферментов происходит подобно другим обменам белков
организма. Ферменты постоянно обновляются, синтезируются и распадаются, что
обеспечивает их надлежащий уровень в тканях.
В результате секреции или отмирании клеток ферменты попадают в кровь.
Пути вывода ферментов из крови различны. В плазме крови проходит инактивация
ферментов, потом они поглощаются клетками ретикулоэндотелиальной системы, где
вследствие катаболизма, распадаются. Часть ферментов выводится через
мочевыводящие пути и желудочно-кишечный тракт. Но, вывод ферментов с мочой и
желчью занимает небольшой удельный вес в механизме вывода ферментов из
организма. В основном, ферменты распадаются в плазме крови и тканях и выводятся
их неиспользованные конечные продукты обычными для белков каналами. Тем не
менее, анализ мочи на содержание ферментов является очень важным
диагностическим инструментом, позволяющим выявить многие патологические
процессы в организме.
В зависимости от типа катализируемых реакций, все ферменты делят на шесть
классов и несколько подклассов. Согласно этой классификации каждый фермент
обозначают шифром, который включает номера класса, подкласса и порядковый номер
фермента в подподклассе (табл. 1).
Таблица 1 Классификация ферментов по А.Ш. Бишевскому и О.А. Терсенову
|
Класс
|
Типа катализируемых реакций
|
|
№
|
Название
|
|
|
1
|
Оксидоредуктазы
|
Окислительно-восстановительные реакции
|
|
2
|
Трансферазы
|
Реакции межмолекулярного переноса: А - В + С = далее = А +
В - С
|
|
3
|
Гидролазы
|
Реакции гидролитического расщепления
|
|
4
|
Лиазы
|
Реакции негидролитического расщепления с образованием
двойных связей
|
|
5
|
Изомеразы
|
Реакции изменения геометрической или пространственной
конфигурации молекулы
|
|
6
|
Лигазы, или синтетазы
|
Реакции объединения двух молекул, сопровождающиеся
гидролизом макроэргов
|
. Методика определения активности ферментов и ферментативного
спектра в жидкостях организма
Методы определения ферментов в биологическом материале имеют свою
специфику, которая обусловлена очень низкой концентрацией ферментов в тканях.
Обычными методами количественного анализа эту концентрацию измерить невозможно,
поэтому измеряют не концентрацию самого фермента, а его активность. Активность
энзима оценивают по скорости специфической химической реакции, которая
катализируется данным ферментом. В свою очередь, скорость химической реакции
пропорциональна количеству превращаемого субстрата или количеству продукта,
который образовался за единицу времени (за час, минуту или секунду). Например,
активность фермента альфа-амилазы определяют по скорости расщепления крахмала,
что является субстратом для этого фермента. В качестве международной единицы
активности принимается количество фермента, способное превратить один микромоль
(мкмоль) субстрата за 1 мин в стандартных условиях. Международные единицы
количества фермента обозначаются символом МО.
МО - это активность фермента, который катализирует преобразование 1
мкмоля субстрата за 1 мин. (мкмоль/мин∙л).
Рекомендована также новая единица каталитической активности - катал
(символ. - кат), что представляет собой количество фермента, способного
осуществить преобразование 1 моля субстрата за 1 с в стандартных условиях.
кат - это активность фермента, который катализирует преобразование 1 моля
субстрата за 1 с в стандартных условиях (моль/с∙л).
Исходя из этого, 1 МО = 16,67 нкат.
В некоторых случаях, активность фермента выражается в единицах массы
субстрата (в граммах, миллиграммах), «преобразованного» 1 литром сыворотки
(плазмы) за единицу времени. Например, активность амилазы сыворотки крови
выражается в ч/(ч мин л).
А иногда активность устанавливается относительно вещества, с которым
фермент выводится, например, по отношению к объёму креатинина в моче.
Известно три типа изменений активности ферментов при патологии:
гиперферментемия - повышение активности ферментов, гипоферментемия - снижение
активности ферментов по сравнению с нормой, дисферментемия - появление в
жидкостях организма нетипичных ферментов.
Гипоферментемия случается относительно редко и касается в основном
секреторных ферментов (напр., холинэстеразы). В подавляющем большинстве случаев
она связана с генетически детерминированными нарушениями синтеза определенных
ферментов, реже - с ингибированием, усиленной деградацией или экскрецией
ферментов. Дисферментемия обусловлена в основном появлением в крови
органоспецифических ферментов (например, сорбитолдегидрогеназы (СДГ),
фруктозо-1-фосфатальдолазы Ф-1- ФА).
Гиперферментемия свидетельствует о некрозе или лизисе (растворении)
клеток, или о нарушении проницаемости клеточных мембран из-за дефицита
кислорода, недостатка глюкозы, действия лекарственных препаратов и других
ксенобиотиков, токсинов, бактерий, вирусов и пр. Развитию гиперферментемии
способствует клеточная пролиферация, усиление синтеза ферментов клетками,
повышение концентрации активаторов в кровяном русле. Степень и
продолжительность гиперферментемии зависят от целого ряда факторов:
молекулярной массы фермента, локализации его в клетке, концентрации в тканях,
степени и характера повреждения органа, массы поражённого органа, скорости
инактивации и вывод фермента. Основной сложностью использования определения
активности ферментов с диагностической целью является отсутствие специфичности
повышения ферментативной активности при повреждении определенной ткани или
органа. Поскольку много ферментов имеется в разных тканях и органах, то
повышение их активности в моче может быть связано с повреждением любого из этих
органов. Задача дифференциальной диагностики может быть решена одним из таких
способов: - определение более чем одного фермента. Разные ткани содержат
ферменты в разных количествах. Так, аланинаминотрансфераза (АлАТ) и
аспартатаминотрансфераза (АсАТ) содержатся в гепатоцитах (клетках печени) и
кардиомиоцитах (клетках сердца), но АлАТ существенным образом больше в печени,
а АсАТ - в сердце. Поэтому при повреждении печени относительно больше
повышается АлАТ, а при повреждении сердца - АсАТ;
определение в моче спектра изоферментов. Этот подход базируется на том,
что отдельные изоформы характерны для разных тканей;
определение активности ферментов в динамике. Скорость изменения
активности фермента в моче определяется разностью между скоростью его появления
в сыворотке крови и в моче. При инфаркте органа и некрозе поврежденных клеток в
сыворотке крови происходит повышение активности внутриклеточных ферментов,
специфических для данной ткани, потом после выхода всего фермента активность
его снижается. Важным является определение динамики изменения фермента и его
активности в период повышения в сыворотке, поскольку слишком раннее взятие
пробы для анализа может предшествовать повышению активности, слишком позднее -
также не разрешит получить необходимую информацию.
Биохимическое исследование мочи для определения ферментного спектра
проводят в лабораторных условиях для выявления различных заболеваний, оценки
состояния организма и динамики болезни, эффективности терапии. Окончательный
диагноз исключительно по анализам мочи не ставят, с его помощью, как правило,
обнаруживают отклонение и это является поводом к назначению дополнительных
исследований, способных окончательно обнаружить нарушение функции почек,
заболевание других внутренних органов, нарушения обмена веществ, скрытое
воспаление и т.д.
. Основные ферменты в моче в норме и при патологии
При анализе ферментного спектра мочи определяют наличие и количество
(ммоль/ ч∙л и т.д.) таких энзимов и веществ их распада как:
аланинаминопептидаза (ААП), амилаза (диастаза), аспартатаминотрансфераза
(АсАТ), бета-глюкуронидаза, гамма-глутамилтранспептидаза (ГГТП),
лактатдегидрогеназа (ЛДГ), лейцинаминопептидаза (ЛАП), лизоцим, холинэстераза
(ХЭ), щелочная фосфатаза (ЩФ), N-ацетил-альфа-гексозаминидаза (НАГ), и их
изоферменты (табл. 2).
Таблица 2 Основные ферменты мочи, анализируемые в лабораторных условиях
|
Название
|
Класс
|
|
Аланинаминопептидаза (ААП)
|
Гидролаза
|
|
Альфа-глюкуронидаза
|
Гидролаза
|
|
Амилаза (диастаза)
|
Гидролаза
|
|
Аспартатаминотрансфераза (АсАТ)
|
Трансфераза
|
|
Гамма-глутамилтранспептидаза (ГГТП),
|
Гидролаза
|
|
Лактатдегидрогеназа (ЛДГ),
|
Оксидоредуктаза
|
|
Лейцинаминопептидаза (ЛАП),
|
Гидролаза
|
|
Лизоцим
|
Гидролаза
|
|
Щелочная фосфатаза (ЩФ)
|
Гидролаза
|
|
N-ацетил-альфа-гексозаминидаза (НАГ)
|
Гидролаза
|
|
Холинэстераза (ХЭ)
|
Гидролаза
|
Аланинаминопептидаза (ААП) - это мембранный фермент, содержащийся в
полости кишечника, почек и др. органов, принимающий участие в гидролизе белков.
Используется как маркер почечных болезней.
Важная роль в почках принадлежит изоформам фермента аланинаминопептидазы
(ААП). Существует 5 изоформ ААП, каждая из которых является характерной для
определенного органа. ААП1 сосредоточена в основном в тканях печени, ААП2 - в
поджелудочной железе, ААП3 - в почках, ААП4 и ААП5 - в разных отделах стенок
кишечника.
Так, появление в моче изофермента ААП3 указывает на повреждение ткани
почки. При острых воспалительных процессах в почках, прежде всего, повышается
проницаемость клубочковых мембран, что служит причиной появления в моче белка,
в частности указанного фермента.
Нормальная активность фермента в моче: 0,97 - 0,12 ммоль/(ч∙л),
100- 190 ед/л. Основные источники фермента: кишечник, почки, печень,
поджелудочная железа.
Причины увеличение активности:
заболевания верхних мочевыводящих путей: гидронефроз, мегауретер,
пузырно-мочеточниковый рефлюкс, нефроптоз.
Амилаза представляет собой особый фермент, который принимает участие в
расщеплении углеводов. Это вещество производится в поджелудочной железе и
некоторых других органах, например, в слюнных железах. С помощью определения
уровня амилазы в крови можно выявить разные болезни органов пищеварительной системы.
Увеличение фермента можно проявить как при анализе мочи, так и при анализе
крови. Если амилаза повышена, это считается тревожным симптомом. Такой симптом
свидетельствует о заболеваниях желудочно-кишечного тракта и других органов.
Амилаза относится к наиболее важным ферментам пищеварения. Кровь человека
содержит два вида альфа-амилазы: S- Тип и Р-тип. Моча содержит около 65%
Р-типа, а кровь - до 60% S-типа. Во избежание путаницы Р-тип альфа-амилазы в
моче называют диастазой. Уровень амилазы в моче в десять раз превышает
активность амилазы в крови.
Нормальная активность диастазы: 20-160 ч/(ч ∙л).
Основные источники: поджелудочная железа, слюнные железы.
Причины увеличения активности: увеличение содержимого этого фермента в
моче является достоверным показателем поражения поджелудочной железы.
Это чаще всего случается при:
остром панкреатите или обострении хронического, поэтому анализ мочи на
диастазу играет важнейшую роль в диагностике этих заболеваний. При панкреатите
диастаза мочи увеличивается в несколько раз и достигает показателя 350- 600
ч/(ч ∙л), что является наиболее характерным симптомом воспаления ткани
поджелудочной железы;
воспалении слюнных желез (паротите), воспалении желчного пузыря
(холецистите), почечной недостаточности и сахарном диабете. Все эти заболевания
сопровождаются увеличением уровня показателя более, чем в 10 раз. Увеличение
этого фермента наблюдается при тяжелых травмах живота. Небольшое увеличение
диастазы мочи сопровождает острые воспалительные заболевания органов брюшной
полости - гастрит, колит, перитонит, аппендицит.
Причины уменьшения активности: снижение активности поджелудочной железы
приводит к снижению уровня диастазы. Такое состояние развивается при остром или
хроническом воспалении печени в стадии обострения, а также при ранних гестозах
беременных.
Аспартатаминотрансфераза (АсАТ) - фермент, который принимает участие в
обмене аминокислот. Катализирует перенесение аминогруппы от аспарагиновой
кислоты на альфа-кетоглутаровую кислоту с образованием щавелевоуксусной и
глутаминовой кислот. Переаминирование происходит при наличии кофермента -
пиридоксальфосфата - производного витамина В6.
Фермент содержится в тканях сердца, печени, скелетной мускулатуры,
нервной ткани и почках, в меньшей мере - в поджелудочной железе, селезенке и
легких. В миокарде активность АсАТ в 10000 раз выше, чем в сыворотке крови. В
эритроцитах энзим содержится в количестве в 10 раз большем, чем в сыворотке
крови.
Активность фермента у женщин ниже, чем у мужчин. При инфаркте миокарда
активность АсАТ в сыворотке может повышаться в 2-20 раз, причем повышенную
активность можно проявить еще до появления типичных признаков инфаркта на ЭКГ.
Существует зависимость между размерами ячейки некроза в сердечной мышце и
уровнем фермента в сыворотке крови.
Важна также прогностическая ценность определения активности АсАТ: если на
3-й день заболевания активность этого фермента не снижается, то прогноз
негативный. Рост активности может свидетельствовать как о расширении ячейки
инфаркта, так и о привлечении к процессу других органов и тканей, например,
печени. В моче наличие фермента свидетельствует о болезнях печени, сердца,
скелетных мышц, почек и др.
Нормальная активность: 0,1-0,45 ммоль/(ч ∙ л), 8-40 ед/мл.
Основные источники: сердечная мышца, печень, скелетная мускулатура,
головной мозг, почки.
Причины увеличения активности:
в 5 и больше раз превышает норму:
острое гепатоцеллюлярное поражение;
инфаркт миокарда;
шок;
острый панкреатит;
инфекционный мононуклеоз;
в 3-5 раз выше нормы:
обструкция желчных путей;
сердечная аритмия;
опухоли печени;
хронический гепатит;
мышечная дистрофия;
дерматомиозит;
до 3 раз выше нормы:
перикардит;
цирроз;
инфаркт легкого;
острые нарушения мозгового кровообращения;
гемолитическая анемия.
Бета-глюкуронидаза представляет собой фермент класса гидролаз,
катализирующий гидролитическое расщепление глюкуронида с образованием
глюкуроновой кислоты и спирта; содержится в большинстве тканей у млекопитающих.
Нормальная активность: 6,9-8,2 мЕ/мг креатинина.
Основные источники: мозговое и корковое вещество почек, клетки дистальных
канальцев.
Причины увеличение активности: острая почечная недостаточность.
Фермент гамма-глутамилтранспептидаза (ГГТП) (гамма-глутамилтрансфераза)
относится к классу трансфераз. Фермент катализирует перенесение глутаминовой
группы с гамма-глутаминового остатка на акцепторный пептид или L-аминокислоту.
Нормальная активность: у мужчины - 15 - 106 ед/л, у женщины - 10-66 ед/л.
Основные источники: ткани печени, почек, поджелудочной железы.
Причины увеличения активности:
обтурация внутрипеченочных и желчевыводящих путей;
заболевания печени (гепатит, цирроз печени, опухоли и метастазы в
печень), особенно те, что протекают при явлениях холестаза (снижения или
прекращения выделения желчи);
панкреатит и опухоли поджелудочной железы;
интоксикации этанолом (даже при воздержанном употреблении алкоголя),
наркотиками и седативными средствами.
Нужно подчеркнуть, что повышение активности ГГТП является одним из
наиболее ощутимых, хотя и неспецифичных, биохимических тестов, указывающих на
наличие поражения паренхимы печени, билиарной системы и алкогольной
интоксикации.
Лактатдегидрогеназа (ЛДГ) принадлежит к важнейшим клеточным ферментам,
которые принимают участие в процессе гликолиза. Как известно, пируват является
конечным продуктом гликолиза. В аэробных условиях пируват, под влиянием
окислительного декарбоксилирования, превращается в ацетил-КоА и потом
окисляется в цикле трикарбоновых кислот, высвобождая значительное количество
энергии. В анаэробных условиях пируват (пировиноградная кислота)
восстанавливается до лактата (молочной кислоты). Эту последнюю реакцию и
катализирует ЛДГ. Реакция обратная: в присутствии О2 лактат снова окисляется до
пирувата.
Нормальная активность: до 3200 нмоль/(с ∙ л) или до 195 МО при 25̊С
до 5330 нмоль/(с ∙ л) или до 320 МО при 30̊С
Основные источники (в порядке снижения): почки, скелетные мышцы,
поджелудочная железа, селезенка, печень, плацента. ЛДГ присутствует также в
эритроцитах, лейкоцитах и тромбоцитах крови.
Выделяют 5 изоферментов ЛДГ, которые представлены объединениям двух
субъединиц - Н (heart -сердце) и М (muscle-мышцы):
ЛДГ1 НННН 19-29 % преобладает в миокарде;
ЛДГ2 НННМ 23-37 % преобладает в миокарде;
ЛДГ3 ННММ 17-25 % неспецифичный изофермент;
ЛДГ4 НМММ 8-17 % преобладает в печени, скелетных мышцах;
ЛДГ5 ММММ 8-18 % преобладает в печени, скелетных мышцах.
Причины повышения активности:
болезни печени;
болезни сердца, в частности инфаркт миокарда;
болезни скелетных мышц;
болезни почек;
онкологические заболевания.
Значительное повышение активности ЛДГ установлено при инфаркте миокарда
(распространенном), остром вирусном гепатите, анемии, лейкозах, гемолитическом
состоянии, инфекционном мононуклеозе, нефропатии, острых массивных поражениях
скелетных мышц.
Умеренное повышение - при хронических поражениях печени, циррозах в
стадии обострения, панкреатите, пневмонии, инфаркте миокарда, инфаркте почки,
легких, мозга, злокачественных новообразованиях, прогрессирующей мышечной
дистрофии.
Следует отметить, что любая тканевая деструкция сопровождается
увеличением активности ЛДГ, при этом степень гиперферментемии зависит от
глубины и распространенности процесса.
Органная специфичность этого ферментного теста значительно возрастает при
определении изоферментов. Увеличение содержимого ЛДГ1 имеет большое значение
при диагностике инфаркта миокарда, ЛДГ2 и ЛДГ3 - острого лейкоза, ЛДГ4 и ЛДГ5 -
паренхиматозного поражения печени, ЛДГ3 - изофермент, активность которого
возрастает при многих злокачественных заболеваниях.
При инфаркте миокарда активность ЛДГ начинает повышаться через 24-36
часов от начала приступа, достигает максимума на 3-4 часу и снижается к норме
на 10-11 часу.
Лейцинаминопептидаза (ЛАП) участвует в пищеварении, действует на
N-конечные аминокислотные остатки белков особенно эффективно, если N-конечной
аминокислотой является L-лейцин. Фермент также откалывает амидные группы от
разных аминокислот.
Нормальная активность: до 6 ед/л.
Основные источники: печень, тонкий кишечник, почки, поджелудочная железа.
Причины повышения активности:
болезни печени: цирроз, вирусный гепатит, алкогольное поражение, желтуха;
болезни почек: хронический пиелонефрит, гломерулонефрит, диабетическая
нефропатия;
острый и хронический панкреатит, рак поджелудочной железы.
Активность ЛАП является чувствительным индикатором патологии печеночной
паренхимы. При остром инфекционном гепатите ее активность значительно
повышается уже в дожелтушный период. Кроме того, ЛАП можно считать одним из
биохимических маркеров холестаза.
Лизоцим, мурамидаза или N-ацетилмурамидкликангидролаза - фермент, который
разрушают клеточную стенку бактерий за счет катализа реакции гидролиза 1,
бета-связей между остатками N-ацетилмурамиевой кислотой и N-ацетил-D-глюкозамином в составе
гликановой цепочки пептидогликана и между остатками N-ацетил-D-глюкозамина в составе хитодекстрина. Лизоцим в
большом количестве содержится во многих секретах животных, таких как слезы,
слюна и слизь.
Нормальная активность в моче: 0,4 - 1,3 мг/100 мл.
Основные источники: почки, слезная жидкость, слизистые оболочки.
Причины увеличения активности:
острая моноцитарная или миеломоноцитарная лейкемия;
болезни почек;
болезни иммунной системы;
хронические инфекции (особенно туберкулёз, саркоидоз).
В моче лизоцим удается обнаружить лишь в тех случаях, когда его
активность в плазме превышает нормальные показатели в 3 раза. Кроме того,
лизоцим образуется в тканях почек, поэтому их повреждение также может
сопровождаться появлением фермента в моче.
Холинэстераза (ХЭ) - фермент из класса гидролаз карбоновых кислот,
субстратом которого являются сложные эфиры холина с уксусной, пропионовой или
масляной кислотами. Одной из важных качественных реакций на фермент является -
ингибирование алкалоидом эзерином.
ХЭ очень важен для нейрогуморальной регуляции организма, а также для
защиты организма от токсических веществ.
Нормальная активность: 6,9-8,2 мЕ/мг креатинина.
Основные источники: нервная ткань, скелетные мышцы, эритроциты.
Причины повышения активности в моче: повреждение клубочков почек.
Причины снижения активности: заболевания почек, инфаркт миокарда,
интоксикации, онкологические заболевания, наследственные нарушения синтеза
холинэстеразы.
Щелочная фосфатаза (ЩФ) - фермент - гидролаза, отщепляющий фосфат
(дефосфорилирование) от многих типов молекул, например, нуклеотидов, белков и
алкалоидов. Фермент проявляет наибольшую активность в щелочной среде.
Нормальная активность: у мужчин- 54-137 ед/л (900-2290 нмоль/ с∙л)
- у женщины - 44-126 ед/л (740-2100 нмоль/ с ∙ л).
Основные источники: костная ткань, паренхима и стенки желчных протоков печени,
проксимальные отделы извилистых канальцев почек, предстательная железа,
молочная железа, клетки слизистой оболочки кишечника, плацента. Особенно много
ее в растущих костях (фермент содержится в мембранах остеобластов), желчи и
плаценте. Локализуясь в клеточной мембране, фермент подключается к процессу
транспортировки биологически важных соединений (фосфора).
ЩФ - гетерогенный энзим, который включает отдельные изоферменты, каждый
из которых сосредоточен в определенном органе: печеночный, костный, кишечный и
плацентарный.
Причины увеличения активности:
физиологические:
детский возраст;
период полового созревания;
беременность;
гиперпаратиреоидизм;
остеомаляция;
остеомиелит;
болезнь Педжета;
остеогенная саркома;
метастазы опухолей в кости;
рахит;
заживание переломов;
гепатобилиарные заболевания:
холестаз;
обтурация селезёнки;
цирроз печени;
гепатит;
другие причины:
карцинома бронхов (особые изоферменты Регана, похожие на плацентарную
ЩФ);
большие дозы витамина D.
Низкая активность щелочной фосфатазы отмечена при гепатолентикулярной
дегенерации Коновалова-Вильсона, кретинизме, накоплении радиоактивных веществ в
костях, цинге, врождённом состоянии - гипофосфатезии. Применение
гиполипидемических препаратов (в частности клофибрата) также ингибирует
активность ЩФ.ацетил-альфа-гексозаминидаза (НАГ) - бактериальная
гликозил-гидролаза, способная гидролизовать α-O-гликозидную связь между галактозил-β1,3-N-ацетил-D-галактозамином и серином или
треонином в разнообразных гликопротеинах животного происхождения.
Нормальная активность: 30,8 мкмоль мальтозы/час на 1 ммоль креатинина.
Основные источники: почки, мышечная ткань.
Причины повышения активности:
болезни почек;
болезни минерально обмена, например, подагра.
биохимический
фермент моча патология
4. Ферментный спектр мочи при заболеваниях почек
При заболеваниях почек в моче появляются специфические ферменты: лизоцим
(мурамидаза), трансамидиназа, урокиназа, бета-глюкуронидаза, ЛАП, ГГТП,
аланинаминотрансфераза (АлАТ), АсАТ, ЛДГ, ААП, альдолаза, арилсульфатаза, НАГ,
глицинаминопептидаза и др.
Исследование ферментов в сыворотке крови при заболеваниях почек и
мочевыводящих органов имеет меньшее диагностическое значение, чем в гепатологии
и кардиологии, как с целью ранней диагностики, так и с целью дифференциальной
диагностики. Основным лабораторным исследовательский приемом у пациентов с
заболеваниями почек и мочевыводящей системы является общий анализ мочи. Этот
рутинный исследовательский прием применяют в диагностике и контроле хода ряда
заболеваний, а также при скрининговых обследованиях. Общий анализ мочи включает
органолептические исследования (количество, цвет, прозрачность, запах),
физик-химические и биохимические исследования (рн, относительная плотность,
осмоляльность, количество белка, мочевины, креатинина, глюкоза и др.), а также
микробиологические исследования и микроскопическое изучение мочевого осадка
(клетки, кристаллы, бактерии, выделение).
В клинической практике для диагностики заболеваний и поражений почек и
мочевыводящих путей используют также ферментурию. Среди приведенных ферментов
важнейшими являются ЛАП, ГГТП, НАГ, бета-глюкуронидаза, ААП.
Так для хронического пиелонефрита характерны полиурия, снижение
относительной плотности мочи, протеинурия, лейкоцитурия, бактериурия. На более
поздних стадиях наблюдают нарушение клиренса мочевины и креатинина, повышение в
крови уровня мочевины, креатинина и остаточного азота, нарушение электролитного
состава крови. При хроническом пиелонефрите в моче может повыситься активность
таких ферментов, как бета-глюкуронидаза, лизоцим и ЛДГ5. В почках в корковом
веществе содержится в основном ЛДГ1, а в мозговом - ЛДГ5. Поскольку при
пиелонефрите поражается в основном мозговое вещество, то этот изофермент имеет
высокую специфичность (до 96 %) для диагностики пиелонефрита.
Специфичность бета-глюкуронидазы, лизоцима и общей активности ЛДГ для
диагностики пиелонефрита относительно низкая. Общая активность ЛДГ в моче
повышается при опухоли мочевого пузыря, рака простаты и почек, при токсичной
нефропатии. Активность лизоцима повышается в моче при лейкозах.
Хронический гломерулонефрит, как аутоиммунное заболевание с диффузным
поражением обеих почек, очень сложно диагностировать. Поражение клубочков при
этом заболевании в 70% случаев обусловлено циркулирующими в крови иммунными
комплексами, которые откладываются вдоль внешней поверхности базальной мембраны
капилляров клубочков, вызывая в них воспаление. Хронический гломерулонефрит
является наиболее частой причиной хронической почечной недостаточности.
Основными изменениями в биохимическом анализе крови и мочи, которые
наблюдаются при этом заболевании, являются: протеинурия, снижение осмолярности
мочи, гематурия, повышение в крови уровня мочевины и креатинина, уменьшение
скорости клубочковой фильтрации (снижение клубочкового клиренса), повышение
содержимого неорганического фосфата в крови. В этих условиях чувствительным
тестом патологического процесса в почках выступает определение активности НАГ в
моче. Активность НАГ не связана с бактериальным загрязнением мочи, наличием в
моче эритроцитов и лейкоцитов, она хорошо коррелирует с эксрецией альбумина и
активностью патологического процесса при экстракапилярной и мембранозной формах
гломерулонефрита.
Причиной повышения НАГ в моче при гломерулонефритах является не
повышенная проницаемость базальной мембраны, а повреждение клеток проксимальных
отделов тубулярного аппарата почек, в лизосомах которых сосредоточенный этот
фермент. Считается, что повышенное выделение лизосомальных ферментов (НАГ,
бета-глюкуронидазаы и др.) из клеток во внеклеточное пространство может быть
обусловлено не только лизисом, а и экзоцитозом, что отображает скорее
функциональное, чем структурное поражение почек. Для диагностики и
дифференциальной диагностики хронических заболеваний почек, в частности хронического
гломерулонефрита, очевидно, наиболее чувствительными и специфическими являются
тесты с определением НАГ и галактозидазы. Однако при нарушении функции почек с
привлечением в патологический процесс тубулярного аппарата диагностическая
ценность этих тестов уменьшается. Клинически диабетическая нефропатия
проявляется протеинурией, гипертензией, снижением функций почек. Для ранней
стадии нефропатии характерными симптомами является микроальбуминурия, что
отражает нарушение физиологического состояния базальной мембраны клубочков, и
повышенное выведение с мочой микроглобулина и лизоцима, которые показывают
проявление канальцевых нарушений. Ранними признаками диабетической нефропатии
также является повышения в моче активности НАГ и ААП.
В целом для диагностики заболевания почек ферментный анализ мочи более
важен, чем ферментный анализ сыворотки крови.
Заключение
Ферменты (энзимы) - это специфические белки, которые выполняют в
организме роль биологических катализаторов. Многие коферменты (небелковые части
энзима) являются витаминами или их производными. Главное их свойство - это
способность выборочно катализировать биохимические процессы при возвратности
ферментативной реакции.
Ферменты очень чувствительны к температуре и кислотно-щелочной среде. В
тканях человека их мало, также как и в жидкостях, в т.ч. в моче. Поэтому
активность фермента оценивают по скорости специфической химической реакции,
которая катализируется данным ферментом. В свою очередь, скорость химической
реакции пропорциональна количеству превращаемого субстрата или количеству
продукта, который образовался за единицу времени. Известно три типа изменений
активности ферментов при патологии: гиперферментемия - повышение активности
ферментов, гипоферментемия - снижение активности ферментов по сравнению с
нормой, дисферментемия - появление в жидкостях организма нетипичных ферментов.
Биохимический анализ мочи, направленный на определение ферментного спектра,
ставит своей целью именно определение активности ферментов и выявления
изменений активности при патологиях (болезнях) для их диагностики. При анализе
ферментного спектра мочи определяют наличие и количество (ммоль/ ч∙л и
т.д.) таких энзимов и веществ их распада как: аланинаминопептидаза (ААП),
амилаза (диастаза), аспартатаминотрансфераза (АсАТ), бета-глюкуронидаза,
гамма-глутамилтранспептидаза (ГГТП), лактатдегидрогеназа (ЛДГ),
лейцинаминопептидаза (ЛАП), лизоцим, холинэстераза (ХЭ), щелочная фосфатаза
(ЩФ), N-ацетил-альфа-гексозаминидаза (НАГ), и их изоферменты.
Особенно эффективен энзимный анализ мочи при выявлении нефропатологий.
Список использованной литературы
1. Батюшкин
М.М., Повилайтете П.Е. Клиническая нефрология. - М.: Джангар, 2009. - 656 с.
. Биссвангер
Х. Практическая энзимология. - М.: Бином. Лаборатория знаний, 2010. - 328 с.
. Брашнов
Д.Г. Болезни почек. Профилактика, диагностика, лечение. - М.: Феникс, 2013. -
192 с.
. В.
Дж. Маршалл, С. К. Бангерт. Клиническая биохимия. - М.: Диалект, 2011. - 408 с.
. Галимова
М.Х. Ферментативная кинетика. Справочник по механизмам реакций. - М.: КомКнига,
2007. - 320 с.
. Гамаюрова
В.С., Зиновьева М.Е. Ферменты. Лабораторный практикум. - М.: Проспект науки,
2011. - 256 с.
. Данилова
Л.А. Анализы крови, мочи и других биологических жидкостей человека в различные
возрастные периоды. - М.: СпецЛит, 2013. - 112 с.
. Камикин
А.Г., Киселева А.С. Физиология и молекулярная биология мембран клеток. -
Academia, 2008. - 592 с.
. Кишкун
А.А. Клиническая лабораторная диагностика. Учебное пособие. - М.: ГЭОТАР-Медиа,
2014. - 720 с.
. Лукашевич
И.И., Савина М.И. Информативная система для оценки биохимических данных //
Клиническая лабораторная диагностика. 2008. № 9. С. 37.
. Марри
Р. и др. Биохимия человека. В двух томах. Там 1. - М.: Бином. Лаборатория
знаний, 2011. - 223с.
. Медицинские
лабораторные технологии. Руководство по клинической лабораторной диагностике. В
2 томах. Том 1. Под ред. Карпищенко А.И. - М.: ГЭОТАР-Медиа, 2012. - 474 с.
. Общая
и биоорганическая химия. Под ред. В.А. Попкова, Берлянда А.С. - М.: Academia,
2011. - 368 с.
. Плакунов
В.К. Основы энзимологии. - М.: Логос, 2011. - 128 с.
. Плакунов
В.К., Николаев Ю.А. Основы динамической биохимии. - М.: Логос, 2010. - 216 с.
. Ройтберг
Г.Е., Струтынский А.В. Внутренние болезни. Лабораторная и инструментальная
диагностика. - М.: МЕДпресс-информ, 2013. - 800 с.
. Строев
Е.А. и др. Практикум по биологической химии. - М.: Медицинское информационное
агентство, 2012. - 384 с.
. Тюкавкина
Н.А. и др. Биоорганическая химия. - М.: ГЭОТАР-Медиа, 2013. - 416 с.
. Хиггинс
К. Расшифровка клинических лабораторных анализов. Перевод Вишневской Е.,
Поповой А. - М.: Бином. Лаборатория знаний, 2013. - 456 с.
. Цынко
Т.Ф. Диагностика заболеваний по анализам крови и мочи. - М.: Феникс. 2010. -
156 с.