|
Назва токсину
|
Продуцент
|
|
Ботулотоксин
|
C. botulinum
|
|
Екзотоксин А
|
P. aeruginosa
|
|
Дифтерійний токсин
|
C. diphtheriae
|
|
Антраксевий токсин
|
B. anthrasis
|
|
Правцевий токсин
|
C. tetani
|
|
Стафілококовий a-токсин
|
S. aureus
|
2.1 Ботулотоксин
Ботулотоксин - це
нейротоксин білкової природи, який продукується бактеріями Clostridium
botulinum. Є одією з найсильніших отрут [5].
Ботулотоксин по серотипу
збудника поділяють на типу A, B, C1, C2, D, E, F, G, H, серед них найчастіше
зустрічається тип А. Летальна доза LD50 у середньому складає 0,001
мкг/кг ваги, найбільш отруйним є тип H (0,000028 мкг/кг ваги) [18].
Ботулотоксин також є
одним з найскладніших білків, що синтезуються живими організмами (див. рис.
2.1). Його маса складає близько 150 тисяч атомних одиниць маси. [5]
Clostridium botulinum, будучи строгими анаеробами, здатні до поділу тільки за умови
повної відсутності кисню. Екзотоксин, що синтезується бактеріями при
розмноженні потрапляє в організм разом з їжею, всмоктується в
шлунково-кишковому тракті впливаючи при цьому на нервову систему, викликає
порушення в роботі черепних нервів, скелетної мускулатури, нервових центрів
серця [18].
Ботулотоксин не має
смаку, кольору і запаху. Руйнується при кип’ятінні протягом 5-10 хвилин. Токсин
не руйнується при взаємодії з соляною кислотою шлункового соку [19].
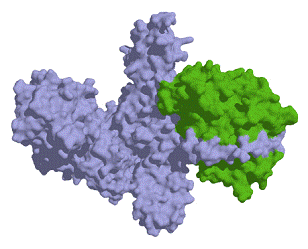
Рисунок 2.1 - 3D модель
поверхні ботулотоксину [19]
2.2 Екзотоксин А
Екзотоксин А, що
синтезується Pseudomonas aeruginosa - це термолабільний білок, який
складається з одного поліпептидного ланцюга довжиною в 613 амінокислот [17].
Він пригнічує синтез
білків через АДФ-рибозилювання і порушення структури матриці білкового синтезу
(фактор елонгації-2). Механізм його дії дуже подібний до дифтерійного токсину.
Дія екзотоксину А відображається в загальному токсичному ефекті, набряках,
некрозах, артеріальній гіпотензії, метаболічному ацидозі, дихальної
недостатності [20].
2.3 Дифтерійний токсин
Дифтерійний токсин, що
синтезується Corynebacterium diphtheriae, - це білок з молекулярною
масою 65,5 кДа, являє собою один поліпептидний ланцюг з 535 амінокислот (див.
рис. 2.2), що складається з двох субодиниць А і В, з’єднаних дисульфідними
містками. Домен В (термостабільний) сприяє зв'язуванню токсину з рецептором і
проникненню домену А в тканини. В свою чергу домен А (термолабільний)
забезпечує цитотоксичний ефект [21]. Незвичним є те, що ген токсину кодується
бактеріофагом. Дифтерійний токсин є одним з самих сильних токсинів у природі,
поступається лише ботулотоксину і правцевому токсинам [8].
Дифтерійний токсин має
механізм дії, схожий до ферменту АДФ-рибозилтрансферази. Він каталізує
перенесення НАД+ до дифтамідного залишку в факторі елонгації-2
еукаріот, інактивуючи цей білок. Таким чином, він діє як інгібітор РНК
трансляції [12, 21].
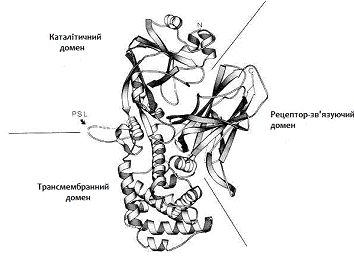
Рисунок
2.2 - Стрічкова діаграма рентгенівської кристалічної структури мономерного
дифтерійного токсину [21]
2.4 Антраксевий токсин
Антраксевий токсин, що
синтезується Bacillus anthracis, є термолабільним трьохкомпонентним
екзотоксином, він складається з трьох компонентів - набрякового (викликає
запалення і набряки), захисного антигена (див. рис. 2.3), який не має токсичних
властивостей і летального компоненту [22].
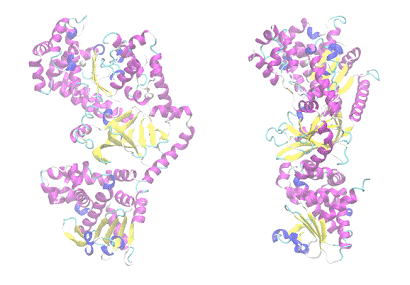
Потрапляючи до
органів-мішеней екзотоксин розпадається на ці три компоненти, поєднання яких в
наступному й буде обумовлювати переважання того чи іншого напрямку в перебігу
хвороби. Об'єднання захисного та набрякового компонентів призводить до
функціональних змін в циклі аденозинтрифосфат-аденозинмонофосфат (АТФ-АМФ) з
накопиченням цАМФ, внаслідок цього виникає прилив великої кількості рідини в
клітини і розвитку значного підшкірного набряку. Поєднання захисного та
летального компонентів зумовлює пригнічення фагоцитарної активності, лізис
макрофагів із вивільненням фактора некрозу пухлин-α та інтерлейкіну-1,
що викликає тяжкі, нерідко смертельні наслідки. Об'єднання набрякового та
летального компонентів полегшує проникнення збудників в клітини-мішені хазяїна [24].
2.5 Правцевий токсин
Правцевий токсин, або
тетанотоксин - це сильний токсин, він проникає в відростки нервових клітин і
потрапляє в центральну нервову систему, пригнічуючи сигнали гальмування в
синапсах (перешкоджаючи вивільнення гальмівних медіаторів) [17].
Тетанотоксин - білок з
молекулярною масою 150 кДа. Він є гетеродимером, що складається з ланцюга А,
масою 50 кДа, і ланцюга В, масою 100 кДа, які з’єднанні дисульфідним зв’язком.
Ланцюг В зв’язується з гангліозидами (GD2 и GD1b) на мембрані нейрона і
забезпечує проникнення в клітину. Ланцюг А - це цинк-залежна ендопептидаза, яка
розщеплює синаптобревін (білок, який здійснює екзоцитоз везикул з
нейромедіаторами в синаптичну щілину) [25].
При інфікуванні людини,
тетанотоксин поширюється по лімфатичній і кровоносній системах (не впливаючи
суттєво на них). Через нервово-м’язий синапс токсин потрапляє в аксон і далі по
механізму ретроградного транспорту, за участі моторних білків потрапляє до
центральної нервової системи [25] [26] (див. рис. 2.4). Там він блокує
вивільнення гліцину (гальмівного нейромедіатора) з нервових закінчень, через
розщеплення синаптобревіна [27]. Токсин необоротно вражає нервові закінчення, і
функція нерва може відновитися тільки шляхом виникнення нових синапсів [25].
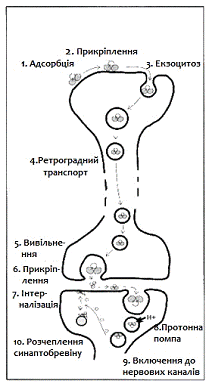
Рисунок 2.4 - Механізм
дії тетанотоксину [26]
3.6 Стафілококовий a-токсин
Стафілококовий a-токсин синтезується Staphylococcus aureus у вигляді
молекули попередника, яка складається з 319 амінокислот і має на N-конці
сигнальну послідовність з 26 амінокислотних залишків. Готовий токсин, що
виділяється являє собою гідрофільну молекулу молекулярної маси близько 33 кДа,
в якій відсутні залишки цистеїну [28, 29].
На поверхні плазматичної
мембрани 7 протомерів токсину утворюють грибоподібний гептамер (232 кДа), який
містить 3 домена (див. рис. 2.5) [30,31]. Домени, що утворюють «шляпку» і
«край», розміщуються на зовнішній поверхні плазматичної мембрани, а домен
«ніжки» виконує роль трансмембранного каналу.
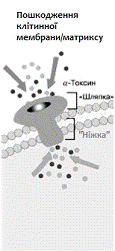
Рисунок 2.5 -
Пошкодження клітинних мембран під дією a-токсину S. aureus [32]
Після зв’язування і
олігомеризації «ніжка» гептамеру a-токсину проникає в уражену клітину і порушує вхід і вихід іонів. a-токсин володіє цитолітичними властивостями по відношенню до
різних типів клітин, включно з моноцитами, лімфоцитами, еритроцитами,
тромбоцитами і ендотеліоцитами людини [29].
Розрізняють три
послідовні стадії пошкодження клітинної мембранни під дією a-токсину. Протомери токсину спочатку зв’язуються з мембраною
клітини-мішені за допомогою рецепторів або неспецифічно абсорбуються
фосфотиділхоліном чи холестеролом, які входять до біліпідного шару мембрани
[28]. Потім, зв’язані з мембраною протомери олігомеризуються в нелітичний гептамерний
комплекс. І в кінці, гептамер зазнає ряд конформативних змін, кінцевим
результатом яких є формування «ніжки», котра проникає крізь цитоплазматичну
мембрану [30,31]. Через пору, що утворилась, відбувається вхід і вихід
невеликих молекул і йонів, що приводить до набухання і загибелі клітин, які
мають ядра, і осмотичному лізису еритроцитів [32].
3. Застосування
екзотоксинів
Деякі з сильних
хвороботворних токсинів використовують при вивченні біології клітин та в
медичних цілях [32].
Багато бактеріальних
екзотоксинів можуть бути модифікованими до анатоксинів, які більше не виявляють
цитотоксичність, але можуть зберегти імуногенність. Екзотоксини можуть бути
використані в якості терапевтичних агентів для лікування різних розладів. Крім
того, бактеріальні токсини використовуються в якості дослідницьких інструментів
для вивчення різних метаболічних шляхів еукаріотів [4].
3.1 Значення в
біотехнології
Велике значення мають
екзотоксини при вивченні біології клітин, оскільки їх можна використовувати як інструменти
при вивченні метаболічних шляхів еукаріотів, наприклад, G-білок-опосередкованої
сигнальної трансдукції; холерний токсин і подібний до нього термолабільний
токсин E. coli, так само як і токсин B. pertussis, застосовуються
при вивченні механізму активації аденілатциклази і ролі цАМФ як вторинного
посередника еукаріотичних клітин. [33-35].
3.2 Значення в медицині
Екзотоксини здобули
досить широке застосування в медицині. Екзотоксини можуть бути використані в
якості терапевтичних агентів для лікування різних розладів, у тому числі при
лікуванні м'язових спазмів від токсину ботулізму. Нетоксичні форми екзотоксинів
були використані в якості носіїв для транспорту гетерологічних молекул, що
викликають імунну відповідь, а також, як агенти у розвитку клітинно-специфічної
хіміотерапії [32].
Активність деяких
сильний екзотоксинів використовується в якості потенціальної терапії ряду
онкологічних захворювань. Вони можуть використовуватись безпосередньо або в
якості компонентів імунотоксинів [36-38]. Например, Stx-токсин ентерогеморагічної
E.coli зв’язується з гліколіпідом CD77, який виділяється В-лімфоцитами
деякий В-лімфом [39,40]. Це стало поштовхом до досліджень, які показали, що
Stx-токсин може «очищати» кістковий мозок гризунів (потенційно - і людський) від
злоякісних CD77+ В-лімфоцитів перед аутологічною пересадкою
кісткового мозку [41]. Інші токсини, які інгібують білковий синтез, такі, як
дифтерійний токсин, екзотоксин А у штамів Pseudomonas spp., часто
використовуються в якості цитотоксичних компонентів імунотоксинів. Ці речовини,
поєднуючи в собі ферментативно активну частину молекули токсину і моноклональні
антитіла, проходять клінічні випробування для лікування хворих на В-лімфоми,
лейкемії та при трансплантації кісткового мозку.
Ботулотоксин типа А має
декілька клінічних показань [42,43]. Один із них - це лікування м’язової
гіперактивності. Мікродози ін’єкцій очищеного токсину в певні точки викликає
параліч м’язів-мішеней і усувають м’язові спазми. Терапію потрібно постійно
продовжувати, оскільки дія токсину продовжується тільки декілька місяців.
Вперше ботулотоксин типу А був застосований при лікуванні порушень функцій
окорухових м’язів [44]. Ефективність ботулотоксин типу А доведена також при
багатьох інших порушень, включно з дистонією м’язів шиї, гортані, і рук, тремор
і нервовий тик [42,43]. Ботулотоксин типу А використовується і в косметичних
цілях для зменшення глибоких зморшок, які викликані контрактурою м’язів обличчя
[45].
Інший бактеріальний
екзотоксин, який використовується в медиині - стрептокіназа деяких патогенних
штамів стрептококів, яка є активатором плазміногену. Протеолітична активність
стрептокінази використовується для відновлення прохідності трамбованих артерій
при інфаркті міокарду [46,47].
Іншим методом
використання екзотоксинів є вакцини. Багато бактеріальних екзотоксинів можуть
бути хімічно модифіковані, до анатоксинів, які більше не виявляють
цитотоксичність, але можуть зберегти імуногенність. Дослідження показали, що
бактеріальні токсини також можуть бути генетично модифікованами в анатоксини,
які забезпечують більш широкий спектр дії вакцин. Вакцини, націлені на
токсичний компонент бактеріальних патогенів, є доведеним ефективним засобом
профілактики деяких хвороб. Токсоїдні вакцини складаються з частково очищених
токсинів, отриманих з над осадової рідини культури бактерій, зокрема C.diphtheriae,
C.tetani, B.anthracis [32]. При виготовлені вакцин застосовують
формальдегід для усунення токсичності дифтерійного чи правцевого токсину;
вакцина проти сибірки містить захисний антиген і невелику кількість летального
і набрякового фактору. Безклітинна вакцина проти коклюшу, яка має у своєму
складі або один анатоксин коклюшу, або ще декілька компонентів, має однакову
ефективність і значно меншу реактогенність у порівнянні з вакциною, яка містить
цілі вбиті клітини [48].
Наступні покоління
вакцин можна поділити на три категорії: очищенні анатоксини, інактивовані
хімічним або генетичним методом; живі ослаблені штами збудників, які продукують
генетично змінений анатоксин; живий ослаблений незв’язаний векторний штам,
наприклад V.cholerae или Salmonella spp., які продукують
необхідний анатоксин [49].
Антитоксини, отримані
проти токсинів дифтерії, ботулізму та правцю використовуються при лікуванні
важкохворих. Досліджуючи можливість використання специфічної антисироватки
проти Stx-токсинів, які виділяються E.coli O157:H7, для попередження
небезпечного для життя ускладнення - гемолітико-уремічного синдрому [32].
Список використаної
літератури
1. Экологический энциклопедический словарь. - Кишинев: Главная
редакция Молдавской советской энциклопедии. И.И. Дедю. 1989.
2. Микробиология: словарь терминов, Фирсов Н.Н., М: Дрофа,
2006 г.]
. Тимаков В.Д., Левашев В.С., Борисов Л.Б., Микробиология:
Учебник. - 2-е изд., перераб. и доп. - М.: Медицина, - 1983. - 517 c.
. Moselio Schaechter, Desk Encyclopedia of Microbiology //
Exotoxins / Edited by Joseph T. Barbieri. - L.: Academic Press, - 2004. - P.
427-435.
. Супотницкий М.В., Микроорганизмы, токсины и эпидемии. -
М.: Вузовская книга, 2000. -376 с.
. Doris V. Sweet, Registry of toxic effects of chemical
substances (RTECS): comprehensive guide to the RTECS. - Cincinnati, Ohio: U.S.
Dept. of Health and Human Services. - 1997. - 177 p.
. Alouf J.E. (2000). Bacterial protein toxins. An overview.
Methods Mol Biol. 145: 1-26.
. Collier, R.J. (1975). Diphtheria toxin: mode of action
and structure. Bacteriol. Rev. 39 (1), 54-85.
. Moss, J., and Vaughan, M. (1990). «ADP-Ribosylating
Toxins and G proteins: Insights into Signal Transduction.» Am. Soc. Microbiol,
Washington, D.C.
. Sixma, T.K., Pronk, S.E., Kalk, K.H., Wartna, E.S., van
Zanten, B.A., Witholt, B., and Hol, W.G. (1991). Crystal structure of a cholera
toxin-related heat-labile enterotoxin from E. coli. Nature 35 (6326), 371-377.
. Saelinger, C.B., and Morris, R.E. (1994). Uptake and
processing of toxins by mammalian cells. Meth. Enzymol. 235, 705-717.
. Barbieri, J.T., and Burns, D. (2003). Bacterial
ADP-ribosylating exotoxins. In. «Bacterial Protein Toxins» (D. Burns, J.T.
Barbieri, B. Iglewski, and R. Rappuoli, eds.), ASM, Washington, DC.
. Sandvig, K., Garred, O., Holm, P.K., and van Deurs, B.
(1993). Endocytosis and intracellular transport of protein toxins. Biochem.
Soc. Trans. 21 (Pt 3), 707-711.
. Stathopoulos, C., Hendrixson. D.R., Thanassi, D.G., Hultgren,
S.J., St Geme, J.W., 3rd, and Curtiss, R., 3rd (2000) Secretion of virulence
determinants by the general secretory pathway in gram-negative pathogens: an
evolving story. Microbes Infect. Jul. 2 (9): 1061-72.
. Lesnick, M.L. Guiney, D.G. (2001). The best defense is a
good offense-Salmonella deploys an ADP-ribosylating toxin. Trends Microbiol.
Jan; 9 (1): 2-4;
. Dobrindt, U., Janke, B., Piechaczek, K., Nagy, G.,
Ziebuhr, W. Fischer, G., Schierhorn, A., Hecker, M., Blum-Oehler, G., and
Hacker, J., 2000 Oct. Toxin genes on pathogenicity islands: impact for
microbial evolution. Int J Med Microbiol. 290 (4-5): 307-11.
. Елинов Н.П. Химическая микробиология. - М.: Высшая школа,
1989. - 448 с.
. Botulinum Toxin as a Biological Weapon: Medical and
Public Health Management / Stephen S. Arnon, R. Schechter, T.V. Inglesby and
others // Journal of the American Medical Association. - 2001. - Vol. 285, №8.
- P. 1059-1070.
. Crystal structure of botulinum neurotoxin type A and
implications for toxicity / D.B. Lacy, W. Tepp, A.C. Cohen and others // Nature
structural biology. - Vol. 5, №10. - P. 898-902.
. Yates S.P., Merrill A.R. Elucidation of eukaryotic
elongation factor-2 contact sites within the catalytic domain of Pseudomonas
aeruginosa exotoxin A // Biochem. J. - 2004. - Vol. 379, №3. - Р. 563-572.
. Baron S. Medical Microbiology, 4th edition // Corynebacterium
Diphtheriae: Diphtheria Toxin Production / Edited by J.R. Murphy. - Galveston:
University of Texas Medical Branch at Galveston, 1996. - Chapter 32.
. Brossier F., Mock M. Toxins of Bacillus anthracis //
Toxicon. - 2001. - Vol. 39, №11. Р. 1747-1755.
. A.D. Pannifer et al. Crystal structure of the anthrax
lethal factor // Nature. - 2001. - Vol. 414. - P. 229-233.
. Голубовська О.А. Інфекційні хвороби. - Київ: ВСВ
«Медицина». - 2012. - С. 728.
. Tetanus / J.J. Farrar, L.M. Yen, Т. Cook and others //
Journal of Neurology, Neurosurgery, and Psychiatry. - 2000. - Vol. 69, №3. - Р.
292-301.
. Lalli G., Gschmeissner S., Schiavo G. Myosin Va and
microtubule-based motors are required for fast axonal retrograde transport of
tetanus toxin in motor neurons // Journal of Cell Science. - 2003. - Vol. 116,
№22. Р. 4639-4650.
. Tetanus and botulinum-B neurotoxins block
neurotransmitter release by proteolytic cleavage of synaptobrevin / G. Schiavo;
F. Benfenati; B. Poulain and others // Nature. - 1992. - Vol. 359. P. 832-835.
. Bhakdi S., Tranum Jensen J. Alpha-toxin of Staphylococcus
aureus // Microbiol Reviews. - 1991. - Vol. 55, №4. - P. 733-751.
. Tomita T., Kamio Y. Molecular biology of the pore-forming
cytolysins from Staphylococcus aureus, alpha - and gamma-hemolysins and
leukocidin // Biosci Biotechnol Biochem. - 1997. - Vol. 61, №4. Р. 565-572.
. Structure of staphylococcal alpha-hemolysin, a heptameric
transmembrane pore / L. Song, M.R. Hobaugh, C. Shustak and others // Science. -
1996. - Vol. 274. - P.1859-1866.
. Membrane insertion: the strategies of toxins / C.
Lesieur, S.B. Vecsey, L. Abrami and others // Molecular Membrane Biology. -
1997. - Vol. 14. - P. 45-64.
. Clare K. Schmitt, Karen C. Meysick, Alison D. O’Brien
Bacterial Toxins: Friends or Foes? // Emerging Infectious Diseases. - 1999.
Vol.5, №2. - Р. 224-233.
. Harnett M.M. Analysis of G-proteins regulating signal
transduction pathways // Methods of Molecular Biology. - 1994. - Vol. 27. - P.
199-211.
. Identification of the predominant substrate for
ADP-ribosylation by islet activating protein / G.M. Bokoch, T. Katada, J.K.
Northup // The Journal of Biolical Chemistry. - 1983. - Vol.258. - P.
2072-2075.
. Neer E.J. Heterotrimeric G proteins: organizers of
transmembrane signals // Cell. - 1995. - Vol. 80. - P. 249-257.
. Pastan I. Targeted therapy of cancer with recombinant
immunotoxins // Biochim Biophys Acta. - 1997. - Vol. 1333. - P.1-6.
. Ghetie M.A., Ghetie V., Vitetta E.S. Immunotoxins for the
treatment of B-cell lymphomas // Molecular Medicine. - 1997. - Vol. 3, №7. -
P.420-427.
. The emerging role of immunotoxins in leukemia and
lymphoma / U. Winkler, S. Barth, R. Schnell and others // Annals of Oncology. -
1997. - Vol.8, №1. - P.139-146.
. Murray L.J., Habeshaw J.A., Wiels J. Expression of Burkitt
lymphoma-associated antigen (defined by the monoclonal antibody 38.13) on both
normal and malignant germinal-centre B cells // Int. J. Cancer. - 1985. -
Vol.36. - P.561-565.
. Taga S., Mangeney M., Tursz T. Differential regulation of
glycosphingolipid biosynthesis in phenotypically distinct Burkitt’s lymphoma
cell lines // Int. J. Cancer. - 1995. - Vol. 61. - P. 261-267.
. LaCasse E.C., Saleh M.T., Patterson B. Shiga-like toxin
purges human lymphoma from bone marrow of severe combined immunodeficient mice
// Blood. - 1996. - Vol. 88, №5. - P.1551-1567.
. Kessler K.R., Benecke R. Botulinum toxin: from poison to
remedy // Neurotoxicology. - 1997. - Vol. 18. - P. 761-770.
. Averbuch-Heller L., Leigh R.J. Medical treatments for
abnormal eye movements: pharmacological, optical and immunological strategies
// Aust. NZJ Ophthalmol. - 1997. - Vol. 25. - P.7-13.
. Carter S.R., Seiff S.R. Cosmetic botulinum toxin
injections // Int. Ophthalmol Clin. - 1997. - Vol. 37. - P. 69-79.
. Maseri A., Andreotti F. Targeting new thrombolytic
regimens at specific patient groups: implications for research and
cost-containment // Eur. Heart J. -1997. - Vol. 18. - P.28-35.
. Levine S.R. Thrombolytic therapy for stroke: the new
paradigm // Hosp. Pract. - 1997. - Vol. 32. - P.57-73.
. Cherry J.D. Comparative efficacy of acellular pertussis
vaccines: an analysis of recent trials // Pediatr. Infect. Dis. - 1997. - Vol.
16. - P. 890-896.
. Michie C.A., Cohen. J. The clinical significance of
T-cell superantigens // Trends Microbiol. - 1998. - Vol. 6, №2. - Р. 61-65.