Розрахунок ректифікаційної колони періодичної дії для розділення суміші бензол–толуол
Зміст
ВСТУП
1. ЗАГАЛЬНІ
ПОЛОЖЕННЯ
1.1
Вибір тиску
.2
Температурний режим
2. ТЕХНОЛОГІЧНИЙ
РОЗРАХУНОК
2.1
Матеріальний розрахунок
2.2
Тепловий розрахунок установки
2.3
Гідравлічний розрахунок тарілок
ВИСНОВОК
СПИСОК ЛІТЕРАТУРИ
ВСТУП
Одним з найбільш
розповсюджених методів розділення рідких однорідних сумішей, які складаються з
двох або більшого числа компонентів є перегонка, що включає в себе дистиляцію
та ректифікацію.
Ректифікація -
процес розділення однорідних рідких сумішей на складові компоненти або групи
складових компонентів шляхом багаторазового часткового випарювання рідини з
подальшою конденсацією утвореної пари, які не знаходяться в термодинамічній
рівновазі та рухаються протитечією. В результаті масообміну пара збагачується
низькокиплячим (легколетким) компонентом, а рідина - висококиплячим
(важколетким) компонентом.
При певному числі
контактів можна отримати пару, яка складається в основному з низькокиплячого та
рідину - з висококиплячого компонента.
Процеси
ректифікації здійснюються в апаратах, конструкція яких визначається способом
організації контакту фаз. Контакт фаз може здійснюватися ступінчасто
(барботажні колони) або безперервно.
Сучасні
ректифікаційні апарати класифікують у залежності від технологічного
призначення, тиску та внутрішнього обладнання, яке забезпечує контакт між парою
та рідиною.
За технологічним
призначенням ректифікаційні апарати поділяються на: колони атмосферно-вакуумних
установок, термічного та каталітичного крекінгу вторинної перегонки
нафтопродуктів, а також на колони для ректифікації зріджених газів,
стабілізації легких нафтових фракцій та інші.
В залежності від
робочого тиску апарати поділяються на вакуумні, атмосферні та ті, що працюють
під тиском. Ректифікаційні апарати в залежності від будови пристроїв поділяють
на: барботажні, насадкові, плівкові та роторні.
До ректифікаційних
апаратів ставлять такі вимоги: висока поділяюча здатність та продуктивність,
достатня надійність та гнучкість у роботі, низькі експлуатаційні витрати,
невелика вага, простота та технологічність конструкції.
Насадкові колони
застосовуються, головним чином, для розділення високоагресивних сумішей або
продуктів із значною в'язкістю, також при необхідності мати невеликий перепад
тиску або малий запас рідини в колоні. Крім того, перевагою колон такого типу
є: простота пристроїв та ефективність для розділення сумішей, компоненти яких
мають невелику різницю температур кипіння. Проте насадкові колони мало придатні
для роботи з забрудненими рідинами, а у разі малої кількості зрошуючої рідини
не дають задовільних результатів, оскільки при малій густині зрошення не
досягає змочування насадки. Крім того, нерівномірний розподіл рідини по
поперечному перерізу колони, може призвести до малого ступеня розділення
компонентів, особливо при значному діаметрі колони.
Періодична
ректифікація використовується, в основному, на малотоннажних .
Виробництвах,
які переробляють невеликі кількості та великий асортимент продуктів.
1. ЗАГАЛЬНІ
ПОЛОЖЕННЯ
РЕФЕРАТ
Розглянемо
періодичний процес ректифікації на прикладі роботи сітчасті колони.
Ректифікаційна установка періодичної дії може працювати з повною або частковою
конденсацією пари. Крім того куб колони може бути виносний або вбудований.
Принципова схема
ректифікаційної установки періодичної дії з повною конденсацією пари та
виносним кубом зображена на рис. 1.
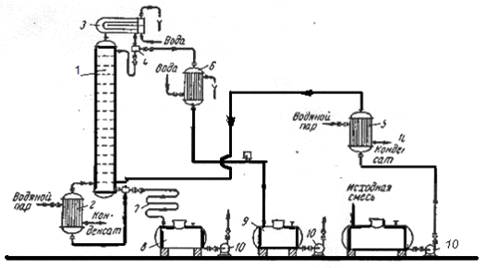
Рис. 1.
Схема ректифікаційної установки періодичної дії:
- колона ректифікації;
- кип'ятильник;
- дефлегматор;
- дільник флегми;
- підігрівач початкової суміші;
- холодильник дистиляту (або
холодильник-конденсатор);
- холодильник кубового залишку (або
нижнього продукту);
,9 - збірники;
- насоси
У деяких випадках в
дефлегматорі відбувається конденсація частини пари. Пара та конденсат,
проходячи крізь дільник, де розділяються. Одна частина конденсату (флегма)
повертається до колони, а друга частина - пара, що надходить до
холодильника-конденсатора, де конденсуються та охолоджуються до заданої
температури дистиляту.
1.1 Вибір тиску
Атмосферний тиск
або незначне перевищення тиску над атмосферним застосовується, якщо пара
дистиляту при цьому тиску може бути сконденсована за допомогою найдешевшого та
доступного холодоагенту, наприклад, води або атмосферного повітря.
При першому
наближенні, обираючи тиск, температуру конденсації пари дистиляту можна
прийняти не менше, ніж на 15 - 20 К вищою від температури охолоджуючого агента
на виході з дефлегматора. Для розташованих після ректифікаційної колони,
необхідно тиск у верхній частині колони дещо підвищити в порівнянні з
розрахунковим. Тиск внизу колони слід збільшити на величину гідравлічного
опору, створеного насадкою.
Підвищення тиску
верха колони при відповідному підвищенні в ній температури, призводить до
зменшення поверхні конденсатора, внаслідок збільшення середньої різниці
температур між парами ректифікату, що конденсується, та охолоджуючим агентом.
Підвищення тиску у колоні застосовують при розділенні сумішей з низькими
температурами кипіння та для розділення сумішей, які при нормальних
температурах будуть газоподібними. Разом з тим, при підвищенні тиску колони,
збільшується і температура залишку, що відбирається з низу колони. Це
призводить до збільшення поверхні куба - кип'ятильника внаслідок зменшення
середньої різниці температур між теплоносієм та нижнім продуктом (кубовим залишком)
або до необхідності використовування більш високотемпературного та більш
дорогого теплоносія.
Зниження тиску в
колоні за відношенням до атмосферного дозволяє знизити температуру в колоні, що
буває необхідним при розділенні суміші, створеної з компонентів, які мають
високі температури кипіння або термічну нестабільність. У випадку ректифікації
з водяною парою використання вакууму дозволяє суттєво скоротити витрату водяної
пари.
Тиск системи, крім
того, впливає на коефіцієнт відносної леткості
компонентів
у суміші. Для більшості сумішей ця характеристика зі збільшенням тиску збільшується.
В деяких випадках може спостерігатися і протилежна залежність. Збільшення
коефіцієнта відносної леткості сприятливо позначається на процесі ректифікації,
дозволяючи знизити кількість зрошення, зменшити висоту колони або підвищити
чіткість розділення компонентів.
Більш значно
погіршуються умови ректифікації в області високих тисків, близьких до
критичного. В цьому випадку крива розподілу фаз стає пологою, тому що величина коефіцієнта
відносної леткості наближається до одиниці.
Тиск у колоні
впливає також на її продуктивність. При збільшенні тиску питома продуктивність
колони зростає. Однак при цьому необхідна більша товщина стінки корпусу колони,
крім того, зростають витрати на перекачування сировини, зрошення та інше.
При виборі тиску
слід враховувати складну залежність цілого ряду факторів, одні з яких
збільшують, а інші зменшують капіталовкладення та експлуатаційні витрати. Тому
при виборі тиску в колоні в кожному конкретному випадку необхідно проводити
всебічний аналіз. Однак основним критерієм, як правило, є забезпечення
сприятливого температурного режиму.
Зараз ще немає
достатнього досвіду з визначення оптимального тиску в різних колонах, тому
наведемо деякі дослідні рекомендації до вибору оптимального режиму.
При ректифікації
під атмосферним та підвищеним тиском рекомендується приймати такий мінімальний
тиск у колоні, при якому ще можливо проводити конденсацію верхнього продукту
при нормальній температурі за допомогою дешевих хладоагентів, тобто віддавати
перевагу більш низьким температурам верху колони. Вважаючи, що цей тиск буде
близький до оптимального, що відповідає оптимальним витратам.
У вакуумних колонах
оптимальним вважається тиск, що відповідає максимально припустимій температурі
для сировини.
1.2
Температурний режим
При ректифікації
бінарних сумішей температура пари дистиляту, температура кипіння вихідної
суміші (початку процесу) та кубового залишку (кінця процесу) визначається за
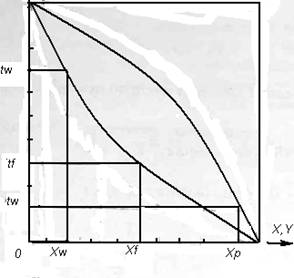
діаграмою І - х,у (рис.2.5), яка будується для конкретної суміші при різних
тисках. Температура кипіння рідини відповідного складу знаходиться за нижньою
кривою, а температура пари - за верхньою кривою.
Розрахунок колони
розглянемо на прикладі сітчастої колони.
Метою
розрахунку колони є визначення основних геометричних розмірів апарата, які
забезпечують задану продуктивність при необхідному технологічному режимові.
Розрахунок
складається з таких розділів:
Технологічний
розрахунок, до якого входять матеріальний та тепловий розрахунки;
Конструктивний
розрахунок, який включає визначення основних геометричних розмірів апарата
(діаметр, висота), його внутрішніх обладнань; гідравлічний розрахунок -
визначення гідравлічного опору апарата; Розрахунки ректифікаційних колон
базуються на загальних фізико-хімічьних закономірностей. До нашого часу в
достатньому для практичного тасування об'ємі розроблено графоаналітичний метод
кінетичного сум ректифікаційного апарата для розділення бінарних систем.
2. ТЕХНОЛОГІЧНИЙ
РОЗРАХУНОК
2.1
Матеріальний розрахунок
Розрахунок масової
кількості вихідної суміші, дистиляту та кубового залишку, кг/опер.
Gp
кг/ч - масова витрата дистиляту;w
кг/ч - масова витрата кубового залишку;
З рівняння матеріального балансу:
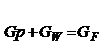
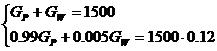
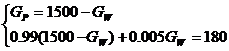
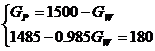
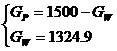
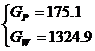
де GP,
GW,
GF
- масові кількості вихідної суміші, дистиляту та
кубового залишку, кг/опер;
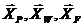 -
концентрація легколеткого компоненту у вихідній суміші, дистиляті та кубовому
залишку, відповідно, в масових частках або масових процентах.
-
концентрація легколеткого компоненту у вихідній суміші, дистиляті та кубовому
залишку, відповідно, в масових частках або масових процентах.
Для подальших розрахунків виразимо
концентрації живлення, дистиляту і кубового залишку в молярних частках:
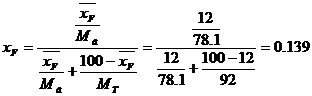
Дистилят:
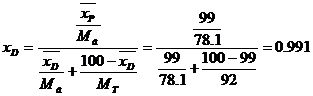
Кубової залишок:
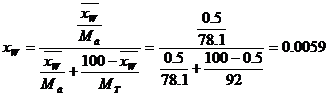
де xW,
xF,
xP
- мольна частка легколеткого компонента у бінарній
суміші;
Мб,
в - молярна
маса даного компоненту у суміші, кг/кмоль.
Побудова графіків
рівноваги у координатах t
- х,у та у*
- х
У технічних
розрахунках, за звичаєм, використовують експериментальні дані фазової рівноваги
. Для сумішей, близьких до ідеальних, дані фазової рівноваги можливо
розрахувати на підставі законів Рауля та Дальтона.
Схема розрахунку:
знаходимо температури кипіння легколеткого та важколеткого компонентів при двох
довільно вибраних тисках. У координатах ln
Р ~ 1/Т будуємо графічну залежність у вигляді двох прямих ліній. Температурний
інтервал розбиваємо в діапазоні температур кипіння чистих компонентів при
атмосферному тиску на рівні проміжки. Для кожної температури у цьому інтервалі
за графіком знаходимо пружність парів чистих компонентів, а потім розраховуємо
молярні частки легколеткого компонента у рідині та парі. За допомогою розрахунку
будують графіки рівноваги.
Таблиця 1 -
Обчислення рівноважного складу фаз
|
t oC
|
Рб,
мм.рт.ст.
|
Рт,
мм.рт.ст.
|
П,
мм.рт.ст.
|
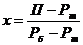 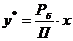
|
|
|
80
|
760
|
330,0
|
760
|
1
|
1
|
|
84
|
852
|
333,0
|
760
|
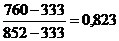 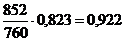
|
|
|
88
|
957
|
379,5
|
760
|
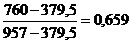 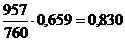
|
|
|
92
|
1078
|
432,0
|
760
|
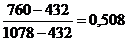 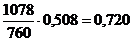
|
|
|
96
|
1204
|
492,5
|
760
|
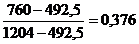 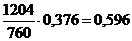
|
|
|
100
|
1344
|
559,0
|
760
|
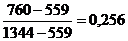  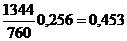
|
|
|
104
|
1495
|
625,5
|
760
|
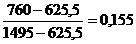 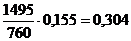
|
|
|
108
|
1659
|
704,5
|
760
|
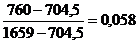
|
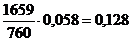
|
|
110
|
1748
|
760,0
|
760
|
0
|
0
|
Рис. 2 - Діаграма
рівноваги в координатах t - х
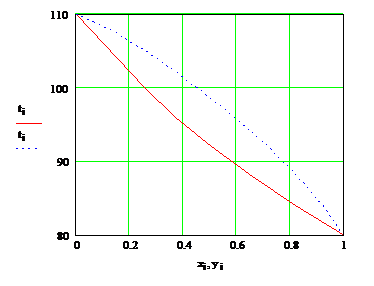
Рис. 3 - Діаграма рівноваги в
координатах у* - х
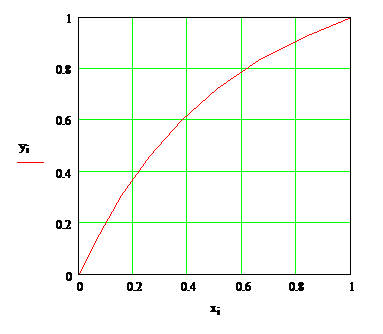
Визначення
флегмового числа
Флегмове число є основним
параметром, який визначає заданий ступінь розділення в процесі ректифікації та
залежить від багатьох величин, які по різному впливають на розміри апарата та
експлуатаційні витрати.
При періодичному процесі
ректифікації склад рідини в кубі колони під час процесу розділення безперервно
змінюється, частка легколеткого компонента зменшується від хF на
початку процесу до хW в кінці. Відповідно безперервно
змінюються і умови розділення по всій колоні.
Процес періодичної
ректифікації можна проводити двома способами:
1)
3 постійним складом дистиляту
(флегмове число при цьому постійно змінюється);
2)
3 постійним флегмовим числом (склад
дистиляту при цьому постійно змінюється).
Робота з постійним
складом дистиляту
У початковий момент
перегонки, коли склад рідини в кубі дорівнює початковому складу хf
мінімальне флегмове число розраховується як і для безперервної ректифікації.
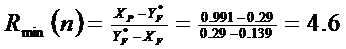
де Y*F -
мольна частка легколеткого компоненту у парі рівноважному зрідиною живлення.
У ході процесу вміст
легколеткого компоненту суміші у куоі зменшується і для збереження постійного
складу дистиляту флегмове число повинне безперервно збільшуватися. Найбільше
значення Rmin
буде в кінцевий момент перегонки, коли склад рідини в кубі досягає заданої
величини Xw.
Для цього моменту значення мінімального флегмового числа розраховується згідно
виразу.
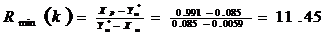
де Y*w -
мольна частка легколеткого компонента у парі, рівноважному з кубовим залишком
(див. рис. 2).
Робоче флегмове число для
кінцевого моменту перегонки:
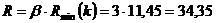
Де 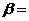 (1,4 - 5) -коефіцієнт надлишку
флегми.
(1,4 - 5) -коефіцієнт надлишку
флегми.
Середнє значення мінімального
флегмового числа для всього процесу визначається згідно з формулою:
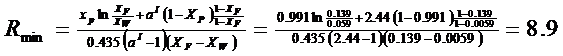
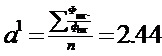 - середня
відносна леткість по колоні;
- середня
відносна леткість по колоні;
тут Фнх та Фвк -
пружність пари, відповідно низько - та висококиплячого компонентів для ряду
температур в інтервалі від температури кипіння легколеткого компонента до
температури кипіння важколеткого компонента;
п - кількість
значень температур.
Розрахункове флегмове число
розраховується за формулою
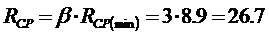
Значення Rср повинне
знаходитися в інтервалі між Rк та Rn.
Обов'язково повинна виконуватися наступна умова:
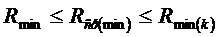
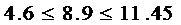
Виконання
цієї умови означає, що помилки в розрахунках не допущені.
Середні
концентрації рідини та пару в мольних частках
Оскільки колони періодичної
дії працюють як колони для зміщення парів, то вони складаються з однієї
частини.
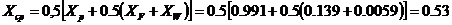
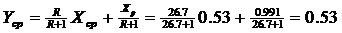
Густина пари
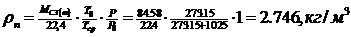
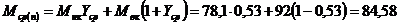
де Мср - середня
мольна маса пари, кт/кмоль; Т0= 273, 15 - абсолютний нуль, К; Тср=Т0+tcр -
середня температура пари. К;
тут tcр - середня
температура пари у колоні, визначена у залежності від Уср (див. рис.2), К;
Ро - атмосферний тиск, Па;
р - тиск
у колоні, Па.
Густина
рідини
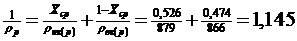
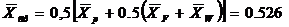 - середня
концентрація рідини; У вольних частках;
- середня
концентрація рідини; У вольних частках;
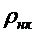 та
та 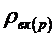 - густина
низькокиплячого та висококиплячого компонентів при tср.
- густина
низькокиплячого та висококиплячого компонентів при tср.
Кількість
пари, що підіймається по колоні
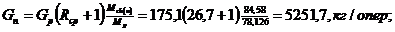
де Mp. = Mнк Хр + Мвк(1
- Xр.) - мольна
маса
дистиляту,
кг/кмоль;
Кількість
рідини, що стікає по колоні;
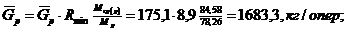
де Mср(р) = Mнк Хср + Мвк(1
- Xср) - середня
мольна маса стікаючої по колоні рідини, кг/кмоль.
2.2
Тепловий розрахунок установки
Тепловий розрахунок
складається з метою визначення необхідної кількості теплоти в кубі - кип'ятильнику,
витрат теплоти, яка передається охолоджуючий воді в дефлегматорі та у водяних
холодильниках дистиляту і кубового залишку, а також для визначення витрати
гріючого пару в кубі та води у згаданих апаратах.
Тепловий
баланс колони
Схема теплових потоків, на
якій кип'ятильник розглядається як складова частина
колони
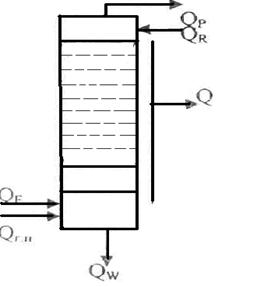
QГ.П + QF
+ QR = QP
+ QW + QF
+ QПОТ,
де QГ.П
- кількість тепла, яке надходить з гріючою парою, що витрачається на
випаровування рідини, Вт;
QF
- тепло, яке надходить з вихідною сумішшю, Вт;
QR
- тепло, яке надходить з флегмою, Вт;
QP
- тепло яке виходить з пароподібним дистилятом, Вт;
QW
- тепло, яке виходить з кубовим залишком, Вт;
QПОТ
- втрати тепла в навколишнє середовище, Вт.
Витрата теплоти,
охолоджуючій воді, що віддається, в дефлегматорі-конденсаторі, знаходимо по
рівнянню:
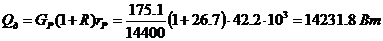
тут
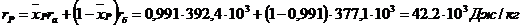
де rа і rб - питомі теплоти
конденсації бензолу і толуолу при температурі 820 С..
Витрата теплоти, одержуваної в
кубі-випарнику від гріючої пари, знаходимо по рівнянню:
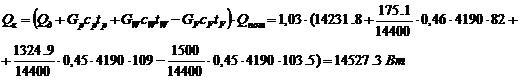
тут питомі теплоємності
узяті відповідно при tp
= 820
С tw=
109 0
С і tf
= 103,50
С , температура кипіння початкової суміші tf
= 103,5 0
С визначена по рис. № 2.
Витрата теплоти в
паровому підігрівачі початкової суміші:
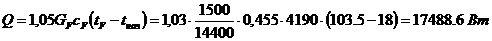
сF =
(0,45.0,43 + 0,55.0,42) 4190 Дж/(кг.К) узята при
середній температурі (92,5 + 18)/2 ≈ 55 0 С.
Витрата теплоти, охолоджуючій воді у
водяному холодильнику, що віддається, дистиляті:
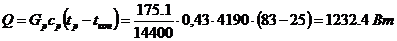
тут питома теплоємність дистиляту Сp
= 0,43*4190
Дж/(кг.До) узята при середній температурі (82
+ 25) /2 = 54 0 С.
Витрата теплоти, охолоджуючій воді,
що віддається, у водяному холодильнику кубового залишку:
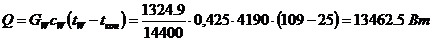
де питома теплоємність
кубового залишку Cw = 0,424*4190
Дж/(кгK)
узята при середній температурі (109 + 25) /2 =
67 0 С.
Витрата гріючої пари:
у кубі-випарнику
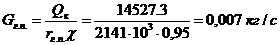
де 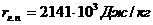 - питома
теплота конденсації гріючої пари; Всього: 0,007 кг/с = 100,8 кг/опер.
- питома
теплота конденсації гріючої пари; Всього: 0,007 кг/с = 100,8 кг/опер.
Витрата охолоджуючої води:
а) у дефлегматорі
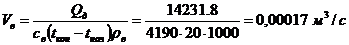
б) у водяному холодильнику
дистиляту
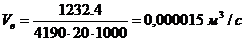
в) у водяному холодильнику
кубового залишку
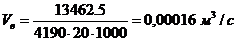
Всього:
0,00017+0,000015+0,00016=0,000345м3/с або 4,97 м3/опер;
Визначення
швидкості пари і діаметру колони:
Рівняння робочoї
лінії:
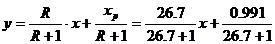
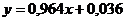
Середні концентрації рідини:
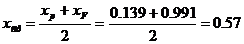
Середні концентрації пари знаходимо
по рівняннях робітників лінії

Середні температури пари визначаємо
по діаграмі t-x,y (рис.2)
- при 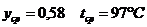
Середні молярні маси і густина пари:
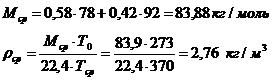
Густина рідких бензолу і толуолу
близька. Температура у верху колони при Xp
= 0,991 дорівнює 820 С,
а в кубі-випарнику при Xw=0,006
вона дорівнює 109 . (рис.2).
Густина рідкого бензолу при t=820
С ρб
= 813 кг/м3, а рідкого толуолу при t=1090 С
ρт = 783 кг/м3.
Приймаємо середню густину рідини в
колоні:
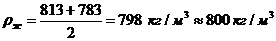
Швидкість пари в колоні
(С=0,032)
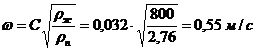
(95+8Об'ємна витрата проходячої
через колону пари при середній температурі в колоні tср= 970
С
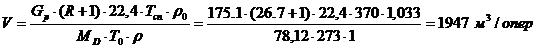
або 0,13 м3/с
де Мр - молярна маса
дистиляту, рівна
Мр = 0,991 .
78 + 0,009 . 92 = 78,12 кг/міль
Діаметр колони:
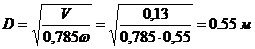
По каталогу довіднику
«Колонні апарати» беремо D=600 мм, тоді швидкість пари в колоні буде:
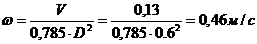
2.3
Гідравлічний розрахунок тарілок
ректифікаційний
установка періодичний тиск
Приймаємо наступні розміри ситчатої
тарілки: діаметр отвір d0 = 4 мм, висота силової перегородки hв = 40 мм.
Вільний перетин тарілки (сумарна площа отворів) 8% від загальної площі тарілки.
Площа, займана двома сегментними переливними стаканами, складає 20% від
загальної площі тарілки.
Розрахуємо гідравлічний опір тарілки
у верхній і нижній частині колони по рівнянню:
Δ
p
= Δ
pсух+
Δ
pσ+
Δ
pпж
Гідравлічний опір сухої тарілки:
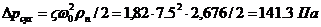
Де ξ=1,82- коефіцієнт
опору незрошуваних ситчатих
тарілок з вільним перетином 7- 10%; ω0= 0,6/0,08=
7,5 м/с
- швидкість пари в отворах тарілки.
Опір, обумовлений силами
поверхневого натягy:
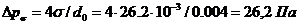
де 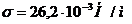 -
поверхневий натяг рідини при середній температурі у колоні 970 С (у
бензолу і толуолу практично однакове поверхневий натяг); d0 = 0,004м - діаметр
отворів тарілки. Опір парорідинного шару на тарілці:
-
поверхневий натяг рідини при середній температурі у колоні 970 С (у
бензолу і толуолу практично однакове поверхневий натяг); d0 = 0,004м - діаметр
отворів тарілки. Опір парорідинного шару на тарілці:
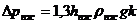
Висота
парорідинного
шару
hпж=
hп+Δh
Величину ∆h - висоту шару над
зливною перегородкою розраховуємо по формулі:
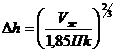
де Vж - об'ємна витрата рідини,
м3/с; П - периметр зливної перегородки, м; k
= ρпж/ρж
- відношення густини парорідинного шару (піни)
до густини рідини, приймаємо приблизно рівним 0,5.
Об'ємна витрата рідини у колоні:
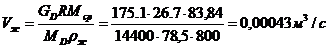
де Мср = 0,7*78 + 0,3*92 =
82,2 - середня молярна маса рідини, кг/кмоль. Периметр зливної перегородки П
знаходимо, вирішуючи систему рівнянь:
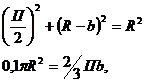
де R = 0,3 м - радіус
тарілки, 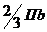 - наближене
значення площі сегменту.
- наближене
значення площі сегменту.
Рішення дає: П = 1,24 м; b =
0,25 м. Знаходимо ∆h:
Висота парорідинного шару на
тарілці:
hпж=
hп+Δh=0,04
+ 0,0052 = 0,0452 м
Опір парорідинного шару:
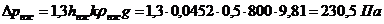
загальний
гідравлічний опір тарілки колоні:
Δ
p
= Δ
pсух+
Δ
pσ+
Δ
pпж
= 141,3 + 26,2 + 230,5 = 398 Па
Перевіримо чи виконується при
відстані між тарілками h
= 0,3 м умова необхідна для нормальної роботі тарілок:
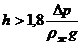
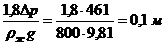
Отже, вищезгадана умова
дотримується
Перевіримо рівномірність
роботи тарілок - розрахуємо мінімальну швидкість пари в отворах ωо.мин,
достатньо для того, щоб ситчата тарілка працювала всіма отворами:
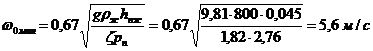
Розрахована швидкість ωо.мин,
= 5,6 м/с; отже, тарілки працюватимуть всіма отворами.. Визначення числа
тарілок і висоти колони.
а.) Наносимо на діаграму у - х
робочі лінії (рис. 5) і знаходимо число ступенів зміни концентрації
nт.
У колоні nт
-11, ступенів.
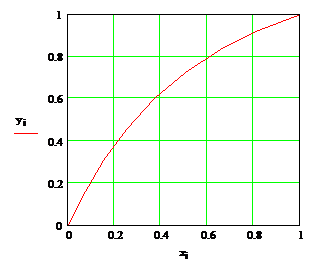
Рис. 5 - Визначення числа
ступенів зміни концентрації
Число тарілок розраховуємо по
рівнянню:
п = пт / η
для визначення середнього к. п. д.
тарілок η знаходимо
коефіцієнт відносної летючості компонентів, що розділяються α
= Ра / Рб і динамічний коефіцієнт в'язкості
початкової суміші μ
при середній температурі в колоні, рівній 97 0 С.
При цій температурі тиск насиченої
пари бензолу Рб = 1239 мм рт.
ст., толуолу Рт = 509 мм рт.
ст. (табл. 1), α
= 1239/509 = 2,43.
Динамічний коефіцієнт в'язкості
бензолу при 97 0 С рівний 0,29 сП, толуолу 0,29 сП. Приймаємо динамічний
коефіцієнт в'язкості початкової суміші μ
= 0,29 сП = 0,29.10-3 Па.с.Тоді по графіку (рис.
6) знаходимо . η
= 0,4 Довжина шляху рідини на тарілці
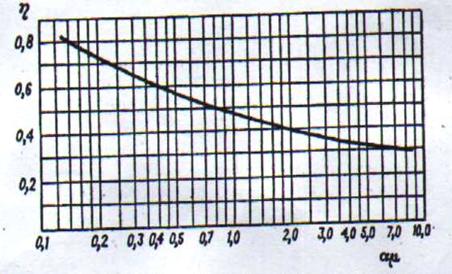
Рис. 6 - Діаграма для наближеного
визначення середнього до. п. д. тарілок
l
= D
- 2b
= 0,6 - 2.0,24 = 0,12 м
По графіку (рис. 7) знаходимо
значення поправки на довжину шляху ∆ = 0,1 середній к. п. д. тарілок по
рівнянню:
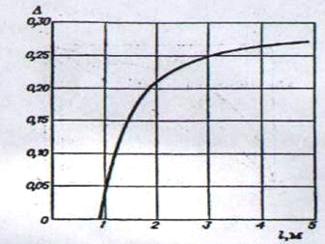
Рис. 7 - Залежність поправки ∆
від довжини шляху рідини на тарілці l
ηl
= η (1
+ Δ)
= 0,4 (1 + 0,1) = 0,47
Для порівняння розрахуємо середній
к. п. д. тарілки η0
по критерійній формулі, одержаній шляхом статистичної обробки численних опитних
даних для колпачкових і ситчатих тарілок:
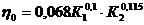
У цій формулі безрозмірні
комплекси:
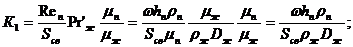
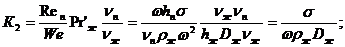
де ω -
швидкість пари в колоні, м/с; Sсв -
відносна площа вільного перетину тарілки; hп -
висота зливної перегородки, м; ρп и ρж -
густина пари і рідини, кг/м3; Dж -
коефіцієнт дифузії легколетучего компоненту в початковій суміші, визначуваний
по формулі, м2/с; σ -
поверхневий натяг рідини живлення, Н/м.
Физико-хімічні константи
віднесені до середньої температури в колоні. Заздалегідь розрахуємо коефіцієнт
дифузії
Dж :
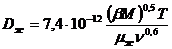
У нашому випадку: β
= 3; μж
= 0,29 сП = 0,29.10-3 Па.с; М = МF
= 83,9 кг/кмоль; υ
= 14,8.3 + 3,7.6 -15 = 96; Т = 97
+ 273 = 370 К.
Коефіцієнт дифузії:
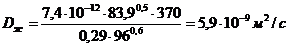
Безрозмірні комплекси:
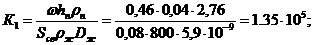
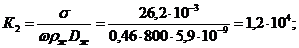
Середній к. п. д. тарілки:
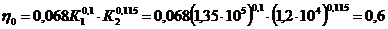
що близьке до знайденого
значення ηl.
Число тарілок:
п = пт / ηl
= 11/0,47
= 23
Загальне число тарілок nт
= 23, із запасом п = 25.
Висота тарільчатої
частини колони:
Нт = (п - 1) h
= (25 - 1) 0,3 = 7,2
м.
Загальний гідравлічний опір тарілок:
Δр
= Δр п =
398*23=9154 Па ≈ 0,09 кгс/см2.
ВИСНОВОК
Загальна кількість
енергетичних витрат при виконанні процесу ректифікації на колоні періодичної
дії з ситчатимі тарілками для розділення при атмосферному тиску 1500 кг/опер
рідкої суміші речовин бензолу і толуолу, що містить 12 мас. % бензолу і 88 мас.
% толуолу, необхідний зміст бензолу в дистиляті 99 мас. %, необхідний зміст
толуолу в кубовому залишку 0,5 мас. % (початкова суміш перед подачею в колону
підігрівається до температури кипіння, при охолоджені водою tп
=
200
С складає 4,97 м3/опер.
СПИСОК Л1ТЕРАТУРИ
1. Касаткин
А.Г. Основные процессы .и аппараты химической технологам. - М-: Химия, 1973. -
750 с.
2 Павлов
К. Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и
аппаратов химической технологии. - Л.: Химия, 1987. - 576 с.
3 Александров
И. А. Ректификационные и абсорбционные аппараты. -
Изд.
3-е. Пер. - М.: Химия, 1978. - 280 с.
4. Стабников
В.Н. Расчет и конструирование контактных устройств
ректификационных
и абсорбционных аппаратов. - Киев: Техника, 1970. -
207 с.
5. Рамм
В.М. Абсорбция газов. - М.: Химия, 1966. - 356 с.
6. Хоблер
Г. Массопередача и абсорбция. - М.: Химия, 1964. - 356 с.
7. Тютюнников
А.Б., Товажнянский Л.Л., Готлинская А.П. Основы расчета и конструирования
массообменных колон. - Киев: Вища шк., 1989. - 223 с.
9. Лащинский
А.А., Толчинский А.Р. Основы конструирования и расчета
химической
аппаратуры. Справочник. - Л.: Машиностроение, 1970. - 752 с.
10. Лащинский А.А.
Конструирование сварных химических аппаратов, справочник.-Л.: Машиностроение,
1981.-382 с.
.Борисов Г.С.,
Брыков В.П., Дытнерский Ю.И. и др. Основные процеси и аппараты химической
технологии. Пособие по проектированию. -Изд. 2-е. Пер. и доп. Под ред. Ю.И.
Дытнерского. - М, Химия, 1991 - 496 с.