Структура лекарственной устойчивости у больных туберкулезом в Республике Хакасия за период 2011-2013 года
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
«ХАКАССКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ им. Н.Ф. КАТАНОВА»
МЕДИКО-ПСИХОЛОГО-СОЦИАЛЬНЫЙ ИНСТИТУТ
Кафедра Внутренние болезни
Курсовая работа
Специальность Лечебное дело
Тема
Структура лекарственной устойчивости
у больных туберкулезом в Республике Хакасия за период 2011-2013 года
ВВЕДЕНИЕ
Цель: Анализ структуры лекарственной устойчивости у больных туберкулезам
в Республике Хакасия за период 2011-2013 года.
Задачи:
1. Изучить распространенность лекарственной устойчивости и определить
половую доминанту среди всех резистентных к ПТП лиц за период 2011-2013 года.
2. Проанализировать структуру первичной лекарственной устойчивости
отдельно у впервые выявленных, лиц с рецидивом, прочих лиц.
. Выявить доминирующую группу лиц с лекарственной устойчивостью
среди впервые выявленных, лиц с рецидивом или прочих лиц для определения
возможной причины распространения лекарственной устойчивости.
. Определить эффективность проводимого лечения среди всех лиц с
резистентностью до и после лечения, по показателю нарастания лекарственной
устойчивости, как возможной причины распространения лекарственной устойчивости.
. Определить районы Республики Хакасия с наибольшей встречаемостью
общей и преобладающей структурой лекарственной устойчивости.
Актуальность:
Лекарственная устойчивость микобактерий туберкулеза является одной из
самых серьезных проблем современной фтизиатрии (Ерохин, 2008).
Эпидемиологическое значение больных туберкулезом с лекарственной
устойчивостью заключается, в том, что они представляют собой наиболее опасный
источник туберкулезной инфекции, определяя уровень инвалидности и смертности от
туберкулеза (Гуревич Г.Л., 2009).
Россия является страной с одним из высоких уровней распространенности
лекарственно-устойчивого туберкулеза (Панин И.В., 2012).
Частота распространения туберкулеза с множественной лекарственной
устойчивостью колеблется в широких пределах в разных странах: в США 3,5% ,
Франции - 0,5%, Англии и Уэлсе - 0,6%, Швейцарии - 1,7% , Италии - 2,5%,
отмечается, что у приезжих из стран с высокой распространенностью туберкулеза
она выше, чем у постоянных жителей (Коровкин В.С., Лаптев А.Н., 2006).
Достоверные исследования говорят о высокой распространенности первичной
МЛУ в Брянской (12,9%), Томской (13,0%) областях, республиках Чувашия (14,2%) и
Марий Эл (16,1%), Владимирской (14,0%), Белгородской (19,2%), Калининградской
(19,3%), Ивановской (20,0%), Архангельской (23,8%), Псковской (27,3%) и
Мурманской областях (28,3%) [19].
Проблема развития и распространения лекарственной устойчивости во
фтизиатрии обостряется в связи с ограниченностью спектра антибактериальных
препаратов, эффективных при этом заболевании, и продолжительностью курса
лечения (Ерохин В.В., 2008).
Для лечения больных с лекарственно устойчивым туберкулезом необходимы
должное медикаментозное обеспечение, клинико-лабораторный и рентгенологический
контроль, индивидуализация лечебной тактики, консультации смежных специалистов
(Перельман М.И., 2004).
В связи с этим данная проблема остаётся до конца не решенной и требует
привлечения методов, средств направленных на борьбу с лекарственной
устойчивостью не только со стороны здравоохранения, но и социальных,
правоохранительных, законодательных структур.
1. ОБЗОР ЛИТЕРАТУРЫ
1.1 Понятие, классификация лекарственной
устойчивости
Лекарственная устойчивость - это сохранение способности микобактерий к
росту при определенных стандартных концентрациях противотуберкулезных
препаратов в питательной среде (Перельман М.И., 2004).
По степени выраженности лекарственной устойчивости туберкулеза Г.Л.
Гуревич и соавторы (2009) выделяют:
1. Монорезистентность - лекарственная устойчивость МБТ к одному ПТП
первого ряда.
. Полирезистентность - это форма ЛУ-ТБ, которая проявляется
нечувствительностью к двум и более медикаментам, исключая случай МЛУ-ТБ (кроме
Изониазида и Рифампицина).
. Множественная лекарственная устойчивость (МЛУ) - это форма ЛУ-ТБ, при
которой микобактерии туберкулеза всегда имеют резистентность как минимум к
Изониазиду и Рифампицину, с или без устойчивости к другим ПТП.
. Широкая лекарственная устойчивость (ШЛУ) представляет собой форму
МЛУ-ТБ с устойчивостью как минимум к Рифампицину и Изониазиду плюс - к любому
из фторхинолонов плюс к одному из инъекционных лекарственных средств второго
ряда (Канамицину, Амикацину или Капреомицину).
Туберкулезу с множественной лекарственной устойчивостью уделяют особое
внимание из-за эпидемической опасности и трудностей лечения (Перельман М.И.,
2004).
1.2 Причины развития лекарственной устойчивости
Основными причинами развития лекарственной устойчивости МБТ к
противотуберкулезным препаратам являются мутации в гене МБТ, ответственном за
гиперпродукцию метаболитов, инактивирующих препарат, в связи с чем происходит
увеличение лекарственно-устойчивых МБТ (Мишин В.Ю., 2007).
Необходимо учитывать, что в каверне величина микобактериальной популяции
высока, а следовательно мутированных лекарственно-устойчивых МБТ к разным
препаратам больше, чем в очагах и осумкованных казеозных фокусах (Мишин, 2007).
Заболеваемость туберкулезом контактных лиц в семьях больных, выделяющих
лекарственноустойчивые штаммы МБТ, в 2 раза выше по сравнению с заболеваемостью
контактов в семьях бактериовыделителей лекарственночувствительных МБТ (Жукова
М.П., 2009).
Экзогенную (первичную, без предшествующей химиотерапии) лекарственную
устойчивость характеризует состояние микобактериальной популяции, циркулирующей
в конкретном регионе, и ее показатели важны для оценки степени напряженности
эпидемической ситуации и выработки стандартных режимов химиотерапии. Вторичная
(приобретенная или эндогенная) лекарственная устойчивость - устойчивость МБТ,
возникающая в процессе химиотерапии, она служит объективным клиническим
критерием неэффективно проводимой химиотерапии (Мишин В.Ю., 2009).
По данным Г.Л. Гуревича и соавторов (2009) причиной развития
лекарственной устойчивости является нарушение всасывания лекарственного
препарата в кишечнике, наличие большого удельного веса (среди больных ТБ
социально-дезадаптированных лиц), которые не соблюдают предписанный режим
лечения или уклоняются от его проведения в условиях непосредственного контроля.
Позднее выявление туберкулеза, массивное бактериовыделение, большая
распространенность туберкулезного поражения и формирование множественных
полостей распада, наличие осложнений, досрочно прерванное или неадекватное
лечение являются факторами влияющими на резистентность к противотуберкулезным
препаратам (Перельман М.И., 2004).
Лица без бактериовыделения являясь официально не заразными, но с
определенной лекарственной устойчивостью к противотуберкулезным препаратам, так
же представляют опасность для окружающих, в виду недостаточности, на
сегодняшний день, мощности в лабораторных методах диагностики
бактериовыделения, и в случаи контакта с ними могут привести к 30%
заболеваемости активным туберкулезом здоровых лиц (Грибова Е., 2006-2013).
Немаловажные факторы риска развития лекарственной устойчивости связаны с
лекарственным обеспечением или качеством препаратов, неадекватным приемом лекарств
пациентами, неполноценным инфекционным контролем в центрах здоровья и
противотуберкулезных диспансерах, нерегулярной терапией, принадлежностью к
женскому полу, миграцией населения, возрастом, отсутствием системы канализации
в домах частного сектора, алкоголизмом и курением (Caminero J. A., 2009).
К факторам риска по развитию ШЛУ-ТБ относят продолжительность полученного
лечения в прошлом, количество ранее принятых противотуберкулезных препаратов
второго ряда и принадлежность к женскому полу (Jeon C. Y et al, 2008).
1.3 Пути решения проблемы лекарственной
устойчивости на мировом уровне и в РХ
Согласно данным В.В. Ерохина и соавторов (2008), для решения задач борьбы
с туберкулезом в 1982 г. Всемирной организацией здравоохранения была предложена
стратегия DOTS.
Одним из пяти основных принципов химиотерапии DOTS, в отношении лекарственной устойчивости, является применение
стандартных режимов химиотерапии (Фелькер И.Г., 2012).
В 1996 г. для организации эффективного лечения больных с МЛУ была
разработана DOTS-PLUS. Для реализации этой стратегии, как и при реализации
DOTS, используется те же принципы, однако особое внимание в этой программе
уделяется качеству исследований лекарственной чувствительности микобактерий
туберкулеза.
И.Г. Фелькер и соавторы (2009) выделили медико-социальные особенности
пациентов с неудачей в лечении по программе DOTS-PLUS:
преимущественно мужчины молодого трудоспособного возраста, проживающие в
сельской местности, не имеющие работы или находившиеся на инвалидности, имеющие
неудовлетворительные условия проживания, побывавшие в местах лишения свободы,
имеющие проблемы связанные со злоупотреблением алкоголем, наличием длительного
стажа курения, преобладанием распространенных деструктивных поликавернозных
процессов. Большая часть пациентов имели остаточные изменения в легких от ранее
перенесенного туберкулеза, двусторонние изменения. Впервые выявленные больные
составили лишь треть, остальные болели туберкулезом раньше или имели
хроническое течение туберкулезного процесса.
Риск неэффективности лечения по программе DOTS-PLUS увеличивается при
выявлении у больного хронически текущего фиброзно-кавернозного туберкулеза,
осложненного дыхательной недостаточностью, анемией или кровохарканьем, с
наличием выраженного дефицита массы тела и сопутствующей патологией со стороны
почек, ЖКТ и бронхолегочной системы, а так же при наличии массивного
бактериовыделения у пациентов с МЛУ ТБ при выявлении заболевания с сочетанной
резистентностью МБТ к ПТП первого и второго ряда (Этионамид, Офлоксацин,
Капреомицин), увеличением интервала времени от выявления туберкулезного
процесса до начала терапии по программе DOTS-PLUS (Фелькер И.Г., 2012).
Результаты прямых методов исследования: микроскопии мазка мокроты,
окрашенного по Цилю - Нельсену, исследование материала методом люминесцентной
микроскопии, посев мокроты на питательные среды становятся известными через 4 -
8 недель (Пунга В.В., 2008).
В связи с длительным получением результатов на МБТ назначение
противотуберкулезных препаратов назначается сразу же после подозрения на
туберкулезный процесс, особенно у пациентов входящих в группу риска: отсутствие
эффекта от повторного курса ХТ и хронические случаи заболевания, контакт с
больным, страдающими МЛУ-ТБ, отсутствие эффекта от краткосрочного курса
лечения, рецидивы и возобновление химиотерапии после перерыва, проживание в
регионах с высокой распространенностью МЛУ-ТБ, наличие сопутствующих
заболеваний, сопровождающихся нарушениями всасывания и значительной диареей,
наличие сопутствующей ВИЧ-инфекции (Гуревич Г.Л., Скрягина Е.М., 2009).
Эмпирическое назначение стандартной комбинации химиопрепаратов первого
ряда в случае первичной МЛУ приводит к усилению резистентности и ее более
широкому распространению. Выходом из этой ситуации является ранняя диагностика
чувствительности к противотуберкулезным препаратам микобактерий, выделяемых
больными туберкулезом. (Коровкин В.С., Лаптев А.Н., 2006).
В настоящее время для сокращения сроков выращивания микобактерий
туберкулеза и ускоренного определения лекарственной устойчивости широко
применяются непрямые методы с использованием жидких питательных сред и
автоматизированных систем (Ерохина В.В., 2008).
Применение жидких сред для бифазного посева, системы БАКТЕК-960,
технически просто и позволяет идентифицировать МБТ, определить их лекарственную
чувствительность в течение недели (Пунга В.В., 2008), а чувствительность к
маркеру МЛУ - Рифампицину в течение 2 дней Ерохина В.В. (2008).
Метод основанный на серодиагностике и определении в исследуемом материале
нуклеиновых кислот МБТ - полимеразно-цепная реакция - ПЦР (Пунга В.В., 2008),
совместно с другими методами способствуют получению результатов в течение 1-2
дней. Молекулярно-генетические методы определения лекарственной устойчивости
основаны на выявлении мутаций в геноме микобактерий, что важно при определении
туберкулеза у в/в больных (Черноусова Л.Н., 2013).
Применение бактериологического метода является обязательным и самым
достоверным при клиническом обследовании больных, в то же время отрицательные
результаты не дают основания для полного исключения наличия инфекции.
Окончательный диагноз туберкулеза может быть поставлен по совокупности
клинико-рентгенологических данных, результатов бактериологического,
бактериоскопического, ПЦР и серологического исследований, на фоне сегментарных
туберкулиновых проб - проб Манту (Гучель Е.В., 2009).
В Республике Хакасия в 2008 году у 127 пациентов первично установлена
лекарственная устойчивость. Из них 68 пациентов - с множественной лекарственной
устойчивостью [20].
В 2010 году в диспансере введена в эксплуатацию автоматизированная
система BACTEC MGIT- 960 с использованием жидкой питательной среды для
выделения микобактерий туберкулеза (МБТ) и определения их лекарственной
устойчивости к противотуберкулезным препаратам, однако мониторинг полученных
данных этим методам стал проводиться с 2013 года. Во 2-м квартале 2012 года
введен в эксплуатацию ПЦР - анализатор GeneXpert, позволяющий в течение суток
выявлять бациллярные формы туберкулеза и наличие множественной лекарственной
устойчивости [21].
В связи с эпидемиологическим неблагополучием по туберкулезу в Республики
Хакасия фтизиатрическая служба региона с 2002 года активно участвует в
международных проектах борьбы с туберкулезом, реализуемых на территории
Российской Федерации. Результаты реализации программы получили высокую оценку
экспертов Всемирной организации здравоохранения, что позволило фтизиатрической
службе республики получить грант на лечение больных лекарственно - устойчивыми
формами туберкулеза. В соответствии с соглашением между Министерством здравоохранения
Республики Хакасия, Комитетом «Зеленый Свет», противотуберкулезным диспансером
и Фондом «Российское здравоохранение» на безвозмездной основе в 2010 году
получены дорогостоящие препараты [22].
В заключении можно сказать, что в РХ ведется активная борьба против
лекарственной устойчивости к туберкулезу, используются все новые средства и
методы для ее снижения.
2. МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследование проводилось на базе республиканского противотуберкулезного
диспансера.
Характеристика структуры лекарственной устойчивости у больных
туберкулезом за период 2011-2013 года в республике Хакасия производилась на
основе ретроспективного когортного исследования отдаленных результатов
статистической отчетности зарегистрированных граждан с активным туберкулезом.
Учитывались контингенты (впервые выявленные, рецидивирующие, прочие лица)
легочной формы туберкулеза, с бактериовыделением (А15 по МКБ - 10), с
определенной первичной или вторичной лекарственной устойчивостью к
противотуберкулезным препаратам первой и второй группы за 2011-2013г.
В анализе структуры лекарственной устойчивости к туберкулезу не
учитывались лица содержащиеся в местах лишения свободы, лица чувствительные к
противотуберкулезному препарату, контингенты с неопределенной устойчивостью,
лица без бактериовыделения (А16 по МКБ 10).
В лабораторной диагностике устойчивости микобактерий были использованы
методы, изложенные в Приказе МЗ РФ от 21.03.2003 г. № 109. Мониторинг
лекарственной устойчивости к противотуберкулезным препаратам с 2011-2012 год
проводили традиционным непрямым методом абсолютных концентраций на плотной
среде Левенштейна-Йенсена, а начиная с 2013 года дополнительно альтернативным
методом - на жидких средах в системах бульонного культивирования BACTEC MGIT-
960 в соответствии с прилагаемыми к ним инструкциями.
3. РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Было проведено ретроспективное когортное исследование отдаленных
результатов лекарственной устойчивости у больных туберкулезом легких за период
2011 - 2013 года. За данный период было зарегистрировано 1904 (100%) человека с
активным туберкулезом, из них, 548 чел. (29%) являются бактериовыделителями
(МБТ +), по результатам микроскопии мазка мокроты или ростом культуры. Из 548
(100%) чел. бактериовыделителей лекарственная устойчивость на твердых средах в
2011-2013 году и дополнительно на жидких средах в системах бульонного
культивирования BACTEC MGIT- 960 в 2013 году, к противотуберкулезным препаратам
выявлена среди 473 (86,3%) пациентов. Из 473 (86,3%) пациентов с лекарственной
устойчивостью резистентность к ПТП у 434 (91,8%) наблюдается до лечения и у 39
(7,4%) пациентов после лечения. На рисунке 1 показана общая структура
лекарственной устойчивости за период 2011-2013 года у выявленных пациентов с
резистентностью.

Рис. 1. Структура лекарственной устойчивости к ПТП до и после лечения за
период 2011-2013 год, %
По данным графика видно: как в структуре ЛУ у не леченных больных
(первичная), так в структуре ЛУ после лечения (вторичная) преобладают формы с
МЛУ т.е. к нескольким препаратам включая Изониазид и Рифампицин единовременно
(самым эффективным препаратам первого ряда). Имеется наиболее опасная
устойчивость у 2 контингентов (у пациента из первичной, у пациента из второй
устойчивости) - ШЛУ.
Среди всех лиц с выявленной резистентностью к ПТП за исследуемый период
(473/100%), количество мужчин в структуре лекарственной устойчивости превышает
количество женщин в 3 раза (335 - 71% мужчин, против 138 - 29% женщин), при
условии что наибольшему риску к развитию лекарственной устойчивости имеют
женщины.
У 6 лиц с рецидивом и 1 чел. с в/в устойчивостью за 2011г, у 7 лиц с в/в
устойчивостью за 2012г, не вошедших в группу «Количество пациентов с
лекарственной устойчивостью», до лечения, была определена чувствительность,
когда как после лечения у всех образовалась устойчивость, преимущественно к
МЛУ. Начиная с 2013 года лекарственная устойчивость регистрируется двумя
методами: определением резистентности выделенных культур микобактерий к
препаратам первого ряда, включая Пиразинамид, с помощью автоматизированной
системы ВАСТЕС 960 и тестированием всех штаммов методом абсолютных концентраций
на плотной среде Левенштейна-Йенсена, как стандартным методом. В результате до
лечения у 9 чел. с чувствительностью и 25 чел. с не определенной лекарственной
устойчивостью на твердых средах, определена устойчивость на жидких,
преимущественно среди в/в с МЛУ включая Z (Пиразинамид) не определяемого на твердых средах.
В течении трех лет, несмотря на то что в группах с впервые выявленной устойчивостью,
рецидивом и прочих лиц уровень устойчивости за исследуемый период снижается не
равномерно, общая резистентность к одному (Монорезистентность), двум
(Полирезистентность) и более препаратам, включая Изониозид и Рифампицин (МЛУ),
постепенно снизилась. Так в 2013 году, по сравнению с 2011 годом устойчивость к
одному препарату уменьшилась в 4 раза - с 25 (5,8/100%), до 6 (1,4/100%), к
двум и более препаратам в 1,5 раза - с 44 (10,1/100%) до 29 (6,7/100%). МЛУ
снизилась приблизительно в 2 раза - с 118 (24,9/100%) в 2011 году до 66
(15,2/100%) в 2013 году. Лекарственная устойчивость в 2012 году к нескольким
препаратам увеличилась на 4 случая - 48 (31/100%) по сравнению с 2011 годом -
44 (23,4/100%), а в целом плавно снижается. Следует отметить, что, несмотря на
значительное снижение резистентности к противотуберкулезным препаратам в 2013
году выявлен один случай наиболее опасной устойчивости (ШЛУ) среди впервые
выявленного контингента женского пола инфильтративной формы туберкулеза до
лечения, по сравнению с 2011 годом когда был выявлен 1 случай ШЛУ у пациента
мужского пола инфильтративной формы туберкулеза до лечения.
Среди всех впервые выявленных, с рецидивом и прочих лиц из всего числа
контингентов с выявленной ЛУ до лечения 434 (100%) наибольшее количество
устойчивых форм наблюдается среди впервые выявленных 296 (68,1%), затем у лиц с
рецидивом 84 (19,4%), прочих 54 (12,5%).
С целю определения эффективности проводимого лечения устойчивых форм за
2011-2013 год был определен показатель нарастания лекарственной устойчивости
микобактерий, выделенных от больных в процессе лечения. Он оценивался как доля
больных, сохранивших бактериовыделение, у которых была выделена культура с
измененным спектром лекарственной чувствительности (в 2011 г это 19 пациентов,
в 2012г - 11, в 2013г - 6) по сравнению с культурой, выделенной до начала
лечения ко всем больным, сохранившим бактериовыделение и обследованным на
лекарственную чувствительность за выбранный период лечения (рис. 2).
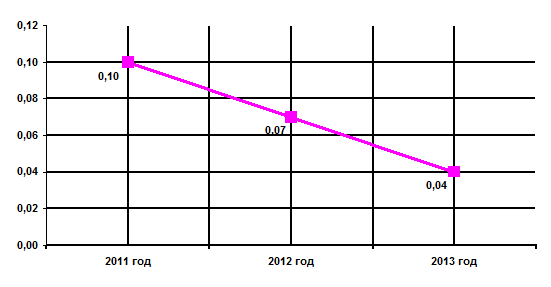
Рис.2. Показатель нарастания лекарственной устойчивости за период 2011 -
1013 года
По данным графика видно: показатель нарастания лекарственной устойчивости
носит линейный характер и в 2013 году достиг минимальных значений (0,04) по
сравнению с предыдущими годами (в 2011г - 0,10, в 2012г 0,07). При этом
отмечается что в 2012 году по сравнению с 2011 годом он уменьшился в 1,5 раза,
когда как в 2013 году в сравнении с 2012 годом приблизительно в 2 раза.
Относительно территориального принципа из 14 субъектов Республики
Хакасия, за исследуемый период из 473 (100%) пациентов исследованных на
лекарственную устойчивость наибольшее количество резистентных, включая МЛУ,
наблюдается в Абакане 136 чел. (28,7%) из них МЛУ 117(24,7%), Черногорске 68
чел. (14,,4%) из них МЛУ 61чел. (12,8%), Аскизком районе 63 чел. (13,3%) из них
с МЛУ 57 (12,0%).
ВЫВОДЫ
В структуре общей распространенности ЛУ за период 2011 - 2013 года до
лечения (первичная), так и после лечения (вторичная) преобладают формы с МЛУ
т.е. к нескольким препаратам включая Изониазид и Рифампицин единовременно
(самым эффективным препаратам первого ряда).
В течении трех лет общая резистентность к одному (Монорезистентность),
двум (Полирезистентность) и более препаратам, включая Изониозид и Рифампицин
(МЛУ), постепенно снизилась. Следует отметить, что, несмотря на значительное
снижение резистентности к противотуберкулезным препаратам в 2013 году выявлен
один случай наиболее опасной устойчивости (ШЛУ) среди впервые выявленного пациента
женского пола инфильтративной формы туберкулеза до лечения, по сравнению с 2011
годом когда был выявлен 1 случай ШЛУ у пациента мужского пола инфильтративной
формы туберкулеза до лечения.
Среди всех контингентов (впервые выявленных, с рецидивом и прочих лиц)
наибольшее количество устойчивых форм наблюдается среди впервые выявленных 296
(68,1%), что свидетельствует о напряженной эпидемической ситуации в силу
распространенности мутирующих МБТ инактивирующих ПТП в популяции здоровых лиц.
Удельный вес с наименьшим количеством устойчивых форм среди всех
контингентов с лекарственной устойчивостью приходится на лиц с рецидивом 84
(19,4%) и прочих лиц 54 (12,5%), что свидетельствует о недостаточно эффективном
лечении или влиянии других факторов на возникновение лекарственной устойчивости
(неблагоприятные санитарно-эпидемиологические условия, соматические заболевания
пациента, неадекватный приемом лекарств пациентами, неполноценный инфекционный
контроль и др.). В виду вышесказанного можно сделать вывод что главная причина
лежит в недостаточно проводимых эпидемических мероприятиях по предотвращению
распространенности мутирующих форм туберкулеза, и лишь затем в неадекватно
подобранных схемах лечения или внешних причинах.
Рассчитанный показатель нарастания лекарственной устойчивости носит
убывающий линейный характер и в 2013 году достиг минимальных значений (0,04) по
сравнению с предыдущими годами (в 2011г - 0,10, в 2012г 0,07). При этом
отмечается что в 2012 году по сравнению с 2011 годом он уменьшился в 1,5 раза,
когда как в 2013 году в сравнении с 2012 годом почти в 2 раза. Это
свидетельствует о том, что проводимое лечение устойчивых форм туберкулеза и
мероприятия направленные на повышение его эффективности, являются успешными, в
особенности начиная с 2012 года.
Относительно территориального принципа из 14 субъектов Республики
Хакасия, за исследуемый период из 473 (100%) пациентов исследованных на
лекарственную устойчивость наибольшее количество резистентных, включая МЛУ,
наблюдается в Абакане 136 чел. (28,7%) из них МЛУ 117(24,7%), Черногорске 68
чел. (14,,4%) из них МЛУ 61чел. (12,8%), Аскизком районе 63 чел. (13,3%) из них
с МЛУ 57 (12,0%), как наиболее крупных территориальных центрах республики
имеющих большое количество частного сектора, а так же возможности для его
ликвидации и улучшении жилищного благополучия граждан, что может способствовать
снижению лекарственной устойчивости среди как местных жителей так и большому
количеству приезжих из других регионов.
Кроме поставленных задач, в ходе анализа полученных данных, выявлена еще
одна важная составляющая: мониторинг лекарственной устойчивости, выделенных
культур микобактерий, с помощью автоматизированной системы ВАСТЕС 960 в 2013г в
дополнение к стандартным методам диагностики на плотной среде Левенштейна-Йенсена
позволяет повысить диагностику лекарственно устойчивых штаммов микобактерий
приблизительно на 8 %., в особенности в сторону МЛУ включая Z (Пиразинамид) не определяемому на
твердых средах.
Выявление причин преобладания количества мужчин в структуре лекарственной
устойчивости над женщинами, при условии что наибольшему риску к развитию
лекарственной устойчивости имеют женщины, требует дополнительного изучения.
Также, появление ШЛУ в 2013 году у впервые выявленного пациента требует поиска
возможных причин, и мобилизации всех противотуберкулезных структур и
мероприятий для предотвращения распространения наиболее опасной ЛУ.
больной
туберкулез лекарственный устойчивость
СПИСОК ЛИТЕРАТУРЫ
1. Гучетль
Е.В., Антохина Н.В. Анализ способов выявления микобактерий при внелегочном
туберкулезе // Научная работа. Клинико - диагностическая лаборатория. - 2009г.
2. Гуревич
Г.Л., Скрягина Е.М. 2009). Клиническое руководство по лечению туберкулеза /
Г.Л. Гуревич, Е.М. Скрягина, О.М. Калечиц ; ГУ «Научно-исследовательский институт
пульмонологии и фтизиатрии» Министерства здравоохранения Республики Беларусь. -
Минск : Белсэнс, 2009. - 125 с.
. Ерохин
В.В. Культуральные методы диагностики туберкулеза. / В.В. Ерохин. // Учебное
пособие для проведения базового курса обучения специалистов бактериологических
лабораторий учреждений противотуберкулезной службы. - М. - Тверь: ООО
«Издательство «Триада», 2008. - 208 с.
. Колесник
А. В., Тимченко О. Б. Два взгляда на DOTS-PLUS стратегию ВОЗ по борьбе с
туберкулезом // Украинский пульмонологический журнал. - 2005г. - № 2.
. Коровкин
В.С, Лаптев А.Н. Молекулярные основы лекарственной устойчивости микобактерий
туберкулеза / В.С Коровкин, А.Н Лаптев // Пульмонология и фтизиатрия: избранные
лекции и обзорные статьи. - Минск. 2006 - С. 225 -236.
. Мишин,
В.Ю. Туберкулез легких с лекарственной устойчивостью возбудителя /В.Ю. Мишин [
и др.]. - М.: ГЭОТАР - Медиа, 2009. - 208с.
. Мишин
В.Ю., Григорьев. Ю.Г. Фтизиопульмонология: Учебник / А.В Митронин, С.П.
Завражнов. - М.: ГЭОТАР - Медиа, 2007. - 504с.: ил.
. Панин
И.В., Добин В.Л., Оськин Д.Н. / Характеристика и тренды первичной лекарственной
устойчивости МБТ в Рязанской области. // Российский медико-биологический
вестник имени академика И.П.Павлова. Оригинальный исследования. Г. Рязань: -
№4. - 2012г.
. Пунга
В.В., Жукова М.П., Волошина Е.П. Эпидемическая опасность больных туберкулезом
бактериовыделителей лекарственно устойчивых и чувствительных штаммов
микобактерий туберкулеза // IV (XIV) съезд научномедицинской ассоциации
фтизиатров: тез. докл. - М. Йошкар Ола, 2009. - С.18.
. Пунга
В.В. Выявление туберкулеза в современных условиях // Пульмонология. Фтизиатрия.
2008г. - №17.
. Перельман
М.И. Фтизиатрия: Учебник, / В.А. Корякин, И.В. Богодельникова. - М.: Мед.,
2004. - 519с.
. Фелькер
И.Г. Предикторы неудачи в лечении по программе DOTS-PLUS у
пациентов, страдающих множественной лекарственно-устойчивым туберкулезом / И.Г.
Фелькер, О.В. Филинюк, Янова Г.В., Щегерцов Д.Ю. // Бюллетень сибирской
медицины. - 2012г. - №4. - С. 171-173.
. Фелькер
И.Г., Филинюк О.В., Янова Г.В., Некрасов Е.В., Буйнова Л.Н., О.В. Анастасов
О.В., Д.Ю. Щегерцов Д.Ю. Медико-Социальные особенности пациентов пролеченных по
программе DOTS-PLUS с исходом неудачи в лечении / И.Г. Фелькер, О.В.
Филинюк, Г.В. Янова, Е.В. Некрасов, Л.Н. Буйнова, О.В. Анастасов, Д.Ю.
Щегерцов. // Инновации в медицине. Социально значимые инфекции / Материалы VIII российско-германской
научно-практической конференции/ Под общей редакцией В.В.Степанова, Г. Хана. -
Новосибирск: ООО «Альфа Виста», 2009. - С. 221-224.
. Черноусова
Л.Н. Современные технологии для микробиологической диагностики
лекарственно-устойчивого туберкулеза. // Лекция «Центральный
научно-исследовательский институт туберкулеза» РАМН, г. Москва, - 2013г.
. Шевцова
А.В. Микробиологическая диагностика туберкулеза с использованием
автоматизированных систем культивирования Mycobacterium tuberculosis // Дипломная работа. - Гомель.:
"Гомельский государственный медицинский университет". 2012г. - 50с.
16. Противотуберкулезной
службе Хакасии исполнилось 75 лет // Агентство информационных сообщений. -
2008г. - URL:
<http://vg-news.ru/news-protivotuberkuleznoi-sluzhbe-khakasii-ispolnilos-75-let>.
. Хакасия - один из
первых регионов России, в котором введены технологии ускоренной диагностики
туберкулеза // Портал Здравоохранения Республики Хакасия. - 2012г. - URL:
<http://mz19.ru/news/detail.php?id=830>.
. Международные
отношения // Республика Хакасия. Портал исполнительных органов государственной
власти. - 2010г. - URL: <http://www.r-19.ru/mainpage/authority/21/health/all-info/mezdunarodnye.html>.
. Контакт с больным
туберкулезом - каков риск заражения / Е. Грибова // Здоровье Украины. Мир
медицины доступный каждому. (2006-2013г.)
. Caminero J. A.
Туберкулез с множественной лекарственной устойчивостью: эпидемиология, факторы
риска и выявление случаев. / J. A. Caminero // Международный журнал «Туберкулез
и легочные заболевания». - 2009. - Том 2, №1- С. 33-39.
21. Jeon C Y,
Hwang S H, Min J H, et al. Extensively drug-resistant tuberculosis in South Korea:
risk factors and treatment outcomes among patients at a tertiary referral
hospital. Clin Infect Dis 2008; 46:
42-49.
22. Goemaere
E, Ford N, Berman D, McDermid C, Cohen R. XDR-TB in South Africa: detention is
not the priority. PLoS Med 2007; 4: e162.
. World
Health Organization. Global tuberculosis control: surveillance, planning,
financing WHO/HTM/TB/2011.16. - Geneva, Switzerland: WHO, 2011.
Приложение А
Таблица 1. Структура лекарственной устойчивости за период 2011 - 2013
года до лечения, N
|
Год
|
2011
|
2012
|
2013
|
|
Количество пациентов с
лекарственной устойчивостью
|
194
|
152
|
127
|
|
Количество контингентов с
выявленной ЛУ до лечения
|
187
|
145
|
102
|
|
Монорезистентность
|
впервые выявленные
|
19
|
16
|
5
|
|
рецидив
|
2
|
2
|
1
|
|
прочие
|
4
|
2
|
0
|
|
Всего с Монорезистентностью
|
20
|
6
|
|
Полирезистентность
|
впервые выявленные
|
33
|
43
|
20
|
|
рецидив
|
7
|
2
|
7
|
|
прочие
|
4
|
3
|
2
|
|
Всего с Полирезистентностью
|
44
|
48
|
29
|
|
МЛУ
|
впервые выявленные
|
63
|
58
|
38
|
|
рецидив
|
34
|
11
|
18
|
|
прочие
|
21
|
8
|
10
|
|
Всего с МЛУ
|
118
|
77
|
66
|
|
ШЛУ
|
впервые выявленные
|
0
|
0
|
1
|
|
рецидив
|
0
|
0
|
0
|
Приложение Б
Таблица 2. Структура лекарственной устойчивости за период 2011 - 2013
года до лечения среди устойчивых форм, %
|
Год
|
2011
|
2012
|
2013
|
|
Монорезистентность
|
впервые выявленные
|
4,3
|
3,7
|
1,2
|
|
рецидив
|
0,5
|
0,5
|
0,2
|
|
прочие
|
0,9
|
0,5
|
0,0
|
|
Всего с Монорезистентностью
|
5,8
|
4,6
|
1,4
|
|
Полирезистентность
|
впервые выявленные
|
9,9
|
4,6
|
|
рецидив
|
1,6
|
0,5
|
1,6
|
|
прочие
|
0,9
|
0,7
|
0,5
|
|
Всего с Полирезистентностью
|
10,1
|
11,0
|
6,7
|
|
МЛУ
|
впервые выявленные
|
14,5
|
13,4
|
8,7
|
|
рецидив
|
7,8
|
2,5
|
4,2
|
|
прочие
|
4,8
|
1,8
|
2,3
|
|
Всего с МЛУ
|
27,2
|
17,7
|
15,2
|
|
ШЛУ
|
впервые выявленные
|
0,0
|
0,0
|
0,2
|
|
рецидив
|
0,0
|
0,0
|
0,0
|
Лист регистрации изменений и дополнений
|
Номер изменения
|
Номер страниц
|
Дата введения изменения
|
Изменение внесено
|
|
Измененных
|
Новых
|
Аннулированных
|
|
Дата
|
Подпись
|
|
|
|
|
|
|
|