|
Лекарственное
средство
|
Прогнозируемое
изменение фармакологического эффекта
|
Фармакогенетический
тест
|
PPV %
|
NPV %
|
|
Трициклические
антидепрессанты
|
Гипотония,
ажитация, сонливость
|
Выявление
"медленных" аллельных вариантов гена CYP2D6
|
63
|
80
|
|
Варфарин
|
Кровотечения
|
Выявление
"медленных" аллельных вариантов гена CYP2С9
|
16
|
97
|
|
D-пенецилламин
|
Высокая
эффективность при ревматоидном артрите
|
Выявление
нулевых аллелей гена GSTM1
|
30
|
87
|
|
Изониазид
|
Полневриты
|
Выявление
"медленных" аллельных вариантов гена NAT2
|
24
|
94
|
Фармакогенетическое тестирование особенно необходимо в следующих
клинических ситуациях:
при применении ЛС с большим спектром и выраженностью НЛР
при длительном применении ЛС (сердечно-сосудистые,
психотропные ЛС, гормональные препараты и др.)
при применении ЛС с узкой терапевтической широтой
у пациентов из групп риска развития НЛР
при применении дорогостоящих ЛС [4]
Список лекарственных средств, при назначении которых
обосновано использование фармакогенетического тестирования растет с каждым
днем. В США он насчитывает уже около 150 позиций [14].
Фармакогенетические тесты, рекомендованные к примененению в
клинической практике в различных странах для снижения риска развития НПР
оральных антикоагулянтов: варфарина, аценокумарола
(определение полиморфизмов генов CYP2C9 и VKORC1)
антидепрессанты и нейролептики (определение полиморфизмов
гена CYP2D6)
изониазид, пиразинамид, рифампицин (определение полиморфизмов
гена NAT2)
оральные контрацептивы (определение т. н. "мутации
Лейдена" в гене V фактора свертывания)
атомоксетин (определение полиморфизмов гена CYP2D6)
вориконазол (определение полиморфизмов гена CYP2С19)
карбамазепин (определение полиморфного маркера HLA-B*1502)
абакавир (определение полиморфного маркера HLA-B*5701)
азатиаприн, 6-меркаптопурин (определение полиморфизмов гена
ТРМТ)
иринотекан (определение полиморфизмов гена UGT1A1)
Клиническая фармакогенетика представляет реальную возможность
индивидуализации выбора ЛС и режимов их дозирования на основании изучения
генотипа конкретного пациента. Однако существование ряда пока неразрешенных
проблем, связанных с фармакогенетикой является причиной того, что
фармакогенетические тесты в клинической практике применяются крайне редко.
Серьезным препятствием к внедрению фармакогененетических
тестов в клиническую практику является их высокая стоимость и низкая
доступность, а также недостаточный уровень знаний в области клинической
фармакогенетики у врачей и организаторов здравоохранения. В настоящее время уже
нет никаких сомнений в том, что внедрение фармакогенетических тестов в
клиническую практику является реальным путем к персонализированной медицине, и,
как следствие повышением эффективности и безопасности фармакотерапии. Уже
разработан ряд фармакогенетических тестов. Однако темпы внедрения
фармакогенетики в реальную клиническую практику неоправданно низки.
1.2 Реакция
N-ацетилирования - одна из наиболее важных систем биотрансформации
ксенобиотиков
Лекарственные вещества, поступающие в системный кровоток,
подвергаются метаболизму (биотрансформации), или же изменению химических
свойств действующих веществ под влиянием ферментов организма [15].
Обычно в результате биотрансформации ЛС снижается его
растворимость в жирах (липофильность) и повышается растворимость в воде
(гидрофильность), а также изменяется его фармакологическая активность [4].
Соответственно, эффективность и безопасность терапии во многих случаях
определяется процессами биотрансформации. Метаболические процессы с участием
ферментов обычно классифицируются как реакции Фазы I или Фазы II [15]. В 1-й
фазе - преимущественно семействами цитохромов CYP450, во 2-й фазе -
ферментами конъюгации, такими как изоформы глутатион-S-трансфераз,
глюкуронилтрансфераз, N-ацетилтрансфераз, метилтрансфераз и сульфотрансфераз
[1].
Фармакокинетический путь при участии определенных ферментов,
находящихся под генетическим контролем, проходят в организме человека и все
лекарственные препараты. Учитывая разнородность человеческой популяции, можно
предположить, что судьба каждого лекарственного средства на каком-то
фармакокинетическом этапе связана с полиморфной системой того или иного фермента
или белка. По этой причине различные индивиды неодинаково реагируют на одно и
то же лекарственное вещество [16].
Известно, что одной из наиболее важной системой
биотрансформации ксенобиотиков является реакция N-ацетилирования.
Ацетилирование эволюционно является одним из ранних механизмов адаптации, так
как эта реакция необходима для синтеза жирных кислот, стероидов,
функционирования цикла Кребса. Система ацетилирования находится под контролем
фермента N-ацетилтрансферазы (NAT), требует присутствия в качестве кофактора
ацетил-кофермента А (Ац-КоА) и протекает в два последовательных этапа. Сначала
ацетильная группа Ац-КоА переносится к цистеиновому остатку внутри активного
центра фермента с высвобождением кофермента А (E-SH + КoA-COCH3 → E-S-COCH3 + КoA-SH), а затем перемещается с
ацетилированного фермента на аминогруппу субстрата. Данный процесс относится ко
II фазе биотрансформации
ксенобиотиков. Для сильноосновных аминов скорость N-ацетилирования определяется
первым шагом, для слабоосновных - вторым. В определенных случаях
N-ацетилтрансферазы могут катализировать и реакцию О-ацетилирования [17, 18].
Сама история изучения ариламин-N-ацетилтрансферазы началась
практически сразу после введения в медицинскую практику изониазида в 1952 году
для лечения туберкулёза. Было обнаружено, что у 40% лиц, принимавших изониазид
в дозе 20 мг/кг в сутки, в течение 3 - 8 недель развивался периферический
неврит. Выяснилось, что это осложнение тесно связано с метаболизмом препарата и
зависит от степени его ацетилирования. Высокая стабильность типа элиминации
свободного изониазида, независимого от характера питания и состояния здоровья,
и большой размах межиндивидуальной изменчивости по этому признаку дали
основание для предположения, что обмен изониазида в сильной степени определяется
наследственными задатками [19]. Авторы номенклатуры предложили корневой символ
для генов ариламин N-ацетилтрансфераз писать тремя латинскими заглавными
буквами (NAT) [7].
К препаратам, ацетилирование которых генетически
детерминировано относятся лекарства, содержащие ароматические аминные или
гидразиновые группы (сульфаниламиды (сульфасалазин, сульфаметоксозол,
сульфадиазин, сульфацетамид), изониазид, прокаинамид, гидралазин (апрессин),
нитразепам, призидилол (прекапиллярный вазодилататор, адреноблокатор), амринон
(инотроп), эндралазин, аминоглутетимид (ингибитор синтеза стероидов в
надпочечниках и периферической ароматизации надпочечниковых андрогенов),
клоназепам и кофеин, широко распространенные загрязнители окружающей среды
(бензидин, аминофлюорен, 4-аминобифенил, β-нафтиламин, ароматические
амины и др.), канцерогенные вещества, содержащиеся в пище и табачном дыме, а
также некоторые эндогенные соединения (серотонин, гистамин, дофамин)
метаболизируются в печени с участием изоферментов ариламин-N-ацетилтрансфераз: NAT1 и NAT2 [20, 31].
Однако подвержены этому влиянию не все препараты, которые
ацетилируются, поскольку некоторые из них ацетилируются с участием различных
ферментов в других органах. Исключениями являются сульфаниламиды,
Р-аминобензойная и Р-аминосалициловая кислоты [20].
К настоящему времени известно существование одного гена NAT
у прокариот (доядерные - бактерии), у эукариот (формы, имеющие ядро)
определено три локуса NAT (NAT1, NAT2, NAT3), нумерация их зависит от
исторической последовательности изучения. N-ацетилтрансферазы являются
цитозольными ферментами, которые были найдены в печени и во многих других
тканях у большинства видов млекопитающих, за исключением лис и собак, которые
неспособны к N-ацетилированию ксенобиотиков. У кроликов и мышей экспрессируется
две формы N-ацетилтрансферазы, обозначаемых NAT1 и NAT2. У человека две формы
фермента NAT1 и NAT2. По последним данным, у человека идентифицировано, кроме
этих 2 классов, еще 3 класса ферментов: арилалкин-N-ацетилтрансфераза (AANAT),
L1-протеин-регулятор адгезии клеток (L1 CAM) и гомолог Saccharomyces cerevisiae
N-ацетилтрансферазы (ARD1) [16, 21].
У человека имеется два функциональных локуса, кодирующих N-ацетилтрансферазы NAT1 и NAT2. Гены,
кодирующие N-ацетилирование,
локализованы в хромосоме 8p21.3-23.1 [21]. N-ацетилтрансферазы для про - и эукариотов
классифицируются в соответствии с международными правилами генетической
номенклатуры, где локус обозначается арабскими цифрами, аллели - латинскими
буквами, отделенными от локуса гена звездочкой [26]. На сегодняшний день
известно 36 аллелей, кодирующих белки с разной степенью ацетилирующей
способности [27]. Все исследованные гены NAT состоят из открытых для
считывания 870 пар оснований, кодирующих каталитически активные белки со средней
молекулярной массой 33,5 кДа [16, 28]. Гены NAT хотя и расположены на одной
хромосоме, но регулируются независимо друг от друга. NAT1 экспрессируется в
большинстве тканей организма, NAT2 - только в печени и кишечнике. Эти ферменты
отличаются по субстратной специфичности. Субстратами, преимущественно
метаболизируемыми NAT1, являются парааминосалициловая кислота,
парааминобензойная кислота и сульфаметоксазол. К веществам, преимущественно
N-ацетилируемым при участии NAT2, относят изониазид, гидралазин, сульфаметазин
и дапсон. Некоторые ксенобиотики, например, 2-аминофлуорен одинаково хорошо
метаболизируются обоими ферментами [22-24].
Считается, что NAT2 обладает меньшей специфичностью и
метаболизирует более широкий круг веществ, поэтому именно NAT2 привлекает
большее внимание исследователей. Blum М. с соавт. (1990) доказали, что ген NAT2
полиморфен, его продукты по - разному инактивируют изониазид, а также данный
ген отвечает за фенотип ацетилирования [28]. Генетический полиморфизм
NAT2 был открыт Vatsis К.Р. с соавт. (1995) [25].
Активность NAT2 в силу своего генетического полиморфизма
значительно варьирует у различных индивидов. Были установлены несколько диких и
мутантных генотипов фермента NAT2 [29, 30]. Распределение генотипов и фенотипов N-ацетилтрансфераз в
различных популяциях на сегодняшний день подвергается активному изучению.
Результаты этих исследований позволяют определить не только предрасположенность
каждого человека к тому или другому заболеванию, но и его индивидуальную
реакцию на то или иное лекарственное средство [28, 31].
Установлено, что по активности N-ацетилтрансферазы 2 (NAT2)
человечество делится на группы - "быстрые", "промежуточные"
и "медленные" ацетиляторы. Распределение скоростей ацетилирования в
популяции бимодальное [20]. Разница между быстрым и медленным N-ацетилированием зависит
от количества печеночной NAT2 в большей степени, чем от изменений ее свойств
[20]. Известно, что быстрое ацетилирование наследуется по
аутосомно-доминантному типу, в то время как медленной ацетилирование - по
рецессивному. Интенсивность ацетилирования в организме человека контролируется β2-адренорецепторами, метаболическими резервами (пантотеновая
кислота, пиридоксин, тиамин, липоевая кислота), генотипом.
Соотношение между лицами со способностью к быстрому
ацетилированию ("быстрые" ацетиляторы) и лицами со способностью к
медленному ацетилированию ("медленные" ацетиляторы) у представителей
разных рас различное [7]. "Быстрый" аллель является исходной формой и
одинаков у всех рас, тогда как "медленные" аллели европеоидов и
монголоидов различны. У "медленных" ацетиляторов - гомозигот по
"медленным" аллелям - скорость работы ферментов снижена на 20%.
Например, у эскимосов и японцев отмечен самый низкий процент медленных
ацетиляторов (около 10%) [32, 33]. У китайцев он несколько выше и составляет
около 20% [34]. Медленные ацетиляторы меньше распространены среди коренного
населения Гонконга, Малайзии и Сингапура. В популяциях европеоидов типично
приблизительно равное распределение быстрых и медленных ацетиляторов. Например,
одно из исследований среди европеоидов Берлина выявило 62% медленных
ацетиляторов [35]. Фенотипирование европеоидов в одном из северных регионов
Германии (Гросхансдорф) определило 71% медленных метаболизаторов [36]. В то же
время у европеоидов Франции данный показатель колеблется от 53% до 61,3% [37,
38]. По данным D. A. P. Evans, удельный вес медленных ацетиляторов в Великобритании составляет
около 62% [39]. В Швеции этот показатель приближается к 68% [40, 41], а в Дании
- к 58% [41]. В Испании частота медленных ацетиляторов среди здорового
населения колеблется от 53-55% до 65,4% [42, 43]. Среди негроидных популяций
частота медленных ацетилятров варьирует от 18 до 80%. Белое население США -
60%, коренное население Северной Америки - 20% медленные ацетиляторы [44].
Частота медленных ацетилятров у индусов - 59% [45, 46]. В Кении выявлено 69,9%
медленных ацетиляторов [47]. Фенотип медленного ацетилирования преобладает на
Ближнем Востоке (Египет, Марокко) и составляет 70%. Например, в иранской популяции
их уровень находится в пределах 78,4%, что соответствует вариациям в арабских
странах и превышает таковые у европейцев [48]. В России подобные исследования
единичны. По их результатам в среднем соотношение медленных и быстрых
ацетиляторов составляет 60% и 40% соответственно [49, 50]. Подобные данные
полученные Сатыровой Т.В. с соавторами, в популяции европеоидов
Юго-Восточного региона Республики Беларусь составляли медленный тип
ацетилирования имел место у 66% населения, а быстрый - у 34% [51].
Индивидуальная активность метаболических процессов имеет
важное биологическое (патогенетическое) значение. Установлено, что некоторые
заболевания связаны с типом ацетилирования. Показано, что медленный тип
N-ацетилирования предрасположен к раку мочевого пузыря (частота рака мочевого
пузыря у "медленных" ацетиляторов в 2-3 раза больше, чем у
"быстрых" ацетиляторов), особенно если носители к тому же являются
курильщиками или подвергаются профессиональному воздействию бициклическими
ароматическими аминами (Indulsky, 2000) [93, 94]. Считается, что фенотип
медленного ацетилирования предрасполагает к повышению уровня метаболитов
токсичных веществ в моче. Взаимодействие между полиморфизмом NAT2, курением табака
(активным или пассивным) является важным фактором риска возникновения рака
легкого и рака молочной железы [92]. При изучении рабочих асбестового
производства было выявлено повышение риска развития рака легкого у
индивидуумов, имеющих фенотип медленного ацетилирования в сочетании с нулевым
генотипом гена GSTM1 (Hirvoven et al., 1995). Курящие женщины в постменопаузе
имеют выраженную предрасположенность к раку молочной железы, если они
"медленные" ацетиляторы, тогда как "быстрые" ацетиляторы
такой ассоциации не имеют [39]. Медленный тип N-ацетилирования характерен также
для ревматоидного артрита (Pawlik A. и др., 2002) [52], вирусного гепатита
(Тихонова Н.Н., 1991), системной красной волчанки (Gunnarsson et al., 1997;
Kato, Yamazoe, 2000) [53], бронхиальной астмы (Вавилин В.А. и др., 2003),
обструктивного бронхита [54, 55], экземы (Аковбян В.А., 1991) [56]. Тогда как,
у "быстрых" ацетиляторов повышен риск рака толстой кишки, который
снижен у "медленных" ацетиляторов (среди "быстрых"
ацетиляторов в 1,8 раз чаще встречается колоноректальный рак). Быстрый тип
ацетилирования характерен также для больных сахарным диабетом (Mrozikiewicz P.
И др., 1994) [57, 59], витилиго (Дворянкова Е.В., 2006) [62], для пациентов со
спаечной болезнью (Чекмазов И.А., 2002) [58], ангиной [60], аллергическим
дерматитом (Nacak M., 2006) [61].
Определение типа ацетилирования важно для оптимизации
терапии, так как у медленных ацетиляторов могут развиваться осложнения, а у
быстрых ацетиляторов фармакотерапия может оказаться неэффективной.
Литературные данные показывают, что процессы метаболизма
ксенобиотиков включают огромное число ферментов и химических реакций,
контролирующих как детоксикацию, так и активацию ксенобитиков [15]. Изучение
гена или фермента в отдельности не является достаточным условием для решения
проблемы индивидуальной чувствительности человека (предрасположенности или
устойчивости) к воздействию ЛС. Наиболее перспективным для разработки
методического подхода к изучению влияния ксенобиотиков на организм человека и
формирования как побочных эффектов, так и заболеваний у человека представляется,
изучение сочетанного эффекта различных генов биотрансформации, задействованных
в процессах детоксикации и активации ксенобиотиков.
Определение ацетиляторного фенотипа основано на изучении
метаболизма некоторых лекарственных средств, например, сульфадимидина,
изониазида, дапсона или кофеина. Большинство эпидемиологических исследований по
выявлению зависимости действия различных лекарственных веществ,
биотрансформация которых протекает с участием N-ацетилтрансферазы или
опосредованно зависит от этих реакций, было проведено до открытия 2 независимых
локусов NAT. Поскольку типирование выполнялось по скорости метаболизма
изониазида или сульфаметазина - типичных субстратов NAT2, выявленные различия
относят к полиморфизму NAT2 [35, 63, 64].
Как правило, отношение концентрации метаболита к концентрации
исходного препарата измеряют в сыворотке, моче или слюне спустя определенное
время после его перорального приема. Распределение частоты отношения в группе
здоровых людей является, в большинстве случаев, бимодальным. В то же время
некоторые исследователи представляют свои данные в виде тримодального
распределения [35, 64].
На генетически предопределенную степень активности фермента
может влиять ряд физиологических параметров: раса, пол (например, зависимая от пола
секреция гормона роста, модифицирующая активность ферментов), возраст,
патологические состояния (например, болезни печени, почек, кишечника, нарушения
печеночного и почечного кровотока), средовые влияния (например, состояние
окружающей среды), профессия; поведенческие особенности (например, характер
пищи, пристрастие к табакокурению и алкоголю). По этой причине ацетиляторный
фенотип не всегда согласуется с соответствующим генотипом [65, 66]. Однако
четкую зависимость активности NAT2 от пола, возраста, массы тела, роста, курения,
употребления кофе, алкоголя, способа кулинарной обработки мяса по результатам
пока еще не многочисленных исследований установить до сих пор не удалось [35,
40, 67-69].
У здоровых людей достаточно часто отмечается высокое соответствие
между ацетиляторным генотипом и фенотипом. Например, при исследовании
ацетиляторного статуса среди китайских женщин установлено почти полное
совпадение частоты встречаемости фенотипа и генотипа быстрых ацетиляторов (78%
и 76% соответственно) [34]. Среди 222 белых американцев распределение медленных
ацетиляторов составило 58,1% и 59,5% по фенотипу и генотипу соответственно.
Конкордантность генотипа и фенотипа NAT2 составила 97,8% в бимодальной модели [44].
Среди 38 европеоидов Германии изучение фенотипа и генотипа ацетилирования
показало их 100% -е соответствие. Распределение медленных и быстрых
ацетиляторов составило 27: 11. Генотипирование показало 11 различных комбинаций
NAT2, среди которых самыми
частыми оказались *5B/*5B, *5B/*6А, *5А/*6С [36]. В России подобные исследования единичны.
Например, исследование московской популяционной выборки волонтеров показало,
что соотношение быстрых и медленных ацетиляторов, определяемое с использованием
2 подходов, не имело достоверных различий и составляло 47% при фенотипировании
и 44% при генотипировании. Абсолютные значения скорости ацетилирования в этом
исследовании варьировали в широких пределах, как для "быстрых", так и
для "медленных" ацетиляторов. Наиболее распространенными аллелями оказались
NAT2*4, NAT2*5 и NAT2*6, генотипами - NAT2*5/*5, NAT2*4/*6 и NAT2*4/*5. Полная
конкордантность между фенотипом и генотипом обнаружена только у 62 из 75
индивидуумов (87%) [92].
На результаты исследований по изучению полиморфизма N-ацетилрования могут в
ряде случаев влиять методологические особенности фенотипирования. Так, O’Neil с соавторами доказали,
что распределение медленных и быстрых ацетиляторов по фенотипу различалось в
зависимости от тестового препарата и составляло 70: 30 при использовании
кофеина и 53: 47 при применении дапсона. Генотип NAT2 показал соотношение
медленных и быстрых ацетиляторов как 45: 55. В группе контроля фенотипирование
по кофеину выявило распределение медленных и быстрых ацетиляторов как 67: 33
против 60: 40 при генотипировании [89]. У здоровых добровольцев в Индии
исследование фенотипа в зависимости от измерений сульфадимидина в моче и
сыворотке показало 58% и 66% медленных ацетиляторов соответственно [45].
Следовательно, генотип фермента NAT2 является более существенной и стационарной
характеристикой популяции по изучаемому признаку и имеет большое значение для
метаболизма и детоксикации лекарственных средств или иных ксенобиотиков.
Таким образом, изучение частоты встречаемости фенотипа и
генотипа N-ацетилирования,
а также их соотношения среди здоровых лиц и больных с различной патологией
сохраняют свою актуальность, так как многие аспекты этой проблемы еще не до
конца изучены, а большинство полученных результатов противоречивы. Решение этой
задачи поможет раскрытию механизмов развития и факторов предрасположенности ко
многим мультифакторным заболеваниям. Фенотип ацетилятора способствует подбору
оптимальной дозы лекарственного препарата пациентам с быстрым типом
ацетилирования и выявлению безопасной дозы лекарственного препарата больным с
медленным типом ацетилирования.
1.3 Методы
определения фенотипа N-ацетилятора
Как было уже сказано, изониазид - лекарственный препарат,
давший толчок исследованию полиморфизма NAT. Методы для определения
ацетиляторного фенотипа, которые осуществляется с помощью противотуберкулезных
препаратов и их метаболитов в сыворотке, плазме крови и моче. Оценка активности
фермента N-ацетилтрансферазы-2 позволяет установить скорость ацетилирования,
которая определяет генетически детерминированные особенности индивидуума в метаболизме
ряда лекарственных веществ [19]. Лекарственные средства, биотрансформация
которых осуществляется путем реакции ацетилирования, содержащие ароматические
аминные или гидразиновые группы (изониазид, прокаинамид, гидралазин (апрессин),
нитразепам, призидилол, амринон (инотроп), эндралазин, аминоглутетимид,
клоназепам и кофеин).
.3.1
Колориметрия и спектрофотометрия
Количественные колориметрические и спектрофотометрические
методы определения изониазида в биологических жидкостях широко используются в
клинической практике. Некоторые из этих методов позволяют также определять
ацетилизониазид. Здесь мы приведем лишь часть из методов.
Описан метод колориметрического определения изониазида в
плазме крови после дериватизации нитропруссидом натрия. Чувствительность метода
5 мг/л. Интерференция с пиразинамидом и ипрониазидом [70].
Спектрофотометрический метод, пригодный для измерения терапевтических
концентраций изониазида в плазме, после дериватизации коричным альдегидом. INH
экстрагируется из 3 мл сыворотки. Наблюдается интерференция с пиразинамидом и
ипрониазидом [71].
Основные недостатки вышеперечисленных методов следующие:
большие объемы образца для анализа, что неприемлемо при
рутинных клинических анализах, требующих отбора проб через малые промежутки времени
для изучения фармакокинетических параметров;
низкая специфичность.
1.3.2 Газовая
хроматография, масс-спектрометрия, флуориметрия
Газовая хроматография обычно не используется для рутинного
определения изониазида в клинических образцах. Плазменно-ионизационный детектор
дает низкую чувствительность даже после дериватизации, азот-чувствительный
детектор не дает лучшие результаты (в моче предел обнаружения 2 мг/л для INH и
AcINH и 400 мг/л для гидразина, моноацетилгидразина и диацетилгидразина) [72].
Компоненты должны быть сначала экстрагированы полярным органическим
растворителем, например, метилен-хлоридом или этилацетатом.
Позднейшие методы используют масс-спектрометрию, но часто
требуют дейтерированных внутренних стандартов или использования утомительной
дифференцирующей экстракции и двойной дериватизационной процедуры получения
триметилсилильных производных, занимающего относительно много времени при
анализе большого числа проб [73]. Этот метод имеет высокую специфичность и
позволяет анализировать производные гидразина вместе с INH и AcINH, что
используется для фармакокинетических исследований. Также есть статьи в которых
используется ГХ-МС для определения пиразинамида и его производных, предел
обнаружения 10 µг/л для PZA.
Флуориметрический метод, разработанный Мисели и Олсоном [74],
позволяет определять как сам INH, так и его ацетильное производное после
гидролиза, на уровне 0,02 мг/л, но необходима крайне сложная и длительная
пробоподготовка.
Суммируя все вышесказанное, можно сделать вывод, что основными
недостатками вышеперечисленных методов являются:
сложность и длительность пробоподготовки;
высокая стоимость анализа.
1.3.3
Капиллярный электрофорез
Обычно считается, что дата возникновения капиллярного
электрофореза (КЭ) - 1981 год, когда Джоргенсон и Лукас описали эффективное
разделение пептидов, используя зонный электрофорез в стеклянном капилляре
диаметром 75 мкм. Сейчас примерно 150 лекарств разных классов измеряются этим
методом в биожидкостях для токсикологических, фармакокинетических и фармакогенетических
целей [75]. Метод имеет ряд несомненных достоинств: малый объем анализируемой
пробы и используемых дорогих растворителей, высокая разделяющая способность,
быстрота, относительно низкая стоимость анализа. Поэтому в будущем этот метод
имеет хорошие перспективы для использования в широкой клинической практике, но
на данный момент вследствие таких недостатков, как относительно низкая
чувствительность и воспроизводимость и недостаточная степень автоматизации,
метод КЭ пока не находит широкого применения для рутинного анализа [76].
Оганесяном с сотрудниками был разработан и охарактеризован метод определения
рифампицина в плазме крови с помощью системы капиллярного электрофореза фирмы
Хьюлетт-Паккард [77]. Предел обнаружения - 1 мкг/мл. Метод был с успехом
использован для изучения биоэквивалентности капсул рифампицина.
1.3.4
Высокоэффективная жидкостная хроматография (ВЭЖХ)
ВЭЖХ как высокочувствительный и универсальный метод анализа,
которому во многих случаях нет альтернативы, позволяет одновременно следить за
изменением концентрации несколько лекарственных веществ, отличается достаточной
селективностью, точностью и воспроизводимостью. Поэтому, начиная с середины
70-х годов, он становится основным аналитическим методом для определения
противотуберкулезных лекарств в сыворотке и плазме крови [19].
1.3.4.1
Приготовление реактивов и образцов при использовании метода ВЭЖХ
А. Подготовка пациента, забор крови, получение и
хранение сыворотки крови
После 12-часового периода голодания пациент должен принять
изониазид в дозе 10 мг на каждый кг массы тела. Через 3 ч. после приема
изониазида из локтевой вены необходимо забрать инъекционным шприцем в
центрифужную пробирку 10 мл венозной крови. Образец выдержать при комнатной
температуре в течение 30 мин. Пробирку не позже через 1 ч после взятия крови в
течение 10 мин центрифугировать при скорости 1500g. Сыворотку перенести
автоматическим дозатором с наконечником 1 000 мкл в две полипропиленовые
пробирки объемом 1,5 мл типа "Eppеndorf". Образцы поместить в морозильную
камеру, заморозить до - 20°С и хранить при данной температуре до 1 мес. вплоть
до проведения количественного анализа содержания ацетизониазида и изониазида.
Температуру в морозильной камере контролировать с помощью термометра [78].
Б. Подготовка образцов сыворотки крови
Подготовку проб сыворотки крови производить методом осаждения
белка. К 1 мл образца сыворотки крови добавить 0,5 мл 10% трихлоруксусной
кислоты. Смесь тщательно перемешать в течение 1 мин, поместить в центрифугу и
центрифугировать в течение 10 мин при 3000 оборотов/мин. После этого для
нейтрализации избытка трихлоруксусной кислоты к 0,5 мл надосадочной жидкости
добавить 0,5 мл 0,5 М (рН 8, 20) раствора ацетата аммония. Объем вводимой пробы
должен составить 10 мм3. Для каждого образца выполнить три инжекции.
Исходный раствор изониазида готовят путем растворения точной
навески стандартного образца изониазида, составляющей 100,0 мг, в мерной колбе
вместимостью 100 мл. В качестве растворителя следует использовать воду для
хроматографии. Концентрация исходного раствора должна составить 1000 мкг/мл.
Рабочий раствор приготовить из исходного раствора изониазида.
Концентрация рабочего раствора должна составить 50 мкг/мл.
Градуировочные растворы различных концентраций изониазида
сделать из рабочего раствора путем разведения сывороткой крови, свободной от
лекарственных веществ. Примерная концентрация градуировочных растворов
изониазида должна составлять 0,5-1,0-2,0-5,0-12,0 мкг/мл [78].
1.3.4.2
Подготовка хроматографа и проведение анализа
А. Условия хроматографического разделения
Разделение проводият в градиентном режиме.
Установить следующие параметры хроматографического
разделения:
скорость потока 1,2 мл/мин;
давление 100-120 бар;
длина волны детектора 275 нм;
температура термостата колонки 20±1°С;
температура устройства для ввода образцов +4°С;
время хроматографирования: 3-кратное время удерживания
основного
пика на хроматограмме испытуемого раствора.
Б. Проведение хроматографического анализа
Убедиться в стабильности скорости потока подвижной фазы и
температуры колонки. Впрыснуть по 10 мм3 испытуемого раствора. Получить
хроматографические кривые. Время выхода изониазида должно составить 2,8±0,1
мин., ацетизониазида - 2,3±0,1 мин. Соотношение времени выхода ацетизониазида к
времени выхода изониазида должно колебаться от 0,83±0,03.
1.3.4.3
Определение фенотипа N-ацетилирования
Фенотип ацетилирования определяют как скорость ацетилирования
изониазида и рассчитывают как отношение концентраций ацетизониазида к
изониазиду (отношение R).
В зависимости от интервала отношения R: [0-0.28];
[0.28-0.37]; [0.37-1] выделяют медленный, промежуточный и быстрый фенотип
ацетилятора. Левый интервал относят к достоверно медленным, правый - к
достоверно быстрым, а средний - к промежуточным или предбыстрым ацетиляторам
[78].
Из вышеизложенного можно сделать вывод, что метод
высокоэффективной жидкостной хроматографии является достаточно удобным для
рутинного определения противотуберкулезных препаратов в биологических средах,
т.к. он отличается быстротой, селективностью, достаточной чувствительностью,
доступностью приборной базы, возможностью одновременного определения нескольких
препаратов при комплексной терапии туберкулеза легких.
Также используют определение фенотипа N-ацетилирования в
основной и контрольной группе с помощью модифицированного метода Bratton &
Marshall (1938) с помощью тестового препарата сульфадимезина (СД) или кофеина.
Пациенты и индивидуумы контрольной группы натощак принимали 0,5 г. СД.
Клинический материал (моча) собирали через 6 часов после приема СД. Определяли
уровень свободного и общего СД методом спектрофотометрии при длине волны 400
нм. Уровень ацетилированного СД определяли по формуле: АЦС = ОБС - СВС, где АЦС
- ацетилированный СД, ОБС - общий СД, СВС - свободный СД. Фенотип
N-ацетилирования определялся как скорость N-ацетилирования СД и рассчитывался
как отношение АЦС к ОБС в %. Быстрыми N-ацетиляторами считали лиц, у которых за
6 часов было ацетилировано от 70% до 100% 0,5 г количества введенного СД.
Остальные обследованные определялись как медленные N-ацетиляторы [79].
Однако, не смотря на высокую чувствительность и способность
измерять даже низкие концентрации, как лекарственных средств, так и их
метаболитов, вышеизложенные методы определения фенотипа ацетилятора не всегда
доступны для практического здравоохранения в силу их дороговизны, сложности и
трудоемкости процесса. По этой причине поиск простых, недорогих и доступных
методов определения фенотипа N-ацетилирования является по-прежнему своевременной и
актуальной задачей современной медицины.
Глава 2.
Методы исследования
2.1
Методология и общая характеристика структуры исследования
Исследование серии случаев, в котором приняло участие 28
пациентов, выполнено на базе Учреждения "Гомельская областная клиническая
больница" в период с марта по июнь 2013 года.
Основные критерии включения:
. Мужчины или небеременные и не кормящие грудью женщины в
возрасте 18 лет и старше (у женщин в детородном возрасте до включения в
исследование должен быть получен отрицательный тест на беременность).
. Пациенты, являющиеся европеоидами и не состоящие между
собой в родстве.
Основные критерия исключения:
. Терапия любыми лекарственными средствами в течение не менее
четырех недель, предшествующих исследованию.
. Клинические и/или лабораторные признаки тяжелых
соматических заболеваний.
. Анамнестические данные о перенесенных ранее хирургических
вмешательств.
.2
Общеклинические, лабораторные и инструментальные методы обследования больных
С целью верификации и выявления сопутствующей патологии всем
пациентам проведено стандартное обследование с использованием клинических,
лабораторных и инструментальных методов.
Клиническое обследование пациентов состояло из сбора жалоб,
анамнеза заболевания и жизни, а также объективного осмотра с определением
антропометрических показателей.
Лабораторные тесты включали в себя клинический, биохимический
анализы крови, анализы мочи и кала. Все лабораторные исследования проводились
по стандартной методике [80, 81].
2.3 Методика
определения вариабельности фенотипа N-ацетилтрансферазы 2
Фенотип ацетилятора устанавливали на основе определения
клиренса мочевой кислоты до и после приема кофеина в качестве тестового
препарата.
Кофеин выбран в качестве тестового препарата в силу схожести
путей его метаболизма с сульфадимезином, которое состоит в участии полиморфной N-ацетилтрансферазы 2 как
в ацетилировании изониазида, так и в ацетилировании метаболитов кофеина [82].
Следовательно, у пациентов с медленным и быстрым типом ацетилирования имеют
место вполне определенные различия в соотношении некоторых промежуточных
метаболитов кофеина (5-ацетиламино-6-формиламина-3-метилурацила и
1-метилксантила), которые используются в качестве показателей, указывающих на
скорость процессов ацетилирования. Количественное определение всех метаболитов
кофеина в большинстве случаев производится с использованием высокоэффективной
жидкостной хроматографии, что ограничивает вследствие недоступности и
трудоемкости метода его применение в практической медицине. Однако эти различия
вполне применимы к конечному продукту метаболизма кофеина - мочевой кислоте,
определение которой вполне доступно и не сопровождается существенными
методическими трудностями [83].
За 24 часа до обследования из диеты испытуемых исключались
продукты, содержащие кофеин (чай, кофе, шоколад, какао, кофеиносодержащие
напитки и др.). В день анализа до приема кофеина определяли клиренс мочевой
кислоты, сопоставляя ее концентрации, как в крови, так и в моче.
Концентрации мочевой кислоты в моче и крови определялись с
помощью набора реагентов для ферментативного фотометрического метода
производителя ООО "Анализ Мед", РБ. Измерение производили с помощью
фотометра автоматизированного РА 2600 ("СОЛАР", РБ) и фотометра PV-1251C ("СОЛАР", РБ).
Принцип метода: определение концентрации мочевой кислоты
происходило при помощи взаимодействия с уриказой. Образующийся при этом Н2О2
реагировал при участии катализа пероксидазы с N-этил-N-
(2-гидрокси-3-сульфопропил) - 3-метиланилин натриевой солью (TOOS) и 4-аминофеназоном (PAP) с образованием
выступающего в качестве индикатора красно-фиолетового красителя.
Состав набора реагентов для ферментативного фотометрического
определения мочевой кислоты представлены в таблице 2.
Таблица 2 - Состав набора реагентов для ферментативного
фотометрического определения мочевой кислоты
|
Состав набора
|
Концентрация
вещества
|
|
1. Буферный
раствор
|
|
Фосфатный буфер
(pH 7,5)
|
100 ммоль/л
|
|
TOOS
|
1 ммоль/л
|
|
Аскорбат
оксидаза
|
>=1 КЕд/л
|
|
2. Ферментный
реагент
|
|
Фосфатный буфер
(pH 7,5)
|
100 ммоль/л
|
|
4-Аминофеназон
|
0,3 ммоль/л
|
|
Гексцаноферрат
калия (II)
|
10 мкмоль/л
|
|
Пероксидаза
|
>= 1 КЕд/л
|
|
Уриказа
|
>= 0,1 КЕд/л
|
|
3. Стандартный
раствор
|
|
Мочевая кислота
|
6 мг/дл (357
мкмоль/л)
|
|
|
|
Реагенты, получаемые в наборе, готовы к применению и могли
сразу использоваться на автоанализаторах (методика R1-R2). Рабочий реагент готовился
посредством смешивания 4 частей буферного раствора с 1 частью ферментного
раствора. Рабочий реагент был стабилен в течение 3 недель при 15-25 ºС и 3-х месяцев при 2-8 ºС.
Для исследования мочи ее собирали в течение 24 часов без
использования консерванта (соляной кислоты). Затем измеряли суммарный объем
мочи (в мл) и фиксировали его в первичной медицинской документации пациента.
После этого отбирали порцию мочи в транспортную пробирку и доставляли ее в
лабораторию. Мочу перед исследованием разбавляли дистиллированной водой в
соотношении 1: 10.
Для определения концентрации мочевой кислоты в крови,
исследуемым материалом являлась сыворотка крови. Из локтевой вены забирали в
центрифужную пробирку 5 мл венозной крови. Образец выдерживали при комнатной
температуре в течение 30 минут. Пробирку не позже, чем через 1 час после взятия
крови в течение 10 минут центрифугировали при скорости 1500g. Затем образцы
переносили автоматическим дозатором с наконечником 1000 мкл в кюветы объемом 25
мкл с рабочим реагентом объемом 1000 мкл. затем смешивали пробы с рабочим
реагентом, инкубировали в термостате суховоздушном ТС-80 5 мин при 37º. После этого пробы колориметрировали на фотометре против холостой
пробы. Измерение производили в диапазоне длины волны 520-540 нм. Длина
оптического пути 1 см, температура 20-25ºС, 37ºС.
Диапазон референтных величин:
мужчины: 200-240 мкмоль/л или 3,4-7,0 мг/дл,
женщины: 140-340 мкмоль/л или 2,4-5,7 мг/дл,
моча: 250-750 мг/24 ч или 1500-4500 мкмоль/сут
Расчет клиренса мочевой кислоты вычисляли по формуле
Ван-Слайка:
= (U×V) /P,
где C - клиренс вещества (мл/мин),- концентрация исследуемого
вещества в моче (ммоль/л),
Р - концентрация того же вещества в крови (ммоль/л),-
количество мочи, выделенное в 1 минуту (мл/мин).
Затем испытуемый принимал кофеин в концентрации 4 мг на
килограмм массы тела, что считается вполне безопасной дозой, так как в сутки
организм поступает около 5 мг кофеина на килограмм массы тела [84]. Через 6
часов по вышеописанной методике повторно проводили определение клиренса мочевой
кислоты.
О типе ацетилирования судили по разнице в клиренсе мочевой
кислоты после и до перорального приема кофеина в качестве тестового препарата.
Пациенты с изменением клиренса меньше, чем на 4,48 мл/мин относили к медленным
ацетиляторам. При увеличении клиренса мочевой кислоты на 4,48 мл/мин и выше
пациенты считались быстрыми ацетиляторами [85].
2.4 Методы
статистической обработки
Статистическую обработку результатов
исследования проводили в операционной среде "Windows-XP" с
использованием пакета прикладных программ "STATISTICA 7.0", США и
"MedCalc", Бельгия.
Соответствие распределения количественных признаков закону
нормального распределения оценивали с помощью теста Колмогорова-Смирнова. Для
показателей, имеющих нормальное распределение признака, вычислялись среднее
арифметическое значение (М) и среднее квадратичное отклонение (s). С учетом наличия
нормального распределения при анализе первичных данных производилось парное
сравнение запланированных независимых и зависимых выборок по количественному
признаку с помощью Т-теста [86]. Оценка взаимосвязи количественных и/или
качественных признаков производилась с помощью ранговой корреляции по Кендаллу
с определением коэффициента ранговой корреляции (τ). Использовалась
следующая классификация силы корреляции в зависимости от значения ее
коэффициента τ:
|τ| 0,25 - слабая
корреляция;
,25 < |τ| < 0,75 - умеренная
корреляция;
|τ| ≥ 0,75 - сильная
корреляция.
При отрицательном значении коэффициента корреляции признаки
обнаруживали обратную связь (чем больше значение одного признака, тем меньше
значение второго признака). И, наоборот, при положительном значении
коэффициента корреляции связь оценивалась как прямая.
Статистически значимыми считали различия при уровне р<0,05
[86-88].
Глава 3.
Материалы исследования
3.1 Принципы
формирования и клиническая характеристика обследованных пациентов
Группа исследования была образована из пациентов,
направленных на профилактический осмотр в Учреждение "Гомельская областная
клиническая больница". В нее вошли 28 здоровых добровольцев (16 мужчин и
12 женщин) в возрасте от 25 до 61 года (М=39,25±9,67 лет).
Все здоровые добровольцы не имели клинических и/или
лабораторных симптомов каких-либо заболеваний, не подвергались хирургическим
вмешательствам и не принимали никаких лекарственных средств в течение не менее
одного месяца до включения в исследование. Все обследованные индивиды являлись
европеоидами и не состояли в родстве.
К группе курящих относили лиц, которые курили на момент
исследования. Степень привязанности к вредной привычке учитывали в суточной
дозе сигарет в пачках. Курящими оказались 9 (32,14%) из 28 опрошенных лиц.
Глава 4.
Результаты собственных исследований
4.1
Фенотипический полиморфизм фермента N-ацетилтрансферазы 2 у здоровых
добровольцев
Вариабельность фенотипа NAT2 изучена у
28 волонтеров из Юго-Восточного региона Республики Беларусь.
Фенотип N-ацетилирования рассчитан по разнице в клиренсе
мочевой кислоты после и до перорального приема кофеина в качестве тестового
препарата, которые в нашем исследовании определялись с помощью набора реагентов
для ферментативного фотометрического определения мочевой кислоты (ООО
"Анализ Мед", РБ). Измерение производили на фотометре
автоматизированного РА 2600 ("СОЛАР", РБ) и фотометре PV-1251C ("СОЛАР", РБ).
В главе 4 соответствие распределения количественных признаков
закону нормального распределения оценивали с помощью теста
Колмогорова-Смирнова. Для показателей, имеющих нормальное распределение
признака, вычислялись среднее арифметическое значение (М) и среднее квадратичное
отклонение (s).
С учетом наличия нормального распределения парное сравнение запланированных
независимых и зависимых выборок по количественному признаку производилось с
помощью Т-теста [86]. Оценка взаимосвязи количественных и/или качественных признаков
производилась с помощью ранговой корреляции по Кендаллу с определением
коэффициента ранговой корреляции (τ).
Результаты определения клиренса мочевой кислоты (мл/мин) и
разница между клиренсом мочевой кислоты после и до нагрузки представлены в
таблице 3.
Таблица 3 - Результаты выявления клиренса мочевой кислоты до
и после приема кофеина (мл/мин) и разница между клиренсом после и до нагрузки
|
№№ пациента
|
Cl до нагрузки
(мл/мин)
|
Cl после
нагрузки (мл/мин)
|
Разница Cl
(мл/мин)
|
|
1
|
11,38
|
13,6
|
2,22
|
|
2
|
5,16
|
14,56
|
9,4
|
|
3
|
6,69
|
8
|
1,31
|
|
4
|
8,32
|
14,88
|
6,56
|
|
5
|
12,25
|
20,01
|
7,76
|
|
6
|
16,65
|
25,77
|
9,12
|
|
7
|
3,77
|
6,9
|
3,13
|
|
8
|
4,75
|
4,94
|
0, 19
|
|
9
|
7,2
|
8
|
0,8
|
|
10
|
5,06
|
5,88
|
0,82
|
|
11
|
6,94
|
16,2
|
9,26
|
|
12
|
13,85
|
10,32
|
3,53
|
|
13
|
1,97
|
8,15
|
6,18
|
|
14
|
0,87
|
2,96
|
2,09
|
|
15
|
1,46
|
1,73
|
0,27
|
|
16
|
0,24
|
1,6
|
1,36
|
|
17
|
2,51
|
7,46
|
4,95
|
3,26
|
5,54
|
2,28
|
|
19
|
6,72
|
10,32
|
3,6
|
|
20
|
2,77
|
9,12
|
6,35
|
|
21
|
3,4
|
11,45
|
8,05
|
|
22
|
4,7
|
8,12
|
3,42
|
|
23
|
2,33
|
7,68
|
5,35
|
|
24
|
5,73
|
8,6
|
2,87
|
|
25
|
7,8
|
9,15
|
1,35
|
|
26
|
3,88
|
8,16
|
4,28
|
|
27
|
3,82
|
6,07
|
2,25
|
|
28
|
2,2
|
3,51
|
1,31
|
Таким образом, волонтеры при разработке способа определения
фенотипа N-ацетилирования
по интенсивности метаболизма кофеина разделились на две группы. За пограничное
значение разницы клиренсов мочевой кислоты после и до приема кофеина была
принята величина 4,48 мл/мл, как минимальное значение показателя для быстрых
ацетиляторов [85].
В результате было выявлено 18 (64,29%) медленных и 10
(35,71%) быстрых ацетиляторов.
Среднее значение клиренса мочевой кислоты в группе волонтеров
до приема кофеина составляло 5,43±3,77 мл/мин, после приема кофеина - 9,36±5,45
мл/мин. Различия между группами статистически достоверны (р<0,0001). В
данном случае и далее в подобных ситуациях с учетом наличия нормального
распределения парное сравнение запланированных зависимых выборок по количественному
признаку производилось с помощью Т-теста.
Сравнение результатов клиренса мочевой кислоты (мл/мин) до и
после приема кофеина в группе волонтеров представлено на рисунке 2.
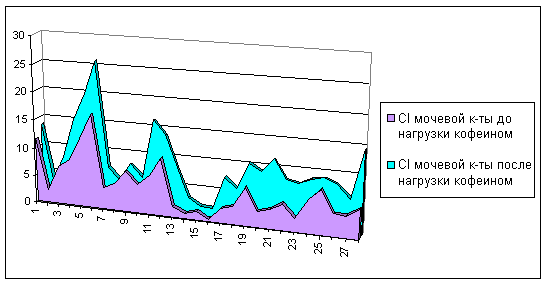
Рисунок 2 - Сравнение результатов клиренса мочевой кислоты до
и после приема кофеина в группе волонтеров
Изменение клиренса мочевой кислоты в группе волонтеров до и
после нагрузки кофеином находилось в пределах от 0,19 до 9,4 мл/мин
(М=3,93±2,89 мл/мин).
В группе пациентов с медленным фенотипом N-ацетилирования клиренс
мочевой кислоты до нагрузки кофеином изменялся от 0,24 до 11,38 мл/мин при
среднем значении 4,99±3,02 мл/мин, после нагрузки кофеином от 1,6 до 13,85
мл/мин при среднем значении 7,05±3,49 мл/мин. Различия между группами
статистически достоверны (р<0,0001).
Результаты определения клиренса мочевой кислоты в группе
пациентов с медленным фенотипом N-ацетилирования
представлены в таблице 4.
Таблица 4 - Результаты выявления клиренса мочевой кислоты до
и после приема кофеина (мл/мин) в группе пациентов с медленным типом N-ацетилирования
|
№№ пациента
|
Cl до нагрузки
(мл/мин)
|
Cl после
нагрузки (мл/мин)
|
|
1
|
11,38
|
13,6
|
|
2
|
2,2
|
3,51
|
|
3
|
3,77
|
6,9
|
|
4
|
4,75
|
4,94
|
|
5
|
7,2
|
8
|
|
6
|
5,06
|
5,88
|
|
7
|
10,32
|
13,85
|
|
8
|
0,87
|
2,96
|
|
9
|
1,46
|
1,73
|
|
10
|
0,24
|
1,6
|
|
11
|
3,26
|
5,54
|
|
12
|
6,72
|
10,32
|
|
13
|
4,7
|
8,12
|
|
14
|
5,73
|
8,6
|
|
15
|
7,8
|
9,15
|
|
16
|
3,88
|
8,16
|
|
17
|
3,82
|
6,07
|
|
18
|
6,69
|
8
|
Сравнение результатов выявления клиренса мочевой кислоты до и
после приема кофеина (мл/мин) в группе пациентов с медленным фенотипом N-ацетилирования
представлено на рисунке 3.
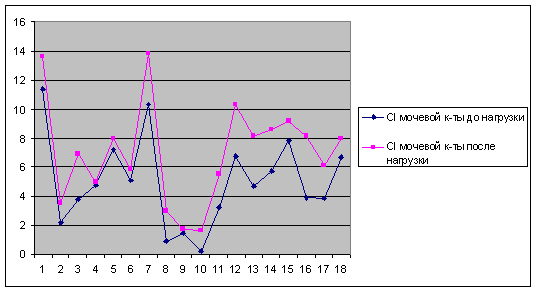
Рисунок 3 - Сравнение результатов выявления клиренса мочевой
кислоты до и после приема кофеина (мл/мин) в группе пациентов с медленным
фенотипом N-ацетилирования
В группе пациентов с быстрым фенотипом N-ацетилирования клиренс
мочевой кислоты до нагрузки кофеином изменялся от 1,97 до 16,65 мл/мин при
среднем значении 6,23±4,92 мл/мин, после нагрузки кофеином от 7,46 до 25,77 при
среднем значении 13,53±6,01 мл/мин. Различия между группами статистически
достоверны (р<0,0001).
Результаты определения клиренса мочевой кислоты в группе
пациентов с быстрым фенотипом N-ацетилирования представлены в таблице 5.
Таблица 5 - Результаты выявления клиренса мочевой кислоты до
и после приема кофеина в группе пациентов с быстрым фенотипом N-ацетилирования
|
№№ пациента
|
Cl до нагрузки
(мл/мин)
|
Cl после
нагрузки (мл/мин)
|
|
1
|
5,16
|
14,56
|
|
2
|
8,32
|
14,88
|
|
3
|
12,25
|
20,01
|
|
4
|
16,65
|
25,77
|
|
5
|
6,94
|
16,2
|
|
6
|
1,97
|
8,15
|
|
7
|
2,51
|
7,46
|
|
8
|
2,77
|
9,12
|
|
9
|
3,4
|
11,45
|
|
10
|
2,33
|
7,68
|
Сравнение результатов выявления клиренса мочевой кислоты до и
после приема кофеина (мл/мин) в группе пациентов с быстрым фенотипом N-ацетилирования
представлено на рисунке 4.
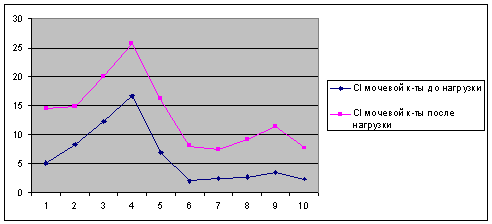
Рисунок 4 - Сравнение результатов выявления клиренса мочевой
кислоты до и после приема кофеина (мл/мин) в группе пациентов с быстрым
фенотипом N-ацетилирования
Клиренс мочевой кислоты до нагрузки кофеином у пациентов с
быстрым фенотипом ацетилятора не отличался от такового у пациентов с медленным
ацетиляторным фенотипом (р=0,41). осле нагрузки кофеином клиренс мочевой
кислоты был статистически достоверно выше у пациентов с быстрым фенотипом
ацетилятора (р=0,001). В данном случае и далее в подобных ситуациях
запланированное сопоставление двух независимых выборок по количественному признаку
произведено с помощью Т-теста. равнение результатов выявления клиренса мочевой
кислоты (мл/мин) до нагрузки кофеином у пациентов с быстрым и медленным
фенотипом ацетилятора представлено на рисунке 5.
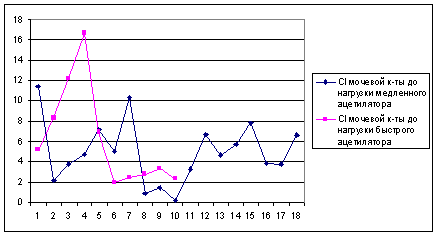
Рисунок 5 - Сравнение результатов выявления клиренса мочевой
кислоты (мл/мин) до нагрузки кофеином у пациентов с быстрым и медленным
ацетиляторным фенотипом
Сравнение результатов выявления клиренса мочевой кислоты
(мл/мин) после нагрузки кофеином у пациентов с быстрым и медленным
ацетиляторным фенотипом представлено на рисунке 6.
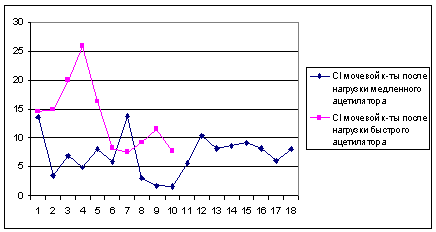
Рисунок 6 - Сравнение результатов выявления клиренса мочевой
кислоты (мл/мин) после нагрузки кофеином у пациентов с быстрым и медленным
ацетиляторным фенотипом
В группе пациентов с медленным фенотипом N-ацетилирования
отмечалось незначительное изменение клиренса мочевой кислоты, которое
варьировала от 0,19 до 4,28 мл/мин и в среднем составляло 2,06±1,22 мл/мин.
Вторая группа обследованных здоровых лиц, рассматриваемых как быстрые
ацетиляторы, отличалась повышенной скоростью образования мочевой кислоты.
Изменение клиренса в данной группе варьировало от 5,35 до 9,4 мл/мин и в
среднем равнялось 7,56±1,42 мл/мин.
Различия в разнице клиренсов мочевой кислоты после и до
нагрузки кофеином между медленными и быстрыми ацетиляторами имели достоверные
статистические различия (р<0,0001).
Сравнение результатов разницы клиренсов мочевой кислоты
(мл/мин) после и до нагрузки кофеином между медленными и быстрыми ацетиляторами
представлено на рисунке 7.
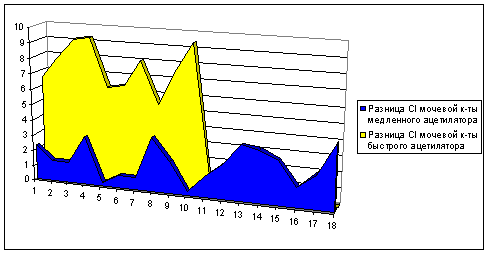
Рисунок 7 - Сравнение результатов разницы клиренсов мочевой
кислоты (мл/мин) после и до нагрузки кофеином между медленными и быстрыми
ацетиляторами
Полученные данные согласуются с результатами единственного
исследования, которое проведено в НИИ детских инфекций г. Санкт-Петербурга. Это
исследование основано на определении разницы в клиренсе мочевой кислоты, но в
отличие от данного исследования проводилось, во-первых, на детской популяции, а,
во-вторых, основывалось на использовании в качестве нагрузки кофеиносодержащих
напитков. Исследователи получили в группе медленных ацетиляторов изменение
клиренса мочевой кислоты в среднем на уровне 1,39±0,97 мл/мин. В группе быстрых
ацетиляторов изменение клиренса мочевой кислоты равнялось 8,13±0,76 мл/мин
[85].
Результаты выявления фенотипа N-ацетилирования на основе
определения изменения клиренса мочевой кислоты после и до нагрузки кофеином у
здоровых лиц представлены в таблице 6.
Таблица 6 - Результаты выявления фенотипа N-ацетилирования на основе
определения изменения клиренса мочевой кислоты после и до нагрузки кофеином у
здоровых лиц
|
Фенотип N-ацетилирования
|
Среднее
значениеCl мочевой кислоты (мл/мин)
|
Диапазон
вариацииCl мочевой кислоты (мл/мин)
|
|
Медленный = 18
человек
|
2,06±1,22
|
от 0,19 до 4,28
|
|
Быстрый = 10
человек
|
7,56±1,42
|
от 5,35 до 9,4
|
Бимодальное фенотипическое распределение пациентов (в %),
полученное по результатам разницы между клиренсом мочевой кислоты после и до
нагрузки кофеином представлены на рисунке 8.
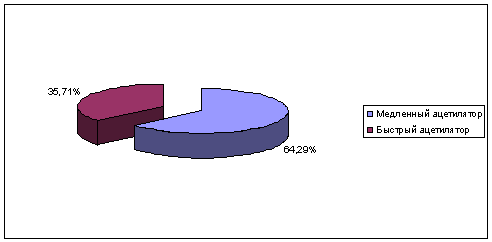
Рисунок 8 - Бимодальное фенотипическое распределение
пациентов (в %), полученное по результатам разницы между клиренсом мочевой
кислоты после и до нагрузки кофеином
Полученные данные согласуются с результатами других
исследований. Например, среди европеоидов Германии частота встречаемости
медленных ацетиляторов, по данным некоторых авторов, колебалась от 62,00% до
71,00% [35, 36], у европеоидов Франции данный показатель варьировал от 53,00%
до 61,30% [89].
Результаты исследования совпадают с данными, полученными
Сатыровой Т.В. с соавторами, которые определили распределение
фенотипов N-ацетилирования
в популяции европеоидов Юго-Восточного региона Республики Беларусь. Определение
фенотипа N-ацетилирования
проводили у 129 волонтеров с помощью метода высокоэффективной жидкостной
хроматографии с ультрафиолетовым обнаружением на аппарате "Agilent 1100" с помощью
тестового препарата "изониазид". Медленный тип ацетилирования имел
место у 66,00% населения, а быстрый - у 34,00% [51]. При сравнении результатов
исследования Сатыровой Т.В. с соавторами с данными, полученными в данном
исследовании, выявлено отсутствие статистически значимых различий (р=0,69).
Установлено, что среди медленных ацетиляторов было 10
(55,56%) мужчин и 8 (44,44%) женщин, среди быстрых ацетиляторов - 6 (60,00%)
мужчин и 4 (40,00%) женщины. Среди курящих волонтеров 5 (55,56%) человек
отнесены к медленным ацетиляторам, 4 (44,44%) - к быстрым ацетиляторам.
Соотношение мужчин и женщин (в %) среди медленных
ацетиляторов представлены на рисунке 9.
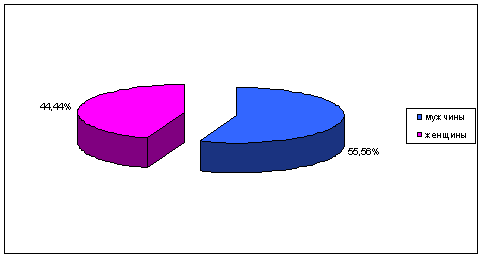
Рисунок 9 - Соотношение мужчин и женщин (в %) среди медленных
ацетиляторов
Соотношение мужчин и женщин (в %) среди быстрых ацетиляторов
представлены на рисунке 10.
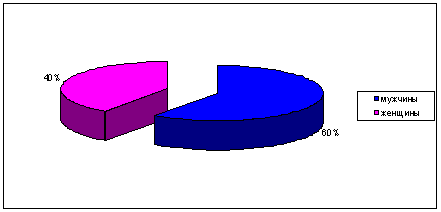
Рисунок 10 - Соотношение мужчин и женщин (в %) среди быстрых
ацетиляторов
Антропометрические характеристики здоровых добровольцев в
зависимости от фенотипа N-ацетилирования представлены в таблице 7.
Таблица 7 - Антропометрические характеристики здоровых
добровольцев в зависимости от фенотипа N-ацетилирования
|
Признак
|
Медленные
ацетиляторы
|
Быстрые
ацетиляторы
|
|
Возраст (М, s, лет)
|
38,78±10,92
|
40,1±7,35
|
|
Масса тела (М, s, кг)
|
72,53±13,23
|
69,1±4,90
|
При изучении статистической взаимосвязи фенотипа N-ацетилирования с
характеристиками здоровых добровольцев не установлено ассоциации активности NAT2 с полом (τ=0,11, р=0,42) добровольцев, их возрастом (τ=0,14, р=0,31), массой тела (τ=-0,03, р=0,79), ростом (τ=-0,06, р=0,64) и пристрастием к курению (τ=0,15, р=0,29). В данном случае оценка взаимосвязи количественных
и/или качественных признаков произведена с помощью ранговой корреляции по
Кендаллу.
Полученные результаты сопоставимы с данными других
исследований. Например, P. A. Philip с соавторами доказали отсутствие корреляции
фенотипа N-ацетилирования
с полом (мужчины - 63: 37, женщины - 59: 41; р>0,05), возрастом (t=0,21, р>0,05; χ2=0,74, р>0,10) и массой тела (t=1,25, р>0,05; rs=-0,053, p>0,50) обследованных
добровольцев [32]. C. B. Ambrosone с соавторами не выявили ассоциации активности NAT2 и курением (отношение
быстрый/медленный ацетилятор составило 37: 63 и 41: 59 среди курящих и
некурящих соответственно, р>0,05) [90].
Таким образом, впервые у здоровых
европеоидов, проживающих в Юго-Восточном регионе Республики Беларусь,
установление вариабельности фенотипа N-ацетилтрансферазы 2 проведено
на основе определения скорости образования конечного продукта метаболизма
кофеина - мочевой кислоты. Установлено, что в популяции Юго-Восточного
региона Республики Беларусь преобладает медленный ацетиляторный статус
(64,29%), а соотношение быстрых и медленных ацетиляторов в
изученной популяции соответствует таковому для большинства стран Европы.
Результаты определения фенотипа ацетилирования
с помощью простого и доступного метода, основанного на разнице клиренсов
мочевой кислоты после и до приема кофеина, сопоставимы с данными, полученными
ранее на той же популяции европеоидов Юго-Восточного региона Республики
Беларусь путем выявления скорости метаболизма изониазида в качестве тестового
препарата с использованием высокоэффективной жидкостной хроматографии. Этот
факт обуславливает возможность использования апробированного метода в
учреждениях практического здравоохранения, так как он не требует больших
материальных и людских затрат, применим не только в стационарах, но и в
поликлиниках, проводится в любых лабораториях.
Метод предполагает замену кофеином
нагрузки другими лекарственными препаратами, обладающими по сравнению с ним
большим числом побочных эффектов. Кофеин является натуральным природным
веществом, алкалоидом пуринового ряда, метаболизм, которого проходит с участием
фермента N-ацетилтрансферазы 2. Описанный метод дает возможность использования
в качестве источников кофеина также и кофеиносодержащих напитков (чай, кофе и
др.). Его можно использовать у беременных и детей.
Предложенный метод предоставляет
возможность практическому врачу без труда определять фенотип ацетилирования,
индивидуализировать фармакотерапию, адекватно оценивать реакцию организма на
проводимое лечение и находить оптимальное соотношение между эффективностью и
безопасностью терапии. Более того, его можно использовать для определения риска
развития целого ряда заболеваний, планировать и проводить в этом направлении
различные профилактические мероприятия.
Таким образом, представленный метод
является простым, быстрым, дешевым, чувствительным и доступным к использованию
в различных клинико-диагностических лабораториях.
Заключение
1. При использовании метода определения фенотипа N-ацетилирования на основе
определения клиренса мочевой кислоты до и после приема кофеина в качестве
тестового препарата среди здоровых европеоидов, проживающих в Юго-Восточном
регионе Республики Беларусь, выявлено 18 (64,29%) медленных и 10 (35,71%)
быстрых ацетиляторов.
. В группе пациентов с медленным типом N-ацетилирования
отмечалось незначительное изменение клиренса мочевой кислоты, которое
изменялось от 0,19 до 4,28 мл/мин (М=2,06±1,22 мл/мин). Быстрые ацетиляторы
отличались повышенной скоростью образования мочевой кислоты с вариацией
изменения клиренса от 5,35 до 9,4 мл/мин (М=7,56±1,42 мл/мин, р<0,0001).
. Распределение фенотипа N-ацетилирования,
полученное с помощью простого и доступного метода, основанного на разнице
клиренсов мочевой кислоты после и до приема кофеина, соответствовало таковому,
полученному на той же популяции европеоидов Юго-Восточного региона Республики
Беларусь путем выявления скорости метаболизма изониазида в качестве тестового
препарата с использованием высокоэффективной жидкостной хроматографии (66%
медленных ацетиляторов, р=0,69).
Практические
рекомендации
1. Для уточнения риска токсичности и ожидаемого
терапевтического эффекта лекарственных средств, метаболизирующихся с помощью
реакций N-ацетилирования,
необходимо определять фенотип N-ацетилирования с использованием простого и доступного
метода, основанного на разнице клиренсов мочевой кислоты после и до приема
кофеина.
. За пограничное значение разницы клиренсов мочевой кислоты
до и после приема кофеина следует принимать величину 4,48 мл/мин, как
минимальное значение показателя для быстрых ацетиляторов.
. Пациентам с медленным фенотипом N-ацетилирования следует
назначать минимальные суточные дозы лекарственных средств, метаболизирующихся с
помощью реакций N-ацетилирования, так как они имеют повышенный риск развития
нежелательных явлений.
. Пациенты с быстрым фенотипом N-ацетилирования нуждаются
в назначении максимальных суточных доз лекарственных средств,
метаболизирующихся с помощью реакций N-ацетилирования, что обеспечит им получение
ожидаемого лечебного эффекта от применения фармакотерапии.
Список
использованных источников
1. Кукес,
В.Г. Клиническая фармакология и фармакотерапия / В.Г. Кукес [и др.]; под общ.
ред.В.Г. Кукеса, А.К. Стародубцева. - 2-е изд., испр. - М.: ГЭОТАР - Медиа,
2006. - 640 с.
2. Баранов,
В. Гены детоксикации, ответственные за биотрансформацию ксенобиотиков / В.
Баранов // Молекулярная биология. - 2000. - Т.34, №4. - С.686.
3. Marsh,
S. Global pharmacogenetics: giving the genome to the masses / S. Marsh, D. J.
van Booven, H. L. McLeod // Pharmacogenomics. - 2006. - Vol.7, № 4. -
P.625-631.
4. Клиническая
фармакология: учеб. / В.Г. Кукеса [и др.]; под общ. ред.В.Г. Кукеса. - 3-е
изд., перераб. и доп. - Москва: "ГЭОТАР - Медиа", 2006. - 154-168 с.
5. Polymorphism
discovery in 51 chemotherapy pathway genes / R. R. Freimuth [et. al.] // Hum.
Mol. Genet. - 2005. - Vol.14, № 23. - P.3595-3603.
. Кукес,
В.Г. Метаболизм лекарственных средств: клинико-фармакологические аспекты / В.Г.
Кукес. - М.: Реафарм, 2004. - 144 c.
. Клиническая
фармакогенетика: учеб. пособие / Д.А. Сычева [и др.]; под общ. ред.В.Г. Кукеса,
Н.П. Бочкова. - Москва: "ГЭОТАР - Медиа", 2007. - 248-267 с.
. Бочков,
Н.П. Клиническая генетика: Учебник / Н.П. Бочков. - 2-е изд., перераб. и доп. -
М.: "ГЭОТАР - Медиа", 2002. - 448 с.
9. Silber, B. M. // Pharmacogenomics / ed. Kalow W., Meyer U., Tyndale R. F. - New York: Marcel Dekker, 2001. -
214 p.
10. Weinshilboum R., Wang L. Pharmacogenomics: bench
to bedside. Nat Rev Drug Disc. 2004; 3: 739-48.
11. Сычев,
Д.А., Фармакогенетическое тестирование: Клиническая интерпретация результатов.
Рекомендации для практикующих врачей / Д.А. Сычев; под общ. ред. Д.А. Сычева. -
Москва, 2011.10-12, 72-76 с.
12. Innocenti F. Pharmacogenomics: Methods and Protocols (Methods in Molecular Biology) // Humana Press, 2005. - 224
p
13. Pharmacogenomics
/ ed. by Rothstein M. A. - New Jersey: Willy-liss, 2003.
14. Новости
"МедАссистанс" [Электронный ресурс] / Применение фармакогенетических
тестов в медицинской практике - Новосибирск, 2012. - [Режим доступа]:
http://medassistans.ru/? p=1536 - Дата доступа: 02.04.2013.
. Белоусов
Ю.Б., Гуревич К.Г. Клиническая фармакология. Практика дозирования лекарств.
Спец. выпуск "Рациональная фармакотерапия"/ Под общ. редакцией Духанина
А.С. - Москва: Литтерра, 2005 - 71-122 с.
. Середенин,
С.Б. Лекции по фармакогенетике / С.Б. Середенин. - М.: Медицинское
информационное агенство, 2004. - 303 с.
. Райс,
Р.Х. Биологические эффекты токсических соединений: курс лекций / Р.Х. Райс, Л.Ф.
Гуляева. - Новосиб. гос. ун-т., Новосибирск, 2003. - 208 с.
18. Sinclair,
J. A fragment consisting of first 204 amino-terminalaminoacids of human
arylamine N-acetyltransferase one and the first transacetylation step of
catalysis / J. Sinclair, E. Sim // Biochem. Pharmacol. - 1997. - Vol.53, № 1. -
P.11-16.
19. Полянская,
Е.М. Определение противотуберкулезных препаратов методом ВЭЖХ для оценки их
фармакокинетики и анализ ее соответствия генетическим предиктором у больных
туберкулезом легкого: автореф. дис. … канд. хим. наук / Е.М. Полянская; НГУ. -
Новосибирск, 2006. - 12-24 с.
. Грэхам-Смит,
Д.Г. Оксфордский справочник по клинической фармакологии и фармакотерапии:
перевод с англ / Д.Г. Грэхам-Смит, Дж.К. Аронсон. - Москва: Медицина, 2000 -
108-109 с.
21. Chromosomal localization of human genes for arylamine N-acetyltransferase
/ D. Hickman [et. al.] // Biochem. J. -
1994. - Vol.297. - P.441-445.
. Meyer,
U. A. Polymorphism of human acetyltransferases / U. A. Meyer // Environmental
Health Perspectives. - 1994. - Vol.102, № 6. - P.213-216.
. Deguchi,
T. Molecular pharmacology of polymorphic arylamine N-acetyltransferase involved
in the metabolism of arylamine drugs / T. Deguchi // Nippon Rinscho. - 1992. -
Vol.50, № 4. - P.877-886.
. Molecular
Genetics and Epidemiology of the NAT1 and NAT2 Acetylation Polymorphisms / D.
W. Hein [et al.] // Cancer Epidemiol. Biomarkers and Prev. - 2000. - Vol.9, №
1. - P.29-42.
25. Vatsis,
K. P. Diverse point mutation in the human gene for polymorphic N-acetyltransferase
/ K. P. Vatsis, R. J. Martell, W. W. Weber // Proc. Natl. Acad. Sci.
USA. - 1991. - Vol.88. - Р.6333-6337.
. Nomenclature
for N-acetyltransferases / K. P. Vatsis [et al.] // Pharmacogenetics. -
1995. - Vol.5, № 1. - Р.1-17.
27. Human NAT2
alleles (Haplotypes) (updated November 1, 2010). Reference gene seuens
published in Genbank Assession Number X14672 [Electronic resourse]. - 2010. -
Mode of access: http://louisville.edu/medschool/pharmacology/
consensus-human-arylamine-n-acetyltransferase-gene-nomenclature/nat_pdf_files
/Human_NAT2_alleles. pdf
<http://louisville.edu/medschool/pharmacology/%20consensus-human-arylamine-n-acetyltransferase-gene-nomenclature/nat_pdf_files%20/Human_NAT2_alleles.pdf>.
- Date of access: 01.11.2010.
. Molecular
mechanism of slow acetylation of drugs and carcinogens in humans / M. Blum [et
al.] // Proc. Natl. Acad. Sci. - 1991. - Vol.88. - P.5237-5241.
. Human
acetyltransferase polymorphisms / D. M. Grant [et. al.] // Mutat. Res. - 1997.
- Vol.376. - P.61-70.
. Arylamine
N-acetyltransferase activity in man / I. Cascorbi [et al.] // Drug. Metab. Rev.
- 1999. - Vol.31. - P.489-502.
. S.
Gardiner, S. Pharmacogenetics, drug-metabilizing enzymes, and clinical practice
/ S. Gardiner, E. Begg // Pharmacol. Rev. - 2006. - Vol.58. - P.521-590.
. Ellard G.
A. Variations between individuals and populations in the acetylation of
isoniazid and its significance for the treatment of pulmonary tuberculosis / G.
A. Ellard // Clin. Pharmacol. Ther. - 1976. - Vol. 19. - P.610-625.
. N-acetyltransferase
2 genotype correlated with isoniazid acetylation in Japanese tuberculous
patients / T. Kita [et al.] // Bio. l Pharm. Bul. l. - 2001. - Vol.5. -
P.544-549.
. Correlation
between acetylation phenotype and genotype in Chinese women / B. Zhao [et al.]
// Eur. J. Clin. Pharmacol.
- 2000. - Vol.56. - P.689-692.
35. Hildebrand,
M. Determination of acetylator phenotype in Caucasians with caffeine / M.
Hildebrand, W. Seifert // Eur. J. Clin. Pharmacol. - 1989. - Vol.37. -
P.525-526.
. Concordance
between the deduced acetylation status generated by high-speed: real-time PCR
based NAT2 genotyping of seven single nucleotide polymorphisms and human NAT2
phenotypes determined by a caffeine assay / H. P. Rihs [et al.] // Clin. Chim.
Acta. - 2007. - Vol.376, № 1/2. - P.240-243.
. N-acetyltransferase
NAT1 and NAT2 genotypes and lung cancer risk / C. Bouchardy [et al.] // Pharmacogenetics.
- 1998. - Vol.8. - P.291-298.
. Acetylation
phenotypes and biological variation in а French Caucasian population / Z. B. Pontes
[et al.] // Eur. J. Clin. Chem. Clin. Biochem. - 1993. - Vol.31, № 2. -
P.59-68.
. Evans, D.
A. P. An improved and simplified method of detecting the acetylator phenotype /
D. A. P. Evans // J. Med. Genet. - 1969. - Vol.6. - P.405-407.
. Paulsen,
O. Distribution of acetylator phenotype in relation to age and sex in Swedish
patients / O. Paulsen, L. G. Nilsson // Eur. J. Clin. Pharmacol. - 1985. -
Vol.28. - P.311-315.
. N-acetyltransferase
phenotype and risk in urinary bladder cancer: approaches in molecular epidemiology.
Preliminary results in Sweden and Denmark / G. M. Lower [et al.] // Environ.
Health. Perspect. - 1979. - Vol.29. - P.71-79.
. Identification
and prevalens study оf 17 allelic variants оf
the human NAT2 gene in а white population / J. A. Agendes [et
al.] // Pharmacogenetics. - 1996. - Vol.6, № 5. - P.423-428.
43. Carrillo,
J. A. Caffein metabolism
in а healthy Spanish population: N-acetylator phenotype
and oxidation pathways / J. A. Carrillo, B. Benthez / Clin.
Pharmacol. Ther. - 1994. -
Vol.55, № 3. - P.293-304.
44. Distribution
and concordance of N-acetyltransferase genotype and phenotype in an American
population / M. Gross [et al.] // Cancer Epidemiol. Biomarkers Prev. - 1999.
- Vol.8. - P.683-692.
. Comparison
between serum and urinary sulphadimidine acetylators as predictors of isoniazid
acetylator status in patients with pulmonary tuberculosis / S. P. N. Singh [et
al.] // Indian. J. Chest. Dis. Allied. Sci. - 1996. - Vol.38. - P.5-11.
. Risk
factors for hepatotoxicity from antituberculosis drugs: A case-control study /
J. N. Pande [et al.] // Thorax. - 1996. - Vol.50. - P.132-136.
47. Rashid,
J. R. Acetylation status
using hydralazine in African hypertensives at Kenyatta National Hospital / J. R.
Rashid, K. Tsepko, F. D. Juma // East Afr. Меd.
J. - 1992. - Vol.69, № 7. - P.406-408.
. N-acetylation
phenotyping with sulfamethazine in an Iranian population / S. Sardas [et
al.] // Pharmacogenetics. - 1993. - Vol.3, № 3. - P.131-134.
49. Характеристика
активности полиморфной N-ацетилтрансферазы у больных бронхиальной астмой /
К.А. Рудинский [и др.] // Пульмонология, 1998. - Прил.: Международный
конгресс Интерастма-98, Москва, 1998. - 20-21 окт. - VIII Национальный конгресс по болезням органов дыхания. - Сб. рез.: 440 с.
. Яковлева, О.А.
Генотипический и фенотипический полиморфизм N-ацетилтрансфераз в роли
предикторов бронхолегочных заболеваний / О.А. Яковлева [и др.] // Пульмонология. - 2003. - № 4. -
С.115-121.
51. Сатырова, Т.В.
Эффективность и безопасность сульфасалазина у пациентов с язвенным колитом в
зависимости от активности N-ацетилтрансферазы 2: автореф. дис. … канд. мед. наук:
14.03.06/Т.В. Сатырова; ГГМУ. - Гомель, 2011. - 51-59 с.
52. Increased genotype frequency of N-acetyltransferase
2 slow acetylation in patients with rheumatoid arthritis / A. Pawlik [et al.] // Clin. Pharmacol. Ther. - 2002. - Vol.72, № 3. -
P.319-325.
. Predisposing
factors in sulphasalazine-induced systemic lupus erythematosus / I. Gunnarsson
[et al.] // The Br. J. of Rheumatol. - 1997. - Vol.36. - P.1089-1094.
54. Прогнозирование
развития обструктивного синдрома у больных хроническим бронхитом с учетом
наследственных факторов / Т.В. Ивчик [и др.] // Тер. архив. - 2001. - № 3. -
С.33-37.
. Характеристика
активности полиморфной N-ацетилтрансферазы у больных бронхиальной астмой /
К.А. Рудинский [и др.] // Пульмонология, 1998. - Прил.: Международный
конгресс Интерастма - 98, Москва, 1998. - 20-21 окт. - VIII Национальный конгресс по болезням органов дыхания. - Сб. рез.: 440 с.
56. Association
between mast cell chymase genotype and atopic eczema: alone and those with
atopic eczema and atopic respiratory disease / K. Tanaka [et al.] // Clin. Exp.
Allergy. - 1999. - Vol.29. - P.800-803.
. Mrozikiewicz
P., Drakoulis N., Roots I. // Clin. Pharmacol. Ther. - 1994. - Vol.56. -
P.626-634.
58. Чекмазов, И.А.
Этиология и патогенез спаек брюшной полости / И.А. Чекмазов // Consilium Medicum [Электронный ресурс]. - 2002. - Т.4, № 1. - Режим
доступа: http://www.consilium-medicum.com/article/13870. - Дата доступа: 21.04.2013.
59. Hepatic
acetylator phenotype in diabetes mellitus / J. M. Ladero [et al.] // Ann. Clin. Res. - 1982. - Vol.14. - P.187-189.
. Оценка фенотипа
ацетилирования у больных ангиной на фоне базисной терапии и лечения ксимедоном
/ И.Э. Кравченко [и др.] // Вопросы биологической, медицинской и
фармацевтической химии. - 2006. - № 4. - С.22-25.
61. Nacak M. Human
arylamine N-acetyltransferase
2 polymorphism and susceptibility to allergic contact dermatitis / Nacak M // Int J Dermatol [Электронный ресурс]. - 2006. - Режим доступа: http://www.ncbi. nlm.
nih.gov/pubmed/16533241. - Дата доступа:
27.04.2013.
. Дворянкова, Е.В.
Терапевтическая эффективность применения отечественного иммуномодулятора
"Полиоксидоний" у больных витилиго: автореф. дис. … канд. мед. наук:
14.00.11/Е.В. Дворянкова; РосМаПО. - М., 2002. - 18 с.
63. Hutabarat,
B. M. Disposition of
drugsin cystic fibrosis. VII. Acetylation of sulphamethoxazol in bloodcells: in
vitro - in vivo соrrelation and characterization of its
kinet-ics of acetylation in lymphocytes / B. M. Hutabarat, A. L. Smith, D.
J. Unadkat // Clin. Pharmacol. Ther.
- 1994. - Vol.44, № 4. - P.427-433.
. Гармонов, С.Ю.
Перспективные методы оценки генетически детерминированной химической
чувствительности организма человека / С.Ю. Гармонов, М.И. Евгеньев, И.Е. Зыкова
// Химическая и биологическая безопасность. - 2003. - № 11/12. - С.3-16.
65. Levy, M.
Drug Acetylation in Liver Disease / M. Levy, Y. Caraco, G. Geisslinger // Clin.
Pharmacokinetics. - 1998. - Vol.34, № 3. - P.219-226.
66. Re-investigation
of the concordance of human NAT2 phenotypes and genotypes / M. Hermann [et al.]
// Archives of Toxicol. - 2005. - Vol.79, № 4. - P. 196-200.
67. Schroder,
H. The Polymorphic acetylation of sulphapyridine in man / H. Schroder, D. A. P.
Evans // J. of Med. Genet. - 1972. - Vol.9. - P.168-171.
68. Influence
of age, sex and body weight on the dapsone acetylation phenotype / P. A. Philip
[et al.] // Br. J. Clin. Pharmac. - 1987. - Vol.23. - P.709-913.
69. Acetylator
phenotype in relation to age and gender in the Baltimore. Longitudinal study of
aging / M. R. Korrapati [et al.] // J. Clin. Pharmacol. - 1997. - Vol.37. -
P.83-91.
. Isoniazid.
International Programme on Chemical Safety. Poisons Information: Monograph
[Electronic resource]. - 2012. - Mode of access: http://www.inchem.org - Date
of access: 02.04.2013.
. Eidu,
L., Harnanansingh, A. A more sensitive spectrophotometric method for
determination of isoniazid in serum or plasma // Clin. Chem. - 1971. - V.17. -
N 6. - Р.492-494.
. Timbrell,
J. A., Wright, J. M., Smith, S. M. Determination of hydrazine metabolites of
isoniazid in human urine by gas chromatography // J. Chromatogr. - 1977. -
V.138 - P.165-172.
. Mehmedagic,
A., Verite, P., Menager, S. Determination of pyrazinamide and its main
metabolites in rat urine by high-performance liquid chromatography // J. Сhromatogr. B. - 1997. - V.695. -
P.365-372.
. W.,
Dayton, P., Israili, Z., Pruitt, A. Spectrophotofluorimetric assay for
isoniazid and acetylisoniazid in plasma adapted to paediatric studies // Clin
Chem. - 1977. - V.23/24. - P.745-748.
. Perrett,
D. Capillary electrophoresis in clinical chemistry // Ann. Clin. Biochem. -
1999. - V.36. - p.133-150.
. Chen,
S-H., Chen, Y-H. Pharmacokinetic applications of capillary electrophoresis //
Electrophoresis. - 1999. - V. 20. - P.3259-3268.
77. Дослiдження бiоеквiвалентностi препаратiв рифампицiну з використанням системи високоефективного капiлярного електрофорезу / А.С. Оганесян [и др.] // Клiнiчна фармацiя. - 2005. - Т.9. - С.22.
78. Инструкция
по применению "Метод определения активности N-ацетилтрансферазы 2 в сыворотке крови": утв. М-вом
здравоохр. Респ. Беларусь 29.12.2010 г., регистрационный № 094-0710/Т.В.
Сатырова, Н.А. Алексеев, Е.И. Михайлова. - Гомель, 2011. - 17 с.
79. Интернет-журнал
"Коммерческая биотехнология" [Электронный ресурс] / Метаболический
паспорт: наука на службе здоровья нации - Москва, 2005. - Режим доступа:
<http://www.cbio.ru/> - Дата доступа: 02.04.2013.
80. Лабораторные
методы исследования в клинике: справочник / В.В. Меньшиков [и др.]; под ред.В.
В. Меньшикова. - М. Медицина, 1987. - 386 с.
81. Звягинцева,
Т.Д. Неспецифический ЯК: современное состояние проблемы / Т.Д. Звягинцева, С.В.
Гриднева // Здоров’я Украiни. -
2006. - № 3 (136). - С.3-5.
82. Grant
P. M., Jang B. K., Kalow W. // J. Clin. Pharmac. Ther. - 1983. - Vol.33. - N 3.
- P.355-359.
83. Лабораторные
методы исследования в клинике: справочник / В.В. Меньшиков [и др.]; под ред.В.
В. Меньшикова. - М. Медицина, 1987. - 221 - 222 с.
84. Axelrod
J., Reichenthal J. // J. Ph. A Exp. Ther. - 1953. - Vol.107. - N 4. - P.519-523.
. Новые
методические подходы к выявлению типа ацетилирования у детей при НВ - вирусной
инфекции: сб. науч. тр. / Науч. - исслед. ин-т детских инфекций г.
Ст-Петербурга. - Санкт-Петербург, 1994. - Вып.4. - С.147-153.
. Берк,
К. Анализ данных с помощью Microsoft Exel.: Пер. с
англ. / К. Берк, П. Кейри. - М.: Издательский дом "Вильямс", 2005. -
560 с.
87. Milliken,
G. Analysis of Messy Data, Vol.1: Designed Experiments / G.milliken, D.
Johnson. - Princeton, N. J.: Van Nostrand, 1984. - P.328.
88. Реброва,
О.Ю. Статистический анализ медицинских данных / О.Ю. Реброва. - М.: Медиа
Сфера, 2006. - 305 с.
89. Acetylator
phenotype and genotype in patients infected with HIV: Discordance between
methods for phenotype determination and genotype / W. M. O’Neil [et al.] // Pharmacogenetics.
- 2000. - Vol.10. - P.171-182.
. Cigarrette
smoking, N-acetyltrasferase 2 genetic polymorphisms and breast cancer risk / C.
B. Ambrosone [et al.] // J. A. M. A. - 1996. - Vol.276, № 18. -
P.1494-1501
91. Сравнительный
анализ результатов фенотипирования и генотипирования по полиморфизму N-ацетилирования
у человека / И.В. Голденкова - Павлова [и др.] // Генетика. - 2006. - Т.42.,
№8. - С.1143-1150.
92. A
pilot study testing the association between N-acetyltransferases 1 and 2 and
risk of oral squamous cell carcinoma in Japanese people / T. Katoh [et al.] // Carcinogenesis.
- 1998. - Vol. 19. - P.1803-1807.
. Johns,
LE. N-acetyltransferase-2 and bladder cancer risk: A meta-analysis / L. E.
Johns, R. S. Houlston Environ // Mol. Mutagen. - 2000. - Vol.36. - P.221-227.
. Evans,
D. A. P. The association of the slow acetylator phenotype with bladder cancer /
D. A. P. Evans, L. C. Eze, E. J. Whibley // J. Med. Genet. - 1983. - Vol. 20, №
5. - P.330-333.