Свойства и получение нитроглицерина
Содержание
ВВЕДЕНИЕ
1. Свойства
жидкостей
2. Физико-химические
свойства нитроглицерина
3
Технология производства
ЗАДАЧА
ЛИТЕРАТУРА
Введение
Нитроглицерин - желтая маслянистая жидкость.
Чрезвычайно мощное и опасное в получении взрывчатых веществ. Работоспособность
550 мл. Взрывается от удара, толчка, перепада температуры. Получают нитрованием
глицерина. От чистоты глицерина зависит выход и безопасность получения
нитроглицерина. Разбавленный водой глицерин должен иметь желтоватую окраску и
нейтральную реакцию на лакмус. Температура плавления глицерина 19 С, кипения
290 С. Получение: 1 гр глицерина при t=20 C медленно ( по каплям ) приливают к
8 гр кислотной смеси состоящей из 60% концентрированной H2SO4 и 40% конц HNO3.
Процесс должен проходить без выделения бурых паров , при повышении температуры
до 50 С взрыв неизбежен. После окончания нитрования нитроглицерин отделяют от
нитрующей смеси и промывают водой и 5% раствором соды, до полного удаления
примесей кислот которые увеличивают его чувствительность.
Свойства жидкостей
Одно и то же вещество в зависимости от
соотношения между средней кинетической и средней потенциальной энергиями частиц
может находиться в одном из трех агрегатных состояниях: твердом, жидком или
газообразном.
Это соотношение энергий определяется внешними
условиями - температурой и давлением. Условия перехода газа в жидкость
определяются изотермами состояния вещества. Изотермой называется кривая
зависимости объема газа от давления при постоянной температуре.
Рассмотрим пример (рис. 1):

Рис. 1. Изотермы газа при
температурах Т1<T2<TКР<T3: АВ - состояние жидкости; В - точка кипения
жидкости; С - точка сухого насыщенного пара; ВС - кипение жидкости; СП -
состояние перегретого пара; К - критическая точка.
Пунктирная кривая ВКС ограничивает
область двухфазных состояний вещества (жидкость+пар). Эта кривая и критическая
изотерма делят диаграмму P-V под изотермой на три области. Под кривой ВКС
расположена область двухфазного состояния, в которой жидкость находится в
равновесии с насыщенным паром, слева от нее находится область жидкого
состояния, а справа область пара. Сверху изотермы АКТКР - газообразное
состояние вещества. Более четко эти области изображены на рисунке 2.

Рис. 2. Фазы состояния в системе
жидкость + пар: Ж - жидкость, П - пар, Г - газ.
Пар (П) отличается от газообразного
состояния (Г) тем, что при изотермическом сжатии переходит в жидкое состояние.
Газ же при Т>TКР не может быть превращен в жидкость ни при каком давлении.
Значения PКР, VКР, TКР называются критическими параметрами газа.
Таким образом, жидкости имеют две
фазы: жидкое и парообразное. Испарение - это процесс, происходящий с
поверхности жидкости. Испарение объясняется вылетом с поверхностного слоя
жидкости молекул, обладающих наибольшей скоростью и энергией. Так что в
результате испарения жидкость охлаждается.
Данное свойство жидкости
используется, например, при тушении пожаров водой: резкое испарение воды
охлаждает зону горения.
Кстати, наш организм при жаркой
погоде выделяет пот. Какой его смысл? А смысл в том, что при испарении пота
охлаждается кожа человека, и он не перегревается.
Испарение происходит при любой
температуре и возрастает при ее повышении до появления кипения. При температуре
кипения интенсивное испарение происходит не только с ее поверхности, но и во
всем объеме жидкости с образованием пузырьков пара. При этом эффект охлаждения
резко возрастает.
Если кипение происходит при
постоянном давлении, то температура жидкости остается постоянной, т.к. все
подводимое тепло тратиться полностью на парообразование (рис. 3).

Рис. 3. Термограмма нагрева жидкости
при P = const: Ткип - температура кипения.
С повышением давления в закрытом
сосуде температура кипения возрастает. Например, ТКИП воды равно 1000С при
P=101,3 кПа и ТКИП=1890С при P=1013 кПа (10 атм). Такая ситуация наблюдается, в
частности, в паровых котлах, где существует вода в жидком виде при температуре
выше 1000С (это так называемая перегретая вода), либо в кастрюле-скороварке
(при РИЗБ=0,2 атм, ТКИП=1200С).
Если прекратить нагрев и расходовать
пар, то кипение продолжается до снижения температуры до 1000С и атмосферного
давления. Если же резко сбросить давление (например, при лопнувшей трубе
котла), то перегретая вода мгновенно превращается в пар с резким скачком его
давления и взрывом. Напротив, в условиях пониженного давления атмосферы
температура кипения снижается. Это повышает взрывоопасность горючих жидкостей,
из-за повышения интенсивности испарения и создания взрывоопасных концентраций
паров.
Каждой температуре жидкости
соответствует свое максимально возможное количество пара над жидкостью. Это так
называемый насыщенный пар, т.е. пар, находящийся в равновесии с жидкостью.
Давление такого пара называется упругостью насыщенного пара. Упругость
насыщенного пара - это максимально возможное количество пара в воздухе над
жидкостью при данной температуре, т.е. максимальное парциальное давление. При
более высоком содержании пар начинает конденсироваться.
С повышением температуры упругость
пара возрастает. Например, для водяных паров при 00С она равна 611 Па, или 0,6
%, при 200С - 2,3%, при температуре кипения 1000С - 100% (рис. 4).
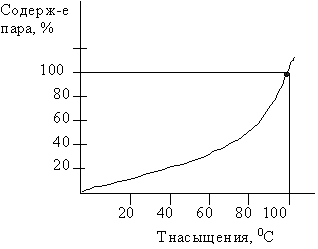
Рис. 4. Диаграмма упругости
насыщенного пара
Зависимость давления насыщенного
пара Рн от температуры жидкости Тж рассчитывается по уравнению Антуана:
lgPH = A - B/(C + Tж), где: А, В, С
- термодинамические константы.
Это уравнение используется для
оценки условий взрываемости паровоздушных смесей.
Физико-химические свойства
нитроглицерина
Сложный эфир
<http://ru.wikipedia.org/wiki/%D0%A1%D0%BB%D0%BE%D0%B6%D0%BD%D1%8B%D0%B9_%D1%8D%D1%84%D0%B8%D1%80> глицерина
<http://ru.wikipedia.org/wiki/%D0%93%D0%BB%D0%B8%D1%86%D0%B5%D1%80%D0%B8%D0%BD>
и азотной кислоты <http://ru.wikipedia.org/wiki/%D0%90%D0%B7%D0%BE%D1%82%D0%BD%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0>.
Прозрачная вязкая нелетучая жидкость (как масло), склонная к переохлаждению
<http://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D1%80%D0%B5%D0%BE%D1%85%D0%BB%D0%B0%D0%B6%D0%B4%D1%91%D0%BD%D0%BD%D0%B0%D1%8F_%D0%B6%D0%B8%D0%B4%D0%BA%D0%BE%D1%81%D1%82%D1%8C>.
Смешивается с органическими растворителями, почти нерастворим в воде (0.13% при
20C, 0,2% при 50C, 0,35 % при 80 °C, по другим данным 1,8 % при 20 °C и 2,5 %
при 50C). При нагревании с водой до 80 °C гидролизуется
<http://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%BE%D0%BB%D0%B8%D0%B7>.
Быстро разлагается щёлочами
<http://ru.wikipedia.org/wiki/%D0%A9%D1%91%D0%BB%D0%BE%D1%87%D1%8C>.
Токсичен, всасывается через кожу,
вызывает головную боль. Очень чувствителен к удару, трению, высоким
температурам, резкому нагреву и т. п. Чувствительность к удару
<http://ru.wikipedia.org/wiki/%D0%A7%D1%83%D0%B2%D1%81%D1%82%D0%B2%D0%B8%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D0%BE%D1%81%D1%82%D1%8C_%D0%BA_%D1%83%D0%B4%D0%B0%D1%80%D1%83>
для груза 2 кг
<http://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D0%BB%D0%BE%D0%B3%D1%80%D0%B0%D0%BC%D0%BC>
- 4 см
<http://ru.wikipedia.org/wiki/%D0%A1%D0%B0%D0%BD%D1%82%D0%B8%D0%BC%D0%B5%D1%82%D1%80>
(гремучая ртуть <http://ru.wikipedia.org/wiki/%D0%93%D1%80%D0%B5%D0%BC%D1%83%D1%87%D0%B0%D1%8F_%D1%80%D1%82%D1%83%D1%82%D1%8C>-
2 см, тротил
<http://ru.wikipedia.org/wiki/%D0%A2%D1%80%D0%BE%D1%82%D0%B8%D0%BB> -
100 см). Весьма опасен в обращении. При осторожном поджигании в малых
количествах неустойчиво горит синим пламенем. Температура кристаллизации 13,5
°C (стабильная модификация
<http://ru.wikipedia.org/w/index.php?title=%D0%A1%D1%82%D0%B0%D0%B1%D0%B8%D0%BB%D1%8C%D0%BD%D0%B0%D1%8F_%D0%BC%D0%BE%D0%B4%D0%B8%D1%84%D0%B8%D0%BA%D0%B0%D1%86%D0%B8%D1%8F&action=edit&redlink=1>,
лабильная
<http://ru.wikipedia.org/w/index.php?title=%D0%9B%D0%B0%D0%B1%D0%B8%D0%BB%D1%8C%D0%BD%D0%B0%D1%8F_%D0%BC%D0%BE%D0%B4%D0%B8%D1%84%D0%B8%D0%BA%D0%B0%D1%86%D0%B8%D1%8F&action=edit&redlink=1>
кристаллизуется при 2,8 °C). Кристаллизуется со значительным увеличением
чувствительности к трению. При нагревании до 50 °C начинает медленно
разлагаться и становится ещё более взрывоопасным. Температура вспышки около 200
°C. Теплота взрыва 6,535 МДж <http://ru.wikipedia.org/wiki/%D0%94%D0%B6%D0%BE%D1%83%D0%BB%D1%8C>/кг.
Температура взрыва 4110 °C. Несмотря на высокую чувствительность,
восприимчивость к детонации довольно низка - для полного взрыва необходим капсюль-детонатор
<http://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D0%BF%D1%81%D1%8E%D0%BB%D1%8C-%D0%B4%D0%B5%D1%82%D0%BE%D0%BD%D0%B0%D1%82%D0%BE%D1%80>
№ 8. Скорость детонации
<http://ru.wikipedia.org/wiki/%D0%A1%D0%BA%D0%BE%D1%80%D0%BE%D1%81%D1%82%D1%8C_%D0%B4%D0%B5%D1%82%D0%BE%D0%BD%D0%B0%D1%86%D0%B8%D0%B8>
7650 м/с. 8000-8200 м/c - в стальной трубе диаметром 35 мм, инициирован с
помощью детонатора
<http://ru.wikipedia.org/wiki/%D0%9A%D0%B0%D0%BF%D1%81%D1%8E%D0%BB%D1%8C-%D0%B4%D0%B5%D1%82%D0%BE%D0%BD%D0%B0%D1%82%D0%BE%D1%80>
№ 8. В обычных условиях жидкий НГЦ часто детонирует в низкоскоростном режиме
1100-2000 м/с. Плотность 1,595 г/см³, в твёрдом виде - 1,735 г/см³. Твёрдый
нитроглицерин менее чувствителен к удару, но более к трению, поэтому очень
опасен. Объем продуктов взрыва 715 л/кг. Фугасность
<http://ru.wikipedia.org/wiki/%D0%A4%D1%83%D0%B3%D0%B0%D1%81%D0%BD%D0%BE%D1%81%D1%82%D1%8C>
и бризантность
<http://ru.wikipedia.org/wiki/%D0%91%D1%80%D0%B8%D0%B7%D0%B0%D0%BD%D1%82%D0%BD%D0%BE%D1%81%D1%82%D1%8C>
сильно зависят от способа инициирования, при использовании слабого детонатора
мощность сравнительно невелика. Фугасность
<http://ru.wikipedia.org/wiki/%D0%A4%D1%83%D0%B3%D0%B0%D1%81%D0%BD%D0%BE%D1%81%D1%82%D1%8C>
в песке - 390 мл, в воде - 590 мл (кристаллического несколько выше),
работоспособность (фугасность) в свинцовой бомбе
<http://ru.wikipedia.org/wiki/%D0%A1%D0%B2%D0%B8%D0%BD%D1%86%D0%BE%D0%B2%D0%B0%D1%8F_%D0%B1%D0%BE%D0%BC%D0%B1%D0%B0>
550 см³.
Применяется
как компонент некоторых жидких ВВ
<http://ru.wikipedia.org/wiki/%D0%92%D0%B7%D1%80%D1%8B%D0%B2%D1%87%D0%B0%D1%82%D1%8B%D0%B5_%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%B0>,
динамитов
<http://ru.wikipedia.org/wiki/%D0%94%D0%B8%D0%BD%D0%B0%D0%BC%D0%B8%D1%82>
и главным образом бездымных порохов
<http://ru.wikipedia.org/wiki/%D0%91%D0%B5%D0%B7%D0%B4%D1%8B%D0%BC%D0%BD%D1%8B%D0%B9_%D0%BF%D0%BE%D1%80%D0%BE%D1%85>
(пластификатор - нитроцеллюлоза
<http://ru.wikipedia.org/wiki/%D0%9D%D0%B8%D1%82%D1%80%D0%BE%D1%86%D0%B5%D0%BB%D0%BB%D1%8E%D0%BB%D0%BE%D0%B7%D0%B0>).
Кроме того, в малых концентрациях применяется в медицине.
Технология производства
Получение нитроглицерина с
последующей сепарацией его от отработанной кислоты является одним из самых
опасных процессов химической технологии.
CH2
- CH - CH2
׀ ׀ ׀ +3 HNO3
→
OH OH
OH
→ CH2 - CH - CH2
׀
׀ ׀
O O O O2H3 -
׀ ׀ ׀
2
NO NO2 2NO
ִכ גוהוםט ודמ
ענובףועס מסמבוםםמ
עשאעוכםי
ךמםענמכ ךאך
סנ, עאך
ט אןןאנאעףנ.
ֽומבץמהטלמו
ףסכמגטו
בוחמןאסםמסעט
ןנמטחגמהסעגא
- עמקםמו
סמבכהוםטו
עוץםמכמדטט ט
ןנאגטכ נאבמע, ךמעמנא המכזםא
ןנמטחגמהטעס גסמךמךגאכטפטצטנמגאםםלט
נאבמקטלט ט
ץמנמרמ
ןמהדמעמגכוםםל
טםזוםונםמ-עוץםטקוסךטל
ןונסמםאכמל. ־הםאךמ
גמחלמזםמסע גחנגא ג
ןנמטחגמהסעגו
םטענמדכטצונטםא
גסו זו
ןמכםמסע םו
טסךכקאועס. ֺמנוםםל
נורוםטול
גמןנמסא
בוחמןאסםמי
נאבמע מבסכףזטגאשודמ
ןונסמםאכא ג עמל
ןנמטחגמהסעגו
למזוע בע עמכךמ
ןמכםי
אגעמלאעטקוסךטי
ךמםענמכ ט
הטסעאםצטמםםמו
ףןנאגכוםטו. ׂאךא מנדאםטחאצט ןנמצוססא
האוע ןמכםף דאנאםעט מעסףעסעגט זונעג
ןנט
גמחלמזםמל
גחנגו
ט ףלוםראוע
גונמעםמסע גחנגא, עאך
ךאך
ןנמטחגמהסעגוםםי
ןנמצוסס
בףהוע
נודףכטנמגאעס לוץאםטחלאלט, ֲ םאסעמשוו
גנול במכרטםסעגמ
ףסעאםמגמך ןמ
ןמכףקוםט םטענמדכטצונטםא
ןונוגוהום םא
אגעמלאעטקוסךטי
ךמםענמכ ט
הטסעאםצטמםםמו
ףןנאגכוםטו.
ֲסו
עוץםמכמדטקוסךטו
סעאהטט
ןנמטחגמהסעגא
םטענמדכטצונטםא, בכאדמהאנ זטהךמלף
אדנודאעםמלף
סמסעמםט נואדוםעמג
ט במכרמי
סךמנמסעט טץ
גחאטלמהויסעגט, כודךמ
מסףשוסעגכועס ג
אןןאנאעאץ
םוןנונגםמדמ
הויסעגט, ךמעמנו, ג
סגמ