Биоинженерия – использование микроорганизмов, вирусов, трансгенных растений и животных в промышленном синтезе
Введение
Биоинженерия одно из самых современных направлений науки, возникшее на
стыке физико-химической биологии, биофизики, генной инженерии и компьютерных
технологий. Бурное развитие этих областей за последние годы позволило ученым
перейти от простого исследования природных биообъектов к их изменению и
усовершенствованию, улучшению их полезных свойств, к созданию совершенно новых
биологических объектов, не существующих в природе. Сфера деятельности
биоинженерии простирается от создания искусственных органов для компенсации
сниженных или утраченных физиологических функций (биомедицинская инженерия) до
разработки генетически модифицированных организмов, например,
сельскохозяйственных растений и животных (генетическая инженерия).
Среди задач биоинженерии - искусственные белки, выполняющие заданные
функции; новые клеточные структуры, обладающие полезными свойствами, и даже
целые живые организмы, сконструированные для нужд человека.
В основе биоинженерии - применение технических подходов для решения
медицинских проблем в целях улучшения охраны здоровья. Эта инженерная
дисциплина направлена на использование знаний и опыта для нахождения и решения
проблем биологии и медицины.
Производство продуктов микробного синтеза первой фазы
К наиболее известным промышленным продуктам микробного синтеза относятся:
ацетон, спирты (этанол, бутанол, изопропанол, глицерин), органические кислоты
(лимонная, уксусная, молочная, глюконовая, итаконовая, пропионовая),
ароматизаторы и вещества, усиливающие запахи (глутамат натрия). Спрос на
последние постоянно увеличивается из-за тенденции к употреблению малокалорийной
и растительной пищи, для придания вкусу и запаху пищи разнообразия.
Ароматические вещества растительного происхождения можно производить путём
экспрессии генов растений в клетках микроорганизмов. Методом генной инженерии в
клетки Е. coli введён ген, кодирующий синтез а-антитрипсина человека,
ингибирующсго активность эластазы. Его образование бактериями достигает 15%
синтеза всех клеточных белков. Таким образом, получают препарат эглин,
применяемый для компенсации врождённого отсутствия а-антитрипсина, приводящего
к тяжёлой форме эмфиземы лёгких. Иммуномодулятор бестатин, ингибитор
поверхностных пептидаз лимфоцитов, продуцирует Streptococcus olivoretuculi.
Микроорганизмы - продуценты ингибиторов других важных в медицине ферментов.
Например, ингибитор амилазы, синтезируемый Streptococcus tendae, блокирует
гидролиз крахмала и снижает содержание сахара в крови; назначается больным
диабетом. Каптоприл из культуральной жидкости стрептококков препятствует
образованию ангиотензина II и снижает артериальное давление (АД) у
гипертоников.
Производство продуктов микробного синтеза второй фазы
С использованием микроорганизмов получают витамины В1, В2 (продуценты-
бактерии, грибы родов Candida, Pichia, Ashbya); фолиевую, пантотеновую кислоты,
пиридоксаль, витамин В12 (продуценты - Propionibacterium shermanii, Pseudomonas
denitrificam или метаногенные бактерии). Витамин С производят путём химического
синтеза, однако этап высокоселективного дегидрирования D-сорбита в L-сорбозу
осуществляют с помощью уксуснокислых бактерий.
Крупномасштабное производство антибиотиков способно давать десятки тысяч
тонн продукта в год. Усовершенствование производства антибиотиков связано с
селекцией культур, резистентных к бактериофагам, а также с применением
мутантных штаммов, у которых отсутствуют системы обратного подавления синтеза
антибиотиков. Крупная веха в истории антибиотиков - возможность химической
модификации природных (образуемых микроорганизмами) антибиотиков. В настоящее
время производят большое количество полусинтетических антибиотиков -
направленное изменение структуры антибиотика позволяет расширить спектр
действия и, отчасти, снять проблему устойчивости к антибиотикам [1].
Производство аминокислот, органических кислот, витаминов
Производство аминокислот относится к одной из наиболее передовых областей
биотехнологии. Аминокислоты получают путем химического синтеза или экстракцией
из белковых гидролизатов.
Незаменимые аминокислоты могут получаться микробиологическим путем более
эффективно, чем путем химического синтеза, так как при биологическом синтезе
используемые микроорганизмы образуют аминокислоты в биологически активной
L-форме. Как продуценты лизина изучаются Brevibacterium lactofermentum и
бактерии рода Corynebacterium, также предложены способы биотехнологического
получения изолейцина, треонина при использовании E. coli. Большинство
исследованных штаммов микроорганизмов независимо от их систематического
положения преимущественно накапливают L-аланин и глутаминовую кислоту.
Значительно меньше штаммов и в меньшем количестве выделяют аспарагиновую
кислоту, лейцин, валин, изолейцин, лизин. За рубежом 60% мощностей по
производству аминокислот занимают глутаминовая кислота, далее идут метионин, лизин
и глицин. Глутаминовая кислота производится при участии в качестве продуцента
штамма Corynebacterium.
С помощью микроорганизмов можно получить до 60 органических кислот.
Многие из них получаются в промышленном масштабе - итаконовая, молочная,
уксусная, лимонная, яблочная, янтарная. Эти пищевые кислоты используются как
регуляторы кислотности и консерванты. Лимонную кислоту получают с помощью
Yarrowia lipolytica, Aspergillus niger, молочную - Endomycopsis fibuligera,
Rhisopus oryzae, Lactobacillus casei, янтарную - Anaerobiospirillum
succiniproducens. Уксусную кислоту получают путем микробиологической конверсии
водорода и углекислого газа бактериями Acetobacterium woodi и Clostridium
aceticum.
Микроорганизмы содержат много витаминов, которые чаще всего входят в
состав ферментов. Состав и количество витаминов в биомассе зависят от
биологических свойств данной культуры микроорганизмов и условий
культивирования. Некоторые витамины микроорганизмы синтезируют, другие напротив
усваивают в готовом виде из окружающей среды. Культура, способная синтезировать
какой-либо витамин, называется автотрофной по отношению к нему, если культура
не способна синтезировать данный витамин, она является авто-гетеротрофной.
Витамины синтезируют в основном химическим путем или получают из
естественных источников. Однако эргостерин, рибофлавин (В2), витамин В12 и
аскорбиновую кислоту (микроорганизмы используются как селективные окислители
сорбита в сорбозу при производстве витамина С) получают микробиологическим
путем. Для синтеза витаминов В1, В2, В6, В12 и аскорбиновой кислоты также
используют кефирные грибки, а бифидобактерии - группы В, РР (никотиновая
кислота) и Н, однако пока эти микроорганизмы не используются как продуценты
витаминов в промышленных масштабах.
Изменяя условия среды, содержание отдельных витаминов можно увеличить.
Так, количество рибофлавина зависит от интенсивности аэрации и содержания
железа в среде. Количество витаминов в клетках, а также их выделение из
последних можно изменить при помощи микроэлементов. Существует производство
рибофлавина на основе использования дрожжеподобных грибов Eremothecium ashbyii
и Ashbia gossypii. Рибофлавин продуцируется также видами Clostridium и
Ascomycetes. Микроводоросль Dunalieiia viridis культивируется с целью получения
β-каротина.
Микроорганизмы являются источником получения липидов специального
назначения с заранее определенными свойствами. Микробные жиры заменяют
растительные (а в ряде случаев и превосходят)и могут использоваться в разных
отраслях промышленности, с.-х., медицине.
Получение пищевых ароматизаторов микробиологическим путем может быть
более выгодным и продуктивным, чем их химический синтез или другие традиционные
способы. Так, в США был разработан экологически безопасный биокаталитический
способ синтеза ванилина из глюкозы с использованием генетически
модифицированного штамма E. coli и грибного фермента дегидрогеназы. Аромат
ванилина при биотехнологическом его получении оказался в несколько раз
интенсивнее обычного.
Весьма перспективно использование грибных культур в качестве продуцентов
сырных, грибных, рыбных ароматизаторов. Освоены биотехнологические способы
получения веществ, имитирующих ароматы земляники, малины, банана, кокоса,
яблока, персика, миндаля.
Микроорганизмы являются важным источником получения полимерных материалов
на основе полисахаридов. Ценным микробным полисахаридом является декстран,
образуемый бактериями рода Leucomonstoс. Декстран служит основой получения
медицинских препаратов (кровезаменителей) и препаратов для биохимических
исследований - сефадексов и др. молекулярных сит. Нуклеозиды, нуклеотиды и их
производные также можно получать с помощью микроорганизмов.
Производство
спиртов и полиолов
Этиловый спирт используется для технических нужд - для производства
синтетического каучука, как растворитель, для синтеза других веществ, а также
на изготовление напитков и медицинские нужды. Спиртовое брожение - хорошо
изученный биохимический процесс. Спиртовое брожение вызывают чаще всего дрожжи,
реже некоторые бактерии (Sarcina) и плесневые грибы (Mucor). В промышленности
дрожжи обычно разделяют на верховые и низовые. Верховые дрожжи интенсивно ведут
брожение и труднее осаждаются. К ним принадлежат спиртовые и хлебопекарные
дрожжиSaccharomyces cerevisiae, а также винные дрожжи из вида Saccharomyces
elipsoideus. К низовым дрожжам относятся виды, используемые в пивоваренной
промышленности. В производстве процесс брожения ведут 2 - 3 суток.
В ходе брожения углеводы распадаются в конечном итоге до этилового
спирта, углекислого газа и воды. Промежуточный продукт - ацетальдегид. Если к
питательной среде добавить сульфиты, которые связывают ацетальдегид, при
брожении можно получить значительное количество глицерина, что и применяется в
промышленности. В этом случае основной конечный продукт брожения - трехатомный
спирт глицерин. В процессе спиртового брожения могут накапливаться изоамиловый,
амиловый и изобутиловый спирты (сивушные масла). Некоторые дрожжи и бактерии
способны продуцировать бутанол, а также 2,3-бутандиол. Эти продукты обычно
синтезируют из нефти, однако микробное получение этанола и других спиртов
вызывает все больший интерес.
В России большая часть этанола получается микробиологическим путем из
растительного сырья. Сырьем могут быть гидролизаты древесины, меласса, крахмал,
молочная сыворотка. Отходы производства этанола содержат белки, углеводы,
рибофлавин и др. витамины, и могут использоваться как кормовая добавка.
При
получении спирта из древесины перед гидролизом древесину размельчают до стружек
толщиной 3 мм, шириной 10 - 70 мм и длиной 25 мм. Гидролиз идет в больших (до
50 кубометров) гидролизных аппаратах, которые наполняют стружкой, добавляют
0,5%-ный раствор Н2SО4 и вводят пар давлением 1-1,2 МПа. Варка идет 40-50 мин.
Выход сахара 45- 48% от сухой массы древесины. Реакция среды полученного
гидролизата кислая, рН 1,8-2,2, поэтому гидролизат нейтрализуют известковым
молоком, в котором содержится 1,1 -1,2 кг/л извести; в гидролизате сравнительно
мало азота и фосфора, поэтому предварительно к каждому кубическому метру
гидролизата добавляют 0,3 кг суперфосфата и 0,15 кг сульфата аммония. При
температуре 85°С через гидролизат продувают воздух, рН среды 5-6. Гипс
осаждают, а прозрачную часть гидролизата после охлаждения используют для
сбраживания. Спирт получают и из мелассы. Предварительная подготовка
питательной среды очень проста - мелассу разбавляют и добавляют питательные
соли. Для приготовления напитков используют спирт
<#"697863.files/image001.jpg">
Среди рекомбинантных белков, полученных из молока трансгенных животных,
известны следующие:
человеческий белок С;
альфа -1- антитрипсин;
химозин.
Получение этих белков достигло такой стадии, которая представляет
коммерческий интерес. В 2006 году разрешено производство и реализация на
фармацевтическом рынке сентритромбина, полученного из молока трансгенных коз
(фирма «GTC Терапевтик»).
Одним из основных преимуществ трансгенной технологии, является её высокая
экономическая эффективность. Потребность мирового рынка в рекомбинантных белках
в 2000 году оценивалась в 13 млрд. долларов, а рынок антител в настоящее время
составляет более 1 млрд. долларов. Производством белков фармакологического
назначения с помощью трансгенных животных занимаются более 20 фирм во всём
мире. Если стоимость 1 г рекомбинантного белка в культуре клеток биореактора
колеблется в пределах 100-1000 долларов в зависимости от выхода белка и
мощности биореактора, то затраты на его производство с молоком
сельскохозяйственных животных составляет 40-50 долларов.
Другим преимуществом этой технологии является высокая производственная
ёмкость молочной железы трансгенных животных.
Если принять во внимание, что концентрация рекомбинантного белка в молоке
будет, по меньшей мере, 1 мг/мл, то можно подсчитать число животных,
необходимых для обеспечения количества того или иного фармацевтического белка.
Таблица 4. Количество трансгенных животных, необходимых для обеспечения
мирового рынка отдельными фармацевтическими белками
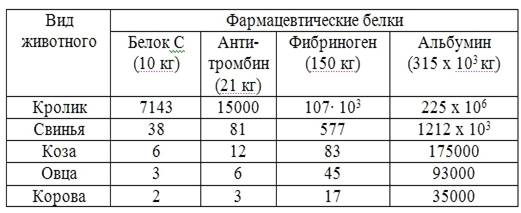
Из данных таблицы можно сделать вывод, что шести коз и двух коров
достаточно, чтобы обеспечить годовую потребность мирового рынка с белке С,
тогда как для такого же его производства потребуется 5 млн. литров донорской
крови. При этом надо учесть, что использование трансгенных животных позволяет
избежать переноса вирусной инфекции.
Группа учёных в Эдинбурге (Великобритания) в 1992г. получила трансгенных овец с
человеческим геном альфа-1-антитрипсина и бета глобулиновым промотором. У
четырёх овец содержание этого белка составляло более 1 г/ л, а одна овца
сначала продуцировала 60 г/л, а затем стабилизировалась на 35 г/л, что
соответствует половине всех белков в молоке. Все овцы здоровы и не имеют
каких-либо нарушений лактации. При таком уровне может быть получено более 10 кг
белка от одного животного в год, что достаточно для 50 пациентов при лечении
эмфиземы лёгких.
Активно проводится работа по созданию трансгенных животных с целью
получения от них белков молока обладающих целебными свойствами. Уже созданы в
США, Австралии, Японии и Беларуси трансгенные коровы, свиньи, козы
продуцирующие лекарственные вещества против: инфекционных заболеваний,
тромбоза, гемофилии, малярии, диабета и др.
Группа учёных в Москве (Л. Эрнст, Г. Брем, М. Прокофьев, И. Гольдман,
2004 г) впервые получила трансгенных овец с геном химозина, которые продуцируют
с молоком в среднем 200-300 мг фермента химозина в 1 л молока. Этот источник
получения химозина может заменить традиционный способ его получения из сычугов
молочных телят и ягнят, но его стоимость в 10 раз ниже.
Испытан новый американский препарат - антитромбин, полученный из молока
трансгенных животных. Считается, что он является лучшим и произвел революцию в
излечении людей от инфарктов.
Созданы трансгенные коровы и козы, в молоке которых содержится
человеческий альбумин, способствующий снижению кровяного давления.
В Канаде от выдающейся трансгенной козы получают белки человека на сумму 20 000
долларов ежедневно [9].
Заключение
В настоящее время описано получение многих видов
трансгенных растений, синтезирующих белки, ценные для фармакологии и медицины.
Эти виды включают как лабораторные модельные растения (табак, арабидопсис), так
и традиционные сельскохозяйственные культуры: злаковые (рис, пшеница, кукуруза)
и плодово-овощные культуры (томаты, бананы, картофель). По-видимому, в
ближайшем будущем будут разработаны различные специализированные системы
продукции белков фармацевтического назначения: «растение (орган, ткань) - ген
целевого белка - регуляторные элементы генетической экспрессии». Для биосинтеза
низкомолекулярных биологически активных вешеств выбор растений-продуцентов
будет определяться присутствием и количественным содержанием конкретных
вторичных метаболитов - субстратов для проведения целевой энзиматической
реакции. Выбор растения-продуцента биологически активных веществ
фармацевтического назначения будет определяться и такими требованиями как
экономичность, затраты на культивирование растений и их хранение, легкость
выделения из них целевых белков.
Список литературы
1. <http://meduniver.com/Medical/Microbiology/131.html>
. <http://www.biotechnolog.ru/>
интерактивный учебник по биотехнологии (Кузьмина Н.А. Омский государственный
педагогический университет
. <http://www.bioplaneta.ru/research/ecology/deodorization.php>
. Gleba, Y. Y.;
Giritch, A. Plant Viral Vectors for Protein Expression // Recent Advances in
Plant Virology. - Caister Academic Press
<http://ru.wikipedia.org/w/index.php?title=Caister_Academic_Press&action=edit&redlink=1>,
2011.
5. «Вопросы
биологической, медицинской и фармацевтической химии» 2006. № 2. С. 3-12 Е.Б.
Рукавцова, Я.И. Бурьянов, Н.Я. Шульга, В.А. Быков
6. http://www.dissercat.com/content/sintez-v-rasteniyakh-poverkhnostnogo-antigena-virusa-gepatita-b-povyshenie-biologicheskoi-be#ixzz2iNfWdAGX
<http://www.dissercat.com/content/sintez-v-rasteniyakh-poverkhnostnogo-antigena-virusa-gepatita-b-povyshenie-biologicheskoi-be>
. <http://pharmapractice.ru/5155>
. <http://www.rusbiotech.ru/novice/zvery_chto.php>
. <http://ggau.by/moodle/mod/resource/view.php?id=6074>