Экологическая оценка процессов загрязнения природных вод и технологий их очистки на станциях 'Водоканала'
Российский
государственный аграрный университет - МСХА
им. К.А.
Тимирязева
Факультет
почвоведения, агрохимии и экологии
Кафедра
экологии
Курсовая
работа
по
дисциплине «Геоэкология»
На
тему: «Экологическая оценка процессов загрязнения природных вод и технологий их
очистки на станциях «Водоканала»
Научный руководитель: профессор И. М. Яшин
Исполнитель: бакалавр 2-го курса 205 группы
Леонова А. В.
Москва 2013
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
КАЧЕСТВО ВОДЫ
АНТРОПОГЕННЫЕ ИСТОЧНИКИ ЗАГРЯЗНЕНИЙ
РАСПРОСТРАНЕНИЕ ЗАГРЯЗНИТЕЛЕЙ
СУЩНОСТЬ ПРОЦЕССА
МЕТОДИКА ОЦЕНКИ ЗАГРЯЗНЕНИЙ
ОХРАНА ВОДНЫХ РЕСУРСОВ
ХАРАКТЕРИСТИКА МОСКВЫ-РЕКИ
ТЕХНОЛОГИИ ОЧИСТКИ ВОДЫ НА СТАНЦИЯХ
«ВОДОКАНАЛА»
СПИСОК ЛИТЕРАТУРЫ
ВВЕДЕНИЕ
Одной из самых острых проблем современности
является нехватка чистой питьевой воды в крупных городах. Реки и озёра уже не
могут выполнять многих своих функций: воду из них нельзя использовать для
приготовления пищи, в них нельзя ловить рыбу, на грязных берегах никто не хочет
отдыхать.
В связи с выполнением работы были поставлены
следующие цели:
· изучить и раскрыть источники
загрязнения гидросферы
· изучить и раскрыть виды загрязнений
· изучить и раскрыть способы
предотвращения загрязнений
· изучить и раскрыть методы очистки
природных вод на станциях «Водоканала»
КАЧЕСТВО ВОДЫ
Понятие качества воды включает в себя
совокупность состава и свойств, определяющих пригодность её для конкретных
видов водопользования и водопотребления. Требования к качеству воды со стороны
водопотребителя различны и зависят от тех функций, которые она выполняет.
Наиболее высокие треования к качеству воды предъявляются при использовании её
для питьевых целей и для разведения рыбы.
Параметры оценки качества воды:
· запах и окраска
· привкус и содержание взвешенных и
плавающих веществ
· температура и значение рН
· наличие кислорода и органических
веществ
· содержание вредных и токсичных
примесей.
Вода считается чистой, если её состав и свойства
ни по одному из показателей не выходят за пределы установленных нормативов.
Вредные вещества в зависимости от их состава и
характера действия нормируются по лимитирующему показателю вредности (ЛПВ).
ЛПВ - наибольшее отрицательное влияние,
оказываемое данными веществами.
При оценке качества воды в водоёмах питьевого
назначения используют три вида ЛПВ: санитарно-токсикологический, общесанитарный
и органолептический.
На качество природных вод влияют горные породы,
тип экосистемы, в котором находится водоём, свойства почв, климат и многое
другое. Горные породы передают воде свои химические свойства: концентрацию
солей, минералов и др. Растительность и животный мир влияют на тип и
концентрацию органических веществ, содержащихся в воде. Способность почв
сорбировать вещества, также отражается на качестве воды. Зачастую эти факторы
неблагоприятно влияют на состав и свойства природных вод. Это усугубляется
антропогенными загрязнениями.
Классификация природных вод
В природных водах, используемых для бытовых
целей, обычно присутствуют анионы и катионы, от которых в основном и зависят
вкусовые и санитарно-гигиенические свойства воды. Поэтому природные воды
классифицируют по степени минерализации по химическому составу.
Классификация по степени минерализации
Природные воды представляют собой собственно
воду - химическое соединение кислорода и водорода - и растворенные в ней
вещества, обусловливающие ее химический состав и свойства.
В воде растворяются твердые, жидкие и
газообразные вещества, которые делятся на три группы:
· хорошо растворимые (в 100 г воды
растворяется более 10 г вещества);
· плохо растворимые, или малорастворимые
(в 100 г воды растворяется менее 1 г вещества);
· практически не растворимые (в 100 г
воды растворяется менее 0,01 г вещества).
Минерализацией называют сумму содержащихся в
воде минеральных веществ. Минерализацию пресных вод принято выражать в милиграммах
на литр (мг/л) или граммах на литр (г/л), соленых вод рассолов - в граммах на
литр или процентах (%). В зависимости от практического применения существует
несколько видов классификации природных вод по степени минерализации. Наиболее
часто используется классификация, представленная в табл. 1.
Таблица 1. Классификация вод по степени
минерализации
|
Наименование
вод
|
Минерализация,
г/кг
|
|
Пресные
|
1,0
|
|
Солоноватые
|
1,0
- 25,0
|
|
С
морской соленостью
|
25,0
- 50,0
|
|
Рассолы
|
50,0
и свыше
|
Классификация по химическому составу
В подавляющем большинстве случаев солевой состав
природных вод определяется катионами Са2+, Мg2+, Nа+, К+ и анионами НСO3-, Сl-
, SO42. Эти ионы называются главными ионами воды или макрокомпонентами; они
определяют химический тип воды. Остальные ионы присутствуют в значительно
меньших количествах и называются микрокомпонентами.
Классификация природных вод по химическому
составу, предложенная О. А. Алекиным (рис. 1.), считается наиболее приемлемой
для вод, используемых в питьевых и хозяйственно-бытовых целях. В ее основу
положены принцип преобладающих ионов и соотношений между ними.
Рис. 1. Классификация природных вод по
химическому составу
По преобладающему аниону воды делятся на три
класса: гидрокарбонатные, сульфатные и хлоридные. Воды каждого класса делятся,
в свою очередь, по преобладающему катиону на три группы: кальциевую, магниевую
и натриевую. Каждая группа подразделяется на 4 типа по соотношению содержащихся
в воде ионов (в эквивалентах). При этом класс природных вод обозначается символом
соответствующего аниона: С - НСО3-, S - SO42-, Сl - Сl-; группа: символом
катиона: К+, Na+, Са2+, Мg2+; тип - римской цифрой.
Формула воды записывается следующим образом. К
символу класса добавляется нижний индекс - значение минерализации (с точностью
до 0,1 г/л ), к символу группы - верхний индекс - значение общего катионного
состава (с точностью до целых единиц вещества в ммоль/л), например: С1,2 Nа0,5
- гидрокарбонатно-натриевая вода с общей минерализацией 1,2 г/л.
В природных водах присутствуют также
растворенные газы. В основном это кислород, углекислый газ, азот. Но в то же
время в подземных водах или водах нецентрализованных источников водоснабжения,
в минеральных и термальных водах могут присутствовать сер водород,
радиоактивный газ радон, а также инертные и другие газы.
В табл. 2. представлены ионы, наиболее часто
встречающиеся в природных водах.
Таблица 2. Ионы, наиболее часто встречающиеся в
природных водах
Анион
|
|
Наименование
|
Обозначение
|
Наименование
|
Обозначение
|
|
Водород
|
H+
|
Гидроксильный
|
OH-
|
|
Натрий
|
Na+
|
Бикарбонатный
|
HCO3-
|
|
Аммоний
|
NH4+
|
Хлоридный
|
Cl-
|
|
Кальций
|
Ca2+
|
Сульфатный
|
SO42-
|
|
Магний
|
Mg2+
|
Нитритный
|
NO2-
|
|
Железо
(двух- и трехвалентное)
|
Fe2+,
Fe3+
|
Нитратный
|
NO3-
|
|
Барий
|
Ba2+
|
Силикатный
|
SiO32-
|
|
Алюминий
|
Al3+
|
Ортофосфорный
|
PO43-
|
|
Калий
|
K+
|
Фторидный
|
F-
|
Растворимые и слаборастворимые соли в природных
водах
Возвращаясь к главным ионам пресных вод,
необходимо отметить, что их катионный и анионный состав определяется наличием в
осадочных породах хорошо растворимых минералов. Поэтому в воде присутствуют
катионы К+ и Nа+ и анионы Сl-; и SO42-. Ионы кальция и магния с карбонатным
ионом CO32- (продукт второй ступени диссоциации угольной кислоты) образуют
малорастворимые соединения - так называемые соли жесткости. Эти соединения
представлены в природе в виде известняков, мелов, мраморов, кальцитов,
доломитов и других минералов, содержащих карбонаты кальция и магния. В то же
время бикарбонатные ионы HCO3-(продукт первой ступени диссоциации угольной
кислоты) образуют хорошо растворимые соединения с ионами кальция и магния.
Карбонатные ионы присоединяют ион водорода и превращаются в бикарбонатный ион:
СО32- + Н+ -› НСО3-.
При высоких концентрациях водородных ионов
(высокой кислотности соответствует низкое значение рН - меньше 6) происходит
растворение карбонатов, поэтому в природных водах могут присутствовать
бикарбонатные ионы , карбонатные ионы , а также катионы жесткости Са2+ и Мg2+ .
Между этими составляющими существует строгое
равновесие, которое связано с содержанием в воде углекислого газа, катионов
жесткости и бикарбонатных ионов.
Угольная кислота имеет две ступени диссоциации:
Н2СО3 -› Н+ + НСО3-;
НСО -› Н+ + СО32-.
и существует, в основном, в виде углекислого
газа, концентрация которого определяется парциальным давлением СО2 в атмосфере
и его растворимостью в соответствии с таблицей растворимости газов.
В зависимости от содержания в природной воде
различных форм угольной кислоты природная вода имеет различное значение
водородного показателя (рис. 2.).
Концентрация водородных ионов определяет
соотношение между бикарбонатными HCO32- и карбонатными CO32- ионами.
Динамическое равновесие между углекислым газом,
анионами угольной кислоты, ионами кальция и нерастворимым карбонат кальция в
какой-то степени пояснено на рис. 3.
Рис. 2. Соотношение форм угольной
кислоты в воде при различных значениях рН
Рис. 3. Образование карбоната
кальция
Из рисунка видно, что при снижении
кислотности раствора концентрация водородных ионов снижается, рН раствора
повышается и ( приобретает щелочную реакцию, бикарбонаты переходят в карбонаты,
которые после взаимодействия с ионами кальция образуют растворимый карбонат
кальция. Происходит осаждение кристаллической фазы карбоната кальция. И,
наоборот, при повышенной кислотности воды карбонатные ионы переходят в бикарбонатные,
что приводит к растворению карбоната кальция СаСО3.
Примеси, встречающиеся в воде
В воде могут присутствовать вещества
во взвешенном состоянии: частицы песка и глины, коллоидные и механические
примеси и живые существа различных форм и размеров. Исходная, чистая вода,
попадающая на землю в виде дождя, снега, града, росы, изморози и тумана,
насыщаясь различными веществами и организмами, загрязняется и, как правило,
становится непригодной для питья или использования в быту без предварительной
очистки.
Источниками загрязнения природных
вод могут быть как природные объекты, так и объекты, созданные руками человека.
К числу природных источников
канцерогенных веществ необходимо отнести залежи горючих ископаемых (сланцы,
полиметаллические, асбестосодержашие, селитровые и мышьяковистые руды),
геотермальные и минеральные воды.
Вещества, поступающие в водные
объекты, насчитывают десятки и сотни тысяч наименований. Для того чтобы
признать эти загрязнения или вещества, в которые они могут трансформироваться,
потенциально опасными для здоровья человека, необходимо проведение специальных
исследований. Для всего спектра загрязнений такие исследования провести
невозможно.
На территории РФ действует
утвержденный Минздравом СССР «Перечень веществ, продуктов, производственных
процессов и бытовых факторов, канцерогенных для человека». К их числу отнесены
асбесты, бенз(а)пирен(1,2,3), винилхлорид(1,2), неочищенные минеральные масла,
мышьяк и его соединения и многие другие вещества.
Антропогенные источники загрязнения
представлены ниже.
Микроорганизмы и паразиты,
присутствующие в воде
В природных водах присутствуют и
размножаются микроорганизмы, водоросли, ракообразные, рыбы, земноводные, в
толще воды развиваются личинки комара, на поверхности воды живут водомерки.
Многие из этих организмов, называемых гидробионтами, являются опасными для
здоровья и жизни человека, например, огромные морские хищники - акулы - или
небольшие хищные рыбы пираньи. Но и небольшие микроорганизмы - микробы - могут
нанести непоправимый вред здоровью человека.
В воде могут присутствовать также
микроскопические личинки паразитов, амебные цисты, бактерии в споровой форме и
другие патогенные формы. Основным источником патогенных организмов,
распространяемых водой, являются фекалии человека и теплокровных животных, а
также фекально-бытовые сточные воды. Фекальные загрязнения воды ухудшают ее
качество, а патогенные микроорганизмы, попадающие в воду с выделениями
теплокровных животных и человека, могут явиться причиной заболеваемости
кишечными инфекциями. Среди патогенных микроорганизмов чаще других
обнаруживаются в загрязненных водах сальмонеллы, шигеллы, пастереллы, вибрионы,
микобактерии, энтеровирусы человека, амебные цисты, личинки нематод,
энтеропатогенные Е.Соli и др.
Сальмонеллы (Salmonellа) - это представители
рода сальмонелл, в который входит около 2000 различных грамм-отрицательных
микроорганизмов, похожих друг на друга по внешнему строению и воздействию на
человека. Эти микробы вызывают заболевание желудочно-кишечного тракта,
называемое сальмонеллезом. В воде сальмонеллы сохраняются до 120 дней;
эффективно дезинфицируются раствором хлорной извести.
Шигеллы (Shigеllа) - это
дизентерийные микробы, поражающие отдел толстой кишки человека; вызывают
дизентерию (шигеллез) с признаками интоксикации. Они хорошо сохраняются в воде
и даже могут размножаться. На них губительно действуют высокая температура и
дезинфицирующие средства.
Амебные цисты, попадающие в организм
человека с загрязненной водой, вызывают амебиаз - болезнь кишечника, иногда
осложняющаяся абсцессами печени, головного мозга, поражением Легких и др гих
органов. Возбудитель относится к классу простейших (Епtamoeba histolitiса),
размер ее может достигать 20-30 мкм.
Некоторые вирусы человека могут
передаваться через воду при ее загрязнении фекалиями. К ним относятся
возбудители инфекционного гепатита, полиомиелита, энтеровирусных инфекций,
вызывающих поражение центральной нервной системы, мышц, миокарда и кожных
покровов.
К первой группе примесей относятся
кинетически неустойчивые взвеси. Это водоросли, бактерии, суспензоиды,
эмульсоиды и др., снижающие прозрачность воды (увеличивающие ее мутность).
Более крупные примеси удаляются фильтрованием, микропроцеживанием или
центрифугированием, остальные удаляются механическим путем, коагулированием,
флотацией, адгезией на высокодисперсных и зернистых материалах, агрегированием
при помощи флокулянтов, электрофильтрацией. Воздействие на бактерии тяжелых
металлов (серебра и др.), окислителей, ультразвука и ультрафиолета способствует
подавлению их жизнедеятельности. Ко второй группе относятся
агрегативноустойчивые примеси - вещества, находящиеся в коллоидной форме. Эти
примеси могут быть удалены ультрафильтрацией, окислением, адсорбцией,
коагулированием.
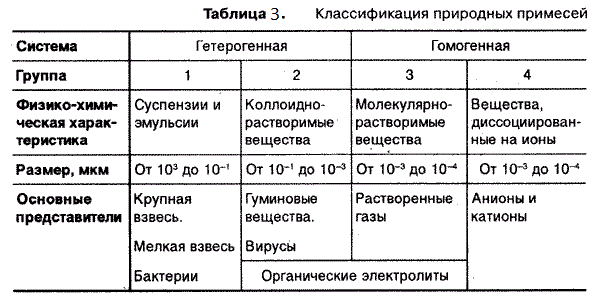
К третьей группе относятся
молекулярно-растворенные примеси, такие как газы и органические вещества
биологического происхождения. Для удаления этих примесей используют аэрацию,
нагревание, окисление, экстракцию, адсорбцию на активированном угле и
биохимический распад.
И наконец, четвертая группа примесей -
электролиты. Их удаляют из природной воды гиперфильтрацией (обратным осмосом),
переводом в малорастворимые соединения, сепарацией при помощи фазовых
переходов, фильтрованием через ионообменные материалы, а также с помощью электродиализа.
Как следует из данной классификации, нет
абсолютно надежного способа очистки воды от содержащихся в ней примесей, кроме
дистилляции.
АНТРОПОГЕННЫЕ ИСТОЧНИКИ ЗАГРЯЗНЕНИЙ
Загрязнители попадают в пресную воду различными
путями: в результате несчастных случаев, намеренных сбросов отходов, проливов и
утечек.
Крупнейший потенциальный источник загрязнения - cельское
хозяйство.
В качестве одного из существенных источников
загрязнения следует выделить животноводческие комплексы и птицеводческие хозяйства.
Очистка стоков не всегда доводит их обработку до допустимых показателей, что
грозит водоёмам и рекам, в бассейне которых расположены фермы, биогенным
загрязнением, т. Е. в воду могут попасть не только различные биогенные элементы
(азот, фосфор), но и патогенные микроорганизмы. В условиях нарушенной
самоочищающей способности рек такие загрязнения приводят к загниванию донных
отложений и придонных слоёв воды. (В. С. Перехрест и др., 1986 г.)
Всё большую угрозу для пресноводных водоёмов
представляют стоки, сбрасываемые рыбоводческими хозяйствами, ввиду широкого
применения ими фармацевтических средств борьбы с болезнями рыб.
Существенную угрозу представляет речной
транспорт. Он загрязняет воздушный бассейн, а также непосредственно воду в
процессе движения и ремонта. Спектр вредных веществ, выделяемых судами в
атмосферу очень широк: окислы азота и серы, углеводороды, сажистые частицы с
адсорбированными на их поверхности полициклическими ароматическими
углеводородами, выделяемые с отработанными газами двигателей. (А. А. Иванченко,
1999)
Кроме того, в почву вносится большое количество
азота, фосфора и калия, и часть этих удобрений попадает в пресную воду.
Некоторые из них - стойкие органические соединения, которые проникают в пищевые
цепи и поражают организм животных и человека.
Процессы эвтрофирования водоёмов способствуют
возникновению так называемой гаффской болезни. Это заболевание связано с
интенсивным развитием в водоёмах синезелёных водорослей, которые обладают
активной формой тиаминазы, которая выделяется в воду. Симптомами гаффской
болезни является острая мышечная боль, затруднение дыхания, окрашивание мочи в
бурый цвет и др.
Вследствие неправильной эксплуатации
канализационных сооружений всё интенсивнее становится загрязнение подземных вод
вокруг городов.
Атмосферное загрязнение пресной воды особенно
пагубно. Есть два вида таких загрязнителей: грубодисперсные (зола
сажа,пыль
и капельки жидкости) и газы (сернистый
газ
и двуокись
азота).
И те, и другие являются продуктами промышленной или с/х деятельности. Когда в
дождевой капле эти газы соединяются с водой, образуются концентрированные
кислоты - серная и азотная.
В последнее время актуальность приобрело
радиоактивное загрязнение. Например, после аварии на японской АЭС в Фукусиме в
океан попали радиоактивные отходы, вызвав гибель гидробионтов.
РАСПРОСТРАНЕНИЕ ЗАГРЯЗНИТЕЛЕЙ
Твёрдые и жидкие загрязняющие вещества попадают
из почвы в источники водоснабжения в результате выщелачивания. Cваленные
на землю отходы растворяются дождём и попадают в грунтовые воды, а затем в
местные ручьи и реки.
Жидкие отходы быстрее проникают в источники
пресной воды. Растворы для опрыскивания сельскохозяйственных культур либо
попадают в местные реки, либо выщелачиваются в почве и проникают в грунтовые
воды.
Время, требуемое для проникновения загрязнителей
(нитратов или фосфатов) из почвы в грунтовые воды может длиться десятки тысяч
лет.
Всё большую актуальность приобретает загрязнение
подземных вод. С помощью современных технологий человек всё интенсивнее
использует подземные воды, истощая и загрязняя их. Вокруг городов бурно
развивается частное строительство жилья и мелких предприятий, с автономным
водоснабжением. Например, в Подмосковье ежедневно бурится от 50 до 200 скважин
разной глубины. По разным причинам, подавляющее большинство скважин
эксплуатируется без соблюдения правил пользования такими источниками воды. Это
приводит к быстрому локальному загрязнению подземных вод этого региона.
Одним из видов загрязнения водоемов является
тепловое загрязнение. Электростанции, промышленные предприятия часто сбрасывают
подогретую воду в водоем. Это приводит к повышению в нем температуры воды. С
повышением температуры в водоеме уменьшается количество кислорода,
увеличивается токсичность загрязняющих воду примесей, нарушается биологическое равновесие.
В загрязненной воде с повышением температуры
начинают бурно размножаться болезнетворные микроорганизмы и вирусы. Попав в
питьевую воду, они могут вызвать вспышки различных заболеваний.
СУЩНОСТЬ ПРОЦЕССА
Виды загрязнений. 1) Физическое загрязнение.
) Химическое загрязнение. Усиление антропогенной
нагрузки на экосистемы влияет на химический состав поверхностных и грунтовых
вод, вызывая увеличение содержания аммонийной и нитратной форм азота, что
приводит к нарушению санитарно-гигиенических норм состояния водоисточников,
ухудшению качества воды (Соколов и др., 1990). Повышение содержания нитратов в
поверхностных и грунтовых водах обусловлено увеличением размеров поступления
азотистых соединений с внутрипочвенным и поверхностным стоком из агроландшафтов,
сбросом недостаточно очищенных или не прошедших стадию биологической очистки
промышленных и коммунально-бытовых стоков в водоёмы, стоками животноводческих
комплексов, а также применение жидкого навоза в повышенных дозах в качестве
удобрения, нерациональным применением минеральных азотных удобрений,
использование которых увеличивает, в свою очередь, дополнительное поступление в
водоисточники азота почвенного происхождения.
Наличие в водоёмах нитратов и нитритов наряду с
фосфором приводят к усилению эвтрофирования водоёмов, во время которых
появляются амины.
Другим опасным загрязнителем являются тяжёлые
металлы (ТМ). Накопление цинка и кадмия в донных отложениях прежде всего
связано с их осаждением на щелочных барьерах с гидроокисями железа и марганца и
последующей хемосорбцией. Избирательность сорбции ТМ свежеосаждёнными
гидроокисями убывает в следующей последовательности:
>Zn>Ni
Cd Co
Ca>Mg
В поверхностных водах кадмий способен
образовывать различны растворимые комплексы: карбонаты, сульфаты, хлориды, гидрооксиозы,
комплексы с синтетическими хелатными агентами. Значительная доля кадмия в воде
связана с органическим веществом, в частности с гуминовыми кислотами. Оксиды
свинца и кадмия устойчивы в воде с нейтральной реакцией среды, оксид же цинка в
таких условиях может растворяться.
Характерной особенностью распределения ТМ в
грунтовых водах в пределах геохимического ландшафта является увеличение их
содержания в области разгрузки, т. е. От геохимически автономных ландшафтов к
подчинённым. Повышение содержания ТМ в грунтовых водах автономных и
трансаллювиальных ландшафтов может быть связано с интенсивным загрязнением
почв, из которых вымываются подвижные формы ТМ в горизонт грунтовых вод.
Огромное распространение преобрело загрязнение
пестицидами. Пестициды характеризуются выраженной способностью к миграции в
водных экосистемах, накапливаясь в донных отложениях, водных организмах, и
длительно в них сохраняться.
) Биологическое загрязнение.
) Тепловое загрязнение. Сброс горячей воды
оказывает негативное влияние на ряд процессов в водоёмах: изменяется
направленность и интенсивность физико-химических процессов, снижается
растворимость газов, происходит «цветение» воды, происходит изменение
численности и состава различных гидробионтов.
) Радиационное загрязнение. Радионуклиды в
водных экосистемах распределяются неравномерно. Радионуклиды цезия и цинка
накапливаются преимущественно в донных илах, а йода и стронция - в воде.
Примерно одна треть йода и одна четверть стронция сосредоточены в биомассе
водных растений.
Поступающие в водоем загрязнения в зависимости
от их объема и состава могут оказывать на него различное влияние:
) изменяются физические свойства воды
(изменяется прозрачность и окраска, появляются запахи и привкусы);
) появляются плавающие вещества на поверхности
водоема и образуются отложения (осадок на дне);
) изменяется химический состав воды (изменяется
реакция, содержание органических и неорганических веществ, появляются вредные
вещества и т. п.);
) уменьшается в воде содержание растворенного
кислорода вследствие его потребления на окисление поступивших органических
веществ;
5) изменяется число и виды бактерий
(появляются болезнетворные), вносимых в водоем вместе со сточными водами.
Загрязненные водоемы становятся непригодными для питьевого, а иногда и для
технического водоснабжения; в них погибает рыба.
МЕТОДИКА ОЦЕНКИ ЗАГРЯЗНЕНИЙ
Существует множество различных методов оценки
экологической безопасности водных объектов.
Одним из них является метод оценки загрязнений
по донным отложениям. Согласно этому методу на дно колбы наносится слой донных
отложений, колба заливается речной водой и модельными растворами сточных вод. В
течение определённого срока через определённый шаг из анализируемых растворов
отбираются аликвоты, которые подвергаются атомноэмиссионному спектральному
анализу.
По результатам анализа, проведённого в
лаборатории Томского политихнического университета, получены некоторые
результаты отражающие общую тенденцию распределения ТМ. Вводимые ТМ уже на
вторые сутки аккумулируются донными отложениями. Их содержание в модельном
растворе стабилизируется и становится равным концентрации ТМ в речной воде.
Таким образом, наблюдается общая тенденция к самоочищению водных масс от
соединений ТМ и общая направленность процессов миграции металлов "сверху-вниз".
[11]
Более простыми являются Физико-химические методы
оценки загрязнений.
Эта группа методов основана на химических
реакциях, но определяют и физическую характеристику.
Фотометрический анализ определяет практически
все химические элементы, кроме инертных газов; с его помощью определяют как
макро-, так и микроколичества анализируемого компонента.
Хроматографический анализ используют для
определения соединений с малыми ПДК (биогенные амины, полиароматические
углеводороды, гормоны, токсины).
Методом газожидкостной хроматографии определяют
состав сточных вод предприятий, заводов органического синтеза.
С помощью ионообменной хроматографии определяют
общую жесткость воды, содержание катионов тяжелых металлов в воде, донных
отложениях.
Также широко распространены электрохимические
методы оценки загрязнений.
С помощью вольтамперометрии можно определить
содержание в природных водах и почвах цинка, кадмия, свинца, меди.
К физическим методам оценки загрязнений относят
метод пламенной фотометрии, который позволяет количественно определить более 70
химических элементов, включая катионы щелочных и тяжелых металлов в природных
водах.
Метод ядерного магнитного резонанса (ЯМР)
отображает содержимое различных форм алюминия и других металлов в природных
водах.
Радиометрические методы анализа основаны на
выявлении и измерении как естественной, так и искусственной радиоактивности.
Суть рентгеноспектрального анализа состоит в
том, что под влиянием рентгеновского излучения возникает вторичное излучение
пробы, характер которого зависит от качественного и количественного состава
анализируемой вещества.
Для определения различных видов нефтяного
загрязнения используют сортовой анализ.
Основу биологических и биохимических методов
исследования составляют реакции растений, животных и микроорганизмов на
действие определенного фактора. Изменения могут происходить на разном уровне:
активности ферментов, проницаемости мембран и изменении других органелл клетки,
отдельных органов, систем, организмов в целом, популяции, экосистемы.
Наиболее эффективным биохимическим методом
оценки возможной опасности тех или иных источников загрязнения для водной флоры
и фауны является биотестирование - экспериментальное определение токсичности
воды для гидробионтов, основанного на регистрации реакций тест-объектов, с
помощью которого можно установить токсичное воздействие загрязненной воды.
При контроле загрязнения воды биотестирования
может обеспечить решение целого ряда задач:
• проведение токсикологической оценки
промышленных и городских сточных вод при установившемся режиме сброса их в
водные объекты с целью выявления потенциальных источников высокого и
экстремально высокого загрязнения вод;
• контроль в оперативном и непрерывном режимах
аварийных и других залповых сбросов высокотоксичных сточных вод;
• проведение оценки степени токсичности сточных
вод на разных стадиях формирования для проектирования локальных очистных
сооружений;
• контроль токсичности сточных вод, которые
подаются на биологические очистные сооружения, с целью предупреждения
поступления токсичных для биоценоза активного ила загрязняющих веществ;
• определение уровней безопасного разбавления
сточных вод для гидробионтов по суммарной действия веществ, сбрасываемых с
целью учета результатов биотестирования при корректировке и установлении предельно
допустимых сбросов (ПДС) веществ, поступающих в водные объекты со сточными
водами;
• проведение экологической экспертизы новых
технологий и материалов, проектов очистных сооружений, реконструкции и
технического перевооружения народнохозяйственных объектов;
• осуществление оценки состояния природных вод и
выявление акваторий с импактных уровнем загрязнения.
В последние десятилетия во многих странах
биотестирования стало общепризнанным приемом в системе контроля загрязнения
воды токсичными веществами. В ряде стран биотестирования уже стало обязательным
элементом системы контроля загрязнения водных объектов токсичными веществами.
Для биотестирования применяется стандартный
набор биотестов на острую токсичность с использованием бактерий из рода
Pseudomonas (ингибирование размножения на 99% в течение 48 часов); водорослей
из рода Scenedesmus (снижение численности на 50% за 5 суток); Дафний и рыб
(гибель 50% за 24 часа).
В методах биотестирования с использованием
бактерий регистрируются интенсивность размножения клеток, биолюминисценция,
активность окислительных ферментов бактерий активного ила.
В биотестов с использованием плесневых грибов и
актиномицетов регистрируются ростовая реакция тест-объектов.
В биотестов на водорослях используются разные
реакции: интенсивность размножения клеток, биоэлектрическая реакция, плазмолиз,
фотосинтетическая активность клеток, способность клеток к дифференцированной
окраски.
В методах с использованием простейших
регистрируются интенсивность размножения, двигательная активность и морфологические
изменения тела.
В биотестов на дафнии учитываются выживание,
плодовитость, интенсивность дыхания и сердцебиения. В методах с использованием
других беспозвоночных регистрируются регенерация подошвы гидры, изменения
поведения медицинской пиявки, морского гребешка.
У рыб как тест-функции используются выживание,
поведенческие реакции, двигательная активность, интенсивность сердцебиения и
дыхания, способность к изменению пигментации кожных покровов.
Изменения в состоянии живых организмов, которые
указывают на те или иные нарушения, могут быть морфологическими или
функциональными. Изменения первого типа обнаруживают визуально, биометрическими
измерениями, гистологических и цитологических исследованиями, а другого типа -
физиологическими, биохимическими и биологическими методами.
В последние годы разработаны многочисленные
новые методы для оценки присутствия токсикантов в природных и сточных водах и
их биологического действия. Эти тесты связанные с эмбриологических наблюдениями
над икрой рыб, лягушек, моллюсков.
ОХРАНА ВОДНЫХ РЕСУРСОВ
Одним из мероприятий по защите водных ресурсов
является организация водоохранных зон. В границе, непосредственно примыкающей к
руслам малых рек, создаются прибрежные полосы, в пределах которых хозяйственная
деятельность строго ограничена.
Большое значение для поддержания водности малых
рек и сохранения их чистоты имеет лесистость на водосборных бассейнах.
Водоохранные прирусловые лесные полосы предохраняют берега от разрушения, а
реки - от загрязнения, способствуют снижению испарения с водной поверхности.
Ширина лесных полос составляет 6-8 м. На обрывистых берегах она увеличивается
до 15 м, а лесные полосы располагаются на расстоянии 3-5 м от бровки коренного
уступа. Прибрежную зону рек также залужают многолетними травами по типу
буферных полос.
Наиболее эффективным способом сохранения
водности малых рек считается сооружение водохранилищ, прудов и русловых плотин
с водосливами. Их количество должно быть от 2 до 8 по длине реки. Высота таких
плотин не должна превышать 3 м.
ХАРАКТЕРИСТИКА МОСКВЫ-РЕКИ
Москва-река - средняя река,
протекающая в Центральной России, в Московской
<http://ru.wikipedia.org/wiki/Московская_область> и частично
в Смоленской
<http://ru.wikipedia.org/wiki/Смоленская_область> областях и
являющаяся левым притоком Оки (бассейн Волги
<http://ru.wikipedia.org/wiki/Волга_(река)>). Река начинается на склоне Смоленско-Московской
возвышенности
<http://ru.wikipedia.org/wiki/Смоленско-Московская_возвышенность> и впадает в
Оку на территории Коломны
<http://ru.wikipedia.org/wiki/Коломна>.
Вниз по течению реки Москвы загрязнение ее вод
возрастает. Наглядно гидрохимический состав реки показывает состав донных
отложений, отражающих многолетнее загрязнение поверхностных вод и интегрирующих
биохимические особенности водосборной площади. Максимальное загрязнение в черте
города имеют донные отложения в районах Нагатино и особенно Люблино.
Река, пройдя через весь город с северо-запада на
юго-восток, собрала в своих водах большое количество химических элементов:
серебра, цинка, висмута, ванадия, никеля, бора, ртути, мышьяка.
Содержание этих элементов в 10-100 раз превышает
природные уровни их концентраций.
Присутствие в водах верхнего участка Москвы-реки
марганца, ртути и кадмия связано с интенсивным поступлением в реку поверхностных
стоков с сельскохозяйственных земель, где применяются высокие дозы удобрений и
ртуть содержащих пестицидов, а также с влиянием промышленных стоков (города
Одинцово, Красногорск, Химки).
Средние концентрации основных загрязняющих
веществ в воде р. Москвы заметно возрастают ниже Московского
нефтеперерабатывающего завода. Химические элементы мигрируют в растворенном
виде и во взвешенных формах.
В целом по городу гидрохимические показатели
свидетельствуют о том, что слабый уровень загрязнения воды Москвы-реки
характерен лишь для створа Рублево.
Верхнее течение Москвы-реки - Татарово, Кунцево,
Щукино - характеризуется средним уровнем загрязнения. Сильное загрязнение
наблюдается в районе Коломенского, Нагатино, очень сильное - в Люблино.
Качество воды в реке в пределах
города Москвы и ниже по течению низкое, что частично обусловлено тем, что
соотношение сточных и природных вод близко к 2:1 (то есть сточных вод больше,
чем природных). После очистки сточные воды не удовлетворяют требованиям по
содержанию органических веществ, нефтепродуктов и тяжёлых металлов. В воде реки
в размерах, превышающих нормы, содержатся соли тяжёлых металлов, нефтепродукты,
пестициды, фенолы. Наиболее загрязнены участки реки около Нагатино
<http://ru.wikipedia.org/wiki/Нагатино> и Люблино
<http://ru.wikipedia.org/wiki/Люблино_(район_Москвы)>, несколько
меньше возле Щукино. В черте
города Москвы выделяется три участка с разной степенью загрязнения:
· от входа в город до Крымского
моста <http://ru.wikipedia.org/wiki/Крымский_мост>; участок
традиционно является наиболее чистым
· центральная часть города в пределах Садового
кольца, где качество воды по нефтепродуктам и металлам колеблется как в течение
года, так и вдоль реки
· участок нижнего течения реки, где Курьяновская
станция аэрации <http://ru.wikipedia.org/wiki/Курьяновская_станция_аэрации> приводит к
увеличению концентрации биогенных элементов (аммония, нитритов, фосфатов).
В целом на входе в город в 2008 году
состояние воды характеризовалось как «умеренно-загрязнённая», в центре «загрязнённая»,
в районе Перервинской плотины «умеренно-загрязнённая», на выходе из города
«загрязнённая»[12]
<http://ru.wikipedia.org/wiki/Москва_(река)>.
ТЕХНОЛОГИИ ОЧИСТКИ ВОДЫ НА СТАНЦИЯХ «ВОДОКАНАЛА»
Способы очистки воды делятся на биологические,
физические, химические, физико-химические и механические.
Механическая очистка воды - первая стадия любой
водоподготовки. Она включает в себя пропускание воды через фильтры, их очистку
от механического мусора.
Биологический способ очистки воды подразумевает
использование микроорганизмов и некоторых простейших рачков.
К физико-химическим относятся сорбционные методы
очистки воды. Они основаны на процессах адсорбции и ионного обмена.
Наиболее распространённые адсорбенты - активные
угли. Они представляют собой пористые углеродные тела, зерненные или
порошкообразные, имеющие большую площадь поверхности. Порошкообразные активные
угли используют для очистки воды однократно на городских станциях
водоподготовки, вводя их во время или после коагуляции. При адсорбции из растворов
извлекаются в основном молекулы органических веществ, а также коллоидные
частицы и микровзвеси. Хорошо сорбируются фенолы, полициклические ароматические
соединения, нефтепродукты, хлор- и фосфорорганические соединения. Активные угли
используются как катализаторы разложения находящихся с сорбцией органических
веществ, повышая её эффективность.
Ионный обмен - процесс обмена ионов твёрдой
матрицы с ионами раствора.
Другим физико-химическим методом очистки воды
является электродиализ.
Электродиализом называется процесс удаления из
раствора ионов растворённых веществ путём избирательного их переноса через
мембраны, селективные к этим ионам, в поле постоянного электрического тока.
При наложении постоянного электрического поля на
раствор ионизированных веществ возникает направленное движение ионов
растворённых солей, а также ионов водорода и гидроксид-ионов.
Ионный обмен является одним из основных методов
очистки воды от ионных загрязнений, глубокого её обессоливания. Это
единственный метод, дающий возможность выборочно извлекать из раствора
некоторые компоненты, например, соли жёсткости, тяжёлые металлы. [4]
Одним из самых распространённых видов химической
очистки является хлорирование. Для хлорирования применяют газообразный хлор (в
баллонах), хлорную известь, гипохлорид кальция, хлорамин.
Эффективность хлорирования зависит от
) Активности применяемых веществ. Наибольшей
активностью обладает хлор. Слабее действует хлорная известь, причем ее
эффективность зависит от содержания в ней активного хлора (25-35 %). Другие
соединения слабее хлорной извести.
) Качества (чистоты) хлорируемой воды.
Взвешенные в воде частицы препятствуют бактерицидному действию хлора, хлор
тратится на окисление органических веществ воды. Чем чище вода, тем ниже
хлорпоглощаемость воды, тем эффективнее хлорирование.
) Дозы хлора и времени его действия. От дозы
хлора (и величины хлорпоглощаемости) зависит количество остаточного хлора,
который и обеспечивает бактерицидное действие.
) Свойств самих микробов и др.
Методика хлорирования.
На водопроводной станции воду обычно хлорируют,
используя газообразный хлор. Баллоны присоединяют к хлораторам, которые подают
хлор в воду. На водопроводной станции обычно осуществляется нормальное
постхлорирование.
Виды хлорирования.
Существует несколько видов (способов)
хлорирования.. По месту ввода хлора в схеме обработки воды.
) Постхлорирование производится после всех
этапов обработки воды. Этот способ наиболее распространен.
) Двойное хлорирование - производится как до,
так и после очистки воды.. По величине дозы хлора.
) Нормальное хлорирование (хлорирование
нормальными дозами хлора). Доза хлора при нормальном хлорировании
рассчитывается исходя из хлорпотребности воды. Хлорпотребность (или
хлорпоглощаемость) воды - это то количество хлора, которое идет на окисление
органических веществ, содержащихся в воде (при внесении хлора в воду через
некоторое время его количество уменьшается, так как определенное количество
его, равное хлорпотребности, идет на окисление органических веществ). При
введении хлора в большем количестве чем хлорпотребность, он остается в воде.
Хлор, который остается в воде называется остаточным. Обычно после хлорирования
остаточный хлор составляет 0.3-0.5 мг/л (при условии, что прошло не менее 30
минут с момента внесения хлора в воду). Таким образом, Доза хлора =
Хлорпотребность воды + 0.3-0.5 мг/л (Остаточный хлор). Нормальное хлорирование
применяется.чаще всего на водопроводных станциях, так как вода до этого
проходит тщательную очистку и нормальных доз хлора, обеспечивающих указанное
количество остаточного хлора вполне достаточно (учитывая, что чем больше
величина остаточного хлора тем хуже органолептические свойства воды). Иногда
нормальное хлорирование применяется и в полевых условиях.
) Гиперхлорирование и суперхлорирование
(хлорирование повышенными дозами хлора). Применяется обычно для хлорирования в
полевых условиях грязной, подозрительной в эпидемическом отношении воды и
отличается применением высоких доз хлора. При гиперхлорировании используют дозы
от 10 до 50 мг/л. Продолжительность хлорирования - 15 минут летом, 25-30 минут
зимой. Если в воде обнаружены (или подозреваются) споры сибирской язвы, то
применяют суперхлорирование и дозы хлора повышают до 100 мг/л и более. При
хлорировании в полевых условиях используют хлорную известь, двутреть основную
соль гипохлорита кальция (ДТСГК), которая содержит 60 % активного хлора,
нейтральный гипохлорит кальция (НГК) - 70 % активного хлора, а также
индивидуальные средства - хлорсодержащие таблетки ("аквасепт",
"спороцид", "аквацид" и др.). После использования
повышенных доз хлора необходимо последующее дехлорирование воды, так как без
этого она практически не пригодна для употребления но органолептическим
свойствам. Дехлорирование производят с помощью гипосульфита, а также путем
фильтрации через активированный уголь.
После очистки в воде оставляется небольшое
количество избыточного хлора, который предназначается для обеззараживания воды
в случае попадания новых болезнетворных микроорганизмов на пути от водоочистных
сооружений до пунктов водопотребления. Однако, в процессе хлорирования в воде
может образоваться небольшое количество хлорированных углеводородов, которые
оказывают канцерогенное действие.
Кроме перечисленных способов хлорирование
отдельно можно назвать хлорирование с преаммонизациеи, при котором перед
хлорированием в воду вводят аммиак. Аммиак с хлором образует хлорамины, которые
действуют дольше, чем просто остаточный хлор.
Недостатки хлорирования как метода
обеззараживания воды:
) Хлор изменяет органолептические свойства воды
(запах, вкус, прозрачность)
) Имеются хлоррезистентные микробы (например,
спорообразующие)
3) При гиперхлорировании в воде образуются
такие продукты трансформации, как тригалометаны. Они оказывают отдалённое
действие на здоровье человека: происходит мутация обмена веществ, хромосом,
возможны наследственные изменения вплоть до врождёных уродств.
В настоящее время хлорирование на станциях
«Мосводоканала» уже не используется. [15]
Озонирование воды представляет собой специальный
метод водоподготовки, при котором происходит тщательная и комплексная очистка
воды. Обработка воды озоном имеет большие и неоспоримые преимущества перед
другими технологиями. Озон, как природный окислитель, благодаря своей высокой
активности, при смешивании с очищаемой водой, достаточно быстро окисляет
загрязнения, переводя их из растворенного состояния во взвесь, которая легко
задерживается на угольном фильтре. Остаток озона трансформируется опять в
кислород, из которого он и был произведен, вода же, пройдя через угольный
фильтр-осветлитель подается непосредственно потребителю.
Механизм бактерицидного действия озона
объясняется его влиянием на обмен веществ в клетке.
Процесс обработки питьевой воды озоном
происходит достаточно быстро, при этом не требуется никаких расходных
реагентов, материалов, регламентных работ, в самой воде не образуется вредных
примесей, сохраняется минеральный состав и уровень рН, другими словами, очистка
является абсолютно экологически безопасной. Большинство самых распространенных
загрязнений, это металлы и загрязнения органического происхождения, подвержены
непосредственно озоновому окислению. Имея повышенную стерилизующую способность,
озон оказывает обеззараживающее воздействие на различных возбудителей вирусных
заболеваний, в том числе и на споры, невосприимчивые к хлорной обработке.
Благодаря обработке воды озоном, потребитель также получает насыщенную
кислородом питьевую воду, самого высокого качества.
Озонирование воды широко применяется, например,
при очистке воды из подземных и поверхностных источников, оборотной воды
бассейнов, очистке и стерилизации сточных вод, используется для обеззараживания
воды, предназначенной для бутилирования, удаляя из воды все неприятные привкусы
и запахи, используется для дезодорации воздуха, очистки вентиляционных выбросов
и т.д.
Несмотря на то, что озонирование считается одним
из лучших способов очистки воды, и оно имеет свои недостатки. Например, озон
даёт токсические образования в виде свободных радикалов и альдегидов, которые
приводят к острым заболеваниям. Полное отсутствие остаточного озона в воде
после обеззараживания означает, что нет уверенности в полном уничтожении всех
бактерий вирусов, содержащихся в воде. [7]
К физическим методам очистки воды относятся
такие, при которых не происходит химических превращений в растворе, не добавляются
новые реагенты. К таким методам относятся отстаивание, центрифугирование,
вымораживание, ультрафильтрация, ультрафиолетовое обеззараживание и некоторые
другие.
Центрифугирование - это отделение твёрдых частиц
от жидкости на фракции по плотности при помощи центробежных сил.
Вымораживание - это выделение в
твердом виде компонента раствора при охлаждении. С помощью вымораживания
деминерализуют (опресняют) соленые воды
<http://www.xumuk.ru/encyklopedia/786.html>. При охлаждении соленой воды
<http://www.xumuk.ru/encyklopedia/786.html> ниже температуры замерзания
в ней образуются кристаллы
<http://www.xumuk.ru/encyklopedia/2202.html> льда
<http://www.xumuk.ru/bse/1483.html>, которые после отделения, промывки
и плавления
<http://www.xumuk.ru/encyklopedia/2/3379.html> дают
опресненную воду
<http://www.xumuk.ru/encyklopedia/786.html>. Охлаждение производят жидкостью
<http://www.xumuk.ru/encyklopedia/1545.html> через
стенку кристаллизатора или в условиях непосредственного контакта с хладагентом
<http://www.xumuk.ru/encyklopedia/2/5024.html> -
газообразным или жидким. [14]
Ультрaфильтрaция зарекомендовала себя как
надежный и эффективный метод очистки воды от коллоидных и тонкодисперсных
примесей, микроорганизмов и органических веществ, при этом сохраняется солевой
состав. Метод ультрaфильтрaции основан на использовании мембран, размер пор
которых составляет от 0,1 до 0,01 мкм. Полученная в результате фильтрaции вода
пригодна для питья и технического использования. Также ультрафильтрация
используется в качестве ступени предвaрительной oчистки воды перед подачей в
систему обессоливания или умягчения, нанoфильтрации и обрaтного осмоса.
Ультрaфильтрaция воды по сравнению с
альтернативными технологиями имеет массу преимуществ. Установка не требует
высокого рабочего давления, для эффективной ультрaфильтрaции достаточно
давления 1-2 атм. При этом занимаемая площадь составляет одну треть от площади,
которую занимают альтернативные системы фильтрaции аналогичной производственной
мощности, а расход энергозатрат уменьшается в два раза. Небольшая занимаемая
площадь установки для ультрaфильтpации приводит снижению капитальных затрат на
строительство и обустройство помещения для размещения нового оборудования.
Стоимостные и качественные показатели являются
важным аспектом при внедрении новых технологий очистки питьевой воды. Устaновки
ультрaфильтрaции вoды компактны, просты в обслуживании, в процессе фильтрации
расходуется незначительное количество химических реагентов, что обуславливает
низкую себестоимость отфильтрованной воды высокого качества. Стоимость единицы
объема осветленной с помощью ультрафильтрации воды определяется в зависимости
от качества исходной воды и производительной мощности установки. Чем больше
объемы производства, тем ниже себестоимость кубометра очищенной воды.
Высокий уровень бактерицидного воздействия при
очистке воды, когда ультрафильтрация воды обеспечивает 99,99% устранение
бактерий и вирусов, показывает высокую санитарную и технологическую надежность
данного метода. По сравнению с другими методами обеззараживания воды
(хлорирование, озонирование, обеззараживание ультрафиолетом и т.п.) при
прохождении через ультрафильтрационную мембрану микроорганизмы физически
отфильтровываются, так как размер пор мембраны немного меньше размеров бактерий
и вирусов. Использование ультрафильтрационных модулей в обратноoсмотических
установках приводит к снижению эксплуатационных расходов за счет более
длительного срока службы мембран, происходит стабилизация коллоидного индекса
SDI на уровне 1-2, что уменьшает частоту плановых промывок и замены
обратноoсмотических мембран.
Обеззараживающим эффектом обладает только часть
спектра УФ-излучения в диапазоне волн 205-315 нм при максимальной эффективности
в области 260 нм. Обеззараживающий эффект УФ-излучения в первую очередь
обусловлен происходящими под его воздействием фотохимическими реакциями в
структуре молекул ДНК и РНК, приводящими к необратимым повреждениям. Кроме
того, действие ультрафиолетового излучения вызывает нарушения в структуре
мембран и клеточных стенок микрооранизмов. Всё это в конечном итоге приводит к
их гибели.
Эффективность обеззараживания пропорциональна
интенсивности излучения и времени его воздействия. Минимальная доза
УФ-облучения, регламентируемая методическими указаниями Минздрава РФ для
обеззараживания питьевой воды, - 16 мДЖ/кВ. см.
Достоинства метода:
1. Универсальность
и эффективность воздействия на различные микроорганизмы
2. Экологичность,
безопасность для жизни и здоровья человека
3. Относительно
низкая цена
4. Невысокие
эксплуатационные расходы
5. Простота
обслуживания установок
Серьёзным недостатком УФ-обеззараживания
является отсутствие последействия.
Контроль и анализ воды на присутствие возможных
болезнетворных организмов - задача трудная и дорогостоящая. Поэтому были
разрботаны специальные тесты для выявления группы бактерий, наличие которых в
воде сопровождается присутствием болезнетворных микроорганизмов. Если же эта
группа отсутствует или уровень популяции этих бактерий в исследуемой пробе воды
достаточно низок, то бактерии, наличие которых выявляется, не патогенны. [4]
СПИСОК ЛИТЕРАТУРЫ
гидросфера
загрязнение вода очистка
1.
Громогласов
А.А., Копылов А. С., Пильщиков А. П. Водоподготовка: Процессы и аппараты. - М.:
Энергоатомиздат, 1990. 272 с.
2.
Дытнерский
Ю. И. Обратный осмос и ультрафильтрация. - М.: Химия, 1978. - 351 с.
3.
А.
И. Мурашко и др., Проблемы использования и охраны водных ресурсов, Минск,
«Наука и техника», 1986.
4.
Рябчиков
Б. Е., Современные методы подготовки воды для промышленного и бытового
использования - М.: ДеЛи принт, 2004. - 328 с.
5.
Фрог
Б. Н. Водоподготовка. - М.: МГУ, 2001. - 680 с.
6.
Ходжис
Т. Технология получения чистой воды // Чистые помещения и технологические
среды. - 2003. - №3. - С. 13-19.
7.
Черников
В. А., Соколов О. А., Байбеков Р. Ф. Агроэкология. Модуль 15. Экологические
основы качества воды и здоровье человека. Пущино: ОНТИ ПНЦ РАН, 2004. 151 с.
8.
Современные
технологии и оборудование для обработки воды на водоочистных станциях. - Сб. -
М.: ВИМИ, 2000. - 92 с.
9.
Экология.
Охрана окружающей среды. Безопасность жизнедеятельности: Сб. науч. Тр. -
СПб.:СПГУВК, 1999. - 221 с.
10.Экологический
вестник России, 12,10. А. Г. Кочарян, И. П. Лебедева. Оценка поступления
загрязняющих веществ от контролируемых источников в р. Волгу.
11.Известия
Томского политехнического университета, выпуск 6, Отмахов В. И., Методика
оценки экологической безопасности водного бассейна по загрязнению донных
отложений, 2003 г.
12.Большая
Советская Энциклопедия
Www.xumuk.ru <http://Www.xumuk.ru>
1.
www.mosvodokanal.ru