Синтез и свойства 2,5-замещенных 1,3,4-оксадиазолов
МИНОБРНАУКИ
РОССИИ
Федеральное
государственное бюджетное образовательное учреждение высшего профессионального
образования
«Чувашский
государственный университет имени И.Н. Ульянова»
Факультет
химико-фармацевтический
КУРСОВАЯ
РАБОТА НА ТЕМУ:
«СИНТЕЗ И
СВОЙСТВА 2,5-ЗАМЕЩЕННЫХ 1,3,4-ОКСАДИАЗОЛОВ»
Выполнила: студентка гр. Х-11-10
Тимофеева Ирина
Проверили: доцент Осипова М.П.
доцент Васильева Т.В.
Чебоксары
2013
Содержание
Введение
. Литературный обзор
. Обсуждение результатов
. Экспериментальная часть
Выводы
Литература
Введение
Одним из наиболее важных и перспективных
направлений использования фосфорорганических соединений является применение их
в качестве пестицидов. Среди таких соединений значительное место занимают те, в
строении которых содержатся гетероциклические радикалы. К таким соединениям
следует отнести производные фосфорной, тиофосфорной кислот с гетероциклическими
радикалами (пиримидиновым, пиридиновым, урациловым и др.).
Известно также, что многие 2-амино-5-алкил
(арил)-1,3,4-оксадиазолы проявляют биологическую активность. Их применяют для
лечения артрита, воспалений кишечника, астмы и других болезней. Другие
производные 1,3,4-оксадиазолов применяются при приготовлении лекарственных
препаратов. Реакцией сульфохлоридов по аминогруппе 1,3,4-оксадиазола
синтезированы сульфамидные препараты, которые далее используются для получения
лекарств.
Некоторые производные 1,3,4-оксадиазола являются
термически стойкими, поэтому их применяют для приготовления фотопленок с
повышенной термической стабильностью. Привлекают внимание сцинтилляционные
свойства 1,3,4-оксадиазола и его производных[2].
В данной курсовой работе рассмотрены физические
и химические свойства 1,3,4-оксадиазолов, способы их получения, а также
производные 1,3,4-оксадиазолов.
С целью синтеза биологически активных соединений
изучить реакции взаимодействия 2-амино-5-алкил(арил)-1,3,4-оксадиазолов с
хлорангидридами кислот фосфора.
1. Литературный обзор
Синтез
2-амино-1,3,4-оксадиазолов
Природные вещества, содержащие оксадиазольные
кольца, неизвестны. Поэтому все известные 1,3,4-оксадиазолы синтезированы в
лабораториях.
В литературе под их правильным названием
2-амино-1,3,4-оксадиазолы впервые были описаны в 1929 году Штолле и Ференбахом,
хотя изучались они и ранее. Еще в 1916 году при окислении иодом некоторых
семикарбазонов α-кетокислот
Бойголт получил 2-амино-1,3,4-оксадиазолы, которые он ошибочно рассматривал как
ацилсемикарбазиды. В своих поздних работах с Поповиком он пришел к
предположению, что этим соединениям присуща структура гидрокситриазола. Гирард
провел реакцию «гидрокситриазолов» Бойголта и Поповика с щелочью и получил при
этом соединение, которое он идентифицировал как
5-замещенный-3-гидрокси-1,2,4-триазол. При этом он представил соединение
Бойголта как триазолоны, а их реакции-как таутомеризацию. Наконец в 1929 году
появилось сообщение Штолле и Ференбаха о 2-амино-1,3,4-оксадиазолах, где были
также описаны их производные с заместителями в пятом положении. Одновременно
был найден новый метод получения замещенных в пятом положении
2-амино-1,3,4-оксадиазолов путем циклизации 1-ацилтиосемикарбазидов, который
более подробно был разработан позднее Хоггартом. В последнее время появились
сообщения о новых аминооксадиазолов и методах их получения.
Циклодегидратация дибензилгидразина при
250-300°С приводит к 2,5-дифенил-1,3,4-оксадиазолу. Аналогичным образом при
пиролизе N-ацетамидо-N-фенилуретана
(при перегонке) происходит отщепление этанола и образуется
2-метил-4,5-дигидро-4-фенил-5-кето-1,3,4-оксадиазол. Диацилгидразиды, по-видимому,являются
промежуточными соединениями как при образовании этих продуктов из
бензоилгидразида, так и при взаимодействии N-фенил-N-аминоуретана
с ацетамидом. [3]
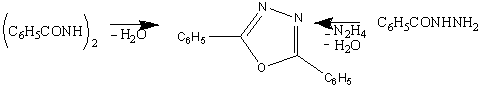
Образованию 1,3,4-оксадиазольного кольца способствуют
следующие дегидратирующие агенты: хлорсульфоновая кислота, хлористый сульфурил,
пятиокись фосфора, n-толуолсульфокислота,
ее хлорангидрид, хлористый тионил, хлорокись фосфора, хлорид цинка, ангидриды
кислот, пятихлористый фосфор, серная кислота.
Синтез 2-арил-1,3,4-оксадиазолов осуществляется
взаимодействием гидразидов карбоновых кислот с избытком ортомуравьиного эфира
по схеме:
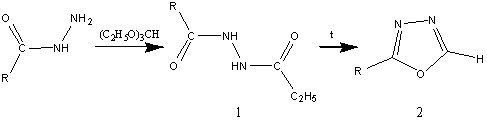
Реакция протекает при температуре кипения
ортомуравьиного эфира; продолжительность нагревания может быть ограничена
моментом полного растворения гидразида в ортоэфире, для чего обычно требуется
несколько часов. Количество ортоэфира может быть снижено до трех молей на один
моль гидразида. Если реакцию проводить при более низкой температуре, то
образуется с количественным выходом продукт (1), который при дальнейшем
нагревании превращается в соответствующий (2). Метод может быть общим только
при инертности функциональных заместителей в исходных гидразидах по отношению к
ортоэфиру.
В некоторых случаях можно получать производные
2-арил-1,3,4-оксадиазола преобразованием функциональных групп в уже готовом
оксадиазоле. Например, 2-(4-аминофенил)-1,3,4-оксадиазол был получен
восстановлением нитрофенилоксадиазола фенилгидразином. Восстановление агентами,
действующими в кислых или щелочных средах, не применимо вследствие легкой
гидролизуемости в таких условиях образующегося оксадиазола.[3]
-Амино-1,3,4-оксадиазол получают отщеплением
сероводорода из тиосемикарбазида при помощи окиси свинца в этаноле:
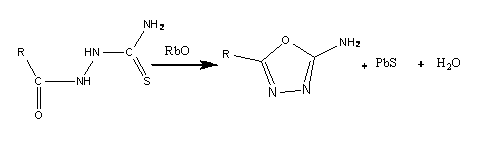
Наряду с 2-амино-1,3,4-оксадиазолом образуется в
значительном количестве 3-меркапто-1,2,4-триазол.[1]
ПОЛУЧЕНИЕ СИММЕТРИЧНЫХ 2,5-ПРОИЗВОДНЫХ
1,3,4-ОКСАДИАЗОЛА
2,5-Диалкил-1,3,4-оксадиазолы
Симметричные 2,5-диалкил-1,3,4-оксадиазолы
получают по схеме:
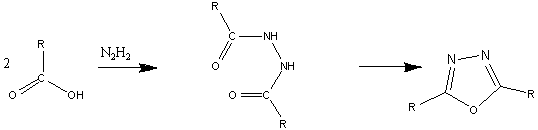
где R=алкил.
Алифатические кислоты легко реагируют с
гидразингидратом при комнатной температуре, образуя с количественным выходом
симметричные 1,2-диацилгидразины, которые циклизуются в соответствующие
оксадиазолы либо нагреванием в вакууме, либо действием фосфатного ангидрида,
хлористого цинка, пятихлористого фосфора, хлорокиси фосфора в бензоле,
хлористого тионила или ангидрида соответствующей алифатической кислоты.
2,5-Диалкил-1 ,3,4-оксадиазолы образуются также при длительном нагревании
эфиров алифатических кислот с гидразингидратом при 150-230°С и при нагревании
соответствующих тетраацилгидразинов при 300-350°С по реакции:
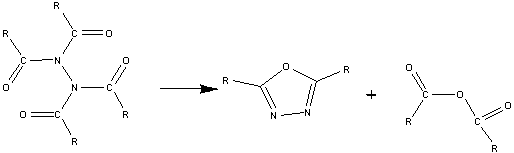
,5-Дибензгидрил-1,3,4-оксадиазол и его
производные были получены следующим путем:
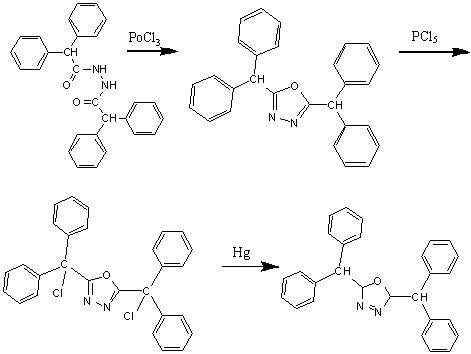
,5-Диарил-1,3,4-оксадиазолы
Для синтеза этих соединений обычно пользуются
схемой:
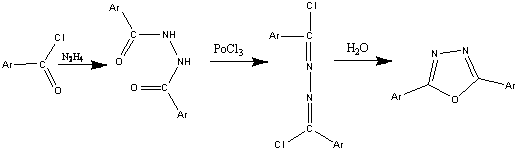
Получение 1,2-диарилгидразина из хлорангидрида
ароматической кислоты и гидразингидрата целесообразно проводить в сухом
пиридине, который связывает выделяющийся в процессе реакции хлористый водород,
благодаря чему исключается необходимость использования избытка гидразингидрата
или проведения реакции в водном растворе щелочи. При синтезе оксадиазола
совершенно нет необходимости и в продолжительном кипячении диароилгидразина с
хлорокисью фосфора, как это иногда рекомендуют; вполне достаточно нагревания до
полного растворения вещества.[2]
Симметричные 2,5-диарил-1,3,4-оксадиазолы
получают также непосредственным нагреванием при 180-350°С соответствующих
диароилгидразинов, или при действии на них фосфорного ангидрида, хлористого
тионила или хлорангидрида щавелевой кислоты. Циклизацию продукта взаимодействия
гидразида с хлорирующими агентами в оксадиазол можно осуществлять при помощи
азотнокислого серебра. 2,5-Диарил-1,3,4-оксадиазолы образуются также при
нагревании моно- или триацилгидразинов по схеме:
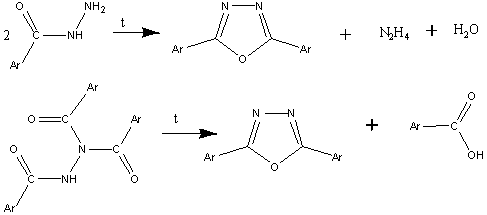
При нагревании серебряных солей 1,
2-диароилгидразинов, и при действии иода на серебряные или ртутные соли
ацилгидразонов:
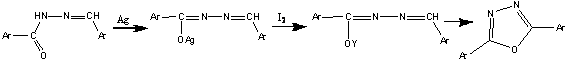
а также при нагревании гидразонов в
предыдущей реакции, при их хлорировании в четыреххлористом углероде и при
кипячении их с разбавленным раствором феррицианида калия в щелочной среде или с
изоамилнитритом. При действии хлорангидридов кислот на серебряные соли
гидразонов образуются дигидрооксадиазолы вида:[4]


Интересны методы получения арилпроизводных
1,3,4-оксадиазола, взаимодействием моноацилгидразинов карбоновых кислот с
хлоргидратами имидоэфиров при 80-160°С или при обработке продукта их
взаимодействии азотистой кислотой:

,5-Диарил-1,3,4-оксадиазолы были также получены
разложением при 280°С производных 1,3,4-оксадиазолона-(5):
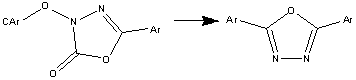
и в результате гидролиза в присутствии
минеральных кислот или щелочей 3,6-диарил-1,2-дигидро-1,2,4,5-тетразинов.[3]
ПОЛУЧЕНИЕ НЕСИММЕТРИЧНЫХ 2,5-ПРОИЗВОДНЫХ
1,3,4-ОКСАДИАЗОЛА
2-Алкил-5-арил-1,3,4-оксадиазолы
Соединения такого типа получают по схеме:

Установлено, что образование гидразидов
алифатических кислот из эфиров кислот и гидразингидрата протекает с
удовлетворительным выходом при комнатной температуре, в других условиях
гидразид легко превращается в симметричный 1,2-диацилгидразин. Изучение
кинетики бензоилирования алифатических гидразидов показало, что в разбавленных
растворах и при комнатной температуре получается с количественным выходом
1,2-диацилгидразин. Производные 2-алкил-5-арил-1,3,4-оксадиазола можно получать
взаимодействием гидразидов с ортоэфирами кислот в условиях, аналогичных синтезу
2-арил-1,3,4-оксадиазолов:

Интересен метод получения
производных оксадиазола из бензгидрильных производных 2-фенил-1,3,4-оксадиазола,
которые получаются нагреванием бензоилгидразида дифенилуксусной кислоты с
фосфорным ангидридом:[2]


,5-Диарил-1,3,4-оксадиазолы
Для получения таких соединений обычно
применяется следующая схема:

Этим методом было получено
большинство смешанных арилпроизводных 1,3,4-оксадиазола, а также моно- и
дифункциональных производных 2,5-дифенил-1,3,4-оксадиазола, причем условия
реакции и выходы не зависят существенно от положения и вида заместителя.
Следует отметить, что, вопреки
литературным данным, диароилгидразины образуются даже на холоду. При повышенных
температурах появляются в заметных количествах побочные продукты - симметричные
диароилгидразины типа (C6H5CONH)2 и (ХС6Н4СОNH)2, что
особенно наблюдалось при наличии в фенильном кольце электроно-акцепторных
заместителей. На стадии получения оксадиазола длительность нагревания
диароилгидразина с хлорокисью фосфора можно ограничить моментом его полного
растворения, вместо многочасового кипячения. Использование вышеприведенной
схемы может осложняться взаимодействием функциональных групп с применяемыми
реагентами. Во избежание этого явления разработана следующая схема:[1]

-Фенил-5-(аминофенил)-1,3,4-оксадиазолы
получаются с хорошим выходом при применении в качестве восстановителя
фенилгидразина. Этим методом осуществлено частичное восстановление
динитропроизводных 1,3,4-оксадиазола с использованием в качестве растворителя α-метилнафталина,
в котором восстановление одной нитро-группы в 2,5-ди-(р-нитрофенил)- и
2,5-ди-(м-нитрофенил)-1,3,4-оксадиазолах протекает довольно хорошо. В
2,5-ди-(о-нитрофенил)-1,3,4-оксадиазоле восстанавливаются одновременно обе
нитро-группы. Установлено также, что нитро-группа легко восстанавливается в
амино-группу и при наличии в молекуле 2,5-дифенил-1,3,4-оксадиазола других
функциональных заместителей, а также в случае замены фенильного кольца остатком
пиридина с образованием 2-(р-аминофенил)-5-(β-пиридил)-1,3,4-оксадиазола.
Однако наличие гетероциклического остатка в аминопроизводных 1,3,4-оксадиазола
существенно ухудшает условия их получения вследствие значительно меньшей
химической стойкости и трудности выделения из реакционной смеси. Амино-группа,
находящаяся в 1,3,4-оксадиазолах, легко вступает в реакции, присущие первичной
ароматической амино-группе, что дало возможность перейти к целому ряду
соответствующих производных 1,3,4-оксадиазола, встречный синтез которых
полностью подтвердил их химическое строение.
Несимметричные 2,5-диарил-1,3,4-оксадиазолы
можно получать с хорошим выходом нагреванием 5-замещенных тетразолов с
хлорангидридами карбоновых кислот в пиридине. Предложен следующий механизм этой
реакции:[1]
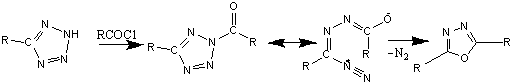
Производные
2-амино-1,3,4-оксадиазола
2-Амино-1,3,4-оксадиазол и его производные
получают отщеплением сероводорода из тиосемикарбазидов при помощи окиси свинца
по схеме:

Реакция протекает с хорошими выходами при
многочасовом нагревании раствора тиосемикарбазида в 95%-ном спирте в присутствии
10-кратного избытка окиси свинца.
2-Амино-5-фенил-1,3,4-оксадиазол синтезирован
следующими путями:

Нагреванием или действием водоотнимающих средств
из соответствующих производных тиосемикарбазида типа:
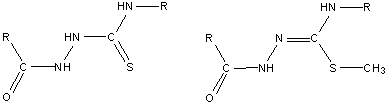
получены производные оксадиазола вида:
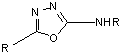
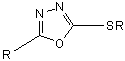
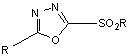
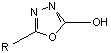
При действии на семикарбазон бензальдегида
5%-ного раствора гипобромида натрия образуется
2-амино-5-фенил-1,3,4-оксадиазол. Получен ряд других производных
2-амино-1,3,4-оксадиазол.[3]
Гетероциклические 2,5-производные
1,3,4-оксадиазола
Производные 1,3,4-оксадиазола с различными
гетероциклическими кольцами синтезируют по общей схеме получения
2,5-диарил-производных 1,3,4-оксадиазола. Синтез ацилгидразидов
гетероциклических кислот их хлорангидридов и гидразидов следует проводить на
холоду, так как при повышенной температуре, наряду с основным продуктом
реакции, образуются диадильные производные гидразида вида RCONHN(COR)2, которые
при гидролизе дают опять моноацилгидразид. При синтезе ароилгидразидов в
кипящих растворах кроме вышеуказанных продуктов получались также и симметричные
1,2-диазоилгидразины. В качестве растворителя при синтезе ацилгидразидов обычно
применяют пиридин, связывающий выделяющийся в результате реакции хлористый
водород, что благоприятствует более полному использованию исходных реагентов, а
также получению ацилгидразидов пиридинкарбоновых кислот в виде свободных
оснований. Следует, однако отметить, что при этом ухудшаются условия извлечения
ацилгидразидов из реакционной массы вследствие их хорошей растворимости в
пиридине.
Представляет интерес синтез гетероциклических
производных 2-амино-1,3,4-оксадиазола из гидразида гетероциклической кислоты и
бромциана по схеме:

или взаимодействием хлорангидрида
гетероциклической кислоты с тиосемикарбазидом с последующей циклизацией
продукта в соответствующий оксадиазол.
Этими методами получен ряд
гетероциклических производных 1,3,4-оксадиазола.[1]
Свойства
производных 1,3,4-оксадиазола
2,5-Производные 1,3,4-оксадиазола -
бесцветные вещества; низшие алкилпроизводные оксадиазола , перегоняющиеся без
разложения жидкости. Замена алкильного остатка арильным радикалом значительно
повышает температуры плавления и кипения. Несимметричные производные
1,3,4-оксадиазола в большинстве случаев плавятся и кипят ниже симметрично
построенных соединений. Введение в арильные остатки молекулы оксадиазола
заместителей неодинаковой электронной природы приводит к появлению окраски у
таких соединений. Некоторые 2,5-производные 1,3,4-оксадиазола, не имеющие
сильных электроноакцепторных групп, люминесцируют в кристаллическом состоянии,
в неполярных или малополярных растворителях и в полистироле.
2-Окси-5-арил-1,3,4-оксадиазолы могут существовать в кетонной форме.
При метилировании
2-амино-5-фенил-1,3,4-оксадиазола йодистым метилом получается
2-имино-3-метил-1,3,4-оксадиазол; ацетилирование и нитрозирование протекает
нормально. Это показывает, что 2-амино-5-фенил-1,3,4-оксадиазол может
реагировать в иминной и аминной формах. Растворимость различных производных
оксадиазола в воде не одинакова, и зависит от заместителей. Так, если
2,5-диметил-1,3,4-оксадиазол смешивается с водой в любых соотношения, то
растворимость в воде 2,5-дифенил-1,3,4-оксадиазола составляет всего лишь 0,03%.
При действии на производное оксадиазола водных растворов минеральных кислот и
щелочей происходит разрыв гетероциклического кольца с образованием
соответствующего гидразида. 2-Арилпроизводные 1,3,4-оксадиазола гидролизуются
почти мгновенно, сразу же после растворения вещества, до первичного гидразида и
муравьиной кислоты.
Подробное изучение этого вопроса
показало, что способность к гидролизу производных оксадиазола не одинакова и
уменьшается с уменьшением их растворимости. Выяснено, что при действии на
2,5-дифенил-1,3,4-оксадиазол концентрированной серной кислоты (уд. в. 1,84) не
происходит сульфирования даже при 100°С в течение четырех часов и более, а лишь
количественно получается его двойная сернокислая соль, которая в разбавленном
водном растворе легко гидролизуется с образованием исходного
2,5-дифенил-1,3,4-оксадиазола.
Концентрированная азотная кислота
(уд. в. 1,51) легко нитрует 2,5-дифенил- 1,3,4-оксадиазол с образованием смеси
о,м,р,-динитропроизводных (выходы 40, 20 и 27% соответственно).
Смесь азотной (уд. в. 1,51) и
концентрированной серной кислоты нитрует 2,5-дифенил-1,3,4-оксадиазол лишь в
2-фенил-5-(м -нитрофенил)- и 2,5-ди-(м -нитрофенил)-1,3,4-оксадиазолы с
выходами 31 и 38%.
Как было уже сказано выше,
нитро-группа в 1,3,4-оксадиазоле легко восстанавливается фенилгидразином в
амино-группу. Восстановление агентами, действующими в кислых или щелочных
средах (цинковая пыль, дисульфид натрия) не приводит к успеху, так как
оксадиазольное кольцо в таких условиях распадается вначале до соответствующего
гидразида, а затем до гидразина и ароматических кислот.
Амино-группа в фенильном кольце
1,3,4-оксадиазола после диазотирования легко замещается на другие
функциональные группы, например, галоиды, окси- и циано-группы, которые, в свою
очередь, дают новые функциональные производные 1,3,4-оксадиазола.
Диазотированные амино-группы легко сочетаются, образуя азокрасители .
-Амино-5-фенил-1,3,4-оксадиазол в
разбавленном солянокислом растворе с азотистой кислотой дает
2-нитрозамино-5-фенил-1,3,4-оксадиазол, который при восстановлении образует
2-гидразино-5-фенил-1,3,4-оксадиазол; при действии на него азотистой кислоты
получается 2-азидо-5-фенил- 1,3,4-оксадиазол .
-Гидразино-5-фенил-1,3,4-оксадиазол
с бензальдегидом образует 2-бензальгидразино-5-фенил-1,3,4-оксадиазол,
разлагающийся при обработке соляной кислотой и водяным паром на H2NNHCONHNH2 ,
С6Н5СНО и С6Н5СООН.
При действии на
2-амино-5-арил-1,3,4-оксадиазолы солянокислого фенилгидразина оксадиазольное
кольцо расщепляется с образованием диаминогуанидина. При нагревании
2-амино-5-алкил-1,3,4-оксадиазолов с гидразингидратом получаются с невысоким
выходом 3-алкил-4,5-диамино-1,2,4-триазолы. 2-Амино-5-фенил-1,3,4-оксадиазол
под действием щелочных агентов превращается в 3-фенил-1,3,4-триазолон. При
действии на производное 1,3,4-оксадиазола никеля Ренея гетероциклическое кольцо
разрушается с образованием соответствующего амида.
Молекулярный бром не бромирует
2,5-дифенил-1,3,4-оксадиазола, но образует лишь комплексные соединения
оксадиазола с бромом. При действии на 2,5-дифенил-1,3,4-оксадиазол смеси хлора
и иода получено комплексное соединение оксадиазола с хлористым иодом.
Производные 1,3,4-оксадиазола также легко дают в спиртовом растворе комплексные
соединения с AgNO3, HgCl2.
-Замещенные 1,3,4-оксадиазолы
количественно определяются потенциометрическим титрованием нитритом натрия;
2,5-диарил-1,3,4-оксадиазолы анализируют аргентометрическим методом. Для
производных 1,3,4-оксадиазола исследованы ультрафиолетов ы е и инфракрасные
спектры, спектры люминисценции и Раман-спектры. Измерены дипольные моменты и
вычислены нормальные вибрационные частоты оксадиазольного кольца, проведены
полярографические исследования. Определена сцинтилляционная эффективность
производных 1,3,4-оксадиазола в толуоле и полистироле.[5]
. Обсуждение результатов
Самыми основными и распространенными
методами получения 1,3,4-оксадиазолов и его производных являются циклизация:
окислительная и дегидратационная.
Дегидратация 1,2-диацилгидразинов.
Циклодегидратация дибензилгидразина
при 250-300°С приводит к 2,5-дифенил-1,3,4-оксадиазолу. Аналогичным образом при
пиролизе N-ацетамидо-N-фенилуретана
(при перегонке) происходит отщепление этанола и образуется
2-метил-4,5-дигидро-4-фенил-5-кето-1,3,4-оксадиазол. Диацилгидразиды,
по-видимому,являются промежуточными соединениями как при образовании этих
продуктов из бензоилгидразида, так и при взаимодействии N-фенил-N-аминоуретана
с ацетамидом. [3]
Образованию 1,3,4-оксадиазольного кольца
способствуют следующие дегидратирующие агенты: хлорсульфоновая кислота,
хлористый сульфурил, пятиокись фосфора, n-толуолсульфокислота,
ее хлорангидрид, хлористый тионил, хлорокись фосфора, хлорид цинка, ангидриды
кислот, пятихлористый фосфор, серная кислота.

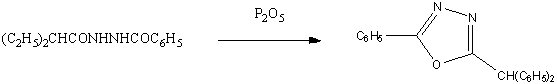
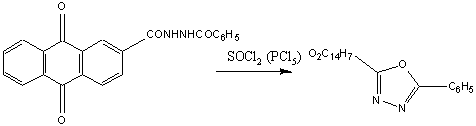
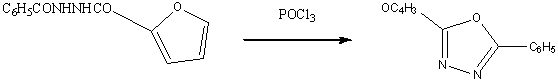
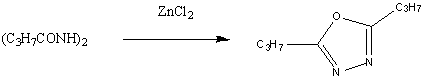
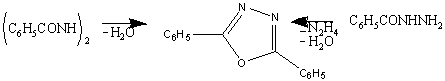
Диацилгидразиды образуются, по-видимому, в
качестве промежуточных продуктов при преращении бис-α-хлорбензилиденгидразинов
в 2,5-дизамещенные 1,3,4-оксадиазолы действием горячей воды или раствора
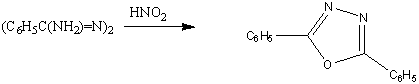
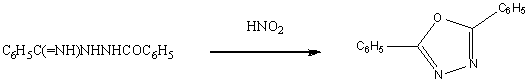
азотнокислого серебра. Аналогичное замыкание цикла протекает при образовании
1,3,4-оксадиазолов из бис-α-аминобензилиденгидразинов
и азотистой кислоты.
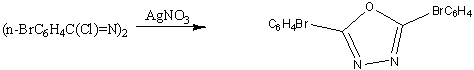
-ортоэфиры и гидразиды арилкарбоновых кислот
Монозамещенные 1,3,4-оксадиазолы можно получить
конденсацией гидразида ароматической карбоновой кислоты с этилортоформиатом,
взятым в избытке. Из высших ортоэфиров получены соответствующие 2-алкил-5-арил-1,3,4-оксадиазолы.
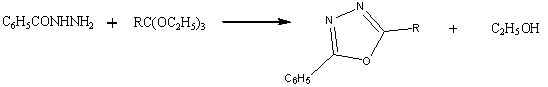
R=H,
СН3, С2Н5
Кроме того, были выделены промежуточно
образующиеся 1-ацил-2-этоксиэтиленгидразины. При замыкании цикла в реакции
между гидразидом пиразолкарбоновой-3(или 5) кислоты и этилформиатом участвует
гетероциклический азот.
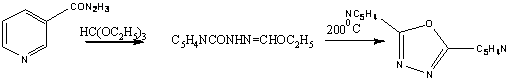
-реакция Гофмана с амидами N-ацил-β-арил-β-аланинов
Гипобромит щелочного металла превращает амид N-ацил-β-фенил-β-аланина
в 5-фенил-1,3,4-оксадиазолон-2(3Н), который идентичен продукту реакции
гипобромита с бензоилмочевиной

-окисление гидразонов
Щелочные растворы феррицианида калия или
изоамилнитрита способны превращать бензоилгидразон бензальдегида
2,5-дифенил-1,3,4-оксадиазол. Продукт, полученный при действии на семикарбозон
бензальдегида гипоиодита или гипобромита Na
был идентифитирован как 2-амино-5-фенил-1,3,4-оксадиазол. В каждой из этих двух
реакций первоначальное окисление или галогенирование, по-видимому,
предпочтительнее идет по атому углерода, а не азота.
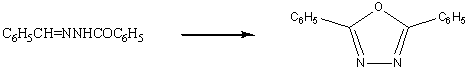
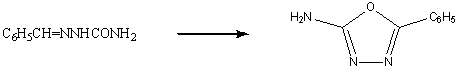
-ацилтиосемикарбозиды
В присутствии окиси свинца или окиси ртути
некоторые ацилтиосемикарбозиды, отщепляя элементы сероводорода, циклизуются в
1,3,4-оксадиазолы. Аналогичное замыкание цикла наблюдается и в присутствии
едкого кали.
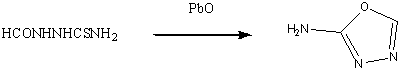
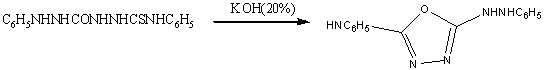
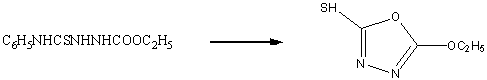
Циклизация 1-карбэтокси-4-фенилтиосемикарбазида,
протекающая в концентрированной соляной кислоте, приводит к
2-этокси-1,3,4-оксадиазолтиолу-5.
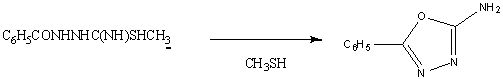
S-метилпроизводное
1-бензоилтиомочевины при пиролизе теряет метилмеркаптании превращается в
2-амино-5-фенил-1,3,4-оксадиазол.
Обработка серебряной соли бензоилгидразона
бензальдегида хлористым ацетилом или бензоилом в инертном растворителе дает
2,5-дифенил-4,5-дигидро-4-ацил-1,3,4-оксадиазол
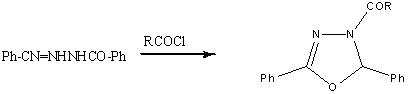
серебряная соль
Различные химические агенты могут
взаимодействовать как на оксадиазольное кольцо, так и на заместители.
-амино-1,3,4-оксадиазолы могут реагировать в
двух таутомерных формах:
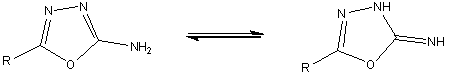
А В
О таутомерии незамещенных аминооксадиазолов
фактически ничего не известно. Оксадиазолы же структуры А однозначно
установлены получением некоторых бензилиден- и фталилпроизводных.
-амино-1,3,4-оксадиазолы растворимы в
минеральных кислотах и образуют с ними изолированные соли, которые при плавлении
распадаются. Длительное воздействие горячих кислот ведет к полному расщеплению
цикла с образованием соответствующих карбоновых кислот, солей гидразина,
аммиака и СО2.
Водные растворы щелочей на холоду и при слабом
нагревании не растворяют большинство 2-амино-1,3,4-оксадиазолов и поэтому
годятся для осаждения.[2]
Среди соединений, обладающих определенным
уровнем антибактериальной активности, особое внимание привлекают и
1,3,4-оксадиазолы. Известно, что оксадиазолы как представители группы
пенициллинов оказывают бактерицидное действие на микроорганизмы, находящиеся в
логарифмической фазе роста. Это связано с их способностью ингибировать
биосинтез компонентов клеточной стенки бактериальной клетки, в регуляции
которого принимает участие специфический энзим - транспептидаза. Благодаря
структурному сходству пенициллинов с пептидным субстратом фермента, антибиотик
конкурирует с ним за активный центр транспептидазы. Взаимодействие молекулы
антибиотика с активным центром энзима является необратимой реакцией. Действие
азолов на бактериальную клетку также связано с прямым влиянием на синтез
компонентов клеточной стенки. 1,3,4-Оксадиазолы М007-М009, М011, М013 подавляли
рост как золотистого стафилококка, так и кишечной палочки, что позволяет их
отнести к группе веществ широкого спектра активности.[6]
Многие производные аминооксадиазолов, полученные
в результате ацилирования аминогруппы, биологически активны. Например, N-оксадиазол
и карбаминовые, полученные конденсацией 2-амино-1,3,4-оксадиазола с
хлорангидридом кислот, обладают антимикробной активностью:
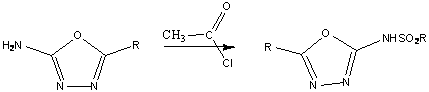
Другие производные 1,3,4-оксадиазолов
применяются при приготовлении лекарственных препаратов. Реакцией сульфохлоридов
по аминогруппе 1,3,4-оксадиазола синтезированы сульфамидные препараты, которые
далее используются для получения лекарств:
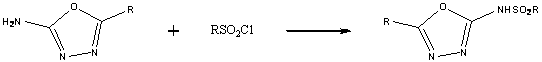
Так же реакцией RCOCl
c N2H4
получают RCO-NHNHCOR,
циклодегидратацией которых действием BF3*OEt2
в диоксане синтезируют новые 2,5-R2-1,3,4-оксадиазолы
[R=(CH2
)14Me, (CH2)16Me,
(CH2)8CH=CH2,
(CH2)7CH=CH(CH2)7Me,
(CH2)7CH=CHCH2CH(OH)(CH2)5Me,
(CH2)7CH(OH)(CH2)2CH=CH(CH2)4Me].
Наличие в радикалах двойных связей позволяет их применять для дальнейшего
синтеза более сложных соединений 1,3,4-оксадиазольного ряда: красителей,
лекарственных препаратов, соединений с гербецидной и фунгицидной активностью.
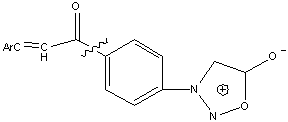
Циклизацией халконов (1 мета- и пара-изомеры) с N2H4
при микроволновом облучении (ПЭГ-200 им АсОН, 240 Вт, 80-85°С, 5-10 мин)
получают сидноны (2 мета- и пара-изомеры, Ar-Ph,
4-толил,4-анизил, R=Н,СНО), при
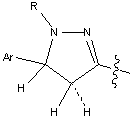
взаимодействии которых с Br2-AcOH
при 20°С с последующим микроволновым облучением (60-65°С) образуются (3 мета-и
пара-изомеры, Ar=Ph,
4-толил,4-анизил, R=CHO,
Ac).
1. 
. 
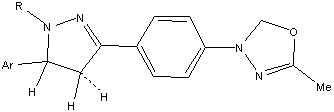
. 
Такой метод синтеза производных
1,3,4-оксадиазола с применением микроволнового облучения является одним из
самых новых и быстрых методов.
В качестве гербецидов и фунгицидов
запатентованы N-ацилпроизводные,
рассматриваемых гетероциклических аминов:

Известны примеры других реакций по аминогруппе.
Амнооксадиазолы вступают в реакцию Манниха, конденсируются с ароматическими
альдегидами с образованием оснований Шиффа:
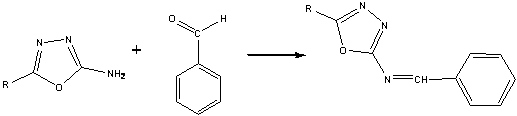
Аминооксадиазолы вступают в реакции
диазотирования, доказывая свою ароматическую природу. Диазотирование
2-анил-5-амино-1,3,4-оксадиазолов нитратом натрия в разбавленной (10%) соляной
кислоте приводит к образованию первичного нитрозоамина.
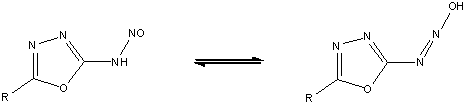
Диазотирование в кислой среде дает соль
диазония. При диазотировании в присутствии трехфтористого бора образуются
устойчивые борфториты диазония.
На основе оксадиазолов получены красители:

Получены азокрасители с применением в качестве
азосоставляющих 1-алил-3-алкил-5-пиразоионов, пригодные к свету крашения и
печати. Запатентованы азокрасители с оксадиазольным циклом с функциональными
группами. Сочетанием диазотированного 2-амино-5-радоно-1,3,4-оксадиазола с
галогенцианатом в присутствии акцептора кислоты, с N-этил-N-(β-цианэтил-)-анилином,
синтезирован диазокраситель хорошей светопрочностью.

Особенно интересны сцинтилляционные свойства
1,3,4-оксадиазола и его производных. Жидкие и пластические сцинтилляторы
применяются для фиксирования β-излучения
из космоса, δ-лучей и быстрых
нейтронов.
Многие производные 1,3,4-оксадиазола обладают
чрезвычайной стабильностью. Известно, что 2,5-дифторалкил-1,3,4-оксадиазолы не
изменяются даже при нагревании в течении 15 часов при 350°С и одного часа при
400°С. Подобные производные 1,3,4-оксадиазола нашли применение в приготовлении
материалов для фотопленок с повышенной термической стабильностью, в
производстве растворителей для фторированных полимеров.[5]
3. Экспериментальная часть
Синтез
2-амино-5-фенил-1,3,4-оксадиазола циклизацией семикарбазона бензальдегида
К суспензии 16,3г семикарбазона бензальдегида и
16,4г уксуснокислого натрия в 100 мл уксусной кислоты при перемешивании с
обратным холодильником прикапывают раствор 8 г брома в 20 мл ледяной уксусной
кислоты. Реакционную смесь перемешивают в течении 6 часов, затем выливают в 1,5
литра холодной воды. Отфильтровывают и высушивают на воздухе выпавшие кристаллы.
Выход 5 г, 62%. Тпл. 245°С
Синтез
2-амино-5-фенил-1,3,4-оксадиазола дигидратацией ацетилтиосемикарбазида.
Раствор 13,3 г ацетилтиосемикарбазида в 300 мл
пропилового спирта нагревают в 100 г окиси свинца при перемешивании с обратным
холодильником на кипящей водяной бане. Отфильтровывают выделившийся сульфид
свинца. Остаток после отгонки растворителя перекристаллизовывают из спирта.
Выделяется 7,5 г белое кристаллическое вещество(иглы).
Тпл. 182-183°С
оксадиазол циклизация синтез
производный
Выводы
В данной курсовой работе рассмотрены физические
и химические свойства 1,3,4-оксадиазолов, способы их получения, а также
производные 1,3,4-оксадиазолов, применение которых в различных областях в
последние годы значительно возросло.
Литература
1. Насыпов Е. П., Греков А. П.,
"Успехи химии", 1964, т. 33, в. 10, с. 1184-97;
. ПАТ США 55580 «Способ получения
оксадиазолов», РХС Хим., 1982, №5.
. Н.К. Кочетков, «Кислород и
серусодержащие гетероциклы»: М.1985
. Поддубный И.С., Беленький Л.И.,
Краюшкин М.М. // ХГС, 1994, №5, с.686-692
. Под редакцией доктора хим. наук
В.Г. Карцева. Химия и биологическая активность синтетических и природных
соединений, "Кислород- и серу содержащие гетероциклы", том 2- М.: IBS
PRESS.стр.45
. Курьянов, М.К. Токарев, И.П.
Отурина // Ученые записки ТНУ. Изучение антимикробной активности новых
синтетических химиопрепаратов. Серия «Биология, химия». -2005.- Т.22 (61), №
7.. - С.65 - 68.