|
Тип погрешности
|
Причина погрешности
|
Расчетная формула погрешности, %
|
|
Водородная
|
Избыток ионов Н+ вследствие недотитрования сильной кислоты
или перетитрования основания (сильного или слабого) сильной кислотой
|
∆H+ = (10-pT*V2*100)/(c*V1)
|
|
Гидроксильная
|
Избыток ионов ОН - вследствие недотитрования сильного
основания или перетитрования кислоты (слабой или сильной) сильным основанием
|
∆ОН- =
(10-(14-pT)*V2*100)/(c*V1)
|
|
Кислотная
|
Избыток молекул слабой кислоты НА при её недотитровании
|
∆НА = (10pK-pT*100)/(1+10pK-pT)
|
|
Щелочная
|
Избыток молекул слабого основания MOH при его
недотитровании
|
∆МОН = 10pK+pT-14*100
|
где V1 и V2 - объемы анализируемого раствора до и после титрования; C - молярная концентрация эквивалента
вещества анализируемого раствора; рК - показатель константы диссоциации слабого
электролита; рТ - показатель титрования индикатора.
. Пусть индикатор, с помощью которого титровали гидроксид аммония серной
кислотой, будет метиловый красный. pT Ind =
5,2 больше pH в точке эквивалентности, равного
5,139. Следовательно, раствор NH4OH недотитрован. Рассчитываем щелочную
ошибку II-ого рода
∆МОН = 10pK+pT-14 * 100
∆МОН =104,75+5,3-14 * 100 = 1.12 * 10-4 %
. Пусть pT бромфенолового синего = 3,8 меньше pH в точке эквивалентности,
равного 5,139. Следовательно, раствор NH4OH
перетитрован H2SO4. Рассчитываем водородную ошибку
(кислотную ошибку I-ого рода):
∆Н = (10-pT * V2 * 100) / C * V1
∆Н = (10-3.8 * (10 + 6) * 100) / 0.5 * 6 = 8.45 * 10-2
%
Вывод
С помощью расчетов точек кривой титрования по методу «нейтрализации» 0,15
M NH4OH - 0,25 M H2SO4, вычислили скачок
титрования, равный от 8.296 (90%) до 2.044 (110%). С помощью расчета
индикаторных ошибок, подобрали оптимальный индикатор. С индикатором метиловый
красный индикаторная ошибка составила 1.12 * 10-4 % следовательно,
раствор NH4OH титруют
3. Окислительно-восстановительное титрование
3.1 Классификация редокс-методов
Известно несколько десятков различных методов ОВ титрования. Обычно их
классифицируют следующим образом:
. Классификация по характеру титранта. В этом случае методы ОВ титрования
подразделяют на две группы:
оксидиметрия - методы определения восстановителей с применением
титранта-окислителя;
редуктометрия - методы определения окислителей с применением
титранта-восстановителя.
. Классификация по природе реагента, взаимодействующего с определяемым
веществом. Ниже после названия соответствующего метода в скобках указано
основное действующее вещество этого метода: броматометрия (KBrO3), бромометрия (Br2), дихроматометрия (K2Cr2O7), иодатометрия (KIO3),
иодометрия (I2), нитритометрия (NaNO2), пермангонатометрия (KMnO4), цериметрия (Ce(SO4)2), титанометрия (Ti3+), ванадатометрия (NH4VO3) и др. Реже применяются некоторые другие методы ОВ
титрования, такие, аскорбинометрия (аскорбиновая кислота).
3.2 Условия проведения реакций окислительно-восстановительного
титрования
Условия, применяемые в методах окислительно-восстановительного титрования
должны отвечать ряду требований, важнейшими из которых являются следующие:
реакция должна протекать практически до конца;
реакция должна протекать достаточно быстро, чтобы равновесие, при котором
реальные окислительно-восстановительные потенциалы обеих резонс-пар равны,
устанавливалось практически мгновенно;
реакция должна протекать стехиометрически, побочные эффекты должны быть
исключены;
конечная точка титрования должна определяться точно и однозначно либо с
индикатором или нет.
3.3 Виды окислительно-восстановительного титрования
.Прямое окислительно-восстановительное титрование проводят тогда, когда
окислительно-восстановительная реакция удовлетворяет основным требованиям к
реакциям этого вида титрования. Определяемое вещество непосредственно
взаимодействует с титрантом.
.Обратное окислительно-восстановительное титрование проводят тогда, когда
применение прямого титрования нецелесообразно по тем или иным причинам. К
аликвоте анализируемого раствора, содержащего определяемый компонент х,
прибавляют точно известное избыточное количество вещества А. Раствор
выдерживают некоторое время для обеспечения полноты реакции между х и А.
Непрореагирующий избыток вещества А оттитровывают стандартным раствором
титранта Т.
.Заместительное окислительно-восстановительное титрование применяют для
определения веществ как вступающих, так и не вступающих в
окислительно-восстановительные реакции. К аликвоте анализируемого раствора,
содержащего определяемый компонент, прибавляют избыточное количество реагента.
Выделившееся вещество оттитровывают определенным титрантом.
3.4 Индикаторы метода
В титрометрическом методе определяют КТТ индикаторным методом. При этом
индикатор может играть роль либо реагента, участвующего в
окислительно-восстановительной реакции, либо являться специальным вводимым
индикатором. В соответствии с этим индикаторы в окислительно-восстановительном
титровании можно классифицировать следующим образом:
. Индикатор-реагент - участвует в окислительно-восстановительной реакции
(пермангонатометрия);
. Индикатор - вступает в непосредственное взаимодействие с окислителем
или восстановителем (участвующими в окислительно-восстановительной реакции) с
образованием различных соединений (крахмал).
. Индикатор - при определенном потенциале раствора окисляется или
восстанавливается с изменением окраски (окислительно-восстановительные
индикаторы).
Окислительно-восстановительные индикаторы бывают обратимыми и необратимыми.
Обратимые индикаторы меняют окраску обратимо при потенциале раствора в точке
эквивалентности или вблизи ее и при этом не разрушаются. Необратимые индикаторы
изменяют окраску при достижении определенного значения потенциала в точке
эквивалентности или вблизи ее и при этом необратимо разрушаются. Пример -
метиловый оранжевый, метиловый красный, нейтральный красный.
3.5 Йодометрия
Йодометрия - метод окислительно-восстановительного титрования, основанный
на реакциях, связанных с окислением восстановителей свободным йодом I2
или с восстановлением окислителей йодидом калия KI. Оба процесса можно выразить
следующей схемой:
2
+ 2е → 2I-
Т.к. стандартный окислительно-восстановительный потенциал пары невелик φ0(I2/2I-) = 0,54 В, йод является
относительно слабым окислителем, а ионы I- - сравнительно сильным
восстановителем.
С помощью метода йодометрии можно определять:
. Восстановители SO32-, S2O32-,
NO2-, S2-, CN-, SCN- и
др.:
а) путем прямого титрования анализируемого раствора раствором йода:
32- + I2
+ 2Н2О = SO42- + 2I- + 2H+
б) путем обратного титрования.
Используется, если скорость взаимодействия восстановителя с йодом
невелика. В этом случае к раствору восстановителя добавляют избыток
титрованного раствора I2, а спустя некоторое время не вступивший в
реакцию йод титруют раствором тиосульфата натрия:
2S2O32- + I2 = S4O62-
+ 2I-
. Окислители Fe3+, Cr2O72-,
H2O2, Cl2, Br2, ClO3-,
MnO4- и др.
Проводить определение, титруя раствор окислителя йодидом калия KI нельзя,
т.к. невозможно фиксировать конец титрования. Поэтому пользуются методом
замещения: к анализируемому раствору окислителя добавляют избыток раствора KI:
2MnO4- + 10I- + 16H+
= 5I2 + 2Mn2+ + 8Н2О
В результате реакции выделяется йод в количестве, эквивалентном
количеству окислителя; йод титруют раствором тиосульфата натрия по уравнению:
S2O32- + I2 = S4O62- + 2I-
3.5.1 Достоинства и недостатки йодометрии
К достоинствам метода йодометрии можно отнести следующие:
. Большая точность по сравнению с другими методами
окислительно-восстановительного титрования.
. Растворы йода окрашены, и титрование можно проводить без индикатора.
Желтая окраска ионов I3- при отсутствии других окрашенных
продуктов отчетливо видна при очень малой концентрации (5•10-5н.).
. Йод хорошо растворяется в органических растворителях, поэтому метод
широко применяется для титрования в неводных средах.
Недостатки метода, вызывающие ошибки при выполнении йодометрических
определений:
. Потери йода из-за его летучести. Поэтому титрование проводят на холоду
и по возможности быстро. При необходимости оставить раствор на некоторое время
для завершения реакции, его хранят под притертой пробкой.
. Окисление ионов йода кислородом воздуха в кислой среде.
. Йодометрическое титрование нельзя проводить в щелочной среде вследствие
диспропорционирования йода.
. Относительно медленные скорости реакций с участием йода.
. В процессе хранения стандартные растворы йода и тиосульфата изменяют
свой титр. Чтобы избежать ошибок, необходимо периодически проверять титр йода
по тиосульфату, а титр тиосульфата по дихромату калия.
3.5.2 Индикаторы йодометрии
Фиксируют конечную точку титрования в методе йодометрии с помощью
специфического индикатора - крахмала, который образует с йодом
комплексно-адсорбционное соединение синего цвета. Эта реакция очень чувствительна,
она позволяет легко обнаруживать йод при концентрации 10-5 н. Т.к.
соединение йода с крахмалом очень прочное, крахмал следует добавлять в конце
титрования, когда окраска раствора становится бледно-желтой. Если вводить
крахмал раньше, то очень много йода будет связано с крахмалом. При титровании
йод с трудом освобождается из соединения с крахмалом, и результат титрования
окажется неточным.
.5.3 Условия титрования
При проведении йодометрических определений следует соблюдать следующие
условия:
. Йод - вещество летучее, поэтому титрование проводят на холоду. Кроме
того, при увеличении температуры снижается чувствительность крахмала как
индикатора (при 500 С индикатор в 10 раз менее чувствителен, чем при
250 С).
. Растворимость йода в воде мала, поэтому определение окислителей
необходимо проводить в присутствии большого избытка KI, который образует с
йодом растворимое нестойкое комплексное соединение:
+ I2 → K[I3]
. Скорость реакции между окислителями и KI обычно невелика, поэтому к
титрованию выделившегося йода обычно приступают спустя некоторое время.
. Йодометрическое титрование нельзя проводить в щелочной среде, т.к.
протекает побочная реакция:
2
+ 2OH- = IO- + I- + Н2О
Образующийся гипойодит является более сильным окислителем, чем йод, он
окисляет тиосульфат до сульфата:
S2O32- + 4IO- +
2OH- = 4I- + 2SO42- + Н2О.
Поэтому во избежание побочных реакций титрование проводят при рН не более
9.
. В кислых растворах йодиды постепенно окисляются кислородом воздуха:
I- + O2 + 4H+ = 2I2 + 2Н2О
Свет ускоряет эту реакцию, поэтому реакционную смесь хранят в темноте.
3.5.4 Приготовление рабочих растворов
Рабочими растворами метода йодометрии являются растворы йода и
тиосульфата натрия.
Титрованный раствор йода можно приготовить исходя из точной навески
химически чистого кристаллического йода, который очищают от примесей путем
возгонки.
Однако очистка йода представляет собой очень трудоемкую операцию. Кроме
того, титрованный раствор в процессе работы с ним и при длительном хранении
меняет свой титр вследствие летучести йода, и периодически его нужно проверять.
Поэтому обычно готовят раствор I2 приблизительно нужной концентрации
(0,05-0,1 н.) растворением навески йода в растворе KI (40 г/л). Точную
концентрацию полученного раствора устанавливают по раствору тиосульфата натрия.
Тиосульфат натрия Na2S2O3•5Н2О
является неустойчивым веществом. Оно легко реагирует с углекислым газом и
кислородом воздуха:
Na2S2O3 + Н2О + СO2 = NaHCO3
+ NaНSO3 + S
2Na2S2O3 + O2 = 2Na2SO4 + 2S
Поэтому готовят приблизительно 0,1 н. раствор тиосульфата, растворяя
навеску соли в свежепрокипяченой воде (для удаления СO2). Хранить
готовый раствор Na2S2O3 рекомендуется в темных
бутылях, защищенных от двуокиси углерода трубкой с натронной известью. В дальнейшем
титр раствора начинает медленно уменьшаться, поэтому его необходимо
периодически проверять.
Для установки концентрации тиосульфата предложено много различных
стандартных веществ, например твердый химически чистый йод, йодат калия KIO3,
бромат калия KBrO3, дихромат калия и др. На практике чаще всего
пользуются дихроматом калия.
3.6 Окислительно-восстановительное титрование 0.2 M HCOOH - 0.25 M K2Cr2O7
K2Cr2O7 + 3HCOOH + 4H2SO4
→ K2SO4 + Cr2(SO4)3
+ 3CO2 + 7H2O
Cr2O72- + 14H+ + 6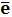
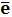 →
2Cr3+ + 7H2O -
окислитель восстанавливается
→
2Cr3+ + 7H2O -
окислитель восстанавливается
HCOOH - 2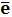
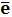 → CO2 + 2H+ -
восстановитель окисляется
→ CO2 + 2H+ -
восстановитель окисляется
Cr2O72- + 8H+ + 3HCOOH →
2Cr3+ + 7H2O + 3CO2
Концентрация HCOOH = 0.2 M, концентрация K2Cr2O7 = 0.25 M.
Сн
(HCOOH) = См / fэкв-ти = 0.2/ 
 = 0.04 H.
= 0.04 H.
Сн
(K2Cr2O7) = См
/ fэкв-ти =
0.25/ 
 = 1.5 H.
= 1.5 H.
Пусть
объем раствора HCOOH будет
равен 10мл.
С
(HCOOH) * V (HCOOH)= С (K2Cr2O7) * V (K2Cr2O7)
V (K2Cr2O7) = С (HCOOH) * V (HCOOH) / С (K2Cr2O7) = 0.4 *
10 / 1.5=
=
2.667 мл.
3.6.1 Расчет точек кривой титрования, потенциалов
До точки эквивалентности считаем по титруемому веществу:
φ = φ0 + 
 * lg
* lg 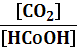
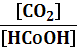
.
1% добавили от необходимого объема
.667
мл - 100%
Х
мл - 1%
Х
= 0.02667 (мл) - добавленный объем K2Cr2O7
Найдем
Сн (K2Cr2O7)
прореагировавшего с учетом разбавления:
Сн
(K2Cr2O7) = Сн
(K2Cr2O7)нач.
* Vдоб / Vобщ.
= 1.5 * 0.02667 / 10 + 0.02667 =
0.003989859
По
закону эквивалентов:
Сн
(HCOOH)прореаг.= Сн (K2Cr2O7)прореаг = 0.003989859
Найдем
Сисх.( HCOOH ) с учетом разбавления:
Сисх.(
HCOOH) = Сн (HCOOH) * Vнач.( HCOOH) / Vобщ. =
=
0.4 * 10 / 10 + 0.02667 = 0.398936037
Найдем
C (HCOOH)ост:
Сост.
= Сисх. - Спрореаг.= 0,398936037 - 0,003989859 =
0,394946178
φ = - 0.20 + 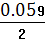
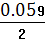 * lg
* lg 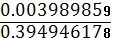
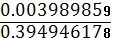 = -
0.2589 B
= -
0.2589 B
.
10% добавили от необходимого объема
.667
мл - 100%
Х
мл - 10%
Х
= 0.2667 (мл)- добавленный объем K2Cr2O7
Найдем
Сн (K2Cr2O7)
прореагировавшего с учетом разбавления:
Сн
(K2Cr2O7) = Сн
(K2Cr2O7)нач.
* Vдоб / Vобщ.
= 1.5 * 0.2667 / 10 + 0.2667 =
=
0.038965782
По
закону эквивалентов:
Сн
(HCOOH)прореаг. = Сн (K2Cr2O7)прореаг = 0.038965782
Найдем
Сисх (HCOOH) с учетом разбавления:
Сисх.(HCOOH)
= Сн (HCOOH) * Vнач.(HCOOH)
/ Vобщ.=
=
0.4 * 10 / 10.2667 = 0.389609124
Найдем
С(HCOOH)ост:
Сост.
= Снач.- Спрореаг.= 0,350643342
φ = - 0.20 + 
 * lg
* lg 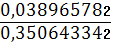
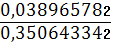 = -
0.228 B
= -
0.228 B
.
50% добавили от необходимого объема
.667
мл - 100%
Х
мл - 50%
Х
= 1.3335 (мл) - добавленный объем K2Cr2O7
Найдем
Сн (K2Cr2O7)
прореагировавшего с учетом разбавления:
Сн
(K2Cr2O7) = Сн
(K2Cr2O7)нач.
* Vдоб / Vобщ.= 1.3335 * 1.5 / 10 + 1.3335 =
=
0.176490051
По
закону эквивалентов:
Найдем
Сисх.(HCOOH) с учетом разбавления:
Сисх.(HCOOH)
= Сн (HCOOH) * Vнач.(HCOOH)
/ Vобщ.= 0.4
* 10 / 11.3335
=
0.352935986
Найдем
С(HCOOH)ост:
Сост.
= Снач.- Спрореаг = 0,176445935
φ = - 0,20 + 
 * lg
* lg 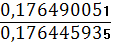
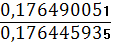 = -
0,199 B
= -
0,199 B
.
90% добавили от необходимого объема
,667
мл - 100%
Х
мл - 90%
Х
= 2,4003 (мл) - добавленный объем K2Cr2O7
Найдем
Сн(K2Cr2O7)
прореагировавшего с учетом разбавления:
Сн
(K2Cr2O7) = Сн
(K2Cr2O7)нач.
* Vдоб / Vобщ.
= 1.5 * 2.4003 / 10 + 2.4003 =
=
0.290351846
По
закону эквивалентов:
Сн
(HCOOH)прореаг.= Сн (K2Cr2O7)прореаг = 0.290351846
Найдем
Сисх.(HCOOH) с учетом разбавления:
Сисх.(HCOOH)
= Сн (HCOOH) * Vнач.(HCOOH)
/ Vобщ.= 0.4
* 10 / 12.4003
=
0.322572841
Найдем
С(HCOOH)ост:
Сост.=
Снач.- Спрореаг.= 0.032220994
φ = - 0.20 + 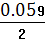
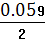 * lg
* lg 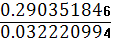
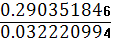 = -
0.1718 B
= -
0.1718 B
.
99.9% добавили от необходимого объема. Точка эквивалентности
.667
мл - 100%
Х
мл - 99,9%
Х
= 2,664333 (мл) - добавленный объем K2Cr2O7
Найдем
Сн (K2Cr2O7)
прореагировавшего с учетом разбавления:
Сн
(K2Cr2O7) = Сн
(K2Cr2O7)нач.
* Vдоб / Vобщ = 1,5 * 2,664333 / 10 +
+
2,66433 = 0,315571258
По
закону эквивалентов:
Сн
(HCOOH)прореаг. = Сн (K2Cr2O7)прореаг
= 0.290351846
Найдем
Сисх.(HCOOH) с учетом разбавления:
Сисх
(HCOOH)= Сн (HCOOH) * Vнач (HCOOH) / Vобщ =
0,4 * 10 /
/
12,664333 = 0,315847664
Найдем
С(HCOOH)ост:
Сост
= Снач - Спрореаг = 0,000276406
φ = - 0.20 + 
 * lg
* lg 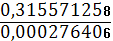
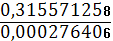 = -
0,1098 B
= -
0,1098 B
.
100% добавили от необходимого объема. Точка эквивалентности
.
φ = (φок*nок+ φвос*nвос) / (nок+ nвос) = (1,36*6+(-0,20)*2) / (6+2) = 0,97 В
.
lgKp =
( φок - φвос) * n /
0.059 = (1,36 + 0,20) * 6 / 0.059 = 158,64
Kp = 10158,64
Kp = 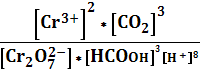
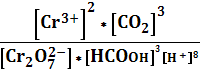
Пусть
[Cr2O72-] = х моль/литр, тогда [HCOOH] = 3х.
[Cr3+] с учетом разбавления в точке эквивалентности равна:
[Cr3+] = (Снач.* Vнач ./ Vобщ ) - x =
(0.25* 2.667 / 12.667) - x = 0.0526 - x
[CO2] с учетом разбавления в точке эквивалентности равна:
[CO2] = (Cнач * Vнач
/ Vобщ) - х = (0,2 * 10 / 12,667) - х = 0,1579 - 3х
Константа
равновесия с учетом следующих соотношений принимает
вид:
10158,64
= 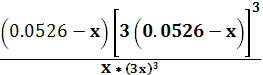
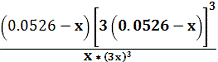 │
│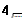
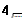
39.66 = 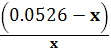
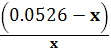
39.66 * x =
0.0526 - x
4.57
* 1039 * x - x = 0.0526
x = 1.15 * 10-41
- равновесная концентрация [Cr2O72-]
φв т.э. =
1.36 + 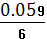
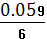 * lg
* lg 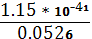
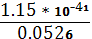 = 0.97 (
по [Cr2O72-] )
= 0.97 (
по [Cr2O72-] )
φв т.э. =
-0.20 + 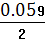
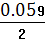 * lg
* lg 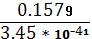
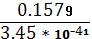 = 0.97 (
по [HCOOH] )
= 0.97 (
по [HCOOH] )
После
точки эквивалентности расчет ведем по титранту
φ = φ0 + 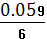
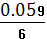 * lg
* lg 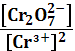
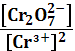
.
100,1% добавили от необходимого объема, раствор перетитрован
.667
мл - 100%
Х
мл - 0.1%
Х
= 0.002667 (мл) - избыточный объем K2Сr2O7
Найдем
С (Cr2O72-)изб с учетом разбавления:
С
(Сr2O72-)изб. = С(K2Cr2O7)нач. * Vдоб / Vобщ =
.= 0.002667 * 1.5 / 10 +
2.667 + 0.002667 = 0.000316
Найдем
C (Cr3+) с
учетом разбавления:
C (Cr3+) = 2.667 * 1.5 * 2 / 12.669667 = 0.6315
φ = 1.36 + 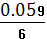
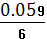 * lg
* lg 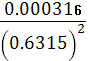
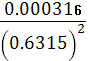 = 1.33 B
= 1.33 B
.
110% добавили от необходимого объема, раствор перетитрован
.667
мл - 100%
Х
мл - 10%
Найдем
С(Cr2O72-)изб с учетом разбавления:
Сн
(Cr2O72-)изб.= С(Cr2O72-)нач.
* Vдоб / Vобщ
=
.= 1.5 * 0.2667 / 10 +
2.667 + 0.2667 = 0.03093
Найдем
С (Cr3+) c
учетом разбавления:
Сн
(Cr3+) =
2,667 * 1,5 * 2 / 12,9337 = 0,619
φ = 1,36 + 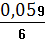
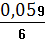 * lg
* lg 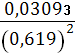
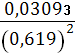 = 1,35 В
= 1,35 В
.
150% добавили от необходимого объема, раствор перетитрован
.667
мл - 100%
Х
мл - 50%
Х
= 1,3335 (мл) - избыточный объем K2Cr2O7
Найдем
С(Cr2O72-)изб с учетом разбавления:
Сн
(Cr2O72-)изб.= С(Cr2O72-)нач.
* Vдоб / Vобщ
=
.= 1.5 * 1,3335 / 10 +
2.667 + 1,3335 = 0,14287
Найдем
С (Cr3+) c
учетом разбавления:
Сн
(Cr3+) =
2,667 * 1,5 * 2 / 14,0005 = 0,05715
φ = 1,36 + 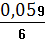
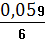 * lg
* lg 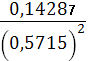
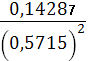 = 1,357
В
= 1,357
В
3.6.2 Построение кривой титрования
Таблица 4. Точки для построения кривой титрования по методу ОВР
|
Процент титрования
|
Потенциал, В
|
|
1% добавили от необходимого объема
|
0.2589
|
|
10% добавили от необходимого объема
|
0.228
|
|
50% добавили от необходимого объема
|
0.199
|
|
90%
добавили от необходимого объема
|
- 0.1718
|
|
99.9%
добавили от необходимого объема
|
0.1098
|
|
100%
добавили от необходимого объема
|
0.97
|
|
100.1%
добавили от необходимого объема
|
1.33
|
|
110% добавили от необходимого объема
|
1.35
|
|
150% добавили от необходимого объема
|
1.357
|
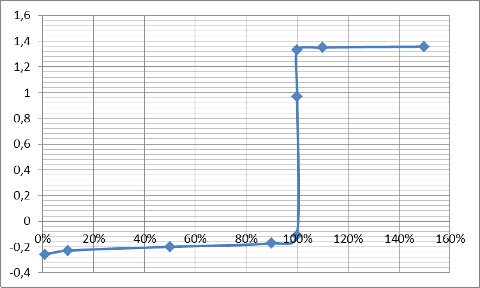
График 2. Кривая титрования 0.2 M HCOOH - 0.25 M K2Cr2O7
3.6.3 Подборка индикатора. Расчет индикаторных ошибок титрования
. Пусть φ (дифениламинсульфоновая кислота) = 0.85 < φ в точке эквивалентности, равного
0.97. Следовательно, раствор HCOOH
недотитрован.
φ = φ0 + 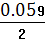
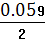 * lg
* lg 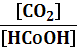
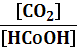
Пусть
ошибка титрования х, тогда:
,85
= -0.20 + 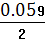
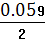 * lg
* lg 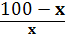
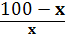
lg 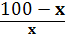
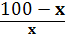 = 35.59
= 35.59
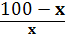
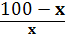 = 1035.59
= 1035.59
100
- х = 3.89 * 1035 * x
x = 2.57 * 10-34%
.
Пусть φ (n-этоксихризоидин) = 1 > φ в точке эквивалентности, равного 0.97. Следовательно,
раствор HCOOH перетитрован раствором K2Cr2O7.
φ = φ0 + 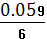
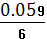 * lg
* lg 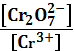
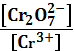
Пусть
ошибка титрования х, тогда:
=
1,36 + 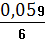
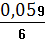 * lg
* lg 

lg 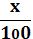
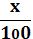 = -
36.61
= -
36.61
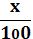
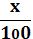 = 2.45 *
10-37
= 2.45 *
10-37
x = 2.45 * 10-35%
Вывод
С
помощью расчетов точек кривой титрования по методу ОВР кривой 0.2 M HCOOH - 0.25 M K2Cr2O7, вычислили скачок титрования, равный от - 0.1098
(99.9%) до 1.33(100.1%). С помощью расчета индикаторных ошибок, подобрали
оптимальные индикаторы. С индикатором дифениламинсульфоновой кислотой
индикаторная ошибка составила 2,57*10-34%. Со вторым индикатором
ошибка составила 2.45*10-35%. Следовательно, титровать раствор HCOOH
раствором K2Cr2O7 можно с
первым индикатором.
нейтрализация титрование йодометрия
Список литературы
1. Васильев В.П. «Аналитическая химия» в двух книгах: Кн.1:
«Титриметрические и гравиметрические методы анализа» Учеб. Для студ. ВУЗов,
обучающихся по химико-технологических спец. - 3-е издание, стереотип. - Москва:
Дрофа, 2003год - 368с.
. Гильманшина С.И. «Основы аналитической химии: курс лекций»
Доп. УМО по направлениям пед образования РФ в качестве учебного пособия для
ВУЗов\С.И.- изд. СПб, Питер 2006год-224с. (Учебное пособие)
. Крешков А.П. «Основы аналитической химии. Теоретические
основы. Количественный анализ» том №1. Издательство №3(перераб.). Учебное
пособие для студентов химико-технологических спец. ВУЗов. Москва,
химия,1970год.471с.
. Лурье Ю.Ю. «Справочник по аналитической химии» 5-е издание,
переработ. И доп. - Москва: химия,1979год-480с
. Харитонов Ю.Я. «Аналитическая химия» кн.1 «Общие
теоретические основы» Количественный анализ: Учеб. - Москва: Высшая школа.
2001год - 615с.
Похожие работы на - Построение кривой титрования по методу нейтрализации (0,15M NH4OH-0,25M H2SO4) и методу ОВ титрования (0,2M HCOOH-0,25M K2Cr2O7)