Получение 4-аминопиридина
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
1. Обзор литературы
1.1
Получение аминопиридинов
1.2 Свойства аминопиридинов
2. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
3.1 Реагенты
.2
Синтез целевых продуктов
3.2.1
Синтез 1-пиридин-4-пиридиния хлорида
.2.2
Синтез 4-аминопиридина
.2.3
Синтез 4-аминопиридина гидрохлорида
ВЫВОДЫ
СПИСОК ЛИТЕРАТУРЫ
аминопиридин синтез гидрохлорид чичибабин
ВВЕДЕНИЕ
Пиридин и его производные имеют широкое
применение в органической химии. Сам пиридин применяется в синтезе различных
красителей, как растворитель для многих органических соединений. Пиридины
служат исходным сырьем для изготовления гербицидов, инсектицидов, фунгицидов,
добавок к каучукам, взрывчатых веществ, клеев. Его производные, в частности
аминопиридины, являются основным исходным соединением для получения ряда
лекарственных средств.
-Аминопиридин является структурным фрагментом
целого ряда лекарственных веществ, применяющихся при ишемических заболеваниях
различных органов. Задачей таких препаратов является действие на рецепторы аденозина
и профилактика или лечение заболеваний сердечно-сосудистой системы
(кардиососудистых заболеваний) или воспалительных заболеваний, однако также
заболеваний мочеполовой системы, дыхательных путей, центральной нервной
системы, диабета (особенно сахарного диабета) и раковых заболеваний [1].
Препараты на основе 3-аминопиридина и
4-аминопиридина продемонстрировали некоторую клиническую эффективность в
терапии усталости при рассеянном склерозе [2].
Наибольший интерес аминопиридины проявляют в
качестве блокаторов калиевых каналов. Также их используют как анестезирующие
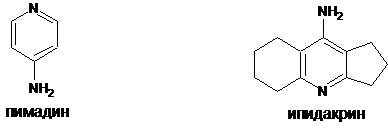
вещества при заболеваниях головного мозга [3]. На основе 4-аминопиридина
создано огромное количество преператов, для устранения мышечного паралича [4],
таких как пимадин, ипидакрин.
Соединения на основе аминопиридинов
пользуются успехом в разработке противовирусных средств. В частности,
4-аминопиридин используют для получения исходного вещества, которое является
фрагментом лекарственного средства против энтеровируса 71 типа (EV71) [5].

В виду обширной области применения,
в том числе и в фармацевтической промышленности, химия аминопиридинов является
очень актуальной для дальнейших исследований.
Целью данной курсовой работы
является синтез 4-аминопиридина.
1. ОБЗОР ЛИТЕРАТУРЫ
.1 Получение аминопиридинов
На протяжении некоторого периода времени
основным способом получения 2-аминопиридина служила реация Чичибабина -
аминирование пиридина амидом натрия, для получения 3- и 4-аминопиридинов
проводили аммонолиз соответствующих 3- и 4-галогенпиридинов [6]:
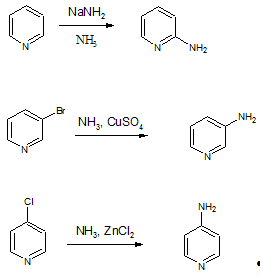
Галогензамещенные пиридины в наше время являются
эффективным источником получения аминопиридинов.
Синтез 4-аминопиридина возможен путем
перекрестного сочетания 4-хлорпиридина с аллил- или N,N-диаллиламином,
катализируемого палладием, с последующем отщеплением аллила [7].

Аминопиридины также можно получить и
из различных арилгалогенидов взаимодействием с водным раствором аммиака и в
присутствии катализатора Cu2O. Этот способ предпочтителен тем, что
нет необходимости в использовании атмосферы инертного газа, дорогостоящих
катализаторов и лигандов, безводных растворителей, а также дополнительных оснований
или других добавок [8].
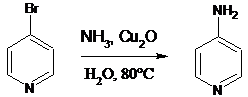
Легко можно получить аминопиридины
взаимодействием галогенпиридинов с аммиаком, при добавлении этиленгликоля. Под
действием оксида меди (I), в качестве катализатора, реакция
происходит быстро и с высокими выходами(85%) [9].

Также, очень актуальным является
использование различных N-оксидов. В литературе встречается
множество способов получения аминопиридинов в следствии явлений
деоксигенирования и восстановления N-оксидов.
Существует система реагентов
LiCl/NaBH4 для получения аминопиридинов путем деоксигенирования
N-оксидов. Эта реакция очень важна и заслуживает особого внимания [10].
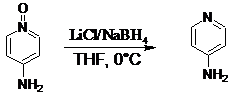
Исследователи Варшавского института
органического синтеза при изучении способа снижения активности N-оксидной
группы в N-оксо-4-нитропиридине обнаружили, что использование различных мольных
отношений в системе реагентов TiCl4/SnCl2 приводит к
получению разных продуктов. Так, например, использование системы TiCl4/SnCl2
(1:2) приводит к образованию 4-аминопиридина с высоким выходом (95%) [11].
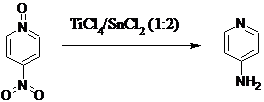
Другие исследования показали, что
получение 4-аминопиридина из N-оксо-4-нитропиридина возможно и с использованием
катализаторов для мягкого, селективного деоксигенирования гетероароматических
N-оксидов в нейтральной среде [12].

Реакции с азидопиридинами, которые
приводят к образованию аминопиридинов, обычно характеризуются высоким выходом и
качеством конечного продукта.
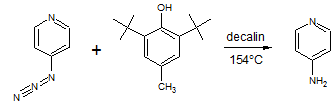
В жестких условиях происходит
реакция пиролиза 4-азидопиридина с образованием 4-аминопиридина. В результате
взаимодействия с 2,6-дитретбутил-4-метил-фенолом в растворе декалина при
высоких температурах получается 4-аминопиридин с достаточно высоким выходом
[13].
Из этого же соединения, но в более
мягких условиях, также можно получить 4-аминопиридин. В результате реакции
фотолиза в гидрогалогеновых кислотах получается смесь продуктов
(4-аминопиридини и 3-амино-4-галогенпиридин), которую потом придется разделять
[14].

Получить аминопиридины можно также
нагреванием 4-гидроксикарбомоилпиридина с формамидом при высоких температрурах
в течение 20 часов. Эта реакция интересна тем, что процесс всегда идет
стабильно с высокой чистотой продукта и хорошим выходом [15].

Особого внимания заслуживает
твердофазный синтез с помощью перегруппировки Курциуса. Ключевой особенностью
является перегруппировка гетероарилкарбоновых кислот с последующим
N-алкиллированием и взаимодействием с гидридом натрия. В результате получаются
гетероарриламины с высоким выходом (95%) [16].
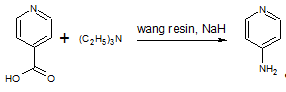
Не менее интересно взаимодействие
N-бензиламинопроизводных с цинковой пылью в растворе формиата аммония.
Селективное удаление защитной группы проходит под действием микроволнового
излучения. В результате реакции образуются соответствующие амины с высоким
выходом (95%) [17].
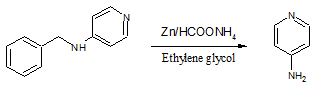
Вопреки мнению некоторых авторов,
4-аминопиридин может быть получен по методу Кенигса и Гренье, при добавления
избытка щелочи к реакционной смеси, из которой и выделяют 4-аминопиридин [18].
Процесс очень трудоемкий и проводится количественно.
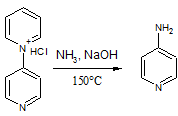
Аминопиридины также образуются в
результате расщепления сульфониламидов. Этот метод очень актуален в наше время
из-за неприхотливости реакции, её быстроты и отсутствия дорогих реагентов.
Нагревание в соляной кислоте приводит к разрушению связи S-N и образованию
готового продукта [19].
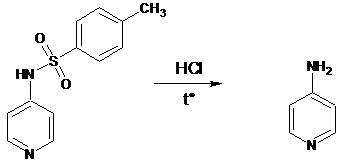
Разрушение R-пиридин-карбаматов
также приводит к образованию аминопиридинов. Этой реакции следует уделить
большое внимание, т.к. в результате превращения образуется чистый продукт с
высоким выходом (97%). Реакция идет быстро, количественно и без нагревания. Это
способ является одним из наиболее оптимальных для получения аминопиридинов
[20].
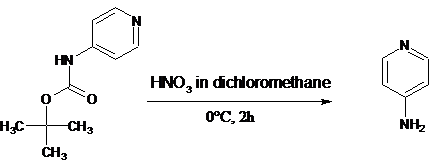
1.2 Свойства аминопиридинов
Аминопроизводные пиридина обладают более
сильными основными свойствами, чем пиридин и анилин. Они содержат в своем
составе два основных центра - атом азота пиридинового типа и атом азота
аминогруппы.
- и 4-Аминопиридины способны к таутомерному
превращению соответственно в 2- и 4-пиридонимины, однако, в обычных условиях
находятся в основном в аминной форме, например:

Моноаминопиридины обладают многими
свойствами первичных аминов. При взаимодействии 2-аминопиридина с алкилирующими
агентами (алкилгалогенидами, алкилсульфатами или диазометаном) алкилируется в
первую очередь кольцевой атом азота. В присутствии NaNH2 образуется
2-алкиламинопиридин.
Дальнейшим
алкилированием получают диалкиламинопиридины [21].

Существенное различие в химических
свойствах изомерных моноаминопиридинов проявляется в их реакциях с HNO2:
3-аминопиридин диазотируется с образованием солей диазония, 2- и
4-аминопиридины образуют в слабокислом растворе гидроксипиридины (пиридоны)
[22].
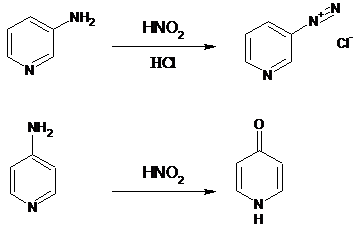
Соли диазосоединений из
2-аминопиридина получают по реакции [23]:
Моноаминопиридины реагируют с
сильными электрофилами. Аминогруппа компенсирует дезактивирующий эффект атома
азота пиридина и ориентирует замещение в кольце. Если аминогруппа находится в
положении 2, 3 или 4, то электрофильное замещение происходит соответственно в
положения 5, 2 или 3 (5). При действии на 2-аминопиридин нитрующей смеси
образуется нитрамин, который в присутствии H2SO4
изомеризуется в смесь 5-нитро- и 3-нитро-2-аминопиридинов с выходами соответственно
80 и 10% [24]:

Особого внимания заслуживает
взаимодействие аминопиридинов с трифенилфосфином в присутствии
диэтилазодикарбоксилата. Реакция служит эффективным способом синтеза
арилиминофосфоранов. Процесс протекает при обычных условиях и комнатной
температуре [25].
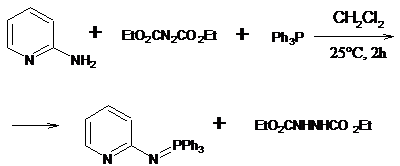
Для аминопиридинов характерны
свойства как аминов, так и гетероциклических соединений, ввиду этого, они
обладают большим синтетическим потенциалом, что позволяет применять их в
качестве исходных веществ для синтеза широкого круга соединений.
2. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Целью данной работы является
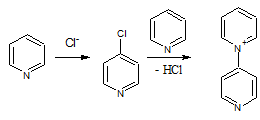
получение 4-аминопиридина. Нами был осуществлен трехстадийный синтез по схеме:
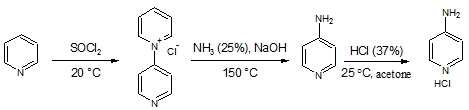
На первой стадии нами была проведена
реакция взаимодействия пиридина и тионилхлорида. Нам было интересно получить
именно такую соль пиридин-пиридиния, т.к. она служит прекрасным исходным
продуктом для дальнейшего синтеза. Реакционную смесь выдерживали в течении 3
суток при комнатной температруре, затем из неё отгоняли избыток тионилхлорида.
Полученный осадок очищали посредством перекристаллизации. Выход чистого
продукта составил 3,5 г (31% от теоретического). Высокие потери, по всей
видимости, связаны с ненадлежащим товарным качеством соляной кислоты,
применяемой для очистки целевого продукта. Т. пл. = 148-149 °С.
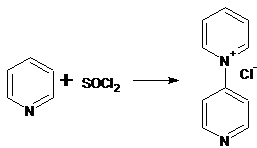
Механизм этой реакции до сих пор
выяснен не до конца. Рассмотрим вариант предполагаемого механизма
(нуклеофильного замещения Sn1).
На первом этапе проходит диссоциация
тионил хлорида с образованием нуклеофила Cl-:

На втором этапе, образовавшийся
нуклеофил атакует пиридин в четвертое положение, с последующим замещением на
пиридин:
На второй стадии синтеза нами была
проведена реакция взаимодействия получившийся соли пиридин-пиридиния
гидрохлорида и водного раствора аммиака. Согласно методике [18], для получения
4-аминопиридина, реакционную смесь, содержащую соль пиридин-пиридиния и раствор
аммиака, нужно нагревать в течение 8 часов в автоклаве. Мы предприняли попытку
осуществить данное взаимодействие при атмосферном давлении. В результате
кипячения смеси с избытком аммиака в течение 10 часов были получены
желтовато-белые кристаллы 4-аминопиридина. Т.пл. = 155-157 °С. ИК спектр (KBr),
см-1: 3448 - первичные амины (-NH2), 1604 -
ароматические соединения. Выход составил 28%. Низкий выход реакции обусловлен
потерей аммиака.
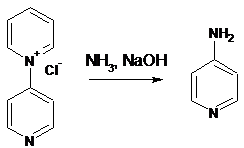
Реакция проходит по механизму
нуклеофильного замещения - Sn1. На первом
этапе нуклеофил (OH-) атакует
соль пиридин-пиридиния с последующим отщеплением катиона пиридиния. Затем,
молекула аммиака замещает гидроксильную группу на амино-группу с образованием
4-аминопиридина.
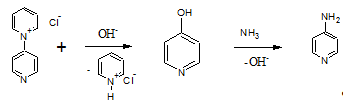
Третья стадия нашего синтеза -
перевод 4-аминопиридина в форму гидрохлорида. Для этого мы растворили
4-аминопиридин в ТГФ, смешали с концентрированной соляной кислотой и
перемешивали в течение 1 часа при комнатной температуре. В результате
образовался белый осадок. Полученную соль фильтровали, промывали и сушили.
Выход составил 95%.
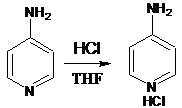
Реакция проходит по механизму:

Нами был проведен синтез целевого
продукта с общим выходом 8%.
3. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
.1 Реагенты
|
Название
|
Формула
|
Масса,
г
|
Объем,
мл
|
Количество
вещества, моль
|
|
Пиридин
|
С5H5N
|
-
|
10
|
0.032
|
|
Тионилхлорид
|
SOCl2
|
-
|
18.3
|
0.0184
|
|
Соляная
кислота
|
HCl
|
-
|
10
|
0.370
|
|
Метанол
|
CH3OH
|
-
|
7
|
0.027
|
|
Аммиак
|
NH3
|
-
|
18.5
|
0.420
|
|
Гидроксид
натрия
|
NaOH
|
1.65
|
-
|
0.036
|
|
Бензол
|
C6H6
|
-
|
16.5
|
0.028
|
|
Толуол
|
C7H9
|
-
|
10
|
.2 Синтез целевых продуктов
.2.1 Получение 1-пиридин-4-пиридиния
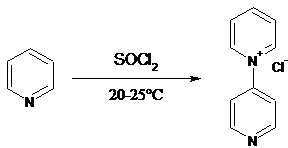
В трёхгорлой колбе, емкостью 250 мл,
снабженной капельной воронкой, мешалкой, обратным холодильником, при энергичной
работе мешалки смешивают 10 мл (0,032 моль) сухого пиридина и 30 г (0,0184
моль) тионилхлорида (технического продукта), поддерживая 20°C.
После полного прибавления
тионилхлорида реакционная смесь оставляется при комнатной температуре на 3 дня.
Затем, тионилхлорид отгоняется в вакууме, причем температура водяной бани
постоянно повышается до кипения, и при этой температуре содержимое колбы
выдерживается дополнительно 2 часа.
Оставшийся в колбе сухой остаток при
кипячении примерно с 7 мл сухого метанола превращается в гомогенную
кристаллическую кашу, которую отсасывают после охлаждения до 0°C. Промытый
небольшим количеством спирта сырой продукт после высушивания при 110°С имеет
температуру плавления 145-148°С. Для дальнейшей очистки сырой продукт
растворяют в небольшом количестве 2н HCl, отфильтровывают и обрабатывают
фильтрат активным углем несколько раз. После упаривания в вакууме и прибавления
спирта выделяются почти белые кристаллы, которые после охлаждения отсасывают и
высушивают. Окончательная перекристаллизация из метанола дает почти бесцветные
кристаллы с температурой плавления 151°С. Выход 3,5г (31% от теоретического).
.2.2 Получение 4-аминопиридина

Сырой хлорид пиридил-пиридиний (3,5
г (0,016 моль)) нагревают в течение 8 часов до 150°С с 18,5 мл (0,42 моля)
25%-ого раствора аммиака. Затем, к реакционной массе добавляют 1,16 (0,036
моль) г твердого гидроксида натрия, после чего смесь выпаривают на водяной
бане, не досуха (при полном испарении наблюдаются потери 4-аминопиридина из-за
сублимации).
Остаток экстрагируют 16,5 мл
бензола, через 2 дня извлекается вещество. Из раствора бензола получаются
твердые, бледно-коричневые кристаллы.
При перекристаллизации из толуола
получают 0,9 г чистого 4-аминопиридина с температурой плавления 155-157°С.
Продукт образует ярко-белые кристаллы с выходом 28% в расчете на хлорид пиридин-пиридиния.
3.2.3 Получение гидрохлорида
4-аминопиридина
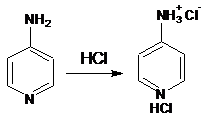
0,9 г 4-Аминопиридина перемешивают с
10 мл 37% соляной кислоты в растворе ТГФ (15 мл) при комнатной температуре в
течение 1 часа. После чего соль отфильтровывают, сушат. В результате образуется
0,85 г (95%) белого осадка.
ВЫВОДЫ
1) Нами был проведен литературный
обзор по теме "Получение аминопиридинов и их химические свойства".
) Проведен синтез 4-аминопиридина с
выходом 28%.
) Строение этого соединения было подтверждено
методом ИК-спектроскопии и соотнесением полученных физических свойств с
литературными данными.
СПИСОК ЛИТЕРАТУРЫ
1. Smith,
D. T.; Shi, R.; Borgens, R. B.; McBride, J. M.; Jackson, K.; Byrn, S. R. //
European Journal of Medicinal Chemistry; vol. 40; nb. 9; (2005); p. 908 - 917
. Gilbert,
I. H.; Mital, A.; Murugesan, D.; Campbell, M.; Charman, S. A.; Katneni, K.;
Morizzi, J.; Shackleford, D. M.; Kaiser, M.; Yeates, C.; Hudson, A. // Journal
of Medicinal Chemistry; vol. 56; nb. 7; (2013); p. 2975 - 2990
. M.
Okamoto, T. Katanashi, Y. Takimoto // Analytical chemistry, 1997, 2019-2021
. Z.Dega-Safran,
A. Kania, B. Nowak-Wyadra, M Safran // J.Mol.Struct, 1994, 232-234
. Chih-Shiang
Chang, Ying-Ting Lin, Shin-Ru Shih, Chung-Chi Lee, Yen-Chun Lee, Chia-Liang Tai
// Journal of Biotechnology and Pharmaceutical Research, 2003, 54-57
6. Jaime-Figueroa, Saul; Liu, Yanzhou; Muchowski, Joseph
M.; Putman, David G. // Tetrahedron Letters, 1998 , vol. 39, # 11 p. 1313 -
1316
7. Ram, S. Raja; Chary, K. Purushothama; Iyengar, D. S. //
Synthetic Communications, 2000 , vol. 30, # 19 p. 3511 - 3516
8. Kaczmarek, Lukasz; Balicki, Roman; Malinowski, Marek. //
Journal fuer Praktische Chemie (Leipzig), 1990 , vol. 332, # 3 p. 423-424
9. Balicki, Roman; Kaczmarek, Lukasz. // Gazzetta Chimica
Italiana, 1994 , vol. 124, # 9 p. 385 - 386
10. Xu, H.; Wolf, C. // Chemical Communications (Cambridge,
United Kingdom), 2009 , p. 3035 - 3037
11. Dyall, L. K.; Wah, W. // Australian Journal of Chemistry,
1985 , vol. 38, # 7 p. 1045 - 1059
12. Sawanishi, H.; Hirai, T. // Tsuchiya, Takashi
Heterocycles, 1982 , vol. 19, # 6 p. 1043 - 104
13. Eckstein, Z.; Lipczynska-Kochany, E.; Krzeminski, J. //
Heterocycles, 1983, vol. 20, # 10 p. 1899 - 1901
14. Sunami, S; Sagara, T; Ohkubo, M; Morishima, H. //
Tetrahedron Letters, 1999 , vol. 40, # 9 p. 1721 - 1724
15. Babu, S. N. Narendra; Gowda, D. Channe; Lakshmi. //
Srinivasa Synthetic Communications, 2004 , vol. 34, # 10 p. 1831 - 1837
16. Wibaut et al. // Recueil des Travaux Chimiques des
Pays-Bas, 1954 , vol. 73, p. 140
17. Solekhova,
M. A.; Kurbatov, Yu. V. // Russian Journal of Organic Chemistry; vol. 38; nb.
8; (2002); p. 1192 - 1194
. Strazzolini,
P; Melloni, T; Giumanini, A. G. // Tetrahedron; vol. 57; nb. 43; (2001); p.
9033 - 9044
19. Lang, F.; Zewge, D.; Houpis, I. N.; Volante, R. P. // Tetrahedron Letters; vol. 42; nb. 19;
(2001); p.3251 - 3254
20. Huisgen,
R. In The Adventure Playground of Mechanisms and Novel reactions: Profiles,
Pathways and Dreams; Seeman, J. I., Ed. // American Chemical Society:
Washington, DC, 1994; p 62;
21. Huisgen,
R.; Blaschke, H.; Brunn, E. // Tetrahedron Letters, 1966, p.
405-409;
. Brunn,
E.; Huisgen, R. Angew. // Chem., Int. Ed. Engl.
1969, 8, 513-515
. Mitsunobu,
O.; Yamada, Y. Bull. // Chem. Soc. Jpn. 1967, 40, 2380-2382.
24. Lu,
X.; Petersen, J. L.; Wang, K. K. // J. Org. Chem.
2002, 67, 7797-7801
. Alonso,
E.; Ramon, D. J.; Yus, M. // Tetrahedron, 2002, 42, 355-368.