Основные вопросы химии
Чему равен при н.у. эквивалентный объём
водорода?
Вычислите эквивалентную массу металла, если на
восстановление 1,017г. его оксида израсходовалось 0,28л водорода (н.у.). Ответ:
32,68г/моль.
эквивалентный
молекулярный гидролиз соль
mMeO = vH2
mэ(MeO)
vmэ(H2)
vmэ(H2)
= 22,4 : 2 = 11,2л
mэ(MeO) = =
40,68г/моль
mэ(Me)
= mэ(MeO)
- mэ
(O2)
40,68 - 8 = 32,68 г/моль
Изотоп никеля-57 образуется при бомбардировке α-частицами
ядер атомов железа-54.
Составьте уравнение этой ядерной реакции и
напишите его в сокращённой форме
54
Fe + 4He → 57Ni + 1n 54 Fe (α,
n) 57Ni
26 2 28 0
Составьте формулы оксидов и гидроксидов
элементов третьего периода периодической системы, отвечающих их высшей степени
окисления. Как изменяется кислотно-основной характер этих соединений при переходе
от натрия к хлору? Напишите уравнения реакций, доказывающих амфотерность
гидроксида алюминия.
Изменение химического характера оксидов и
гидроксидов элементов 3 периода
Таблица
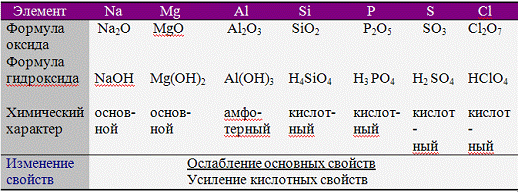
В первой из приведенных ниже реакций Al(OH)3
реагирует как обычное основание, а в следующих - как кислота:
Al(OH)3 + 3 H2SO4
= Al2(SO4)3 + 6 H2O.
Al(OH)3 H3AlO3
+ NaOH = NaH2AlO3 + H2O,
Al(OH)3 + NaOH = NaAlO2 +
2 H2O (при сплавлении);(OH)3 + NaOH = Na[Al(OH)4]
(при добавлении раствора NaOH без нагревания)
Таким образом, амфотерные гидроксиды
взаимодействуют как с растворами кислот, так и с растворами щелочей.
Сколько неспаренных электронов имеет атом хлора
в нормальном и возбуждённом состояниях? Распределите эти электроны по квантовым
ячейкам. Чему равны валентность хлора, обусловленная неспаренными электронами?
Последовательное возбуждение электрона из трех
пар в атоме хлора на незанятые энергетические состояния в d
- подуровне позволяет повысить валентность его от 1 до 3, 5 и 7.
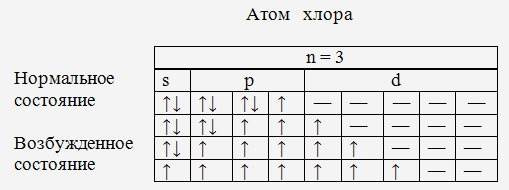
Рис.
Тепловой эффект какой реакции равен теплоте
образования NO?
Вычислите теплоту образования NO,
исходя из следующих термохимических уравненений:
NH3(г)
+ 5 O2
(г) = 4 NO (г) + 6 H2O
(ж); Δ
H = -1168,80 кДж.
NH3(г)
+ 3 O2
(г) = 2 N2(г)
+ 6 H2O
(ж); Δ
H = 1530,28 кДж.
Ответ: 90,37 кДж.
Тепловой эффект прямой реакции всегда равен
тепловому эффекту обратной реакции с противоположным знаком.
Реакция N2 (г.) + О2 (г.)
= 2NО (г.) - 180,7 кДж эндотермическая
Q = ΔH
= +90,37кД
NH3(г)
+ 3 O2
(г) = 2 N2(г)
+ 6 H2O
(ж)
NH3(г)
+ 5 O2
(г) = 4 NO (г) + 6 H2O
(ж)
2 O2
(г) = 2 N2(г)
- 4NO(г)
2 O2
(г) - 2 N2(г)
+ 4NO(г) = 1530,28 - (-
1168,80) = 2699,08
4NO(г)
= 2699,08(г) = 90,37
Δ
H NO = 90,37 кДж.
H2(г)
+ СO2
(г) = СО(г) + H2O
(ж); Δ
H = -2,85 кДж.?
Зная тепловой эффект реакции и абсолютные
стандартные энтропии соответствующих веществ, определите Δ
Gº298
этой реакции.
Ответ: +19,91 кДж.
H2(г)
+ СO2
(г) = СО(г) + H2O
(ж); Δ
H = -2,85 кДж.?
ΔGo
= ΔHo
-
TΔSo
ΔHoх.р=
∑ΔHопрод.
- ∑ΔHoисх.
ΔS
oх.р=
∑ ΔS
опрод. - ∑ΔSoисх.
ΔHoх.р=
-110,52 - 285,84 - (-393,51) =-2,85кДж;
ΔS
oх.р=
(197,91 + 69,94) - (213,65 +130,59) = -76,39 = 0,07639кДж/(моль∙ К);
ΔGo
=-2,85 + 298 ∙ 0,07639 = 19,91 кДж.
Так как ΔGo
>
0, то реакция при стандартных условиях невозможна.
Вычислите, во сколько раз уменьшится скорость
реакции, протекающей в газовой фазе, если понизить температуру от 120 до 80ºС.
Температурный коэффициент скорости реакции 3.
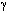 =
= 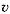 T+10/
T+10/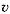 T.
T.
При повышении температуры от T до T'
отношение скоростей реакций 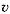 T' и
T' и 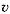 T равно
температурному коэффициенту скорости в степени (T' - T)/10:
T равно
температурному коэффициенту скорости в степени (T' - T)/10:
T'/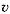 T =
T = 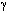 (T'-T)/10.
(T'-T)/10.
vT2 = vT1 γ = = -4 vT2 = vT1 3-4
= vT1 = ;
Скорость реакции уменьшится в 81раз.
Сколько и какого вещества останется в избытке,
если к 75 см3 0,3н раствора H2SO4
прибавить 125 см3 0,2н. раствора KOH?
Ответ: 0,14 г
KOH.
2SO4
+ 2KOH = K2SO4 + 2H2O
Количества эквивалентов: n(H2SO4)
= 0,3 ∙ 75/1000 = 0,0225;(KOH) = 0,2 ∙ 125/1000 = 0,025.
Эквивалентная масса КОН - 56 г/моль
Тогда масса оставшегося в избытке КОН равна:
0,0025 ∙ 56 = 0,14 г
Вычислите мольную массу неэлектролита, зная, что
раствор, содержащий 2,25г этого вещества в 250г воды, кристаллизуется при
-0,279ºС. Криоскопическая
константа воды 1,86º.
Ответ: 60 г/моль.
Δt
= 0 - (-0,279) = 0,279
m = = 9
= K = = 60
Составьте молекулярные и ионно - молекулярные
уравнения реакций взаимодействия в растворах между а) CuSO4
и H2S;
б) BaCO3 и
HNO3;
в) FeCl3 и
KOH.) CuSO4 + H2S = CuS + H2SO4
Cu2+ + H2S =
CuS + 2H+
б) BaCO3
<#"661109.files/image005.gif"> NaOH + NaHS
2 Na+ + S2- + H2O 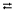 Na+
+ OH- + Na+ + HS- S2- + H2O
Na+
+ OH- + Na+ + HS- S2- + H2O
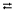 OH-
+ HS- II: NaHS + H2O
OH-
+ HS- II: NaHS + H2O 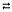 NaOH + H2S
NaOH + H2S
Na+ + HS-
+ H2O
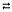 Na+
+ OH- + H2S HS- + H2O
Na+
+ OH- + H2S HS- + H2O 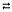 OH-
+ H2S
OH-
+ H2S
Гидролиз хлорид алюминия AlCl3:
Первая ступень:
а) Al3+
+ HOH 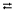 AlOH2+
+ H+;
AlOH2+
+ H+;
б) Al3+
+ 3Сl-
+ H2O 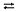 AlOH2+
+ 2Сl-
+ H+ + Сl-;
AlOH2+
+ 2Сl-
+ H+ + Сl-;
в) AlCl3
+ H2O 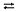 AlOHCl2
+ HCl.
AlOHCl2
+ HCl.
Вторая ступень:
а) AlOH2+ + H2O 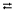 Al(OH)2+
+ H+
Al(OH)2+
+ H+
б) AlOH2+ + 2Сl- + H2O 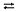 Al(OH)+2+
Сl- + H+ + Сl-;
Al(OH)+2+
Сl- + H+ + Сl-;
Итак, в растворе [Н+]
> [ОН-] pH < 7.
NiSO4 гидролизуется по катиону, поэтому в
растворе избыток катионов водорода H+, среда кислая, и pH<7.
гидролиз по первой ступени:
Ni 2+
+ SO42- + HOH 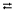 Ni(OH)+ + SO42-
+ H+ Ni2+ + HOH
Ni(OH)+ + SO42-
+ H+ Ni2+ + HOH 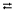 Ni(OH)+ + H+
2 NiSO4 + 2H2O
Ni(OH)+ + H+
2 NiSO4 + 2H2O 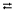 (NiOH)2SO4 +
H2SO4
(NiOH)2SO4 +
H2SO4
по второй ступени (практически не
идёт без условий):
(OH)+
+ SO42- + HOH 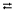 Ni(OH)2↓ + SO42-
+ H+ Ni(OH)+ + HOH
Ni(OH)2↓ + SO42-
+ H+ Ni(OH)+ + HOH 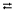 Ni(OH)2↓ + H+
(NiOH)2SO4 + 2H2O
Ni(OH)2↓ + H+
(NiOH)2SO4 + 2H2O  2 Ni(OH)2↓
+ H2SO4
2 Ni(OH)2↓
+ H2SO4