Люминесцентные свойства нанопорошков состава EuxAlyOz, синтезированных золь-гель методом
МИНИСТЕРСТВО
ОБРАЗОВАНИЯ РЕСПУБЛИКИ БЕЛАРУСЬ
Учреждение
образования
«Гомельский
государственный университет
имени
Франциска Скорины»
Физический
факультет
Кафедра
радиофизики и электроники
Люминесцентные
свойства нанопорошков состава, синтезированных золь-гель методом
Курсовая
работа
Исполнитель:
студент группы Ф-41
Хорошкевич А.В.
Научный
руководитель:
кандидат
физико-математических
наук, доцент
Мышковец В. Н.
Гомель
2011
Реферат
Курсовая работа содержит 24 страницы, 3
рисунков, 28 литературных источников
Ключевые слова: лантаниды, оксиды европия и
алюминия, люминесценция, спектр, порошки, золь-гель метод
Объект исследования: порошки оксидного
соединения EuxAlyOz
Методы исследования: сравнение теоретических и
экспериментальных данных
Цель работы: изучение спектров люминесценции
сложного оксида EuxAlyOz
Содержание
Введение
1.
Люминесцентные свойства европия в сложных соединениях. Влияние алюминия на
люминесцентные свойства редкоземельных металлов
.1
Усиление люминесценции редкоземельных металлов в присутствии алюминия
.2
Люминесцентные свойства европия в составе различных комплексных соединений
.3
Люминесцентные свойства Eu3+-Al-cодержащих комплексных соединений
.
Получение порошков оксида EuxAlyOz
.1
Физико-химические методы получения нанопорошков
.2
Получение порошка оксида EuxAlyOz
.
Спектры люминесценции EuxAlyOz
Заключение
Список
использованной литературы
Введение
Актуальность темы курсовой работы определяется
все более широким применением материалов на основе соединений лантанидов в
различных областях науки и техники и возрастающей ролью оптической
спектроскопии в их исследовании и разработке. Решаемые в работе задачи связаны
с поиском способов синтеза сложных оксидных соединений лантанидов с другими
металлами, преимущественно для квантовой и молекулярной электроники.
Интерес физиков и химиков к соединениям
лантанидов не ослабевает на протяжении нескольких десятилетий, начиная с
момента основания атомной промышленности (экстракция и разделение металлов), а
позднее - со времени рождения квантовой электроники. Многочисленные
исследования координационных соединений лантанидов связаны с их использованием
в качестве сдвигающих реагентов в ЯМР спектроскопии при исследовании структуры
органических молекул [1-4], в аналитической химии, фармакологии, биологии,
медицинской диагностике [5-8], для мониторинга окружающей среды [9, 10], для
развития методов "зеленой химии" [11]. Начиная с 70-х годов прошлого
века ионы лантанидов стали применять в качестве метки для исследования их взаимодействия
с комплексонами, аминокислотами, макромолекулярными лигандами, а также для
изучения биологически активных систем, в которых ионы Ln3+ способны
функционально и изоструктурно замещать ионы кальция [4, 12-15]. Характеристики
соединений, необходимые для применений в иммунолюминесцентном анализе,
микроскопии с разрешением по времени, медицинской ЯМР диагностике, обсуждаются
в обзорах [5, 16].
1. Люминесцентные свойства европия в сложных
соединениях. Влияние алюминия на люминесцентные свойства редкоземельных
металлов
.1 Усиление люминесценции редкоземельных
металлов в присутствии алюминия
В работе [17] исследована зависимость
интенсивности люминесценции от концентрации коактиватора (Al) в соединении
SrTiO3:Pr3+:Al. Люминесцентный материал SrTiO3, активированный празеодимом Pr,
имеет красный цвет свечения, но обладает малой эффективностью люминесценции и
поэтому не находит практического применения. В тоже время, если в качестве
добавки в этот фосфор вводить ионы III-b группы, такие, например, как Al или
Ga, то эффективность люминесценции при фото- и электронном (низковольтным
катодном) возбуждении в значительной степени повышается. Считается, что такие
эффективные фосфоры SrTiO3:Pr3+:Ga, SrTiO3:Pr3+:Al и SrTiO3:Pr3+:Al,Ga,
обладающие красным цветом свечения, являются весьма перспективными материалами
для использования их в качестве люминесцентных слоёв для вакуумных
люминесцентных дисплеев и дисплеев с автоэлектронной (полевой) эмиссией. А так
как эти фосфоры при возбуждении в фундаментальную область являются и весьма
эффективными фотолюминофорами красного цвета свечения, то они могут найти
применение при производстве миниатюрных люминесцентных ламп и других устройств,
основанных на фотовозбуждении, поэтому исследования их фотолюминесцентных
свойств представляют и самостоятельный интерес.
Ясно, что введение в SrTiO3 других
редкоземельных активаторов может привести к созданию необходимой цветовой
гаммы, а следовательно, и номенклатуры материалов, удовлетворяющих
разработчиков полноцветных
плоских
дисплеев. Однако для решения такой проблемы прежде всего необходимо выяснить
роль коактиватора и причины, приводящие к значительному усилению люминесценции
при возбуждении основания кристаллофосфора прежде всего для ставшего уже
классическим SrTiO3:Pr3+:Al.
В другой работе [18] исследованы ИКЛ и ФЛ
компактов и керамических матриц Al2O3, SiO2, а также композита SiO2/ZnO,
полученных из наноразмерных порошков. Обнаружена интенсивная люминесценция
метастабильных форм наноструктурного Al2O3 в широком спектральном диапазоне, что
открывает перспективу создания на их основе люминофоров белого света.
Установлена зависимость спектров ИКЛ от фазового состава Al2O3. Показано, что
наноструктурная матрица α- Al2O3
характеризуется интенсивным свечением в красной области спектра, а керамический
композит SiO2/ZnO, синтезированный из нанопорошков, является эффективным
катодолюминофором с зеленым свечением. Проведенные исследования свидетельствуют
о возможности создания люминофоров с высоким световым выходом на основе
наноразмерных оксидов алюминия и кремния.
Методом золь-гель синтезированы легированные
тербием слои ксерогеля оксида алюминия в порах пленки пористого анодного оксида
алюминия толщиной 1 мкм с диаметром пор 150−180 нм, выращенной на кремнии
[19]. В данной работе приведены результаты исследования спектров фото- и
рентгенолюминесценции (РЛ), а также импульсной катодолюминесценции (ИКЛ)
структур, сформированных на основе пленок пористого анодного оксида алюминия на
кремнии, содержащих в порах легированный тербием ксерогель оксида алюминия и
ксерогель, соответствующий составу алюмоиттриевого граната.
Сформированные структуры демонстрируют
фотолюминесценцию тербия с характерными полосами, соответствующими термам
трехвалентного тербия. Впервые обнаружена рентгенолюминесценция тербия для
подобной структуры с наиболее интенсивной полосой излучения при 542 нм. Таким
образом, продемонстрирована принципиальная возможность создания наноразмерного
матричного люминесцентного преобразователя ионизирующих излучений в видимое.
Матричная структура преобразователя получена
методом золь-гель, используя синтез легированного тербием ксерогеля оксида
алюминия в матрице пористого анодного оксида алюминия. Следует учесть также,
что метод золь-гель позволяет осуществить легирование ксерогеля тяжелыми элементами,
например стронцием или лютецием, а выбор режимов анодирования обеспечивает
возможность для последующей оптимизации структуры мезопористой матрицы.
.2 Люминесцентные свойства европия в составе
различных комплексных соединений
Сенсибилизированная люминесценция (СЛ) европия
(III) и тербия (III) в их комплексах с различными лекарственными препаратами
эффективно используется для определения последних. В качестве аналитических
форм для определения лагандо-сенсибилизатора люминесценции центрального иона применяют
однородно- и разнолагидные комплексы.
Наиболее важную роль в биохимических
исследованиях отводится ионам европия (III) и тербия (III), для которых
энергетические зазоры между низшим излучательном уровнем и основным состоянием
обеспечивают наиболее высокую интенсивность люминесценции.
В работе [20] изучались люминесцентные свойства
кристаллов CaGa2Se4:Eu. Одним из малоизученных соединений в системе M-Ga -
S(Se) является CaGa2Se4. Соединение CaGa2Se4 кристаллизуется в
псевдо-орторомбической подрешетке при одновременном существовании двойникования
и сверхструктуры. О кристаллической структуре и некоторых физических свойствах
(электропроводность, удельное сопротивление) этого соединения сообщается в
некоторых работах. Однако, нет подробной информации о люминесцентных свойствах
CaGa2Se4. Представляет интерес исследование люминесцентных свойств кристаллов
CaGa2Se4 активированных ионами редкоземельных элементов как с точки зрения
выяснения механизма фотолюминесценции, так и с точки зрения их практического
применения. Для этой цели были получены кристаллы CaGa2Se4, активированные
ионами Eu2+.
Таким образом, активирование кристаллов CaGa2Se4
ионами Eu2+
приводит
к возникновению в них широкополосный интенсивный люминесценции связанный с
внутрицентровыми переходами 4f65d -4f7(8S7/2) ионов Eu2+. Исследование ТЛ
позволяет определить глубину залегания ловушек: 0,31; 0,44; 0,53 и 0,59 эВ.
В работе [21] Синтезированы и изучены
фотофизические характеристики (электронные спектры поглощения и спектры
фотолюминесценции)(ацетилацетонато)фталоцианина европия Eu(acac)Pc и
(оксихинолинато)фталоцианина европия Eu(q)Pc, различающиеся аксиальными
лигандами.
Целью работы явилось сравнительное изучение
спектральных характеристик растворов (ацетилацетонато)фталоцианина европия Eu(acac)Pc
(1) и (оксихинолинато)фталоцианина европия Eu(q)Pc (2) и выявление влияния
объемных аксиальных лигандов
Комплексные соединения фталоцианинов лантаноидов
отличаются разнообразием архитектурных типов: моно-, ди- и трисфталоцианинов.
Особенностью монофталоцианиновых комплексов является наличие в координационной
сфере комплекса как фталоцианинового лиганда, так и дополнительного
экстралиганда различной химической природы. Сочетание в одной молекуле иона
лантаноида, жесткого планарного фталоцианинового макрогетероцикла с различными
экстралигандами открывает путь изменения спектральных характеристик, управления
рядом физико-химических свойств и, следовательно, областью потенциального
применения. При этом экстралиганды должны существенно влиять и на саму геометрию
комплексов. Изменение дизайна соединения в свою очередь сказывается и на их
фотофизических и фотохимических свойствах. Фталоцианиновые комплексы
редкоземельных элементов привлекают внимание многих исследователей благодаря
важным для практического использования свойствам: спектральным, электрохромным,
полупроводниковым и др. Интерес к таким соединениям в настоящее время только
растет. Очевидна актуальность исследования, когда в качестве экстралигандов
выступают молекулы оксихинолина. Комплексы оксихинолинатов металлов прекрасно
зарекомендовали себя способностью к пере носу заряда, большой подвижностью
дырок в процессах переноса энергии. На примере исследования люминесценции смеси
свободного фталоцианинового лиганда и трис(оксихинолината)алюминия в красной и
ближней
ИК-областях показано, что доминирующим
механизмом в таких системах является направленный перенос заряда. Недавно был
изучен процесс переноса энергии с эффектом антенны для макрогетероциклических
каликсареновых комплексов европия, содержащих оксихинолиновые лиганды. Было
отмечено уменьшение люминесценции лиганда и появление интенсивного узкого пика
люминесценции Eu.
Были синтезированы и изучены комплексы
монофталоцианинов европия с различными аксиальными лигандами. Показано, что
аксиальныйлиганд практически не влияет на электронные спектры поглощения,
однако значительно влияет на фотолюминесцентные характеристики. Таким образом,
для получения узкой полосы свечения атома европия в монофталоцианиновых
комплексах необходим тщательный подбор аксиальных лигандов с определенными
энергетическими характеристиками.
.3 Люминесцентные свойства Eu3+-Al-cодержащих
комплексных соединений
Узкая красная люминесценция европия делает
материалы на его основе очень востребованными, но прямое возбуждение иона европия
невозможно: молярный коэффициент поглощения иона Eu3+ составляет менее 10
л/(моль см). Поэтому для увеличения интенсивности люминесценции нужно
использовать поглощатель - сенсибилизатор - который будет поглощать энергию и
передавать на центральный ион европия. Такой сенсибилизатор должен
взаимодействовать с европиевым центром, а между донорным уровнем и уровнем,
соответствующем возбужденному состоянию европия, должно быть существенное
перекрывание. В качестве таких сенсибилизаторов в коммерческих образцах
используют неорганические матрицы, например, Ln2O3, Y2O3, SrAl12O19, Ca3Al2O6,
YPO4, YVO4, YBO3, ZnO или Al2O3. Но они с течением времени поглощают воду из
воздуха, что приводит к снижению эффективности люминесценции. Распространенным
классом сенсибилизаторов являются органические молекулы. В зависимости от
природы органического фрагмента это может обеспечивать органическим комплексам
множество применений, но большинство таких соединений оказываются со временем
не стабильны по отношению к УФ излучению. Поэтому разумно использование в
дополнении к органическому сенсибилизатору неорганической матрицы: она будет
являться защитным слоем и увеличит стабильность всей системы.
Отличными кандидатами на эту роль являются
слоистые двойные гидроксиды (СДГ): их просто синтезировать и они стабильны на
воздухе. При этом как ионы европия, так и сенсибилизатор можно вводить а) между
слоями и б) прямо в гидроксидный слой. Какой из подходов более оправдан, пока
сложно судить, поэтому особенно важно, что появляются работы, в которых
испытывается возможность каждого варианта.
Самым простым является введение катиона и
сенсибилизатора между слоями СДГ. Например, уже в 2005 году между слоями Zn/Al
СДГ Гаго и др. вводили комплексы европия и гадолиния. В качестве лиганда они
использовали бипиридиндикарбоксилат, а дипиколинатные комплексы европия и церия
немного позже вводили между слоями таких же СДГ в группе Чанга. При этом ученые
наблюдали увеличение интенсивности люминесценции.
Но недавно стали появляться работы, в которых
ионы металлов вводятся прямо в слой гидроксида. Так, Чен и др. наблюдали
интенсивную люминесценцию ионов европия, введенных в слои Zn/Al СДГ, при
сенсибилизации интеркалированными хлорид-анионами. мусумеси
Однако наличие дополнительного эффективного
сенсибилизатора все равно необходимо, и органические молекулы здесь наиболее
эффективны. Первой такой работой стало введение Гунаваном и Ху бифенилацетата
для сенсибилизации ионов тербия в СДГ. Более подробно такой способ исследовали
Гао и др., рассмотрев ряд 1,5-нафтилдисульфоновая кислота -
2,6-нафтилдикарбоновая кислота - терефталевая кислота - бензойная кислота.
Оказалось, что, хотя важно учитывать и геометрию молекулы (изменение
межслоевого расстояния в зависимости от расположения молекулы), важнейшую роль
играют кроме положение уровней и степень экранирования сенсибилизатора
матрицей: максимальное возбуждение обеспечивается в случае терефталевой
кислоты, причина же этого - максимальная степень поглощения ей УФ излучения.
Кроме того, сравнение полученных результатов с данными по сенсибилизации
люминесценции европия нитрат-анионом показало, что однозначно надо продолжать
именно введение органических сенсибилизаторов [22 - 26].
В работе [27] методом золь-гель-технологии
синтезированы монолитные образцы поликристаллического корунда α-Al2О3,
активированного примесными трехзарядными редкоземельными ионами RE3+(Eu3+,
Er3+, Pr3+).
В огромном числе статей, посвященных изучению
спектроскопических свойств примесных ионов редких земель (RE) в диэлектрических
кристаллах, практически не содержится сведений о свойствах ионов RE как
активаторов в кристаллах корунда α-Al2О3.
Действительно, в то время как в решетке корунда ионы Al3+ легко замещаются
3d-ионами группы железа (рубин α-Al2О3:Cr3+),
внедрение в решетку корунда больших по размеру RЕ3+-ионов трудно реализовать
при традиционных высокотемпературных методах выращивания кристаллов. Недавно
сообщалось о легировании монокристаллов корунда ионами Er3+ путем имплантации
быстрых ионов. Настоящая работа посвящена первым исследования оптических
спектров трехзарядных редкоземельных ионов (Eu3+, Er3+, Pr3+) в
поликристаллическом корунде а- Al2О3, синтезированном с помощью
золь-гель-технологии. Показано, что ионы RE3+, внедренные в решетку корунда,
образуют строго определенный доминирующий тип центров с характерным
узколинейчатым спектром f- f-переходов. Определена энергетическая схема уровней
ионов Eu3+ и Er3+ в корунде.
Корунд - α-Al2О3-
с примесью редкоземельных ионов Eu3+, Er3+ и Pr3+ был синтезирован по золь-гель
(ЗГ) технологии с использованием алкокси-метода, в котором исходными веществами
были алкоксиды алюминия - Al(OR)3. На начальной стадии получения Al2О3 по
ЗГ-технологии необходимо сформировать агрегативно-устойчивые коллоидные
растворы - золи и гели моногидроксида алюминия - y-Д1ООН, которые получались
гидролизом Al(OR)3. Агрегативная устойчивость золей γ-AlOOH
в
широком интервале концентраций электролитов позволяет вводить строго
контролируемые количества солей редкоземельных элементов, которые равномерно
распределяются по всему объему золя. Старение и обезвоживание золей проводились
при 80-100°C, что приводит к образованию гелей и ксерогелей. Эти процессы
сопровождаются хемосорбцией RE3+-ионов на поверхности коллоидных частиц
моногидроксида алюминия с образованием мостиковых связей типа Al−O−RE.
На заключительной стадии образцы Al2О3 получались
термическим отжигом ксерогелей. При температуре 450°C, отвечающей минимуму
второго эндоэффекта на кривой, полученной методом ДТА (дифференциального
термического анализа), моногидроксид алюминия теряет воду и переходит в γ-Al2О3
- первую низкотемпературную модификацию оксида алюминия, стабильную до 900° C.
Оптические и другие физико-химические свойства γ-Al2О3
исследовались на образцах, полученных отжигом при 750°C в течение часа. При
температуре отжига 750° C формировался монолитный твердый прозрачный
высокопористый образец γ-Al2О3:RE3+,
построенный из близких по размеру кристаллических частиц нанометрового размера,
имеющих структурно-разупорядоченную кубическую решетку γ
-фазы
Al2О3. При нагревании выше 900° C γ-Al2О3
переходит в корунд через серию полиморфных превращений γ
→
δ →
θ →
γ-Al2О3 .
В работе [28] была исследована фотолюминесценция
SrTiO3:Eu, Al. В настоящее время люминесцентные материалы, активаторами в
которых служат ионы редкоземельных элементов (РЗЭ), привлекают особое внимание
многих исследователей. Специфика этих центров состоит в том, что излучательные
переходы в ионах РЗЭ могут быть осуществлены в пределах замкнутой
4f-электронной оболочки (внутриконфигурационные переходы), которая экранирована
внешней 5s25p6 -оболочкой от матрицы. Переходы 4f-4f формируют узкие полосы
люминесценции. Это позволяет использовать РЗЭ для активирования
кристаллофосфоров с целью получения на их основе лучших по чистоте цвета активных
слоев для средств отображения информации.
Данная работа посвящена изучению
фотолюминесцентных свойств кристаллофосфора оранжевого цвета свечения
SrTiO3:Eu, Al.
Исследуемый образец был получен методом
твердофазного синтеза (температура и время прокалки, соответственно 1300 ºС,
6 часов). Концентрации активатора Eu 0,2 мас. %, соактиватора 17 моль % по
отношению к SrTiO3.
На первом этапе исследования был получен спектр
фотолюминесценции SrTiO3:Eu, Al. Спектр состоит из четырех неперекрывающихся
полос 5D0 → 7F1 (595 нм), 5D0 → 7F2 (620 нм), 5D0 → 7F4 (685
нм, 705 нм). Переход 5D0 → 7F1 является магнитным дипольным, так как идет
с изменением орбитального углового момента на 1. Переходы, 5D0 → 7F2
электрическими дипольными, орбитальный угловой момент у них изменяется на 2 и
4. Существование электрических дипольных переходов в спектре указывает на то,
что в SrTiO3:Eu, Al ион Eu3+, занимает кристаллографическое положение не
совпадающее с центром симметрии и может быть вызвано наличием в
кристаллофосфоре примесных дефектов, образованных Al, и вакансий кислорода.
Как известно ион европия обладает переменной
валентностью и может присутствовать в твердом теле в двух состояниях Eu2+ ,
Eu3+. При этом у Eu2+, в отличие от Eu3+ наблюдается широкая полоса
люминесценции (поглощения) связанная с одним переходом с уровня 4f5d на уровень
основного состояния 8S7/2. Положение этой полосы сильно зависит от
кристаллического поля, так как 5d уровень неэкранирован. Кроме того, переходы
4f-5d являются межконфигурационными и поэтому разрешены по четности и имеют высокую
интенсивность поглощения (люминесценции). Учитывая выше сказанное, полосу
фотовозбуждения с энергией 3,15 эВ можно связать с переходом из основного
состояния 8S7/2 в возбужденное 4f5d иона Eu2+. В дальнейшем энергия,
выделяющаяся при обратном переходе резонансно передается иону Eu3+ и
наблюдаются характерные для SrTiO3:Eu, Al полосы люминесценции.
2. Получение порошков оксида EuxAlyOz
.1 Физико-химические методы получения
нанопорошков
Один из методов, широко применяемых для
производства нанопорошков - вакуумное осаждение. Процесс включает три
последовательные стадии: испарение вещества, его транспорт к подложке и
конденсацию. Тигель с расплавом материала (металла или оксида), разогретого до
высокой температуры лазерным излучением, пучком электронов, постоянным или
вихревым током, помещается в вакуумированный сосуд. Если испаряемый материал
проводит ток и при этом без плавления может обеспечить достаточно высокое
давление паров, из него делают проволоку, служащую при пропускании тока
источником атомов.
Испаряющийся при температуре 500-1200 °С
материал конденсируется на охлаждаемой поверхности в виде порошка наночастиц.
Чтобы понизить кинетическую энергию испарившихся атомов и облегчить их
конденсацию, процесс проводится в атмосфере инертного газа, например, He или
Ar, при невысоком давлении (~ 103 Па).
В процессе химического вакуумного осаждения
исходный реагент испаряют, и затем он диффундирует к нагретой подложке. На ее
поверхности он разлагается и ли реагирует с парами второго реагента. Нелетучий
твердый продукт реакции формирует поверхностные наноструктуры, а побочные
летучие продукты удаляются. Процесс могут катализировать частицы переходных
металлов - Fe, Ni или Co. Этим методом получены наночастицы Fe2O3, TiO2, SiC и
некоторые другие.
При лазерной абляции материал испаряется под
действием импульсного лазерного излучения и затем конденсируется в виде частиц.
Специфика лазерного нагрева ярко проявляется при облучении твердой мишени,
погруженной в жидкость. В этом случае закономерности диспергирования материала
существенно изменяются. В первую очередь это вызвано тем, что наночастицы
образуют коллоидный раствор, вследствие чего могут вернуться в лазерный пучок и
повторно подвергнуться облучению.
Закономерности лазерной абляции наночастиц и
объемного материала существенно отличаются. В металлических наночастицах,
размеры которых меньше длины свободного пробега электронов, возникают
коллективные колебания электронного газа на плазменной частоте. В спектрах
растворов таких частиц возникает плазмонная полоса поглощения. Для большинства
металлов она лежит в УФ области, а для Au, Ag и Cu - в видимой области спектра.
Частицы интенсивно поглощают излучение на плазменной частоте, плавятся и
локально испаряют окружающую их жидкость. Неравномерное распределение давления
паров жидкости вызывает повторное дробление капель расплава. В результате
лазерное облучение коллоидного раствора приводит как к измельчению частиц, так
и к изменению их распределения по размерам.
Следует отметить, что интенсивность поглощения
излучения сильно зависит от формы частиц. Поэтому в процессе лазерной абляции
происходит селекция наночастиц. Например, при распылении золота и серебра
«выживают» преимущественно дискообразные частицы, толщина которых намного
меньше диаметра. Таким образом, использование лазерной абляции в сочетании с
другими факторами (растворителем, стабилизирующими и легирующими добавками)
открывает возможности для управления не только размером, но и формой частиц.
Лазерной абляцией в жидкостях получают
наночастицы благородных металлов и их сплавов, Ti, Zn, Cu, Co, Ni, оксидов CuO,
ZnO, полупроводников CdS, ZnSe и других веществ.
Для синтеза нанодисперсных порошков тугоплавких
металлов и их соединений (карбидов, нитридов и др.) перспективен
плазмохимический метод, представляющий собой восстановление металлов из их
соединений под действием газов. В плазмотроне электрической дугой высокой
интенсивности создается плазма с температурой 4000-10000 °С. В плазме, через
которую пропускают газообразный восстановитель (водород или углеводороды и
конвертированный природный газ), исходный материал превращается в
конденсированную дисперсную фазу. Таким методом получают порошки тугоплавких
металлов W, Mo, Ni.
Восстановление - один из наиболее дешевых
методов, позволяющих получать высокочистые порошки. Несколько более дорог
электролитический метод. Применяется электролиз как водных растворов, дающий
порошки Fe, Cu, Ni, так и расплавов солей Ti, Zr, Nb, Ta, Fe, U. В результате
электролиза обычно образуются частицы дендритной формы с размерами порядка
десятков нм.
При золь-методе в разогретую смесь первичного
реагента с различными добавками быстро вводят второй реагент. В результате
химической реакции образуется пересыщенный раствор целевого соединения, быстро
проходящего нуклеацию и вступающего в стадию роста. Если продолжительность
нуклеации намного короче стадии роста, получаются нанокристаллы с узким
распределением по размерам.
Другой вариант применения метода состоит в том,
что готовится «холодная» смесь реагентов, в которой скорость образования
целевого вещества мала. Затем этот раствор нагревается до температуры, при
которой образуется целевой продукт с концентрацией, достаточной для нуклеации.
После быстрой и интенсивной нуклеации концентрация падает и дальше происходит
только рост образовавшихся частиц. Во время роста поддерживается температура,
при которой скорость образования целевого вещества ниже скорости его
кристаллизации.
Размером, формой и степенью кристалличности
наночастиц, образовавшихся в золь-методе, можно управлять, варьируя температуру
и соотношение концентраций исходных реагентов и стабилизатора. Для остановки
роста частиц во всех случаях обычно достаточно быстро охладить реакционную
смесь. Чтобы выделить наночастицы, добавляют осадитель - растворитель,
смешивающийся с реакционной системой, но плохо растворяющий «защитные оболочки»
наночастиц и потому дестабилизирующий суспензию. В результате наночастицы
осаждаются в виде порошка, который отделяют центрифугированием. Золь-метод
позволяет получать практически монодисперсные наночастицы различных
полупроводников и металлов.
.2 Получение порошка оксида EuxAlyOz
Потребность в новых материалах для таких
интенсивно развивающихся отраслей как оптическое приборостроение, волоконная
оптика и оптоэлек-троника является причиной неослабевающего интереса к
материалам, активированным ионами редкоземельных элементов, в частности, к
порошку, содержащим ионы лантаноидов. Спектрально-люминесцентные свойства этих
материалов позволяют с успехом применять их в вышеперечисленных областях.
В качестве исходного сырья использовали:
соли Al, Eu
этиленгликоль
лимонная кислота
этилендиамин
Соли европия получали путем добавления в оксид
европия (Eu2O3) концентрированной азотной кислоты (HNO3) и нагревание
полученной смеси до выпадения соли европия (европий-азоткислый) и испарение
остатков азотной кислоты, а также дальнейшее охлаждение на воздухе. Были
использованы смеси солей с различной концентрацией в них солей алюминия и
европия:
Таблица 2.1 - Массовое соотношение солей
металлов
|
Металл
|
Масса
(г)
|
|
Eu
|
1
|
1
|
0,5
|
|
Al
|
1
|
0,5
|
1
|
В каждую из полученных смесей солей добавлял по
5 мл. этиленгликоля. Данные золи подвергалась ультразвуковой обработке в
течение 1 часа до полного растворения. После этого в каждый из образцов
добавлялся этилен-диамин в количестве, необходимом для получения pH 5-7 в
исходных составах. При добавлении этого вещества происходит нагрев золей и
образование геля, который при охлаждении затвердевает. Поэтому необходимо как
можно быстрее нанести данные гели на подложки, на которых будет осуществляться
термическая обработка. Переход золя в гель представляет собой многостадийный
иерархический процесс, распространяющийся от атомно-молекулярного до
макроскопического уровня. С точки зрения термодинамики он является сложным
неравновесным процессом, характеризующимся многокомпонентностью и
многофазностью, совмещенностью явлений различной физико-химической природы. Он
способен к самоорганизации и эволюции во времени.
Формирование геля носит сложный характер,
обусловленный одновременным протеканием нескольких альтернативных процессов.
Это - агрегация частиц и обратный процесс - фрагментация агрегатов. При этом
процесс агрегации складывается из двух типов взаимодействий: частица - кластер
и кластер - кластер. Все эти процессы приводят к формированию аморфных гелиевых
структур, характеризующихся высокой неупорядоченностью.
Отжиг геля приводит к удалению из него воды,
спирта, органических остатков, что проявляется в уменьшении массы и объема
(усадке) геля и в изменении его плотности.
Отжиг проводится в атмосфере при температуре 800
°С. В керамической чашке малого объёма для предотвращения растекания его по
поверхности печки. При этом наблюдается увеличение объёма состава и образование
структуры, внешне похожей на «шар», при этом плотность состава уменьшается в
разы. Далее печь отключается и исходная структура охлаждается вместе с печкой.
В итоге мы получаем структуру белого цвета, которая при механическом
воздействии разрушается, превращаясь в мелко дисперсный порошок, который крайне
летуч.

Рисунок 2.1 - Блок-схема получения порошка
оксида EuxAlyOz
3. Спектры люминесценции EuxAlyOz
На рисунке 3.1 представлены спектры
люминесценции порошков с различным соотношением в них алюминия и европия. Длина
волны возбуждения 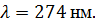 Видно, что на
длине волны
Видно, что на
длине волны 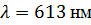 . наблюдается
максимум интенсивности для всех трех концентраций. Также наблюдаются максимумы
интенсивности и на других значениях волн.
. наблюдается
максимум интенсивности для всех трех концентраций. Также наблюдаются максимумы
интенсивности и на других значениях волн.
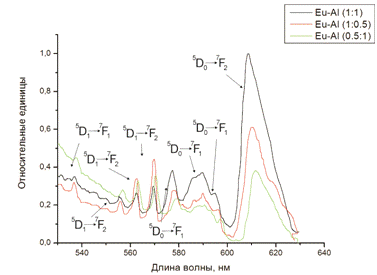
Рисунок 3.1 -График зависимости интенсивности
люминесценции различных соотношений европия и алюминия в соединениях от длины
волны
Таблица 3.1 - Максимумы интенсивности и
соответствующий для них переходы
|
Переход
|
Длина
волны 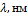
|
|
5D1
→ 7F1
|
537
|
|
5D1
→ 7F2
|
563
|
|
5D0
→ 7F1
|
590
|
|
5D0
→ 7F2
|
613
|
Видно, что разным переходам соответствуют разные
максимумы интенсивности люминесценции. Однако для соотношения Eu-Al (0.5:1)
главный максимум совпадает с промежуточным, а именно при 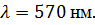
Переход 5D0 → 7F1 является
магнитодипольным, так как идет с изменением орбитального углового момента на 1.
Переходы, 5D0 → 7F2 электрическими дипольными, орбитальный угловой момент
у них изменяется на 2 и 4 [28].
Полученные максимумы и соответствующие им
переходы совпадают с данными, полученными в работе [29], в которой
исследовались оптические и люминесцентные свойства стекла с нанесенным на него
покрытием Eu3+
: Al(NO3)3-SiO2, полученных золь-гель методом.
С помощью электронного микроскопа были получены
изображения порошка:
а)
 б)
б)

в)
 г)
г)

Рисунок 3.2 - Изображения порошка оксида
EuxAlyOz, полученного электронным микроскопом с различным разрешением (а - г).
Из приведенных изображений видно, что частицы
порошка слиплись между собой, механически разъединить их уже не представляется
возможным. Можем заметить, что самые мелкие частицы имеют размеры порядка
100-130 нм, что говорит о правильности соблюдения всех этапов получения этого
порошка.
Из рисунка 3.1 можно увидеть, что максимум
интенсивности люминесценции приходится на длину волны λ
= 613
нм. Наблюдается усиление люминесценции в 2,5 раза для соотношения Eu-Al (1:1),
и в 1,5 раза для соотношения Eu-Al (1:0,5), по сравнению с оксидом с массовым
отношением Eu-Al (0,5:1). Этим пикам соответствует электронный переход 5D0 →
7F2. Поэтому можно говорить о том, что наиболее оптимальным массовым
соотношением является значение Eu-Al (1:1).
Заключение
Потребность в спектроскопических методах
активного поиска принципиально новых дешевых люминесцентных материалов с
высокой яркостью, определенной цветностью излучения для устройств квантовой и
молекулярной электроники стимулировали исследования, представленные в курсовой
работе.
В данной курсовой работе золь-гель методом были
получены сложные оксиды европия и алюминия с различным массовым соотношением.
Также мною были получены спектры люминесценции данных порошков. Результаты,
полученные в данной работе, совпадают с результатами, полученными в других
работах аналогичного характера (в частности, полосы люминесценции и
соответствующие им электронные переходы). На электронном микроскопе с различным
увеличение были получены изображения частиц порошка.
Было установлено, что максимум интенсивности
люминесценции приходится на длину волны λ = 613 нм.
Наблюдается усиление люминесценции в 2,5 раза для соотношения Eu-Al (1:1), и в 1,5
раза для соотношения Eu-Al (1:0,5), по сравнению с оксидом с массовым
отношением Eu-Al (0,5:1). Поэтому можно говорить о том, что наиболее
оптимальным массовым соотношением для получения оксида является значение Eu-Al
(1:1).
Список использованной литературы
1.
С.С.
Hinckley, J. Am. Chem. Soc. 91 (1969) 5160.2. "NMR shift reagents".
Ed. R.E. Sievers. New York. Acad. Press, 1973,410 p.
.
И.Я.
Слоним,
A.X. Буслай,
Успехи
химии
42 (1973) 1976.
3.
JI.Г. Коренева, В.Ф. Золин, "Редкоземельный зонд в химии и биологии",
М., "Наука", 1980, 360 с.
4.
I. Hemmila, J. Alloys Compd 225 (1995) 480.
.
M.G. Duarte, M.I.M. Prata, M.H.M. Gil, C.F.G.C. Geraldes, J. Alloys Compd 344
(2002) 4.
.
N. Fatin-Rouge, E. Toth, R. Meuli, J.-C. Biinzli, J. Alloys Compd 374 (2004)
298.
.
M.I. Gaiduk, V.V. Grigor'yants, A.F. Mironov, V.D. Rumyantseva, V.I. Chissov,
G.M. Sukhin, J. Photochem. Photobiol. B: Biol. 7 (1990) 15.
.
M. Bethencourt, F.J. Botana, J.J. Calvino, M. Marcos, M.A. Rodrigues-Chacou,
Corrosion Science 40 (1998) 1803.
.
M.A. Caro de la Torre, A. Gomez-Hens, Analyt. Chim. Acta 407 (2000) 53.
.
G.A. Broker, M.A. Klingshirn, R.D. Rogers, J. Alloys Compd 344 (2002) 123.
11.
В.Ф. Золин, Л.Г. Коренева, В.И. Царюк, Биофизика 20 (1975), 194с.
.
В.Ф. Золин, Л.Г. Коренева, Биофизика 21 (1976), 55 с.
.
Л.Г. Коренева, А.В. Викторов, Л.И. Барсуков и др., Биофизика 23 (1978), 624 с.
.
Л.Г. Коренева, В.А. Барабанов, В.Ф. Золин, С.Л. Давыдова, Коорд. химия 4
(1978),193 с.
15.
С.
Kremer, J. Torres, S. Dominguez, A. Mederos, Coord. Chem.
Rev. 249 (2005), 567 p.
.
A.M. Гурвич, Спектроскопия кристаллов Л., Наука, 1985, с. 59-70.
.
Б.М. Синельников, Н.И. Каргин, Л.В. Михнев, В.А. Воробьев, Е.А. Бондаренко,
Ю.В. Кузнецов, А.С. Гусев, В.А. Тарала, ст. Исследование люминесцентных свойств
SrTiO3:Pr3+:Al при фотовозбуждении, 2004.
.
Кортов В.С., Иванов В.В., Котов Ю.А., Кайгородов А.С., Зацепин А.Ф., Звонарев
С.В., Хрустов В.Р., ст. Наноструктурные люминофоры на основе оксидов алюминия и
кремния, 2006.
.
Н.В. Гапоненко, В.С. Кортов, Т.И. Ореховская, И.А. Николаенко, В.А. Пустоваров,
С.В. Звонарев, А.И. Слесарев, С.Я. Прислопский, Физика и техника
полупроводников, 2011, том 45, вып. 7, 980-983 с.
.
Б.Г.Тагиев, С.А.Абушов, О.Б. Тагиев, ст. Люминесценция кристалловSe4 , 2007.
.
А.В. Зиминов, Т.А. Юрре, С.М.Рамш, М.М.Мездрогина, Спектральные характеристики
фталоцианинатов европия с различными аксиальными лигандами, Физика твердого
тела, 2010, том 52, вып. 9, 1785-1788.
22.
S. Gago, M. Pillinger, R. A. S. Ferreira, L. D. Carlos, T. M. Santos and I. S.
Goncalves, Chem. Mater., 2005, 17, 5803.
.
Z. Chang, D. Evans, X. Duan, P. Boutinaud, M. de Roy and C. Forano, J. Phys.
Chem. Solids, 2006, 67, 1054.
.
A. W. Musumeci, Z. P. Xu, S. V. Smith, R. F. Minchin and D. J. Martin, J.
Nanopart. Res., 2010, 12, 111.
.
P. Gunawan and R. Xu, J. Phys. Chem. C, 2009, 113, 17206.
.
Xiaorui Gao, Meng Hu et al., Chem. Commun., 2010.
.
А.А. Каплянский, А.Б. Кулинкин, А.Б. Куценко, С.П. Феофилов, Р.И. Захарченя,
Т.Н. Василевская, Оптические спектры трехзарядных редкоземельных ионов в
поликристаллическом корунде, Физика твердого тела, 1998, том 40, № 8, 1442-1449
с.
.
Бондаренко Е.А., Михнев Л.В., Гусев А.С., Бондаренко С.А., Каргин Н.И.,
Исследование фотолюминесценции SrTiO3:Eu, Al., Химия твердого тела и
современные микро и нанотехнологии. VII Международная
конференция.
Кисловодск
- Ставрополь:
СевКавГТУ,
2007 - 510 с.
.
S. Hazarika, S. Rai, Structural, optical and non-linear investigation of Eu3+
:
Al(NO3)3-SiO2 sol-gel glass, Bull. Mater. Sci., Vol. 27, No. 3, June 2004, pp.
273-279.