Проект цеха переработки фторсодержащих отходов алюминиевого производства, производительностью 1500 т/год по исходному сырью
Содержание
Введение
1. Аналитический обзор
.1 Алюминиевая промышленность
.2 Сырье для производства алюминия
.3 Общая схема производства алюминия
.4 Производство глинозема
.5 Способы получения и применение фтористого алюминия
2. Технология
получения фтористого водорода
. Химические
и физические свойства исследуемых веществ
.1 Фторид
натрия
3.2 Сульфат натрия
3.3 Серная
кислота
3.4 Фтористый водород
.5 Гексафторалюминат натрия
. Теоретическая часть
.1 Термодинамика процесса
4.2 Источник
ошибок при расчете равновесия
.3
Теоретические основы получения фтороводорода из фторида натрия
.5 Описание
технологической схемы
. Расчетная
часть
.1 Расчет
барабанно-вращающейся установки сульфатизации
.1.1
Материальный расчет
.1.2 Тепловой
расчет
.1.3
Конструктивный расчет барабанной вращающейся установки
.1.4
Конструктивный расчет барабана
.1.5
Прочностной расчет барабана
.1.6 Расчет
барабана на жесткость
.1.7 Расчет
бандажа барабанной печи
.1.8
Определение реакций опорных роликов
.1.9
Определение геометрических размеров бандажа из условия его работы на изгиб и
контактную прочность
.1.10
Определение размеров упорных роликов
.1.11
Определение диаметра упорного регулировочного винта
.1.12
Основные составные части вращающейся установки с барабаном
.2 Расчет
форконденсатора
.2.2
Материальный и тепловой расчет
.2.3
Определение движущей силы процесса теплопередачи
.2.4
Определение средних температур теплоносителей
.2.5 Тепловой
расчет
.2.3
Конструктивный расчет
.3 Расчет
абсорбционной колонны
.3.1 Введение
.3.2 Данные
для расчета
.3.3
Материальный расчет абсорбционной колонны
.3.4
Определение движущей силы и конструктивный расчет абсорбера
.3.5
Конструктивный расчет абсорбера
. Схема
контроля и автоматизации процесса
7. Охрана труда и техника безопасности
. Экономическая часть
Список
литературы
Введение
Российская алюминиевая промышленность является
наиболее преуспевающей из отечественных металлургических отраслей, являясь
крупнейшим в мире экспортером алюминия. Из 20 млн. выплавляемого в мире
первичного алюминия на Россию приходится примерно 15% или 3 млн. т. Из них
более 75% приходится на алюминиевые заводы, расположенные в Сибири.
При получении металлического алюминия используются
фтористые соли алюминия: AlF3, Na3AlF6, и оксид Al2O3. На производство 1 т первичного
алюминия расходуется 25-30 кг и около 20 кг криолита.
Одной из актуальных проблем при производстве алюминия является
образование большого количества твердых отходов, состоящих из соединений фтора,
натрия, серы, углерода и других элементов. Для решения этой проблемы необходимо
организовывать переработку твердых фторсодержащих отходов алюминиевого
производства, значительную часть которых составляют пыли и шламы газоочистки, с
возвращением в процесс электролиза фтористых солей и улучшением
технико-экономических и экологических показателей работы алюминиевых заводов.
1. Аналитический обзор
.1 Алюминиевая промышленность
Основным сырьем для производства глинозема являются
бокситы, нефелины и алуниты, основные месторождения которых в России
расположены на Урале, в Республике Коми, Архангельской, Курской и Ленинградской
областях. Но производимого в России глинозема не хватает для нужд российской
алюминиевой промышленности. Это является одной из наиболее важных особенностей
развития алюминиевой промышленности страны. [18]
.2 Сырье для производства алюминия
Алюминий входит в состав многих минералов, однако в
качестве алюминиевых руд используются только бокситы, нефелины, алуниты и
каолины. Они различаются составом и концентрацией оксида алюминия. Важнейшей
алюминиевой рудой являются бокситы, содержащие гидратированный оксид алюминия
А12Оз•nН2О. В
зависимости от степени гидратации алюминиевый компонент в бокситах может
находиться в форме диаспора А12Оз•Н2О или иначе HAlO2 или в форме гидроаргелита А12Оз•ЗН2О
(или А1(ОН)з. Помимо оксида алюминия в состав бокситов входит оксид
кремния (от 0,5 до 20%) и различные соединения железа, кальция и магния.
Основная характеристика бокситов, от которой зависит выбор метода их
переработки - кремневый модуль - отношение содержания в них оксида алюминия к
содержанию оксида кремния А2О3/SiO2. Для бокситов, используемых в качестве сырья в
алюминиевой промышленности, модуль должен быть не ниже 2,6; для бокситов
среднего качества он составляет 5-7, чему соответствует содержание оксида
алюминия 46-48%.
Нефелины представляют собой сложную тройную соль
состава (Nа,К)20•А12O3•SiO2
и входят как составная часть в апатито-нефелиновую
руду, содержащую кроме нефелина апатит ЗСа3(РО4)2•СаF2. Для производства алюминия используют нефелиновый
концентрат с содержанием оксида алюминия 20-30%. Его получают наряду с
апатитовым концентратом переработкой апатито-нефелиновой руды.
Алуниты представляют двойную основную сернокислую соль
алюминия и калия состава К2 SО4А12(SО4)3•4А1(ОН). [18]
.3 Общая схема производства алюминия
Технология получения металлического алюминия из руд
достаточно сложна и состоит из четырех производств, связанных между собой
технологической цепочкой и производимыми продуктами. Она включает:
производство глинозема (оксида алюминия);
производство фтористых солей и криолита;
производство угольных изделий (электродов и блоков
футеровки);
производство электролитического алюминия.
Основными производствами, составляющими
технологическую цепочку Руда - Глинозем - Алюминий, является производства
глинозема и алюминия. Территориально они обычно разделены. Вследствие высокой
энергоемкости процесса электролитического восстановления алюминия алюминиевые
заводы располагаются в районах с дешевой электроэнергией ГЭС. Производства
глинозема, наоборот, базируются в местах добычи алюминиевых руд с тем, чтобы
сократить расходы на перевозку сырья. Примером производства с полным циклом (от
руды до рафинированного металлического алюминия) являются Волховский и
Каменец-Уральский заводы. На других предприятиях этой отрасли осуществляется
только часть технологической цепочки: производство глинозема (Ачинск,
Бокситогорск) или выплавка алюминия (Кандалакша, Волгоград, Новокузнецк,
Братск, Красноярск).
Производство фтористых солей и криолита ставит целью
получение растворителя для глинозема и добавок, снижающих температуру плавления
электролита.
Организация отдельного производства угольных изделий
вызвана тем, что в процессе электролиза угольные аноды и футеровка
электролизеров расходуется, и требуют непрерывного пополнения.
.4 Производство глинозема
Исходный материал для электролитического производства
алюминия - это чистый оксид алюминия - глинозем. Для выделения глинозема из
алюминиевых руд его переводят в растворимую соль (алюминат натрия), которую
отделяют от остальных компонентов руды, осаждают из ее раствора гидроксид
алюминия и кальцинацией последнего получают глинозем.
Метод выделения глинозема из руды зависит от ее состава. Эти методы
подразделяются на химико-термические (пирометаллургические), кислотные и
щелочные (гидрометаллургические).
.5 Способы получения и применение
фтористого алюминия
Фторид алюминия. А1F3, бесцветные кристаллы, существующие в нескольких
модификациях. При обычных условиях устойчива α-модифи-кация с тригональной решеткой;
плотность 1,882 г/см. Известна устойчивая до 710-720° С γ-модификация с тетрагональной решеткой
(а - 0,354 нм, с- 0,600 нм). Температура возгонки 1270°С; Сp° = 75,10 Дж/(моль*К); уравнения
температурной зависимости давления пара:
lgр (Па) = 16,565-16 967/T (980<T<1123К);
lgp (Па) = 14,719-14 974/T (1027<T<1184К).
Фторид алюминия имеет координационную решетку. Он
резко отличается по своим свойствам от остальных галогенидов, и прежде всего,
сравнительно слабой реакционной способностью.
Фторид алюминия плохо растворим в воде (0,41% (масс.)
при 25° С), лучше растворяется в растворах фторида водорода, не растворяется в
органических растворителях. Образует кристаллогидраты с 1, 3 и 9 молекулами
воды. В процессе нагревания гидролизуется парами воды, слабо реагирует с
концентрированной серной кислотой, разлагается растворами и расплавами щелочей.
Фторид алюминия А1F3 получают в процессе пропускания сухого газообразного фторида
водорода над алюминием или оксидом алюминия при 450-600°С по схеме
А1+6НF = 2АlF3 + ЗН2
А12О3 + 6НF = 2А1F3 + ЗН2О
А1F3 получают также взаимодействием
водных растворов фторида водорода с А2О3 или А1(ОН)3
по схеме
А12О3 + 6НF= 2А1FЗ•Н2О
Аl(ОН)3
+ ЗНF = А1F3•ЗН2О
Образующийся кристаллогидрат выделяют из растворов,
сушат и обезвоживают термообработкой при 500-600°С.
В промышленности широко применяется способ получения
фторида алюминия взаимодействием гидроксида алюминия с водным раствором фторида
аммония:
Аl(ОН)3
+ ЗNН4F = АlF3 + 3NH4ОН
Трифторид алюминия применяется в качестве компонента
электролита (5-7%) в производстве металлического алюминия. Он входит в состав
флюсов, эмалей, стекол, глазурей, керамики и покрытий сварочных электродов,
является катализатором в органической химической технологии. [18]
|
Плавик Плавиковошпатовый
концентрат
|
Шпат
|
CaF2
|
|
Гидроксид алюминия
|
Гидрат
|
Al(OH)3
|
|
Кальцинированная сода
|
Сода
|
Na2Co3
|
|
Серная кислота
|
Кислота
|
H2SO4
|
|
Известняк флюсовый
|
Известняк
|
CaCO3
|
2. Технология получения фтористого водорода
Производство фтористоводородной кислоты и фтористого водорода.
Получение фтороводорода сульфатизацией CaF2.
Среди многочисленных способов получения HF наибольшее промышленное значение имеет взаимодействие CaF2 и c
концентрированной серной кислотой. В первом приближении процесс протекает по
уравнению:
CaF2+H2SO4→2HF=CaSO4,
Хотя в действительности его механизм значительно сложнее. Более того,
техническая реализация этого способа требует проведения большого числа операций
с использованием специфического оборудования.
В самом общем виде технологические операции, осуществляемые на заводах при
производстве безводного HF
сернокислотным разложением CaF2, можно
сгруппировать следующим образом:
собственно сернокислотное разложение,
выделение HF из реакционных
газов,
Обезвреживание отходов и утилизация побочных продуктов.
В лабораторных и полупромышленных масштабах опробованы десятки способов
проведения сернокислотного разложения, многочисленные способы выделения HF из газов и его очистки от примесей.
Однако в крупномасштабном производстве применяется ограниченное число
вариантов, которым отдано предпочтение в последующем изложении.
Длительное время на заводах всех промышленных стран мира использовался
одностадийный способ сернокислотного разложения, по которому исходная смесь
перед подачей в печь или непосредственно в печи образовывала текучую пульпу.
В конце 50-х годов инженеры швейцарской фирмы Бусс разработали
двухстадийный способ сернокислотного разложения, который постепенно вытеснил
одностадийный. Этот способ предусматривает использование концентрированной
серной кислоты. На первой стадии, проводимой при интенсивном перемешивании
реагентов, реакция проходит на 30-40% с образованием сыпучего продукта. На
второй стадии используется этот продукт и реакция проходит до конца без
осложнений, связанных со схватыванием пульпы и с повышенной коррозией из-за
образования паров воды. Двухстадийный способ позволяет снизить расход реагентов
на единицу продукта и повысить выход фтороводорода. Технологическая схема
двухстадийного способа по проспектакм фирмы Бусс и дочерней фирмы Лист
приведена на рисунке
Получаемый таким способом фтороводород содержит 99,9% основного вещества.
Рассмотрим наиболее подробно отдельные стадии процесса и возможности их
дальнейшего усовершенствования [3].
Технологическая схема получения фтористого водорода
В системе Ca2SO4-H2SO4 при концентрации кислоты 98-100% и
температуре 20-80°C существует гидросульфат состава CaSO4•3H2SO4.
Повышение температуры до 85°C к инконгуэнтному плавлению этого
гидросульфата и образованию Ca2SO4•H2SO4, который в свою очередь, инконгруэнтно плавится при
200°C. Изменение концентрации H2O в системе меняет температурные
границы устойчивости гидросульфатов поэтому и механизм сульфатизации CaF2 может менятся в зависимости как от температуры, так и
от исходной концентрации серной кислоты.
Как показал С.В. Островский, реакция CaF2 со 100%-й серной кислотой начинается
уже при комнатной температуре. В условиях непрерывного повышения температуры
выделяющийся твердый продукт растворяется в серной кислоте, однако при 50°C и
достижением определенной концентрации из полученного раствора кристаллизуется β - модификация CaSO4•3H2SO4. Дальнейшее повышение температуры
вызывает образование большого числа мелких кристаллов CaSO4•H2SO4, что приводит к схватыванию реакционной массы. При
температурах выше 90°C происходит интенсивное выделение газообразного HF, а при 115-120°C - полное
исчезновение жидкой фазы и прекращение выделения HF.
Реакция, закончившаяся при взаимодействии примерно половины CaF2, вновь возобновляется при
температурах выше 200-250°C и протекает с поглощением тепла.
Многие исследователи считают, что на промежуточных стадиях взаимодействия
CaF2 и H2SO4
образуется кислая
соль CaF2 H2SO4.
Так, В.К. Фомин (1987 г.) установил, что такая соль изотермически
образуется уже в начале взаимодействия, а при повышении температуры
соответственно до 130 и 170°C она разлагается по уравнениям:
CaF2•H2SO4 → Ca (HSO4)
F + HF, (HSO4) F→CaSO4 + HF
Соединение Ca (HSO4) F при
тех же температурах взаимодействует с H2SO4:
Ca (HSO4) F + H2SO4 →CaSO4•H2SO4
+ HF.
Процесс осложняется из-за образования фторсульфоновой кислоты, которая
уменьшает выход HF и увеличивает
содержание CaF2 в твердом продукте:
H2SO4+HF→HSO3F+H2O
Эта реакция обратимак и при определенном количестве воды её равновесие
смещается влево.
Особенности реагирования в системе CaF2-H2SO4, свойства реагентов и продуктов определяют сложности
практического протекания процесса.
Чем больше концентрация воды в серной кислоте или в реакционной смеси,
тем выше текучесть смеси тем меньше вероятность образования HSO3F, и тем легче осуществлять перемешивание и нагревание смеси.
Однако увеличение концентрации воды в серной кислоте резко усиливает
коррозионное воздействие смеси на материалы аппаратуры.
Принципиальная схема отделения приготовления рабочей смеси кислот:
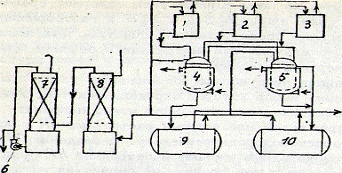
- мерный бак для кубовой и грязевиковой кислот; 2 - мерный бак для
купоросного масла; 3 - мерный бак для олеума; 4 - смеситель для рабочей смеси;
5 - смеситель для моногидрата; 6 - насос; 7 - колонна орошаемая щелочью; 8 -
колонна орошаемая водой; 9, 10 - цистерны.
Принципиальная схема печного отделения:
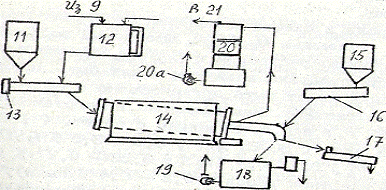
- бункер CaF2; 12 - напорный бак рабочей смеси; 13
- дозатор; 14 - вращающаяся печь; 15 - бункер для извести; 16 - шнековый
питатель; 17 - двухвалковый смеситель для сухого удаления отвала; 18 -
репульпатор отвала; 19 - насос для откачивания пульпы; 20 - «грязевик»; 20а -
насос для перекачивания грязевиковой кислоты в отделение хранения кислот.
Двухстадийный способ сернокислотного разложения CaF2 предлагает использование двух
аппаратов - первичного и основного.
В стандартных установках фирмы Бусс первичный реактор, монтируемый
непосредственно ко вторичному - вращающейся печи, - представляет собой шнековый
аппарат особой конструкции.
Важную роль в схемах выделения HF играют процессы его абсорбции из газв с помощью серной кислоты.
Фтористый водород при комнатной температуре хорошо растворим в серной кислоте,
однако при повышении температуры и при продувке воздухом может быть
десорбирован из раствора. Абсорбция может происходить в соответствии схемы,
показанной на рисунке.
Принципиальная аппаратурная схема узла выделения HF из газов:
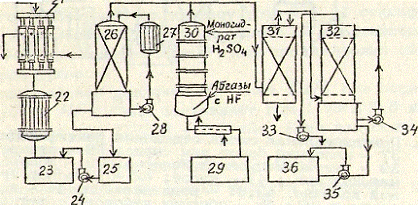
- форконденсатор; 22 - конденсатор; 23 - ёмкость для HF - сырца; 24, 28, 33 - 35 - насосы;
25 - сборник фтористоводородной кислоты; 26 - абсорбционная колонна для
поглощения HF фтористоводородной кислотой; 27 -
холодильник; 29 - сборник отработанной H2SO4; 30 - сернокислотная абсорбционная
колонна; 31 - абсорбционная колонна, орошаемая водой; 32 - щелочная
абсорбционная колонна; 36 - приемник щелочи.
Обработка реакционного газа оборотной кислотой и смеси инертных газов в
насадочных колоннах обеспечивает удаление из газа основной части серной кислоты
и воды, частичную десорбцию HF из
кислоты, обеспыливание газов и их охлаждение до 30-40°C. В результате этого
снижается концентрация примесей в конденсате HF, упрощается ректификация HF и повышается его качество десорбцию HF можно также проводить при пропускании электрического тока
через раствор.
Поскольку избыточное количество HF в H2SO4,подаваемое на разложение CaF2 ухудшает разложение, HF необходимо отгонять. Для этого
оборотную кислоту смешивают с олеумом, что приводит к повышению температуры
смеси и десорбции значительного количества HF.
Полученный при конденсации HF
содержит заметное количество примесей.
Удаление этих примесей проводят методом двухступенчатой ректификации: на
первой стадии удаляют легколетучие смеси SO2 и SiF4, на второй
стадии удаляют высококипящие примеси H2SO4 и H2O переводимые в кубовый остаток.
Принципиальная схема отделения ректификации HF:
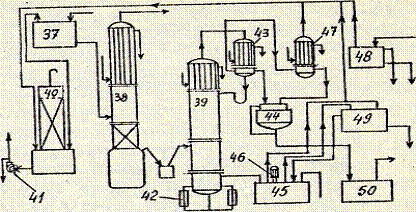
37 - напорный бачек для сырца; 38 - отпарочная колонна; 39 -
ректификационная колонна; 40 - абсорбционная колонна; 41 - насос; 42 - выносной
куб ректификационной колонны; 43, 47 - конденсаторы; 44 - промежуточный сборник
HF; 45 - сборник кубового остатка;46 -
погружной насос; 48 - приёмник H2SO4; 49 - напорный бак; 50 - цистерна с HF.
К недостаткам пирогидролитического разложения флюоритовых руд в его
современном варианте относится повышенный расход энергии и невозможность
производства безводного фторида. Однако здесь в переработку могут быть включены
бедные руды и отходы производства[3].
3. Химические и физические свойства исследуемых веществ
.1 Фторид натрия
По внешнему виду NaF - кристаллический порошок белого или серого цвета в
зависимости от содержания в нем примесей. По ГОСТ 2871-67 высший сорт NaF содержит 94%, а первый сорт - 84%
основного вещества. Он широко применялся в качестве инсектицида для борьбы с
некоторыми видами вредных насекомых, для уничтожения грызунов, для консервации
древесины, для борьбы с вредителями в с/х, для фторирования воды, при
изготовлении флюсов и эмалей и обезлиствования хлопчатника перед его уборкой. В
настоящее время основным потребителем NaF является алюминиевая промышленность.
Свойства NaF[7]:
Плотность Г/см3……………………………2,766
C0p, Дж/(Моль•К)…………………………..46,82
ΔH0обр, КДж/Моль………………………….-576,6
S0298, Дж/(Моль•К)………………………….51,6
ΔC°обр, КДж/Моль………………………….-542,6
ΔN°пл, КДж/Моль………………………….34,25
ΔH°возг, КДж/Моль………………………….280,7
Фтористый натрий, NaF, соль; бесцветные кристаллы, плотность 2,79 г/см3,
tпл=992°С. Растворимость в воде (%):
3,90 (20°С), 4,83 (100°С). В природе NaF встречается в виде минерала вильомита. В промышленности его получают
спеканием плавикового шпата с содой и кремнезёмом по реакции:
СаF2 + Nа2СО3 + SiO2 = 2NaF +
СаSiO3 + СО2
Служит для консервирования древесины, иногда как
инсектицид; входит в состав эмалей. Кислый NaF - натрия гидрофторид NaНF2, применяется как составная часть
флюсов при пайке алюминия.
На криолитовых заводах NaF получают путем обработки раствора НF содой:
НF+ Nа2СО3 = 2NaF + СО2 + Н2O
Осадок NaF
отделяют от маточного раствора фильтрацией. Полученную пасту NaF сушат при (130-140)°С. Как
промежуточный продукт NaF
образуется при спекании смеси СаF2, SiO2 и Nа2СО3
по реакции:
СаF2+ Na2СО3 + SiO2=2NaF +СаSiO3+ СО2
С последующим выщелачиванием NaF водой.
Значительный интерес представляет получение NaF из кремнефторсодержащих газов
заводов по производству фосфорных удобрений. В качестве исходного продукта
заслуживает внимания Na2SiF6. Существует несколько способов переработки Na2SiF6 на NaF.
От способа переработки зависит чистота продукта.
Получение фтористого натрия суспензионным способом
Содосуспензионный способ получения NaF основан на взаимодействии Na2SiF6 с Na2СО3 в присутствии воды:
Na2SiF6 + 2 На2СО3
= 6 NaF + 2СО2 + SiO2
В результате экзотермической реакции образуется NaF в смеси с SiO2.
Для полноты прохождения реакции необходимо
дополнительно подогревать реакционную смесь до 70°С и перемешивать ее в течение
30 мин. При этом удается получить NaF с содержанием около 75% основного вещества.
Получение фтористого натрия термическим способом
Исторически термический способ был первым способом
получения NaF. Он был предложен С.И. Вольфковичем
в 1925 г. [10] и заключается в разложении Na2SiF6 при
прокаливании в интервале температур 580-620°С
Na2SiF6=2 NaF + SiF4-25,8 ккал.
Выделяющийся при разложении SiF4 абсорбируется водой и в дальнейшем при обработке
раствором поваренной соли образует Na2SiF6. Упругость
диссоциации Na2SiF6 составляет 786 мм рт. ст. при 894,5°С [11, 76].
Промышленные испытания этого способа во вращающейся трубчатой печи показали
возможность получения продукта, содержащего 87-89% NaF.
По данному способу получается низкосортный NaF. Это связано прежде всего с тем, что
обогрев печи ведется изнутри продуктами сгорания углеводородного топлива.
Применение наружного обогрева барабана печи приведет к образованию NaF, практически свободного от
кремнезема. Помимо этого появляется возможность получить поток
концентрированного SiF4, переработка которого будет описана
далее.
Так же фторид натрия очень широко применяется в
медицине. Фармакологические свойства:
. Корректоры метаболизма костной и хрящевой ткани,
микроэлементы. Макро и микроэлементы.
. Стоматологические средства
Нозологическая классификация (МКБ-10): М81.4
. Лекарственный остеопороз. М81.9
. Остеопороз неуточненный. М89.5
. Остеолиз
Применение:
• Остеопороз первичный (постменопаузальный,
пресенильный, сенильный, идиопатический)
• Остеопороз стероидный (профилактика и лечение)
• Локальные остеопатии,
• профилактика кариеса у детей и взрослых, при содержании в питьевой
воде фторидов ниже 0,6 мг/мл [1].
.2 Сульфат натрия
Na2SО4,
бесцветные кристаллы; известен в трех полиморфных модификациях; показатели
преломления: меньший Nр = 1,469, средний Nm = 1,476, больший Ng = 1,481; кристаллизуется из водных
растворов выше 32,384°С. В интервале от - 1,2 до 32,4°С кристаллизуется
декагидрат, от -3,5 до 24,25°С - также метастабильный гептагидрат.
Растворимость безводного натрия сульфата в воде 21,9% по ассе (25°С). Т. кип.
насыщенного водного раствора (29,7% по массе натрия сульфата) 102,88°С. Плохо
растворим в водно-спиртовых средах; растворимость при 20°С в этаноле 0,439% по
массе, метаноле - 2,40%. С К2SО4, Li2SО4 и рядом других образует
непрерывный ряд твердых растворов, с сульфатами Sс и Y -
двойные соли, с SrSО4 -
эвтектику.
Натрий сульфат встречается в природе в виде минералов
тенардита Na2SО4, мирабилита (глауберова соль) Na2SО4•10Н2О, входит в состав астрахонита Na2Мg(SО4)2•4Н2О,
вантгоф-фита Na6Mg(SО4)4,
глауберита Na2Са(SО4)2
и другие наиболее крупные запасы сульфата натрия в СССР, США, Чили, Испании.
На хим. предприятиях сульфат натрия получают как
побочный продукт при производстве соляной кислоты, соединений Сг, утилизации
сульфатных щелоков в производстве искусственного волокна на металлургических
заводах и т.д. Сульфат натрия - компонент шихты в производстве стекла;
используется при сульфатной варке целлюлозы, при крашении хлопчатобумажных
тканей; сырье для получения силикатов Na, Na2S, Н2SО4,
соды и др.; компонент осадительной, ванны в производстве вискозного волокна;
глауберова соль-слабительное средство. ПДК в воздухе рабочей зоны 10,0 мг/м3
[2].
Плотность Г/см3……………………………2,663
C0p, Дж/(Моль•К)…………………………..128,04
ΔH0обр, КДж/Моль………………………….-1387,9
S0298, Дж/(Моль•К)………………………….149,58
.3 Серная кислота
Серная кислота Н2SО4, мол. м. 98,082; бесцветная маслянистая
жидкость без запаха. Очень сильная двухосновная кислота. Серная кислота
отвечающая 100%-ному содержанию Н2SО4, имеет состав (%): Н2SО4 99,5, НSО4-0,18, Н3SО4+0,14, Н3О+
0,09, Н2S2О7 0,04, НS2О7-0,05. Смешивается с водой и SО3 во всех соотношениях. В
водных растворах серная кислота практически полностью диссоциирует на Н+,
НSО4- и SО42-.
С повышением температуры усиливается диссоциация Н2SО4↔Н2О +SО3 - Q. При повышении концентрации и
понижении температуры теплопроводность λ уменьшается: λ = 0,518 + 0,0016t - (0,25 + t/1293)•С/100,
где С-концентрация серной кислоты, в %. Максимальную вязкость имеет олеум Н2SО4•SО3, с повышением
температуры η снижается. Серная кислота -довольно сильный окислитель,
особенно при нагревании.
Разбавленная Н2SО4 взаимодействует со всеми металлами,
находящимися в электрохимическом ряду напряжений левее водорода, с выделением Н2.
Окислит, свойства для разбавыленной Н2SО4 нехарактерны. Серная кислота дает два ряда
солей: средние-сульфаты и кислые-гидросульфаты.
Получение. Сырьем для получения серной кислоты
служат: S, сульфиды металлов, Н2S, отходящие газы теплоэлектростанций,
сульфаты Fе, Са и др. Основные стадии получения
cерной кислоты: 1) обжиг сырья с
получением SО2; 2) окисление SО2 до SО3 (конверсия); 3)
абсорбция SО3.
Производство серной кислоты из серы по методу двойного
контактирования и двойной абсорбции состоит из следующих стадий. Воздух после
очистки от пыли подается газодувкой в сушильную башню, где он осушается 93-98%
-ной серная кислота до содержания влаги 0,01% по объему. Осушенный воздух
поступает в серную печь после предварительного подогрева в одном из
теплообменников контактного узла. В печи сжигается сера, подаваемая форсунками:
S+О2 → SО2 +297,028 кДж. Газ,
содержащий 10-14% по объему SО2,
охлаждается в котле и после разбавления воздухом до содержания SО2 9-10% по объему при 420
°С поступает в контактный аппарат на первую стадию конверсии, которая протекает
на трех слоях катализатора (SО2
+ 1/2Ог →SО3 + 96,296 кДж), после чего газ охлаждается в
теплообменниках. Затем газ, содержащий 8,5-9,5% SО3, при 200°С поступает на первую стадию абсорбции
в абсорбер, орошаемый олеумом и 98%-ной серной кислотой: SО3+Н2О→Н2SО4+130,56кДж. Далее газ
проходит очистку от брызг серной кислоты, нагревается до 420°С и поступает на
вторую стадию конверсии, протекающую на двух слоях катализатора. Перед второй
стадией абсорбции газ охлаждается в экономайзере и подается в абсорбер второй
ступени, орошаемый 98% - ной серной кислотой, и затем после очистки от брызг
выбрасывается в атмосферу [1].
Свойства серной кислоты [7]:
Плотность Г/см3……………………………2,766
C0p, Дж/(Моль•К)…………………………..138,9
S0298, Дж/(Моль•К)………………………….156,9
ΔH°пл, КДж/Моль………………………….10,73
η, 10-3 Па•с………………………………....
24,74
Т.пл., °C…………………………………… 10,31
Т.кип., °C …………………………………. 279,6
ΔH°обр КДж/Моль………………………….-813,99
.4 Фтористый водород
Свойства HF[7]:
C0p, Дж/(Моль•К)…………………………..29,14
ΔH0обр, КДж/Моль…………………………. -273,3
S0298, Дж/(Моль•К)………………………….173,675
Т.пл.,°C ……………………………………… -83,36
Т.кип.,°C …………………………………….. 19,52
t крит., °C ……………………………………. 230
p крит., МПа ………………………………… 6,49
Фтороводород, бесцветный газ или подвижная жидкость,
дымящая на воздухе.
Характерное свойствово НF - склонность к ассоциации. Средняя степень ассоциации в
жидкости п = 6. В газовой фазе могут присутствовать линейные и циклические
олигомеры с n = 4, 6-12.
Фтороводород реагирует со мнногими простыми веществами
с образованием фторидов, с оксидами - оксифторидов или фторидов, замещает
галоген в галогенидах металлов, с фторидами щелочных и др. одновалентных
металлов образует гидрофториды металлов, с фторидами и оксифторидами многих
элементов в присутвие воды - фторсодержащие кислотыты.
Фтороводород к неограниченно растворяется в воде с
образованием фтористоводородной кислоты. Сам НF - хороший растворитель для многих веществ.
Фторид водорода - сильная кислота, функция кислотности
Гаммета -15,05, однако даже небольшой избыток фторид-ионов резко ее снижает.
Основной способ получения НF - реакция флюорита СаF2 с Н2SО4, которую проводят в трубчатых вращающихся и шнековых печах
при 120-180°С. Реакционные газы очищают от пыли, конденсируют из них НF и подвергают его двухступенчатой
ректификации. Менее распространены сернокислотное разложение NН4HF2 и термическое разложение NН4HF2. В лаборатории НF удобно получать термическим
разложением гидрофторидов.
Фтористый водород - катализатор гидрирования,
дегидрирования, алкилирования в органической химии, реагент в производстве
хладонов и фторопластов, исходное вещество для получения F2
Фтороводород раздражает дыхательные пути, является
сильнейшим водоотнимающим веществом и при попадании на кожу вызывает
образование долго не заживающих язв, а при длительной экспозиции - обугливание.
ПДК в атмосфере воздухе 0,005 мг/м3, в воде 0,05 мг/л.
Жидкий фтороводород хранят в стальных герметичных
танках и цистернах, а также в баллонах аммиачного типа, имеющих защитную
окраску с красной полосой [1].
.5 Гексафторалюминат натрия
Na3AlF6[7]
C0p, Дж/(Моль•К)…………………………….216
ΔH0обр, КДж/Моль…………………………..-3312
ΔG0обр, КДж/Моль……………………………-3148
S0298, Дж/(Моль•К)……………………………238
Т.пл.,°C ……………………………………… 1011
Плотность, г/см3………………………………2,97
Гексафтороалюминат натрия Nа3А1F6
- бесцветные
кристаллы, плохо растворим в воде (0,42% по массе при 25°С) и органических
растворителяхрителях. Взаимодействует с концентрированной Н2SО4, при нагревании
гидролизуется парами воды. Расплав Nа3 А1F6 электропроводен и является хорошим
растворителем для А12О3 и др. оксидов. Криолит получают
действием Na2СО3 или NaF на раствор А1(ОН)3 или А12О3
в НF, взаимодействием водных растворов А1F3 и NaF,
взаимодействием А1(ОН)3 и Nа2СОз или NaAlO2 с водным раствором NН4F.
Криолит - редкий в природе минерал, основной компонент
(80-85%) электролита в производстве Аl, металлургический флюс, компонент стекол и эмалей, наполнитель резин.
Вывод:
В аналитическом обзоре описана технология производства
фтористых солей алюминия с получением криолита, фторида натрия и фторида
алюминия. Рассмотрена технология получения фтороводорода.
Приведены основные химическое и физическое свойства веществ,
вступающих в выше перечисленных переделах.
Отходами производства фторида алюминия являются
фтористый натрий и криолит.
Эти отходы складируются на предприятиях и не
перерабатываются, но в них содержится ценный компонент - F. Который можно извлекать, действуя
на NaF и Na3AlF6 серной
кислотой.
4. Теоретическая часть
.1 Термодинамика процесса
Термодинамический расчет основан на законе сохранения и превращения
энергии, являющимся наиболее общим законом природы. Этот закон используется в
форме первого закона термодинамики. Точнее, термодинамический аппарат основан
на законе сохранения энергии и принципе существования энтропии, на базе которых
получено основное уравнение термодинамики. Это объясняет универсальность
термодинамического аппарата, достоверность выводов термодинамики, всех ее
уравнений и зависимостей, равно достоверности закона сохранения энергии.
Основные понятия и термины.
Термодинамикой называется наука, изучающая законы превращения энергии и
особенности процессов этих превращений.
Термодинамика, изучающая превращения энергии в химических реакциях и
исследующая возникающие при этом тепловые явления, называется химической
термодинамикой.
Применение термодинамических методов для исследования химических реакций
в настоящее время дает возможность установить, какие из реакций в
рассматриваемой системе при заданных температуре, давлении и концентрациях
могут протекать самопроизвольно (т. е. без затраты работы извне), каков предел
их самопроизвольного протекания (т. е. каково положение равновесия) и как
следует изменить эти условия, чтобы процесс мог совершаться в нужном
направлении в требуемой степени.
При этом наиболее часто используют данные об изменении энтальпии (∆Н),
теплоемкости (∆CP), энтропии (∆S),
энергии Гиббса (∆G) и о
константе равновесия (К)
Энтальпия - функция состояния термодинамической системы при независимых
параметрах энтропии S и давлении р,
связанная с внутренней энергией U
соотношением:
H = U + pV,
где V - объем системы.
Энтропия - функция состояния термодинамической системы, изменение которой
(dS) в равновесном процессе равно
отношению количества теплоты (dQ),
сообщенного системе или отведенного от неё, к термодинамической температуре (Т)
системы: dS = dQ/T.
Теплоемкость - отношение количества теплоты, полученного телом (веществом)
при бесконечно малом изменении его состояния в каком-либо процессе, к
вызванному им приращению температуры.
Гиббса энергия (изобарно-изотермический потенциал, свободная энтальпия) -
функция состояния термодинамической системы, определяемая равенством:
G = H - TS,
где H - энтальпия, T - абсолютная температура, S - энтропия.
Константа равновесия - величина, количественно выражающая закон
действующих масс и связанная со стандартным изменением энергии Гиббса ∆G0 соотношением: ln Kp = -∆G/RT. Константа
равновесия выражает взаимную зависимость между концентрациями веществ в системе
при достижении равновесия и характеризует степень направленности реакции в
сторону образования тех или иных продуктов.
Принципиальная осуществимость процесса определяется знаком ∆G: если при заданных условиях ∆G < 0, то реакция возможна, если ∆G > 0, то реакция неосуществима;
при ∆G = 0 система находится в равновесии.
Значение ∆G (при ∆G < 0) позволяет установить,
насколько изучаемая система далека от состояния равновесия.
Если при ∆G <
0 реакция не идет, то это указывает лишь на необходимость преодоления
тормозящих реакцию препятствий (как правило, низких температур) и вывода
системы из состояния ложного равновесия.
Таким образом, реакция может не протекать как вследствие близости к
состоянию равновесия, так и вследствие торможения. Для того, чтобы вызвать
реакцию, в первом случае необходимо изменить условия ее протекания, а во втором
- ее скорость. В заторможенной системе реакция может быть возбуждена
нагреванием.
Без знания термодинамики процесса нельзя указать, какая доля наблюдаемого
эффекта в каждом отдельном случае обусловлена изменением скорости, и какая -
смещением равновесия.
Проведем термодинамический расчет процесса взамодействия фторида натрия и
серной кислоты.
2NaF+H2SO4 →Na2SO4+2HF
Таблица 4.1
Значения термодинамических параметров веществ, учавствующих в реакции
|
вещество
|
ΔH0обр, КДж/Моль
|
S0298, Дж/(Моль•К)
|
C0p,
Дж/(Моль•К)
|
|
NaF
|
-576,6
|
51,6
|
46,82
|
|
H2SO4
|
-813,99
|
156,9
|
138,9
|
|
Na2SO4
|
-1387,9
|
149,58
|
128,04
|
|
HF
|
-273,3
|
173,675
|
29,14
|
|
Na3AlF6
|
-3312
|
238
|
216
|
|
Na2SO4
|
-1387,9
|
149,58
|
128,04
|
|
Al2(SO4)3
|
-3444,1
|
239,4
|
259,6
|
Определив константу равновесия можно судить о направлении процесса. Если
Kp>1, то направление реакции в сторону образования продуктов реакции. Изменение
энергии Гиббса определяются:
Расчет ведем по следующим формулам:
∆GT =∆H298 - T∆S298 + ∆Cp0 (T-298-T ln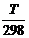 )
)
∆G298=∆H298 - T∆S298
∆G
= ∆Hp - T∆S, где:
∆Hp
- тепловой эффект реакции, кДж/моль;- температура протекания процесса;
∆S
- изменение энтропии, Дж/моль.
Константу
равновесие химической реакции определяют по формуле:Kp = -∆G/2,3RT, где:
∆G
- изменение энергии Гиббса;- универсальная газовая постоянная;
Полученные
данные сводим в таблицу:
Таблица 4.2
Энергия Гиббса и константа равновесия выше указанной реакции
|
T, K
|
300
|
400
|
500
|
600
|
700
|
800
|
900
|
1000
|
|
∆G, Дж/моль•K
|
-12527
|
-12550
|
-12572
|
-12593
|
-12613
|
-12632
|
-12651
|
-12670
|
|
Kp
|
21
|
16
|
13
|
10
|
94
|
82
|
73
|
66
|
Тепловой эффект реакции определяется по формуле:
DHреакц=-1387.9-2•(-273.3)+2•576.6+813.99=
32.69 кДж/моль.
В результате проведения термодинамического расчета мы посчитали энергию
Гиббса и константу равновесия данной химической реакции и убедились, что
реакция между фторидом натрия и серной кислотой будет осуществляться при любых
температурах и будет смещена в сторону образования продуктов реакции.
Посчитаем термодинамические свойства второй реакции:
2Na3AlF6+6H2SO4→3Na2SO4+Al2(SO4)3+12HF
По исходным данным также как в предыдущей реакции рассчитываем энергию
Гиббса и константу равновесия реакции.
Таблица 4.3
Энергия Гиббса и константа равновесия выше указанной реакции
|
T, K
|
300
|
400
|
466
|
500
|
600
|
700
|
800
|
900
|
1000
|
|
∆G, кДж/моль•K
|
214
|
83
|
0
|
-41
|
-160
|
-275
|
-385
|
-492
|
-596
|
|
Kp
|
-38
|
-11
|
0,02
|
4
|
13
|
20
|
25
|
28
|
31
|
В результате полученных данных мы можем сказать, что реакция между Na3AlF6 и H2SO4 при температуре до 466 К не будет
осуществлятся. При температуре более 466 К реакция пойдет. По результату
константы равновесия мы можем сказать, что при температуре более 466°C реакция
будет направлена в сторону продуктов реакции.
Посчитаем енергию Гиббса и константу равновесия побочных реакций:
Таблица 4.4
Значения термодинамических параметров веществ, учавствующих в реакции
|
Вещество
|
∆H0обр,
КДж/моль
|
S0298, Дж/(Моль•К)
|
C0p,
Дж/(Моль•К)
|
|
SiO2
|
-861,5
|
278
|
42,97
|
|
HF
|
-273,3
|
173,6
|
29,14
|
|
SiF4
|
-1614,9
|
282,65
|
29,1
|
|
H2O
|
-242
|
278
|
75,3
|
|
H2SO4
|
-813,9
|
156,9
|
138,9
|
|
FeF3
|
|
|
|
Найдем энергию Гиббса и константу равновесия для первой реакции:
1) SiO2+4HF=SiF4+2H2O
Таблица 4.5
Энергия Гиббса и константа равновесия выше рассчитанной реакции
|
T, K
|
300
|
400
|
500
|
600
|
700
|
800
|
900
|
1000
|
1100
|
1193
|
1200
|
|
∆G,
кДж/моль•K
|
-104
|
-91
|
-78
|
-66
|
-55
|
-43
|
-32
|
-21
|
-10
|
0
|
1
|
|
Kp
|
18
|
11
|
8
|
5
|
4
|
2
|
1,5
|
1
|
0,3
|
0,01
|
-0,2
|
По полученным данным можно сказать что реакция между диоксидом кремния и
фтороводородом в нашем случае и при нашей температуре будет проходить.
Анализируя данные можно сказать, что при температуре более чем 1193 К реакция в
сторону образования продуктов идти не будет, так как ∆G=0 при температуре
1193 К [5].
4.2 Источник ошибок при расчете равновесия
Ошибки, обусловленные неточностью экспериментальных данных
Ошибки могут быть вызваны неизотермическими условиями при измерении
равновесия. Источником ошибок может быть весьма малая скорость реакции, когда
практически невозможно достигнуть равновесия. Очень большая скорость реакции, в
свою очередь, приводит к серьезным затруднениям при анализе равновесия смеси.
Кроме того, исследуемая реакция может не дойти до состояния равновесия.
Критерием достижения равновесия обычно служит неизменность состава смеси,
выходящей из зоны реакции, с изменением объемной скорости. Ошибки могут
появиться, если не будет учтено влияние степени измельчения.
Неточность значений ∆H
служит, как правило, источником гораздо больших ошибок, чем погрешность
значений S, даже если энтропии оценены
расчетным путем.
Надежность результатов косвенного расчета ∆G зависит от точности, с которой могут быть определены эти
величины в используемых для расчета реакциях. Поэтому, когда искомая величина
невелика, ошибка может стать весьма большой, особенно если отдельные ошибки
имеют одинаковые знаки.
Ошибки, связанные с обработкой экспериментальных данных
Ошибки могут возникнуть в результате применения уравнения, в которое в
условиях опыта не точно. Поэтому, прежде чем выбирать то или иное приближенное
уравнение, следует оценить величину заведомо вносимой ошибки, сопоставив ее с
надежностью исходных данных и с требуемой точностью результатов вычислений.
Теоретическая и практическая степени протекания реакции
В практических условиях, реакции редко доходят до равновесия, и степень
их протекания зависит от многих факторов, в первую очередь, от скорости
процесса, роль которой особенно велика при одновременном или последовательном
протекании ряда реакций. Следовательно, пренебрежение кинетикой процесса может
привести к большим ошибкам и вместе с тем к невольному умалению значения
термодинамики в решении практических вопросов.
В некоторых случаях в результате реакции образуются не те вещества, которые
должны были бы получиться при данных температуре, давлении и концентрации.
Вместо предполагаемой реакции идет другая, хотя условия для нее неблагоприятны.
Это может означать, что первая реакция обладает, в данных условиях, ничтожной
скоростью, в то время как вторая протекает очень быстро. Ясно, что в подобных
случаях увеличение длительности процесса приведет к изменению состава смеси.
Поскольку практическая степень протекания реакции зависит от длительности
процесса, все факторы, увеличивающие скорость реакции, вместе с этим
увеличивают и степень превращения за любой промежуток времени, недостаточный
для установления равновесия. Общими факторами, влияющими и на кинетику, и на
статику процессов, являются температура, давление и концентрация реагентов.
4.3 Теоретические основы получения фтороводорода из фторида
натрия
Отходом алюминиевой промышленности являются фторосодержащие вещества -
это фторид натрия и гексафторалюминат натрия. В моём проекте рассмотрена
переработка фторида натрия. Целью его переработки является продукт HF-сырец с содержанием жидкого
фтороводорода 99%.
.5 Описание технологической схемы
Общетехнологическая схема включает следующие процессы:
• Сернокислотное разложения фторида натрия в барабанной врвщающейся
установке;
•Очистка газов от пыли и основной массы серной кислоты и воды в
грязевиковой колонне;
•Охаждение газа до температуры 25⁰C
• Выделение HF из реакционных
газови в конденсаторе;
• Обезвреживание отходов и утилизация побочных продуктов.
Из бункера поз. А 101 поступает NaF на шнековый питатель поз. А 103, по которому идет в установку
сульфатизации поз. А 104. одновременно из бункера поз. А 102 поступает H2SO4 в установку сульфатизации поз. А 104. Где происходит
смешение NaF с H2SO4 и разложение NaF. В результате разложения образуется
фтористый водород и сульфат натрия. Так как NaF содержит примеси диоксид кремния и фтридторид железа,
то в установке сульфатизации наряду с выше указанной реакцией протекает реакция
взаимодействии SiO2 с NaF с образованием SiF4 и H2O. Вторая реакция взаимодействия FeF3 с серной кислотой, продуктами реакции является Fe2(SO4)3 и НF. Через нижний разгрузочный бункер
выходит Na2SO4 и идет на гашение известью поступающей из поз А 105, чтобы
нейтрализовать остатки серной кислоты и далее идет в поз. А 107. Серная кислота
поступает в емкость поз. А 108 и перекачивается насосом поз. А 109 в емкость
поз. А 102.
Через верхнюю часть установки сульфатизации выходит газообразные продукты
и далее по газоходу поступает в «грязевик» поз. А 110.
После отчистки газа от пыли и серной кислоты в «грязевике», серная
кислота удаляется через нижнюю часть колонны насосом поз. А 111 в ёмкость поз.
А 102.
Из «грязевика» поз. А105 газ поступает на охлаждение в форконденсаторе
поз. А 112 до температуры 25⁰C. В качестве хладогента используется техническая вода
с температурой 20⁰C,. Далее газ поступает в конденсатор поз. А 113. В качестве
хладогента в конденсаторе используется рассол с начальной температурой -10⁰C. Температура кипения фтороводорода
составляет 19,5⁰C а четырехфтористого кремния -89⁰C, поэтому SiF4 конденсироваться не будет и удаляется через верхнюю
часть конденсатора унося с собой часть фтороводорода. на выходе из конденсатора
мы имеем практически чистый продукт HF-сырец который поступает в сборник поз. А 114.
SiF4 поступает
на улавливание фтороводорода серной кислотой в абсорбере поз. А 116.
Абсорбционные газы подаются в нижнюю часть абсорбера а серная кислота в верхнюю
часть. Через нижнюю часть абсорбера выходит насыщенный абсорбент и поступае в
промежуточный сборник, затем насосом поз. А 118 транспортируется в «грязевик»
поз. А 110. SiF4 выходит через верхнюю часть абсорбера и по газоходу
поступает на абсорбцию водой в нижнюю часть абсорбера поз А 117, в верхнюю
часть абсорбера подается вода. H2SiF6 удаляется через нижнюю часть абсорбера и поступает в
сборник H2SiF6 поз. А119.На рисунке 4.1 изображена схема получения
фтористого водорода и фтористого натрия.
5. Расчетная часть
.1 Расчет барабанно-вращающейся установки сульфатизации
.1.1 Материальный расчет
Целью данного расчета является определение расхода реагентов для
проведения технологического процесса. Исходя из суточной массы
перерабатываемого фторида натрия определим количественную массу веществ,
вступающих в химическую реакцию.
Таблица 5.1
Состав фторосодержащего компонента
|
Фторосодержащего компонента
NaF SiO2 FeF3 H2O
|
% 98 1.1 0.5 0.4
|
|
Избыток серной кислоты, %
|
20
|
|
Время процесса, час
|
3
|
|
Степень разложения NaF, %
|
98,6
|
|
Производительность
фторосодержащему компоненту, кг/ч
|
208.3
|
Реакции протекающие в процессе:
2) 2NaF+H2SO4 →Na2SO4+2HF
3) SiO2+4HF=SiF4+2H2O
4) 2FeF3+3H2SO4=Fe2(SO4)3+6HF
Учитывая состав фторосодержащего реагента, определим расход каждого
химического соединения:
GNaF=98•208,3/100=204,134 кг/ч;
GSiO2=1,1•208,3/100=2,29
кг/ч;
GFeF3=0,5•208,3/100=1.04
кг/ч;
GH2O=0,4•208,3/100=0,83
кг/ч.
Расчет реакции 1
,134 Х1 Х2 Х3
2NaF+H2SO4 →Na2SO4+2HF
84 98 142 40
Расход серной кислоты с избытком:
GH2SO4=GNaF•MH2SO4/MNaF•β,
где β=1,2 - коэффициент избытка серной кислоты,
G H2SO4(изб.)=204.134•98/84•1.2=285.78 кг/ч.H2SO4(ост.)= G H2SO4(изб.)- GNaF MH2SO4/MNaF•α,
где α - степень разложения NaF.
H2SO4(ост.)= 285.78-204,134•98/84•0,99=50кг/ч.
Расход
Na2SO4:
Na2SO4= GNaF•α•M Na2SO4/ MNaF=204,134•0,99•142/84=341.63кг/ч.
Расход
HF:
HF= GNaF•MHF/ MNaF•α=204.134•40/84•0.99=96.23кг/ч.
Непрореагировавший NaF
NaF(ост)= GNaF(1-α)=204.134•0.01=2.041 кг/ч.
Составляем таблицу материального баланса этой реакции
Таблица 5.2
Материальный баланс выше указанной реакции
|
Приход
|
кг/ч
|
Расход
|
кг/ч
|
|
1 NaF 2 H2SO4(изб)
|
204.134 285.78
|
1 NaF(ост) 2 Na2SO4 3 HF 4 H2SO4(ост)
|
2.041 341.63
96.23 50
|
|
Итого
|
489.9
|
Итого
|
489.9
|
Расчет реакции 2
SiO2+4HF=SiF4+2H2O
6 0 80 104 36HF=GSiO2•MHF/MSiO2=2,29•80/60=3.05
кг/ч,SiF4= GSiO2•MSiF4/
MSiO2=2.29•104/60=3.97 кг/ч,H2O= GSiO2•MH2O/
MSiO2=2.29•36/60=1.374 кг/ч.
Составляем таблицу материального баланса.
Таблица 5.3
Материальный баланс выше указанной реакции
|
Приход
|
кг/ч
|
Расход
|
кг/ч
|
|
1 SiO2 2 HF
|
2,29 3,05
|
1 SiF4 2 H2O
|
3,97 1,374
|
|
Итого
|
5,34
|
Итого
|
5,344
|
Расчет реакции 3
2FeF3+3H2SO4=Fe2(SO4)3+6HF
294 400 120H2SO4=GFeF3•M H2SO4/M
FeF3=1.04•294/226=1.35 кг/ч,Fe2(SO4)3= GFeF3•M
Fe2(SO4)3/ M FeF3=1.04•400/226=1.84 кг/ч,HF= GFeF3•M HF/ M FeF3=1.04•120/226=0.552
кг/ч.
Составляем таблицу материального баланса
Таблица 5.4
Материальный баланс выше указанной реакции
|
Приход
|
кг/ч
|
Расход
|
кг/ч
|
|
FeF3 H2SO4(изб)
|
1,04 1,35
|
Fe2(SO4)3 HF
|
1,84 0,552
|
|
Итого
|
2,39
|
Итого
|
2,39
|
Таблица 5.5
Суммарный материальный баланс
|
Приход
|
Расход
|
|
Статьи прихода
|
кг/ч % от общего
|
Статьи расхода
|
кг/ч % от общего
|
|
1NaF 2 SiO2 3
H2SO4 4 HF 5 FeF3 6 H2O
|
204.134 40,96 2.29 0,46
287,13 57,33 3.05 0,61 1.04 0,2 0,83 0,17
|
1 HF 2 SiF4 3
H2O 4 Na2SO4 5 Fe2(SO4)3 6 NaF 7
H2SO4(ост)
|
96.78 19,42 3.97 0,79 2.204
0,44 341.63 68,55 1,84 0,37 2.041 0,41 50 10,03
|
|
Итого
|
498.4 100
|
Итого
|
498.4 100
|
Выходящие из установки газы содержат сравнительно большое количество
пыли, паров серной кислоты, воды и газообразных примесей. Их подают в аппарат
предварительной очистки, чаще называемый «грязевиком». Это круглая или
квадратная в сечение башня, иногда содержащая инертную насадку.
Посчитаем массу и содержанием газа выходящие из «грязевика». В грязевике
газ также частично отчищается от серной кислоты и воды. По расчетам
материального баланса барабанной установки расход второводорода 96,78 кг/ч, SiF4 3,97 кг/ч. Общая расход газа равен 96,78+3,97=100,75
и плюс 3% от этого газа серной кислоты «пар» и 2% воды «пар». Расход газа равен
100,75+3,0225+2,015=105,787 кг/ч[9].
.1.2 Тепловой расчет
Тепловой расчет процесса сульфатизации включает в себя определение
тепловых потоков и составление таблицы теплового баланса.
Так как реакция взаимодействия фторида натрия с серной кислотой идет при
комнатной температуре, поэтому подвод тепла не нужен.
Расчет тепловых потоков проводится на основании уравнения теплового
баланса, которое в общем виде запишется по формуле:
∑Qприх.= ∑Qрасх.,
где ∑Qприх. - количество тепла, вносимое в
аппарат с исходными веществами, кДж/ч;
∑Qрасх.- количество тепла, уносимое из
аппарата продуктами аппарата и теряемое в окружающую среду, кДж/ч
• Приход
тепла:
NaF
Q1=m NaF•C NaF •t н=204,134•128,04•20/84=6223,17 Дж/ч;
H2SO42=m H2SO4•C H2SO4•tн=287,13•138,9•20/98=8139,25 Дж/ч;2O3=m H2O•C H2O•t н=0,83•33,57•20/1=557.26Дж/ч;4=mHF •CHF •tн =3,05•29,14•20/40=44,44 Дж/ч;
• Расход тепла:
С газовой фазой, в том числе:
HF
Q5.1=m HF•C HF •t н=96,22•29,14•20/40= 1401.9Дж/ч;
Q5.2 m HF•C HF •t н=0,552•29,14•20/120=2.7 Дж/ч;
Na2SO46=m Na2SO4 •C
Na2SO4 •t н=341.63•128,4•20/142=6178.2 Дж/ч;7=m NaF•C
NaF •t н=2,041•128,04•20/84=62.2 Дж/ч;2O8=m
H2O•C H2O•t н=1,374•33,57•20/36=25.62Дж/ч;2SO4(ост)9=m H2SO4•C H2SO4•tн=50•138,9•20/98=1417.34Дж/ч;410=m SiF4•C SiF4 •tн=3.97•73.6•20/104=66.19Дж/ч;
Тепловой эффект реакции определяется по формуле:
DHреакц. = DHNa2SO4 + 2DHHF - 2DHNaF - DHH2SO4;
DHреакц=-1387.9-2•(-273.3)+2•576.6+813.99=
32.69кДж/моль.
Определим тепло реакции:
Qреакции = (204.134•32.69)/84 =79.44 кДж/ч
.1.3 Конструктивный расчет барабанной вращающейся установки
Конструкция барабанной печи
Барабанная вращающаяся печь состоит из барабана, наклоненного к горизонту
под углом 20. Барабан приводится во вращение электродвигателем через
редуктор и цепную передачу.
Таблица 5.6
Тепловой баланс
|
Статья прихода
|
Количество тепла, кДж/ч
|
Статья расхода
|
Количество тепла, кДж/ч
|
|
с NaF
Q1
|
6.223
|
с HF Q5.1
|
1.402
|
|
|
с HF Q5.2
|
0.0027
|
|
с H2SO4 Q2
|
8.139
|
с Na2SO4 Q6
|
6.178
|
|
с H2O Q3
|
0.557
|
с NaF Q7
|
0.0622
|
|
с HF Q4
|
0.044
|
с H2O Q8
|
0.0256
|
|
Q потерь
|
73,69
|
с H2SO4(ост) Q9
|
1,4173
|
|
|
с SiF4 Q10
|
0.0662
|
|
|
Тепло р. Qр.
|
79.44
|
|
Итого
|
88,59
|
Итого
|
88.59
|
Для передачи давления от масс всех вращающихся частей аппарата, барабан
снабжен бандажами, которые опираются на опорные ролики опорных станций. Для
предотвращения перемещения барабана в горизонтальной плоскости, установлены
упорные ролики опорно-упорной станции.
С одной стороны барабана установлены: бункер загрузки фтористого натрия и
серной кислоты. Загрузка в печь происходит с помощью шнекового питателя.
Движение материала внутри барабана происходит за счет его вращения и наклона к
горизонту. На другом конце барабана снизу установлена камера выгрузки, откуда
выгружается сульфат натрия, остаточная серная кислота и остаточный фторид
натрия. На конце барабана сверху патрубок вывода газов.
.1.4 Конструктивный расчет барабана
Внутренний диаметр и длина барабана определяются по формулам
D =
0,434•GT0,34
L =
2,59•GT0,447,
где GT - суточная производительность печи,
т/сутки;
D -
диаметр барабана, м;
L -
длина барабана, м;
GT=497.9•24/1000=11.9 т/сутки
D=0,4342•Gt0,34=0,4342•11,90,34=0,4342•2,3=0,99
м.
Длина барабана:
L=2.59•
Gt0,447=2,5•11,90,447=7,49м
Принимаем D=1м, L=7,5м.
Определение мощности.
Определим число оборотов барабана:
n =
0,6-1,8 об/мин.
Установочная мощность двигателя определяется по формуле
N=0,0013
•D3•L • ρсм •n •j,
N=0,0013
•13•7,5•2431•1,8•0,09 = 3,8 кВТ
Принимаем с учетом пускового момента 6 = кВт[11]
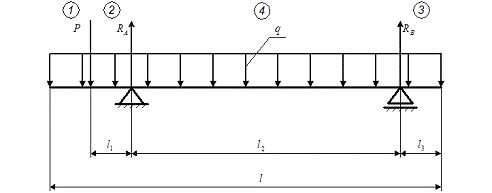
Рисунок 2. Распределение нагрузок на барабан
5.1.5 Прочностной расчет барабана
Прочностной расчет барабана выполняем согласно методике.
Схема распределения нагрузок на барабан показана на рисунке 4.2. Барабан
представляет собой балку постоянного сечения, длиной L=7,5 м с действующей на нее, постоянной по всей длине,
распределенной нагрузкой. Балка установлена на опорах, расстояние между
которыми принимаем равным l2=5 м, расстояние от края барабана до
упорного бандажа (опора А) l1=1 м, от другого края барабана до
опорного бандажа (опора В) l3=1,5 м, расстояние от опорного
бандажа до цепной звездочки l3= 0,5м. Нагрузка от цепной звездочки Q3 = 2 кН.
Расчет барабана на прочность
Толщину стенки барабана выбираем из условия:
Sб
= (0,007…0,01)•D,
Где D - наружный диаметр барабана, м.
Sб=0,007•1=0,007 м.
Принимаем Sб=0,01 м.
Внутренний диаметр барабана
Dв=Dн - 2•Sб=1 - 2•0,01=0,98 м.
Масса материала, находящегося в печи определяется по формуле:
mM=j·ρm•L•π•Dв/4,
mM=0,09•2431•7,5•3,14•0,982/4=1237 кг,
Масса корпуса барабана определяется по формуле:
mK=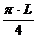 •(DH2-DB2)•ρстали,
•(DH2-DB2)•ρстали,
mK=(3,14•7,5/4)•(12
- 0,982)•7800= 1822кг.
Суммарная
масса барабана и материала:
m=mK + mM =1237 +
1822=3059кг.
Линейная
нагрузка, действующая на барабан, определяется по формуле:
q=mg/L,
q=3059•9,81/7,5=4001Н/м.
Условие
прочности для барабана печи:
σ =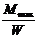 ≤[σ],
≤[σ],
[σ]=25…30 МПа - допускаемое напряжение для аппарата из
стали марки 12Х18Н10Т при рабочей температуре t<7000С;
W - момент
сопротивления сечения барабана, м3;
Ммах
- максимальный изгибающий момент, действующий на барабан, Нм
W=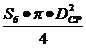 ,
,
Где
Dср -
средний диаметр барабана, м.
W=0,01•3,14•0,992/4=0,008
м3.
Для определения максимального изгибающего момента MZmax построим эпюры поперечных сил QY и изгибающих моментов MZ (рисунок 4.3), для чего определим
реакции опор RA и RB от действия q и Q3.
Составим уравнение моментов всех внешних сил относительно опор, а для
проверки правильности определения реакций опор составим уравнение проекций этих
сил на ось Y:
∑MA=0: RB•l2-P•(l2+l3)-Q•l4=0,
∑MB=0: Q•(l2-l4)-RA•l2-P•l3=0,
∑Y=0: RA+RB-P-Q=0,=q•L=4001 •7,5=
30007 Н.
Из (4.14) выразим RB:
RB=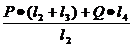 =2000•6,5+30007•2,5/5=17603,5 Н.
=2000•6,5+30007•2,5/5=17603,5 Н.
Из
(4.15) выразим RA:
RA=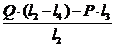 =30007•2,5-2000•1,5/5=14403,5 Н.
=30007•2,5-2000•1,5/5=14403,5 Н.
Проверим
правильность определения реакций опор, подставив значения RA и RB в выражение (4.16), получим:
,5
+ 14403,5 - 2000 -30007=0
=0
- следовательно, реакции опор RA и RB определены верно.
Используя
метод сечений, определим QY и MZ:
Сечение
1-1слева (0<x<l): QY(x1)=-q•x, MZ(x2)=-q•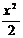 ;
;
При
x=0: QY(x) =0, MZ(x)=0;
При
x=1: QY(x) =-q•1=-4001 •0,5= -2000,5 Н
MZ(x2) =-q•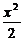 = -4001•
= -4001• = 2000,5
-Н•м
= 2000,5
-Н•м
Сечение
2-2слева (l<x<(l+l2)): QY(x)=RA-q•x, MZ(x)=RA•(x-l)-q•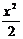 ;
;
При
x=l: QY(x) =RA-q•1=14403,5-4007•1=10396,5 Н,
MZ(x2) =RA•(l-l)-q•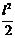 =14403,5 •2,5 - 4007 •52/2= -9749,7 Н∙м;
=14403,5 •2,5 - 4007 •52/2= -9749,7 Н∙м;
При
x=(l+l2): QY(x)=RA-q•(l+l2)=14403,5-
4007 •6= -9639 Н,
MZ(x2) =RA•(l-l+l2)-q•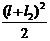 =14403,5 •5-4007•62/2= 115228-84647=-
=14403,5 •5-4007•62/2= 115228-84647=-
Н•м;
При
x=(l+l2/2): QY(x) =RA-q•(l+l2/2)=
14403,5-4007•6/2= 2382 Н,
MZ(x2)=RA•(l-l+l2/2)-q•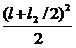 =14403•5 - 4007 •3,52/2=47472 Н•м;
=14403•5 - 4007 •3,52/2=47472 Н•м;
При
x=(l+0,75•l2): QY(x) =RA-q•(l+0,75•l2)=14403 -
4007•4,75= 4630,3 Н,
MZ(x2)=RA•(l-l+0,75•l2)-q•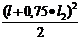 =14403•3,75- 4007 •11,3= 8732
=14403•3,75- 4007 •11,3= 8732
Н∙м;
При
x=(l+0,25•l2): QY(x) =RA-q•(l+0,25•l2)=14403
•4007•2,25= 9001 Н,
MZ(x2)=RA•(l-l+0,25•l2)-q•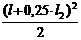 = 14403•1,25- 4007
= 14403•1,25- 4007
•2,5=7985,5Н∙м;
При
x=2 м: QY(x) =0,
MZ(x2) =RA•(4,18-l)-q•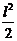 =14403•(4,18 - 1,5) - 4007•22/2 = 20007
Н•м;
=14403•(4,18 - 1,5) - 4007•22/2 = 20007
Н•м;
Сечение
3-3справа (0<x<(l1-l3)): QY(x) = q•x, MZ(x2) =-q•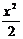 ;
;
При
x=0: QY(x) =0, MZ(x)=0;
При
x=(l1-l3): QY(x) =q•(l1-l3)= 4007 • 0,5 = 2003,5 Н,
MZ(x2) =-q•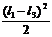 = -4007•0,52/2 = -500Н•м;
= -4007•0,52/2 = -500Н•м;
Сечение
4-4справа ((l1-l3)<x<l1): QY(x)=q•x+P, MZ(x2)=- q•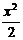 -P•(x-l1+l3);
-P•(x-l1+l3);
При
x=(l1-l3): QY(x)=q•(l1-l3)+P=4007•0,5 +2000= 4003,5 Н,
MZ(x2) =-q•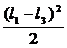 -P•(l1-l3-l1+l3)= -4003 •0,52/2 - 2000•0= -500,4 Н•м;
-P•(l1-l3-l1+l3)= -4003 •0,52/2 - 2000•0= -500,4 Н•м;
При
x=l1: QY(x)=q•l1+P=4007
• 1 + 2000 = 6007 Н,
MZ(x2) =-q•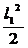 -P•(l1-l1+l3)= -4007
•12/2 - 2000•1= -4003,5 Н•м;
-P•(l1-l1+l3)= -4007
•12/2 - 2000•1= -4003,5 Н•м;
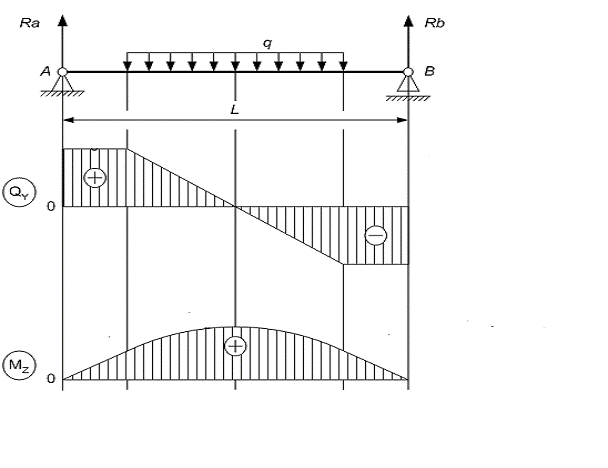
Рисунок
3. Эпюры поперечных сил и изгибающих моментов действующих на барабан
Из расчетов видно, что максимальный изгибающий момент, действующий на
барабан:
MZmax = 20007 Н•м;
Подставив полученные значения MZmax и W в
условие прочности (4.18) получим:
σ=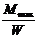 ≤[σ],(4.24)
≤[σ],(4.24)
Условие
прочности выполняется: σ≤[σ], (2,4<25 МПа)
.1.6
Расчет барабана на жесткость
Условие
жесткости для барабана:
Ε = ymax/Dср≤[ε],
где
ymax - суммарный максимальный прогиб от действующих
нагрузок, м;
ε - относительный прогиб;
[ε]=1/200 - допускаемый относительный прогиб (для барабана без
футеровки);
Суммарный
максимальный прогиб от действующих нагрузок:
ymax=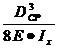 •(0,04•q1+0,002•q2),
•(0,04•q1+0,002•q2),
где
q1 -
линейная нагрузка от массы обрабатываемого материала, Н/м;
где
q2 -
линейная нагрузка от массы барабана, Н/м;
E=1,36•105
МПа - модуль упругости материала корпуса при рабочей температуре (t≤7000C);
Ix=1•sσ3/12 -
момент инерции единичного кольцевого участка барабана, м3.
q1=g•mM/L=9,81•1237/7,5= 1618 Н/м,
q2=g•mK/L=9,81•1822/7,5= 2389 Н/м,
Ix=0,013/12=8,333•10-8
м3,
ymax=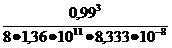 •(0,04•1618+0,002•2389)= 0,9•10-3 м.
•(0,04•1618+0,002•2389)= 0,9•10-3 м.
Подставив
полученные значения в условие жесткости (4.20) получим:
ε=ymax/Dср= 0,9•10-3/1,58= 0,57•10-3,
Условие
жесткости выполняется: ε≤[ε], (0,57•10-3<5•10-3).[9]
.1.7
Расчет бандажа барабанной печи
Для
бандажа барабанной печи принимаем: число башмаков nб=8, диаметр опорного ролика dр=400 мм, угол между опорными роликами 2ψ=600,
материал бандажа и роликов - сталь 45Л (модуль упругости бандажа и опорного
ролика E1=E2=2•105 МПа, допускаемое напряжение на изгиб
[σ]из=50 МПа, допускаемое контактное
напряжение [σ]к=500 МПа).
.1.8
Определение реакций опорных роликов
Реакции
опорных роликов определяются из уравнения равновесия сил
Rоп=-2Т•cos ψ,(4.21)
Где
Rоп - max (RA, RB) - реакция опоры, Н;
Т
- реакция опорного ролика, Н;
2ψ - угол между роликами.
cos ψ=cos(π-β),
следовательно
Т=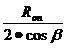 , Т= 17603/2 cos 150o=8380,6
Н.
, Т= 17603/2 cos 150o=8380,6
Н.
.1.9
Определение геометрических размеров бандажа из условия его работы на изгиб и
контактную прочность
Угол
между башмаками
j1=2π/nσ=2•1800/8=450.
Число
башмаков в одном квадранте
n=(nσ-2)/4=(8-2)/4=1,5.
Принимаем
nσ=2.
Сила,
действующая на самый нижний башмак, определяется по формуле:
Q0=4•Rоп/nσ= 4•17603/8=8801 ≈8,8 кН.
Силы,
действующие на башмаки, по формулам:
Q1=Q0•cos j1= 8,8•cos
45=3,29≈ 6,16кН,2=Q0•cos
(2j1)= 4,66•cos
90 =0.
Расчетные
углы для определения пар сил:
Q0: Q0: = 1800;
sin1800=0; cos1800=-1;1: Q0: = 1350;
sin1350= 0,7; cos1800=-0,7;2: Q0: =
900; sin900=1; cos900=0;
β=1500; tg1500=-0,57; cos1500=-0,866;
Средний
диаметр бандажа
Dср = (1,14 - 1,22)• DН =1,2•1=1,2м,
следовательно,
Rср= Dср/2=1,2/2=0,6
м,
Изгибающий
момент в местах приложения сил определяется по формулам:
M00=-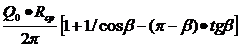 =8,8•0,6/2•3,14[1+1/cos150-(3,14-
=8,8•0,6/2•3,14[1+1/cos150-(3,14-
,61) •tg150]= -0,155 кН•м,01=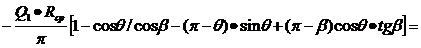
,16•0,6/2•3,14[1-cos135/cos150-(3,14-2,355)sin135+(3,14-2,61)cos135
•tg150]= 0,226+ кН•м,
Суммарный
изгибающий момент в ключевом сечении
М0=М00+М01=
-0,155+0,226=0,071 кН•м.
Нормальное
усилие определяется по формуле:
N0=N00+N01,
N00= - (Q0/2π)[(π - β)•tgβ]= - (8,8/2 •3,14)[(3,14 - 2,61)•tg150]=0,4кН,
N01= -(Q1/π)[(π-θ1)•sin θ1-(π - β)•cos θ1•tgβ]= -(6,16/3,14)[(3,14-
2,355)•sin135-
(3,14 - 2,61)•cos 135•tg150]= -0,72 кН,0=0,4-
0,72 =-0,32 кН.
Ширина
бандажа при DН.Б.> DCp.Б. (DН.Б.
=1,3 м) определяется по формуле:
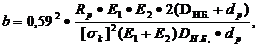
Где
DН.Б. -
наружный диаметр бандажа, м.
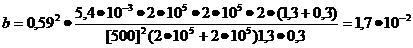 м.
м.
Принимаем
конструктивно b=0,05 м.
Высота
сечения бандажа определяется из условия прочности:
σН=Mmax/W=≤[σ]H,
где
W - момент сопротивления сечения бандажа, м3.
W=(b•h2)/6,
Где
h - высота сечения бандажа, м.
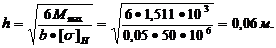
Ширина
опорного ролика определяется по формуле:
bp= b+α•∆t•l2 +
(0,03+0,04),
где
α-коэффициент линейного расширения материала барабана, С-1;
α=1,86•10-7 С-1;
∆t -
разность между температурами барабана при монтаже и в рабочем состоянии,
0С; ∙∆t=480
0С;
l2 - расстояние между бандажами (опорами), м.
bp=
0,05+1,86•10-7•480∙5 +0,04=0,11м.
Внутренний
диаметр бандажа надетого на башмаки
DВ.Б.=DСр.Б. - h=1,3-0,06=1,24
м.
Диаметр
внешней опорной поверхности башмаков
DОП=DВ.Б.- α•∆t•DСр.Б.-0,02=1,24-1,86•10-7•480•1-0,2=1м.
.1.10
Определение размеров упорных роликов
Нагрузка
на упорный ролик определяется по формуле:
A=G•sinα,
где
G - сила тяжести барабана, Н;
α - угол наклона барабана к горизонтали, град.
Сила
T2, нормальная
к боковой поверхности ролика определяется по формуле:
T2=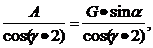
где
γ - угол при вершине конуса; принимаем γ =170.
T2=19532,2•9,81•sin2/cos(17•2)=8066
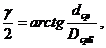
где
dуp - средний диаметр упорного
ролика, м.
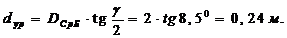
Окончательно
принимаем dуp=0,18 м.
Ширина
упорного ролика определяется по формуле:
bур=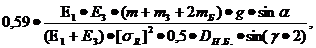 (4.25)
(4.25)
где
E3=2•105
МПа - модуль упругости материала упорного ролика;
m3 = 204 кг - масса звездочки и ее крепления;
mБ = 127 кг - масса бандажа.
bур=0.59(2•105•2•105(19532,2+204+2•1,27)106•9,81sin2/(2•105+2•105)5002•
,5•1,3•sin(17•2))
Принимаем bур= 0,043м.
.1.11 Определение диаметра упорного регулировочного винта
В процессе регулировки на каждый из двух упорных винтов приходится усилие
p1, Н, которое определяют как полусумму горизонтальной
составляющей реакции в опоре и силы трения в основании опоры
p1=-0,5•(Тsinψ+f•Tcosψ),
где f - коэффициент трения между рамой и
плитами; для стали f=0,2.
После подстановки значения реакции опоры из формулы получается
p1=0,25•Rоп•(tg ψ+f).
При ψ=300 для стали
p1=0,2•Rоп=0,2•18,85=4 кН.
Минимальный диаметр регулировочного винта из условия прочности
dр.в.=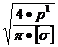 =
= 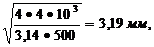
где
[σ]=500 МПа - допускаемое напряжение растяжения для
материала винта.
Принимаем
конструктивно dр.в.=10 мм
[9].
В
результате проведенных расчетов была спроектирована барабанная вращающаяся печь
для сульфатизации фторида натрия
Основные
характеристики печи приведены в таблице 5.7.
Таблица 5.7
Основные характеристики печи
|
Длина барабана, м
|
7,5
|
|
Диаметр барабана, м
|
1
|
|
Толщина стенки барабана, м
|
0,01
|
|
Наружный диаметр бандажа, м
|
1,3
|
|
Внутренний диаметр бандажа,
м
|
1,24
|
|
Высота сечения бандажа, м
|
0,06
|
|
Ширина бандажа, м
|
0,05
|
|
Диаметр опорного ролика, м
|
0,3
|
|
Ширина опорного ролика, м
|
0,09
|
|
Диаметр упорного ролика, м
|
0,018
|
|
Ширина упорного ролика, м
|
0,03
|
Исходя из полученных значений основных характеристик печи можно сделать
вывод, что данные печи являются аппаратами непрерывного действия и
предназначены для термической и термохимической обработки сыпучих материалов в
химической, лесохимической, рудной и других отраслях промышленности.
.1.12 Основные составные части вращающейся установки с
барабаном:
Барабан, поворотная рама с приводом вращения барабана, основание
установки, устройство загрузки со шнековым питателем, устройство разгрузки,
домкрат, уплотнитель, площадка обслуживания, шкаф управления.
Приводная станция состоит из электродвигателя, редуктора, подвенцовой
шестерни. Зубчатый венец, связанный с приводной станцией через шестерню, служит
для приведения во вращение барабана аппарата.
Устройство загрузки со шнековым питателем присоединяется к загрузочной
стороне барабана и служит для подачи материала.
Разгрузочное устройство выполнено с вибратором и присоединяется к
барабану со стороны выхода готового продукта.
Камеры разгрузки служат для выгрузки обрабатываемого материала, а также для
отвода технологического отработанного газа.
Выводы:
В результате расчетов определены геометрические размеры барабанной
вращающейся установки, расчет барабана на прочность и жесткость, а так же
мощность, затрачиваемая на вращение барабана и число оборотов барабана.
5.2 Расчет форконденсатора
.2.1 Введение
Тепловые балансы. При расчете тепловых балансов необходимо знать удельные
величины теплоемкости, энтальпии (теплосодержание), теплоты фазовых или
химических превращений.
Удельная теплоемкость - это количество тепла, необходимого для нагревания
(или охлаждения) 1 кг вещества на 1 градус (дж/кг град). Теплоемкость
характеризует способность тела аккумулировать тепло. Так как теплоемкость
зависит от температуры, то различают истинную теплоемкость при данной
температуре с и среднюю теплоемкость в некотором интервале температур
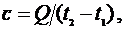
где
Q - количество тепла, сообщаемого единице количества
вещества при изменении температуры от 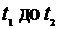 . В
практике тепловых расчетов, как правило, приходится пользоваться средними
теплоемкостями.
. В
практике тепловых расчетов, как правило, приходится пользоваться средними
теплоемкостями.
Удельная
энтальпия i (если все расчеты вести от 0 С) определяется
количеством тепла, которое необходимо для нагревания 1 кг вещества от 0 С до
данной температуры, энтальпия i измеряется в Дж/кг, в технической системе ккал/кг.
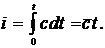
Удельная
теплота фазовых или химических превращений r - это
количество тепла, которое выделяется (или поглащается) при изменении
агрегатного состояния или химическом превращении единицы массы вещества. Она
измеряется Дж/кг, а в технической системе ккал/кг.
«Внутренний»
метод составления теплового баланса (с использование величин
теплоемкостей). В непрерывно действующем теплообменнике
Если
процесс теплообмена происходит, в первой среде, фазовые или химические
превращения (испарения жидкости, конденсация пара, плавление, химические
реакции, и т.п.), то уравнение теплового баланса имеет следующий вид:
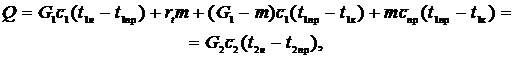
«Внешний»
метод составления теплового баланса (с использованием величин удельных
энтальпий). Тепловой баланс составляется исходя из того, что количество тепла Q1,
поступающего в аппарат за 1 час с входящими средами, равно количеству тепла,
уходящего со средами из аппарата за то же время,
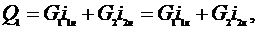
где
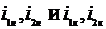 - энтальпии веществ, соответственно входящих в
аппарат и выходящих из него.
- энтальпии веществ, соответственно входящих в
аппарат и выходящих из него.
В
отличие от внутреннего метода составления теплового баланса, где
рассматривается перераспределение тепла между теплообменивающимися средами в
самом аппарате, в данном методе тепловой баланс составляется как бы по внешним
показателям: до аппарата и после аппарат.
Из
уравнения (2.5) можно определить количество тепла Q, переданного
от одной среды к другой, как разность энтальпий
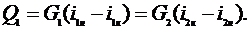
При
наличии фазовых или химических превращений в теплообменнике количество тепла,
переданного от одной среды к другой,
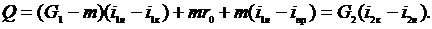
где
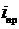 - энтальпия продуктов превращения при температуре
выхода из аппарата
- энтальпия продуктов превращения при температуре
выхода из аппарата 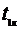 .
.
Кинетика
теплопередачи. Различают три вида (механизма) теплопередачи:
теплопроводность, конвекция и излучение.
Передача
тепла теплопроводностью. Под теплопроводностью понимают переход тепловой
энергии в среде без массовых ее движений относительно направления
теплоперехода. Здесь тепло передается как энергия упругих колебаний атомов и
молекул около их среднего положения. Эта энергия переходит к соседним атомам и
молекулам в направлении ее уменьшения, т.е. уменьшения температуры
Коэффициент
теплопроводности. Он определяет скорость передачи тепла, т.е. количество
тепла, проходящего в единицу времени через единицу поверхности тела при длине
его в направлении теплопередачи, равной единице и разности температур 1 град.
Наибольшее значение 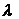 имеют металлы - от нескольких десятков до нескольких
сотен вт/(м град). Значительно меньшие коэффициенты теплопроводности имеют
твердые тела - не металлы. Теплопроводность жидкостей меньше теплопроводности
большинства твердых тел. Для них
имеют металлы - от нескольких десятков до нескольких
сотен вт/(м град). Значительно меньшие коэффициенты теплопроводности имеют
твердые тела - не металлы. Теплопроводность жидкостей меньше теплопроводности
большинства твердых тел. Для них 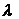 колеблется
в пределах десятых долей вт/(м град). Коэффициенты теплопроводности еще меньше.
колеблется
в пределах десятых долей вт/(м град). Коэффициенты теплопроводности еще меньше.
Безразмерные
комплексы имею наименования:
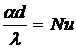 -
критерий Нуссельта, включающий в себя искомую величину коэффициента теплоотдачи
-
критерий Нуссельта, включающий в себя искомую величину коэффициента теплоотдачи
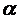 (Нуссельт впервые применил теорию подобия для решения
вопросов теплообмена);
(Нуссельт впервые применил теорию подобия для решения
вопросов теплообмена);
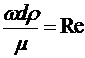 -
критерий Рейнольдса, определяющий гидравлическую характеристику потока:
-
критерий Рейнольдса, определяющий гидравлическую характеристику потока:
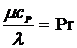 -
критерий Прандтля, характеризующий физические свойства среды.
-
критерий Прандтля, характеризующий физические свойства среды.
Определение
А, а и е производится на основе экспериментальных исследований.
Средняя
разность температур. В основу расчетов требуемой поверхности теплообмена
F для передачи заданного тепловым балансом количества
тепла в единицу времени Q положено уравнение (2.19). В подавляющем большинстве
случаев температуры сред в процессе теплопередачи будут изменяться в результате
происходящего теплообмена, а следовательно, будет изменяться и разность
температур 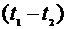 вдоль поверхности теплообмена. Поэтому рассчитывают
среднюю разность температур по длине аппарата
вдоль поверхности теплообмена. Поэтому рассчитывают
среднюю разность температур по длине аппарата 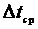 , но так
как это изменение не линейно то рассчитываю логарифмическую разность
температур.
, но так
как это изменение не линейно то рассчитываю логарифмическую разность
температур.
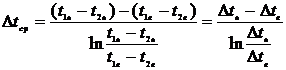 ; (2.21)
; (2.21)
Это
доказано математическими выкладками. При противотоке всегда требуется меньшая
теплопередающая поверхность, чем при прямотоке, для передачи равного количества
тепла в одинаковых условиях начальных и конечных температур сред.
В
случае смешивания тока в одном ходу теплообменника среды движется противотоком,
а в другом прямотоком. В этих случаях среднюю разность температур 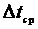 определяют из соотношения
определяют из соотношения
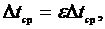 (2.22)
(2.22)
где
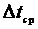 - средняя логарифмическая разность температур при
противотоке;
- средняя логарифмическая разность температур при
противотоке; 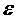 - поправочный коэффициент, который всегда меньше
единицы.
- поправочный коэффициент, который всегда меньше
единицы.
Кожухотрубные
теплообменники. Кожухотрубный теплообменник является наиболее
распространенным аппаратом в следствии компактного размещения большой
теплопередающей поверхности в единице объема аппарата. Поверхность теплообмена
в нем образуется пучком параллельно расположенных трубок концы которых
закреплены в двух трубных досках (решетках). Трубки заключены в цилиндрический
кожух, приваренный к трубным доскам или соединенный с ними фланцами. К трубным
решеткам крепятся на болтах распределительные головки (днища), что позволяет
легко снять их и произвести чистку трубок или в случае необходимости заменить
новыми. Для подачи и отвода теплообменивающихся сред в аппарате имеются
штуцера. В целях предупреждения смешения сред трубки закрепляются в решетах
чаще всего развальцовкой, сваркой или реже для предупреждения термических
напряжений с помощью сальников.
Преимущества
проведения процессов теплообмена по принципу противотока, что обычно и
выполняется в кожухотрубных теплообменных аппаратах. При этом охлаждаемую среду
можно направить сверху вниз, а нагреваемую на встречу ей, или наоборот. Выбор,
какую среду направить в межтрубное пространство и какую внутрь трубок, решается
сопоставлением ряда условий:
- среду с наименьшим
значением 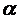 следует направлять в трубки для увеличения скорости ее
движения, а следовательно, и для увеличения ее коэффициента теплоотдачи;
следует направлять в трубки для увеличения скорости ее
движения, а следовательно, и для увеличения ее коэффициента теплоотдачи;
- внутреннюю
поверхность трубок легче чистить от загрязнений, поэтому теплоноситель, который
может загрязнять теплопередающую поверхность, следует направлять в трубки;
- среду под
высоким давлением целесообразно направлять в трубки, опасность разрыва которых
меньше по сравнению с кожухом;
- среду с очень
высокой или наоборот с низкой температурой лучше подавать в трубки для
уменьшения потерь тепла в окружающую среду.
Работу кожухотрубных теплообменников можно интенсифицировать, применяя
трубы малого диаметра. Необходимо иметь в виду, что при уменьшении диаметра
труб увеличивается гидравлическое сопротивление теплообменника.
Наиболее простой путь обеспечения высоких скоростей состоит в устройстве
многоходовых теплообменников. Число ходов в трубном пространстве может доходить
до 8-12. При этом часто не удается сохранить принцип противотока. Наличие
смешанного тока буден несколько снижать движущую силу процесса теплопередачи,
что соответственно снизит эффективность работы. С помощью перегородок
увеличивается скорость движения той среды, у которой меньше значение
коэффициента теплоотдачи. Следует иметь в виду, что в длинных, особенно в
многоходовых, теплообменниках уменьшается смешение поступающей среды со всем ее
количеством, находящемся в аппарате, и этим предупреждается возможное
дополнительное уменьшение средней разности температур.
В кожухотрубных теплообменниках при большой разности температур между
средами возникают значительные термические напряжения, особенно в момент пуска
или остановки аппарата, вызванные различным удлинением трубок и кожуха под
воздействием различных температур. Во избежание возникновения таких напряжений
используются следующие меры:
1 Установка в корпусе аппарата
линзового компрессора.
2 Установка в теплообменнике только
одной трубной решетки, в которой закреплены трубки U - образной формы.
3 Устройство теплообменников с
«плавающей головкой».
4 Закрепление трубок в одной из трубных
решеток с помощью сальников.
5 Сальниковое соединение трубной
решетки с кожухом.
Теплообменники
типа «труба в трубе». Теплообменники этого типа смонтированы из труб,
каждая из которых окружена трубой несколько большего диаметра. Одна среда течет
по внутренней трубе, другая - по кольцевому каналу. Внутренние трубы соединены
последовательно «калачами», а наружные - патрубками. При необходимости получить
большую поверхность теплопередачи возможно не только последовательное, но и
параллельное и комбинированное соединение таких секций с помощью коллекторов. В
теплообменнике типа «труба в трубе» соответствующим подбором диаметров труб для
обеих теплообменивающих сред можно назначить любую скорость, а следовательно
получить соответственно высокие значения величин 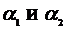 .
Недостатком таких теплообменников является большой расход металла на единицу
тепло передающей поверхности вследствие затрат на бесполезные для теплообмена
внешние трубы, что приводит к значительному увеличению стоимости аппарата. Этот
недостаток становится менее ощутимым, если внешние трубы изготовлены из обычной
углеродистой стали, а внутренние - из дорогостоящего материала в условиях
агрессивных сред. Теплообменники типа «труба в трубе» особенно широко
применяются тогда, когда среды подаются под высоким давлением (десятков и сотен
атмосфер) [1].
.
Недостатком таких теплообменников является большой расход металла на единицу
тепло передающей поверхности вследствие затрат на бесполезные для теплообмена
внешние трубы, что приводит к значительному увеличению стоимости аппарата. Этот
недостаток становится менее ощутимым, если внешние трубы изготовлены из обычной
углеродистой стали, а внутренние - из дорогостоящего материала в условиях
агрессивных сред. Теплообменники типа «труба в трубе» особенно широко
применяются тогда, когда среды подаются под высоким давлением (десятков и сотен
атмосфер) [1].
5.2.2
Материальный и тепловой расчет
Таблица 5.8
Расход газов поступающих в аппарат
|
Расход,кг/ч
|
%
|
С0р,
ДЖ/моль•к
|
|
HF
|
96,78
|
87.3
|
29,14
|
|
SiF4
|
3,97
|
3,6
|
27
|
|
H2O
|
1.75
|
1,57
|
75,34
|
|
H2SO4
|
1.25
|
1.13
|
138,9
|
|
воздух
|
7,1
|
6,41
|
29,1
|
|
итого
|
110,85
|
100
|
|
Температура газа на входе равна 55⁰C = 328⁰К.
Температура газа на выходе равна 25⁰C = 298⁰К.
Температура воды на входе равна 21⁰C = 294⁰К.
Температура воды на выходе равна 23⁰C = 296⁰К.
.2.3 Определение движущей силы процесса теплопередачи

Рис 5. Температурная диаграмма
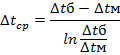
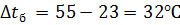
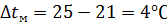
Так как отношение Δtб/Δtм = 32/4 = 8,0 >2, то
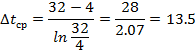
5.2.4 Определение средних температур теплоносителей
Trcp =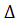 tcp + tx.c.p.
tcp + tx.c.p.
Txcp = tг.cp - tср.
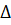 tг
=tг.н - tгк = 55-25 = 30
tг
=tг.н - tгк = 55-25 = 30
 tx = tx.k - tx.н = 23-21= 2
tx = tx.k - tx.н = 23-21= 2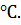
txcp = 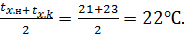
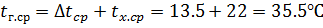 .
.
.2.5 Тепловой расчет
Уравнение теплового баланса:
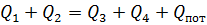
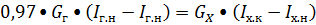
Посчитаем количество тепла, которое необходимо отводить по уравнению:
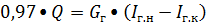
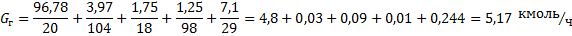
Рассчитаем энтальпию газа:
Энтальпия смеси газов рассчитывается по уравнению:
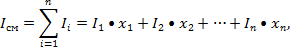
где 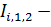 это энтальпии индивидуальных веществ;
это энтальпии индивидуальных веществ;
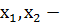 массовые доли компонентов в смеси.
массовые доли компонентов в смеси.
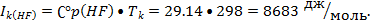
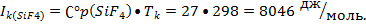
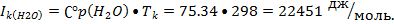
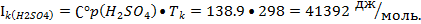
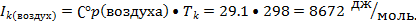
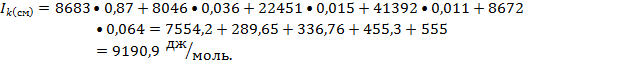
Также рассчитываем 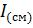 для начальной температуры, T= 328
для начальной температуры, T= 328 K.
K.
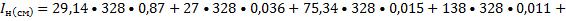
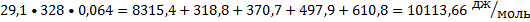 .
.
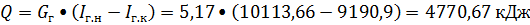
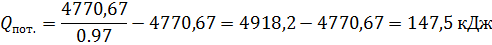
Найдем расход холодной воды по уравнению:
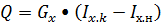
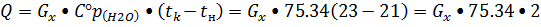
По тепловому балансу правая часть уравнения равна левой, следует, что Q = 4918,2 и можно выразить 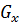 :
:
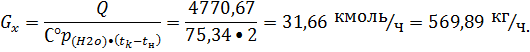
Приход тепла:
. С горячим теплоносителем:
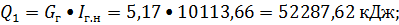
. С холодным теплоносителем:
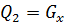 •
•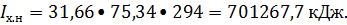
Расход тепла:
. С горячим теплоносителем:
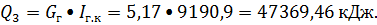
. С холодным теплоносителем:
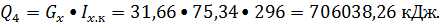
Таблица 5.9
Тепловой баланс
|
Статья прихода, кДж/ч
|
Статья расхода, кДж/ч
|
|
1. С горячим
теплоносителем. Q1=52287,62
|
1. С горячим
теплоносителем. Q3
= 47369,46
|
|
2. С холодным теплоносителем. Q2 =701267,7
|
2. С холодным теплоносителем.
Q4 =
706038,26 Тепловые потери. Qпот.=147,6
|
|
Итого: 753555,3
|
5.2.3 Конструктивный расчет
Форконденсатор выбираем типа «труба в трубе». Расчет его сводится
копрделению необходимой поверхности теплообмена и его геометрических размеров.
Выбираем размеры труб форконденсатора:
· внутренняя труба 38х3,5
· наружная труба 57х4.
Площадь поперечного сечения внутренней трубы равняется:
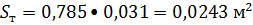
Площадь поперечного сечения межтрубного пространства:
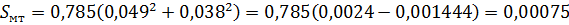
Эквивалентный диаметр межтрубного пространства:
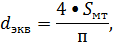
где п - полный периметр поперечного сечения потока, м.
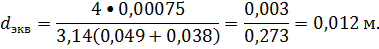
Скорость движения воды в межтрубном пространстве:
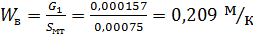 .
.
Для расчетов критериев подобия, входящих в уравнение конвективной
теплоотдачи выбираем параметры физических свойств воды при температуре 20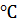 :
:
· плотность ρ, 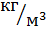 . 998;
. 998;
· теплоемкость с, 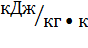 4,19;
4,19;
· теплопроводность λ,  0,599;
0,599;
· динамическая вязкость μ, Па•с 10-3.
Для охлаждающей воды протекающей в межтрубном пространстве теплообменника
рассчитываем величины критериев.
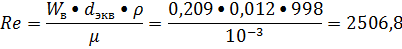
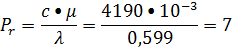
При 2300<Re<10000 для
нахождения критерия Нуссельта используем формулу:
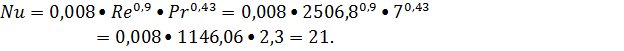
Так как 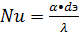 , то
, то 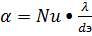
Коэффициент теплоотдачи от стенки к охлажденной воде равен:
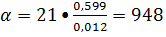 Вт/м2•к.
Вт/м2•к.
Рассчитываем величину коэффициента теплоотдачи от охлажденного газа к
стенке внутренней трубы:
Из материального расчета через форконденсатор проходит реакционный газ в
количестве 110,85 кг/ч, в том числе фтористого водорода 96,78 кг/ч,
четырехфтористого кремния 2,97 кг/ч паров воды 1,75 кг/ч, серной кислоты 1,25
кг/ч, воздуха 7,1 кг/ч.
Объемный расход газа при нормальных условиях составляет:
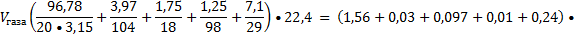
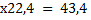 м3/с.
м3/с.
(С учетом фактора ассоциации фтористого водорода 3,1 при средней
температуре газа 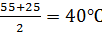 ) или равна 0,012 м/с.
) или равна 0,012 м/с.
Линейная скорость газа в трубе:
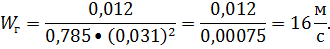
Плотность газа равна:
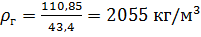 .
.
Параметры других физических величин, входящих в критерии подобия
принимаем как для фтористого водорода при температуре 40⁰C.
Теплоемкость
Сг=29,1 кДж/моль•к = 1455Дж/кг•к;
Теплопроводность
λг = 278•10-4 Дж/м•с•к;
Вязкость газа
μг = 1014•10-5 Па•с.
Рассчитаем величины критериев Рейнольдса и Прандля для газов потока:
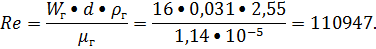
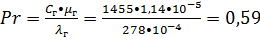 .
.
При значении критерия Рейнольдса >10000 критерий Нусельта рассчитываем
по уравнению:
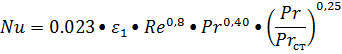
Значение коэффициента ε1 выбираем из таблицы в зависимости от отношения длины
трубы к ее диаметру.
Для данного случая
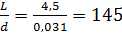 и ε1=1.
и ε1=1.
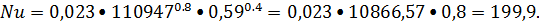
Коэффициент теплоотдачи от газа к стенке.
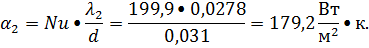
Рассчитываем величину коэффициента теплоотдачи от газа к охлаждающей воде
с учетом термического сопротивления стенки:
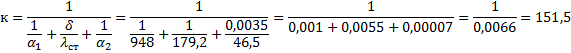
Необходимую величину поверхности теплообмена рассчитываем по формуле:
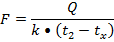
Для этого предварительно рассчитываем среднюю разность температур в
форконденсаторе.
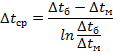
Наибольшая разность температур.
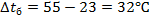
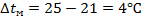
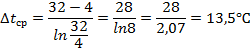
Из материального расчета при охлаждении газа до температуры 25⁰C требуется отводить тепла 4770,67
кДж/ч или 1325 Дж/сек.
Поверхность теплообмена равна:
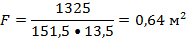
Необходимая длина труб диаметром 0,038 мм.
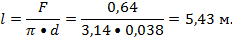
При такой длине труб выбираем двухходовый фторконденсатор длиной каждый
секции 3 м [9].
5.3 Расчет абсорбционной колонны
.3.1 Введение
Абсорбцией называют процесс поглощения газа или пара жидким поглотителем
(абсорбентом). Поглощение газа может происходить либо за счет его растворения в
абсорбенте, либо в результате его химического взаимодействия с абсорбентом. В
первом случае процесс называют физической абсорбцией, а во втором случае -
хемосорбцией. Возможно также сочетание обоих механизмов процесса.
В промышленности абсорбция широко применяется для выделения из газовых
смесей ценных компонентов, для очистки технологических и горючих газов от
вредных примесей, для санитарной очистки газов и т.д.
При переходе из газовой фазы в жидкую, энергия молекул распределяемого
компонента уменьшается. Поэтому процесс абсорбции сопровождается выделением
тепла и повышением температуры системы. Кроме того, объем системы в процессе
абсорбции уменьшается за счет уменьшения объема газовой фазы. Следовательно,
согласно принципу Ле-Шателье, растворимость газа в жидкости увеличивается при
повышении давления и уменьшении температуры процесса. Статика процесса
абсорбции описывается уравнением Генри, а кинетика - основными уравнениями
массопередачи.
При абсорбции процесс массопередачи протекает на поверхности
соприкосновения фаз. Поэтому в аппаратах для поглощения газов жидкостями
(абсорберах) должна быть создана развитая поверхность соприкосновения между
газом и жидкостью. По способу образования этой поверхности абсорбционные
аппараты можно разделить на поверхностные, барботажные и распыливающие.
В абсорберах поверхностного типа поверхностью соприкосновения фаз
является зеркало жидкости или поверхность стекающей пленки.
Насадочные колонны представляют собой колонны, загруженные насадкой -
твердыми телами различной формы; при наличии насадки увеличивается поверхности
соприкосновения газа и жидкости.
Эффективность работы насадочного абсорбера во многом зависит не только от
гидродинамического режима, но и от типа выбранной насадки. Разнообразие
применяемых насадок объясняется множеством предъявляемых к ним требований:
большая удельная поверхность и свободный объем, малое гидравлическое
сопротивление газовому потоку, равномерное распределение абсорбента, хорошая
смачиваемость, коррозионная стойкость, малая насыпная плотность и низкая
стоимость.
В барботажных абсорберах поверхность соприкосновения фаз развивается
потоками газа, распределяющегося в жидкости в виде пузырьков и струек. Такое
движение газа, называемое барботажем, осуществляется в тарельчатых колоннах с
колпачкаовыми, ситчатыми или провальными тарелками. Особенностью тарельчатых
колонн является ступенчатый характер проводимого в них процесса (в отличие от
непрерывного процесса в наса-дочных колоннах) газ и жидкость последовательно
соприкасаются на отдельных ступенях (тарелках) аппарата
В распыливающих абсорберах поверхность соприкосновения создается путем
распыления жидкости в массе газа на мелкие капли. Такие абсорберы изготовляются
обычно в виде колонн, в которых распыление жидкости производится сверху, а газ
движется снизу вверх [12].
барабанный установка фтористый алюминий
5.3.2 Данные для расчета
Назначение колонны - улавливание фтористого водорода из газов, отходящих
со стадии конденсации технического фтористого водорода.
Таблица 6.1
Общее количество на входе в аппарат
|
вещество
|
Расход, кг/ч
|
%
|
|
HF
|
7,82
|
47,39
|
|
SiF4
|
3,9
|
23,6
|
|
воздух
|
4,78
|
28,9
|
|
итого
|
16,5
|
100
|
5.3.3 Материальный расчет абсорбционной колонны
Насыщенность серной кислоты фтороводородом равна 87%.
Поэтому количество поглощенного фтороводорода равна:
,82•0,87=6,8 кг/ч.
,82-6,8=1,01 кг/ч.
Расход газа на выходе будет равен:
SiF4 и воздуха
не поглощается серной кислотой, поэтому их расход будет такой же, как приход.
Расход фтооводорода равен общему количеству прихода HF без поглощенного фтороводорода:
,82-6,8=1,01 кг/ч.
Состав серной кислоты: H2SO4 - 93%; H2O -
7%.
Количество серной кислоты 10,45 кг/ч;
Количество H2O 0,78 кг/ч.
Расход насыщенного абсорбента:
,45+0,78+6,81=18 кг/ч.
Таблица 6.2
Материальный баланс
|
Приход, кг/ч
|
%
|
Расход, кг/ч
|
%
|
|
HF 7,82
|
28,23
|
HF 1,01
|
3,64
|
|
SiF4 3,9
|
14
|
SiF4 3,9
|
14
|
|
Воздух 4,78
|
17,25
|
Воздух 4,78
|
17,2
|
|
H2SO4 10,45
|
37,7
|
H2SO4(нас.HF) 17,29
|
62,4
|
|
H2O 0,78
|
2,81
|
H2O 0,78
|
2,81
|
|
Итого: 27,7
|
100
|
Итого: 27,7
|
100
|
5.3.4 Определение движущей силы и конструктивный расчет
абсорбера
С тем, чтобы рассчитать абсорбционную колонну необходимо рассчитать
диаграмму равновесного состояния абсорбции в реальных температурах и по ней
определить число единиц переноса.
Орошаемая серная кислота поступает в абсорбционную колонну из рассольного
холодильника при температуре близкой к 0⁰C. Принимаем, что при смешении
кислоты и газа в колонне температура выравнивается на уровне, близком к -5⁰C.
При этом температуре упругость насыщенного пара фтористого водорода над
насыщенным абсорбентом равна произведению упругости пара чистого фтористого
водорода и мольной доли в жидкости. То есть.
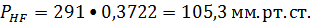
Парциальное давление фтористого водорода в газе на входе в колонну
составляет:
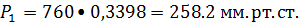
Следовательно, движущая сила абсорбции на входе в колонну равна:
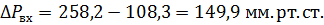
Рассчитаем парциальное давление фтороводорода в газе на выходе из
колонны.
Масса газа на выходе 9,7 кг/ч в том числе фтороводорода 1,01 кг/ч. В
пересчете на объем при нормальных условиях, с учетом фактора ассоциации
фтористого водорода 3,83 объем газа на выходе составляет:
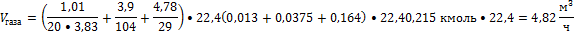
или 0,0013388 м^3/с в том числе 0,29 м^3/ч фтористого водорода.
Мольная доля фтористого водорода в газе на выходе из колонны равна 0,060
или 6% объемных и его парциальное давление равно.
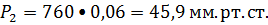
Отсюда следует, что движущая сила абсорбции на выходе газа из колонны
относительно купоросного масла, не содержащего фтористого водорода равна 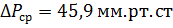
Средняя движущая сила абсорбции по всей колонне будет равна:
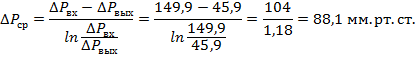
Число единиц переноса рассчитываем по уравнению:
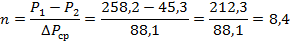
5.3.5 Конструктивный расчет абсорбера
Диаметр абсорбционной колонны рассчитываем из среднего расхода газа с
учетом скорости движения его в колонне. Как указывалось выше расход газа на
входе в колонну составляет 0,0019 м3/с, а на выходе 0,0013м3/с.
Средний расход газа равен 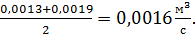
Скорость движение газа в колонне выбираем из следующих соображений.
Пределом устойчивой работы насадочных абсорбционных колонн является скорость
газа, соответствующая точке захлебывания Wз, которая определяется следующим образом.

Для дальнейшего расчета возьмем физические величины:
α - удельная поверхность насадки, м2/м3;-
ускорение свободного падения, м/сек2;
Fсв
- свободное сечение
насадки, м2/м2;
μж - вязкость купоросного масла: 3•10-3,
Па•с;
L’ и G’ - расходы жидкости и газа, кг/сек;
A=0,079
- для систем жидкость-газ;
ρж - плотность купоросного масла, 1,77 г/см3.
Плотность газа равна 2,4 кг/м3= 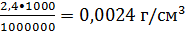 .
.
Найдем 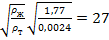 , далее по графику определяем k1=0,34
, далее по графику определяем k1=0,34
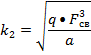
По таблице значение комплекса 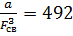 с насадкой из колец Рашига.
с насадкой из колец Рашига.
Вследствие чего 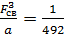 .
.
Найденные значения подставляем в уравнение.
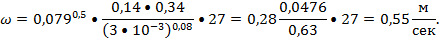
Расчет по данному уравнению показал, что для нашей системы ωз=0,55 м/сек. Чтобы уйти от режимов захлебывания и
подвисания жидкости и обеспечить работу колонны в пленочном режиме, при котором
наименьшее гидровлическое сопротивление колонны, принимаем фиктивную скорость
газа равной 0,24 м/с.
Тогда поперечное сечение колонны составит: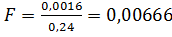 , а диаметр равен:
, а диаметр равен:
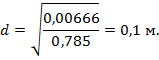
Таким образом, диаметр абсорбционной колонны принимаем равный 0,1 м.
Рабочую высоту аппарата (высоту слоя насадки) рассчитываем по уравнению: H=n•h.
H-
рабочая высота аппарата, м;
n
-число единиц переноса;
h -
высота единицы переноса (ВЕП), м.
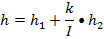
h1 - ВЕП для газовой фазы;
h2- ВЕП для жидкой фазы;
k -
Тангенс угла наклона равновесной линии в координатах y=f(x)
Для нашего случая 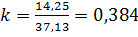
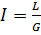 - отношение между массами жидкой и газовой фазами.
- отношение между массами жидкой и газовой фазами.
При плотности орошения насадки 7м3/м2•час = 0,0019
7м3/м2•сек;
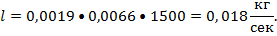
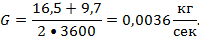
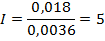
Рассчитываем ВЕП для газовой фазы по уравнению:
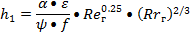
где, ε - свободный объем насадки;
ψ - коэффициент смачиваемости
насадки;- удельная поверхность насадки;
Reг - критерий Рейнольдса для газа;
Pr
-критерий Прандтля для газа.
Для насадки из колец Рашига ε = 0,785; ψ=1; f = 90 м2/м3;α = 8,13
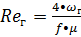 ;
;
Где ωг - массовая скорость газа отнесенная к полному сечению
аппарата, кг/м2•сек;
μ - динамическая вязкость газа, Па•с;
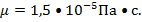
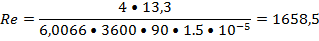
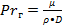 ;
;
Где D -коэффициент диффузии, м2/сек.
Величину коэффициента диффузии газа рассчитываем по уравнению:
 ,
,
Где VA и VB - молекулярные объемы газов;
MA иMB -
молекулярные массы газов;
Т - абсолютная температура, к;
Р - абсолютное давление;
Т = -5+273=268 к Р= 1 атм.
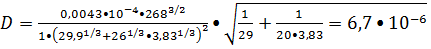 м2/сек.
м2/сек.
где 3,83 коэффициент ассоциации HF при -5⁰C.
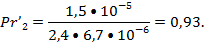
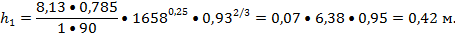
Рассчитываем ВЕП для жидкой фазы.
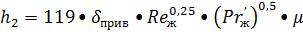 ,
,
где Reж и Prж - критерий Re иPr для жидкости;
δ - приведенная толщина пленки,
которая рассчитывается по уравнению:
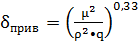 , где
, где
μ - вязкость жидкости, для серной
кислоты
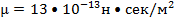
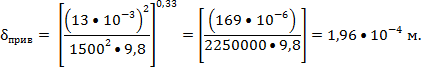
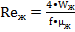 ,
,
где ωж
- массовая скорость жидкости отнесенная к полному сечению аппарата.
При плотности орошения насадки
м3/м2•ч=0,0019 7м3/м2•сек.
ωж = 0,0019•1500=2,9 кг/м2•с.
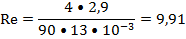
При температуре -5⁰C величина критерия Прандтля равна: Prж = 190
Отсюда ВЕП для жидкой фазы:
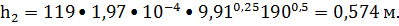
Общая высота единицы переноса равна:
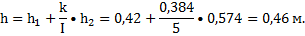
общая высота слоя насадки в виде колец Рашига 50х50х5 мм в абсорбционной
колонне:
H=n•h=2,5•0,45=1,13
Примем высоту равной 1,5 м.
Итак, основные размеры колонны:
Внешний диаметр 0,100 м;
Высота насадки 1,5 м.
Рассчитываем число оборотов абсорбционной кислоты через колонну для
обеспечения плотности орошения насадки равной 7м3/м2•ч.
На абсорбцию в колонну подается 11,23 кг/ч купоросного масла, а отводится 18 кг
насыщенного абсорбента.
Средний расход поглощающей кислоты равен 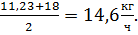
При плотности орошения 7м3/м2•ч количество
поглощающей кислоты должно составлять 7м3/м2•ч•0,006 м3•1500кгм3=63
кг/ч.
Следовательно, абсорбционная кислота в течении одного часа должна сделать
через колонну 63/14,6=4,3 оборота.
6. Схема контроля и автоматизации процесса
.1 Описание технологической схемы переработки отходов
алюминиевого производства
Перерабатываемым продуктом является фтористый натрий. Целью его
переработки является извлечение ценного компонента фтороводорода.
Из бункера А101 и емкости А102 поступают фтористый натрий и серная
кислота соответственно в установку сульфатизации А104. В результате химической
реакции на выходе газообразный продукт фтороводород с примесями и, избыток
серной кислоты и сульфат натрия. Далее газ идет на очистку в колонну А110 - это
круглая в сечении башня. Фтороводород очищенный от пыли, основной части серной
кислоты и воды поступает на стадию форконденсации А112, где идет охлаждение
газа до температуры 25⁰C. Далее идет стадия конденсации фтороводорода в конденсаторе
А113 при температуре -10⁰C, а не конденсировавшийся четырехфтористый кремний с частью
фтороводорода идёт на улавливание фтороводорода в абсорбере А116 серной
кислотой. Готовый продукт на выходе из конденсатора поступает в промежуточный
сборник А114.
.2 Описание функциональной схемы автоматизации
Для измерения уровня бункере исходного сырья А101 и ёмкостях А102, А108,
А114, А115, установлены уровнемеры соответственно (позиции 1-1, 2-1, 7-1, 12-1,
15-1). Расход исходного сырья регулируется вентилями (позиции 1-8, 2-8)
входящих в контур регулирования 1-1÷1-8 и 2-1÷2-8. В форконденсаторе А112 и
конденсаторе А113 установлен датчик для измерения температуры (позиция 10-1 и
11-1 соответственно)
6.3 Перечни технологических параметров подлежащих контролю,
регулированию и сигнализации
Параметры, подлежащие контролю:
· уровни веществ в бункерах А101, А102, А108, А114, А115 (позиции 1-1, 2-1,
7-1, 12-1, 15-1);
· температура форконденсатора и конденсатора, А112 и А113 (поз.
10-1, 11-1 );
Контролю подлежат, прежде всего, те параметры, знание которых облегчает
пуск, наладку и нормальное ведение технологического процесса. К таким
параметрам относятся все регулируемые величины, нерегулируемые внутренние
параметры, входные и выходные параметры, при изменении которых в объект могут
поступать возмущающие воздействия.
Для того чтобы обеспечить заданное протекание процесса необходимо
контролировать и поддерживать технологические параметры.
Параметры, подлежащие сигнализации:
) нижний уровень исходных веществ и уровень в приемных бункерах А101,
А102, А108, А114, А115, (поз. 1-1, 2-1,7-1,12-1,15-1);
2) температура форконденсаторе А112 и конденсаторе А113 (позиции
10-1 и 11-1)
сигнализации подлежат все параметры, изменения которых могут привести к
аварии, несчастным случаям или серьёзному нарушению технологического режима.
Основным назначением устройств сигнализации является оповещение обслуживающего
персонала о нарушениях технологического процесса.
Параметры, подлежащие регулированию:
Расход серной кислоты в абсорбер А116 ( позиции 14-7).
6.4 Выбор датчиков
Для получения информации о состоянии объекта и условиях работы служат
устройства контроля (контрольно-измерительные приборы). Они могут быть
выполнены либо в виде отдельных приборов, предназначенных для визуального
контроля параметров процесса, либо являться составной частью устройств
регулирования, сигнализации и защиты. Контрольно-измерительные приборы
устанавливают непосредственно у технологических аппаратов (местный контроль)
или на центральных щитах управления (дистанционный контроль).
В нашей функциональной схеме используются следующие
контрольно-измерительные приборы:
) Датчик измерения температуры - термостат марки NTC TMF:
Основные технические данные:
Пределы измеряемой температуры……………………-20….+400С
Погрешность………………………………………………..0,5%.
Выходной сигнал………………………………………… 4-20мА
Позиция: 10-1, 11-1.
) Измеритель-сигнализатор уровня ИСУ 100И предназначен для непрерывного
измерения уровня различных жидких и сыпучих сред контроля заданных предельных
уровней в резервуарах, в емкостях.
Основные функции - преобразование входного непрерывного частотного
сигнала датчика уровня в выходные сигналы. Отображение результатов измерений на
цифровом индикаторе в относительных единицах измерения. Формирование выходного
релейного сигнала и световой сигнализации для каждой из двух независимых
предельных уставок, задаваемых потребителем.
Основные технические данные:
Пределы допускаемой основной погрешности …………..± 1 %.
Выходной сигнал…………………………………………4-20 мА.
Позиция: 1-1, 2-1, 9-1, 12-1,15-1.
.5 Автоматизация процесса с использованием ЭВМ
Система автоматизации химических производств обычно выполняют
трехуровневыми. На нижнем уровне системы находятся датчики, приборы и
исполнительные устройства: термопары, нормирующий преобразователь. Исходные,
т.е. физические величины параметров технологического процесса, через
соответствующие преобразователи и устройства связи с объектами отображаются
местными приборами, преобразуются в электрические сигналы и поступают на
программируемые контроллеры - устройства среднего уровня системы. Для этого
контроллеры имеют определённый набор каналов аналогового и дискретного
ввода/вывода, на которые поступают сигналы с местных щитов автоматизации.
Далее на основе параметров, измеренных устройствами нижнего уровня
системы, контроллерами формируются необходимые управляющие воздействия, которые
через соответствующие преобразователи и устройства сопряжения поступают на
исполнительные механизмы.
Контроллеры (блоки регулирования) размещены по месту в специальных шкафах
и имеют информационные каналы связи, как с управляющим компьютером, так и между
собой. Получаемые контроллерами данные передаются на управляющий компьютер,
т.е. на верхний уровень системы.
В системе предусматривается возможность как автоматического
регулирования, с помощью регуляторов, реализующих определенный закон управления,
так и возможность регулировать технологический процесс вручную.
Режим прямого цифрового управления используется для управления
исполнительными механизмами и электродвигателями (позиции 1-7, 2-7, 3-1, 4-1,
8-1, 9-1, 16-1, 17-1, 18-1, 19-1).
На верхнем уровне системы организуется компьютерная сеть, которая
позволяет отображать технологический процесс и осуществлять с их помощью
оперативное управление процессом. Диспетчер наблюдает работу производства на
мониторах, установленных на его рабочем месте. На экран выводится информация о
ходе процесса спекания и температурном режиме. В случае возникновения
отклонений в работе или аварийных ситуаций компьютер выдаёт соответствующий
визуальный сигнал оператору, который принимает соответствующее решение.
При реализации режима ПЦУ на ЭВМ обычно организуют автоматизированные
рабочие места операторов, обеспечивающие отображение и регистрацию
технологической информации и прием команд оператора (т.е. человеко-машинный
интерфейс). Функции программно-логического управления, технологических и
противоаварийных блокировок, а также аналогового локального регулирования
выполняют микропроцессорные контроллеры.
Автоматизированные рабочие места операторов содержат специальные средства
отображения информации: мониторы ЭВМ, плазменные и жидкокристаллические экраны
большой площади для отображения мнемосхем и цифробуквенной информации,
печатающие устройства, а также клавиатур и специальных манипуляторов для ввода
команд оператора и управления устройствами отображения.
Функции и режимы работы АСУ ТП реализуются техническим, программным и
другими видами обеспечений. Техническое обеспечение образовано чувствительными
элементами, преобразователями, вычислительной техникой, вторичными КИП и
автоматическими регуляторами, исполнительными механизмами и т.д.
Программное обеспечение состоит из специальных программ, обеспечивающих
сбор, обработку, отображение, регистрацию технологической информации, а также
выработку управляющих воздействий. В настоящее время для этой цели разработаны
специальные пакеты программ, называемые SCADA-системами.
В данной схеме автоматизации используется ЭВМ, которая работает в двух
режимах: режиме прямого цифрового управления (ПЦУ), когда регулирующее
воздействие, вырабатывающееся ЭВМ, подается непосредственно на исполнительный
механизм; режиме советчика оператора, когда на экран монитора выводится
рекомендация, что надо изменить тот или иной параметр.
Задание температуры в контурах 10-1 и 11-1 задается
оператором. Показание приборов выводится на ЭВМ. Во всех остальных контурах ЭВМ
используется в информационном режиме.
Данная система автоматизации обеспечивает надёжное управление и контроль
производства и облегчает труд обслуживающего персонала.
.6 Действия оператора
Действия оператора при пуске технологического процесса:
Оператор включает тумблер питания установки сульфатизации, затем тумблер
питания шнека загрузки фтористого натрия а также подачу серной кислоты. Далее
выставляется расход серной кислоты в абсорбер, затем производится пуск
двигателей смесителя, шнека для подачи соды для нейтрализации побочного
продукта и насосов.
Действия оператора при нормальном режиме технологического процесса:
Оператор должен осуществлять контроль за расходом серной кислоты в
абсорбер, температуру конденсатора и форконденсатора, а также контролировать
поступление реагентов и расход исходного сырья.
Действия оператора при остановке технологического процесса:
Первым делом оператор последовательно отключает подачу раствора и
реагентов. Далее последовательное отключение двигателей установки сульфатизации
и смесителя. Последнюю очередь отключается шнеки подачи сырья, кальцинированной
соды и насосы [15].
Вывод: в результате анализа технологического процесса разработана
функциональная схема процесса получения фтороводорода из отходов алюминиевого
производства, на основе которой были подобраны необходимые приборы для контроля
и поддержания технологических параметров на заданном уровне.
7. Охрана труда и техника
безопасности
.1 Введение
Охрана труда (ОТ) в России рассматривалась как одно из
важнейших социально-экономических, санитарно-гигиенических и экологических
мероприятий, направленных на обеспечение безопасных и здоровых условий труда.
Основными законодательными документами, лежащими в основе трудового
законодательства и ОТ, являются:
Конституция РФ (ст. 7 п 2 «В РФ охраняется труд и здоровье людей…», ст.
37 п.3. «Каждый человек имеет право на безопасный труд…», ст.181 «Об основах
охраны труда в Российской федерации»).
Трудовой кодекс РФ, в котром говорится о том, что государство заботится
об улучшении условий и охране труда на предприятиях. Каждый работник имеет
право на условия, отвечающие требованиям безопасности и гигиены, а
администрация обязана внедрять современные средства безопасности,
предупреждающие возникновение профессиональных заболеваний рабочих и служащих.
При проектирование цеха следует учесть следующие
характеристики опасностей имеющих место на производстве фтористого водорода:
опасность поражения химически агрессивными веществами;
- опасность поражения, электрическим током;- взрыво- и
пожароопасность;- возможность получения механических травм.
.2 Опасность поражения химически
агрессивными веществами
В цехе следует особо отметить следующее фторсодержащее
вещество: фтороводород, четырехфтористый кремний, фторид натрия.
При гидролизе во влажном воздухе все они оказывают
более или менеесильное раздражающеевоздействие на дыхательные пути.
Фтороводород - токсичное вещество при взаимодействии с влагой воздуха
образует плавиковую кислоту, разъедающий яд, поражающий слизистые оболочки
глаз, рта, гортани, бронхов, легких, желудка, а так же кожу. Всасываясь через
слизистые оболочки, он вызывает токсическое давление за счет фтор-иона.
Попадание его на кожу вызывает химические ожоги, долго не заживаемые язвы.
При попадание в организм отмечаются явления острого отравления. ПДК HF в воздухе - 0,005мг/м3(1
класс).
SiF4 - также токсическое вещество при взаимодействии с
влагой воздуха образует H2SiF6, паражающий слизистые оболочки, глаз рта гортани,
бронхов, легких желудка а также кожу. ПДК SiF4 в воздухе - 0,2 мг/м3 ( 2 класс).
.3 Меры предупреждения
Во избежание воздействия агрессивных химических
веществ на человека применяются меры по коллективной и индивидуальной защите
работающих.
К коллективной безопасности относится:
- применять только цельные трубы из стойкого металла;
- полная герметизация оборудования;
окрашивать емкости и коммуникации в определенный цвет;
- изолированное хранение емкостей под давлением;
- эффективная вентиляция и ежедневная проверка ее
работы;
полная автоматизация и механизация технологического
процесса;
- постоянный контроль состава воздуха на присутствие в
нем фторидов;
четкое ведение технологического процесса и возможное
отключение всех аппаратов в случае нарушений приводящих к загрязнению воздуха и
нарушению технологического процесса;
обязательное наличие в рабочем помещение аптечки:
противоожоговой мази, раствора аммиака, борной кислоты, питьевой соды и других
средств обеззараживания и нейтрализации вредного воздействия токсических и
агрессивных веществ.
К индивидуальной безопасности относится обязательное
наличие индивидуальных средств защиты, т.е. полногокомплекта спецодежды,
резиновых перчаток, защитных очков, противогазов марки ПШ-2 и др.
.4 Опасность поражения электрическим
током
Электробезопасность - система организационных и
технических мероприятий и средств, обеспечивающих защиту людей от вредного и
опасного воздействия электрического тока, электрической дуги, электромагнитного
поля и статического электричества.
Проходя через организм, электрический ток оказывает
термическое, электролитическое и биологическое действия, поэтому
электробезопасность в промышленности играет не менее важную роль. Вероятность
смерти при поражении электрическим током выше, чем при других видах
травматизма.
Основными источниками поражения электрическим током
являются:
- оголенная электропроводка;
рубильники, пускатели, предохранители;
- автоматы включения и выключения;
незаземленные и незащищенные провода;
корпуса электродвигателей.
Основными видами опасности связанными с электрическим
током являются:
- опасность напряжения прикосновением;
опасность шагового напряжения;
- опасность пробоя воздушного промежутка;
- опасность токов перегрузки;
опасность токов короткого замыкания.
Поражающими факторами электрического тока являются:
- напряжение от 43 В;
- сила тока свыше 10 мА;
продолжительность воздействия;
путь электрического тока;
сопротивление тела человека;
среда.
Для защиты людей от поражения электрическим током в
условиях производства применяют следующие меры:
- применение токов безопасного напряжения;
изоляция токоведущих частей и приводов;
механические ограждения источников поражения;
- защитные заземления;
- блокирующие устройства;
защитные средства (перчатки, боты);
предупреждающие плакаты.
Все работающие должны быть обучены способам оказания
первой помощи. При оказании первой помощи необходимо удалить пострадавшего от
токоведущего предмета, и в свою очередь защитить себя от поражения. При
легких поражениях следует вынести человека на свежий воздух, расстегнуть
одежду, привести в сознание, вызвать врача. При более тяжелых поражениях
провести искусственное дыхание и непрямой массаж сердца.
.5 Взрыво- и пожароопасность
Цех переработки фтористого натрия относится к
помещениям класса А, т.к в результате реакции сульфатизации выделяется
фтороводород, существует взрывоопасность его при взаимодействии с огнем или
искрой, поэтому электрооборудование в отделении применяется в обычном
исполнении с повышенной герметичностью. Так как все оборудование сделано из
стали X18Н10Т, ЭИ825, материалов, способных
гореть, то отделение переработки фтористого натрия относится к зданиям I категории. Во избежание
возникновения пожара необходимо соблюдать следующие правила:
- запрещается пользоваться органическими смазочными
материалами;
соблюдать герметичность аппаратов, не допускать
смешения газовой смеси с парами воды;
не допускать перегрузок токоведущих частей;
не загромождать помещение и проходы к аппаратам
постороннимоборудованием и материалами, способными гореть;
курить только в специально отведенных местах;
- обеспечить наличие в помещениях средств
пожаротушения: углекислотные огнетушители ОУ-2, ОУ-5; порошковые огнетушители
ОПС-6, ОПС-10, асбестовое полотно.
Мероприятия по предотвращению возникновения пожаров и
взрывов зависит от быстрых и слаженных действий персонала.
В случае возникновения пожара необходимо немедленно
эвакуировать весь рабочий персонал из цеха и сообщить пожарной команде.
Немедленно отключить подачу газовой смеси, отключить ток, удалить находящиеся
вблизи огня горючие и огнеопасные материалы, охладить место возгорания струей
из огнетушителя. Необходимо предусмотреть автоматическое отключение системы по
аварийному режиму.
Меры противопожарной безопасности:
исключения применения пожаро- и взрывоопасных веществ,
либо снижение их доли;
автоматизация и механизация процесса, своевременный
контроль технологической аппаратуры;
строгое соблюдение технологического режима;
использование электрооборудования в закрытом
исполнении;
административно-режимные мероприятия (запрещение
открытого огня);
установка звуковой и световой сигнализации;
установка на пожароопасных участках средств
пожаротушения;
обучение персонала действиям в условиях пожара.
.6 Производственная санитария
Производственная санитария представляет собой систему
организационных, гигиенических и санитарно-технических мероприятий и средств,
предотвращающих воздействие на работающих вредных производственных факторов.
В химической промышленности на работающих могут
оказывать вредное влияние различные физические факторы производственной среды:
метеорологические условия, шум, вибрация, недостаточное и плохое качество
производственного освещения и др.
.7 Метеорологические условия,
вентиляция и отопление
Метеорологические условия производственной среды складываются
из температуры воздуха, его влажности и скорости движения, а также излучений от
нагретых предметов. Метеорологические условия оказывают большое влияние на
здоровье, самочувствие и работоспособность человека.
Большие скорости движения воздушных потоков создают
сквозняки, неблагоприятно действующие на организм человека при высоких, и
особенно, при низких температурах.
Для выполнения работ средней тяжести, которые ведутся
в данном отделении, оптимальными являются следующие условия:
1. температура воздуха в холодное время года 16-18°С и 20-23°С в теплое
время года;
2. относительная влажность воздуха в течение года 40-60%;
3. скорость движения воздуха в течение года 0,3 м/с. Так как на одного
работающего приходится более 20 м3 помещения, то необходимо
установить приточную вентиляцию. Удаляя из производственного помещения нагретый
воздух и одновременно подавая свежий, более прохладный, вентиляционные
устройства поддерживают необходимые температурные условия. Кратность воздуха 5
час-1.
.8 Шум и вибрация
Шум и вибрация являются результатом колебания тел,
передаваемого непосредственно или на расстояние другим объектам. Шум и вибрация
различаются частотой колебаний в секунду. Вибрация вызывает так называемую
вибрационную болезнь и особенно неблагоприятно действует на женский организм.
Кроме того, вибрация приводит к преждевременному износу деталей, механизмов,
может вызвать аварию, вредно действует на сердечно-сосудистую и нервную системы
организма, вызывает снижение слуха и даже стойкую глухоту, является причиной
снижения работоспособности, ослабления памяти, внимания, остроты зрения, что
увеличивает возможность травматизма.
В химической промышленности проявления шума и вибрации
встречаются нередко. В цехе переработки фтористого натрия источниками шума являются:
установка сульфатизации, насосы и система вентиляции сила звука которых не
превышает 70 ДБ.
Мероприятия по борьбе с шумом и вибрацией во многом
сходны между собой. Прежде всего, стремятся устранить или уменьшить шум в
источнике его образования. Например, насосы устанавливать на нижних этажах
здания, в специальных углублениях и нишах.
При конструировании машин и оборудования там, где это
возможно, заменяют возвратно-поступательное движение на вращательное, применяют
лучшие кинематические схемы с более равномерным ходом, ослабляют звучание
ударных частей путем уменьшения размаха колебаний и ограничения размеров
поверхностей, соударяющихся деталей, уравновешивают движущиеся части. Вместо
металлических деталей все шире применяются бесшумные пластмассовые.
В тех случаях, когда меры по уменьшению шума в
источнике его образования исчерпаны, применяют меры снижения шума по пути его
распространения. Агрегаты с повышенным уровнем шума и вибрации стараются
размещать в отдельных изолированных помещениях. Стены покрывают
звукопоглощающими материалами (акустической штукатуркой, перфорированными
панелями, стекловолокном и др.). Фундаменты для шумящих машин устанавливают
независимо от фундамента здания и от полов, изолируют со всех сторон воздушным
промежутком (акустические швы) или заполняют свободное пространство материалом,
поглощающим вибрацию (пробка, войлок, шлак и др.).
Если не удается добиться снижения шума до допустимого
уровня, то применяют средства индивидуальной защиты. Их делят на три группы:
наушники, вкладыши и шлемы. Наушники бывают двух типов: независимые и
встроенные в головной убор. В наушниках типа ВЦНИИОТ-2М используют в качестве
защитного материала ультратонкую стекловату и тонкие трубки, наполненные
глицерином. Они могут снижать шум на 20 - 40 дБ. Вкладыши - это затычки,
забиваемые в ушные раковины. Шлем закрывает часть головы и уши.
.9 Производственное освещение
Работа аппаратчика заключается в непрерывном
наблюдение за показаниями контрольно-измерительных приборов, за механизмами и
аппаратурой, запорными устройствами, трубопроводами, что неосуществимо без
правильного освещения. Поэтому в помещениях с постоянным пребыванием людей
должно применяться естественное освещение (в светлое время суток), которое
создается через оконные и другие остекленные проемы, а также через световые
фонари, расположенные на крыше здания. Искусственное освещение создается
светильниками и может быть: общее, предназначенное для освещения всего рабочего
помещения, местное, освещающее только рабочее место, и комбинированное,
состоящее одновременно из общего и местного освещения.
Естественное освещение какой-либо точки помещения
характеризуется коэффициентом естественной освещенности (КЕО), буквенное
обозначение определяется по формуле:
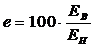 ,%
,%
где
 - естественная освещенность, создаваемая в некоторой
точке заданной плоскости внутри помещения светом неба;
- естественная освещенность, создаваемая в некоторой
точке заданной плоскости внутри помещения светом неба; 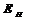 - наружная горизонтальная освещенность, создаваемая
светом полностью открытого небосвода.
- наружная горизонтальная освещенность, создаваемая
светом полностью открытого небосвода.
За
единицу освещенности принимается люкс (лк). Степень освещенности меняется в
очень широких пределах, однако глаз человека обладает громадной способностью
приспосабливаться (адаптироваться) к переменам освещенности, и человек в известных
пределах хорошо видит и при большой и при малой освещенности.
Использовать
только местное освещение не разрешается. Это вызвано тем, что резкая
неравномерность освещенности на рабочем месте и в помещении снижает
работоспособность зрения и вызывает его утомление.
Чтобы
создать необходимые благоприятные условия для работы, степень освещенности в
производственных помещениях нормируется. В зависимости от условий труда
санитарные нормы определяют освещенность на рабочем месте в пределах от 500 до
50 лк. При общем наблюдении за ходом производственного процесса, если требуется
постоянное наблюдение, освещенность установлена не менее 75 лк, а при
периодическом наблюдении - не менее 50 лк.
В
цехе устраивается аварийное освещение на тот случай, если внезапно прекратится
действие основного рабочего освещения.
Искусственное
освещение является комбинированным (к общему освещению добавляется местное
освещение рабочих мест). Используют люминесцентные светильники типа ОДА, ПВЛ -
1. Число светильников для цеха определяется по формуле:
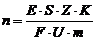 ,
,
где
Е - нормированная освещенность, Е = 250 лк;
S - площадь
помещения, S = 500 м2;
Z - поправочный
коэффициент, Z = 1,2;
F - световой
поток одной лампы, ЛД 40 F = 2130 лм;
U - коэффициент
использования, U = 0,55;
m - число ламп в
светильнике, m = 2.
n=100
светильников.
Личная
гигиена
В
рабочих помещениях не допускается курение, хранение и прием пищи. Перед приемом
пищи в столовой нужно вымыть руки, доступ в столовую в спецодежде запрещен.
После работы все должны тщательно вымыться в душе.
.10
Охрана окружающей среды
Борьба
за чистоту окружающей среды - это вопрос, который стоит в центре внимания не
только работников химической промышленности, но и всех людей планеты. Охрана -
это система государственных общественных мероприятий, обеспечивающих сохранение
природной среды, пригодной для жизнедеятельности нынешних и будущих поколений
людей. Основные направления в решении задач охраны природы определены
Конституцией Российской Федерации, рядом законов, решениями правительства.
Борьба
с химическим заражением и загрязнением окружающей среды заключается в
устройстве замкнутого цикла реагентов и надежной очистке воздуха, выходящего из
производственных помещений.
При
проектировании новых и реконструкции действующих предприятий должен быть
предварительно сделан расчет, доказывающий, что при их последующей эксплуатации
ПДК будут обеспечены. Проект каждого новостроящегося и реконструируемого
предприятия без раздела об очистке отходов производства, загрязняющих водоемы
или воздушную атмосферу, не утверждается и не выделяется ассигнований на его
строительство. Без очистных сооружений запрещены приемка новых или
реконструированных предприятий и их эксплуатация.
При
переработке фтористого натрия наиболее вероятно химическое воздействие на
окружающую среду.
Химическое
загрязнение обусловлено выбросом в атмосферу отработанных технологических газов
(легколетучих фторидов), проскочивших систему улавливания. Для их улавливания
необходимо установить систему «тонкой» очистки, предусматривающую полное
поглощение этих соединений.
При
строительстве предприятий следует учитывать «розу ветров», рельеф местности и
условия строительства на данной территории, с целью наименьшего загрязнения
важных народнохозяйственных объектов и населенных пунктов.
Основными
мероприятиями по борьбе с загрязнениями окружающей среды являются следующие:
)
организация технологического процесса, исключающая выброс газаи пыли в
атмосферу;
)
надежна герметизация оборудования.
)
организация эффективной системы очистки выходящих газов в местах
специализированного выброса.
При
оценке последствий воздействия на природу важное место занимают предельно
допустимые концентрации веществ, загрязняющих воздух и воду. В соответствии с
требованиями, содержание вредных примесей в атмосферном воздухе и водоемах не
должно вызывать патологических реакций в организме человека или приводить к
заметным воздействиям на флору и фауну. Необходимо отменить, что ПДК нормирует
не содержание вредных веществ в самих выбросах, а содержание этих веществ в
атмосферном воздухе или воде водоемов после смешения с выбросами.
В
России приняты два вида нормативов атмосферных загрязнений - максимально
разовые и среднесуточные ПДК. Назначение первых - предохранять население от
неблагоприятных реакций при кратковременном воздействии токсичных веществ во
вдыхаемом воздухе. Среднесуточные ПДК имеют своей целью предупредить вредное
влияние на население атмосферных загрязнений при их длительном вдыхании.
Вывод:
В
данном разделе охраны окружающей среды мной рассмотрены вопросы образующихся
отходов производства и предусмотрены мероприятия по их обезвреживанию и защите
окружающей среды. Запланированные мероприятия соответствуют санитарным
нормам[17].
8. Экономическая часть
Введение
Технико-экономическое обоснование (ТЭО) это документ, который
разрабатывается для вновь создаваемых и реконструируемых предприятий и
подтверждает экономичность проектирования и работы будущего предприятия, цеха,
технологического участка. В процессе ТЭО устанавливается производственная
мощность производства, потребности его в материалах, сырье, полуфабрикатах и
источниках их получения, решаются транспортные вопросы, определяется
себестоимость продукции и общие затраты на ее производство, необходимые
капитальные вложения и их экономическая эффективность. От качества ТЭО зависит
не только решение кратковременных проблем, связанных с капитальным
строительством и комплектацией новой техникой, но и эффективность дальнейшей
деятельности. В связи с этим очевидна необходимость в исследовательской работе.
В новых экономических условиях (в условиях рыночных отношений) данное
исследование проводится на этапе формирования бизнес-плана. Этот документ
отражает все стороны деятельности нового предприятия, его связи с поставщиками
и потребителями, планируемые затраты и сроки их окупаемости и т.д.
В данной работе рассматривается составление бизнес-плана на примере
конкретных исходных данных.
.1 Расчет эффективного фонда времени цеха
За основной расчетный период принимаем календарный год - 365 дней или 8760
часов.
Номинальный фонд работы оборудования:
Тн = Д р•Rр,
где Д р - количество рабочих дней в расчетном периоде;
Rр - количество рабочих часов в сутки.
При непрерывном режиме работы номинальный фонд времени равен
календарному:
Тн = Тк = 8760 часов.
Эффективный фонд времени будет составлять:
Тэф = Тк - Трем - Тто,
где Трем - время простоя оборудования на ремонтах;
Тто - время технологических остановок.
Определим Трем (по основному аппарату):
Таблица 8.1
Время работы между ремонтами и время простоя при ремонте
|
Время работы между
ремонтами, час
|
Время простоя при ремонте,
час
|
|
Капитальный
|
Средний
|
Текущий
|
Капитальный
|
Средний
|
Текущий
|
|
51840 (6 лет)
|
17280 (2 года)
|
720 (6 мес.)
|
2160 (3 мес.)
|
400
|
16
|
Общее количество ремонтов за ремонтный период:
R = Rц / Тт,
где Rц - длительность ремонтного цикла;
Тт - пробег оборудования между текущими ремонтами.
R =
51840/720 = 72 ремонта за ремонтный цикл.
Длительность ремонтного цикла:
Rц /
Тн =51840/8760 = 6 лет.
Количество средних ремонтов за ремонтный цикл:
Rc = Rц /Тс - 1,
где Тс - пробег оборудования между средними ремонтами;
Rc = 51840/17280 - 1 = 2 средних ремонта за ремонтный цикл.
Количество текущих ремонтов:
Rт = Rц / Тт - Rc - 1 = 69 текущих ремонтов.
Всего ремонтов в течение расчетного времени 72 / 6 = 12, т. е. 1 средний
и 11 текущих ремонтов.
Время на ремонт оборудования в расчетный период:
Трем = 11• Тт¢ + Т¢с р = 11•16 + 400 = 576 часа.
Время технологически неизбежных остановок:
Тто =Тп + Тпо,
где Тпо - время остановки (8 ч);
Тп - время пуска (8 ч).
Тто = 8 + 8 = 16 часов.
Эффективный фонд работы оборудования:
Тэф
= Тн - Трем - Тто, 
Тэф
= 8168 ч. (340 дней).
8.2
Организация труда и заработной платы
Цех
будет работать в 3 смены продолжительностью по 8 часов. Работа будет
производиться 4-ю производственными бригадами.
Таблица 8.2
График
сменности бригад
|
Дни Смены
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
15
|
16
|
17
|
18
|
19
|
20
|
21
|
22
|
23
|
24
|
25
|
26
|
27
|
28
|
29
|
30
|
31
|
|
с 0 до 8
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
|
с8до 16
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
|
с16до24
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
|
Выходные
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
Б
|
Б
|
В
|
В
|
В
|
Г
|
Г
|
Г
|
А
|
А
|
А
|
Б
|
где А, Б, В, Г, - бригады.
Длительность сменооборота:
Тсм.об. = ns•Тм,
где ns - число бригад;
Тм - число дней, когда бригада ходит в смену (3 дня).
Тсм.об. = 15 дней.
За длительность сменооборота бригада отдыхает 6 дней, за год 146 дней.
Таким образом, на одного среднесписочного рабочего приходится 146 выходных
дней.
Таблица 8.3
Баланс рабочего времени среднесписочного рабочего
|
Элементы времени
|
Количество дней
|
|
Календарное число дней
|
365
|
|
Нерабочие дни, выходные
|
146
|
|
Номинальный фонд рабочего
времени
|
219
|
|
Планируемые выходные: А)
очередные отпуска Б) по болезни В) выполнение общественных обязанностей Г)
отпуск в связи с учебой
|
42 8 1 3
|
|
ИТОГО:
|
54
|
|
Эффективный фонд рабочего
времени
|
194
|
8.3 Расчет численности рабочих, служащих, ИТР и МОП
Определим явочное число основных рабочих в сутки:
Rяв =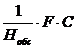 ,
,
F - количество
установок (9);
С
- количество смен в сутки (3).
Rяв = = 9 чел.
= 9 чел.
Определим
списочное число основных рабочих:
Rсп = Rяв•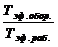 ,
,
где
Тэф.обор. - проектируемое число дней работы оборудования в год;
Тэф.раб.
- проектируемое число дней работы в год одного рабочего.
Rсп = 9•340 / 194 = 15 чел.
Приведем
состав рабочего персонала ниже в таблице.
Таблица 8.4
Состав рабочего персонала
|
Наименование профессии
|
Раазряд
|
Число рабочих в смену
|
Rсп в
сутки
|
Число рабочих дней в году
|
Число рабочих дней
оборудования.
|
Число смен в сутки
|
|
Аппаратчик
|
5
|
1
|
3
|
6
|
194
|
340
|
3
|
|
Аппаратчик
|
4
|
1
|
3
|
6
|
194
|
|
|
|
Аппаратчик
|
3
|
1
|
3
|
6
|
194
|
|
|
8.3.1 Расчет численности дежурного персонала
Дежурный слесарь - 1
Дежурный электрик - 1
Дежурный КИПиА - 1
Списочное число рабочих дежурного персонала:
Rяв = 9 чел/сут;
Rсп = 12 чел.
Сведем число дежурного персонала в таблицу.
Таблица 8.5
Количество дежурного персонала
|
Профессия
|
Разряд
|
Число рабочих в смену
|
Число смен
|
Rяв
|
Rсп
|
Число рабочих дней в году
|
Число рабочих дней оборуд.
|
|
Слесарь
|
5
|
1
|
3
|
3
|
5
|
230
|
340
|
|
Электрик
|
5
|
1
|
3
|
3
|
5
|
230
|
340
|
|
Сл. КИПиА
|
5
|
1
|
3
|
3
|
5
|
230
|
340
|
8.3.2 Расчет численности ИТР и служащих
Расчет производится с учетом потребности цеха в каждой группе работников.
Таблица 8.6
Численность ИТР, служащих и МОП
|
№
|
Наименование должности
|
Категория
|
Количество работников
|
|
1
|
Начальник цеха
|
ИТР
|
1
|
|
2
|
Технолог цеха
|
ИТР
|
1
|
|
3
|
Мастер смены
|
ИТР
|
5
|
|
4
|
Лаборант
|
ИТР
|
5
|
|
5
|
Уборщица
|
МОП
|
2
|
|
Итого:
|
14
|
8.4 Расчет годового фонда заработной платы
8.4.1 Расчет фонда заработной платы основных рабочих
Расчетный фонд заработной платы (ЗП) складывается из основной и
дополнительной заработной платы.
Основной фонд (ЗП):
Зосн. = Зтар + Дпр + Дн.вр. +
Дбр + Дпраз. + Фм,
где Зтар - тарифный фонд;
Дпр - оплата премий;
Дн.вр. - доплаты за ночные смены;
Дбр - доплата за бригадирство;
Дпраз. - доплата за работу в праздники;
Фм - фонд мастера.
а) Тарифный фонд
Зтар = З3тар + З4тар
+ З5тар,
где З3тар,З4тар, З5тар
- ЗП по тарифным ставкам рабочих различной квалификации.
Зтар = Rсп •Тэф
•Тсп,
где Rсп - списочное число рабочих;
Тэф - эффективное время работы одного среднесписочного
рабочего;
Тсп - тарифная часовая ставка.
Часовая тарифная ставка составляет для аппаратчиков:
го разряда - 80 руб/час;
го разряда - 70 руб/час;
го разряда - 60 руб/час.
З5тар = 3•1872•80= 449280 руб.
З4тар = 3•1872•70 = 392120 руб.
З3тар = 3•1872•60 = 336950 руб.
Зтар = 449280+392120+336950 = 1178360 руб.
б) Доплата за работу в ночное время осуществляется отчислением 100% от
тарифной ЗП:
Дн.вр.
= Зтар •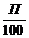 ,
,
где
П - процент отчисления.
Дн.вр.
= 1178360•100 / 100 = 1178360 руб.
в)
Доплата премий - 20% от тарифной ЗП:
Дпр
= Зтар •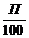 = 1178360•20/100 =235672 руб.
= 1178360•20/100 =235672 руб.
г)
Доплата за бригадирство 10% от З5тар (осуществляется
аппаратчиком 5го разряда):
Дбр
= З5тар•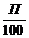 =
449280•10/100 = 44928 руб.
=
449280•10/100 = 44928 руб.
д)
Доплата за работу в праздничные дни.
Принято
11 праздничных дней в году. Доплата в праздничные дни осуществляется по двойным
тарифным ставкам:
Дпр
= Дпр3 + Дпр4 + Дпр5.
Дпр
= Rяв•N•Тст,
где
N - число праздничных дней в году.
Дпр3
= 3•60•121 = 21780 руб.
Дпр4
= 3•70•121 = 25410 руб.
Дпр5
= 3•80•121 = 29040 руб.
Дпр
= 21780+ 25410 +29040 = 76230 руб.
ж)
Премия из фонда мастера - 3% от Зтар:
Фм
= Зтар •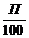 =1178360 •3/100 = 35507,6 руб.
=1178360 •3/100 = 35507,6 руб.
Зосн
= 1178360 + 1178360 +235672+ 44928 +35507 +76230 = 2749057руб.
8.4.2
Расчет фонда дополнительной заработной платы
Определим
процент дополнительной заработной платы:
Пд.з.
= Тотп /Тэф.б.•100%,
где
Дн - планируемые целодневные невыходы в год;
Вп
- планируемое количество дней работы одного среднесуточного рабочего.
Пд.з.
= (42/194)•100 = 21%
Здоп
= Зосн•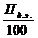 = 2749057*(21/100) = 549811
руб.
= 2749057*(21/100) = 549811
руб.
Годовой
фонд ЗП основных рабочих:
З¢ = Зосн + Здоп = 2749057+ 549811
= 3298868,4 руб.
С
учетом районного коэффициента:
З
= З¢•Кр = 3298868,4 •1,3 = 4288528 руб.
8.4.3
Расчет фонда заработной платы вспомогательных рабочих
Зобщ
= Зосн + Здоп.
Зосн
= Зтар + Дпр + Дн.вр. + Фм +
Дпразд.
а)
Тарифный фонд ЗП вспомогательных рабочих:
Зтар
= Rсп•Тэф•Тсп.
Зтар3
= 12•1872•60 = 1387840 руб.
б)
Премии - 10% от Зтар:
Дпр =1387840 •0,1 = 138784 руб.
в) Доплата за работу в ночное время - 100 % от Зтар:
Дн.вр = 1387840•1 =1387840 руб.
г) Доплата за работу в праздничные дни:
Дпраз = Rяв•N•Тсп = 60•12•121 = 87120 руб.
д) Доплата из фонда мастера - 3% от Зтар:
Фм = 87120 •0,03 = 2640 руб.
Зосн = 1387840 + 138784+ 1387840 +87120 + 2640= 3003894 руб.
Учитывая районный коэффициент:
Здоп = Зосн•0,4 = 1201000 руб.
З¢ = Зосн + Здоп
= 3003894+ 1201000 = 4205463руб.
З = З¢•1,3 =
4205463•1,3 = 5467102 руб.
8.4.4 Расчет годового фонда заработной платы ИТР и служащих
Оклады должностных лиц ИТР, служащих устанавливаются в зависимости от
категории цеха.
Начальник цеха - 20000 руб.
Технолог - 18000 руб.
Мастер смены - 14000 руб.
Лаборант - 8000 руб.
Уборщица - 3000 руб.
а) Фонд ЗП вычисляем путем умножения числа штатных единиц на их месячный
оклад и на число месяцев работы в году. Число месяцев работы в году для ИТР
принимаем равным 11 месяцев, для служащих - 11,3 месяца.
Фосн = 1•11•20000+1•11•18000+5•11•14000+5•11•8000+2•11,3•3000
=
руб.
б) Дополнительная ЗП ИТР и служащих находится по формуле:
Здоп
= 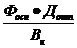 ,
,
где
Фосн - основной фонд заработной платы;
Дотп
-календарное количество дней отпуска: для ИТР - 30 дней, для служащих - 24;
Вк
- календарный год - 365 дней.
Здоп= =8802,2 р.
=8802,2 р.
в)
Доплата за работу в праздничные дни (рассчитывалась для мастера смены и
уборщицы):
Дпр
=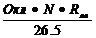 , (6.21.)
, (6.21.)
где
Окл. - месячный оклад;
N - количество
праздничных дней в году;
,5
- среднемесячное число рабочих дней.
Дпр
= 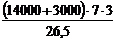 = 13472 руб.
= 13472 руб.
г)
Годовой фонд заработной платы ИТР, служащих и МОП:
Фзп
= Фосн + Здоп + Дпр = 1695800+8802,2
+13472=1718074,2 руб.
С
учетом районного коэффициента:
Фзп
= 1718074,2 •1,3 = 2233496,4 руб.
.5
Расчет капитальных затрат
Расчет
стоимости оборудования
Для организации участка необходима закупка или изготовление следующего
оборудования (согласно технологической схеме и плану участка)
Таблица 8.7
Стоимость оборудования
|
№
|
Наименование оборудования
|
Цена за шт. тыс. руб.
|
Кол.
|
Стоимость тыс. руб
|
|
1
|
Загрузочный бункер
|
72
|
1
|
144
|
|
2
|
Установка сульфатизации
|
3731
|
1
|
3731
|
|
3
|
Абсорбционная колонна
|
1671
|
1
|
1671
|
|
4
|
Форконденсатор
|
473,5
|
1
|
473,5
|
|
5
|
конденсатор
|
543
|
1
|
543
|
|
6
|
насос
|
120
|
5
|
600
|
|
7
|
Шнек
|
50,4
|
2
|
100,8
|
|
8
|
ёмкость
|
18
|
7
|
129,4
|
|
9
|
Конденсатор-холодильник
|
567
|
1
|
567
|
|
10
|
Газоочистительная колонна
|
103
|
1
|
103
|
|
ИТОГО
|
8348,9
|
9062,7
|
Расходы на содержание и эксплуатацию оборудования:
транспортные расходы на перевозку оборудования, заготовительно -
складские работы составляют 8% от стоимости оборудования:
Зтр = 9062740•0,08 = 725019,2 руб.
стоимость монтажных работ составляет 20% от стоимости оборудования:
Змонт. = 9062740•0,2 = 1812548 руб.
стоимость специальных работ принимаем 10% от стоимости оборудования
(строительство фундаментов, трубопроводов, пусконаладочных работ):
Зсп. р. = 9062740•0,1 = 906274 руб.
Капитальные затраты на оборудование составят:
Зк.об.=Соб +Зтран.+Змонт.+Зсп.р.=9062740+725019,2+1812548+906274
=
,2 руб.
Сумма капитальных затрат:
åЗкап = Сзд. + Зк. об. =
0+12506581,2 = 12506581,2 руб.
Расчет затрат на производство
Расходы на охрану труда и технику безопасности составляют 12% от Фз.
п.:
Зо. т. = 11836000 •0,12 = 1420320 руб.
Балансовая стоимость здания условно принята 2000000 рублей.
Затраты на текущий ремонт здания составляют 2% от стоимости здания:
Зт. р. =2000000•0,02 = 40000 руб.
Содержание здания (включает в себя затраты на освещение, отопление,
вентиляцию) - 2% от стоимости здания:
Зсод. = 2000000•0,02= 40000 руб.
Амортизационные отчисления - 3,7% от стоимости здания:
Зам. = 2000000•0,037 = 74000 руб.
Сумма затрат на содержание и эксплуатацию здания составляет:
åЗ = 40000 + 40000 + 74000 = 154000 руб.
Текущий ремонт производственного оборудования обходится в 7% от стоимости
оборудования:
Зт. р. = 9062740•0,07 = 634391,8 руб.
Отчисления на амортизацию оборудования -10% от стоимости оборудования:
Зам = 9062740•0,1 = 906274 руб.
Расходы на содержание оборудования составляют 3% от стоимости оборудования:
Зсод. =9062740•0,03 = 271882,2 руб.
Сумма расходов на содержание и эксплуатацию оборудования составляет:
åЗ = 634391,8 +906274+271882,2 = 1812548 руб.
Таким образом, общепроизводственные расходы составят:
Зобщ. = 154000+ 1812548 = 1966548 руб.
8.6 Расчет технологических затрат
Расчет затрат на электроэнергию
Зэн. = Тэ•Nт•Тр.
об.,
где Тэ - стоимость 1 кВт×ч электроэнергии, руб. (2,62 руб.);
Nт - суммарная мощность приводов, кВт×ч (25 кВт×ч);
Тр. об. - время работы оборудования в год, час (8088час.).
Зэн. = 2,62•25•8088 = 533808 руб.
Расчет затрат на воду.
Звод. = Тв•Тр. об.•В,
где Тв. - стоимость 1м3 воды, руб. (55 руб/м3);
В - часовой расход воды, м3 (1 м3/ч).
Звод. =55•8088•1=444840 руб.
Расчет затрат на серную кислоту:
Зк-та = Тг• Тр. об.•К,
Где Тг - стоимость 1т, руб. (700 руб.);
К - часовой расход серной кислоты, тонны (0,287 т/ч).
Зк-та = 700•8088•0,277 = 1568263 руб.
Отчисления на социальные нужды
Отчисления на социальные нужды составляют 26% от Фз. п.:
Сумма (26%) составляет:1099896,4 руб.
Калькуляция себестоимости
Сумма цеховой себестоимости и общезаводских расходов составляет
общезаводскую себестоимость:
Соб. зав. = Сцех. + Зоб. зав.,
где Сцех. - цеховая себестоимость (складывается из суммы
условно-переменных и условно-постоянных затрат);
Зоб.зав. - общезаводские расходы (составляют 15% от цеховой
себестоимости).
Планируемый объём получения фтороводорода 836 тонн/год.
Таблица 8.8
Проектная калькуляция себестоимости 1кг фтороводорода
|
Статьи расходов
|
Годовые затраты
|
|
На 1 кг фтороводорода, руб
|
В год, руб.
|
|
Химические реагенты: Серная
кислота Электроэнергия, кВт×ч 3. Вода техническая, м3
|
1,9 0,64
0,53
|
1568263 533808 444840
|
|
Итого:
условно-переменные затраты
|
3,1
|
2546911
|
|
Фонд ЗП: -основных рабочих
-Вспомогательных рабочих -ИТР и служащих
|
5,1 6,5 2,7
|
4288528 5467102 2233496
|
|
5. Отчисления из Фзп
на соц. нужды
|
1,35
|
1099896,4
|
|
6. Расходы на ОТ и ТБ
|
1,69
|
1420320
|
|
- амортизация оборудования
тек. и кап. ремонт содержание оборудования
|
1,1 0,75 0,32
|
906274 634391,8 271882,2
|
|
7. - амортизация здания
тек. и кап. ремонт содержание здания
|
0,09 0,05 0,05
|
74000 40000 40000
|
|
Итого:
условно-постоянные затраты
|
19,7
|
|
8. Цеховая себестоимость
|
22,8
|
19022800
|
|
9. Общезаводские расходы
|
3,42
|
2853420
|
|
10.Общезаводская
себестоимость
|
26,22
|
21876220
|
|
|
|
|
Анализируя данные таблицы 6.8. делаем вывод, что себестоимость получения
1кг фтороводорода равна 26,22 рублей.
Цена продукта учитывая НДС и 50% процент на прибыль составляет:
Ц = 26,22 + 26,22•0,18+26,22•0,5= 44,05 руб/кг
.7 Анализ экономических показателей
Для проведения данного анализа необходимо составить сводку основных
экономических показателей. К ним относятся:
1. Прибыль валовая и чистая
2. Рентабельность производства;
3. Срок окупаемости
4. Эффективность проекта.
.7.1 Общая прибыль
Общая прибыль составит:
Пр = Ц ∙ Vпр,
= Ц ∙ Vпр,
где:
Ц- цена за единицу продукта,
Vпр-объем производства,
Пр =39,33 ∙ 836000 =30096000руб.
=39,33 ∙ 836000 =30096000руб.
Следовательно
балансовая прибыль составит:
Пр = Пр
= Пр - С.,
- С.,
где:
С - общезаводская себестоимость,
Пр =32879880-21876220=11003860 руб.
=32879880-21876220=11003860 руб.
Определим
чистую прибыль производства:
Пр = Пр
= Пр - Пр
- Пр •0,24,
•0,24,
Пр =11003860 - 11003860 •0,24= 8362981руб
=11003860 - 11003860 •0,24= 8362981руб
8.8.2 Рентабельность производства
Величина рентабельности производства составляет:
Re = (R /С)•100%,
/С)•100%,
где:
С - общезаводская себестоимость,
Rt - годичная сумма денежных поступлений от реализации
проекта,
Re =
(9343255/21876220)•100% = 42% т. е. на 100 руб. затрат приходится 42 руб.
прибыли.
8.8.3 Срок окупаемости
Срок окупаемости определяем по формуле:
Ток=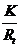 ,
,
где
К - капитальные вложения
R =Пр.+Аморт.отчисл.= 8362981+
(906274+74000)= 9343255
=Пр.+Аморт.отчисл.= 8362981+
(906274+74000)= 9343255
Ток
=12506581,2 / 9343255= 2,4года.
Оценка
эффективности
Оценку
эффективности проекта проводим на основании рассчитанных значений ЧДД, ВНД и
ИД.
Чистый
дисконтированный доход (ЧДД) определяется как:
ЧДД
= Σ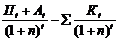 ,
,
где
Пt - прибыль, равная руб. 30096000
Аt
- амортизационные отчисления, равные 980274 руб.
K - годовые затраты на производство 19022800 руб.
- годовые затраты на производство 19022800 руб.
t - время
существования проекта(10 лет)
n - норма
дисконта (n = 0,2);
Если
ЧДД > 0, то проект является эффективным.
В первый год прибыль будет отсутствовать, а будут лишь затраты на
строительство здания, во второй год будут присутствовать затраты на закупку
оборудования и сырья для первого запуска:
ЧДД1 =(0+0)/(1+0.2)1-12506582 /(1+0.2)1=-10422150
руб.
ЧДД2 =8236900руб.
ЧДД3=6950236 руб.
ЧДД4=6102369 руб.
ЧДД5=4863298 руб.
ЧДД6=4105696 руб.
ЧДД7=3421036 руб.
ЧДД8=2820369 руб.
ЧДД9=2421000 руб.
ЧДД10=2105690 руб.
ЧДД
= 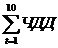 = 30235600 руб
= 30235600 руб
Индекс доходности (ИД) рассчитывается по формуле:
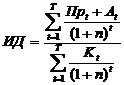 = 2,4
> 1,0
= 2,4
> 1,0
следовательно,
проект является эффективным.
Таблица 8.9
Основные технико-экономические показатели
|
Показатель
|
Размерность
|
Значение
|
|
Объём производства
|
т/год
|
836
|
|
Капитальные вложения
|
млн. руб.
|
12,506
|
|
Зароботная плата основных
рабочих
|
млн. руб.
|
4,28
|
|
Общезаводская себестоимость
|
руб.
|
26,22
|
|
Цена кг готовой продукции
|
руб.
|
44
|
|
Критический объем
производства
|
тыс. кг/год
|
425
|
|
Чистая прибыль
|
млн. руб.
|
8362981
|
|
Рентабельность производства
|
%
|
42
|
|
Срок окупаемости проекта
|
годы
|
2,4
|
Выводы:
В данном проекте произведён расчёт себестоимости получения одного
килограмма фтороводорода. Цена продукта 44 руб. На основании построения графика
безубыточности делаем вывод, что безубыточность данного производства составила
425000 кг/год. Так как проектная мощность нашего производства составляет 836
т/год, следовательно, чистая прибыль составит 8362981 руб.
Заключение
по проекту:
. На основании обобщения литературных данных сделан вывод о необходимости
переработки фторида натрия
. Наиболее удобным способом разложения фторида натрия является метод
сульфатизации в барабанной установке.
. Проведён термодинамический расчет, который показал, что реакция идет во
всём интервале исследуемых температур. Равновесие реакции необратимо сдвинуто в
сторону образования продуктов. Реакция интенсивно проходит при нормальном
давлении, температуре и времени 120 мин достигается 98.6% степень реагирования.
. На основании проведённых экспериментальных работ предложена общая
аппаратурная и технологическая схема процесса, рассчитана себестоимость.
. Основными продуктами предложенной технологии являются HF-сырец, который применяется в
получении фторида алюминия в алюминиевом производстве
Список литературы
1. Глинка
Н.Л. Общая химия: Учебное пособие для вузов. - Л.: Химия. - 1986. - 704с.
2. Е.И.
Мельниченко, И.Г. Масленикова, Д.Г. Эпов, С.Б. Буланова // Журнал прикладной
химии - 1999. -Т. 72. Вып. 3. - С. 362-366.
. Раков Э.Г.
Химия и технология неорганических фторидов. М.: Изд. МХТИ им. Менделеева, 1990.162
с.
. Л.Г. Рысс.
Химия фтора и его неорганических соединений. М. - 1965. - 543 с., С 583-592.
. Карапетьянц
М.Х. Химическая термодинамика. - М.: Химия. - 1975. - 584с.
. Киреев В.А.
Методы практических расчетов в термодинамике химических реакций. - М.: Химия. -
1975.
. Наумов
Г.Б., Рыженко Б.Н., Ходаковский Н.А. Справочник термодинамических величин (для
геологов). - М.: Атомиздат, 1971. - 240с.
8. Дельмон Б. Кинетика гетерогенных реакций. - М.: «Мир», 1972.
9. Основные процессы и аппараты химической технологии: Пособие по
проектированию. Под ред. Ю.И. Дытнерского. - М.: «Химия», 1983. 272 с.
10. Э.Г.
Раков, В.В. Тесленко, Пирогидролиз неорганических фторидов, М.:
Энергоатомиздат, 1987, С 76-81.
11. Михалев М.Ф., Третьяков Н.П., Мильченко А.И., Зобнин В.В. Расчет и
конструирование машин и аппаратов химических производств: Примеры и задачи:
Учебное пособие для вузов. Л.: «Машиностроение», 1984. 301 с.
И.А. Александров. Ректификационные и абсорбционные аппарата
. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу
процессов и аппаратов химической технологии. Л.: «Химия», 1976. 552 с.
. Касаткин А.Г. Основные процессы и аппараты химической технологии. М.:
«Госхимиздат», 1960. 830 с.
15. Лапшенков
Г.И., Полоцкий Л.М., «Автоматизация химических производств. Теория, расчет и
проектирование систем автоматизации», М., «Химия», 1982 г., с. 9., с. 178.
. Безопасное
обращение с отходами. Сборник нормативно методических документов. С.- Пб.: 2002
г.
. Сушков
А.И., Троицкий И.А. «Металлургия алюминия», Москва 1965 г.
ОТЗЫВ РЕЦЕНЗЕНТА
На дипломную работу студента гр. 0442 Портного Ивана Васильевича
На тему: «Проект цеха переработки фторсодержащих отходов алюминиевого
производства, производительностью 1500 т/год по исходному сырью».
Дипломный проект Портного И.В. изложен на 97 листах пояснительной записки
и 7 листах графической части.
В работе приведен литературный обзор, включающий анализ технологии
производства алюминия с выявлением основных отходов производства, описана
технология получения фтористого водорода.
Проанализированы преимущества предлагаемого метода переработки
фторсодержащих отходов производства фторида алюминия.
В дипломном проекте проведен термодинамический расчет процесса
сернокислотного разложения криолита и фторида натрия.
Студентом произведены материальный, тепловой, аппаратурный расчеты,
разработаны технологическая, аппаратурная схемы, схема автоматизации процесса
переработки фторида натрия до фтороводорода. Произведен расчет барабанно -
вращающейся печи, форконденсатора, абсорбционной колонны. Проведены необходимые
расчеты по экономике, рассмотрены вопросы охраны труда и техники безопасности.
В ходе реализации дипломного проекта студентом не в полном объеме
проработан вопрос взаимодействия отдельных узлов и аппаратов цеха.
За время дипломирования Портной И.В. зарекомендовал себя
коммуникабельным, бесконфликтным, настойчивым студентом. Успешно справляющимся
с поставленной задачей, проявляющим инициативу. Уверенно работает
самостоятельно и в команде.
Учитывая вышесказанное, считаю, что дипломный проект заслуживает оценки
«Хорошо», а Портной И.В. присвоения квалификации «инженера - технолога».
Руководитель работы ст. преподаватель Крайденко Р.И.