Расчет материального баланса производства глинозема способом Байера. Оценка распределения в нем органических примесей
Курсовой проект
Расчет материального
баланса производства глинозема способом Байера. Оценка распределения в нем
органических примесей
1. Способ Байера. Общие сведения
Промышленные способы получения глинозема
Из различных алюминиевых руд глинозем можно получать
щелочными и кислотными способами вследствие наличия у него амфотерных свойств.
В промышленности применяются пока только щелочные способы; чисто кислотные и
кислотно-щелочные способы находятся в стадии лабораторных и полузаводских исследодваний.
Промышленные щелочные способы производства глинозема из
бокситов, нефелинов и алунитов подразделяют на:
1. гидрохимический (способ Байера);
2. способ спекания;
3. комбинированный способ (сочетание способа Байера со
способом спекания в параллельном или последовательном варианте).
Для нефелиновых руд применяется только способ спекания с
известняком или с известняком и содой. выбор же способа переработки бокситов
определяется следующими основными факторами:
1. кремневым модулем;
2. содержанием Fe2O3;
. содержанием вредных примесей: карбонатов, сульфидов
и органических веществ;
. минералогическим составом сырья.
При прочих благоприятных условиях бокситы с кремневым модулем
>6-7 целесообразно перерабатывать по способу Байера, бокситы с кремневым
модулем <6 и с умеренным содержанием оксида железа (не более 20% Fe2O3)
- по последовательному варианту комбинированного способа Байер-спекание и,
наконец, бокситы с модулем <6, но с повышенным содержанием Fe2O3
- по способу спекания. Под благоприятными условиями имеется в виду малое
содержание в бокситах карбонатов и сульфидов (особенно FeCO3 и FeS2).
Из-за повышенного содержания этих примесей может оказаться невыгодным способ
Байера для бокситов с кремневым модулем >6-7 вследствие больших потерь
каустической щелочи (переход ее в соду и сульфат натрия), плохого отстаивания
красного шлама и загрязнения алюминатных растворов двухвалентным железом.
Способ Байера - самый дешевый и самый распространенный,
однако лдя его осуществления требуются высококачественные бокситы. Способ
спекания - наиболее дорогой, но более универсальный и может применяться к
любому высококремнистому алюминиевому сырью. С большим успехом применяются
комбинированные щелочные способы. Параллельный вариант используют для
термической каустификации соды и компенсации потерь дорогой каустической щелочи
более дешевой содой; для спекательной ветви этого варианта может применяться
как высококачественный байеровский боксит, так и спекательный. Последовательный
вариант комбинированного способа по технико-экономическим показателям занимает
промежуточное положение между способом Байера и способом спекания и применяется
для высококремнистых бокситов для максимального извлечения из них глинозема.
Основы способа Байера
Способ Байера основан на свойстве алюминатных растворов
находится в устойчивом состоянии при повышенных температурах и концентрациях и
на самопроизвольном их разложении (гидролизе) с выделением в осадок гидроксида
алюминия при понижении температуры и концентрации. В основу этого способа
положены патенты К. Байера (Германские патенты №43977 от 3 августа 1889 г. и
№65604 от 3 сентября 1892 г.), работавшего в России на химическом заводе в
Санкт-Петербурге. Согласно этим патентам получение глинозема из бокситов
заключается в выщелачивании их оборотными алюминатно-щелочными растворами,
отделении красного шлама и разложении насыщенных алюминием алюминатных
растворов при перемешивании с затравкой - свежеосажденным гидроксидом алюминия.
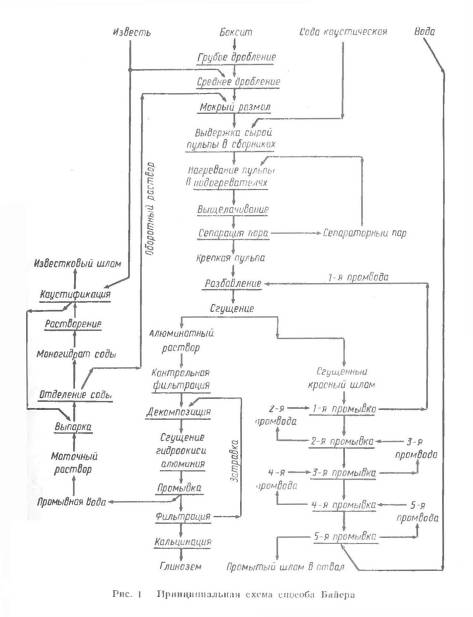
Принципиальная схема способа Байера представлена на рис. 1. В
зависимости от состава боксита и местных условий могут быть различные варианты
этой схемы.
Поступающий на склад боксит после крупного и среднего
дробления смешивают с небольшим оъемом оборотного щелочного раствора (ж:т =
0,8-1,2) и направляют в мельницу мокрого размола. Такое низкое отношение ж:т в
мельнице обеспечивает максимальную ее производительность. К диаспоровому
бокситу добавляют 3-5% извести. Мельницы обычно работают в замкнутом цикле с
реечными или спиральными классификаторами, которые иногда заменяют или дополняют
гидроциклонами. Пульпа из мельниц собирается в сборниках, куда подают остальное
количество оборотного раствора. Здесь ее нагревают паром сепарации до 90-100°С
и выдерживают несколько часов при перемешивании для предварительного
обескремнивания боксита, т.е. перевода большей части кремнезема из боксита в
раствор и далее в осадок в виде гидроалюмосиликата натрия. Этим достигается
меньшее зарастание алюмосиликатной накипью трубок подогревателей, через которые
проходит пульпа в автоклавы.
Далее пульпа нагревается в системе подогревателей и подается
в автоклавную батарею для выщелачивания боксита. Из последнего автоклава
батареи «варения» пульпа перетекает в систему сепараторов (пароотделителей),
где от самоиспарения алюминатного раствора образуется пар, используемый для
предварительного нагрева пульпы в подогревателях перед автоклавами. из
последнего сепаратора охлажденная пульпа поступает в мешалки для разбавления
промывной водой и далее на отделение и промывку красного шлама в систему
сгустителей, работающих по принципу противотока.
Промытый и сгущенный в последнем сгустителе красный шлам
откачивается в отвал на шламовое поле, а алюминатный раствор (слив) из первого
(основного) сгустителя подается на контрольную фильтрацию для полного отделения
взвеси шлама. Чистый алюминатный раствор охлаждается до 55-60°С в
теплообменниках и поступает вместе с затравочным гидроксидом на разложение
(декомпозицию) в батарею декомпозеров.
После разложения в течении 40-100 ч полученная пульпа
гидроксида алюминия поступает на сгущение, отделяется маточный раствор (слив),
а сгущенный гидроксид алюминия после классификации по крупности (или без нее)
делят на две части: одну часть (крупная фракция в случае классификации)
тщательно отмывают от щелочи и отправляют на кальцинацию; другую часть (около ¾ всего гидроксида) используют в качестве затравки. Иногда
затравочный гидроксид также предварительно промывают, но не так тщательно, как
товарый (для кальцинации).
Маточный алюминатный раствор с 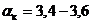 и воду от промывки гидроксида (промводу) направляют на выпарку в
вакуумные многокорпусные аппараты, где концентрацию Na2Oк
в растворе повышают до 200-300 г./л. Так как растворимость соды уменьшается с
повышением содержания каустической щелочи в растворе, то часть соды выпадает в
виде одноводной по мере выпаривания маточного раствора. При установившемся
процессе выпариванием выделяется столько же соды, сколько ее накапливается за
весь процесс. Этим предотвращается накопление соды в растворе, и концентрация
ее поддерживается в определенных пределах.
и воду от промывки гидроксида (промводу) направляют на выпарку в
вакуумные многокорпусные аппараты, где концентрацию Na2Oк
в растворе повышают до 200-300 г./л. Так как растворимость соды уменьшается с
повышением содержания каустической щелочи в растворе, то часть соды выпадает в
виде одноводной по мере выпаривания маточного раствора. При установившемся
процессе выпариванием выделяется столько же соды, сколько ее накапливается за
весь процесс. Этим предотвращается накопление соды в растворе, и концентрация
ее поддерживается в определенных пределах.
Для уменьшения удельного расхода свежей каустической щелочи
отделенную от оборотного раствора соду растворяют в воде для каустификации
известковым молоком. Получающийся при этом разбавленный раствор каустической
щелочи упаривают вместе с маточным раствором или же в отдельных выпарных
аппаратах. К упаренному маточному раствору добавляют свежую едкую щелочь для
возмещения химических и механических потерь ее, и раствор направляют на
выщелачивание боксита.
Готовый гидроксид алюминия фильтруют и прокаливают при температуре
около 1200°С во вращающихся трубчатых печах, топочные газы которых тщательно
очищают от глинозема.
Взаимодействие органических веществ с растворами NaOH
Помимо основных составляющих - Al2O3, Fe2O3, SiO2 и TiO2, входящих в состав
различных минералов, в бокситах могут содержаться многочисленные примеси
органических веществ, соединений серы, фосфора, ванадия, хрома, галлия, фтора и
др. в малых или незначительных количествах.
В производстве глинозема по способу Байера маточные растворы
- оборотные, поэтому даже незначительные примеси в боксите постепенно могут
накапливаться в процессе, осложняя его и загрязняя Al(OH)3.
Органические вещества содержатся в бокситах в форме гуминов и
битумов. Гуминовые вещества состоят главным образом из гуминовых кислот -
продукта превращения лигина. Они хорошо реагируют с растворами щелочей, образуя
различные соединения щелочных гуматов, превращающихся в легко растворимый
оксалат натрия и в разные смолистые вещества, дающие с едкой щелочью коллоидные
растворы.
Гумины имеют сложный состав, химическая формула которых до
настоящего времени не установлена. Элементарный состав гуминов может быть
выражен следующими средними цифрами: 58% С, 36% О2, 4% Н2,
2% N2 и некоторых др.
Битумы отличаются от гуминов большим содержанием углерода и
водорода, они мало растворяются в щелочных растворах. Следовательно, не вся
органика, содержащаяся в бокситах, должна рассматриваться как одинаково вредная
примесь.
Хотя содержание органических веществ в бокситах составляет
только сотые доли процента, а в раствор переходит только гуминовая доля и то
лишь часть ее, но, как показала практика, через определенное число циклов в
растворах накапливаются значительные количества этих веществ. Многие
органические вещества оказывают вредное влияние на выщелачивание бокситов, на
сгущение и промывку красного шлама вследствие заметного повышения вязкости
алюминатных растворов, причем гидроксид алюминия получается более мелкий. Наконец,
эти вещества ухудшают работу выпарных аппаратов и кристаллизацию соды из
оборотных растворов.
Основной источник органических веществ - боксит; кроме того,
они попадают в растворы в результате взаимодействия их с фильтровальным
полотном и органическим флокулянтом (ржаной мукой). Органические вещества
частично удаляются на разных переделах, больше всего с красным шламом, готовым
гидроксидом алюминия, моногидратом соды (рыжей содой), выделяющимся при выпарке
маточных растворов, и с известковым шламом от каустификации рыжей соды. Чем
больше органических веществ, тем больше их выходит из цикла этими путями.
По достижении в цикле определенного количества органических
веществ наступает равновесие между их поступлением и выводом. При таком
равновесии содержание этих веществ должно оставаться ниже предельного, в
противном случае нужны дополнительные меры для очистки растворов. Обжиг, а в
некоторых случаях и промывка бокситов могут снизить предельную концентрацию
органических веществ в алюминатных растворах.
Среди упомянутых выше поглотителей органических веществ из
алюминатных растворов на разных переделах наилучшая адсорбционная способность у
моногидрата соды. Из-за адсорбции быстро прекращается рост кристалликов
моногидрата; выпадающий осадок состоит из мельчайших частиц, следовательно,
имеет большую удельную поверхность, а концентрация органических веществ в
выпарном растворе до начала кристаллизации соды наибольшая. Моногидрат соды
окрашен органикой, поэтому на заводах его называют «рыжей содой». Гидроксид
алюминия, полученный декомпозицией, тоже окрашен органическими веществами: он
розоватый в отличие от белоснежного гидроксида, получаемого по способу
спекания.
Количество органических веществ, адсорбируемых красным
шламом, зависит от его выхода, минералогического и дисперсионного состава, т.е.
от активной поверхности шлама, а так же от концентрации органических веществ в
алюминатном растворе.
2.
Материальный баланс производства глинозема из бокситов по способу Байера
Исходные данные
1. химический состав боксита, %:
Al2O3 54,0; Fe2O3 23,6; SiO2 4,0; TiO2 2,2; CaO 2,0; CO2 1,6; п.п.п. 11,0; прочие 1,6 (всего 100%); влага
(H2O) 7,0;
. химический состав извести, %:акт 86,4;
CaOсвяз 2,6; SiO2 3,6; CO2 2,0; прочие 5,4
(всего 100%); влага (H2O) 7,0;
. товарный выход Al2O3 89,0%;
4. расход извести 3,0% от массы сухого боксита;
. состав оборотного раствора, г/л:
Na2Oк 300,0; Al2O3
129,87; Na2Oу 26,10; CO2 18,52; H2O 945,50; плотность 1420 кг/м3; αк=3,8;
. состав алюминатного раствора Al2O3
145,15 г./л; плотность 1240 кг/м3; αк=1,7;
7. потери Na2O 62,9 кг;
. ж:т в уплотненной пульпе со сгустителя 3,0; с
последнего промывателя 2,5;
. содержание Na2O в жидкой фазе отвального шлама 2,145 г./л;
. разбавление пульпы при выщелачивании с учетом
самоиспарения в сепараторах составляет 1,5%;
. затравочное отношение (З.О.) 2,0; влажность
затравочной гидроокиси алюминия 20,0%; в сгущенной гидроокиси алюминия ж:т=1,0;
. расход воды на промывку гидроокиси алюминия 1 т,
влажность отфильтрованной гидроокиси 10,0%;
. с моногидратом соды увлекается оборотного раствора
25% от массы влажного осадка;
. количество извести при каустификации 125% от
стехиометрического; степень каустификации 90%;
. Na2Oобщ в растворе известковой
пульпы 10,0%, содержание влаги в отвальном известковом шламе 25,8%.
Расчет потерь
При товарном выходе Al2O3 89,0%, если в 1 т
полученного глинозема содержится 990,0 кг Al2O3,
потребуется сухого боксита 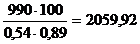 кг. В нем должно содержаться
кг. В нем должно содержаться  кг Al2O3.
кг Al2O3.
Следовательно, общие потери Al2O3 составляют
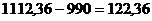 кг. Из этого количества потерь Al2O3
при дроблении теряется 0,2% Al2O3, или
кг. Из этого количества потерь Al2O3
при дроблении теряется 0,2% Al2O3, или 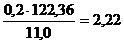 кг, что соответствует потере
кг, что соответствует потере 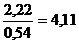 кг сухого боксита.
кг сухого боксита.
На размол поступает 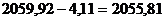 кг сухого боксита и сухой извести
кг сухого боксита и сухой извести 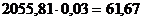 кг. Потери Al2O3 те же, что и при дроблении,
т.е. в сырой пульпе, поступающей на автоклавное выщелачивание, содержится
кг. Потери Al2O3 те же, что и при дроблении,
т.е. в сырой пульпе, поступающей на автоклавное выщелачивание, содержится 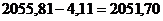 кг сухого боксита.
кг сухого боксита.
На выщелачивание поступает, кг:
|
С бокситом
|
|
Al2O3
|
|
2051,70·0,540=1107,92
|
|
Fe2O3
|
|
2051,70·0,236=484,20
|
|
SiO2
|
|
2051,70·0,040=82,07
|
|
TiO2
|
|
2051,70·0,022=45,14
|
|
CaO
|
|
2051,70·0,020=41,03
|
|
CO2
|
|
2051,70·0,016=32,83
|
|
П.п.п.
|
|
2051,70·0,110=225,68
|
|
Прочие
|
|
2051,70·0,016=32,83
|
|
Итого
|
|
2051,70
|
|
Влага
|
|
2051,70·0,07=143,62
|
|
С известью
|
|
CaO
|
|
61,67·0,89=54,89
|
|
SiO2
|
|
61,67·0,036=2,22
|
|
CO2
|
|
61,67·0,02=1,23
|
|
Прочие
|
|
61,67·0,054=3,33
|
|
Итого
|
|
61,67
|
|
Влага
|
|
61,67·0,05=3,08
|
Каустика необходимо ввести: 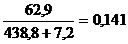 м3 или
м3 или 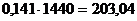 кг.
кг.
С каустиком поступает, кг:
|
Na2Oобщ
|
|
62,90
|
|
CO2
|
|
5,1·0,141=0,72
|
|
H2O
(по разности)
|
139,42
|
|
Итого
|
|
203,04
|
Примерный состав красного шлама, кг:
|
Al2O3
|
|
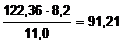 , без учета потерь от гидролиза, где 8,2
и 11,0% - потери Al2O3 с красным шламом в нерастворимой
форме и общие потери (см. табл. 1) , без учета потерь от гидролиза, где 8,2
и 11,0% - потери Al2O3 с красным шламом в нерастворимой
форме и общие потери (см. табл. 1)
|
|
Na2O
|
|
41,70
|
|
Fe2O3
|
|
484,20
|
|
TiO2
|
|
45,14
|
|
SiO2
|
|
82,07+2,22=84,29
|
|
CaO
|
|
41,03+54,89=95,92
|
|
Прочие
|
|
32,83+3,33=36,16
|
|
П.п.п.
|
|
63,19
|
В красном шламе должно содержаться Fe2O3,
TiO2, SiO2, CaO и прочих столько, сколько этих
компонентов в автоклавной пульпе.
Масса красного шлама без учета п.п.п. равна 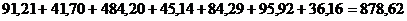 кг. П.п.п. подсчитываем так:
кг. П.п.п. подсчитываем так:
. SiO2 находится шламе в составе
гидроалюмосиликата натрия Na2O·Al2O3·2SiO2·2H2O; тогда с 84,29 кг SiO2 связаны 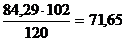 кг Al2O3 и
кг Al2O3 и 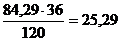 кг H2O;
кг H2O;
. CaO в шламе находится в составе CaO·TiO2·H2O; тогда с 45,14 кг TiO2 связанно 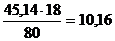 кг H2O;
кг H2O;
3. Al2O3, не
связанный в гидроалюмосиликат натрия, находится в шламе в составе 3CaO· Al2O3·6H2O; тогда с 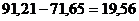 кг Al2O3 связанно
кг Al2O3 связанно 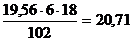 кг H2O;
кг H2O;
. примем, что 1,85 Fe2O3 находятся в
шламе в виде Fe(OH)3, тогда с 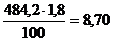 кг Fe2O3 будет связанно
кг Fe2O3 будет связанно 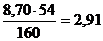 кг H2O.
кг H2O.
Итого п.п.п.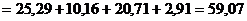 кг. Всего масса шлама
кг. Всего масса шлама 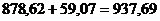 кг, а с учетом потерь 7,79 кг Al2O3 от
гидролиза масса шалма составит
кг, а с учетом потерь 7,79 кг Al2O3 от
гидролиза масса шалма составит 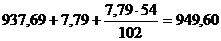 кг.
кг.
Химические потери Na2O несколько ниже, чем то количество,
которое должно быть связанно в составе Na2O·Al2O3·2SiO2·2H2O с 84,29 кг SiO2 т.е. в гидроалюмосиликате натрия часть Na2O
замещена оксидом кальция.
Вследствие неполной отмывки с отвальным шламом теряется 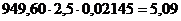 кг Na2O, в том числе 4,69 кг Na2Oк,
где 2,5 это ж:т в отвальном шламе; 2,145 - содержание Na2O в жидкой
фазе отвального шлама, г/л.
кг Na2O, в том числе 4,69 кг Na2Oк,
где 2,5 это ж:т в отвальном шламе; 2,145 - содержание Na2O в жидкой
фазе отвального шлама, г/л.
При 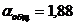 в жидкой фазе отвального шлама потери Al2O3 составят
4,45 кг, или 0,40%. Остальные потери Al2O3 по переделам принимаем по данным практики.
в жидкой фазе отвального шлама потери Al2O3 составят
4,45 кг, или 0,40%. Остальные потери Al2O3 по переделам принимаем по данным практики.
Составляем таблицу потерь (табл. 1).
Таблица 1. Потери Al2O3 и Na2O
|
Статьи потерь
|
Al2O3
|
Na2O,
кг
|
|
% от содержания
в боксите
|
кг
|
|
|
При хранении и
дроблении
|
0,2
|
2,22
|
-
|
|
При размоле
|
0,2
|
2,22
|
0,5
|
|
В красным
шламом:
|
|
|
|
|
в нерастворимой
форме
|
8,2
|
91,21
|
41,7
|
|
в растворимой
форме
|
0,4
|
4,45
|
5,19
|
|
за счет
гидролиза
|
0,7
|
7,79
|
-
|
|
При
декомпозиции
|
0,2
|
2,23
|
3,8
|
|
При выпарке и
выделении соды
|
0,2
|
2,23
|
4
|
|
С известковым
шламом
|
0,2
|
2,22
|
3,8
|
|
При кальцинации
(и с итоговой продукцией)
|
0,7
|
7,79
|
4
|
|
Всего
|
11
|
122,36
|
62,9
|
Расчет состава и количества оборотного раствора
Выход Al2O3 при декомпозиции
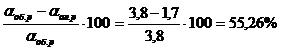 .
.
Следовательно, в составе алюминатного раствора, поступающего на
декомпозицию, содержится Al2O3, кг:
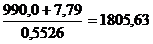 ,
,
где 7,79 - потери Al2O3 на кальцинации, кг;
,0 - содержание Al2O3 в 1 т глинозема, кг.
Если бы отсутствовали механические потери на декомпозиции, то в
маточном растворе осталось Al2O3, кг:
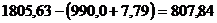 .
.
С учетом потерь Al2O3 на декомпозиции,
выпарке и каустификации соды получим, что в оборотном растворе содержится Al2O3,
кг:
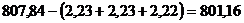 (см. табл. 1).
(см. табл. 1).
При 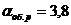 в нем содержится Na2Oк
в нем содержится Na2Oк
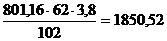 ;
;
2Oу
= 8% от Na2Oобщ, т.е. 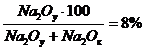 .
.
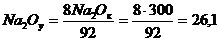 г/л.
г/л.
Объем оборотного раствора, м3: 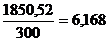 ;
;
Масса оборотного раствора, кг: 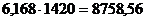 ;
;
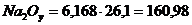 кг;
кг;
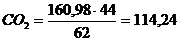 кг;
кг;
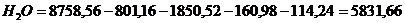 кг.
кг.
Масса сырой пульпы = масса влажного боксита + масса влажной
извести + масса каустической щелочи + масса оборотного раствора.
Масса сырой пульпы, кг: 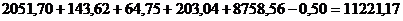 , где 0,50 - потери Na2O при размоле, кг.
, где 0,50 - потери Na2O при размоле, кг.
Разбавление пульпы при выщелачивании с учетом самоиспарения в
сепараторах составляет 1,5%, или 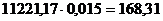 кг.
кг.
На основании полученных данных составляем баланс автоклавного
выщелачивания (табл. 2).
Разбавление и уплотнение пульпы. Промывка красного шлама
Принимаем, что концентрация Na2Oк в жидкой
фазе разбавленной пульпы (или в алюминатном растворе) 150,0 г/л; тогда при 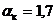 концентрация Al2O3
145,15 г./л.
концентрация Al2O3
145,15 г./л.
При 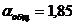 концентрация Na2Oу
в алюминатном растворе будет
концентрация Na2Oу
в алюминатном растворе будет 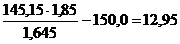 г/л, а концентрация CO2
г/л, а концентрация CO2 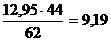 г/л. При плотности раствора 1240 кг/м3 концентрация H2O составит, г/л:
г/л. При плотности раствора 1240 кг/м3 концентрация H2O составит, г/л:
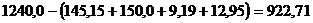 .
.
Состав алюминатного раствора приведен в табл. 3.
Со шламом увлекается алюминатного раствора 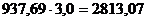 кг,
кг,
где 937,69 - масса красного шлама без учета потерь с ним Al2O3
в составе Al(OH)3, кг;
Таблица 2. Баланс автоклавного выщелачивания
|
Введено, кг
|
Получено, кг
|
|
Боксит:
|
|
|
Автоклавная
пульпа:
|
|
Al2O3
|
|
1107,92
|
Al2O3
|
|
1909,08
|
|
Fe2O3
|
|
484,20
|
Na2Oобщ
|
|
2073,90*
|
|
SiO2
|
|
82,07
|
Fe2O3
|
|
484,20
|
|
TiO2
|
|
45,14
|
SiO2
|
|
84,29
|
|
CaO
|
|
41,03
|
TiO2
|
|
45,14
|
|
CO2
|
|
32,83
|
CaO
|
|
95,92
|
|
прочие
|
|
32,83
|
CO2
|
|
149,02
|
|
п.п.п.
|
|
225,68
|
прочие
|
|
36,16
|
|
H2O
|
|
143,62
|
п.п.п.
|
|
225,68
|
|
Итого
|
|
2195,32
|
H2O
|
|
6286,09
|
|
|
|
Итого
|
|
11389,48
|
|
Известь:
|
|
|
|
|
|
|
CaO
|
|
54,89
|
|
|
|
|
SiO2
|
|
2,22
|
|
|
|
|
CO2
|
|
1,23
|
|
|
|
|
прочие
|
|
3,33
|
|
|
|
|
H2O
|
|
3,08
|
|
|
|
|
Итого
|
|
64,75
|
|
|
|
|
|
|
|
|
|
|
Каустик:
|
|
|
|
|
|
|
Na2Oк
|
|
61,89
|
|
|
|
|
Na2Oу
|
|
1,01
|
|
|
|
|
CO2
|
|
0,72
|
|
|
|
|
H2O
|
|
139,42
|
|
|
|
|
Итого
|
|
203,04
|
|
|
|
|
|
|
|
|
|
|
Оборотный
раствор:
|
|
|
|
|
|
Al2O3
|
|
801,16
|
|
|
|
|
Na2Oк
|
|
1850,52
|
|
|
|
|
Na2Oу
|
|
160,98
|
|
|
|
|
CO2
|
|
114,24
|
|
|
|
|
H2O
|
|
5831,66
|
|
|
|
|
Итого
|
|
8758,56
|
|
|
|
|
Конденсат
|
168,31
|
|
|
|
|
Всего
|
|
11389,98
|
Всего
|
|
11389,98*
|
|
*За вычетом
потерь (0,5 кг Na2O) на размоле.
|
Таблица 3. Состав алюминатного раствора
|
Компоненты
|
Концентрация
|
|
г/л
|
%
|
|
Al2O3
|
145,15
|
11,71
|
|
Na2Oк
|
150,00
|
12,10
|
|
Na2Oу
|
12,95
|
1,04
|
|
CO2
|
9,19
|
0,74
|
|
H2O
|
922,71
|
74,41
|
|
Всего
|
1240,0
|
100,0
|
В этом растворе содержится, кг:
|
Al2O3
|
|
2813,07·0,1171=329,41
|
|
Na2Oк
|
|
2813,07·0,121=340,38
|
|
Na2Oу
|
|
2813,07·0,0104=29,26
|
|
CO2
|
|
2813,07·0,0074=20,82
|
|
H2O
|
|
2813,07·0,7441=2093,20
|
С жидкой фазой отвального шлама теряется 4,45 кг Al2O3
и 5,09 кг Na2Oобщ, в том числе 4,69 кг Na2Oк
и 0,40 кг Na2Oу. Потери за счет гидролиза составляют 7,79
кг Al2O3 и 4,12 кг H2O.
Тогда с 1-й промводой возвращается на разбавление, кг:
|
Al2O3
|
|
329,41-4,45-7,79=317,17
|
|
Na2Oк
|
|
340,38-4,69=335,69
|
|
Na2Oу
|
|
29,26-0,40=28,86
|
|
CO2
|
|
20,82-0,28=20,54
|
|
H2O (по
разности)
|
7129,91
|
|
Итого
|
|
7832,17
|
С промводой на разбавление автоклавной пульпы поступает вода,
количество которой определяется как разность между количествами воды в
алюминатном растворе, красном шламе и автоклавной пульпе.
В алюминатном растворе на 117,10 кг Al2O3
приходится 744,10 кг H2O (см. табл. 3), а на 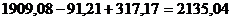 кг Al2O3 приходится H2O
кг Al2O3 приходится H2O
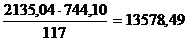 кг,
кг,
где 1909,08 - содержание Al2O3 в автоклавной
пульпе, кг;
,21 - то же, Al2O3 в красном шламе, кг;
,17 - то же, Al2O3 в 1-й промводе, кг.
H2O в промводе содержится:
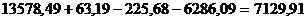 кг,
кг,
,19 - п.п.п. в красном шламе;
,68 - п.п.п. а автоклавной пульпе (см. табл. 2);
,09 - H2O в автоклавной пульпе (см. табл. 2).
На основании расчетов составляем балансы разбавления, уплотнения и
промывки красного шлама (табл. 4-6).
Таблица 4. Баланс разбавления
|
Введено, кг
|
Получено, кг
|
|
Автоклавная
пульпа (см. табл. 2):
|
Разбавленная
пульпа
|
19034,38
|
|
Al2O3
|
|
1909,08
|
Красный шлам:
|
|
|
Na2Oобщ
|
|
2073,90
|
Al2O3
|
|
91,21
|
|
Fe2O3
|
|
484,20
|
Na2O
|
|
41,70
|
|
SiO2
|
|
84,29
|
Fe2O3
|
|
484,20
|
|
TiO2
|
|
45,14
|
TiO2
|
|
45,14
|
|
CaO
|
|
95,92
|
SiO2
|
|
84,29
|
|
CO2
|
|
149,02
|
CaO
|
|
95,92
|
|
прочие
|
|
36,16
|
Прочие
|
|
36,16
|
|
п.п.п.
|
|
225,68
|
П.п.п.
|
|
59,07
|
|
H2O
|
|
6286,09
|
Итого
|
|
937,69
|
|
Итого
|
|
11389,48
|
|
|
|
|
|
|
|
|
|
|
Промвода (см.
с. 7):
|
Алюминатный
раствор (по разности):
|
|
Al2O3
|
|
317,17
|
Al2O3
|
|
2135,04
|
|
Na2Oк
|
|
335,69
|
Na2Oк
|
|
2157,83
|
|
Na2Oу
|
|
28,86
|
Na2Oу
|
|
238,92
|
|
CO2
|
|
20,54
|
CO2
|
|
169,56
|
|
H2O
|
|
7129,91
|
H2O
|
|
13582,61
|
|
Итого
|
|
7832,17
|
Итого
|
|
18283,96
|
|
Всего
|
|
19221,65
|
Всего
|
|
19221,65
|
Таблица 5. Баланс уплотнения
|
Введено, кг
|
Получено, кг
|
|
Разбавленная
пульпа:
|
Красный шлам
|
937,69
|
|
красный шлам
(см. табл. 4)
|
937,69
|
Алюминатный
раствор (в красном шламе):
|
|
алюминатный
раствор:
|
Al2O3
|
|
329,41
|
|
Al2O3
|
|
2135,04
|
Na2Oк
|
|
340,38
|
|
Na2Oк
|
|
2157,83
|
Na2Oу
|
|
29,26
|
|
Na2Oу
|
|
238,92
|
CO2
|
|
20,82
|
|
CO2
|
|
169,56
|
H2O
|
|
2093,20
|
|
H2O
|
|
13582,61
|
Итого
|
|
2813,07
|
|
Итого
|
|
18283,96
|
|
|
|
|
|
|
Алюминатный
раствор на декомпозицию (по разности):
|
|
|
|
Al2O3
|
|
1805,63
|
|
|
|
Na2Oк
|
|
1817,45
|
|
|
|
Na2Oу
|
|
209,66
|
|
|
|
CO2
|
|
148,74
|
|
|
|
H2O
|
|
11489,41
|
|
|
|
Итого
|
|
15470,89
|
|
Всего
|
|
19221,65
|
Всего
|
|
19221,65
|
Таблица 6. Баланс промывки красного шлама
|
Введено, кг
|
Получено, кг
|
|
Красный шлам
(без учета гидролиза) (см. табл. 5)
|
937,69
|
Отвальный шлам
(с учетом гидролиза)
|
949,60
|
|
Алюминатный
раствор (в красном шламе) (см. табл. 5):
|
Жидкая фаза
отвального шлама:
|
|
Al2O3
|
329,41
|
Al2O3
|
|
4,45
|
|
Na2Oк
|
340,38
|
Na2Oк
|
|
4,69
|
|
Na2Oу
|
29,26
|
Na2Oу
|
|
0,40
|
|
CO2
|
20,82
|
CO2
|
|
0,27
|
|
H2O
|
2093,20
|
H2O
|
|
2364,19
|
|
Итого
|
2813,07
|
Итого
|
|
2374,00
|
|
|
|
|
|
|
Свежая вода на
промывку
|
7405,01
|
Промвода на
разбавление (по разности):
|
|
|
Al2O3
|
|
317,17
|
|
|
Na2Oк
|
|
335,69
|
|
|
Na2Oу
|
|
28,86
|
|
|
CO2
|
|
20,54
|
|
|
H2O
|
|
7129,91
|
|
|
Итого
|
|
7832,17
|
|
Всего
|
11155,77
|
Всего
|
|
11155,77
|
|
|
|
|
|
|
Разложение алюминатного раствора (декомпозиция)
Из 1805,63 кг Al2O3, поступающих на
декомпозицию, в оборотном растворе остается 801,16 кг (см. табл. 2). Теряется
на декомпозиции, выпарке и каустификации 6,68 кг Al2O3
(см. табл. 1). Следовательно, с гидроксидом алюминия выпадает 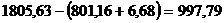 кг Al2O3. Выход при
декомпозиции
кг Al2O3. Выход при
декомпозиции 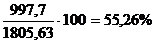 . В маточном растворе остается
. В маточном растворе остается 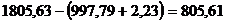 кг Al2O3, а щелочи
- такое же количество, что и в алюминатном растворе за вычетом потерь Na2O
на декомпозиции (см. табл. 1), кг:
кг Al2O3, а щелочи
- такое же количество, что и в алюминатном растворе за вычетом потерь Na2O
на декомпозиции (см. табл. 1), кг:
|
Na2Oк
|
1817,45-3,41=1814,04
|
|
Na2Oу
|
209,66-0,39=209,27
|
|
CO2
|
148,74-0,28=148,46
|
|
H2O
|
11489,41-528,24*=10961,17
|
|
Итого
|
13938,55
|
|
* С 997,79 кг
Al2O3 в Al(OH)3 связанно 528,24 кг H2O.
|
Общая масса гидроксида алюминия 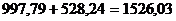 кг Al(OH)3.
кг Al(OH)3.
При затравочном отношении (отношение массы Al2O3
в затравке к массе Al2O3 в алюминатном растворе) 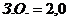 с затравкой вносится 3611,26 кг Al2O3
и 1911,84 кг H2O. Итого 5523,10 кг Al(OH)3. При влажности затравочного
гидроксида 20% с ним поступает
с затравкой вносится 3611,26 кг Al2O3
и 1911,84 кг H2O. Итого 5523,10 кг Al(OH)3. При влажности затравочного
гидроксида 20% с ним поступает 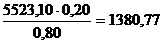 кг маточного раствора.
кг маточного раствора.
В 1380,77 кг маточного раствора содержится, кг:
|
Al2O3
|
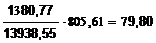
|
|
Na2Oк
|
0,009061·1814,04=179,70
|
|
Na2Oу
|
0,009061·209,27=20,73
|
|
CO2
|
0,009061·148,46=14,71
|
|
H2O
|
0,009061·10961,17=1085,83
|
|
Всего
|
1380,77
|
На основании расчетов составляем баланс декомпозиции (табл.
7).
Таблица 7. Баланс декомпозиции
|
Введено, кг
|
Получено, кг
|
|
Алюминатный
раствор (см. табл. 5):
|
Пульпа
гидроксида алюминия:
|
|
Al2O3
|
|
1805,63
|
Al(OH)3
|
|
7049,13*
|
|
Na2Oк
|
|
1817,45
|
Al2O3
|
|
4609,05*
|
|
Na2Oу
|
|
209,66
|
H2O
|
|
2440,08
|
|
CO2
|
|
148,74
|
|
|
|
|
H2O
|
|
11489,41
|
Маточный
раствор (по разности)
|
15319,32
|
|
Итого
|
|
15470,89
|
Al2O3
|
|
885,41
|
|
|
|
Na2Oк
|
|
1993,74
|
|
Затравка (гидроксид
алюминия)
|
5523,10
|
Na2Oу
|
|
230,00
|
|
CO2
|
|
163,17
|
|
Маточный
раствор (в затравке):
|
H2O
|
|
12047,06
|
|
Al2O3
|
|
79,80
|
Итого
|
|
22368,45
|
|
Na2Oк
|
|
179,70
|
|
|
|
|
Na2Oу
|
|
20,73
|
Потери (см.
табл. 1):
|
|
CO2
|
|
14,71
|
Al2O3
|
|
2,23
|
|
H2O
|
|
1085,83
|
Na2Oк
|
|
3,41
|
|
Итого
|
|
1380,76
|
Na2Oу
|
|
0,39
|
|
|
|
CO2
|
|
0,28
|
|
|
|
Итого
|
|
6,31
|
|
Всего
|
|
22374,76
|
Всего
|
|
22374,76
|
|
* Количество Al2O3
определяется как сумма Al2O3, выпадающей с гидроксидом
алюминия (997,79 кг) и Al2O3, выносимой с затравкой
(3611,26 кг); H2O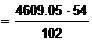 . .
|
Сгущение пульпы гидроксида алюминия
При сгущении пульпы гидроксида алюминия образуются сгущенная
пульпа с ж:т=1,0 и маточный раствор, поступающий на выпарку. Одна часть
сгущенной пульпы фильтруется и гидроксид влажностью 20,0% поступает на
затравку; другая часть - продукционный гидроксид, в котором содержится 1526,03
кг Al(OH)3, также фильтруется до влажности 10%, репульпируется
водой, промывается водой и поступает на кальцинацию (на прокаливание). С
продукционным гидроксидом увлекается 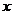 кг маточного раствора:
кг маточного раствора:
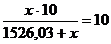 ;
; 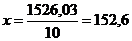 кг.
кг.
В этом маточном растворе содержится, кг:
|
Al2O3
|
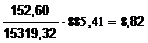
|
|
Na2Oк
|
0,00996·1993,74=19,86
|
|
Na2Oу
|
0,00996·230,00=2,29
|
|
CO2
|
0,00996·163,17=1,63
|
|
H2O
(по разности)
|
120,00
|
По полученным результатам составляем баланс сгущения пульпы
гидроксида алюминия (табл. 8).
Таблица 8. Баланс сгущения пульпы гидроксида алюминия
|
Введено, кг
|
Получено, кг
|
|
Пульпа
гидроксида алюминия (см. табл. 7):
|
Затравочный
гидроксид (см. табл. 7)
|
5523,10
|
|
Al(OH)3
|
7049,13
|
|
|
|
|
Маточный
раствор затравки (см. табл. 7):
|
|
Маточный
раствор (см. табл. 7)
|
15319,32
|
Al2O3
|
79,80
|
|
(Al2O3
|
885,41
|
Na2Oк
|
179,70
|
|
Na2Oк
|
1993,74
|
Na2Oу
|
20,73
|
|
Na2Oу
|
230,00
|
CO2
|
14,71
|
|
CO2
|
163,17
|
H2O
|
1085,83
|
|
H2O
|
12047,00)
|
Итого
|
1380,77
|
|
Итого
|
22368,45
|
|
|
|
|
Продукционный
гидроксид (см. с. 10)
|
1526,03
|
|
|
Маточный
раствор (в продукционном гидроксиде, см. с. 11):
|
|
|
Al2O3
|
8,82
|
|
|
Na2Oк
|
19,86
|
|
|
Na2Oу
|
2,29
|
|
|
CO2
|
1,63
|
|
|
H2O
|
120,00
|
|
|
Итого
|
152,60
|
|
|
Маточный
раствор на выпарку (по разности):
|
|
|
Al2O3
|
796,79
|
|
|
Na2Oк
|
1794,18
|
|
|
Na2Oу
|
|
|
CO2
|
146,83
|
|
|
H2O
|
10841,17
|
|
|
Итого
|
13785,95
|
|
Всего
|
22368,45
|
Всего
|
22368,45
|
Промывка продукционного гидроксида алюминия и кальцинация
Для составления баланса промывки гидроксида алюминия (табл.
9) условно принимаем, что во влаге промытого и отфильтрованного гидроксида
алюминия содержится такое количество щелочи, которое соответствует потере Na2O
на кальцинации и с глиноземом, т.е. 4,0 кг Na2Oобщ, в том
числе 3,6 кг Na2Oк и 0,4 кг Na2Oу.
С этим количеством Na2O связанно 1,6 кг Al2O3
и 0,28 кг CO2.
Таблица 9. Баланс промывки гидроксида алюминия
|
Введено, кг
|
Получено, кг
|
|
Продукционный
гидроксид алюминия
|
1526,03
|
Промытый
гидроксид алюминия
|
1523,60*
|
|
В том числе:
|
В том числе:
|
|
Al2O3
|
997,79
|
Al2O3
|
996,19
|
|
H2O
|
528,24
|
H2O
|
527,41
|
|
Маточный
раствор в продукционном гидроксиде (см. табл. 8):
|
Промвода (в
гидроксиде) (см. табл. 1):
|
|
Al2O3
|
8,82
|
Al2O3
|
1,60
|
|
Na2Oк
|
19,86
|
Na2Oк
|
3,60
|
|
Na2Oу
|
2,29
|
Na2Oу
|
0,40
|
|
CO2
|
1,63
|
CO2
|
0,28
|
|
H2O
|
120,00
|
H2O
|
146,48
|
|
Итого
|
152,60
|
Итого
|
152,36
|
|
Свежая вода
(см. исходные данные)
|
1000,0
|
Промвода на
выпарку (по разности):
|
|
|
Al2O3
|
8,82
|
|
|
Na2Oк
|
16,26
|
|
|
Na2Oу
|
1,89
|
|
|
CO2
|
1,35
|
|
|
H2O
|
974,35
|
|
|
Итого
|
1002,67
|
|
Всего
|
2678,63
|
Всего
|
2678,63
|
|
* Условно
принимаем, что вымывается кг Al(OH)3, в том числе 1,6 кг Al2O3
и 0,83 кг H2O.
|
Таблица 10. Баланс кальцинации гидроксида алюминия
|
Введено, кг
|
Получено, кг
|
|
Промытый гидроксид
алюминия
|
1523,60
|
Глинозем:
|
|
Провода (в
гидроксиде) (см. табл. 9):
|
Al2O3
|
990,0
|
|
Al2O3
|
1,60
|
п.п.п. +
примеси
|
6,5
|
|
Na2Oк
|
3,60
|
Na2O
|
3,5
|
|
Na2Oу
|
0,40
|
Итого
|
1000,0
|
|
CO2
|
0,28
|
|
|
|
H2O
|
146,48
|
Потери (см.
табл. 1):
|
|
Итого
|
152,36
|
Al2O3
|
7,79
|
|
|
Na2Oу
|
0,40
|
|
|
CO2
|
0,28
|
|
|
H2O
|
667,56
|
|
|
Итого
|
675,96
|
|
Всего
|
1675,96
|
Всего
|
1675,96
|
Каустификация соды
Так как растворимость соды с повышением концентрации щелочи
понижается, то при упаривании маточного раствора часть соды
выкристаллизовывается в виде моногидрата, который затем растворяют в воде и
подвергают каустификации.
Количество соды, выпадающей из раствора за каждый цикл
процесса Байера, равно количеству соды, перешедшему в раствор за тот же период.
В оборотном растворе после упаривания маточного раствора должно содержаться (с
учетом потерь на выпарке) (см. табл. 1 и 2), кг:
|
Na2Oк
|
|
1850,52
|
|
Na2Oу
|
|
160,98
|
|
CO2
|
|
114,24
|
|
Al2O3
|
|
801,16
|
|
H2O
|
|
5831,66
|
|
Итого
|
|
8758,56,
|
а в маточном растворе (и в промводе) содержится (см. табл. 8
и 9), кг:
|
Na2Oк
|
|
1794,18+16,26=1810,44
|
|
Na2Oу
|
|
206,98+1,89=208,87
|
|
CO2
|
|
146,83+1,35=148,18
|
|
Al2O3
|
|
796,79+8,82=805,61
|
Следовательно, на выпарке в составе моногидрата соды выделяется 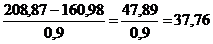 кг Na2Oу. С этим
количеством Na2Oу связанно 37,76 кг CO2 и
15,45 кг H2O:
кг Na2Oу. С этим
количеством Na2Oу связанно 37,76 кг CO2 и
15,45 кг H2O:
Na2CO3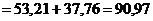 кг;
кг; 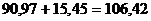 кг Na2CO3·H2O.
кг Na2CO3·H2O.
Общая масса моногидрата соды 106,42 кг; с ним увлекается 25% (от
массы влажного осадка) оборотного раствора 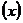 , т.е.
, т.е. 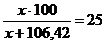 .
.
Отсюда 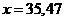 кг, или
кг, или 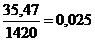 м3; в оборотном растворе содержится (см. состав
оборотного раствора), кг:
м3; в оборотном растворе содержится (см. состав
оборотного раствора), кг:
|
Na2Oк
|
|
0,025·330=7,5
|
|
Na2Oу
|
|
0,025·129,87=3,25
|
|
CO2
|
|
0,025·26,10=0,65
|
|
Al2O3
|
|
0,025·18,52=0,46
|
|
H2O
|
|
0,025·945,50=23,61
|
|
Итого
|
|
35,47
|
В соответствии с реакцией каустификации
Na2CO3 + CaO + H2O
→ CaCO3 + 2NaOH
при условии, что извести берется 125% от стехиометрического (см
исходные данные) количества, ее потребуется: 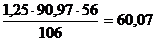 кг СаО или
кг СаО или 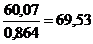 кг технической извести, в которой
содержится 60,07 кг СаО (0,864 - содержание СаОакт в извести, кг);
9,46 кг примесей, в том числе 1,81 СаОсв, 1,39 кг СО2 и
кг технической извести, в которой
содержится 60,07 кг СаО (0,864 - содержание СаОакт в извести, кг);
9,46 кг примесей, в том числе 1,81 СаОсв, 1,39 кг СО2 и 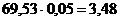 кг H2O (см. состав извести).
кг H2O (см. состав извести).
При степени каустификации 90% прореагирует 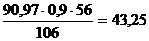 кг СаОакт, а
кг СаОакт, а 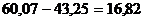 кг СаО перейдет в шлам вместе с 9,46 кг
примесей.
кг СаО перейдет в шлам вместе с 9,46 кг
примесей.
В результате взаимодействия 43,25 кг СаО образуется 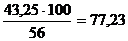 кг CaCO3,
в том числе
кг CaCO3,
в том числе 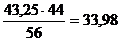 кг СО2 и
кг СО2 и 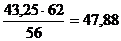 кг Na2Oк.
кг Na2Oк.
Для растворения моногидрата соды берется такое количество воды,
чтобы получить 10%-ный раствор Na2Oобщ, т.е. 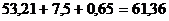 кг. Общее количество H2O
кг. Общее количество H2O 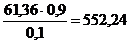 кг.
кг.
Известь гасят промводой известкового шлама из расчета получения
известкового молока с содержанием 300 г./л СаО (ρ=1250 кг/м3).
На 60,07 кг СаО потребуется 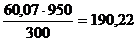 кг H2O.
кг H2O.
Следовательно, в содоизвестковую пульпу поступает вода из
следующих источников, кг:
|
С моногидратом
соды
|
15,45
|
|
С оборотным
раствором
|
23,61
|
|
С известковым
молоком
|
190,22
|
|
Итого
|
229,28
|
Отсюда на растворение соды должно быть подано свежей воды 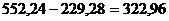 кг. Отвальный известковый шлам содержит,
кг:
кг. Отвальный известковый шлам содержит,
кг:
|
СаО
|
|
43,25+16,82+1,81=61,88
|
|
Na2Oу
|
|
3,80
|
|
Al2O3
|
|
2,22
|
|
Примеси
|
|
9,46 -
(1,81+1,39)=6,26
|
|
СО2
|
|
33,98+1,39=35,37
|
|
П.п.п.
|
|
2,35
|
|
Итого
|
|
108,08
|
С ним увлекается 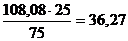 кг щелочного раствора.
кг щелочного раствора.
На основании полученных расчетных данных составляем баланс
каустификации соды (табл. 11).
Таблица 11. Баланс каустификации соды
|
Введено, кг
|
Получено, кг
|
|
Моногидрат соды
(см. с. 14-15):
|
Известковый
шлам (см. с. 15):
|
|
Na2Oу
|
53,21
|
СаО
|
61,88
|
|
СО2
|
37,76
|
Al2O3
|
2,22
|
|
H2O
|
15,45
|
примеси
|
6,26
|
|
Итого
|
106,42
|
СО2
|
35,37
|
|
|
п.п.п.
|
2,35
|
|
Оборотный
раствор с моногидратом соды (см. с. 14):
|
Итого
|
108,08
|
|
Al2O3
|
3,25
|
|
|
|
Na2Oк
|
7,50
|
Отвальная вода
с известковым шламом (см. табл. 1):
|
|
Na2Oу
|
0,65
|
Na2Oк
|
3,78
|
|
CO2
|
0,46
|
Na2Oу
|
0,02
|
|
H2O
|
23,61
|
CO2
|
0,02
|
|
Итого
|
35,47
|
H2O
|
32,45
|
|
|
Итого
|
36,27
|
|
Известковое
молоко (см. с. 14-15):
|
|
|
|
СаО
|
61,88
|
Щелочной
раствор на выпарку (по разности):
|
|
СО2
|
1,39
|
Al2O3
|
1,03
|
|
примеси
|
6,26
|
Na2Oк
|
51,61
|
|
H2O
|
190,22
|
Na2Oу
|
5,95
|
|
Итого
|
259,75
|
CO2
|
4,22
|
|
|
H2O
|
517,44
|
|
Вода на
расторение соды (см. с. 14-15)
|
322,96
|
Итого
|
580,25
|
|
Всего
|
724,60
|
Всего
|
724,60
|
Выпарка и отделение соды
Для составления баланса выпарки (табл. 12) следует учитывать,
что в результате упаривания маточного раствора, промводы гидроксида алюминия и
щелочного раствора с каустификации получается оборотный раствор, который по
составу должен отвечать расчетным данным, и моногидрату соды.
Разница между составом полученного раствора (см. табл. 12) и
составом раствора в табл. 2 0,03 Na2Oк - 0,03 Na2Oу + 0,006 СО2,
что в пределах точности расчета.
Таблица 12. Баланс выпарки
|
Введено, кг
|
Получено, кг
|
|
Маточный
раствор с декомпозиции (см. табл. 8):
|
Моногидрат соды
(см. табл. 11)
|
|
Al2O3
|
796,79
|
Na2Oу
|
53,21
|
|
Na2Oк
|
1794,18
|
CO2
|
37,76
|
|
Na2Oу
|
206,98
|
H2O
|
15,45
|
|
CO2
|
146,83
|
Итого
|
106,42
|
|
H2O
|
10841,17
|
|
|
|
Итого
|
13785,95
|
Оборотный
раствор с моногидратом соды (см. табл. 11):
|
|
|
Al2O3
|
3,25
|
|
Промвода после
промывки гидроксида (см. табл. 9):
|
Na2Oк
|
7,50
|
|
Al2O3
|
8,82
|
Na2Oу
|
0,65
|
|
Na2Oк
|
16,26
|
CO2
|
0,46
|
|
Na2Oу
|
1,89
|
H2O
|
23,61
|
|
CO2
|
1,35
|
Итого
|
35,47
|
|
H2O
|
974,35
|
|
|
|
Итого
|
1002,67
|
Потери (см.
табл. 1):
|
|
|
Al2O3
|
2,23
|
|
Щелочной
раствор с каустификации (см. табл. 11):
|
Na2O
|
4,00
|
|
Al2O3
|
1,03
|
Итого
|
6,23
|
|
Na2Oк
|
51,61
|
|
|
|
Na2Oу
|
5,95
|
Оборотный
раствор на мокрый размол (по разности):
|
|
CO2
|
4,22
|
Al2O3
|
801,16
|
|
H2O
|
517,44
|
Na2Oк
|
1850,52
|
|
Итого
|
580,25
|
Na2Oу
|
160,98
|
|
|
CO2
|
114,24
|
5831,66
|
|
|
Итого
|
8758,56
|
|
|
|
|
|
|
Конденсат пара
|
6462,19
|
|
Всего
|
15368,87
|
Всего
|
15368,87
|
Распределение органических примесей
Баланс органических примесей может быть составлен только
путем практического анализа производственных растворов, продуктов и
полупродуктов цикла Байера. Данные о распределении и процентном содержании
органики представлены в табл. 13.
Таблица 13. Баланс распределения органических веществ
в цикле Байера
|
Статьи баланса
|
Баланс
органических веществ, кт/т глинозема
|
Доля
органических веществ от Σприхода, %
|
|
Приход:
|
|
|
|
Боксит
|
1,110
|
42,55
|
|
Мука
|
1,020
|
39,10
|
|
Синтетический
флоккулянт
|
0,009
|
0,34
|
|
Кристаллический
модификатор роста
|
0
|
0
|
|
Оборотная вода
|
0,470
|
18,01
|
|
Σприхода
|
2,609
|
100,00
|
|
Обедненный
раствор
|
96,46
|
|
|
Расход:
|
|
|
|
Красный шлам в
озеро
|
1,893
|
72,56
|
|
Продукционный
гидроксид алюминия
|
0,609
|
23,34
|
|
Промывная вода
мелкой затравки
|
0
|
0
|
|
Из-за каустификации
раствора
|
0
|
0
|
|
Σрасхода
|
2,502
|
95,90
|
|
Разница (Σприхода - Σрасхода)
|
0,107
|
4,10
|
Список
используемой литературы
1. Лайнер
А.И. Производство глинозема/ А.И. Лайнер, Н.И. Еремин, Ю.А. Лайнер, И.З.
Певзнер. М.: Металлургия, 1978. 344 с.
2. Справочник
металлурга по цветным металлам. Производство глинозема/ А.А. Аграновский, В.И.
Берх, В.А. Кавина и др. Под редакцией Ю.В. Баймакова, Я.Е. Контровича. М.:
Металлургия, 1970. 320 с.
. Самарянова
Л.Б. Технологические расчеты в производстве глинозема/ Л.Б. Самарянова, А.И.
Лайнер. М.: Металлургия, 1981. 280 с.
. Еремин
Н.И. Процессы и аппараты глиноземного производства/ Н.И. Еремин, А.Н Наумчик,
В.Г. Казаков. Под редакцией Н.И. Еремина. М.: Металлургия, 1980. 360 с.
. Dr.
Károly Solimár. Determination
and evolution of organic balances of alumina refineries/ Dr. Károly Solimár, Mrs.
Márta Gimpel-Kazár, Mrs. Elenóra Molnár // Light
Metals, 1996. p. 29-35.