Подавление экспрессии гена EGFP в клетках с использованием конъюгатов олигонуклеотида с пиреном
Список используемых сокращений
- алкил- base, азотистое основание- 2-(N,N-диметиламино)-пиридин-
диметилсульфоксид- смесь дезоксинуклеозидтрифосфатов- дитиотреитол- этил
LNA - locked nucleic acid- метилODN
- метилфосфонатный
олигонуклеотид-
олигодезоксинуклеотид-
peptide nucleic acidODN - фосфоротиоатный
олигонуклеотид
АА - акриламид
мРНК - матричная РНК
о.е. - оптическая единица
ОТ - обратная транскрипция
ПААГ - полиакриламидный гель
пре-мРНК - незрелая матричная РНК (не
подврегшаяся процессингу)
ПЦР - полимеразная цепная реакция
РС - реакционная смесь
ЭДТА - этилендиаминтетрауксусная кислота
Введение
Разработка лекарственных препаратов
направленного действия является приоритетной задачей современных молекулярной
биологии, биоорганической химии и медицины. В настоящее время существует
большое количество работ, отражающих различные подходы для решения этой задачи.
По ряду причин наиболее перспективным является подход, основанный на выборе в
качестве мишени мРНК патогенного белка и использование свойства комплементарности
при взаимодействии нуклеиновых кислот друг с другом. На сегодняшний день работы
ведутся в трёх направлениях:
- антисмысловые олигонуклеотиды;
- рибозимы и ДНКзимы;
- siRNA
и miRNA.
В основе этих методов лежит использование
коротких молекул нуклеиновых кислот (17 - 70 н.) с последовательностью,
частично или полностью комплементарной участку мРНК - мишени. Общие принципы
действия таких агентов объединяют их и в области возникающих проблем, среди
которых наиболее острыми являются доставка в клетку, устойчивость к действию
нуклеаз и эффективность взаимодействия с мРНК-мишенью. Химические модификации
НК-агентов помогают частично или полностью решить многие из этих проблем и
повысить эффективность действия агентов.
Изучение механизмов подавления экспрессии гена,
используя комплиментарные взаимодействия требует использования методов анализа,
позволяющих однозначно определить антисмысловое действие олигонуклеотидов.
Целью настоящей работы является отработка метода
подавления экспрессии гена EGFP
в клетках с использованием конъюгатов олигонуклеотида с пиреном.
1. Модификации антисмысловых
олигонуклеотидов (Литературный обзор)
Разработка лекарственных препаратов, позволяющих
на уровне гена предотвращать развитие заболеваний, вызванных экспрессией патогенных
белков (вирусные, продукты онкогенов) или белков, препятствующих его излечению
(MDR), привела к появлению и развитию антисенс-технологии. Принцип
антисенс-технологии просто: антисмысловые олигорибонуклеотиды вызывают
подавление экспрессии гена-мишени сиквенс-специфическим образом, используя
способность олигонуклеотидов гибридизоваться с мРНК-мишенью посредством
Уотсон-Криковских взаимодействий. Олигонуклеотид, связываясь с РНК-мишенью,
препятствует её дальнейшему процессингу [1-3]. Эксперименты на клеточных
культурах показали, что использование олигодезоксирибонуклеотидов (далее ODN)
длиной 20 - 30 н., комплиментарных участку мРНК значительно снижает уровень
экспрессии кодируемого ею белка. Развитие метода показало ряд причин,
приводящих к снижению эффективности ODN:
короткое время жизни ODN
в сыворотке, низкая эффективность проникновения (транспорта) в клетку и
недостаточная эффективность связывания со структурированными фрагментами РНК.
Развитие органической химии, в частности, химии
нуклеиновых кислот, позволяет искать пути решения возникающих проблем внесением
различных химических модификаций ODN.
Химической модификации могут подвергаться как азотистые основания, так и
сахаро-фосфатный остов, что приводит к повышению его нуклеазоустойчивости ODN
и эффективности его связывания с комплементарной последовательностью. Повышение
эффективности доставки ODN
в клетку пытаются решить введением в его состав по одному из концов различных
групп, облегчающих прохождение через мембрану [1,3].
В основном выделяют два механизма действия
антисмысловых олигонуклеотидов: арест трансляции за счёт связывания
регуляторной области и расщепление РНК в составе РНК-ДНК-гетеродуплекса.
Ведение модификаций может оказывать различное влияние по тому или другому
механизму, что следует учитывать при выборе варианта модификации [1,3,4].
1.1 Механизм действия антисмысловых
олигонуклеотидов
При взаимодействии антисмыслового
олигонуклеотида с мРНК происходят два события: стерическое блокирование и
расщепление мРНК-мишени РНКазой H. Для одних олигонуклеотидов происходят оба
события (РНКаза H-компетентные олигонуклеотиды), для других - только
стерическое блокирование (РНКаза H-независимые). Эти два варианта основаны на
различных клеточных механизмах. Наиболее широкий спектр молекулярных механизмов
затрачивается при использовании второго варианта. Это достигается адресацией
олигонуклеотидов к определённым регуляторным последовательностям, как в
пре-мРНК, так и в мРНК. В случае пре-мРНК адресация ODN к граничной области
между интроном и экзоном нарушает сплайсинг, что приводит либо к его остановке,
либо к образованию мРНК, кодирующей нефункциональный белок (см. рис.1). Другим
перспективным участком связывания ODN в пре-мРНК является 5’-концевой регион.
Взаимодействие ODN с этим регионом приводит к блокированию кепирования [2,4,5].
При взаимодействии ODN с мРНК происходит
нарушение её трансляции, а следовательно и синтеза белка за счёт блокирования
движения рибосомы по мРНК или даже её сборки в зависимости от положения сайта
связывания [4].
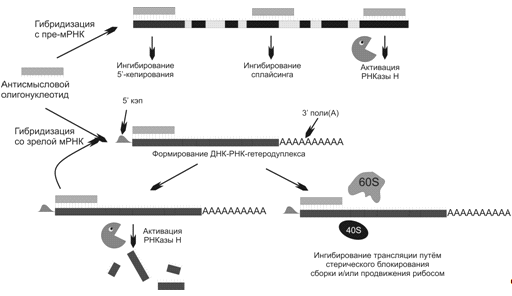
Рис.1. Различные механизмы действия
антисмысловых олигонуклеотидов.
РНКаза H-компетентные
ODN могут быть адресованы к любому участку пре-мРНК и мРНК, так как их действие
основано на активации РНКазы H,
субстратом которой является РНК в составе дуплексов РНК - ДНК. Однако многие
химически модифицированные антисмысловые олигонуклеотиды неспособны включать
этот механизм ввиду высокой стерической специфичности РНКазы H. Это связано с
тем, что большинство модификаций приводит к изменению параметров спирали
дуплекса ODN - РНК, и они перестают быть субстратами для РНКазы H.
Антисмысловые олигонуклеотиды второго поколения
- модифицированные по 2’-положению остатка сахара, не являются субстратами
РНКазы Н, поэтому нужно искать другие расщепляющие агенты (искусственные
РНКазы). Ряд малых молекул (интеркаляторы, поликатионы) способны расщеплять
РНК-мишень. Прикрепление к олигонуклеотидам реакционноспособных групп приводит
к расщеплению желаемых участков РНК-мишени. Такие группы - это комплексы
металлов, амины, олигопептиды и молекулярные конструкциями с группами активного
центра нуклеаз (имидазольное кольцо, COO--, NH2-группы,
гуанидин) [3-7].
1.2 Модификации антисмысловых
олигонуклеотидов
1.2.1 Стратегии развития химических
модификаций олигонуклеотидов
На основе накопленных данных по применению
антисмысловых олигонуклеотидов был сформулирован ряд критериев, которым должен
удовлетворять ODN, чтобы быть
эффективным терапевтическим агентом [1,5,8,9]:
· устойчивость к нуклеазам
· высокая аффинность к мишени
· формирование субстрата РНКазы H
· различные механизмы действия
(влияние альтернативный сплайсинг, арест трансляции)
· нетоксичность и специфичность
· возможность неспецифического
связывания с белками для транспорта
· лёгкость синтеза, патентабельность,
выгода
Нативные ODN не способны полностью удовлетворять
всем перечисленным критериям. Основными ограничениями выступают слабая
нуклеазная устойчивость и недостаточно стабильные комплексы ODN - РНК. Введение
химических модификаций в ODN по всем или отдельно взятым нуклеотидам позволяют
в значительной степени устранить имеющиеся недостатки. Модификации ODN проводят
по фосфатной группе, остатку сахарозы, азотистому основанию или по концевым
фосфатным остаткам. Для повышения нуклеазной устойчивости чаще всего проводят
модификацию по фосфатной группе и остатку дезоксирибозы [5-7,11]. Повышение
эффективности связывания получают за счёт модификации азотистых оснований
[22,23], а также остатка дезоксирибозы [6,16-21]. Для повышения эффективности связывания
с белками и улучшения транспорта производят конъюгацию с лигандами различной
природы [20,24-32]. В ряде случаев присоединённые химические конструкции
выполняют роль катализаторов фосфодиэфирных связей в РНК [3,10].
1.2.2 Модификации фосфатной группы
Расщепление нуклеазами фосфодиэфирных связей в
ДНК происходит через эффективное связывание в активном центре и с
использованием кислотно-основных свойств фосфатной группы. Один из способов
повысить устойчивость связей ODN
к действию нуклеаз - изменить электронную конфигурацию фосфатной группы. Для
этого один из несвязанных атомов кислорода заменяют атомом другого элемента.
Одним из первых в качестве такого элемента использовали серу, в результате чего
были получены фосфоротиоаты (модифицированные антисмысловые олигонуклеотиды
первого поколения; см. рис. 2, II).
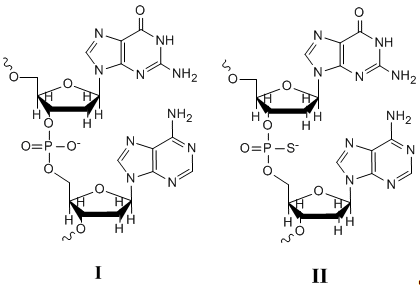
Рис. 2. ДНК (I)
и фосфоротиоат (II).
Фосфоротиоаты проявили высокую устойчивость к
действию нуклеаз, однако такая модификация значительно повысила токсичность ODN
[5,6].
Заменой несвязанного атома кислорода фосфатной
группы метильной группой получают метилфосфонаты (см. рис. 3, III),
проявляющие высокую устойчивость к действию нуклеаз. Модификацию часто проводят
только по концевым нуклеотидам, что приводит к уменьшению токсичности [7].
Если заменить атом кислорода фосфата остатком BH3-,
получаются боранофосфаты. Остаток -BH3- изоэлектронен
атому кислорода в фосфодиэфирных связях, за счёт чего боранофосфаты сохраняют
свой отрицательный заряд, хорошо растворимы в воде и формируют комплексы с
РНК-мишенью. Также этот остаток изоэлектронен и изостеричен метильной группе,
благодаря чему от них следует ожидать свойства, аналогичные свойствам
метилфосфонатов, такие как устойчивость к нуклеазам [11].
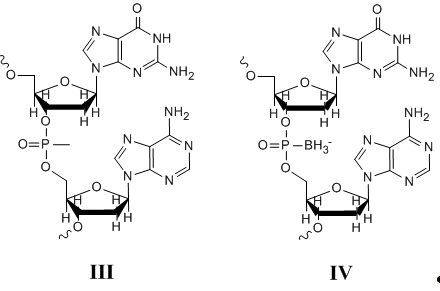
Рис. 3. Метилфосфонат (III)
и боранофосфат(IV).
1.2.3 Модификации остатка сахара
Модификации фосфодиэфирных связей не оказывают
значительного эффекта на стабильность гетеродуплекса ДНК - РНК. Поэтому, кроме
модифицированных олигодезоксинуклеотидов, представляют интерес так называемые
модифицированные антисмысловые олигонуклеотиды второго поколения - это
замещённые по 2’-гидроксильной группе остатка рибозы олигорибонуклеотиды. Такая
модификации также повышает устойчивость к действию нуклеаз. Хотя РНК
значительно менее устойчивы к воздействию окружающей среды по сравнению с ДНК
за счёт наличия 2’-OH-группы,
именно модификации по этой группе позволяют получить стабильные продукты,
проявляющие меньшую токсичность по сравнению с фосфонатами. Также к
модифицированным антисмысловым олигонуклеотидам второго поколения часто относят
и олигонуклеотиды с модифицированным остовом не сахарофосфатной природы,
например, пептидные нуклеиновые кислоты, также проявляющие нуклеазоустойчивость
и образование термодинамически стабильных гибридов с молекулами мРНК-мишени.
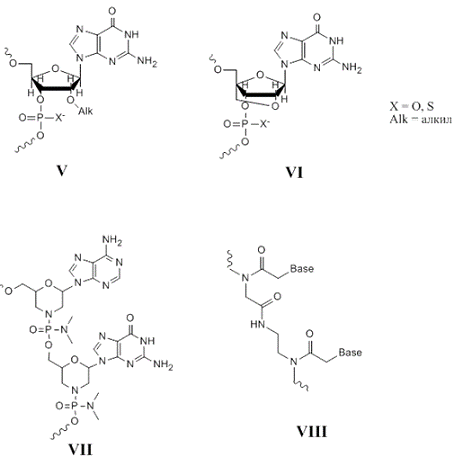
Рис.4. Модификации второго поколения: V
- 2’-O-алкил-РНК, VI
- LNA, VII
- Morpholino, VIII
- PNA.
Анализ данных по использованию ряда 2’-O-алкильных
производных РНК, содержащих от одного до пяти метиленовых звеньев в алкильном
радикале, показал, что с увеличением количества метиленовых звеньев возрастает
устойчивость модифицированного олигонуклеотида к действию нуклеаз (пентокси
> пропокси > метокси > дезокси). Эта зависимость может объясняться
стерической недоступностью нуклеотида при присоединении более объемного
заместителя. Однако, стерические затруднения, вызванные наличием объёмных
заместителей, снижают эффективность образования комплементарных комплексов с
мРНК-мишенью, поэтому наибольшего сродства к мишени достигли при использовании
малых заместителей [5-7]. При сравнении физико-химических параметров
2’-O-метилированных фосфоротиоатов (Me-S-ODN), S-DNA и немодифицированной ДНК
выяснилось, что температура плавления (Tm) гетеродуплексов ДНК - РНК
возрастает в следующем порядке: Me-S-ODN - RNA > normal DNA - RNA > S-ODN
- RNA [6]. Недостаток данной модификации состоит в том, что РНКаза H не может
расщепить мРНК-мишень в РНК - РНК-комплексе. Как следствие этого недостатка,
такие олигонуклеотиды являются менее мощными ингибиторами экспрессии генов по
сравнению с немодифицированными [3,5,12-15].
’-катионные модификации приводят к образованию
цвиттер-ионных олигонуклеотидов. Такие олигонуклеотиды, кроме образования более
стабильных гетеродуплексов, по сравнению с немодифицированными, обладают
большей способностью проникать через биологические мембраны и высокую
стабильность к действию нуклеаз вследствие своего заряда. 2′-O-[2-[2-(N,N-диметиламино)этокси]этил]олигонуклеотиды
(2’-O-DMAEOE,
см. рис 5), благодаря эффекту заряда, образуют гетеродуплексы с РНК-мишенью с
температурой плавления на 2 ºС
больше по сравнению с немодифицированными олигонуклеотидами [16].
Цвиттер-ионные олигонуклеотиды сохраняют РНКаза H-компетентность, если
модификации разбросаны по всей длине олигонуклеотида.

Рис. 5. 2’-O-DMAEOE
Конформационно ограниченные «блокированные»
нуклеиновые кислоты (Locked
Nucleic Acids,
LNA) -
модифицированные нуклеиновые кислоты, имеющие как минимум один мономер с
бициклической фуранозой в качестве сахарного остатка (см. рис. 4, VI).
Они обладают большим сродством к комплементарной последовательности
(температура плавления дуплекса возрастает на 6 °С при модификации одного нуклеотида
[17]), что является и достоинством (эффективное связывание мишени), и
недостатком (образование шпилек). Такое сродство необходимо учитывать при
конструировании LNA [18]. Исследования на мышах показали малотоксичность LNA
[19].
Пептидные нуклеиновые кислоты (PNA)
- аналоги нуклеиновых кислот, в которых сахарофосфатный остов заменён на
псевдопептидный N-(2-аминоэтил)-глициновый полимер. N-конец иминирует 3’-конец
олигонуклеотида, а C-конец - его
5’-конец (см. рис. 3, VII).
Комплексы PNA - РНК более
стабильны, чем комплексы ДНК - ДНК и РНК - РНК. Несмотря на то, что PNA могут
связывать мишень как в антипараллельной (по Уотсону - Крику), так и в
параллельной (по Хугстину) ориентации, более стабильные комплексы образуются
при антипараллельной ориентации PNA. Исследования показали малую токсичность
PNA [20].
Морфолины (см. рис. 3, VIII) - это
реагенты, совмещающие стабильность, резистентность к действию нуклеаз,
эффективность, активность в течение долгого периода, водорастворимость, высокую
специфичность и низкую токсичность. Молекулы имеют нейтральный заряд [12,21].
Производством морфолинов занимается компания Gene Tools, LLC (<#"606668.files/image006.gif">
Рис. 6. Дополнительные водородные связи между С
и G clamp
(X), между T
и ANH2
(XI)
с присоединёнными к остаткам азотистых оснований
катионными и цвиттер-ионными группами (например, спермидиновой, рис. 7) за счёт
своего положительного заряда не только обладают бόльшим
сродством к мишени, но и улучшенной способности к проникновению в клетку и
стабильностью к действию нуклеаз [3].
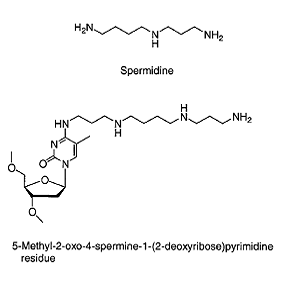
Рис. 7. Спермидиновое производное азотистого
основания как пример катионной модификации.
С концевыми азотистыми основаниями для
визуализации места расположения ODN
в клетке конъюгируют большие флуоресцирующие лиганды, такие как флуоресцеин
[7].
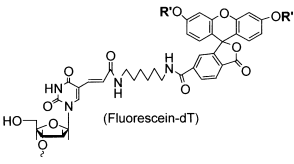 XIV
XIV
Рис.8. Присоединение остатка флюоресцеина к
тимину.
Способность проникать внутрь клетки, минуя
клеточную мембрану, - одно из качеств, которое должно присутствовать у
эффективного антисмыслового олигонуклеотида. Большинство описанных выше
модификаций нуклеотидов в составе ODN
не оказывают значительного влияния на транспорт ODN
через клеточную мембрану. Существует несколько путей проникновения молекул
через плазмалемму, но для ODN
важны два: диффузный, или не рецептор-опосредованный, и
рецептор-опосредованный. Транспорт по первому варианту затрудняется суммарным
отрицательным зарядом ODN
и их гидрофильностью. Использование второго пути ограничено недостаточными
данными о поверхностных белках мембраны клеток, отвечающих за транспорт
нуклеиновых кислот в клетку. Создание конъюгатов ODN
с различными химическими группами способствует повышению эффективности
транспорта по тому или иному пути в зависимости от типа химической группы и
места её присоединения к ODN.
На рисунке 9 представлены варианты линкеров, которые используются при получении
конъюгатов. Лиганды можно присоединять к азотистым основаниям, концевым
фосфатам, фосфодиэфирным (или аналогичным им) связям, а также остаткам сахара.
Некоторые типы химических групп позволяют также визуализировать
компартментализацию путём детекции флуоресценции. модификация
олигонуклеотид антисмысловый реакция
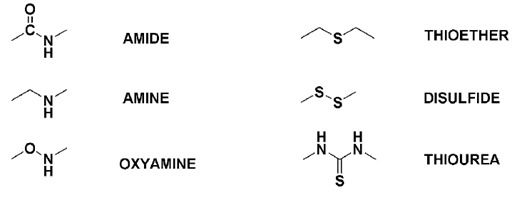
Рис.9. Примеры линкеров для
присоединения лигандов.
Частичная и даже полная
нейтрализация отрицательного заряда ODN не
оказывает существенного эффекта на способность ODN к
самопроизвольному транспорту в клетку. Присоединение различных объёмных
гидрофобных лигандов, в частности, тех, что изображены на рисунке 9, облегчает
транспорт ODN через
мембрану.

Рис.10. Примеры липофильных
лигандов.
Хорошо изучены конъюгаты с
холестеролом [3,4,24,25]. Механизм, улучшающий проникновение в клетку за счёт
присоединения холестерола, ещё не до конца ясен, хотя, предполагается
рецептор-опосредованное включение липопротеидов [25]. Холестероловые конъюгаты
образуют мицеллы, что облегчает их транспорт внутрь клетки. Присоединяют
остаток холестерола обычно по концевым 5’- и 3’-фосфатам, причём
3’-монохолестерилолигонуклеотиды более эффективны по сравнению с
5’-монохолестерилолигонуклеотиды, а самыми действенными являются
5’,3’-бисхолестерилолигонуклеотиды. К примеру, через 6 мин после инъекции в
кровь мыши уровень в тканях 3’-мономодифицированных фосфоротиоатиов был в 4
раза, а 5’-моно- и 3’,5’-бисмодифицированных - в 7 раз выше по сравнению с немодифицированными
фосфоротиоатами [27].
Используют мономеры с 5’- или/и
3’-холестерилзамещённым фосфатом [2,24], олигонуклеотиды с лигандом,
конъюгированным с фосфодиэфирной связью перед 3’-концевым нуклеозидом [25], а
также холестериловые дендримеры с остатком лизина в качестве линкера (см. рис.
11) [23].
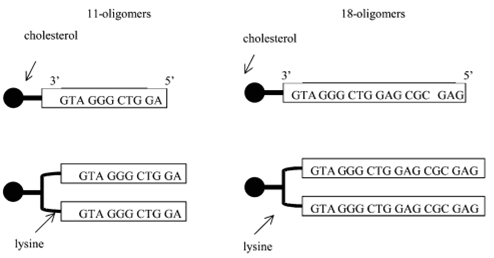
Рис.11. Неразветвлённые и
разветвлённые конъюгаты с холестеролом.
Олигонуклеотиды, конъюгированные с
другими гидрофобными молекулами (адамантан, пирен, эйкозановая кислота и др.),
были синтезированы и сравнены с холестероловыми. Холестероловые конъюгаты
показали оптимальную липофильность, а также хорошую способность к аккумуляции в
печени [24].
Конъюгация с производными пирена,
кроме улучшения способности к транспорту, представляет интерес по причине их
способности к флюоресценции. Бис-пиренильные производные способны образовывать
эксимеры - бимолекулярные комплексы, в которых одна молекула находится в
основном состоянии, другая - в возбуждённым. Такие комплексы очень чувствительны
к пространственному окружению, по уровню флуоресценции можно судить о том,
находится ODN в связанном
с РНК-мишенью состоянии или нет [29-32]:
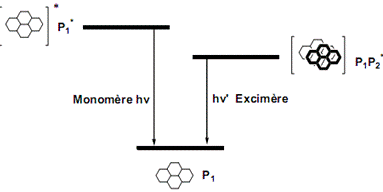
Рис.12. Эксимерная флюоресценция
биспиренильных конъюгатов..
Для улучшения эффективности
транспорта в клетку используются также пептидные конъюганты. К
олигонуклеотидам, в т.ч. PNA, присоединяют пептид,
способный переносить через мембрану большие полярные заряженные молекулы [3].
Так, пептид Antennapedia имеет сайты
связывания ДНК. PNA с присоединённым пептидом Antennapedia не только
эффективно проникает в клетку, но и мигрирует в ядро [20].
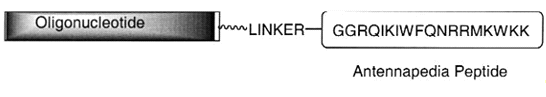
Рис.13. Пептидный конъюгат.
Присоединение к концам молекул
антисмысловых ODN больших
плоских интеркалирующих молекул, таких, как акридин (см. рис. 14), представляет
интерес в качестве увеличителя эффективности расщепления молекулы РНК-мишени.
За счёт интеркаляции локально разрыхляется взаимодействие ODN - РНК. В
следствие увеличения расстояния между ДНК и РНК за счёт размеров молекулы
интеркалятора образуется «выпетливание» молекулы РНК из двойной спирали
гетеродуплекса. Катионы тяжёлых металлов, например Lu3+,
координированные с атомами азота остатка акридина, катализируют гидролиз РНК
без участия РНКазы H, а «выпетливание» как
дестабилизирующая структура ускоряет этот процесс [39].
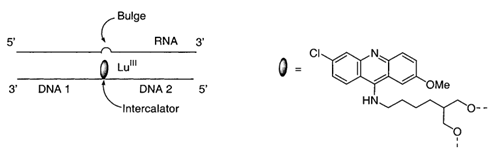
Рис. 14. Конъюгат с интеркалирующим
агентом.
1.3 Физико-химические аспекты
взаимодействия олигонуклеотида и РНК-мишени
Эффективность действия антисмысловых
олигонуклеотидов количественно характеризуется сродством ODN
к мРНК-мишени и эффективной константой расщепления последней.
Сродство ODN
к адресуемой ему РНК (или свободная энергия образования гетеродуплекса)
описывает стабильность гибрида ДНК - РНК. DrG
может быть измерена калориметрически [17], либо рассчитана теоретически
[34,35]. При расчете свободной энергии Гиббса образования гетеродуплекса
используется закон Гесса (свободная энергия Гиббса сложной реакции не зависит
от её пути) и расчеты энергий образования вторичных и третичных структур по
правилу «ближайшего соседа» (nearest
neighbor
rule) с помощью
программы mfold,
разработанной Цукером и соавторами. Реакцию можно представить следующим
образом:
В этой схеме М, O,
H - соответственно
мРНК-мишень, антисмысловой ODN
и гетеродуплекс ODN
- РНК с учётом их вторичной и третичной структуры, Мu,
Ou, Hu
- соответственно мРНК-мишень, антисмысловой ODN
и гетеродуплекс ODN
- РНК без учёта их вторичной и третичной структуры, DunG(M),
DunG(O),
DunG(H)
- свободные энергии Гиббса укладки их во вторичную и третичную структуру, DrG,
DrG(unfolded)
- свободные энергии гибридизации ODN
и мРНК в свёрнутом и полностью денатурированном состоянии соответственно.
DunG(M),
DunG(O),
DunG(H)
и DrG(unfolded)
могут быть теоретически рассчитаны. Тогда свободная энергия гибридизации
находится по закону Гесса:
Константу равновесия процесса ассощиации
гетеродуплекса K1
можно
найти, исходя из рассчитанной свободной энергии Гиббса процесса гибридизации:
Для оценки температуры плавления гетеродуплекса
также пользуются правилом «ближайшего соседа» и рассчитывают её с помощью
соответствующих программ.
Экспериментально можно найти эффективную
константу скорости keff брутто-реакции превращения мРНК M
в условный продукт X (эта
условность не влияет на результат кинетических расчетов, но значительно их
упрощает):
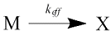
Эффективная константа скорости брутто-реакции
показывает наблюдаемую скорость расщепления мРНК-мишени.
Механизм реакции можно представить следующей
схемой:
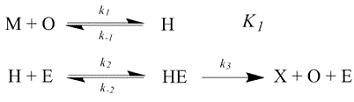
В этой схеме E - фермент РНКаза H,
HE - промежуточный
комплекс её с субстратом H,
K1
- константа ассоциации гетеродуплекса, рассчитываемая по формуле (3).
Для данной кинетической схемы можно составить
систему кинетических уравнений:
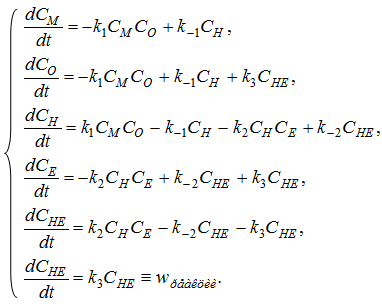
где СA
- концентрация вещества A,
ki
- константа
скорости i-й элементарной
реакции.
Обычно измеряемым параметром является
концентрация мРНК в растворе (исходная CM0
и текущая CM),
поэтому keff считают относительно к матрице:
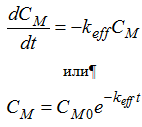
Использовав квазистационарное приближение по
промежуточному продукту HE и упростив выражение для скорости реакции w
с помощью уравнения Михаэлиса - Ментен:
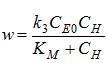
где 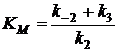 - константа Михаэиса, можно
преобразовать выражение для скорости изменения концентрации гетеродуплекса H:
- константа Михаэиса, можно
преобразовать выражение для скорости изменения концентрации гетеродуплекса H:
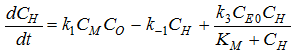
Найдём выражение для эффективной константы
скорости расщепления мРНК-мишени в двух случаях: когда процесс лимитируется
связыванием мРНК антисмысловым ODN и лимитируется каталитическим расщеплением
мРНК-мишени в составе гетеродуплекса.
Случай 1. Лимитирование
гибридизацией.
В этом случае процесс расщепления
идёт значительно быстрей, чем гибридизация. Поэтому можно допустить
предположение об установлении стационарной концентрации гетеродуплекса H, т.е.:
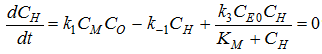
С другой стороны, легко увидеть (6),
что:
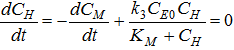
поэтому:
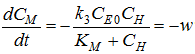
То есть, в данном случае выражение
для скорости расщепления мРНК совпадает по абсолютному значению с выражением
скорости реакции (скорости образования условного продукта Х). Воспользовавшись
этим, преобразуем выражение для скорости изменения концентрации
олигонуклеотида, мы увидим, что его концентрацию можно считать практически
неизменной:
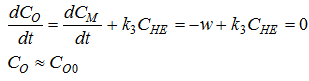
Воспользовавшись выражением (14) и,
как следствие, пренебрегая вкладом члена k-1СH
в
находим скорость расщепления мРНК в новом виде и выражаем keff.
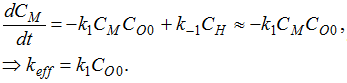
Случай 2. Лимитирование
каталитическим расщеплением субстрата.
В случае, когда расщепление идёт
значительно медленнее образования гетеродуплекса, можно считать, что успевает
установиться равновесие.
Равновесной концентрацией
гетеродуплекса можно пренебречь по сравнению с константой Михаэлиса в выражении
скорости:
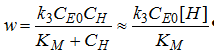
Записав выражение константы
равновесия K1 и уравнения
материального баланса для М и О, получаем достаточно условий для решения
уравнения:
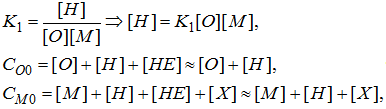
где [ A ] -
равновесная концентрация, СА 0 - исходная
концентрация вещества.
С учётом (17) и (18), получаем
выражения равновесных концентраций H и O:
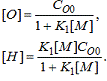
Подставляя (21) в уравнение
Михаэлиса - Ментен (16), получаем модифицированное уравнение скорости реакции:
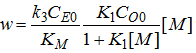
Подставляя выражения (20), (21) и
(22) в (12) и опуская громоздкие промежуточные расчеты, получаем выражение для
скорости каталитического расщепления мРНК:
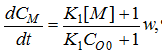
откуда нетрудно найти формулу
эффективной константы скорости брутто-процесса:
На пути создания лекарств на основе
антисмысловых ODN лежит
множество преград: слабая способность к интернализации, неустойчивость к
нуклеазам, токсичность и другие. Химические модификации способны устранить
многие из этих проблем, но лишь частично, и трудно найти компромисс между
достоинствами и недостатками какой-либо модификации. Несмотря на это, многие
препараты на основе ODN прошли испытания. Первое лекарство
на основе ODN - Vitravene, направленное на борьбу с цитомегаловирусной инфекции
у больных СПИДом [2].
2. Материалы и методы
.1 Реактивы, используемые в работе
В работе использовались следующие реактивы:
дезоксинуклеозидтрифосфаты, минеральное масло производства фирмы «Sigma»
(США), N,N'-метиленбисакриламид производства «MP
Biomedicals» (Германия),
акриламид производства «Sigma»
(США) с чистотой не менее 99%, агароза производства «MP
Biomedicals» (Германия) (electrophoresis
grade), трис
производства фирм «MP
Biomedicals» (Германия)
(техн.) и «ICN
Biomedicals» (США) (ultra pure
grade), ЭДТА
производства фирмы «ICN
Biomedicals» (США), борная
кислота производства «MP
Biomedicals» (Германия),
мочевина производства MP
Biomedicals» (Германия), TEMED
производства «Sigma» (США), DTT
производства фирмы «Fluka
Chemica» (Швейцария),
цитавлон, дипиридилдисульфид производства фирм «Fluka
Chemica» (Швейцария) и «Aldrich»
(Германия), трифенилфосфин производства фирм «Fluka
Chemica» (Швейцария) и «Aldrich»
(Германия), 2-(N,N-диметиламино)-пиридин
производства фирм «Fluka
Chemica» (Швейцария) и «Aldrich»
(Германия), триэтиламин производства фирмы «Sigma-Aldrich»
(США), пиренил-1-метиламин, любезно предоставленный …, соли хлорид магния,
хлорид натрия, хлорид кальция, ацетат натрия, перхлорат лития персульфат
аммония квалификации «ОСЧ», остальные реактивы имели квалификацию не ниже «ХЧ».
В работе использовали ферменты: ДНКаза I,
свободная от РНКаз, производства фирмы «Fermentas»
(Литва), обратная транскриптаза (ревертаза) MuML-V и термофильная
Taq-полимераза (Taq-pol), любезно предоставленные Ходыревой С.Н.
Используемые растворители: DMSO (абс.), ацетон
(«ОСЧ»), диэтиловый эфир, этанол (перегн., 96 %), метанол (перегн.).
Все буферы, использованные в работе, были
профильтрованы через нитроцеллюлозные мембраны фирмы «Millipore»
с диаметром пор 0,45 мкм.
2.2 Олигонуклеотиды, использовавшиеся
в работе
В работе были использованы олигонуклеотиды,
указанные в таблице 2:
Таблица 2. Последовательности используемых в
работе олигонуколеотидов.
|
EGFP-A
|
5’-ACTTGTGGCCGTTTACGTCGC-3’
|
|
5’p-EGFP-A
|
5’-pACTTGTGGCCGTTTACGTCGC-3’
|
|
EGFP-B
|
5’-GAACTTCAGGGTCAGCTTGCCG-3’
|
|
5’p-EGFP-B
|
5’-pGAACTTCAGGGTCAGCTTGCCG-3’
|
|
Scr-1
|
5’-CTTTCGGTAGCATAGCATCGTCTA-3’
|
|
5’p-Scr-1
|
5’-pCTTTCGGTAGCATAGCATCGTCTA-3’
|
|
EGFP-1
|
5’-AGAAGAACGGCATCAAGGT-3’
|
|
EGFP-2
|
5’-GGTGCTCAGGTAGTGGTTGT-3'
|
|
EGFP-3
|
5’-GAACGGCATCAAGGTGAA-3'
|
|
EGFP-5
|
5’-ACCACTACCAGCAGAACACC-3'
|
|
EGFP-6
|
5’-GGTCACGAACTCCAGCAG-3’
|
|
Случайный
гексарибонуклеотид («гексапраймер»)
|
Случайная
последовательность рибонуклеотидов
|
Олигонуклеотиды были синтезированы в ИХБФМ СО
РАН и очищены с помощью ВЭЖХ. Чистоту олигонуклеотидов тестировали с помощью
электрофореза в 18% GFFU
в денатурирующих условиях, визуализацию олигонуклеотидов в геле проводили с
помощью краски «Stains-All».
2.3 Буферные растворы,
использовавшиеся в работе
Таблица 3. Состав буферных растворов, использовавшихся
в работе.
|
TBE0,09
М Tris; 0,087 М H3BO3; 2 мМ
ЭДТА, pH = 8,0
|
|
|
Буфер
для ДНКазы I
|
10
мМ Tris•HCl, pH = 7,0;
0,1 мМ CaCl2; 10 мM
MgCl2
|
|
Буфер
для ОТ
|
50
мМ Tris•HCl, pH = 8,3; 3
мM
MgCl2; 75 мМ KCl
|
|
Буфер
для ПЦР
|
10
мМ Tris•HCl, pH = 8,3;
1,5 Мm
MgCl2; 50 мМ KCl; 0,01 % Tween-20
|
|
Буфер
для лизиса
|
5 мМ Tris•HCl,
pH 7.8; 0.1 % Nonidet P-40; 1 мM ЭДТА
|
|
PBS
|
10 мM Na2HPO4;
2 мМ
KH2PO4; 0,15 M KCl; 0,14 M NaCl
|
2.4 Разделение олигонуклеотидов с
помощью ВЭЖХ
ВЭЖХ проводили на хроматографе «Waters
2996», на колонке длиной 150 мм с обращено-фазовым сорбентом Symmetry®
C18
с диаметром микрочастиц 5 мкм, в линейном градиенте ацетонитрила в воде (0 -
30%) в присутствии 50 мМ LiCLO4;
скорость потока 1 мл/мин.
2.5 Электрофорез нуклеиновых кислот
2.5.1 Электрофорез нуклеиновых
кислот в ПААГ в денатурирующих условиях
В экспериментах для разденения реакционных
смесей и анализа изменении подвижности олигонуклеотида при конъюгации с
лигандом использовали электрофорез в 12%, 16% и 18% полиакриламидном геле (GFFU)
при массовом соотношении N,N'-метиленбисакриламид / акриламид 20:1 в
присутствии 8 М мочевины и 1-кратного буфера TBE
при напряжённости электрического поля 15 - 45 В/см. При анализе
олигонуклеотидов и их пиренильных производных гель окрашивали в растворе «Stains-All»
(0,5 г красителя «Stains-All»
в 200 мл 50% водного формамида) в течение 10 минут в темноте. Обесцвечивание
геля проводили в воде на ярком свету.
2.5.2 Электрофорез нуклеиновых
кислот в агарозном геле
Разделение фрагментов ДНК - продуктов ПЦР, проводили
с помощью электрофореза в 1,5 % агарозном геле в присутствии 1-кратного буфера TBE
и 0,002 %(объ.) бромистого этидия при комнатной температуре и напряжённости
электрического поля 5 - 10 В/см. Визуализацию ПЦР продуктов проводили на
трансиллюминаторе за счёт разгорания флюоресценции молекул бромистого этидия
при интеркаляции дцДНК.
2.6 Приготовление цитавлоновых солей
олигонуклеотидов
Для получения цитавлоновых солей олигонуклеотида
готовили раствор, содержащий 1 - 6,5 о.е. олигодезоксирибонуклеотида в 90 мкл
воды. Расчет добавляемого в реакционную смесь 2% водного раствора цитавлона
производили с учётом 2,5-кратного избытка цитавлона по отношению к суммарному
количеству атомов фосфора в составе 5’-концевого фосфата и фосфодиэфирных
связей олигодезоксирибонуклеотида. Раствор цитавлона добавляли порциями, причём
после добавления каждой должен выпадать белый осадок, что свидетельствует о
протекании реакции.
Добавляли сначала 1/3 рассчитанного объёма
раствора цитавлона к раствору олигодезоксинуклеотида, реакционную смесь
перемешивали и центрифугировали при комнатной температуре в течение 5 минут с
круговой частотой, равной 12500 об/мин.
После этого в реакционную смесь вносили 1/4
рассчитанного объёма раствора цитавлона, повторяли перемешивание и центрифугирование.
Аналогичные действия выполняли и при добавлении
1/6 рассчитанного объёма раствора цитавлона.
После последнего центрифугирования супернатант
отбрасывали, а к осадку добавлялои 100 мкл метанола.
Метанол выпаривали на вакуумном испарителе,
полученную соль олигонуклеотида высушивали над P2O5
в вакуумированном эксикаторе.
2.7 Получение биспиренилного
производного олигонуклеотида
Конъюгаты получали согласно модифицированной
методике [30]
Активация. Реакционная
смесь содержала 1 - 4 о.е. (5 - 20 нмоль) цитавлоновой соли
олигодезоксирибонуклеотда и по 10 мг высушенных DMAP,
PPh3
и (PyS)2.
Активацию 5’-концевого фосфата проводили следующим образом: сначала 4 раза
повторяли термостатирование при 50 ºС
в течение 1 - 1,5 мин и последующее интенсивное перемешивание в течение 5 - 10
с, затем инкубировали при 37 ºС
в течение 15 мин.
Конъюгация. К
раствору олигонуклеотида с активированным 5’-концевым фосфатом добавляли
пиренилметиламин (2 мг), высушенный в эксикаторе над P2O5
под вакуумом. Реакционная смесь непрерывно перемешивали в течение 2 часов при
56 ºС.
Выделение продукта. Продукты
осаждали из раствора 1,2 мл диэтилового эфира, растворяли в 50 мкл 3 М водного
раствора перхлората лития, переосаждали 1,2 мл смеси диэтилового эфира и 2%
раствора перхлората лития в ацетоне (1:1) и растворяли в 50 мкл воды. Смесь
продуктов реакции разделяли с помощью обращено-фазовой хроматографии в
градиенте ацетонитрила (см. 2.4). Фракции анализировали методом задержки в геле
с помощью электрофореза в ПААГ в денатурирующих условиях.
2.8 Выделение суммарной РНК из
клеток
2.8.1 Выделение суммарной РНК
методом хлороформ-фенольной экстракции
Суспензию клеток центрифугировали при 4 ºС
с круговой частотой 1000 об/мин в течение 10 мин. Супернатант отбрасывали, к
осадку клеток добавляли 500 мкл буфера PBS,
полученную суспензию центрифугировали при 4 ºС
с круговой частотой 1000 об/мин в течение 10 мин. К осадку добавляли буфер для
лизиса из расчета 200 мкл/106 клеток и инкубировали во льду в
течение 13 мин. Затем суспензию центрифугировали при 4 ºС
с круговой частотой 13000 об/мин в течение 10 мин, осадок отбрасывали. К
полученному раствору добавляли десятую часть его объёма раствора ацетата натрия
с pH = 4,2. Дважды
проводили фенольную экстракцию и один раз - экстракцию смесью фенола и
хлороворма в объёмном отношении 1:1, каждый рас отбрасывая органическую фазу.
РНК из смеси осаждали тройным объёмным избытком этанола в присутствии 0,3 М
ацетата аммония в течение суток при - 20 ºС.
Осаждённую РНК растворяли в 50 мкл воды. Качество выделенной РНК проверяли
отношением оптических плотностей на длинах волн 260 и 280 нм и разделением методом
электрофореза в агарозном геле.
2.8.2 Выделение суммарной РНК с
помощью набора «Gen Elute™ Mammalian Total RNA Kit» фирмы «Sigma»
Выделение РНК проводили согласно методике,
прилагаемой разработчиками к набору.
Суспензию клеток центрифугировали при комнатной
температуре с круговой частотой 800 об/мин в течение 3 мин, к осадку клеток
добавляли 5 мкл меркаптоэтанола и 245 мкл «Lysis
Solution». Суспензию
фильтровали в колонке для фильтрования (Filtration
Column), к фильтрованному
лизату добавляли 250 мкл 70 % водного этанола. Лизат в колонке для фильтрации
при центрифугировании при максимальной круговой частоте в течение 15 с,
маточный раствор отбрасывается. Осадок промывается 500 мкл растворов для
промывки при центрифугировании при максимальной круговой частоте в течение 15
с: сначала Wash
Solution 1, затем Wash
Solution 2; маточный
раствор каждый раз отбрасывается. РНК из колонки элюируется 50 мкл воды.
Качество выделенной РНК проверяли отношением оптических плотностей на длинах
волн 260 и 280 нм (оптимальное отношение 1,8) и разделением методом
электрофореза в агарозном геле. Качество выделенной РНК проверяли отношением
оптических плотностей на длинах волн 260 и 280 нм и разделением методом
электрофореза в агарозном геле.
2.9 Получение кДНК с помощью реакции
обратной транскрипции
Образец РНК подвергали гидролизу ДНКазой I
для очистки от остатков ДНК в присутствии 1-кратного буфера для ДНКазы I.
Реакционную смесь инкубировали при 37 ºС
в течение 1 ч. РНК осаждали из реакционной смеси избытком этанола в присутствии
ацетата натрия. Осадок растворяли воде. Измеряли оптическую плотность очищенной
РНК.
Готовили водный раствор смеси РНК и
«гексапраймера» и инкубировали его в течение 3 мин при 70 ºС,
затем 1,5 мин во льду. После этого к смеси добавляли остальные компоненты
(буфер для ОТ, dNTP, DTT, ревертаза MuMLV). Концентрации компонентов в РС
приведены в табл. 4.
Таблица 4. Состав РС для ОТ.
|
Компонент
|
Концентрация
или количество в РС
|
|
Буфер
для ОТ
|
1
х
|
|
dNTP
|
1
мМ
|
|
DTT
|
5
мМ
|
|
«Гексапраймер»
|
25
мкМ
|
|
MuML-V
|
40
е.а.
|
|
РНК
|
2
мкг
|
РС инкубировали 10 минут при комнатной
температуре, затем 1 час при 42 ºС,
затем, для гидролиза остатков РНК, 10 минут при 70 ºС.
Качество полученной кДНК оценивали методом ПЦР с использованием специфических
пар праймеров.
2.10 Проведение полимеразной цепной
реакции
Амплификацию производили с использованием
кДНК-матрицы и специфической к ней пары праймеров. Готовили реакционную смесь,
содержащую dNTP, прямой и
обратный праймеры, Taq-полимеразу
и ДНК-матрицу в присутствии 1-кратного буфера для ПЦР. Реакционную смесь
помещали в термоциклер «Терцик» фирмы «ДНК-Технология» (Россия) с установленной
программой изменения температуры: 1 цикл: 94ºС,
3 мин, затем 27 циклов: 94 ºС,
45 с, Тотжига (варьируется в разных экспериментах), 30 с, 72ºС,
30 с, и последний цикл: 72 ºС,
2 мин. Визуализацию проводили методом электрофореза в агарозном геле.
2.11 Подбор условий проведения ПЦР с
парами праймеров EGFP-1,2,
EGFP-3,2
и EGFP-5,6
2.11.1 Сравнение эффективности
амплификации при использовании пар праймеров EGFP-1,2,
EGFP-3,2
и EGFP-5,6
Праймеры EGFP-1,2,3,5,6
были подобраны с помощью программы Primer
3.
При сравнении эффективности амплификации при
использовании пар праймеров EGFP-1,2, EGFP-3,2 и EGFP-5,6 в качестве
ДНК-матрицы использовали кДНК BHK,
полученная путём обратной транскрипции суммарной РНК, выделенной из клеток
линии BHK и очищенная
от ДНК ДНКазой I. Как
отрицательный контроль бралась вода. Амплификацию проводили при температуре
отжига 57 ºС и концентрацией
компонентов:
Таблица 5. Состав РС для ПЦР.
|
Компонент
|
Концентрация
или количество в РС
|
|
Буфер
для ПЦР
|
1
х
|
|
dNTP
|
0,3
мМ
|
|
Прямой
праймер
|
5
мкМ
|
|
Обратный
праймер
|
5
мкМ
|
|
Taq-pol
|
0,1
е.а./мкл
|
Визуализацию продуктов ПЦР проводили с помощью
метода электрофореза в агарозном геле. По относительной интенсивности бендов
судили об относительной эффективности амплификации.
2.11.2 Подбор оптимальных
температуры отжига и концентрации хлорида магния
Готовили 24 реакционные смеси, каждой из которых
для удобства и наглядности было присвоено условное название. Названия
реакционных смесей приведены в таблице 6.
Таблица 6. Обозначения реакционных смесей.
|
праймеры
|
матрица
|
СMg2+,
мМ
|
Температура
отжига, ºС
|
|
|
|
55,5
|
57
|
59,5
|
61
|
|
EGFP-3,2
|
H2O
|
5
|
«11»
|
«21»
|
«31»
|
«41»
|
|
кДНК
BHK
|
1,5
|
«12»
|
«22»
|
«32»
|
«42»
|
|
|
3
|
«13»
|
«33»
|
«43»
|
|
|
5
|
«14»
|
«24»
|
«34»
|
«44»
|
|
EGFP-5,6
|
H2O
|
5
|
«15»
|
«25»
|
«35»
|
«45»
|
|
кДНК
BHK
|
1,5
|
«16»
|
«26»
|
«36»
|
«46»
|
|
|
3
|
«17»
|
«27»
|
«37»
|
«47»
|
|
|
5
|
«18»
|
«28»
|
«38»
|
«48»
|
Для каждой реакционной смеси проводили ПЦР.
Визуализацию продуктов ПЦР проводили с помощью метода электрофореза в агарозном
геле. По относительной интенсивности бендов судили об относительной
эффективности амплификации.
2.11.3 Подбор оптимальных
концентраций дезоксинуклеозидтрифосфатов и праймеров
Готовили 10 реакционных смесей с разными
условиями проведения реакции. Для удобства и наглядности каждой реакционной
смеси присваивали условное название. Контрольный эксперимент (реакционная смесь
«0») проводили при максимальной концентрации праймеров (0,5 мкМ) и dNTP
(1 мМ) в отсутствие ДНК-матрицы. Названия реакционных смесей, содержащих
матрицу приведены в таблице 7.
Таблица 7. Обозначения реакционных смесей.
|
СdNTP,
мкМ
Спраймеров, мкМ
|
50
|
250
|
1000
|
|
0,15
|
«1»
|
«2»
|
«3»
|
|
0,3
|
«4»
|
«5»
|
«6»
|
|
0,5
|
«7»
|
«8»
|
«9»
|
Для каждой реакционной смеси проводили ПЦР.
Визуализацию продуктов ПЦР проводили с помощью метода электрофореза в агарозном
геле. По относительной интенсивности бендов судили об относительной
эффективности амплификации.
3. Результаты и обсуждения
Метод подавления экспрессии гена, используя
антисмысловые олигонуклеотиды, предложен более 15 лет назад [], однако работы
над его оптимизацией остаются актуальными и в настоящее время. Антисмысловые
олигонуклеотиды являются потенциальными терапевтическими агентами, подавляющими
экспрессию патогенных белков. За последние 15 лет развитие биоорганической
химии позволило получить ряд химически модифицированных олигонуклеотидов,
обладающих улучшенными биологическими свойствами по сравнению с
немодифицированными антисмысловыми ODN:
большей устойчивостью к действию нуклеаз, образованием стабильных
гетеродуплексов, способностью проникать в клетку.
Эксперимент по «выключению» гена антисмысловыми
олигонуклеотидами включает в себя несколько этапов:
1. Выбор и проведение необходимых для
эффективного антисмыслового действия химических модификаций олигонуклеотида.
2. Оптимизация условий проведения ОТ ПЦР
реального как метода, количественно измеряющего количество молекул РНК,
содержащих ген-мишень.
. Доставка антисмыловых олигонуклеотидов
в клетки.
. Количественная характеристика антисмыслового
действия: сравнение количества мРНК-мишени в клетках, обработанных
модифицированным и немодифицированным олигонуклеотидами, и в интактных клетках.
Если количество мРНК-мишени в клетках,
обработанных антисмысловыми олигонуклеотидами, мало по сравнению с количеством
мРНК-мишени в интактных клетках, то антисмысловой олигонуклеотид эффективно
подавляет экспрессию гена-мишени. Адекватно подобранный ряд химических
модификаций должен усиливать антисмысловой эффект.
Антисмыловой агент, эффективно ингибирующий
продукцию патогенного белка, должен пройти ещё ряд доклинических и клинических
испытаний, прежде чем стать продажным медикаментом.
В настоящей работе в качестве модели
исследования был выбран ген EGFP, продуцирующий флюоресцирующий белок.
Преимуществом выбранной модели является возможность измерения экспрессии
гена-мишени двумя методами: ОТ ПЦР и измерение интенсивности флюоресценции,
производимой белком, кодируемым геном-мишенью.
Был проведён синтез 5’-монопиренильных
конъюгатов двух антисмыловых ODN,
адресованных к мРНК-мишени (EGFP-A,
EGFP-B),
и одного «смешанного» (scrambled)
олигонуклеотида (Scr-1),
содержащего разбросанные и перемешанные участки антисмысловой
последовательности. Также были оптимизированы условия проведения ОТ ПЦР как
метода диагностики наличия генов EGFP в образцах РНК, выделенных из клеток.
3.1 Синтез пиренильных производных
олигодезоксинуклеотидов
Синтез проводили по методике, описанной в п.
2.7. Процедуру конъюгации можно разделить на 2 этапа: активация 5’-концевого
фосфата (рис. 15, а,б) и присоединение производного пирена (рис 15, в).
Механизм реакции можно представить следующей схемой:
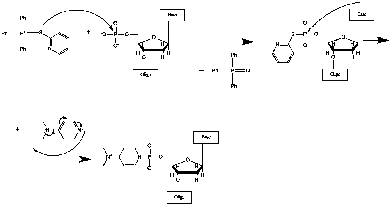
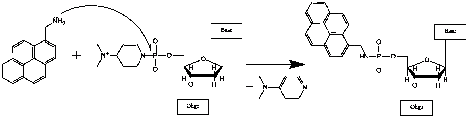
Рис. 15. Механизм присоединения
пиренил-1-метиламина к 5’-концевому фосфату олигонуклеотида.
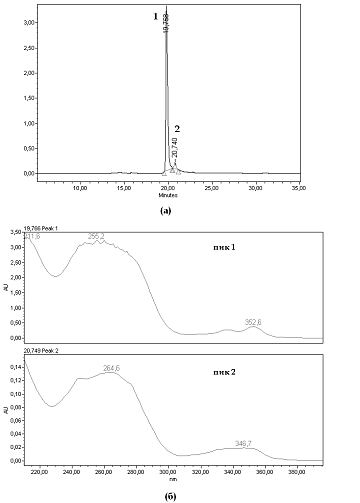
Рис. 16. а - хроматограмма монопиренильного
производного ODN
EGFP-B;
б - УФ спектры поглощения продуктов, содержащихся в пиках (1) и (2).
Были получены и охарактеризованы методом
задержки в геле и УФ-спектрометрией конъюгаты ODN
и пиренил-1-метиламина. Задержка в геле, УФ спектры и спектры флюоресценции
свидетельствуют о получении монопиренильных производных.
Анализ продуктов методом электрофореза в ПААГ в
денатурирующих условиях показал зелёное флюоресцентное свечение бенда в геле,
характерное для пиреновых конъюгатов, и небольшую задержку конъюгатов в геле по
сравнению с исходными олигонуклеотидами, что характерно для монопроизводных.
3.2 Сравнение эффективности
выделения РНК из клеток методом хлороформ-фенольной экстракции и с помощью
набора Gen Elute™ Mammalian Total RNA Kit» фирмы «Sigma»
Были получены суспензии клеток линии R1198,
содержащие по 3,6•106 клеток. Из каждой суспензии клеток выделяли
«суммарная» РНК обоими методами и сравнивали эффективность выделения.
Критериями эффективности выделения служили поглощение на длине волны 260 нм
(количественная характеристика) и отношение оптических плотностей на длинах
волн 260 нм и 280 нм (для чистой РНК оно должно быть близко к 1,8).
В обоих случаях на агарозном геле после
проведения в нём электрофореза была получена качественная картина, характерная
для «суммарной» РНК:
Спектрофотометрические данные показали более
эффективное выделение РНК набором Gen Elute™ Mammalian Total RNA Kit» фирмы
«Sigma» по сравнению с классическим методом хлороформ-фенольной экстракции:
Таблица 8. Сравнение эффективности методов
выделения РНК из клеток.
|
Метод
выделения
|
A260, о.е./мл
|
A260/A280
|
|
Хлороформ-фенольная
экстракция
|
2,2
|
1,909
|
|
Использование
набора для выделения РНК
|
9,9
|
1,800
|
Таким образом, выделение методом
хлороформ-фенольной экстракции проигрывает набору для выделения РНК фирмы «Sigma»
в плане более значительного количества примесей ДНК, в 4,5 раза меньшего
количества выделенной РНК и больших затрат времени на процесс выделения.
3.3 Постановка метода ПЦР для
определения мРНК гена EGFP
Была проведена ПЦР с использованием пар
праймеров EGFP-1,2, EGFP-3,2 и EGFP-5,6, адресованных к гену EGFP.
Положительным контролем (при использовании которого достоверно идёт амплификация)
являлась пара праймеров AE-7,6,
адресованных к гену AML-ETO.
В качестве ДНК-матрицы использовали кДНК, полученную из клеток линии R1198
и содержащую ампликоны обоих генов. На рис. 20 приведена фотография
прокрашенного бромистым этидием агарозного геля после разделеня в нём продуктов
ПЦР.
EGFP-1,2
(дорожки 1,2), EGFP-3,2
(дорожки 3,4),
EGFP-5,6
(дорожки 5,6) и AE-7,6
(дорожки 7,8).
В качестве матрицы в 2,4,6,8 использовалась кДНК
клеток линии R1198,
,3,5,7 - контрольные эксперименты (без
добавлен7ия матрицы в РС).
При использовании ODN
EGDP-1,2 в качестве
пары праймеров амплификация практически не идёт, имеет место лишь такой
артефакт, как «димеры праймеров» (см. рис…). Пары праймеров EGFP-3,2 и EGFP-5,6
сравнимы по эффективности амплификации.
Затем для каждой пары праймеров EGFP-3,2 и
EGFP-5,6 подбирали оптимальную температуру отжига и концентрацию хлорида магния
в реакционной смеси. Обозначения реакционных смесей в соответствии с условиями
проведения ПЦР приведены в п. 2.11.2 настоящей работы. На рис. 21 приведена
фотография прокрашенного бромистым этидием агарозного геля после разделения в
нём продуктов ПЦР.
Наиболее интенсивно флюоресцируют бенды на
дорожках 44 для EGFP-3,2
и на дорожках 36,37 для пары праймеров EGFP-5,6,
что соответствует оптимальным условиям проведения ПЦР с использованием данных
пар праймеров.
Таблица 9. Подбор оптимальной температуры отжига
и концентрации катионов мангия в РС.
|
Пара
праймеров
|
Дорожка
|
CMg2+, мМ
|
Тотжига,
ºС
|
|
EGFP-3,2
|
44
|
5
|
61
|
|
EGFP-5,6
|
37
|
1,5
|
59,5
|
|
38
|
3
|
|
Наиболее интенсивно флюоресцирующий бенд для
пары праймеров EGFP-3,2
соответствует максимальной концентрации катионов магния в реакционной смеси и,
как следствие, большому количеству неспецифических продуктов («шмер», см.
рис…). В то же время, сравнимые с этим бендом по интенсивности флюоресценции
бенды дорожек 36 и 37, соответсвтующие продуктам ПЦР с использованием пары
праймеров EGFP-5,6,
характеризуются меньшим количеством неспецифических продуктов. Условия реакции,
в которых получен продукт ПЦР, обнаруженный на дорожке 36, являются наиболее
подходящими для выявления EGFP
в образцах. Эту пару праймеров в дальнейшем мы и использовали для дальнейшей
оптимизации условий проведения ПЦР.
Далее были подобраны оптимальные концертрации
праймеров EGFP-5 и EGFP-6
и дезоксинуклеозидтрифосфатов в указанных выше условиях: температура отжига
59,5 ºС,
а концентрация катионов магния в реакционной смеси 1,5 мМ. Обозначения
реакционных смесей в соответствии с условиями проведения ПЦР приведены в п.
2.11.3 настоящей работы. На рис. 22 приведена фотография прокрашенного
бромистым этидием агарозного геля после проведения в нём разделения продуктов
ПЦР.
При максимальной концентрации (1 мМ) dNTP
наблюдалось большое количество образующихся неспецифических продуктов при почти
полном отсутствии основного. Интерес представляют условия «8» (наиболее
интенсивно флюоресцирующий бенд) и «4» (второй по интенсивности), т.е.:
Таблица 9. Подбор оптимальной концентрации
праймеров и dNTP в РС.
|
Дорожка
|
Спраймера,
мкМ
|
СdNTP,
мкМ
|
|
«8»
|
0,5
|
250
|
|
«4»
|
0,3
|
50
|
Условия «4» более предпочтительны ввиду меньшего
количества неспецифических продуктов, а также меньшего расхода реагентов.
Таким образом, оптимальные условия для
обнаружения EGFP методом ОТ-ПЦР можно просуммировать в табл. 9.
Таблица 9. Оптимальные условия проведения ПЦР.
|
Прямой
праймер
|
EGFP-5
|
|
Обратный
праймер
|
EGFP-6
|
|
Концентрация
праймеров в РС
|
0,3
мкМ
|
|
Концентрация
dNTP
в
РС
|
50
мкМ
|
|
Концентрация
Mg2+
в
РС
|
1,5
мМ
|
|
Температура
отжига
|
59,5
ºС
|
Выводы
2. Проведено сравнение двух методов
выделения суммарной РНК из клеток. Показано, что выделение суммарной РНК из
клеток с использованием фирменного набора осуществляется проще, быстрее и с
большим выходом, однако содержит примеси ДНК и требует стадии обработки
ДНКазой. Выделение РНК с использованием экстракции смесью фенол-хлороформ
больше времени, затрат турда и имеет меньший выход, однако приводит к получению
чистого продукта.
. Для оценки биологического действия
антисмысловых олиогуклеотидов выбран метод основанный на ПЦР. Был проведен
выбор праймеров к кДНК гена EGFP
исходя из оценки термодинамических параметров возможных структур, формируемых
ими в растворе и условий взаимодействия с мишенью с последующим тестированием
их в условиях эксперимента. Для наиболее эффективной пары праймеров проведена
оптимизация условий ПЦР и определены оптимальные параметры.
Список литературы
1. A.D. Branch (1996). A
Hitchhiker’s Guide to Antisense and Nonantisense Biochemical Pathways. Hepatology,
24: 1517-1529.
2. U.
Galderisi, A. Cascino, A. Giordano (1999). Antisense
Oligonucleotides as Therapeutic Agents. J. Cell. Physiol, 181: 251-257
. M. Manoharan (2002).
Oligonucleotide Conjugates as Potential Antisense Drugs with Improved Uptake,
Biodistribution, Targeted Delivery, and Mechanism of Action. Antisense &
nucleic acid drug development,
12:103-128
. I.M. Lagoja, P.
Hedrdewijn (2007). Use of RNA in drug design. Expert Opin. Drug Discov.
2(6): 889 - 903.
. C.M. Roth, M.L.
Yarmush (1999). Nuclear acid biotechnology. Annu. Rev. Biomed. Eng.
01:265-297
. Byong Hoon Yoo, Elena
Bochkareva, Alexey Bochkarev, Tung-Chung Mou, Donald M. Gray (2004). 2’-O-methyl-modified
phosphorothioate antisense oligonucleotides have reduced non-specific effects
in vitro. Nucleic Acids Research, 32(6): 2008 - 2016.
. Chrissy E. Prater,
Paul S. Miller (2004). 3′-Methylphosphonate-Modified Oligo-2′-O-methylribonucleotides
and Their Tat Peptide Conjugates: Uptake and Stability in Mouse Fibroblasts in
Culture. Bioconjugate Chem., 15: 498−507.
8. P.A. Morcos (2003).
Morpholino oligos can block translation or nuclear processing of mRNA. Gene
Tools, LLC.
. F. E. Cotter (1997). Antisense
therapy for lymphomas. Hematological Oncology, 15: 3-11
. C.A. Stein, R.
Narayanan (1996). Antisense oligodeoxynucleotides: Internalization,
compartmentalization and non-sequence specificity. Perspectives in Drug
Discovery and Design, 4: 41 - 50.
. B.R. Shaw, J. Madison,
A. Sood, B.E. Spielvogel (1993). Oligonucleoside Boranophosphate (Borane
Phosphonate). Methods in Molecular Biology, 20: 225 - 243.
. J. Summerton (1999).
Morpholino antisense oligomers: the case for an RNase H-independent structural
type. Biochimica et Biophysica Acta,
1489:
141
- 158.
. H. Inoue, M. Shimizu,
T. Furukawa, T. Tamura, M. Matsui, E. Ohtsuka (1999). Site-Specific RNA
Cleavage Using Terpyridine·Cu(II)-Linked 2’-O-Methyloligonucleotides. Nucleosides
& Nucleotides, 18(6&7): 1503 - 1505.
. V.Vlassov, T.
Abramova, T. Godovikova, R. Giege, V. Silnikov. Sequence-Specific Cleavage of
Yeast tRNAPhe with Oligonucleotides Conjugated to a Diimidazole
Construct (1997). Antisense & Nucleic Acid Drug, 7: 39 - 42.
. M.A. Reynolds, T.A.
Beck, P.B. Say, D.A. Schwartz, B.P. Dwyer, W.J. Daily, M.D. Metzler, R.E. Klem,
L.J. Arnold Jr (1996). Antisense oligonucleotides containing an internal,
non-nucleotide-baced linker promote site-specific cleavage of RNA. Nucleic
Acids Research, 24(4): 760 - 765.
. M. Prhavc, T.P.
Prakash, G. Minasov, P. Dan Cook, M. Egli, M. Manoharan (2002). 2′-O-[2-[2-(N,N-Dimethylamino)ethoxy]ethyl]
Modified Oligonucleotides: Symbiosis of Charge Interaction Factors and
Stereoelectronic Effects. Organic Letters, Vol. 5, No. 12, pp. 2017 -
2020.
. Kaur H, Arora A,
Wengel J, Maiti S. (2008). Thermodynamic, counterion and hydration effects for
the incorporation of locked nucleic acid (LNA) nucleotides in duplex. Nucleic
Acids Symp Ser (Oxf), 52: 425 - 426.
. B. Vester, J. Wengel
(2004). LNA (Locked Nucleic Acid): High-Affinity Targeting of Complementary RNA
and DNA. Biochemistry, 43(42): 13233 - 13240.
19. J. Kurrek, E. Wyszko, C.
Gillen, V.A. Erdmann (2002). Design Of Antisense
Nucleotides Stablized By Locked Nucleic Acids. Nucl. Acids Res., 30(9):
1911 - 1918.
20. Lidia C
Boffa, Elisabetta M.Carpaneto, Benedetta Granelli, Maria R. Mariani (2000). PNA
(peptide nucleic acid) anti-gene/antisense can access intact viable cells and
downregulate target genes. Gene Ther Mol Biol, 5: 47-53.
. Bianca L. Gebski,
Chrisopher J. Mann, Susan Fletcher and Stephen D. Wilton (2003). Morpholino
antisense oligonucleotide induced dystrophin exon 23 skipping in mdx mouse
muscle. Human Molecular Genetics, 12(15):
1801-1811
. W. Michael Flanagan,
John J. Wolf, Peter Olson, Debbie Grant, Kuei-Ying Lin, Richard W. Wagner, Mark
D. Matteucci (1999). A cytosine analog that confers enhanced potency to
antisense oligonucleotides. Proc. Natl. Acad. Sci. USA, 96: 3513-3518.
23. K.-H. Hung, A. Marx
(2005). Nucleotide analogues as probes for
DNA polymerases. Cellular and Molecular Life Sciences, 62: 2080 - 2091.
24. P. Chaltin, A. Margineanu,
D. Marchand, A. Van Aerschot, J. Rozenski, F. De Schryver, A. Herrmann, K.
Müllen, R. Juliano, M. H. Fisher, Hyunmin Kang,
S. De Feyter, P. Herdewijn (2005). Delivery of
Antisense Oligonucleotides Using Cholesterol-Modified Sense Dendrimers and
Cationic Lipids. Bioconjugate Chem , 16: 827−836.
. Martin K.
Bijsterbosch, Muthiah Manoharan, Rick Dorland, Richard Van Veghel, Erik A. L.
Biessen, Theo J. C. Van Berkel (2002). bis-Cholesteryl-Conjugated
Phosphorothioate Oligodeoxynucleotides Are Highly Selectively Taken Up by the
Liver. The Journal Of Pharmacology And Experimental Therapeutics, 302(2):
619 - 626.
26. C. Beltinger, H.Un
Saragovi, R.M. Smith, L. LeSauteur, N. Shah, L. DeDionisio, L. Christensen, A.
Raible, L. Jarett, A.M. Gewirtz (1995). Binding, Uptake, and Intracellular
Trafficking of Phosphorothioate-modified Oligodeoxynucleotides. J. Clin. Invest.,
95: 1814 - 1823.
. M. Dizik, P. Nero, M.
Metzler, D. Bubonovich, S. Sher-Rill, T. Beck, L. Borozdina, R.Hogrefe, M.M
Vaghefi, M. Woodle, (1995). Pharmacokinetics of cholesterol-conjugated
oligonucleotide phosphorothioates in mice. Proc. Int. Symp. Controlled
Release Bioact. Mater. 22:
578-579.
28. Robert L. Letsinger,
Guangrong Zhang, Daisy K. Sun, Tohru Ikeuchi, And Prem S. Sarin (1989).
Cholesteryl-conjugated oligonucleotides: Synthesis, properties, and activity as
inhibitors of replication of human immunodeficiency virus in cell culture. Proc.
Nati. Acad. Sci. USA, 86: 6553-6556.
29. P. Clivio, A. Boutorine
(2004). Synthèse et études de sondes oligonucléotidiques
dont le signal fluorescent est modifié au cours de l'hybridation.
30. D. S. Novopashina, O. S.
Totskaya, S. A. Kholodar’, M. I. Meshchaninova, A. G. Ven’yaminova (2008). Oligo(2'-O-methylribonucleotides)
and Their Derivatives: III. 5'-Mono- and 5'-Bispyrenyl Derivatives of
Oligo(2'-O-methylribonucleotides) and Their 3'-Modified Analogues: Synthesis
and Properties. Russian Journal Of Bioorganic Chemistry, 34(5): 602 -
612.
. Kostenko, E.,
Dobrikov, M., Komarova, N., Pyshniy, D., Vlassov, V., Zenkova, M.(2001).
5'-Bis-Pyrenylated Oligonucleotides Display Enhanced Excimer Fluorescence Upon
Hybridization With Dna And Rna. Nucleosides, Nucleotides and Nucleic Acids,
20(10): 1859 - 1870
. E. Kostenko, M.
Dobrikov, D. Pyshnyi, V. Petyuk, N. Komarova, V. Vlassov, M. Zenkova (2001).
5’-bis-pyrenylated oligonucleotides displaying eximer fluorescence provide
sensetive probes of RNA sequence and structure. Nucleic Acids Res., 29(17):
3611 - 3620.
. Akinori Kuzuya and
Makoto Komiyama (2000). Non-covalent ternary systems (DNA-acridine hybrid/DNA/
lanthanide(III) for efficient and site-selective RNA scission. Chem. Commun.
(Cambridge), 20: 2019-2020.
. S. Patrick Walton,
Gregory N. Stephanopoulos, Martin L. Yarmush, and Charles M. Roth (2002).
Thermodynamic and Kinetic Characterization of Antisense Oligodeoxynucleotide
Binding to a Structured mRNA. Biophysical Journal,
82:
366-377
. S.P. Walton, G.N.
Stephanopoulos, M.L. Yarmush, C.M. Roth (1999). Prediction of Antisense
Oligonucleotide Binding Affinity to a Structured RNA Target. Biotechnol
Bioeng 65: 1-9, 1999.