Горение топлива
Задание
Выполнить расчет горения топлива (смеси газов). Топливо - смесь
коксового и доменного газов с теплотой сгорания 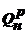 =9 МДж/м3. Коэффициент избытка воздуха a=1,05.
=9 МДж/м3. Коэффициент избытка воздуха a=1,05.
Определить теоретически необходимое и действительное количество
воздуха, количество продуктов сгорания, их процентный состав и
калориметрическую температуру.
топливо горение доменный калориметрический
Расчёт
Итак, имеем топливо с низшей теплотой сгорания 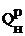 =9000 кДж/м3 и a=1,05. Топливо представляет собой смесь
доменного и коксового газа, поэтому зададимся химическим составом этих газов
[2]:
=9000 кДж/м3 и a=1,05. Топливо представляет собой смесь
доменного и коксового газа, поэтому зададимся химическим составом этих газов
[2]:
Характеристика видов топлива
|
Газ
|
Состав топлива
в объёмных процентах (на сухую массу).
|
|
H2С
|
COС
|
CH4С
|
C2H4С
|
CO2С
|
N2С
|
|
Доменный
|
3,3
|
27,4
|
0,9
|
-
|
10
|
58,4
|
|
Коксовый
|
50,8
|
5,4
|
26,5
|
1,7
|
2,3
|
13,3
|
Принимаем влажность газов fк=fд=25 г./м3 [2]
Определяем содержание влаги во влажных газах [1]:
- в доменном

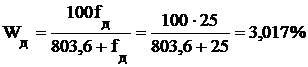
- в коксовом
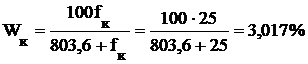
Теперь
пересчитываем состав сухих газов на рабочую массу [1]:
Для коксового газа содержание Н2 рассчитывается
следующим образом:
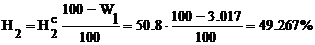
Аналогично находим содержание компонентов CO, CH4, CO2 и N2 во влажном коксовом газе, используя COС, C2H4С, CH4С, CO2С и N2С соответственно.
Таким же образом рассчитываем состав влажного доменного газа.
Полученные результаты заносим в таблицу 2.
Характеристика
видов топлива
|
Газ
|
Состав топлива
в объёмных процентах (на рабочую массу)
|
|
H2Р COРCH4РC2H4РCO2РN2РWР COРCH4РC2H4РCO2РN2РWР
|
|
|
|
|
|
|
|
Доменный
|
3,2
|
26,574
|
0,873
|
-
|
9,698
|
56,638
|
3,017
|
|
Коксовый
|
49,267
|
5,237
|
25,7
|
1,649
|
2,231
|
12,899
|
3,017
|
Определяем низшую теплоту сгорания газов [1]:
Для доменного газа:
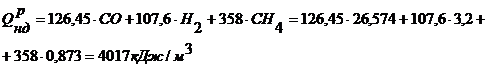
Для коксового газа:
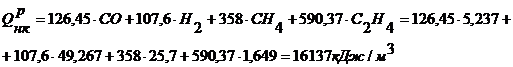
Находим долю доменного и коксового газов [1]:
Пусть х - доля доменного газа:
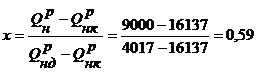
тогда доля коксового газа будет равна 1-х=1-0,59=0,41.
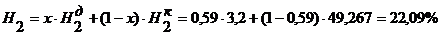
Аналогично определяем содержание других компонентов
смешанного газа и получаем его состав:
Состав топливной смеси
COР
|
CH4Р
|
C2H4Р
|
CO2Р
|
N2Р
|
WР
|
|
22,09
|
17,82
|
11,05
|
0,68
|
6,64
|
38,7
|
3,017
|
Для проверки точности расчёта определяем теплоту сгорания
смешанного газа:
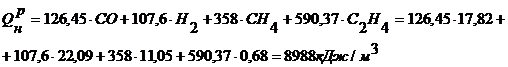
Рассчитаем погрешность между расчетной и заданной теплотой
сгорания [1]:
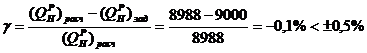
Теперь переходим к расчету удельного теоретического количества
воздуха и продуктов горения табличным способом, основанном на том, что объемы
газов в реакции относятся так же как их стехиометрические коэффициенты, и учитывающим
то, что процентное соотношение содержания азота к содержанию кислорода в
воздухе равно 3,76.
Расчет горения газа (на 100 м3 при a=1). Определяем удельное действительное
количество воздуха, количество и состав продуктов горения для нашего коэффициента
расхода воздуха a=1,05 [1]:
Удельное количество воздуха:
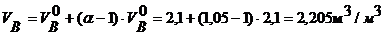
Удельное количество продуктов горения:
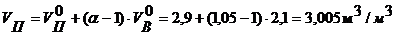
Удельное количество азота:
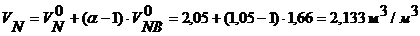
Удельное количество кислорода:
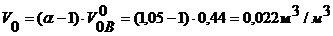
Удельное количество других компонентов продуктов горения:
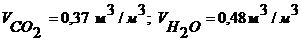
Определяем химический состав продуктов горения [1]:
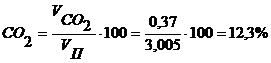
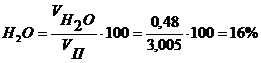

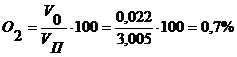
Теперь посчитаем плотность газа и продуктов горения.
Плотность смешанного газа [1]:
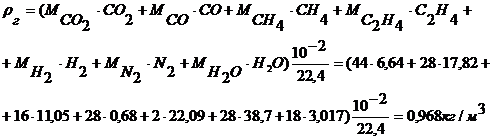
Плотность продуктов горения:
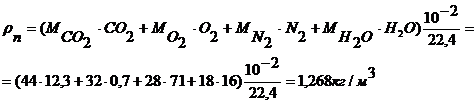
Точность расчета проверяем составлением материального баланса
горения на 1 м3 газа.
Поступило:
газа rгVг=0,968.1=0,968 кг
воздуха rвVв=1,29.2,205=2,85 кг
Всего m1= 3,82 кг
Получено:
продуктов горения
m2=rпVп=1,275.3,005=3,83
кг
невязка 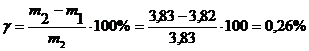
то есть g=0,26%<0,5%
следовательно расчет выполнен с достаточной степенью точности и пересчета не
требуется.
Расчет калориметрической температуры горения.
Энтальпия продуктов горения [1]:
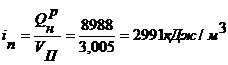
Предварительно принимаем температуру tк=1800оС.
С помощью справочной литературы находим энтальпию продуктов горения при 1800оС
[2]:
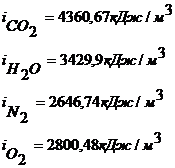
Следовательно энтальпия продуктов горения [1]:
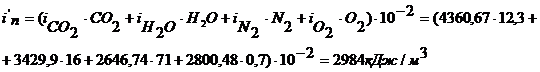
Так как 2991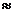 2984 (кДж/м3), то есть i’П
2984 (кДж/м3), то есть i’П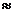 iП, то c достаточной степенью точности можно принять калориметрическую
температуру горения tк = 18000С.
iП, то c достаточной степенью точности можно принять калориметрическую
температуру горения tк = 18000С.
Итак, по результатам расчетов определили:
- теоретически необходимое количество воздуха:
Vв0 = 2,1 м3/м3
- действительное количество воздуха:
Vв = 2,205 м3/м3
- количество продуктов сгорания и их процентный состав:
Vп = 3,005 м3/м3
СО2 = 12,3%
Н2О = 16%
N2 = 71%
О2 = 0,7%
- калориметрическую температуру горения  tк=18000С.
tк=18000С.