Физические свойства магния
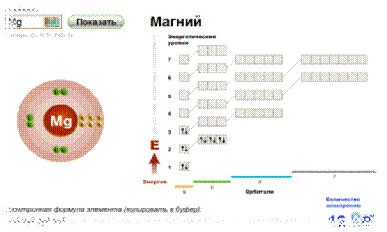
Магний
Магний - элемент главной подгруппы
второй группы, третьего периода с атомным номером 12.
Строение атома:
1) Конфигурация электронного облака
1s2 | 2s2 2p6 3s2
2) Радиус атома 145 · 10-12
(Метр)
) Атомная масса 24.305 (г/моль)
Физические
свойства:
1) металл серебристо-белого
цвета, обладает металлическим блеском
) пластичный и ковкий металл,
хорошо прессуется, прокатывается и поддаётся обработке резанием.
) теплопроводность при 20°C -
156 Вт/(м•К)
) мягкий (твердость магния 2
по шкале Мооса)
) температура кипения tкип =
1103°C
) температура плавления
металла tпл = 651°C
) плотность магния при 20°C -
1,737 г./смі
) цветной металл
) проводит электричество
(удельное электрическое сопротивление проводников (при 20°C) - 4.400 · 10-8
(Ом · Метр)
) по магнитным свойствам
парамагнетик
Распространение в
природе
Магний - это один из самых
распространённых элементов земной коры. Главными видами нахождения
магнезиального сырья являются:
карналлит - MgCl2 • KCl •
6H2O (Mg 8,7%),
бишофит - MgCl2 • 6H2O
(Mg 11,9%),
кизерит - MgSO4 • H2O
(Mg 17,6%),
эпсомит - MgSO4 • 7H2O
(Mg 16,3%),
каинит - KCl • MgSO4 • 3H2O
(Mg 9,8%),
магнезит - MgCO3 (Mg
28,7%),
доломит - CaCO3 • MgCO3
(Mg 13,1%),
брусит - Mg(OH)2 (Mg
41,6%).
Магний есть в кристаллических горных
породах в виде нерастворимых карбонатов или сульфатов, а также (в менее
доступной форме) в виде силикатов. Оценка его общего содержания существенно
зависит от используемой геохимической модели, в частности, от весовых отношений
вулканических и осадочных горных пород. Сейчас используются значения от 2 до
13,3%. Возможно, наиболее приемлемым является значение 2,76%, которое по
распространенности ставит магний шестым после кальция (4,66%) перед натрием
(2,27%) и калием (1,84%).
Большие области суши, такие как
Доломитовые Альпы в Италии состоят преимущественно из минерала доломита. Там
встречаются и осадочные минералы - магнезит, эпсомит, карналлит, лангбейнит.
Залежи доломита есть во многих
других районах, в том числе в Московской и Ленинградской областях. Богатые
месторождения магнезита найдены на Среднем Урале и в Оренбургской области. В
районе г. Соликамска разрабатывается крупнейшее месторождение карналлита.
Силикаты магния представлены базальтовым минералом оливином, мыльным камнем
(тальк), асбестом (хризотил) и слюдой. Шпинель относится к драгоценным камням.
Большое количество магния содержится
в водах морей и океанов и в природных рассолах. В некоторых странах именно они
являются сырьем для получения магния. По содержанию в морской воде из
металлических элементов он уступает только натрию. В каждом кубометре морской
воды содержится около 4 кг магния. Магний есть и в пресной воде, обусловливая,
наряду с кальцием, ее жесткость.
Магний всегда содержится в
растениях, так как входит в состав хлорофиллов.
Химические
свойства:
1) конфигурация внешних
электронов атома Магния 3s2
) во всех стабильных
соединениях Магний двухвалентен
) активный металл
) радиус атома 145 • 10-12
(Метр)
) гексагональная
кристаллическая решёткой
) металлическая
кристаллическая решетка
Важнейшие
соединения магния и их применение.
Гидрид магния MgH2.
Твердое белое нелетучее вещество. Мало растворим в воде. Разлагает
воду и спирты. Распадается на элементы при нагревании. Образуется при
взаимодействии магния с водородом при нагревании. Является одним из наиболее
ёмких аккумуляторов водорода, применяемых для его хранения.
Оксид (белая магнезия,
жженая магнезия) магния MgO. Встречается в природе
в виде серовато-зеленых прозрачных октаэдрических кристаллов. Мало растворим в
воде, растворяется в спирте, разбавленных кислотах. Можно получить, сжигая
магний в кислороде, прокаливанием гидроксида или карбоната магния.
Применяется для изготовления лабораторных
изделий (тиглей, лодочек, багетов, трубок для сжигания), огнеупорного кирпича,
магнезиального цемента.
Гидроксид магния Mg(OH)2. Встречается в природе в виде белого волокнистого вещества,
называемого бруситом. Бесцветные тригональные кристаллы со слоистой решеткой.
Слабое основание. Растворяется в разбавленных кислотах и солях аммония. Мало
растворим в воде. Обезвоживается при нагревании. В промышленности извлекается
из морской воды путем осаждения известковым или доломитовым молоком. Можно получить
действием гидроксидов щелочных металлов на соли магния.
Используется в качестве пищевой
добавки, для связывания диоксида серы, как флокулянт для очистки сточных вод, в
качестве огнезащитного средства в термопластических полимерах (полиолефины,
ПВХ), как добавка в моющие средства, для получения оксида магния, рафинирования
сахара, в качестве компонента зубных паст. В медицине его применяют в качестве
лекарства для нейтрализации кислоты в желудке, а также как очень сильное
слабительное. В Европейском союзе гидроксид магния зарегистрирован в качестве
пищевой добавки E528.
Фторид магния MgF2. Бесцветные диамагнитные тетраэдрические кристаллы. Мало
растворим в воде и ацетоне, растворяется в растворах фторидов и сульфатов
щелочных металлов. Можно получить, сжигая магний в атмосфере фтора или действуя
плавиковой кислотой на оксид магния.
Применяется для защиты металлов от
коррозии и изготовления матового стекла и керамики.
Хлорид магния MgCl2. Бесцветные гексагональные кристаллы со слоистой структурой,
очень гигроскопичные. Хорошо растворим в воде, спирте, пиридине, мало растворим
в ацетоне. Можно получить, сжигая магний в хлоре, действуя соляной кислотой на
металлический магний.
Применяется для электролитического
получения металлического магния, для пропитки тканей и древесины, для
производства магнезиальных цементов, а также в медицине.
Бромид магния MgBr2. Бесцветные гексагональные диамагнитные кристаллы. Растворяется в
воде, спирте. Легко присоединяет аммиак, пиридин и этилендиамин. Получают
взаимодействием магния и брома при нагревании.
Применяется для получения
элементарного брома, бромида серебра и других мало растворимых в воде бромидов.
Иодид магния MgI2. Бесцветные кристаллы, очень гигроскопичные. Легко растворяется в
воде, спирте, эфире. Получают непосредственным взаимодействием магния и йода
или реакцией между хлоридом магния и иодидом аммония.
Используется в некоторых
гомеопатических препаратах.
Сульфид магния MgS. Бесцветные кубические кристаллы. Мало растворим в воде. Реагирует
с галогенами. Разлагается разбавленными кислотами с образованием солей и
выделением сероводорода. Получают взаимодействием магния с серой или
сероводородом.
Сульфат магния MgSO4. Бесцветные ромбоэдрические диамагнитные кристаллы. Растворяется в
воде, спирте и эфире. Можно получить в лаборатории взаимодействием оксида или
карбоната магния с серной кислотой. В промышленности получают из морской воды
или из природных минералов - карналлита и кизерита.
Применяется для отделки тканей,
производства огнестойких тканей и бумаги, при дублении кожи, в качестве
протравы в красильной промышленности.
Нитрат магния Mg(NO3)2. Бесцветные кристаллы. Растворяется в воде, спирте и
концентрированной азотной кислоте. В промышленности получают из природного
минерала нитромагнезита. Получают в лаборатории взаимодействием магния, оксида
магния или гидроксида магния с разбавленной азотной кислотой.
Используется в качестве удобрения.
Карбонат магния MgCO3. Бесцветные тригональные диамагнитные кристаллы. Мало растворим в
холодной воде. В горячей воде переходит в основные карбонаты. Растворяется в
кислотах. Разлагается при нагревании. Получают обработкой хлорида или сульфата
магния карбонатом натрия или кальция в избытке углекислого газа. В
промышленности можно получить из природных минералов магнезита и доломита.
Гидрокарбонат магния
Mg(HCO3)2.
Получают в растворе при пропускании углекислого газа через водную суспензию
оксида, гидроксида или карбоната магния. Наличие гидрокарбоната магния в воде
обуславливает ее временную жесткость, которая устраняется кипячением или
добавлением соды.
Химические свойства оксида и
гидроксида магния
Оксид магния (жжёная магнезия,
периклаз) - химическое соединение с формулой MgO, бесцветные кристаллы,
нерастворимые в воде, пожаро- и взрывобезопасен. Основная форма - минерал
периклаз.
Химические свойства
) Легко реагирует с
разбавленными кислотами и водой с образованием солей и Mg(OH)2:
+ 2HCl→ MgCl2 + H2O;+
H2O → Mg(OH)2.
Гидроксид магния - неорганический
гидроксид щелочноземельного металла магния. Относится к классу нерастворимых
оснований.
Химические свойства:
) Разложение при нагревании
до 350°C:
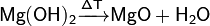
) Взаимодействие с кислотами
с образованием соли и воды (реакция нейтрализации):
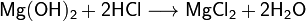
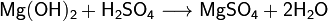
) Взаимодействие с кислотными
оксидами с образованием соли и воды:
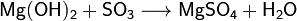
) Взаимодействие с горячими
концентрированными растворами щелочей с образованием гидроксомагнезатов:
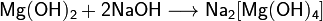
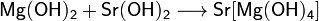
Способы получения
элемента.
Обычный промышленный метод получения
металлического магния - это электролиз расплава смеси безводных хлоридов магния
MgCl2, натрия NaCl и калия KCl. В этом расплаве электрохимическому
восстановлению подвергается хлорид магния:
Расплавленный металл периодически
отбирают из электролизной ванны, а в нее добавляют новые порции
магнийсодержащего сырья. Так как полученный таким способом магний содержит
сравнительно много - около 0,1% примесей, при необходимости «сырой» магний
подвергают дополнительной очистке. С этой целью используют электролитическое
рафинирование, переплавку в вакууме с использованием специальных добавок -
флюсов, которые «отнимают» примеси от магния, или перегонку (сублимацию)
металла в вакууме. Чистота рафинированного магния достигает 99,999% и выше.
Разработан и другой способ получения
магния - термический. В этом случае для восстановления оксида магния при
высокой температуре используют кремний или кокс:
магний химический соединение
MgO + C = Mg + CO
Применение кремния позволяет
получать магний из такого сырья, как доломит CaCO3·MgCO3,
не проводя предварительного разделения магния и кальция. С участием доломита
протекают реакции:
CaCO3·MgCO3 = CaO + MgO + 2CO2,
2MgO + 2CaO + Si = Ca2SiO4
+ 2Mg.
Преимущество термического способа
состоит в том, что он позволяет получать магний более высокой чистоты. Для
получения магния используют не только минеральное сырье, но и морскую воду.
Влияние элемента на
организм человека.
Magnifique - значит великолепный. От
этого французского слова получил название элемент периодической таблицы -
магний. На открытом воздухе горит это вещество очень эффектно, великолепным
ярким пламенем. Отсюда и магний. Однако великолепен магний не только тем, что
горит красиво.
Необычайно важна роль магния в
организме человека для обеспечения протекания различных жизненных процессов. И,
к счастью, с горением это не связано никак. А какие это процессы? Давайте
рассмотрим.
Организма человека содержит, в
среднем, 20 - 30 миллиграммов магния. 70% этого количества включают в себя
кости скелета, остальной объём содержится в мышцах, железах внутренней
секреции. Небольшое количество магния присутствует в крови. Магний успокаивает
нервную систему, и центральную, и периферическую. Вообще, магний необходим для
регулировки равновесия в мышечной и нервной тканях. Магний как бы обеспечивает
«внутренний покой» организма.
Магний является фактором и
активатором некоторых ферментов - энолазы, щелочной фосфатазы, карбоксилазы,
гексокиназы. Установлено участие магния в фосфорном и углеводном обмене.
Элемент оказывает асептическое и сосудорасширяющее действие. Под воздействием
соединений магния усиливается перистальтика кишечника, лучше отделяется желчь и
выводится холестерин, снижается нервно-мышечная возбудимость. Магний участвует
в синтезе белка. Наряду с вышеперечисленным роль магния в организме человека
заключается в оказании щелочного действия на органы и ткани.
С участием магния протекает более
трёх сотен ферментативных реакций. Особенно активно магний участвует в
процессах, которые связаны с утилизацией энергии, в частности, с расщеплением
глюкозы и удалением из организма отработанных шлаков и токсинов. В процессах
синтеза белка роль магния - производство ДНК. Получено подтверждение, что
тиамин (В1), пиридоксин (В6) и витамин С полноценно усваиваются именно в
присутствии магния. Благодаря магнию более устойчивой становится структура
клеток во время их роста, эффективнее проходит регенерация и обновление клеток
тканей и органов. Магний, этот «великолепный» элемент, стабилизирует костную структуру
и придаёт костям твёрдость.