Исследование свойств смесей желтого железооксидного пигмента и шунгита
Реферат
ЖЕЛЕЗООКСИДНЫЕ ПИГМЕНТЫ, ШУНГИТ, СМЕЩЕНИЕ, ПРОКАЛИВАНИЕ, СПЕКТРЫ
ДИФФУЗНОГО ОТРАЖЕНИЯ, ЦВЕТ, СВОЙСТВА ПИГМЕНТА, МАСЛОЕМКОСТЬ, УКРЫВИСТОСТЬ,
СВОЙСТВА ПОКРЫТИЯ
Объектами исследования являются желтый и красный железооксидные пигменты
и шунгит.
Целью данной работы является исследование свойств смесей желтого
железооксидного пигмента и шунгита и пигментов на основе таких смесей.
В процессе работы проводились изучения основных свойств смесей желтого
железооксидного пигмента с шунгитом в различном соотношении, синтез коричневых
пигментов на основе таких смесей прокалочным методом и определение основных
свойств синтезированных пигментов. Были получены пигментированные лакокрасочные
материалы и покрытия на основе синтезированных пигментов.
В результате исследования было определено влияние массовой доли шунгита в
смеси на ее цвет и физико-химические свойства; влияние температуры, времени и
массовой доли шунгита в смеси на цвет и физико-химические свойства
синтезированных пигментов. Также были исследованы защитно-декоративные свойства
пигментированных лакокрасочных покрытий на основе синтезированных пигментов.
шунгит синтезированный пигмент лакокрасочный
Содержание
Введение
. Литературный обзор
.1 Шунгит
.2 Железооксидные пигменты
.2.1 Желтые железооксидные пигменты
.2.2 Красные железооксидные пигменты
.2.3 Коричневые железооксидные пигменты
. Объекты и методы исследования
.1 Объекты исследования
.2 Методы исследования
.2.1 Определение цвета пигмента
.2.2 Определение маслоемкости
.2.3 Определение укрывистости
.2.4 Определение плотности пигмента пикнометрическим методом
.2.5 Дериватографический анализ
.2.6 Получение лакокрасочных покрытий методом налива
.2.7 Определение прочности лакокрасочных покрытий при ударе
.2.8 Определение относительной твердости
.2.9 Определение адгезионной прочности
.2.10 Определение эластичности пленки при изгибе
. Результаты и их обсуждение
.1 Исследование свойств смесей желтого железооксидного
пигмента и шунгита
.2 Получение коричневого пигмента из смесей шунгита с желтым
железооксидным пигментом
.Охрана труда и защита окружающей среды
.1 Свойства, применяемых в работе, материалов
.2 Меры пожарной профилактики
.2.1 Определение категорий помещений по взрывопожароопасности
по НПБ 105-03 и класса помещения по ПУЭ
4.2.2 Средства пожаротушения
4.2.3 Нормы хранения ЛВЖ и ГЖ лаборатории
.2.4 Правила работы с ЛВЖ и ГЖ
.2.5 Метеорологические и санитарно-гигиенические условия в
лаборатории
.3 Вентиляция лабораторных помещений
.4 Освещение лабораторных помещений
.5 Электробезопасность на рабочем месте
.6 Водоснабжение. Удаление сливов и отходов
.7 Условия безопасного проведения исследований
Заключение
Список литературы
Приложение
Введение
Без лакокрасочной продукции не может обойтись ни одна отрасль народного
хозяйства, так как лакокрасочные материалы при нанесении на различные подложки
выполняют множество функций: защитные, декоративные и другие. Применяемые
лакокрасочные материалы могут быть как ненаполненными (лаки), так и
наполненными - пигментированными (краски, эмали, грунтовки). Пигментированные
лакокрасочные материалы представляют собой дисперсные системы, содержащие в
качестве дисперсной фазы пигменты и наполнители, а в качестве дисперсионной
среды растворы или полимеры пленкообразователя с различными целевыми добавками.
Пигменты - это высокодисперсные вещества, нерастворимые (в отличие от
красителей) в воде, органических растворителях, пленкообразователях и других
дисперсионных средах, обладающие определённым набором оптических, механических,
сорбционных свойств.
Пигменты являются твердыми компонентами композиционных лакокрасочных
материалов - красок, эмалей, грунтовок, шпатлевок и порошковых композиций.
Взаимодействуя с органическими пленкообразователями, пигменты создают с ними
структурные сетки, увеличивая прочность и долговечность покрытий. За счёт
полного или частичного рассеивания света пигменты придают пленке цвет. Пигменты
игольчатой и чешуйчатой формы армируют пленку, снижают ее газо- и
водопроницаемость, повышают механическую прочность и атмосферостойкость
лакокрасочных покрытий.
Пигментные частицы в пленке, поглощая, отражая и рассеивая равномерно или
избирательно лучи падающего света, придают белую, черную или цветную окраску
пленке, полностью укрывая цвет находящейся под пленкой подложки. Одновременно
пигменты защищают органическое полимерное вещество от деструкции под
воздействием солнечных лучей, задерживая его разрушение.
Выбор пигментов определяется свойствами пигмента и материала, характером
их взаимодействия, а также параметрами переработки и условиями эксплуатации
изделий. При выборе следует иметь в виду, что технические свойства пигмента
(оттенок, укрывистость, светостойкость, интенсивность и др.) зависят не только
от химического состава пигментов, но в большей степени от размеров и формы
частиц, которые в свою очередь, зависят от условий получения пигмента:
концентрации и температуры исходных растворов, интенсивности их перемешивания,
температуры и т.д.
Особое место среди многообразия существующих пигментов занимают
железооксидные пигменты (ЖОП). Они обладают высокой укрывистостью и
интенсивностью, они стойки к действию света, солей, слабых кислот и оснований,
непрозрачны для ультрафиолетовых лучей и придают красочной пленке значительную
механическую прочность и непроницаемость для влаги; красные железооксидные
пигменты также термостойки. Следует заметить, что железооксидные пигменты также
относительно доступны и легко синтезируются. В основном применяются пигменты
желтого и красного цветов. Ограниченное применение находят черные пигменты,
представляющие собой закись-окись железа Fe3O4. Коричневые пигменты представляют
собой смесь красной и черной окиси железа. Получают коричневые пигменты
осадочным способом, регулируя процесс таким образом, чтобы в результате
окисления образовывалась смесь красного и черного пигмента [1]. Коричневые
пигменты можно также получать путем механического смешения красных и черных
пигментов. В качестве красных пигментов используются красные ЖОП, в качестве
черных - технический углерод, черный ЖОП. Но такие пигменты обладают рядом
недостатков - они имеют холодные оттенки цвета, их гранулометрический состав
может отличаться большой неоднородностью.
В последнее время в лакокрасочной промышленности наметилась тенденция
замены в лакокрасочных материалах черных пигментов шунгитом [статья]. Обладая
дифильностью, шунгит способен совмещаться со многими пленкообразователями, но
обладает невысокой укрывистостью. Поэтому зачастую его используют в сочетании с
хорошо укрывающими пигментами, например, диоксидом титана, желтым или красным
ЖО пигментами. Возможно также использование шунгита и для получения смешанных
коричневых пигментов.
Цель работы
В данной работе изучены свойства смесей шунгита с желтым железоксидным
пигментом и возможность получения коричневых пигментов на основе таких смесей.
Полученные пигменты, возможно, позволят расширить области применения шунгита и
гамму цветов коричневых пигментов.
1. Литературный обзор
Применяемые в лакокрасочной промышленности пигменты принято подразделять
на органические и неорганические. В качестве неорганических используют
нерастворимые в воде, растворителях и пленкообразователях соли, оксиды или
гидратированные оксиды металлов (цинка, титана, железа, свинца). В качестве
черного пигмента широко применяется углерод. И если в последнее время пигменты
на основе соединений свинца практически вытеснены органическими пигментами, то
желозосодержащие, наоборот, продолжают широко применятся. Они обладают рядом
преимуществ перед органическими соединениями, например, большей светостойкостью
и термостойкостью, укрывистостью, флотационной устойчивостью. На их основе
возможно получение черных и коричневых пигментов. Также, в последнее время
наметилась тенденция использования в качестве пигмента природного минерала
шунгита, как доступного и относительного дешевого сырья. Его возможности как
наполнителя пигментированных лакокрасочных материалов в полной мере еще не
исследованы.
.1 Шунгит
Шунгит представляет собой природный композит - это комплексное
углеродсодержащее природное сырье, состоящее из особой разновидности аморфного
углерода и силикатных минералов, среди которых преобладает кварц. Выпускается
шунгит в виде высокодисперсного порошка черного или темно-серого цвета.
Единственные в мире месторождения шунгитовых горных пород находится в
Карелии и шунгитовые породы различных месторождений содержат от 2 до 98 %
углерода [3]. Основное месторождение, промышленная разработка которого ведется
в настоящее время - Зажогинское, представлено шунгитом, содержащим 57-60 % SiO2
и 28-32 % углерода. Средний химический состав шунгитовых пород определенный по
64 пробам из 3-х скважин Зажогинского месторождения, приведен в таблице 1.1
[4].
Таблица 1.1 - Химический состав шунгитовой горной породы из 3-х скважин
Зажогинского месторождения
|
Компоненты
|
SiO2
|
TiO2
|
Al2O3
|
Fe2O3
|
MgO
|
CaO
|
Na2O
|
K2O
|
P2O5
|
S
|
C
|
H2Oкр
|
|
Содержание, %
|
57,5
|
0,21
|
3,95
|
2,44
|
1,11
|
0,24
|
0,20
|
1,50
|
0,06
|
1,11
|
28,6
|
4,2
|
Химический состав шунгитовых пород Карелии представлен в таблице 1.2.
Таблица 1.2 - Химический состав шунгитовых пород Карелии.
|
Содер, %
|
SiO2
|
TiO2
|
Al2O3
|
Fe2O3
|
FeO
|
MgO
|
CaO
|
Na2O
|
K2O
|
Cсв
|
S(общ)
|
|
Трещиноватые
|
|
Среднее
|
47,04
|
0,25
|
4,16
|
1,13
|
0,42
|
0,57
|
0,08
|
0,117
|
1,225
|
44,57
|
0,38
|
|
Мин.
|
38,62
|
0,19
|
3,11
|
0,35
|
0,27
|
0,43
|
0,01
|
0,03
|
0,94
|
31,9
|
0,13
|
|
Макс.
|
61,02
|
0,38
|
5,6
|
2,06
|
0,52
|
0,88
|
0,14
|
0,52
|
1,56
|
53,32
|
0,93
|
|
Массивные
|
|
Среднее
|
54,42
|
0,23
|
3,74
|
1,49
|
0,55
|
0,59
|
0,17
|
0,062
|
1,342
|
36,57
|
0,9
|
|
Мин.
|
41,82
|
0,14
|
2,1
|
0,37
|
0,14
|
0,21
|
0,07
|
0,03
|
0,58
|
22,17
|
0,11
|
|
Макс.
|
71,04
|
0,3
|
5,09
|
2.96
|
1,72
|
1,67
|
0,56
|
0,12
|
2,24
|
50,4
|
1,9
|
|
Кварц-шунгитовые брекчии с
миндалинами
|
|
Среднее
|
60,58
|
0,201
|
3,16
|
1,17
|
1,06
|
0,54
|
0,13
|
0,048
|
0,964
|
31,42
|
0,73
|
|
Мин.
|
44,57
|
0,14
|
2,27
|
0,21
|
0,45
|
0,26
|
0,01
|
0,02
|
0,6
|
22,8
|
0,2
|
|
Макс.
|
70,07
|
0,32
|
4
|
4,12
|
4,04
|
1,65
|
0,43
|
0,1
|
1,74
|
44,31
|
2,65
|
|
Кварц-шунгитовые брекчии
|
|
Среднее
|
62,44
|
0,182
|
2,96
|
1,07
|
0,42
|
0,44
|
0,09
|
0,039
|
0,789
|
31,04
|
0,38
|
В 1992 году в лаборатории Аризонского университета было обнаружено
наличие в образцах шунгита небольшого количества (0,1 %) фуллеренов - особой
разновидности полимерного углерода, который впервые был получен искусственным
путем в 1985 году. Многоатомные полимеры фуллеренового углерода образуют
кластеры со сферической структурой, из которых наиболее стабильны молекулы С60,
С70 и С84. Первые два вида углеродных молекул могут
получаться в количествах достаточных для проведения с ними прикладных и
фундаментальных исследований. Эти искусственно полученные молекулы углерода
из-за их сферической структуры названы фуллеренами в честь Фуллера Бакминстера
- изобретателя "геодезического купола". Как и у покрышки футбольного
мяча, структура молекулы С60 состоит из шести и пяти атомных колец,
образующих квазисферическую оболочку. У молекулы С60 она состоит из
20 шестиатомных и 12 пятиатомных колец. Фуллерены получают при высоких
температурах из парообразного графита путем его испарения лазерным лучом или в
электрической дуге и последующей конденсации паров. При этом образуются
углеродные кластеры в виде полициклических сетевых структур, по мере роста
которых происходит их закрутка и образование совершенных сферических структур -
фуллеренов. Фуллерены в бескислородной атмосфере отличаются высокой химической
инертностью и стабильностью до температуры 1700 К. Однако в присутствии
кислорода окисление этой формы углерода начинается уже при температуре 500 К с
образованием СО и СО2. Повышение температуры до 700 К приводит к
интенсивному окислению углерода и к разрушению упорядоченной структуры
фуллерена и к образованию аморфной структуры [2].
Средний размер силикатных частиц около 1 мкм. Между углеродной и
силикатной компонентой существует прочная связь. Тонкодисперсный углерод и
силикаты в шунгите равномерно распределены по объему и имеют большую удельную
поверхность контактов (до 20 и более м2/г породы). Помимо углерода и кварца в
минеральный состав шунгитовых пород входят хлориты (сложные
железо-магний-алюмо-гидросиликаты). Углерод в шунгитовых породах присутствует в
виде глобул размером 100-200 Ао, пачек, стекловолокна, а также микродисперсного
кристаллического графита. Структура шунгита представлена на рисунке 1.1

Рисунок 1.1 - Структура шунгита [13]
Породы в пределах Зажогинского месторождения достаточно стабильны по
составу. Содержание углерода и оксида кремния в сумме находится в пределах 83 -
88%. На рисунке 1.2 представлено распределение содержания углерода и оксида
кремния в породе.
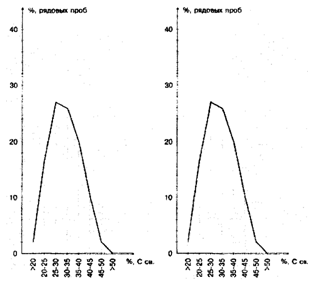
Рисунок 1.2 - Распределение содержания углерода (а) и оксида кремния (б)
в шунгитовой породе.
Силикаты распределены в шунгитовой матрице равномерно.

Рисунок 1.3 - Излучение Si -
К-альфа [13].
Содержащийся в породах кварц с учетом его дисперсного состояния и
равномерного распределения в углеродной матрице является полезным компонентом.
Вследствие исключительно развитого контакта между активным углеродом и
силикатами при нагреве шунгитовой породы активно протекают реакции
восстановления кремнезема до металлического кремния и карбида кремния.
SiО2+2C → Si+2COО2+3C → SiC+2CO
Эти реакции протекают в шунгите более энергично и с меньшими
энер-гозатратами, чем в традиционной шихте на основе кремнезема и кокса.
Поверхность дробленых, молотых и даже тонкомолотых материалов на основе
шунгита Зажогинского месторождения обладает биполярными свойствами, поэтому
шунгитовые наполнители способны смешиваться без исключения со всеми связующими
как органической, так и неорганической природы. Благодаря биполярности, порошки
шунгитовых пород смешиваются со всеми известными веществами: водными
суспензиями и фторопластами, каучуками, смолами и цементами и прочими
пленокобразователями. Такая структура и состав пород
сообщают шунгитовым материалам ряд необычных физических, химических,
физико-химических и технологических свойств. Частицы шунгитового порошка даже
микронных размеров содержат разные по полярности фазы. Следствием высокой
совместимости шунгитов со связующими является способность создавать
высоконаполненные композиции, в том числе на основе каучуков. При применении
шунгитовых пород необходимо учитывать их химический и минеральный состав. Шунгитовый углерод представляет собой необычный по структуре
углерод - некристаллический, неграфитирующий, фуллереноподобный. Он обладает
высокой активностью в окислительно-восстановительных реакциях, адсорбционными и
каталитическими свойствами. По реакционной способности такой углерод аналогичен
коксу и способен заменить его в реакциях восстановления в электротермических
процессах. По химической стойкости к некоторым средам даже превосходит его.
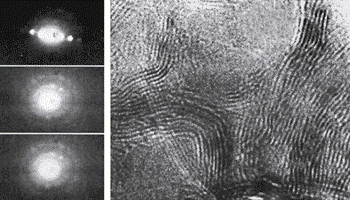
Рисунок 1.4 - Нанодифракционная картина шунгитового углерода (зонд 0,3 -
0,7 нм.)
Благодаря высокой удельной поверхности шунгитовые породы обладают
сорбционными, каталитическими и бактерицидными свойствами. Эти свойства находят
применение при использовании шунгитов в фильтрах подготовки питьевой воды и
воды в плавательных бассейнах, катализаторах в процессе оргсинтеза. По
способности очищать воду от нефтепродуктов шунгитовые породы не уступают
активированному углю, но значительно дешевле. Шунгит - универсальный сорбент и средство,
выделяющее в соединении с водой различные органические и минеральные вещества.
Настои воды на шунгите и шунгитовые пасты обладают лекарственными
свойствами, эффективно лечат многие заболевания - аллергические, респираторные,
гинекологические, мышечные и др.
Новый углеродный продукт имеет ряд преимуществ перед традиционными видами
углерода (коксом, графитом, сажей):
) Его получение исключает сложные, энергоемкие, экологически грязные
химические и термические технологии, по которым производят кокс, графит, сажу.
) Простота добычи и подготовка пород к промышленному использованию
обуславливает исключительную рентабельность по отношению к другим видам
углеродного сырья.
) Высокая механическая прочность шунгитовых пород - необходимая
предпосылка прочности композиционных материалов, а отсутствие пористости в них
- условие высокой морозостойкости композитов. Другим условием придания
композитам высокой механической прочности является совместимость шунгитового
наполнителя со связующим.
) Благодаря наличию минеральных фаз различной по полярности природы
(полярных силикатных и неполярной углеродной фазе) шунгитовая порода хорошо
совмещается почти со всеми неорганическими связующими - цементом, известью,
жидким стеклом. По механическим и строительным свойствам шунгитовые материалы
практически ни в чем не уступают обычным строительным, а по некоторым
свойствам, например, по прочности на удар, даже превосходят традиционные.
.2 Железооксидные пигменты
Пигменты, окраска которых обусловлена присутствием в них одного из
оксидов железа, называют железооксидными. Железо
с кислородом образует ряд оксидов: оксид железа (II) (FeO), оксид железа (III) (Fe2О3), оксид железа (II, III) (Fe3О4), гидрат оксида железа (II) FeO·H2O, и
гидрат оксида железа (III) Fe2O3·nH2O. Почти все соединения железа
окрашены: при наличии в них катиона Fe 2+, являющегося слабым хромофором, - в
светлый зеленовато-желтый цвет, а при наличии катиона Fe3 +, сильного хромофора, - в буро-красный или
желто-бурый цвет. Совместное присутствие ионов Fe2+ и Fe3 + вызывает синее или
черно-синее окрашивание.
По химическому составу железооксидные пигменты представляют собой оксид
железа (II или III), гидрат оксида железа (II или III) или оксид железа (II,
III). Эти соединения в чистом виде, в смеси между собой и в смеси с
наполнителями образуют весь комплекс железооксидных пигментов - синтетических и
природных.
Синтетические железооксидные пигменты получаются из солей железа путем
осаждения и прокаливания, а также из металлического железа путем окисления. Между химическим составом и цветом железооксидных пигментов
существует определенная зависимость, а именно: желтые пигменты являются
гидратами оксида железа (III), красные - оксидом железа (III), черные - оксидом
железа (II, III), а коричневые - гидратированным оксидом железа (II) или смесью
желтых и красных пигментов. Железоксидные
пигменты обладают высокой укрывистостью, стойки к действию солей, слабых кислот
и щелочей, непрозрачны для ультрафиолетовых лучей и придают пигментированной
пленке значительную механическую прочность и непроницаемость для влаги; красные
пигменты также термостойки. Окраска смесью железооксидных пигментов с цинковой
или свинцовой пылью, оксидом цинка или свинцовым суриком придает металлическим
изделиям исключительную коррозионную стойкость.
В связи с этим, а также со сравнительной дешевизной и доступностью
железооксидные пигменты широко применяются для грунтовок и наружных покрытий,
для изготовления высококачественных красок, эмалей на основе любых
пленкообразователей, а также для окрашивания в массе пластмасс, резин,
строительных материалов[1].
1.2.1 Желтые железооксидные пигменты
По химической природе являются гидратом оксида железа состава FeO(OH) или Fе2Оз·Н2О.
В действительности же существует ряд гидратов железа (II) , различающихся по
составу (по содержанию гидратной воды), по кристаллической структуре, а также
по физическому состоянию частиц.
При взаимодействии соли оксида железа (II) со щелочами гидрат оксида
железа (II) выделяется в виде аморфного осадка буро-желтого цвета, который при высыхании
переходит в гель с переменным содержанием воды.[1]
Моногидрат оксида железа (Ш) может кристаллизоваться в трех
кристаллических модификациях: α - FeO(OH)
(гетит), метастабильная β - FeO(OH) и γ- FeO(OH)
(лепидокрокит). В качестве пигмента применяется, главным образом, гетит [2].
Модификации кристаллизуются в ромбической системе, но различаются группировкой
атомов.
Константы кристаллической решетки: гетита - а=4,64 А , b=10,00 А , с
=3,03 А; лепидокрокита - а = 3,87 А, b = 12,51 А, с = 3,06 А. Обе модификации
обладают постоянным химическим составом Fe203-H20 или FeOOH; формулу FeOOH следует признать более правильной, так как в кристаллической решетке
этих гидратов отсутствуют группы Н20 и имеются ионы ОН-.
Элементарная ячейка гетита содержит две молекулы FeOOH, а лепидокрокита - четыре.
Кристаллические гидраты оксида железа (III) способны прочно адсорбировать
определенное число молекул воды, сохраняя при этом без изменения свою
кристаллическую решетку [1].
Все гидраты оксида железа (Ш) обладают различным цветом (оттенком) и
различными пигментными свойствами, в соответствии, с чем можно, изменяя условия
образования гидрата оксида железа (Ш), изменять цвет (оттенок) и пигментные
свойства желтых железооксидных пигментов в очень широких пределах. Например,
пигмент, получаемый окислением металлического железа, обладает чистым и ярким
цветом и пригоден для применения во всех видах окрасочных работ. Он известен
под названием желтый железооксидный пигмент, обладает высокими пигментными
свойствами (таблица 1.3). Он атмосферостоек и светостоек. А пигмент, полученный
от взаимодействия солей оксида железа (III) с содой или мелом с последующим
окислением образовавшегося осадка кислородом воздуха или бертолетовой солью,
применяют преимущественно для производства художественных красок и для клеевых
накрасок. Такие пигменты называются желтые марсы [1].
Таблица 1.3 - Некоторые свойства желтого железооксидного пигмента
|
Свойства
|
Показатели
|
|
Укрывистость, г/м2
|
10-12
|
|
Маслоемкость, г/100г
|
40-60
|
|
Удельная поверхность, м2/г
|
11,2
|
|
Насыпной вес, г/л
|
420-550
|
|
Средняя величина частиц,
мкм
|
0,2-0,6
|
Желтый железооксидный пигмент применяют для производства красок и эмалей
всех типов: масляных, нитролаковых, клеевых, фасадных и художественных. Кроме
того, пигмент используется в резиновой промышленности, а так же в качестве
сырья для синтеза красного железооксидного пигмента [2].
Известно множество методов синтеза железооксидных пигментов, однако все
методы сводятся к одной цели - получение оксида железа (II) и оксида железа
(Ш). Одним из самых распространенных методов является метод получения пигментов
осадочным способом из различных солей железа. Суть его сводится к получению
гидроксидов железа (II) или (Ш), с последующим их окислением различными
окислителями. Различие наблюдается только в технологии осаждения гидроксидов, в
использовании различных солей железа в качестве сырья (или самого
металлического железа) и в способе окисления (кислородом воздуха, окислительной
смесью или сильными сухими окислителями, например бертолетовой солью (КСlз)). Все эти методы можно объединить
в следующие две основные группы:
1) методы, основанные на взаимодействии солей оксида железа (II) с
основаниями (получение гидроксидов железа II или III) и последующем окислении.
) окисление металлического железа различными окислителями в
растворе электролита (с использованием зародышей пигмента). Рассмотрим
некоторые из этих методов более подробно.
Желтый железооксидный пигмент получают обычно в результате гидролиза
ионов Fe в кислой среде, которые образуются в
растворе при окислении ионов Fe2+ кислородом воздуха. Ионы Fe 3+ и Fe2 + в водных растворах
обычно гидролизованы. Гидролиз идет через стадию образования оксокислот [Fе(Н2О)б]2+
для Fe2+ и [Fe(H2О)6]3+ для Fe 3+. Кислотность среды при гидролизе повышается за счет
диссоциации этих кислот:
[Fe(H2О)6]2+↔[Fe(H2О)5OH]++Н+
[Fe(H2О)6]3+↔[Fe(H2О)5OH]2+ + Н+
Константа гидролиза ионов Fe3 + значительно выше
константы гидролиза ионов Fe2 + вследствие большего
заряда центрального атома в комплексе.[1]
Непосредственным осаждением гидрата оксида железа (III) из растворов Fe3+ получить продукт, обладающий
пигментными свойствами, не удается, так как он неизбежно образуется в виде
коллоидного осадка, поэтому процесс проводят в растворе солей железа (II),
осуществляя гидролиз ионов Fe3+, получающихся при окислении
кислородом воздуха ионов Fe 2+:
Fe2+ + 0,5О2 + 2Н+→2Fe3+ + Н2О
Регулирование при осаждении рН, от значения которого зависят многие
свойства получаемого пигмента, проводится путем введения нейтрализующего
агента, в качестве которого используют аммиак или, чаще всего, железо в виде
металлического лома. В этом случае суммарная реакция образования желтого
железооксидного пигмента соответствует следующему уравнению:
Fe +
1,5О2 + Н2О → 2FeO(OH).
Для исключения образования коллоидного гидроксида железа синтез проводят
в присутствии зародышей, которыми служит гидроксид железа (III), полученный
окислением гидроксида железа (II), обычно осаждаемого аммиаком:
[Fe(H2О)5OH]+
+ ОН- →Fe(OH)2 + 5Н2О Fe(OH)2 + 0,5О2 → 2FeO(OH) + Н2О.
Зародыши готовят в отдельных реакторах или в реакторах синтеза пигмента,
куда затем погружают железные стружки или обрезь и заливают раствор сульфата
железа (II). Через реакционную массу продувают воздух в течение 2-3 суток.
Раствор сульфата железа, в среде которого происходит синтез пигмента,
практически не расходуется, но загрязняется примесями, имеющимися в железе, и
ионами аммония, вводимыми с суспензией зародышей. Поэтому весь раствор или его
часть обновляется в каждом цикле периодически осуществляемого процесса синтеза.
Раствор сульфата железа, отделенный фильтрованием от полученного пигмента,
окисляют кислородом воздуха при температуре 60 - 70 °С и нейтрализуют до рН =
7,5. Высажденный темно-желтый осадок также используется в качестве пигмента.
Промывные воды освобождаются от ионов железа и сульфат-ионов
нейтрализацией гидроксидом кальция с одновременной продувкой воздуха.
Образуется гипс, окрашенный гидроксидом железа (III), который используется в
строительных материалах [2].
Описанный выше способ, является наиболее широко распространенным, однако,
существуют множество других методов получения желтых железооксидных пигментов,
отличающихся по свойствам, структуре и используемому сырью.
Пигмент на основе гидрата оксида железа (III) формулы FeO(OH) в виде кристаллов желтого цвета игольчатой формы размером в
среднем 0,12-0,7 мкм получают реакцией сульфата железа (II) с неорганическим
основанием и органическим ароматическим нитропроизводным [5]. На первой стадии
получают суспензию зародышевых кристаллов наполнителя гидрата оксида железа
(II) (FeO(OH)) реакцией сульфата железа (II) в водном растворе с водным
раствором аммиака и ароматическим нитропроизводным в молярном отношении аммиака
и сульфата железа < 1:1 и молярном отношении аммиака и нитрогрупп в ароматическом
нитросоединении < 6:1. Реакцию проводят при 20-70 °С до установления
постоянной величины рН реакционной смеси. При этом получают суспензию пигмента,
содержащую твердые частицы (предположительно гидрат оксида железа (II)) в
количестве ≈80 г/л. На второй стадии смешивают зародышевые кристаллы с
раствором сульфата железа (II) и органическим нитропроизводным при 20-70 °С и
постепенно прибавляют к смеси водный раствор аммиака так, чтобы рН раствора был
8,5, в молярном отношении аммиака и органического нитропроизводного 6:1 - 12:1.
При этом получают суспензию гидрата оксида железа (II), содержащую 120 г/л
твердых частиц, причем зародышевые частицы применяют в количестве 8 - 20 ч.
масс. на 100 ч. масс. наполнителя. Из реакционной смеси выделяют пигментный
гидрат оксида железа (II) и образующийся в процессе реакции амин.
При получении цинксодержащего гетита с частицами пластинчатой формы,
характеризующегося повышенной термостойкостью [6], соль железа (III), а в
частности сульфат железа (III) или хлорид железа (III), обрабатывают в водной
среде щелочью (например, едким натром). Обработку ведут в присутствии
аминоспирта (моноэтаноламин, триэтаноламин) и соединения цинка (сульфат цинка,
хлорид цинка). Суспензию выпадающего осадка гидроксида железа (III) подвергают
гидротермальной обработке, в результате чего образуется цинксодержащий гетит с
частицами пластинчатой формы имеющими поперечник 0,01-1 мм и отношением
поперечника к толщине от 1 до 10. Продукт рекомендуют использовать для
получения желтых пигментов, а также для изготовления магнитных порошков,
используемых в магнитных элементах памяти.
Как видно из представленного обзора, существует множество различных
способов получения гетита, для различных областей применения. Однако можно
заметить некоторые сходства во всех представленных технологиях: это получение
гидроксидов железа (II или III), рост (выдержка) зародышей, и последующее их
окисление, - воздухом или кислородом[1].
Существуют также технологии, где в качестве окислителя применяются
различные "сухие" окислители, например бертолетова соль (КС1з) или
хлорид-гипохлорит кальция (СаС12О). Для получения пигмента в реактор
сливают при перемешивании 10% растворы железного купороса и кальцинированной
соды:
2FeSО4 + 2Na2CО3 →2FeCО3+Na2SО4 2FeCО3 +H2О + 0,5O2 →Fe2О3·H2О
В результате реакции выпадает осадок углекислого железа светло-зеленого
цвета, который затем окисляют раствором бертолетовой соли при 50-60 °С.
Окисление ведут в течение 3-4 часов. Сначала окисление протекает очень быстро,
а затем сильно замедляется. Процесс окисления может быть закончен при наличии в
осадке до 5-6 % соли железа (II), так как во время высушивания его происходит
доокисление солей железа (II).[1]
По такой технологии получают т.н. желтый марс. Повышение температуры
окисления сильно ухудшает цвет пигмента. Так, при 70-80 °С образуются черные
или черно-бурые продукты. Применяется данный пигмент в масляных красках, так
как не отличается яркостью и бархатистостью [1].
.2.2 Красные железооксидные пигменты
Группа красных железооксидных пигментов объединяет ряд пигментов,
обладающих оттенками от оранжево-красного до фиолетово-красного цветов и
состоящих в основном из оксида железа (III). Оттенок зависит от условий
получения пигмента.
Оксид железа (III) (Fe2О3) существует в двух кристаллических
модификациях: гематита - гексагональной системы и маггемита - кубической
системы. В качестве пигментов применяется главным образом оксидом железа (Ш)
гексагональной системы. Различие оттенков этих пигментов обусловлено только
физическим состоянием частиц, поэтому они все объединяются в одну группу -
красного железооксидного пигмента.
Красный железооксидный пигмент по химическому составу представляет собой
чистый оксид железа (III) (Fe2О3). Свойства красного железооксидного
пигмента находятся в зависимости его оттенка: плотность светлых оттенков
составляет 4,8 г/см, темных - 4,9-5,0 г/см , маслоемкость соответственно 48
г/100г и 22 г/100г, насыпной вес 500-740 г/л.
Размер частиц красного железооксидного пигмента возрастает с переходом от
светлых оттенков к темным и колеблется в пределах 0,1 - 0,8 мкм. Форма частиц
светлых оттенков пластинчатая, темных - зернистая.
Красный железооксидный пигмент очень устойчив к действию солнечного
света, атмосферных влияний, щелочей и слабых кислот; в крепкой серной кислоте
он растворяется только при нагревании [1]. Свойства красного железооксидного
пигмента представлены в таблице 1.4.
Таблица 1.4 - Свойства красного железооксидного пигмента
|
Свойства
|
Показатели
|
|
Плотность, кг/м3
|
4500-5000
|
|
рН водной вытяжки
|
5,5-7,0
|
|
Насыпной объем, Vнас-103
, м3 /кг
|
2,2-2,4
|
|
Маслоемкость, г/100 г
|
25-35
|
|
Укрывистость, г/м2
|
6-8
|
Пигмент применяется для получения грунтовок, эмалей и красок на основе
любых пленкообразователей, в пищевой промышленности. Используется для
окрашивания резины, пластмасс, древесно-стружечных материалов.
Красный железооксидный пигмент получают чаще всего термическим
разложением железного купороса с предварительной его дегидратацией до
одноводного сульфата во избежание спекания конечного продукта [2]: Применяют
данную технологию на ООО "ГАК "ТИТАН" респ. Крым, Украина.
FeSО4·H2О → Fe2О3
+ SО2 + SО3 + 2H2О
При температуре 700-725 °С получается красно-оранжевый пигмент, при
температуре 730-780 °С - красный, при температуре 850 °С -
пур-пурно-фиолетовый.
Термическое разложение гептагидрата сульфата железа (II) в присутствии
кислорода воздуха происходит в три стадии: 1) дегидратация с превращением
семиводного кристаллогидрата в одноводный; 2) окисление двухвалентного железа в
трехвалентное; 3) превращение сульфата оксида железа (II) в оксид железа (III).
Потеря воды из гептагидрата сульфата железа происходит уже при комнатной
температуре, а при 100-120 °С протекает быстро по уравнению:
FeSО4·7H2ОТВ.→FeSО4 ·H2ОTB. + 6Н2Ог.
Разложение моногидрата сульфата оксида железа оксид железа (II)
начинается только выше 300°С, а при 400 °С происходит полностью. Одновре-менно
с дегидратацией идет окисление железа (II) в железо (III) [7]:
FeSО4·H2OТВ. + О2г→Fe2(SО4)3TB. + SО3r. + 4Н2Ог.
Разложение сульфата трехвалентного железа протекает при температуре
680-700 °С по уравнению:
Fe2(SО4)3 ↔ Fe2О3 + 3SО3
Первая стадия производства красного железооксидного пигмента из купороса
заключается в сушке исходного материала. При выборе осуществления этой операции
следует учитывать, что: 1) железный купорос уже при 64°С плавится и
растворяется в собственной кристаллизационной воде, а при дальнейшем нагревании
материал спекается в твердые куски, что затрудняет прокаливание; 2) для
производства серной кислоты может быть использован отходящий газ, содержащий
выделившиеся при прокаливании оксиды серы(IV) и (VI), если они не разжижены
водяным паром. По этим причинам обычно железный купорос вначале сушат до
моногидрата, а лишь затем обжигают с целью получения красного железооксидного
пигмента.
На обжиг следует подавать мелкий моногидрат, частицы которого должны быть
одинакового размера. Так как, при нагревании разложение начинается на
поверхности зерен, то превращение крупных частиц требует много времени, при
этом уже готовый гематит перекаливается и приобретает фиолетовый оттенок, в то
время как внутри зерен остается сульфат железа желто-зеленого цвета. [8]
Хорошо прокаленный материал содержит только 1-2 % растворимых в воде
солей. После промывки, сушки и измельчения он используется в качестве красного
железооксидного пигмента [8].
Получают красный железооксидный пигмент и дегидратацией желтого
железооксидного пигмента [2]:
FeO(OH) Fe2О3 + Н2О.
Красный железооксидный пигмент удовлетворительного цвета можно получить
также прокаливанием углекислого железа без перевода его в гидрат оксида железа
(II) [1].
Также красный железооксидный пигмент можно получить при прокаливании
оксида железа (II, III) (Fe3О4) (черный или коричневый железооксидный
пигмент). Окисление происходит при сравнительно низких температурах (275 - 300
°С) и протекает по реакции [1]:
(FeO·Fe2О3) + 0,5О2 → 3Fe2О3
Однако в этом случае, так же как и при прокаливании гетита, пигмент
хорошего цвета получается в результате прокаливания только при температуре выше
500 °С (при 600 - 700 °С).
Используется для получения красного железооксидного пигмента и осадочный
способ, аналогичный способу получения желтого. Основное отличие заключается в
методе синтеза зародышей, которые получаются при рН >11.
Синтез пигмента проводится в присутствии солей алюминия и цинка.
Назначение этих солей - предотвращение взаимодействия гидроксидов железа в
разных степенях окисления и образования смешанного оксида железа (II, III) -
магнетита [2].
Существуют также способы получения красного железооксидного пигмента из
суспензии магнетита или гетита, полученную восстановлением ароматического
нитропроизводного (например, нитробензола) [10], [11]. По этой технологии
получают пигмент, частицы которого имеют сферическую форму. Получают указанную
суспензию в присутствии кислого раствора соли железа (II) (например, хлорид
железа (II)). В течение нескольких часов при 20-90 °С добавляют раствор соли
алюминия или алюмината, при этом рН суспензии за это время изменяется с 3-5 до
5,5-6,5. Пигмент (гетит или магнетит) отделяют от суспензии и отмывают от
реакционной среды, а затем прокаливают при 600 - 1100 °С. В процессе окисления рН поддерживают при значении 3,5
регулированием подачи металлического железного лома. Процесс окисления ведут
48часов, окисляют воздухом при температуре 90 °С до образования суспензии
пигмента в количестве ≈200 г/л. Осадок пигмента отфильтровывают,
промывают и сушат при температуре ≤120 °С. Полученный продукт имеет
чистый красный цвет и содержит 96% оксида железа (Ш) (Fe2О3) и < 3% гетита. Для получения пигмента, состоящего из сферических частиц
диаметром 0,1 - 0,4 мкм и отличающегося повышенной красящей способностью
применяют способ [10], аналогичный [7] и [9]: пигмент получают восстановлением
ароматических нитросоединений солями железа (II), например железным купоросом,
являющегося побочным продуктом процесса получения диоксида титана. Сначала
смешивают водный раствор купороса, гидроксид щелочного металла (едкий натр) и
ароматическое нитросоединение (нитробензол, п- и о-нитротолуол, п- и
о-хлорнитробензол и др.) при температуре от 85-95 °С до температуры кипения
смеси при нормальном давлении; рН среды 7,5. Молекулярное отношение щелочи к
купоросу 1:1; отношение числа молей щелочи и эквивалентного числа молей
ароматического нитросоединения составляет 12:1. В результате взаимодействия
указанных соединений за 0,5 -3 часа получают суспензию, содержащую
приблизительно 40 г/л зерен пигмента, которые затем смешивают при температуре,
одинаковой с температурой 1-ой стадии, с водным раствором железного купороса,
ароматического нитросоединения и щелочи при рН среды 6-7,5. Молекулярное
отношение щелочи к железному купоросу 2:1; отношение числа молей щелочи к
эквивалентному числу молей ароматического нитросоединения также составляет
12:1. Получают суспензию, содержащую 110 г/л твердых частиц пигмента. Из
суспензии экстракцией с водяным паром выводят анилин. Затем после фильтрации,
промывки и сушки получают готовый красный железооксидный пигмент.
Также были поставлены опыты получения красного железооксидного пигмента
из осадка, образующегося при выщелачивании водой продуктов обезвоживания и
окисления железного купороса. Процесс выщелачивания осуществлялся в установке
со взвешенным слоем материала периодического действия. Щелочность воды была
такой, чтобы компенсировать кислотность от сульфата трехвалентного железа. Существует технология получения красного железооксидного
пигмента из пентакарбонила железа. Пентакарбонил железа (Fe(CO)5) представляет собой бесцветную жидкость плотностью 1453
кг/м и с температурой кипения 102,7 °С. При нагревании пентакарбонил железа
сгорает с образованием оксида железа (III) и углекислого газа:
Fe(CO)5 + 1302 →
2Fe2О3 + 20СО2
Пигмент, полученный по этому методу, отличается своей дисперсностью -
размер частиц пигмента приближается к размеру частиц сажи. Вследствие высокой
стоимости этого пигмента применение его ограничено - в основном он используется
для окраски изделий из резины и кож [1].
1.2.3 Коричневые железооксидные пигменты
Коричневые железооксидные пигменты представляют собой смесь красного и черного
оксидов железа, получаемых путем осаждения, прокаливания или механического
смешения. Иногда к коричневым железооксидным пиг-ментам относят также
гидратированный оксид железа (III), известный подназванием гидрогематита.
Цвет этих пигментов колеблется в широких пределах в зависимости от
соотношения между оксидом железа (II) и оксидом железа (III), а в случае
гидрогематитов - от содержания воды. Во всех случаях на цвет пигмента оказывает
большое влияние физическое состояние частиц [2].
Коричневые железооксидные пигменты характеризуются, как правило, меньшей
длинной волны, т.е. меньшим содержанием красного компонента; оттенок их в
разбеле (при смешении с белилами в соотношении, например 1:10) колеблется от
желтоватого до холодного синеватого.
По своим свойствам коричневые железооксидные пигменты близки к другим
железооксидным пигментам - их плотность колеблется в пределах 4,4-4,5 г/см ,
маслоемкость 17-25 г/100г. По укрывистости пигменты делятся на две группы:
укрывистые (укрывистость 4-20 г/м) и прозрачные, или лессирующие (укрывистость
более 50 г/м2). Красящая способность всех железооксидных пигментов,
как правило, довольно высокая и обусловлена размером частиц, лежащим обычно в
интервале 0,1-1 мкм [11].
Технические требования к коричневым железооксидным пигментам разнообразны
и зависят от целевого назначения пигмента.
Коричневые железооксидные пигменты на основе смеси оксидов и гидроксидов
железа в зависимости от соотношения компонентов имеют различные оттенки.
Компонентами смесей являются: гидроксид железа а-Fe2OOH
(гетит) желтого цвета, смешанный оксид железа (II) и (III) - Fe2О3 (магнетит) черного
цвета, оксид железа (III)
а-Fe2О3 (гематит) красно-коричневого цвета.
Коричневые железооксидные пигменты обладают высокой дисперсностью, хорошей
красящей способностью и укрывистостью, светостойкостью и стойкостью к щелочам,
однако, благодаря присутствию желтого гидроксида железа, они не кислостойки.
Средний размер частиц 0,25- 0,75 мкм. Наличие нетермостойких компонентов -
гидроксида железа и оксида железа (II), претерпевающих полиморфное превращение
в оксид железа (III) при температуре 200 °С, обуславливает низкую
термостойкость пигмента: при температуре выше 180 °С начинается изменение
цвета. [11]
Коричневые железооксидные пигменты этого типа применяются для
изготовления эмалей или в смеси с наполнителями - дешевых красок и грунтовок.
) Коричневые пигменты на основе смеси оксидов железа и других металлов.
Хорошо известны коричневые пигменты, основой которых является смесь
оксидов железа и других металлов ( марганца, хрома, меди, никеля, кобальта и
др.). Многие термостойкие коричневые железооксидные пигменты содержат марганец.
Содержание диоксида марганца в составе пигмента колеблется от 1 до 20 %.
Пигменты получают из водных растворов сульфатов железа (II) и марганца
осаждением основаниями при рН 3,5-6,5 с окислением воздухом, а также окислением
смеси металлического железа и марганца ароматическими нитросоединениями в
присутствии растворов сульфатов железа (II) и марганца. Осадки промывают, сушат
и прокаливают при температуре 600-800 °С. При соотношении Fe:Mn от 10:1 до 50:1 получаются коричневые пигменты различных
оттенков. Эти пигменты обладают насыщенным коричневым цветом, хорошими
пигментными свойствами (красящей и кроющей способностью) и высокой
термостойкостью. [11]
Коричневые железо-хромовые пигменты получают восстановлением хроматов или
дихроматов в растворе солями железа (II) и осаждением щелочью смешанных
гидроксидов железа (III) и хрома (III). Осажденные продукты промывают, сушат и
прокаливают при температуре 500-900°С.
Пигменты на основе смеси оксидов в большинстве случаев по составу
представляют собой механическую смесь этих оксидов. Однако иногда при
соосаждении и прокаливании гидроксидов происходит взаимодействие гидроксида
железа с гидроксидом металла с образованием феррита. Как правило, ферриты
образуются лишь при высокой температуре (порядка 800°С и выше). При
прокаливании соосажденных гидроксидов образование ферритов происходит при более
низкой температуре, чем при прокаливании механической смеси оксидов. Так, в
системе с гидроксидами меди, цинка и магния соответствующие ферриты образуются
при температуре 400-500°С [11]
) Коричневые пигменты на основе гидратированного оксида железа.
К коричневым железооксидным пигментам относят гидратированный оксид
железа (гидрогематит). Он образуется при взаимодействии растворов солей железа
(III) с растворами щелочей и имеет состав Fe2О3. nH2О, где n может в зависимости от условий осаждения принимать различные
значения. Наиболее устойчивым является моногидрат.
Пигменты на основе гидратированного оксида железа имеют коричневый цвет с
желтым оттенком, зависящим от условий осаждения, и благодаря очень малым
размерам частиц, обладают лессирующей способностью.[11]
) Пигменты на основе γ-оксида железа
Кроме широко распространенного под названием "красный железооксидный
пигмент" α-оксида железа известны другие кристаллические модификации
оксида железа, из которых γ-Fe2О3 и α-Fe2О3 обладают коричневым цветом.
Структура γ-Fe2О3 является переходной
между структурами магнетита и гематита:
2О3
→
γ - Fe2О3 →α- Fe2О3
Малярно-технические свойства γ-Fe2О и α-Fe2О3 довольно близки, но у гамма-формы несколько
большая удельная поверхность и соответственно более высокая маслоемкость 35
г/100 г; плотность 4900 кг/м3.
Пигмент обладает хорошими пигментными свойствами, высокой термостойкостью
[11].
В заключение можно заметить, что если технологии синтеза красных и желтых
ЖОП достаточно отработаны, то получение коричневых пигментов вызывает
определенные трудности. Кроме того, цветовая гамма их ограничена. Использование
шунгита как черного пигмента в смесях, или углерода, содержащегося в нем, как
восстановителя, может обеспечить получение коричневых железооксидных пигментов
и расширить цветовую гамму неорганических пигментов. В связи с этим цель работы
является актуальной.
2. Объекты и методы исследования
.1 Объекты исследования
В качестве объектов исследования были выбраны шунгит марки Т-20, желтый
железоокисный пигмент, красный железоокисный пигмент. В качестве
вспомогательных веществ использовали раствор поливинилового спирта, диоксид
титана марки Kemira R-706, льняное масло, ксилол, лак ПФ-283, лак МЛ-0197.
.1.1 Шунгит марки Т-20.
Свойства используемого шунгита представлены в таблице 2.1.
Таблица 2.1 - Физико-химические показатели шунгита марки Т-20
|
Наименование показателя
|
Величина показателя
|
|
Насыпная плотность, г/дм3
|
500-600
|
|
Влагосодержание, %
|
0,5-1,5
|
|
Потери при прокаливании, %
|
8-14
|
|
Массовая доля остатка на
сите №0045
|
Менее 0,08
|
|
Маслоемкость, г/100г
|
26,5
|
|
Укрывистость, г/м2
|
48,2
|
|
рН водной вытяжки
|
3,56
|
|
Плотность пигмента, г/см3
|
2,08
|
|
Содержание водорастворимых
солей, %
|
2,97
|
.1.2 Желтый железоокисный пигмент
Желтый железоокисный пигмент использовали в виде водной пасты с влажностью
(58,5 ±2) %. Некоторые свойства желтого железооксидного пигмента представлены в
таблице 2.2.
Таблица 2.2 -Свойства желтого железооксидного пигмента
|
Свойства
|
Показатели
|
|
Укрывистость, г/м2
|
10-12
|
|
Маслоемкость, г/100г
|
40-60
|
|
Удельная поверхность, м2/г
|
11,2
|
|
Насыпной вес, г/л
|
420-550
|
|
Средняя величина частиц,
мкм
|
0,2-0,6
|
.1.3 Красный железоокисный пигмент
Таблица 2.3 - Свойства красного железооксидного пигмента
|
Свойства
|
Показатели
|
|
Плотность, кг/м3
|
4500-5000
|
|
рН водной вытяжки
|
5,5-7,0
|
|
Насыпной объем, Vнас-103
, м3 /кг
|
2,2-2,4
|
|
Маслоемкость, г/100 г
|
25-35
|
|
Укрывистость, г/м2
|
6-8
|
.1.4 Вспомогательные вещества
Поливиниловый спирт, ГОСТ 10779-78;
Льняное масло, ГОСТ 7931-76;
Ксилол, ГОСТ 9410-7;
Ацетон, ГОСТ 2768-84;
Лак ПФ-283 по ГОСТ 5470-75
Основные показатели лака ПФ-283 представлены в таблице 2.2.
Таблица 2.4 - Основные показатели лака ПФ-283
|
Наименование показателей
|
Норма по ГОСТ
|
|
Цвет лака по
йодометрической шкале, мгI2/100 см3,
не темнее
|
130
|
|
Внешний вид пленки
|
Однородная прозрачная, без посторонних
включений
|
|
Блеск пленки по
фотоэлектрическому блескомеру, % не менее
|
80
|
|
Условная вязкость по
вязкозиметру тапа ВЗ-246 с диаметром сопла 4 мм при температуре (20,0±0,5) оС,
с
|
40-60
|
|
Массовая доля нелетучих
веществ, %
|
50±2
|
|
Время высыхания до степени
3, ч., не более - при температуре (20±2) оС - при температуре
(60±2) оС
|
36 3
|
|
Эластичность пленки при
изгибе, мм, не более
|
1
|
|
Твердость пленки по
маятникову прибору типа М-3, условные единицы, не менее
|
0,35
|
|
Стойкость пленки к
статическому воздействию воды при температуре (20±2) оС, ч., не
менее
|
8
|
Лак ПФ-283 представляет собой раствор алкидных смол, модифицированных
растительными маслами, жирными кислотами растительных масел и продуктов их
переработки, дистиллированными жирными кислотами таллового масла и
дистиллированным талловым маслом в органических растворителях с добавлением
сиккатива марки НФ-1.
Лак МЛ-0197 по СТП 6-10-200-272-87.
Основные показатели лака МЛ-0197 приведены в таблице 2.5
Таблица 2.5 - Основные показатели лака МЛ-0197
|
Наименование показателей
|
Норма по СТП
6-10-200-272-87
|
|
Цвет лака по
йодометрической шкале, мгI2/100 см3,
не темнее
|
80
|
|
Внешний вид пленки
|
Однородная прозрачная
жидкость
|
|
Условная вязкость при
температуре (20±0,5)°С по вискозиметру типа ВЗ-246 с диаметром сопла 4 мм,
с
|
100-150
|
|
Чистота лака
|
Слой лака, нанесенный
наливом на стеклянную пластинку, должен быть прозрачным и не иметь
механических примесей
|
|
Массовая доля нелетучих
веществ, %
|
63,5±2
|
|
Кислотное число в пересчете
на массовую долю нелетучих веществ, мгKOH/г, не
более
|
18,0
|
|
Твердость пленки лака,
относительные еденицы, не менее, по маятникову прибору типа ТМЛ (маятник А)
По маятникову прибору типа М-3, условные еденицы
|
0,20
|
|
0,5
|
Представляет собой раствор в смеси органических растворителей полиэфира
глицерина, триметилопропана и фталевого ангидрида, модифицированный касторовым,
кокосовым маслами и бензойной кисло-той с добавлением меламино-формальдегидной
смолыК-423-02. Применяется для производства автоэмалей.
.2 Методы исследования
.2.1 Определение цвета пигмента
Цвет пигмента определяется по ГОСТ 5233-67 с помощью спектрофотометров
"Радуга 2М" и "Пульсар". Для определения цвета делалась
накраска из дисперсии пигмента в растворе поливинилового спирта на плотной
чертежной бумаге. Накраска высушивалась при комнатной температуре, после чего
снимался спектр отражения. Расчет координат цвета проводился методом взвешенных
ординат по спектру отражения[12].
.2.2 Определение маслоемкости
Маслоемкость пигментов определялась по ГОСТ 21119.8-75. На аналитических
весах взвешивали тигель с точностью 0,01 г. В тигель помещали пигмент на 1/3
высоты и снова взвешивали. Капельницу с льняным маслом взвешивали с точностью
до 0,01 г. Перемешивая пигмент стеклянной палочкой с округленным концом,
вводили по 4-5 капель масла, тщательно перемешивая массу после каждой порции
масла. Перемешивание следует проводить с максимальным усилием, добиваясь
истирания массы под давлением. После образования неслипающихся комочков
пигмента их собирали в большой комок однородной, некрошащейся и нерастекающейся
пасты [12]. Общее время перемешивания 20-25 мин.
Расчет маслоемкости пигмента вели по формуле:
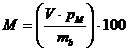 или
или 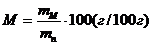
где - V-объем израсходованного масла, мл
mп - навеска пигмента, г
рм - плотность льняного масла (0,93 г/см3 )
.2.3 Определение укрывистости
Укрывистость определялась по ГОСТ 8784-75. Взвешивали от 2 до 3 г
пигмента с точностью до 0,01 г. Взвешивали капельницу с льняным маслом. Пигмент
растирали с маслом на плите курантом до малярной консистенции. На
предварительно взвешенную стеклянную пластинку наносили краску движениями кисти
вдоль и поперек пластинки так, чтобы получить слой краски равномерной толщины.
Выдержав пластинку до исчезновения штрихов от кисти, ее накладывали на горизонтально
расположенную непрозрачную подложку вида шахматной доски с белыми и черными
квадратами. Просвечивание через слой краски белых и черных квадратов
рассматривалось при рассеянном дневном свете или дневном свете. Толщину слоя
краски увеличивали постепенно до тех пор, пока визуально под слоем краски
полностью не исчезали белые и черные квадраты. Достигнув полного укрытия,
удаляли подтеки краски с обратной стороны и ребер пластинки и взвешивали ее с
точностью до 0,01 г [12].
Расчет проводили по формуле:
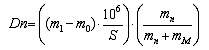
где m1- масса пластинки со слоем краски, г
m0- масса неокрашенной пластинки, г
mп - навеска пигмента, израсходованного
при получении краски, г
mм- навеска льняного масла,
израсходованного при получении краски, г
S -
площадь поверхности укрытой пластинки, мм
.2.4 Определение плотности пигмента пикнометрическим методом
Плотность определяли по ГОСТ 21119.5-75. Плотность пигмента определялась
с помощью стеклянного пикнометра вместимостью 5-10 мл, в качестве смачивающей
жидкости использовался уайт-спирит.
Предварительно исследуемый пигмент и тщательно вымытый пикнометр
высушивали при 105 °С до постоянной массы. Пикнометр взвешивали с точностью до
0,0002 г, наполняли пигментом приблизительно до половины его объема и снова
взвешивали с точностью до 0,0002 г. Затем с помощью пипетки в пикнометр с
пигментом добавляли уайт-спирит, осторожно встряхивая содержимое пикнометра, в
таком количестве, чтобы над поверхностью пигмента образовался слой жидкости
высотой 5-7 мм. Пикнометр закрывали пробкой и для удаления пузырьков воздуха из
суспензии пигмента помещали в водяную баню, нагретую до 60 °С.
Через 1-1,5 ч. пикнометр вынимали из бани, охлаждали до 20 °С в водяном
термостате, доливали немного выше метки уайт-спиритом и снова выдерживали при
20 °С в течение 1 часа. По истечению указанного времени пикнометр вынимается из
термостата, тщательно обтирается фильтровальной бумагой, доводится до метки
уровень уайт-спирита, обтирая излишек кусочками фильтровальной бумаги, и
взвешивается с точностью до 0,0002 г. Затем пикнометр, вымытый и высушенный при
105 °С до постоянной массы, заполняли уайт-спиритом немного выше метки,
выдерживали в водяном термостате при 20 °С в течение 30 мин, доводили уровень
жидкости до метки так же, как было указано выше, насухо вытирали пикнометр и
взвешивали с точностью до 0,0002 г [12].
Плотность пигмента рп (в г/см ) вычисляли по формуле:
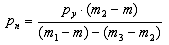
где m - масса пустого пикнометра, г;
m1- масса пикнометра с уайт-спиритом,
г;
m2- масса пикнометра с пигментом, г;
m3 - масса пикнометра с пигментом и
уайт-спиритом, г;
ру- плотность уайт-спирита, г/см .
.2.5 Дериватографический анализ
Дериватографические исследования образцов проводились с использованием
дериватографа Q-1500 D, системы Паулик, Паулик и Эрдей.
Дериватограф представляет собой комплексное
термоаналитическое устройство. В процессе исследования одновременно измеряется
температура (Т), изменение массы (ТГ), скорость изменения массы (ДТГ) и
изменение содержания тепла (ДТА) исследуемого вещества в зависимости от
времени.
Применяя дилатационный адаптер, можно измерять
териодилатационное изменение длины (ТД) и скорость термодилатационного
изменения длины (ДТД).
Дериватограф Q-1500 D позволяет проводить обычные
термоаналитические исследования в сканирующем и изотермических режимах до
температуры 1500°С, а также пригоден для квази-изотермических и квази-изобарных
ТГ исследований до 1000°С. Квази-изотермическое и квази-изобарное измерение ТГ
обеспечивает значительно большую селективность, по сравнению о традиционным
методом. Кроме того, полученный результат не зависит от большого количества
условий исследования, которые при обычных термоаналитическпх исследованиях
значительно влияют на температуру ступени. Запись
дериватограмм производится с помощью шестиканального универсального
регистратора, обеспечивающего возможность регистрации результатов в зависимости
от времени или от температуры.
Исследование образцов проводилось в открытом
корундовом тигле или в платиновом лабиринтном тигле (закрытом). Для нагрева
использовалась печь с температурой до 1000 ºС, скорость изменения температуры 10
градусов в минуту, чувствительность прибора по изменению массы - 100 мг на
шкалу.
Навеска массой 250-300 мг помещалась в выбранный
тигель. В тигель сравнения помещалась навеска оксида алюминия. Тигли
устанавливались на термоизмерительную систему и закрывались кварцевым стаканом,
для исключения влияния на измерения массы конвекционных потоков. На
термоизмерительную систему опускалась печь, включалась программа нагрева и
образец нагревался до температуры 850 ºС. В процессе нагрева одновременно
фиксировались температура образца, изменение массы образца, скорость изменения
массы образца и изменение содержания тепла.
.2.6 Получение лакокрасочных покрытий методом налива
Лакокрасочный материал наносился на стеклянные, металлические, жестяные
пластины методом налива в один слой. Подготовленную стеклянную пластину одной
рукой держат за края горизонтально над ванночкой, а другой наливают эмаль из
стакана на 1/4 часть поверхности пластины. Затем пластина поворачивается и
устанавливается в вытяжном шкафу под углом 45° в таком положении чтобы эмаль,
нанесенная на верхнюю часть пластины, растекалась по пластине в течение 10 мин.
После чего помещали пластинку на горизонтальную поверхность.
Отверждение покрытий на основе лака ПФ-283 производили при температуре 20
°С в течении 24 часов. Покрытия на
основе лака МЛ-0197 отверждали при температуре (105±2) °С в течение 45 минут.
2.2.7 Определение прочности лакокрасочных покрытий при ударе
Определение прочности лакокрасочных покрытий при ударе проводили с
помощью прибора У1-А. Метод основан на мгновенной деформации образца
(металлической пластины с покрытием) при свободном падении на него груза.
Прочность пленки при ударе выражают произведением величины груза (Н) на
максимальную высоту (м), с которой падает груз, не вызывая механических
разрушений пленки. За результат испытания принимают среднее арифметическое трех
параллельных определений, отклонение величины которых от среднего арифметического
не должны превышать 2 см.
.2.8 Определение относительной твердости пленок
Относительную твердость пленок определяли с помощью маятникового прибора
ТМЛ-2141 (тип А) в соответствии с ГОСТ 5233-89 (ISO 1522) [12].
Относительную твердость покрытия рассчитывали по формуле:
Т=n/ncn ,
где Т - относительная твердость;
n -
количество колебаний маятника на пленке;
nст
- количество
колебаний маятника на стекле
.2.9 Определение адгезионной прочности покрытия методом решетчатых
надрезов
Адгезию лакокрасочных покрытий оценивали методом решетчатых надрезов по
ГОСТ 15140-78.
Метод заключается в оценке степени прилипания лакокрасочной пленки к
подложке по числу ячеек, отслоившихся от подложки после нарезания пленки.
На поверхности покрытия бритвой по линейке наносили не менее пяти
параллельных надрезов до подложки на расстоянии 1 мм друг от друга (для
покрытий толщиной до 60 мкм). Столько же аналогичных надрезов делали
перпендикулярно первым. На покрытии образовывалась решетка из квадратов
одинакового размера. После нанесения квадратов очищали пленку от отслоившихся
кусочков пленки мягкой кистью.
Адгезию покрытия к подложке оценивали по состоянию надрезов на покрытии в
баллах (по четырехбалльной системе) в соответствии со шкалой, приведенной ниже.
Таблица 2.6 - Шкала оценки адгезии
|
Края надрезов должны быть
гладкими, кусочков отслоившихся покрытий не наблюдается
|
1
|
|
Незначительное отслаивание
покрытий в виде точек вдоль линии надреза или в местах их пересечения
|
2
|
|
Отслаивание покрытий вдоль
линии надрезов или полос (до 35 % поверхности с каждой решетки)
|
3
|
|
Полное или частичное
отслаивание покрытий полосами или квадратами вдоль линий надрезов (более 35%
поверхности с каждой решетки)
|
4
|
За результат принимали среднее значение балла, полученного при испытании
не менее двух образцов и на трех участках поверхности каждого образца.
.2.10 Определение эластичности пленки при изгибе
Эластичность лакокрасочного покрытия определяли в соотвествии с
требованими ГОСТ 6806-73 при помощи шкалы гибкости ШГ-1.
Метод заключается в определении минимального диаметра металлического
цилиндрического стержня, изгибание на котором окрашенной металлической
пластинки не вызывает механического разрушения или отслаивания однослойной или
многослойной лакокрасочной пленки.
Пластинку накладывают на стержень наибольшего диаметра покрытием наружу
и, плотно прижимая ее к стержню, плавно изгибают в течение 1 - 2 с на 180°
вокруг стержня, затем покрытие в месте изгиба рассматривают в лупу на наличие
трещин и отслаивания. Если эти дефекты отсутствуют, то производят изгибание
пластинки каждый раз в другом месте последовательно от стержня большего
диаметра к меньшему до тех пор, пока не будут обнаружены указанные выше
дефекты.
За результат испытания принимают минимальный диаметр стержня в
миллиметрах, при изгибании образца на котором испытуемая пленка осталась
неповрежденной. Результат испытания должен совпадать не менее, чем для двух
испытуемых пластинок, если совпадение не достигнуто, испытание повторяют на
шести образцах.
3. Результаты и их обсуждение
Среди неорганических пигментов железооксидные пигменты получили
наибольшее распространение. Существующие технологии позволяют получать пигменты
красных, желтых, коричневых и черных цветов. Если технологии синтеза красных и
желтых ЖОП достаточно давно освоены, то в производстве коричневых и черных
существуют определенные трудности. Как правило, их получают смешением черных и
красных пигментов, или частичным восстановлением трехвалентного железа в
смешанном оксиде Fe3O4.
В тоже время, благодаря доступности, относительной дешевизне и
физико-химическим свойствам, наметилась тенденция использования в качестве
наполнителя в лакокрасочных материалах природного минерала шунгита. Сочетание
кислотно-основных свойств поверхности позволяет ему совмещаться со многими
пленкообразователями, а углерод, входящий в его состав, может быть
восстановителем металлов при синтезе новых пигментов.
Целью настоящей работы является получение коричневых железооксидных
пигментов и изучение их свойств.
Для достижения поставленной цели необходимо было изучить:
– свойства смешанных композиций желтого железоокидного пигмента и
шунгита и возможность получения коричневых пигментов при прокалке таких смесей;
– влияние температуры и времени прокалки на цвет и свойства
получаемых пигментов;
– возможность получения и свойства лакокрасочных покрытий,
наполненных такими пигментами;
На начальном этапе выполнения работы были получены механические смеси
желтого ЖОП с шунгитом в различном соотношении и исследованы их основные
свойства. Затем полученные смеси подвергались прокалке без доступа кислорода
при различной температуре и в течение различного времени. У полученных
пигментов определялись цветовые характеристики, физико-химические свойства и
влияние различных факторов на них.
Также с применением синтезированных пигментов были получены
пигментированные лакокрасочные материалы и покрытия на их основе. У покрытий
были определены основные свойства.
.1 Исследование свойств смесей желтого железооксидного пигмента и шунгита
С целью изучения возможности получения коричневых пигментов механическим
смешением черного шунгита и желтого железооксидного пигмента были приготовлены
их композиции в различном соотношении. Для более равномерного распределения
частиц пигмента по объему смешение компонентов производилось в виде водных
суспензий.
Предварительно была определена рабочая концентрация шунгита в суспензии.
При заданных оборотах мешалки в воду постепенно засыпался шунгит до получения
суспензии с вязкостью, позволяющей реализовать эффективное перемешивание. Рабочая
концентрация шунгита в водной суспензии составила 30 %.
Водные суспензии шунгита и желтого ЖОП смешивали в различных соотношениях
между компонентами. Суспензия перемешивалась в течении 30 минут, после чего
отфильтровывалась через воронку Бюхнера и высушивалась до постоянной массы при
температуре (102±2) оС. У высушенной композиции определяли цвет и
некоторые физико-химические показатели.
Физико-химические характеристики полученных композиций представлены в
таблице 3.1.
Таблица 3.1 Физико-химические показатели смесей желтого железооксидного
пигмента и шунгита
|
Содержание шунгита, %
|
100
|
80
|
54
|
46
|
20
|
0
|
|
Маслоемкость, г /100 г
|
26,5
|
40,56
|
42,67
|
43,55
|
48,22
|
40-60
|
|
pH водной вытяжки
|
3,56
|
4,58
|
3,72
|
4,06
|
4,61
|
-
|
|
Насыпная плотность, г/см3
|
0,6
|
0,597
|
0,472
|
0,449
|
0,398
|
0,43
|
Как видно из таблицы, с увеличением содержания желтого ЖОП маслоемкость
смешанного пигмента увеличивается и приближается к величине маслоемкости
желтого железооксидного пигмента. Насыпная плотность смешанного пигмента
уменьшается и стремится к величине насыпной плотности желтого пигмента. Т.е. в
результате образуется физическая смесь двух разных пигментов, свойства которой
зависят от доли одного из компонентов.
В таблице 3.2 представлены координаты цвета полученных смесей. На рисунке
3.1 представлены спектры диффузного отражения, на рисунке 3.2 представлено
расположение векторов цвета исследуемых композиций в плоскости а*-b*.
Таблица 3.2 - Координаты цвета полученных пигментов
|
Содержание шунгита, %
|
L*
|
a*
|
b*
|
C
|
h
|
|
0
|
68,55
|
8,90
|
64,75
|
65,36
|
82,17
|
|
20
|
59,46
|
3,12
|
51,38
|
51,48
|
86,52
|
|
46
|
54,93
|
-2,74
|
42,79
|
42,87
|
93,66
|
|
54
|
46,42
|
-4,23
|
30,40
|
30,69
|
97,91
|
|
80
|
35,20
|
-5,43
|
11,78
|
12,97
|
114,72
|
|
100
|
26,04
|
-4,14
|
6,74
|
7,91
|
121,54
|
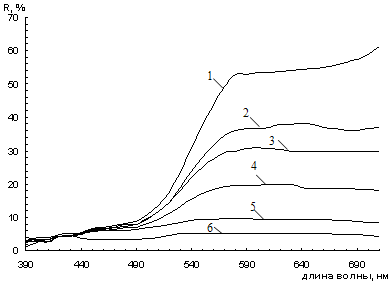
Рисунок 3.1 - Спектры диффузного отражения смесей железооксидного
пигмента с шунгитом при его различном содержании (1 - 0 %, 2 - 20 %, 3-46%, 4 -
54%, 5 - 80%, 6 - 100%).
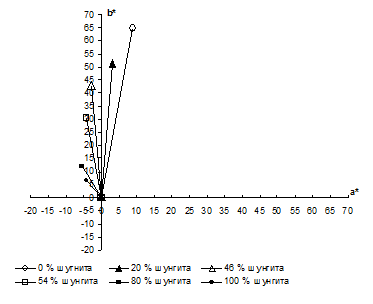
Рисунок 3.2 - Расположение векторов цвета полученных композиций на
диаграмме цветности CIEL*a*b*
Из приведенных данных следует, что увеличение содержания шунгита в
смешанном пигменте приводит к уменьшению коэффициента отражения в
длинноволновой области, снижению насыщенности цвета пигмента и смещению
цветового тона в зеленую область за счет увеличения поглощения падающего
излучения шунгитом. Поглощение света и цвет полученной композиции зависит
только от соотношения между компонентами.
Для определения влияния рассеивающей и поглощающей способности частиц
шунгита на цвет получаемых композиций было рассчитано значение функции
Гуревича-Кубелки-Мунка (ГКМ) в зависимости от длины волны при различном
содержании шунгита в композиции.
На рисунке 3.2 представлена зависимость функции ГКМ от длины волны, на
рисунке 3.3 представлена зависимость функции ГКМ при длине волны 600 нм от
содержания шунгита в композиции.
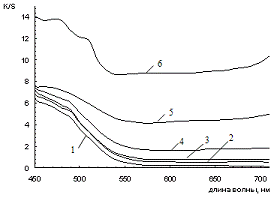
Рисунок 3.2 - Зависимость функции ГКМ от длины волны для смесей желтого
железооксидного пигмента с шунгитом при различном его содержании (1 - 0 %, 2 -
20%, 3-46%, 4-54%, 5-80%, 6-100%).
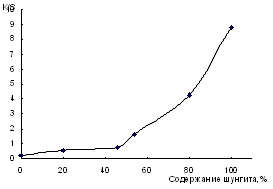
Рисунок 3.3 - Зависимость функции ГКМ от доли шунгита в пигменте при
длине волны 600 нм.
С увеличением содержания шунгита происходит увеличение значения функции
ГКМ в длинноволновой области (рисунок 3.2), что связано с преобладанием
поглощения света частицами шунгита над отражением света частицами желтого ЖОП.
Резкое изменение значения функции ГКМ (рис 3.3) происходит при содержании
шунгита с 45 %. При этом соотношении имеет место инверсия оптических свойств
системы пигмент-воздух, что связано с изменением перекрытия рассеяния света
гетита частицами шунгита. Точка инверсии определяется соотношением между
дисперсностей и плотностей компонентов.
Таким образом, в результате механического смешения желтого
железооксидного пигмента с шунгитом не удается получить коричневые пигменты с
достаточной чистотой цвета и требуемым цветовым тоном.
.2 Получение коричневых пигментов из смесей шунгита с желтым
железооксидным пигментом
Из литературных данных известно, что при прокалке желтого железоокисного
пигмента при температуре 600-700 °С протекают процессы дегидратации, пигмент переходит в оксид
железа (III) и приобретает красный цвет.
Известно также, что при прокалке шунгита при температуре 500-600 °С происходит окисление углерода,
содержащегося в минерале, кислородом воздуха с образованием двуокиси углерода.
В отсутствии доступа воздуха углерод шунгита может быть восстановителем,
например, может восстанавливать оксид кремния до металлического кремния [1].
Поэтому следует ожидать, что в процессе прокалки смесей желтого
жжелезооксидного пигмента с шунгитом при температурах 600-800 °С без доступа кислорода воздуха будет
происходить как дегидратация желтого пигмента, так и восстановление
трехвалентного железа до двухвалентного углеродом, входящим в состав шунгита. В
результате возможно образование окиси-закиси железа черного цвета и получение
коричневых пигментов.
Это предположение можно подтвердить данными дериватографических
исследований процесса прокалки смесей железооксидных пигментов с различным
содержанием шунгита в открытом и закрытом тиглях (при доступе кислорода воздуха
и без доступа кислорода).
На рисунках 3.4-3.7 представлены дериватограммы процесса прокалки
композиций с различным содержанием шунгита, на рисунках 3.8 и 3.9 -
дериватограммы процессо прокалки желтого железооксидного пигмента и шунгита
соотвественно.
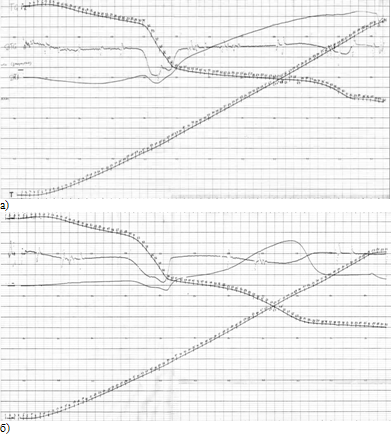
Рисунок 3.4 - Дериватограмма прокалки пигмента с содержанием шунгита 20%
в закрытом (а) и в открытом (б) тиглях.
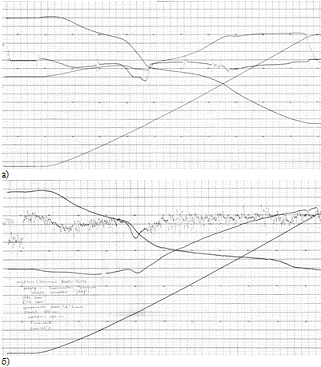
Рисунок 3.5 - Дериватограмма прокалки пигмента с содержанием шунгита 46%
в закрытом (а) и в открытом (б) тиглях.
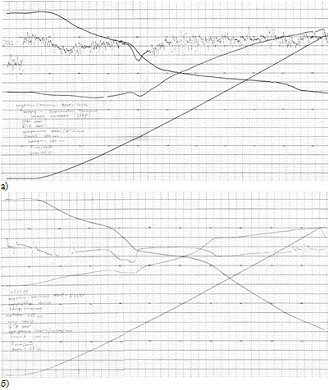
Рисунок 3.6 - Дериватограмма прокалки пигмента с содержанием шунгита 54%
в закрытом (а) и в открытом (б) тиглях.
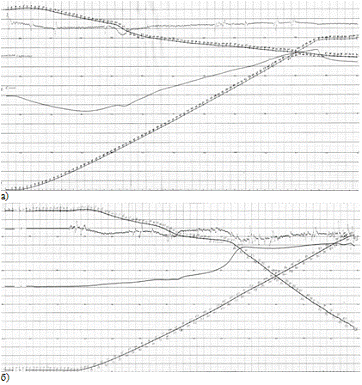
Рисунок 3.7 - Дериватограмма прокалки пигмента с содержанием шунгита 80%
в закрытом (а) и в открытом (б) тиглях.
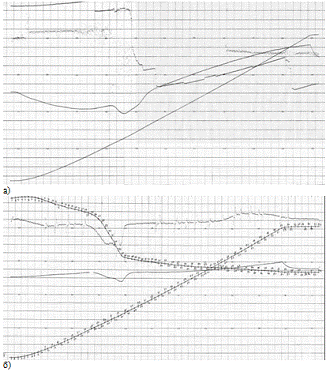
Рисунок 3.8 - Дериватограмма прокалки желтого железооксидного пигмента в
закрытом (а) и в открытом (б) тиглях.
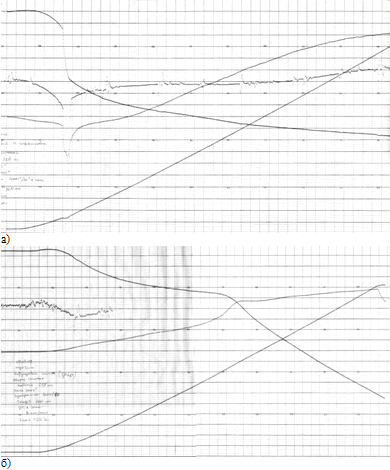
Рисунок 3.9 - Дериватограмма прокалки шунгита закрытом (а) и в открытом
(б) тиглях.
Из рисунка 3.8 можно заметить, что в процессе прокалки желтого ЖОП при
температуре 240-250 °С
наблюдается эндотермический эффект, сопровождающийся потерями массы. Согласно
литературным данным, именно при этой температуре начинается дегидратация
желтого железооксидного пигмента [1]. Небольшой экзотермический эффект в начале
процесса (рисунок 3.8б) соответствует окислению двухвалентного железа, в
небольшом количестве присутствующего в желтом ЖОП, кислородом воздуха до
трехвалентного. При прокалке без доступа кислорода (рисунок 3.8 а) такой эффект
не наблюдается.
При прокалке смешанных композиций в открытом тигле (рисунок 3.4-3.7 б)
также наблюдаются эндо-эффекты в области температур 90-150 °С и экзо-эффекты с потерями массы в
области 240-340 °С.
С увеличением доли желтого железоокисного пигмента тепловой эффект становится
более выраженным. При прокалке смеси в закрытом тигле наблюдается только
эндотермический тепловой эффект, связанный с началом дегидратации желтого
пигмента (рисунки 3.4-3.7 а).
В диапазоне температур 500-600 °С при прокалке в открытом и в закрытом тиглях наблюдается еще
один экзотермический эффект, также сопровождающийся потерями массы. Но при
использовании открытого тигля потери массы более значительные, чем при
использовании закрытого тигля. Потери массы увеличиваются за счет окисления углерода
шунгита кислородом воздуха и удалением углекислого газа. Такое предположение
также подтверждается дериватограммой прокалки шунгита в открытом тигле (рисунок
3,9 б): при температуре 500-550 °С происходит существенная потеря массы.
Для изучения влияния температуры и времени прокалки на цвет и свойства
синтезируемого пигмента смешанные композиции желтого железооксидного пигмента и
шунгита прокаливали в муфельной печи при различной температуре и времени. Смесь
шунгита и желтого железооксидного пигмента засыпали в тигель, плотно
закупоривали асбестовой тканью и асбестокартоном и прокаливали в муфельной
печи. После прокалки тигель охлаждали, пигмент пересыпали в чашку Петри и
анализировали его свойства.
Из полученных при различной температуре пигментов делались накраски и
снимался спектр отражения. На рисунке 3.10-3.13 приведены спектры отражения
пигментов с различным содержанием шунгита в зависимости от температуры
прокалки. Время прокалки 20 минут.
В таблице 3.3 представлены цветовые характеристики полученных пигментов.
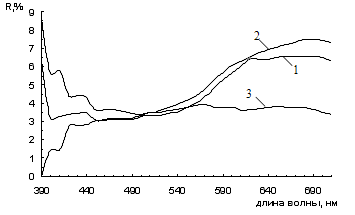
Рисунок 3.10 - Спектры отражения пигментов, полученных прокаливанием
желтого железооксидного пигмента с шунгитом при соотношении 20: 80, при
различной температуре (1 - 600 °С, 2 - 700 °С,
3 - 800 °С).
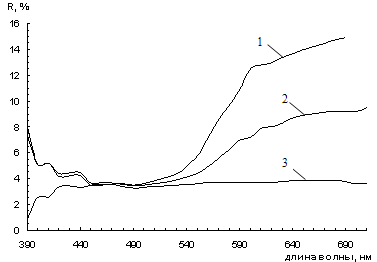
Рисунок 3.11 - Спектры отражения пигментов, полученных прокаливанием
желтого железооксидного пигмента с шунгитом при соотношении 54:46 при различной
температуре (1 - 600 °С,
2 - 700 °С, 3 - 800 °С).
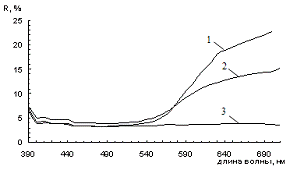
Рисунок 3.12 - Спектры отражения пигментов, полученных прокаливанием
желтого железооксидного пигмента с шунгитом при соотношении 46:54 при различной
температуре (1 - 600 °С,
2 - 700 °С, 3 - 800 °С)
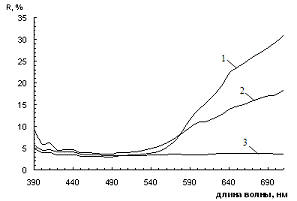
Рисунок 3.13 - Спектры отражения пигментов, полученных прокаливанием
желтого железооксидного пигмента с шунгитом при соотношении 20:80 при различной
температуре (1 - 600 °С,
2 - 700 °С, 3 - 800 °С).
Таблица 3.3 - Координаты цвета пигментов, синтезированных прокалкой смеси
желтого железооксидного пигмента и шунгита
|
Содержание шунгита, %
|
Координаты цвета в системе CIEL*a*b*
|
|
L*
|
a*
|
b*
|
C
|
h
|
|
Т=600оС
|
|
20
|
33,44
|
23,20
|
21,87
|
31,88
|
43,31
|
|
46
|
31,01
|
17,01
|
15,98
|
23,34
|
43,22
|
|
54
|
29,19
|
13,61
|
23,03
|
36,21
|
|
80
|
23,41
|
0,94
|
6,53
|
6,60
|
81,81
|
|
Т=700оС
|
|
20
|
32,09
|
13,28
|
14,26
|
19,49
|
47,04
|
|
46
|
31,45
|
13,23
|
12,36
|
18,10
|
43,04
|
|
54
|
27,87
|
9,15
|
7,82
|
12,04
|
40,49
|
|
80
|
25,98
|
5,49
|
8,83
|
10,40
|
58,15
|
|
Т=800оС
|
|
20
|
21,72
|
1,85
|
-1,15
|
2,18
|
238,27
|
|
46
|
22,02
|
1,15
|
0,41
|
1,22
|
19,55
|
|
54
|
22,46
|
1,30
|
-0,37
|
1,35
|
254,06
|
|
80
|
22,83
|
0,83
|
-0,71
|
1,09
|
229,31
|
Координаты цвета красного железооксидного пигмента L*= 33,04; a*= 24,33; b*=
20,21; С= 31,63; h=219,72. На рисунках 3.14-3.16 показано положение векторов цвета
синтезированных пигментов на диаграмме цветности CIEL*a*b*.
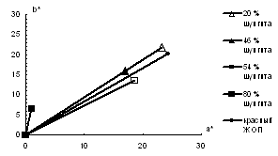
Рисунок 3.14 - Расположение векторов цвета пигмента полученного прокалкой
при 600 °С.
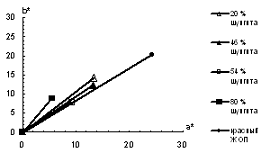
Рисунок 3.15 - Расположение векторов цвета пигмента полученного прокалкой
при 700 °С.
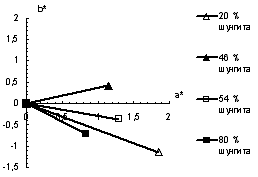
Рисунок 3.16 - Расположение векторов цвета пигмента полученного прокалкой
при 800 °С.
Как видно из таблицы 3.3 и рисунков 3.14 при содержании шунгита в
исходной композиции от 20 до 54 % цветовой тон пигментов, полученных при
прокаливании при температуре 600 °С в течение 20 минут мало отличается от цветового тона
красного железооксидного пигмента. Некоторое снижение чистоты цвета отмечается
для пигментов, полученных из смесей, содержащих около 50 % шунгита. По всей
вероятности при таких условиях прокалки желтый железооксидный пигмент переходит
в красный, а продукты сгорания шунгита, являющиеся в основном силикатами
металлов, выступают в роли наполнителя, незначительно снижающего чистоту цвета
образующегося пигмента. При содержании в смеси 80 % шунгита цветовой тон
смещается в желтую область при значительном снижении чистоты цвета. По всей
вероятности при такой температуре в течение короткого промежутка времени не
происходит полного сгорания углерода, входящего в состав шунгита, что приводит
к заметному отличию цветового тона от остальных образцов.
Повышение температуры прокаливания до 700 °С приводит при всех исследованных соотношениях к
потемнению пигмента, на что указывает снижение светлоты и насыщенности
образцов. Это связано с частичным восстановлением трехвалентного железа и
образованием смешанного оксида железа черного цвета. Вероятность такого процесса
подтверждается термогравиметрическим анализом, показывающим экзо-эффект в
области 680 °С. При высоком
содержании шунгита в исходной смеси также не происходит полного сгорания
углерода шунгита, т.к. цветовой тон пигмента смещен в желтую область, но в меньшей
степени, чем при 600 °С.
Пигменты, полученные прокаливанием при температуре 800 °С имеют черный цвет вне зависимости
от содержания шунгита, о чем свидетельствуют величины координат цветности.
Если при температуре 600 °С в основном протекает процесс дегидратации желтого железооксидного
пигмента с переходом его в красный, то с увеличением температуры начинают
преобладать процессы восстановления железа. При этом происходит снижение
коэффициента отражения в длинноволновой области, за счет восстановления
углеродом шунгита трехвалентного железа в двухвалентное и образование
смешанного оксида двух- и трехвалентного железа черного цвета. Увеличение температуры до 800 °С кроме того приводит к образованию пигмента,
обладающего магнитными свойствами, что свидетельствует о переходе смешанного
оксида Fe3O4 в g-модификацию. Таким образом, показано, что цвет синтезируемого пигмента
определяется температурным и временным режимом прокаливания, определяющим
полноту сгорания углерода шунгита. При повышении температуры прокаливания до
800 °С получаются черные пигменты,
представляющие собой смешанные оксиды железа g-модификации, обладающие магнитными свойствами.
В связи с тем, что пигменты, получаемые прокалкой при 600 °С обладают более высокой
насыщенностью по сравнению с другими образцами, нами было изучено влияние
времени прокалки на цветовые характеристики и свойства таких пигментов.
На рисунке 3.17 представлены спектры отражения прокаленных пигментов при
температуре 600 °С в
течении 20 минут в зависимости от содержания шунгита в исходной композиции.
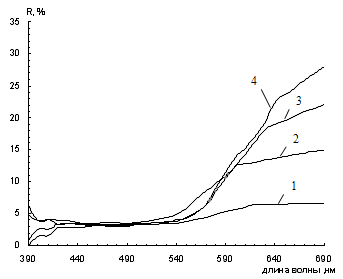
Рисунок 3.17 - Спектры отражения пигментов прокаленных в течение 20 минут
при температуре 600 °С в
зависимости от содержания шунгита исходной композиции (1 - 20 %; 2 - 46 %; 3 -
54 %; 4 - 80 %)
С увеличением доли шунгита коэффициент отражения прокаленного пигмента в
длинноволновой области уменьшается пропорционально содержанию шунгита. Цвет
пигмента при этом изменяется от красного с коричневым оттенком до темного
красно-коричневого (таблица 3.3). Поскольку восстановление железа при этой
температуре происходит в незначительной степени, в итоге образуется смешанный
пигмент, состоящий из красного железоокисного пигмента и шунгита. Поскольку
доступ кислорода исключен разложение шунгита также непроисходит.
На рисунках 3.18-3.21 приведены спектры отражения пигментов полученных из
композицый с различным содержанием шунгита в ависимости от времени прокалки. В
таблице 3.4 приведены цветовые характеристики полученных пигментов. На рисунках
3.22-3.25 показано расположение векторов цветов пигментов в зависимости от
времени прокалки.
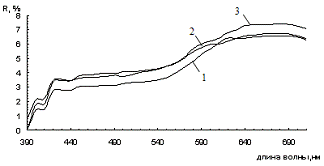
Рисунок 3.18 - Спектры диффузного отражения пигмента полученного из
композиции с содержанием шунгита 80 %. в зависимости от времени прокалки при
600 °С (1 - 20 мин, 2 - 40 мин, 3 - 60
мин).
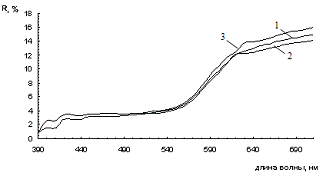
Рисунок 3.19 - Спектры диффузного отражения пигмента полученного из
композиции с содержанием шунгита 54 % в зависимости от времени прокалки при 600
°С (1-20 мин, 2- 40 мин, 3- 60 мин).
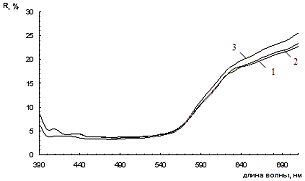
Рисунок 3.20 - Спектры диффузного отражения пигмента полученного из
композиции с содержанием шунгита 46 %. в зависимости от времени прокалки при
600 °С (1 - 20 мин, 2 - 40 мин, 3 - 60
мин).
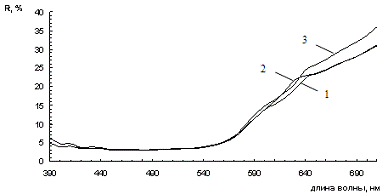
Рисунок 3.21 - Спектры диффузного отражения пигмента полученного из
композиции с содержанием шунгита 20 %. в зависимости от времени прокалки при
600 °С (1-20 мин, 2- 40 мин, 3- 60 мин).
Коэффициент отражения пигмента прокаленного в течении 40 минут больше,
чем двух других Подобное явление можно объяснить тем, что за 40 минут
достигается большая степень дегидратации желтого ЖОП. Падение коэффициента
отражения пигмента прокаленного в течение 60 минут, возможно, объясняется
частичным восстановлением железа (III) и уменьшением отражательной способности пигмента. У пигмента,
полученного прокалкой в течении 40 минут также уменьшается насыщенность и
цветовой тон смещается в сторону зеленых оттенков (рисунок 3.22, таблица 3.3)
Таблица 3.3 - Координаты цвета прокаленных пигментов.
|
Время прокалки, мин.
|
Координаты цвета в системе CIEL*a*b*
|
|
L*
|
a*
|
b*
|
С
|
H
|
|
20% шунгита
|
|
20минут
|
33,44
|
23,20
|
21,87
|
31,88
|
43,31
|
|
40минут
|
33,79
|
24,18
|
21,75
|
32,52
|
41,97
|
|
60минут
|
34,40
|
25,06
|
22,24
|
33,51
|
41,59
|
|
45% шунгита
|
|
20минут
|
31,01
|
17,01
|
15,98
|
23,34
|
43,21
|
|
40минут
|
31,49
|
17,13
|
14,04
|
22,15
|
39,34
|
|
60минут
|
32,57
|
18,66
|
15,63
|
24,34
|
39,95
|
|
54% шунгита
|
|
20минут
|
29,19
|
18,58
|
13,61
|
23,03
|
36,22
|
|
40минут
|
28,31
|
19,45
|
15,49
|
24,86
|
38,53
|
|
60минут
|
30,05
|
17,78
|
15,50
|
23,59
|
41,08
|
|
80% шунгита
|
|
20минут
|
23,41
|
0,94
|
6,53
|
6,60
|
81,81
|
|
40минут
|
23,78
|
-7,88
|
2,47
|
8,26
|
162,60
|
|
60минут
|
25,81
|
1,42
|
6,44
|
6,59
|
77,57
|
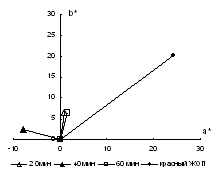
Рисунок 3.22 - Положение векторов цвета пигментов, полученных
прокаливанием при Т=600 °С
смеси желтого железооксидного пигмента с шунгитом в соотношении 80:20.
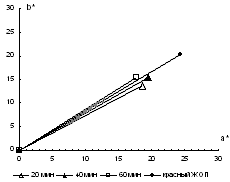
Рисунок 3.23 - Положение векторов цвета пигментов, полученных
прокаливанием при Т=600 °С
смеси желтого железооксидного пигмента с шунгитом в соотношении 54:46.
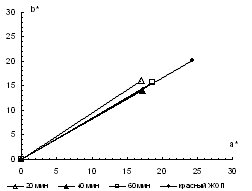
Рисунок 3.24 - Положение векторов цвета пигментов, полученных
прокаливанием при Т=600 °С
смеси желтого железооксидного пигмента с шунгитом в соотношении 46:54.
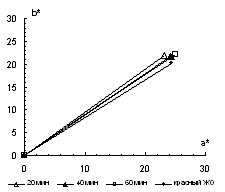
Рисунок 3.25 - Положение векторов цвета пигментов, полученных
прокаливанием при Т=600 °С
смеси желтого железооксидного пигмента с шунгитом в соотношении 20:80.
Из приведенных данных следует, что при содержании шунгита в смеси с
желтым железооксидным пигментом до 54 % увеличение времени прокалки практически
не влияет на цветовой тон синтезируемого пигмента. Однако, чистота цвета в
процессе прокалки все больше приближается к чистоте цвета красного
железооксидного пигмента. При высоком содержании шунгита в исходной смеси
увеличение времени прокалки не приводит к увеличению насыщенности пигмента по
всей вероятности из-за неполного сгорания углерода шунгита.
Для определения влияния времени прокалки на красящую способность
синтезируемого пигмента были сделаны накраски разбелов данных пигментов
диоксидом титана Kemira R-706 в соотношении 1 к 3. и сняты
спектры отражения. По полученным спектрам отражения была рассчитана красящая
способность по изменению значения функции ГКМ. В таблице 3.4 представлены
значения красящей способности синтезированных пигментов.
Таблица 3.4 - Красящая способность пигментов, полученных прокалкой при
600 ºС смесей желтого ЖОП и шунгита в
различном соотношении в зависимости от времени прокалки, %
|
Время прокалки, мин
|
Доля шунгита в исходной
смеси, %
|
|
20
|
46
|
54
|
80
|
|
20
|
100
|
100
|
100
|
100
|
|
40
|
101,9
|
86
|
68,3
|
94,7
|
|
60
|
59,9
|
44,8
|
64,3
|
61,1
|
Как видно из таблицы 3.4, с увеличением времени прокалки красящая
способность пигмента уменьшается, что, возможно, вызвано агломерацией,
спеканием частиц пигмента в процессе прокалки.
Для всех синтезированных пигментов были определены их физико-химические
показатели (таблица 3.5)
Таблица 3.5 - Некоторые свойства синтезированных при 600 °С пигментов
|
Содержание шунгита
|
80
|
54
|
46
|
20
|
|
Показатель
|
время прокалки, мин
|
время прокалки, мин
|
время прокалки, мин
|
время прокалки, мин
|
|
20
|
40
|
60
|
20
|
40
|
60
|
20
|
40
|
60
|
20
|
40
|
60
|
|
маслоемкость, г/100 г
|
41,1
|
35,9
|
38,2
|
50,1
|
43,6
|
35,0
|
53,6
|
50,0
|
49,9
|
57,5
|
60,8
|
59,8
|
|
насыпная плотность, г/см3
|
|
|
0,633
|
|
|
0,444
|
|
|
0,378
|
|
|
-
|
|
истинная плотность, г/см3
|
|
4,89
|
|
|
4,12
|
|
|
3,72
|
|
|
3,98
|
|
|
укрывистость, г/м2
|
|
24,7
|
|
|
40,5
|
|
|
|
|
|
30,3
|
|
|
pH водной вытяжки
|
|
|
5,48
|
|
|
5,73
|
|
|
5,75
|
|
|
4,87
|
Из таблицы 3.5 можно заметить, что увеличение содержания шунгита в
исходной композиции приводит к снижению маслоемкости полученных пигментов:
маслоемкость приближается к значению таковой для красного ЖОП. Время прокалки
практически не влияет на величину маслоемкости. Кроме того, происходит
увеличение истинной и насыпной плотности пигмента. Наибольшей укрывистостью обладает пигмент полученный из
композиции с долей шунгита 54 %. Такое явление можно объяснить теми же
причинами, что и резкое изменение функции ГКМ при увеличении доли шунгита.
Изменение значения функции ГКМ (и, соотвественно, укрывистости) при таком
содержании шунгита происходит за счет инверсии оптических свойств системы
пигмент-воздух, что связано с изменением перекрытия рассеяния света гематита
частицами шунгита.
С целью изучения возможности получения лакокрасочных материалов,
наполненных синтезированными пигментами, были рассчитаны значения критической
объемной концентрации пигмента в пленке, исходя из их маслоемкости. Для
получения наполненных материалов был выбраны пигменты, полученные прокалкой при
600 °С в течение 40 минут смеси желтого
железооксидного пигмента с шунгитом при всех исследуемых соотношениях. Критическое объемное содержание (критическая объемная
концентрация пигмента - КОКП) рассчитывается по следующей формуле:
КОКП=100 / (1+0.01 · М · рп),
где М - маслоемкость пигмента
rп -
плотность пигмента, г/см3
Значения КОКП для пигментов полученных при 600 С в течении 40 минут
представлены в таблице 3.6
Таблица 3.6 - Значение КОКП пигментов, полученных прокалкой смеси желтого
железооксидного пигмента с шунгитом в различном соотношении при 600 0С
в течение 40 минут.
|
Содержание шунгита, %
|
80
|
54
|
46
|
20
|
|
КОКП
|
36,3
|
35,8
|
34,9
|
29,2
|
Исходя из требований по содержанию пигмента в пленке, предъявляемых к эмалям
на основе лаков ПФ-283 и МЛ-0193 были получены лакокрасочные материалы с
объемной долей пигмента в пленке 5 %, что составило около 11 % от КОКП. На
основе этих материалов методом налива были получены покрытия на стальных и
стеклянных подложках и определены основные свойства покрытий, представленые в
таблицах 3.7 и 3.8
Таблица 3.7 - Результаты испытаний покрытий на основе лака ПФ-283
|
Показатель
|
Содержание шунгита в
синтезированном пигменте, %
|
|
80
|
54
|
46
|
20
|
|
Относительная твердость
|
0,2
|
0,2
|
0,23
|
0,23
|
|
адгезия, баллы
|
1
|
1
|
1
|
1
|
|
прочность покрытия при
ударе, см
|
50
|
50
|
50
|
45
|
|
эластичность пленки при
изгибе, мм
|
1
|
1
|
1
|
1
|
Таблица 3.8 - Результаты испытаний покрытий на основе лака МЛ-0193
|
Показатель
|
Содержание шунгита в
синтезированном пигменте, %
|
|
80
|
54
|
46
|
20
|
|
Относительная твердость
|
0,36
|
0,13*)
|
0,14*)
|
0,26**)
|
|
адгезия, баллы
|
1
|
1
|
1
|
1
|
|
прочность покрытия при
ударе, см
|
50
|
50
|
50
|
45
|
|
эластичность пленки при
изгибе, мм
|
1
|
1
|
1
|
1
|
Как следует из таблиц 3.7 и 3.8 все покрытия обладают высокими
физико-механическими свойствами. Кроме того, с помощью спектрофотометра
"Пульсар" были определены цветовые характеристики покрытий на основе
лака ПФ-283, представленные в таблице 3.9.
Таблица 3.9 - Цветовые характеристики лакокрасочных покрытий на основе
лака ПФ-283
|
Доля шунгита в
синтезированном пигменте, %
|
L
|
a*
|
b*
|
С
|
h
|
|
80
|
11,17
|
-3,88
|
-27,96
|
28,23
|
262,11
|
|
54
|
18,05
|
7,033
|
-24,79
|
25,77
|
285,84
|
19,89
|
13,30
|
-21,85
|
25,58
|
301,32
|
|
20
|
23,35
|
9,25
|
-20,28
|
22,24
|
294,58
|
Из таблицы 3.9 можно заметить, что видно, что с увеличением доли шунгита
светлота и желтизна увеличивается.
По результатам испытаний покрытий наполненных синтезированными пигментами
можно сделать вывод, что данные пигменты пригодны для получения
пигментированных лакокрасочных материалов.
4. Охрана труда и защита окружающей среды
4.1 Свойства
применяемых в работе материалов
Токсичные свойства используемых в работе веществ, представлены в
таблице 4.1
Таблица 4.1 -Токсикологические характеристики применяемых материалов
|
Наименование вещества,
формула
|
Характер действия на
организм человека
|
Агрегатное состояние
|
ПДК
|
Класс опасности по ГОСТ
12.1.007-76
|
Средства анализа воздушной
среды
|
Средства индивидуальной
защиты
|
|
|
|
В воздухе рабочей зоны,
мг/м3
|
В промышленных сточных
водах, мг/л
|
|
|
|
|
Пигмент желтый
железоокисный
|
Вещество малоопасное.
Действует прижигающе на пищеварительный тракт. При длительном воздействии
откладывается в легких, вызывая сидероз. Действует на слизистые оболочки
верхних дыхательных путей.
|
Твердый, порошок
|
10
|
-
|
IV
|
-
|
Спецодежда, перчатки.
|
|
Пигмент красный
железоокисный
|
Вещество малоопасное.
Действует прижигающе на пищеварительный тракт. При длительном воздействии
откладывается в легких, вызывая сидероз. Действует на слизистые оболочки
верхних дыхательных путей.
|
Твердое, порошкообразное
вещество
|
6
|
-
|
IV
|
-
|
Спецодежда, перчатки
|
|
Двуокись титана
|
Вещество малоопасное может
вызывать заболевания дыхательных путей.
|
Твердое порошкообразное
вещество
|
10
|
0,1
|
III
|
-
|
Спецодежда, перчатки
|
|
Смола полиэфирная ПФ-283
|
Токсичность смолы
определяется наличием растворителей, входящих в ее состав.
|
Вязкая жидкость
|
-
|
-
|
-
|
-
|
Спецодежда,очки, перчатки
|
|
Алкидно-меламиноформальдегидный
лак МЛ-0197
|
Токсичность смолы
определяется наличием растворителей, входящих в ее состав.
|
Вязкая жидкость
|
-
|
-
|
-
|
-
|
Спецодежда,очки, перчатки
|
|
Ксилол
|
Токсичен. Пары действуют
наркотически на ЦНС, раздражают слизистую оболочку, кожу, глаза.
|
Жидкость
|
50
|
0,05
|
III
|
Газовая хроматография
|
Противогаз марки
"А", спецодежда
|
|
Ацетон
|
Наркотическое действие,
может всасываться через неповрежденную кожу, отравление возможно при вдыхании
паров ацетона в концентрации, превышающей ПДК
|
Жидкость
|
200
|
0,05
|
IV
|
Газовая хроматография
|
Противогаз марки
"А", спецодежда
|
Взрывопожароопасные
свойства используемых веществ, приведены в таблице 4.2
Таблица 4.2 -
Взрыво- и пожароопасные свойства материалов
|
Наименование вещества
|
Агрегатное состояние
|
Температура кипения, °C
|
Плотность, г/см3
|
Температура, °С
|
Пределы воспламенения
|
|
|
|
|
вспышки
|
воспламенения
|
самовоспламенения
|
концентрацион. (%об)
|
температурные, °C
|
|
Ксилол
|
Жидкость
|
139
|
0,863
|
29
|
-
|
590
|
0,9-4,5
|
+24 - +50
|
|
Ацетон
|
Жидкость
|
56
|
0,790
|
-18
|
-
|
465
|
2,2-13,0
|
-20 - +6
|
4.2 Меры
пожарной профилактики
4.2.1
Определение категории помещения по взрывопожароопасности по НПБ 105-03 и класса
помещения по ПУЭ
Расчетный критерий - испарение с поверхности разлившейся жидкости
(ацетон) в количестве 1литр.
DР=((Рmax-Р0)
· m · z · 100 · 1)/Vсв · r · Сcm · Кн,
где DР- избыточное
давление взрыва, кПа;
Рmax - максимальное давление взрыва,
принимаем равным 900 кПа;
Ро - атмосферное давление в помещении, принимаем 101 кПа;
m -
масса горючих веществ, участвующих во взрыве, кг;
z -
коэффициент участия во взрыве горючего вещества, принимаем 0,3;
Vсв - свободный объём помещения, м3;
r - плотность веществ, участвующих во взрыве, кг/м3;
Ссm
- стехиометрический коэффициент горючего вещества;
Кн - коэффициент негерметичности помещения.
Масса ЛВЖ определяется следующим образом:
=W · F · t,
где W - интенсивность испарения, кг/м2с;
F -
площадь испарения, м2;
t - время испарения, с.
=10-6 · h · М1/2 · Рн,
где h -
коэффициент, зависящий от скорости движения воздуха и температуры в помещении;
Рн =23,99 - давление насыщенных паров при данной температуре,
кПа;
При скорости движения воздуха в тяге 0,1м/с и температуре воздуха 200С
h =2,4;
М =58,08 - молекулярная масса вещества;
Ссm=100/1+4,84КО2;
где КО2 - стехиометрический коэффициент О2 в
реакции горения;
КО2=nс+(nн-nх)/4-nо/2;
где nс, nн, nх, nо - число атомов углерода, кислорода,
галогенов соответственно.
КО2=3+6/4-1/2=4;
Ссm=100/1+4,84*4=4,91;
W=4,39
· 10-4 кг/с;
m=4,39
· 10-4 · 1 · 3600=1,58 кг;
Vсв=0,8 · 108=86,4 м3;
Р=(900-100) · (1,58 · 0,3/(86,4 · 3,66)) · (100/4,91 · 3)=8,13
кПа.
В соответствии с НПБ 105-03 лаборатория, в которой проводились
эксперименты, имеет категорию "А" по взрывопожароопасности и класс
В-1б в соответствии с ПУЭ.
.2.2 Средства пожаротушения
Средства пожаротушения в лаборатории: асбестовое одеяло, песок, вода,
огнетушитель пенный ОХП-10, огнетушитель углекислотный ОУ-2.
4.2.3 Нормы
хранения ЛВЖ и ГЖ лаборатории
Химические реактивы хранятся в закрытых банках, стеклянных сосудах. На
каждом сосуде должна быть этикетка с точным названием вещества и его подробная
характеристика (концентрация, плотность, чистота).
Низкокипящие жидкости, ЛВЖ и ГЖ хранить в толстостенной посуде, которую
помещают в жёлтый ящик. При переносе небольших количеств веществ, находящихся в
стеклянных сосудах, необходимо применять вёдра.
Нормы хранения ЛВЖ и ГЖ в лаборатории устанавливаются такими, чтобы в
случае одновременного розлива всех ЛВЖ и ГЖ, имеющихся в помещении, не
создавались взрывоопасные концентрации. Нормы хранения ЛВЖ: 1 литр на
сотрудника, но не более 3 литров на комнату.
4.2.4 Правила
работы с ЛВЖ и ГЖ
ЛВЖ и ГЖ следует доставлять в лабораторию в плотно закрытой посуде,
помещённой в специальный металлический ящик с ручками. Запрещается хранить в
лабораторном помещении ЛВЖ с температурой кипения ниже 50 С. Все работы с ЛВЖ и
ГЖ должны проводиться в вытяжном шкафу при работающей вентиляции, выключенных
газовых и нагревательных приборах. При
случайных розливах ЛВЖ, а также при утечке горючих газов, необходимо выключить
все источники открытого огня, электронагревательные приборы. Место розлива
засыпать песком, затем собрать его деревянной лопаткой или совком.
Сосуды, в которых проводилась работа с ЛВЖ и горючими веществами, по
окончании работы должны быть промыты. Запрещается сливать ЛВЖ и ГЖ в
канализацию. Отработанные жидкости следует собирать раздельно, в специальную
герметичную тару. Спецодежду, загрязнённую ЛВЖ и ГЖ, необходимо заменить во
избежание возможного воспламенения.
4.2.5 Метеорологические и санитарно-гигиенические условия в лаборатории
В соответствии с нормами на одного человека должно приходиться 4,5м2
площади. Объём производственного помещения 135 м3. Высота
лаборатории не менее 3м. На одного человека должно приходиться 1,0-1,5 м длины
вытяжного шкафа. В холодное и переходное время года температура воздуха должна
поддерживаться 21-25 0С, влажность воздуха 40-60%, скорость движения
0,1-0,3 м/с. В тёплое время года - 22-28 0С; 55%; 0,1-0,3 м/с соответственно.
Исходя из метеорологических условий, в лаборатории может выполняться лёгкая
физическая работа категории 1 по ГОСТ 12.1.005-88, и средней тяжести 2 (а,б).
4.3
Вентиляция лабораторного помещения
Лаборатория оснащена вытяжной вентиляцией. Скорость воздуха в рабочем
проёме составляет 0,5 м/с. Кратность воздухообмена в вытяжном шкафу при высоте
поднятой шторки 0,3 м рассчитывается по формуле:
К=W/V,
где К - кратность воздухообмена, ч-1;
W -
объём воздуха, удаляемого из помещения в единицу времени, м3/ч;
V -
объём вытяжного шкафа или лаборатории, м3.
=v · S · 3600,
где v - скорость воздуха в рабочем проёме,
м/с;
S -
площадь сечения, м2;
W=0,5
· 1,5 · 3600 = 2700 (м3/ч)
Кратность воздухообмена для вытяжного шкафа:
К= 2700/1,89 = 1428 (ч-1);
Кратность воздухообмена для лаборатории:
К= 2700/135 = 20(ч-1).
.4 Освещение лабораторного помещения
В соответствии со СНиП 23-05-95 в лаборатории предусмотрено естественное
боковое освещение. Искусственное освещение осуществляется люминесцентными лампами
ЛД (дневного света - 8 ламп). Освещённость не менее 300 лк. На одно рабочее
место. Освещение вытяжного шкафа осуществляется светильниками ВЗГ - 300.
Коэффициент естественного освещения в вытяжном шкафу 1 - 0,75%, на поверхности
стола 1,5%. Застеклённая площадь окон 20%. В лаборатории можно проводить
зрительные работы высокой и средней точности. Разряд зрительной работы 3 и 4.
Группа помещения 1.
4.5
Электробезопасность на рабочем месте
Категория помещения по электробезопасности - 1, без повышенной опасности.
Источниками возгорания могут являться неисправные электроприборы и
электропроводка в электроприборах.
Электронагревательные приборы при ежедневной эксплуатации должны
очищаться от пыли и грязи. При использовании масляной бани необходимо следить,
чтобы масло не попадало на электроплитку и рядом не находились ЛВЖ и ГЖ. Все
приборы должны иметь своё постоянное место с достаточной тепловой изоляцией. В
качестве изолирующего материала используется керамическая плитка, асбест. В
лаборатории имеется заземление и питающая сеть с напряжением 220 В.
4.6
Водоснабжение. Удаление сливов и отходов
Водоснабжение горячей и холодной водой осуществляется от городской сети,
в соответствии со СНиП 2.04.01 - 85. Отходы химических веществ подлежат сливу в
специально оборудованные ёмкости для слива органики, кислот, щелочей.
Запрещается сливать в канализацию опасные химические вещества. По мере
заполнения тары отходы подлежат утилизации.
4.7 Условия
безопасного проведения исследований
При нормальном режиме работы в лаборатории концентрация вредных веществ в
воздухе не превышает ПДК, все нагревательные приборы находится в исправности,
работает вентиляция, оборудование отвечает предъявляемым к нему требованиям.
Аварийным режимом работы считается наличие условий способных вызвать
взрыв, пожар, отравление работающих.
Причинами аварийного режима работы могут служить:
·
воспламенение ГЖ
при нагревании на электроплитке;
·
розлив в
лаборатории легколетучих жидкостей образующих ядовитые пары, а так же большого
количества азота.
При попадании паров огне-, взрывоопасных веществ в помещении лаборатории
необходимо открыть окна, включить вентиляцию. При создании опасной концентрации
паров огне-, взрывоопасных веществ вблизи от работающих электроприборов
выключить их общим рубильником в коридоре, но не выключать вилку или рубильник
в аварийном помещении.
В условиях аварийного режима работы разрешается пользоваться инструментом
во взрывоопасном исполнении.
Заключение
В процессе работы были определены основные свойств смесей желтого железооксидного
пигмента с шунгитом в различном соотношении. Показано, что цвет и
физико-химические свойства данных смесей зависят от массовой доли шунгита в
композиции. Определено, что при содержании шунгита около 60 % происходит
инверсия оптических свойств.
Методом дериватографии изучены процессы, протекающие при прокалке смесей
желтого ЖОП и шунгита. Прокалочным методом из исходных смесей синтезированы
красные, коричневые и черные ЖО пигменты и определены их физико-химические
свойства. Определено влияние температуры, времени прокалки и массовой доли
шунгита в исходной смеси на оптические свойства синтезируемых пигментов.
Показана возможность использования углерода шунгита, как восстановителя, при
синтезе коричневых и черных ЖО пигментов.
Были получены пигментированные лакокрасочные материалы и покрытия на
основе синтезированных пигментов. Определены механические и оптические свойства
покрытий. Показана возможность использования синтезированных пигментов для
получения наполненных ЛКМ.
Список литературы
. Беленький Е.Ф., Рискин И.В. Химия и технология пигментов -
Л.: Химия
2. Ермилов П.И., Индейкин Е.А., Толмачев И.А. Пигменты и
пигментированные лакокрасочные матерьялы: Учебное пособие для вузов. - Л.:
Химия, 1987. - 240 с.
. Рысьев О.А. Шунгит - национальный камень России.
Санкт-Петербург
4. Туктамышев И.Ш. Разработка и промышленное опробование
технологии получения карбида кремния из шунгитовой породы. Диссертация на
соискание ученой степени кандидата технических наук. Москва. НИИГРАФИТ. 2000 г.
178 с.
. Патент, США, №4142915, публикация 06.03.79, МКИ С 09 С
1/24, НКИ
6. Патент , Япония, заявка 82 - 7638, заявл. 02.07.85, №60 -
146391, опубл. 14.01.87, МКИ С 01 G 49/00.
. Патент, ФРГ, кл. С 09 С 1/24, №2826941, заявл. 20.06.78,
опубл. 10.01.08.
. Полински К.О. Получение красного железооксидного пигмента
из железного купороса: ЖПХ, № 2, 1969. - с.272.
. Патент, США, №4163472, публикация 08.05.79, МКИ С 09 С 1/24
10. Патент, Франция, кл. С 09 С 1/24, № 2376839, заявл.
30.11.77, № 7736066, опубл. 04.08.78.
. Корсунский Л.Ф. Неорганические пигменты: Справочник.
. Горловский И.А., Индейкин Е.А., Толмачев И.А. Лабораторный
практикум по пигментам и пигментированным лакокрасочным материалам: Учеб.
пособие для вузов. - Л.: Химия, 1990. - 240с.
.Интернет ресурс #"599789.files/image035.gif">
Рисунок А.1- Спектры диффузного отражения разбеленных диокисдом титана 1
к 3 пигментов, полученных прокалкой при 600 ºС смесей желтого ЖОП и шунгита в соотношении
80:20 (а), 54:46 (б), 46:54 (в), 20:80 (г) при различном времени (1-20 мин, 2-
40 мин, 3- 60 мин).
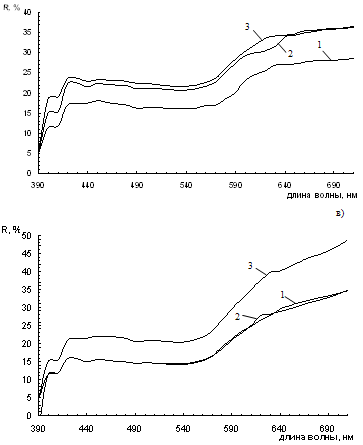
Рисунок А.1- Спектры диффузного отражения разбеленных диокисдом титана 1
к 3 пигментов, полученных прокалкой при 600 ºС смесей желтого ЖОП и шунгита в
соотношении 80:20 (а), 54:46 (б), 46:54 (в), 20:80 (г) при различном времени
(1-20 мин, 2- 40 мин, 3- 60 мин).