|
Клас
|
Назва класу
|
Деякі
представники
|
|
I
|
В-Лактами
(основні группы: пеніциліни, цефалоспоріни
|
Бензилпеніцилін,
оксацилін, цефотаксим
|
|
II
|
Макроліди і
лінкозаміди
|
Еритроміцин,
лінкоміцин
|
|
III
|
Аміноглікозіди
|
Стрептоміцин,
гентаміцин
|
|
IV
|
Тетрациклін
|
Доксіциклін
|
|
V
|
Поліпептиди
|
Поліміксин
|
|
VI
|
Полієни
|
Ністатин,
Амфотерицин В
|
|
VII
|
Ріфампіцини
|
Ріфампіцин
|
|
Інші
|
|
Лєвоміцетин,
гризєофульвин
|
Найбільш важливими класами синтетичних
антибіотиків являються хінолони і фторхінолони (наприклад, ципрофлоксацин),
сульфаніламіди (сульфадіметоксин), імідазолы (метронідазол), нітрофурани
(фурадонін, фурагін).
Велика частина антибіотиків має природне
походження, і їх основними продуцентами є мікроби. Мікроорганізми, знаходячись
у своєму природному місці існування - в основному в грунті, роблять антибіотики
в якості засобу боротьби за існування з собі подібними [11]. Антибіотики, як
хіміотерапевтичні речовини, отриманні на основі життєдіяльності мікро - і
макроорганізмів, відрізняються від звичайних метаболітів специфічністю та
виключно високою біологічною активністю відносно чутливих до них
мікроорганізмів [6].
Залежно від джерела отримання розрізняють сім
груп антибіотиків:
антибіотики, отримані з грибів, наприклад роду
Penicillium (пеніциліни, гризеофульвин), роду Cephalosporium (цефалоспоріни) і
т.д.;
антибіотики, отримані з актиноміцетів [11].
Найбільше відомо антибіотиків актиноміцетного походження. Актіноміцети -
переважно грунтові мікроорганізми. В умовах великої кількості і різноманітності
грунтових мікроорганізмів їх антогонізм, у тому числі за допомогою вироблення
антибіотиків - один з механізмів їх виживання [13]. Ця група включає близько 80
% усіх антибіотиків. Серед актіноміцетів основне значення мають представники
роду Streptomyces які є продуцентами стрептоміцину, еритроміцину, лєвоміцетіну,
ністатину і багатьох інших антибіотиків;
антибіотики, продуцентами яких є власне бактерії.
Найчастіше з цією метою використовують представників родів Bacillus і
Pseudomonas. Прикладами антибіотиків даної групи є поліміксини;
бацитрацин;
антибіотики тваринного походження - з риб'ячого
жиру отримують эктерицид;
антибіотики рослинного походження. До них можна
віднести фітонциди, які виділяють цибуля, часник, інші рослини. У чистому
вигляді вони не отримані, оскільки є надзвичайно нестійкими з'єднаннями.
Антимікробною дією володіють багато рослин, наприклад ромашка, шалфей,
календула;
синтетичні антибіотики [11].
3. Способи
отримання антибіотиків
Існують три способи отримання антибіотиків.
Біологічний синтез. Для отримання антибіотиків
цим способом використовують високопродуктивні штами мікроорганізмів і
спеціальні поживні середовища, на яких їх вирощують. За допомогою біологічного
синтезу отримують, наприклад, пеніцилін [11].
До теперішнього часу виділено і описано більше
5000 антибіотиків.
Приблизно 50 % відомих антибіотиків синтезуються
штамами, належними до актиноміцетів, головним чином до одного з родів - роду
Streptomyces. Велике число антибіотиків є продуктами життєдіяльності інших
бактерій, але серед цих антибіотиків лише небагато знайшли практичне
застосування. Майже усі антибіотики бактерійного походження по хімічній природі
являються пептидними. Серед бактерій-продуцентів слід виділити спорооутворюючі
бактерії Bacillus subtilis, які здатні утворювати близько 70 різних
поліпептидних антибіотиків, Вacillus polymyxa - 20 антибіотиків, які
відносяться до сімейства полімиксинових, Bacillus brevis - 23 антибіотики. Антибіотики
продукуються також багатьма видами плісневих грибів.
Здатність до синтезу антибіотиків не являється
строго специфічною ознакою. Один і той же антибіотик може утворюватися
мікроорганізмами, що відносяться до різних видів, родів і навіть порядків. Крім
того, штами, що належать до одного виду, можуть синтезувати різні антибіотики.
Проте, як правило, чим далі знаходяться друг від друга організми в
таксономічному відношенні, тим менше вірогідність, що вони синтезують один і
той же тип антибіотика [10].
Хімічний синтез. Після вивчення структури деяких
природних антибіотиків стало можливим їх отримання шляхом хімічного синтезу.
Одним з перших препаратів, отриманих таким методом, був левоміцетін. Крім того,
за допомогою цього методу створені усі синтетичні антибіотики.
Комбінований метод. Цей метод представляє собою
поєднання двох попередніх: за допомогою біологічного синтезу отримують
антибіотик, виділяють з нього так зване ядро (наприклад, 6-амінопеніцилланову
кислоту з пеніциліну) і хімічним шляхом додають до нього різні радикали.
Антибіотики, отримані за допомогою цього методу, називаються напівсинтетичними.
Наприклад, напівсинтетичними пеніцилінами є оксацилін, азлоцилін. Широко
використовуються напівсинтетичні цефалоспоріни, тетрациклін та ін. Доброю
ознакою напівсинтетичних антибіотиків є чутливість до них стійких до природних
антибіотиків мікроорганізмів. Крім того, це найбільш економічно вигідний засіб
виробництва антибіотиків: з одного природного антибіотика, вартість отримання
якого дуже висока, можна створити приблизно 100 напівсинтетичних препаратів з
різними властивостями [11].
Синтез антибіотиків починається тільки після
майже повного припинення росту мікроорганізмів, що продукують їх.
Антибіотики отримують за допомогою методів
глибинного культивування в глибоких ферментерах з нержавіючої сталі, вміст яких
інтенсивно аерують і перемішують.
Іноді антибіотики піддають наступній хімічній
модифікації. Один з прикладів - хімічне заміщення ацильної групи природних
пеніцилінів з утворенням різноманітних напівсинтетичних пеніцилінів. Ще один
приклад - каталітичне відщеплення хлористого водню від хлортетрацикліна з
утворенням більш активного з'єднання тетрацикліну [14].
4.
Основні властивості антибіотиків
По хімічному складу антибіотики є
найрізноманітнішими речовинами - від простих з'єднань до дуже складних
поліпептидних структур [11]. Антибіотики в хімічному відношенні представляють гетерогенну
групу з'єднань:
молекулярна маса антибіотиків варіює від 150 до
500. Тобто це низькомолекулярні речовини;
молекули одних антибіотиків складаються не лише з
атомів С і Н, але частіше із С, О, Н і N; інші антибіотики містять також атоми
сірки фосфору і галогенів;
у молекулах антибіотиків представлені майже усі
функциональні групи, відомі в органічній хімії (гідроксильна, карбоксильна,
карбонільна, азотовмісні функціональні групи та ін.), а також аліфатичні і
аліциклічні ланцюги, ароматичні кільця і т.д. Загальним для усіх антибіотиків є
те, що вони можуть бути отримані в кристалічному виді [10].
Хімічна будова вивчена у більшості антибіотиків і
покладена в основу їх класифікації. Згідно М.М. Шемякіну і А.С. Хохлову,
розрізняють антибіотики ациклічної і ароматичної будови, хінони, кисеньвмісні
гетероциклічні з'єднання, пеніциліни, стрептоміцини, антибіотики-поліпептиди,
антибіотики зі встановленою і невстановленою сумарною формулою. З хімічною
структурою антибіотика пов'язано багато його властивостей: розчинність,
стійкість, токсичність. Важливою особливістю антибіотиків є вибірковість дії:
кожен з них активний тільки по відношенню до певної групи мікроорганізмів і
інгібує строго певні біохімічні функції. Наприклад, пеніцилін діє тільки на
зростаючі клітини грампозитивних бактерій, тоді як грамнегативні до нього менш
чутливі. У цьому полягає одна з істотних відмінностей антибіотиків від
загальнобіологічних отрут - сулеми, миш'яку, фенолу, які пригнічують
життєдіяльність будь-якого організму, що вступив з ними в контакт. Характер дії
антибіотиків різний. Більшість з них бактеріостатичні, тобто затримують ріст
чутливих мікробів; інші, маючи бактерицидну властивість, викликають загибель
відповідних мікробів. Значно менше антибіотиків, що мають бактеріолітичні
властивості. Ефективність антибіотиків залежить від дози і тривалості дії:
короткочасна дія в малих дозах затримує ріст, а вищі концентрації і тривала дія
викликають загибель тих же мікробів.
Тетрацикліни - група хімічно близьких
антибіотиків. Вони мають широкий спектр дії: активні відносно грампозитивних і
грамнегативних бактерій, рикетсій і ряду великих вірусів. Тетрациклін широко
застосовується в медичній практиці, в тваринництві як стимулятори росту тварин
і птахів, в харчовій промисловості як консерванти швидкопсувних продуктів. До
теперішнього часу відомі шість препаратів тетрацикліну. Першим був отриманий
хлортетрациклин - ауреомицин (1949) з культуральної рідини Str. aureofaciens,
який вирощується глибинним методом при безперервній аерації. Очищений препарат
має ясно-жовтий колір, погано розчинний у воді. Хлортетрациклии випускається
промисловістю під різними назвами - біоміцин, ауреоміцин, дуоміцин і
застосовується при лікуванні пневмоній, бруцельозу, туляремії, рикетсіозів і
деяких вірусних захворювань. Неочищений, так званий кормовий, біомицин
використовується в тваринництві.
З антибіотиків актиноміцетного походження
привертають увагу хлорамфенікол, або хлороміцетин - продуцент Act. venezuelae і
група актиноміцинів, продуцентами яких є багато видів актиноміцетів.
Хлорамфенікол (левомицетин) відноситися до антибіотиків широкого спектру дії і
в дуже малих концентраціях пригнічує ріст багатьох бактерій. На відміну від
пеніциліну і стрептоміцину він діє на великі віруси - збудників трахоми,
венеричною лімфогранульомы, а також на ряд рикетсій - збудника сипного тифу,
лихоманки Q і плямистої лихоманки Скелястих гір.
Еритроміцин належить до групи
антибіотиків-макролідів. Для них характерна велика, складно побудована
молекула. Продуцентом еритроміцину служить Saccharopolospora erythreus,
виділений з грунтів Філіппін. Еритроміцин є антибіотиком широкого спектру дії,
він активніший по відношенню до грампозитивних мікробів. Він діє також на
рикетсії, великі віруси і мікобактерії. Найбільше практичне значення має дія
його на золотистий стафілокок, особливо на штами, стійкі до пеніциліну.
Окрім антибіотиків, які пригнічують розвиток
хвороботворних мікроорганізмів, деякі актиноміцети можуть продукувати речовини,
що затримують розвиток злоякісних пухлин. Це так звані протиракові антибіотики.
Актиноміцин - перший відомий протираковий антибіотик, виділений С. Ваксманом і
Г. Вудрефом з Str. antibioticus в 1940 р. Він має сильну антибактеріальну дію,
пригнічує розвиток актиноміцетів і деяких дріжджів. Протиракова дія його була
відкрита в 1952 р. Він гальмує розвиток карциноми Эрліха і ракових захворювань
лімфатичної системи. Застосування актиноміцину обмежене із-за його високої
токсичності. До теперішнього часу отриманий цілий ряд актиноміцинів. Вони добре
вивчені, встановлена сфера їх клінічного застосування.
У СРСР в 1963 р. був отриманий протираковий
антибіотик брунеоміцин. Продуцентом його став Str. аlbus var. bruneomycini.
Брунеомиции пригнічує ріст деяких пухлин людини і пухлин лабораторних тварин,
що перевиваються. Він вибірково інгібує синтез ДНК і викликає її деградацію в
клітинах бактерій. До протиракових антибіотиків, отриманих з актиноміцетів,
відносяться рубоміцин, оливоміцин, стрептонігрин, дауноміцин та ін. Наявні
протиракові антибіотики доки ие дають таких успішних результатів, як
антибіотики, вживані для лікування бактерійних захворювань. Роботи по
дослідженню нових ефективних антибіотиків проти ракових захворювань тривають
[6].
4.1
Спектр і механізм дії антибіотиків
Пошуки нових антибіотиків залишаються чисто
емпіричним процесом, а їх фізіологічне значення для мікроорганізмів, що
продукують їх, неясне. Проте причини виборчої токсичності антибіотиків нині у
більшості випадків відомі. В цілому це пов'язано з фундаментальними
біохімічними відмінностями між клітинами прокаріот і эукаріот, а токсична дія
антибіотиків є наслідок їх здатності пригнічувати одну необхідну біохімічну
реакцію, специфічну для клітини того або іншого типу [14]. По спектру дії
антибіотики ділять на п'ять груп в залежності від того, на які мікроорганізми
вони діють. Кожна з цих груп включає дві підгрупи: антибіотики широкого і
вузького спектру дії (рис 4.1.1).
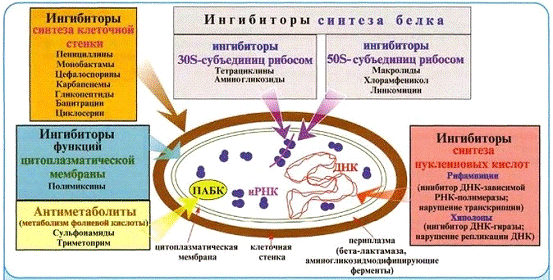
Рис.4.1.1 Механізм дії антибіотиків на бактерії [1].
Антибактеріальні антибіотики складають
найчисленнішу групу препаратів. Переважають в ній антибіотики широкого спектру
дії, що чинять вплив на представників усіх трьох відділів бактерій. До
антибіотиків широкого спектру дії відносяться аміноглікозиди, тетрацикліни та
ін. Антибіотики вузького спектру дії ефективні відносно невеликого круга
бактерій, наприклад поліміксини діють на грацилікутні, ванкоміцин впливає на
грампозитивні бактерії.
У окремі групи виділяють протитуберкульозні,
противолепрозні, протисифілітичні препарати [11].
Протисифілітічні препарати.
До основних препаратів для лікування сифілісу
відносять пеніциліни; препарати короткої (наприклад, бензилпеніциліна калієва
або натрієва солі) або пролонгованої дії (біциліни). При несприйнятті
бензилпеніциліну застосовують тетрациклін, макроліди або азаліди. Окрім
антибіотиків, призначають препарати вісмуту - бійохінбл і бісмовербл.
Бактеріостатична дія останніх пов'язана з пригніченням активності ферментів,
содержуючих сульфгідрильні групи.
Протитуберкульозні препарати.
У зв'язку з лікарською стійкістю Mycobacterium
tuberculosis при лікуванні туберкульозу застосовують комбінації антибіотиків
(рифампіцин, стрептоміцин, циклосерин, канаміцин, біоміцин) з синтетичними
препаратами різних класів (ізоніазид, этамбутол, натрію пара-аминосаліцилат).
Ізоніазид структурно близький піридоксину.
Механізм антибактеріального ефекту пов'язаний із здатністю ізоніазида
інгібувати активність ферментів, що беруть участь в синтезі міколевих кислот,
що є основними структурними компонентами клітинної стінки мікобактерій.
Препарат діє і на внутрішньоклітинно розташовані бактерії. При монотера-пії до
нього швидко розвивається резистентність. Етамбутол пригнічує синтез РНК і
ефективний тільки відносно збудника туберкульозу. Натрію парааміносаліцилат
чинить бактеріостатичну дію тільки на туберкульозну паличку, що обумовлено
конкурентними взаємодіями з р-амінобензойною кислотою, необхідної для синтезу фолієвої
кислоти [12].
Протигрибкові антибіотики включають значно меншу
кількість препаратів. Широкий спектр дії має, наприклад, амфотерицин В,
ефективний при кандідозах, бластомікозах, аспергільозах; в той же час ністатин,
діючий на гриби роду Candida, є антибіотиком вузького спектру дії [11].
Протигрибкові препарати.
Арсенал засобів специфічної терапії грибкових
уражень людини різноманітний і містить препарати, діючі на різні етапи
метаболізму збудників. Механізм дії переважної більшості протигрибкових засобів
пов'язаний з порушенням синтезу стеролів, що входять до складу клітинної
стінки.
Азоли (імідазолы та триазоли) блокують активність
ферментів, що беруть участь в 14-деметиліруванні ланостерола, що веде до
порушення синтезу ергостабілу. Зміна структури ЦПМ грибкових клітин призводить
до виходу макромолекул і іонів назовні. Чутливість ферментів ссавців до азолів
значно нижче, ніж ферментів грибів. Речовини проявляють широкий спектр
фунгіцидної активності. Найбільш відомі клотримазол, міконазол, ітраконазол і
кетоконазол.
Фторцитозин (флуцитозин) - антиметаболіт,
нуклеотидний аналог, що пригнічує синтез нуклеїнових кислот. Після проникнення
в клітину молекула піддається дезамінуванню і перетворюється на 5-фторурацил,
інгібірувальний активність тимідилат синтетази - ферменту синтеза тимідиловой
кислоти. Ці фунгістатики застосовують при лікуванні системних дріжджових
мікозів, його часто комбінують з амфотерицином В (особливо при криптококкозі).
Аморолфін - похідне морфолінів, інгібітор синтезу
ергостабілу, блокує перетворення фекостерина в эпістерин. Призначають при
оніхомікозах, що викликаються дріжджовими і плісневими грибами.
Аліламіни (нафтіфин, тербінафін) чинять
фунгіцидну дію внаслідок інгібування активності скваленепоксидази і порушення
синтезу ергостабілу.
Грізеофульвін - антибіотик, продукований
Penicillium griseofulvum - проявляє фунгістатичну дію відносно грибів родів
Trichophyton, Мicrosporum і Epidermophyton, не діє на дріжжеподібні гриби і
бактерії. Механізм антигрибкової активності зумовлено порушенням організації
мікротрубочок [12].
Антипротозойні і антивірусні антибіотики
нараховують невелику кільуість препаратів [11].
Протипротозойні препарати.
Найпростіші резистентні до більшості
антибактеріальних препаратів, але все таки ряд антибіотиків пригнічує їх
життєдіяльність (наприклад, доксіциклін активний відносно балантидієв і
малярійних плазмодіїв, кліндаміцин і мономіцин - малярійних плазмодіїв і
дизентерийних амеб). У зв'язку з тим, що метаболізм найпростіших швидше нагадує
такий у тварин, ця схожість біохімічних процесів може призвести після прийому
протипротозойних препаратів до розвитку токсичних ефектів у людини. Ця
обставина значно зменшує потенційну кількість мішеней для фармакологічної дії
на найпростіших і обмежує арсенал протипротозойних лікарських засобів. Мішенями
для лікарських засобів у найпростіших виступають ферменти, наявні тільки у них
(унікальні ферменти), або абсолютно незамінні для їх життєдіяльності (незамінні
ферменти).
Унікальні ферменти найпростіших.
Ферменти цієї групи беруть участь в синтезі
нуклеотидів, енергетичному метаболізмі і окисно-відновних реакціях. Препарати,
пригноблюючі унікальні ферменти найпростіших, нетоксичні для клітин ссавців.
Дигідроптероатсінтетаза.
Споровики (малярійні плазмодії, токсоплазми та
ін.) не здатні утилізувати экзогенні фолати і мають ферменти, що каталізують їх
синтез. Дигідроптероат синтетаза перетворює птеридин і р-амінобензойну кислоту
в дигідроптероєву кислоту - попередник дигідрофолієвої кислоти. Активність
ферменту пригнічує сульфадоксин, а також конкурентні антагоністи
р-амінобензойної кислоти - сульфаніламіди і сульфони.
Піруватсінтетаза.
Піруват сінтетаза (піруват-ферредоксин
оксідоредуктаза). У анаеробних найпростіших (трихомонади, ентоамебы) немає
мітохондрій, але вони експресують піруват синтетазу. Фермент катализує
утворення ацетил-КоА в ході електронного транспорту, у тому числі перенесення
электронів від пірувату на нітрогрупи похідних нітроімідазола (метронідазол). В
результаті нітрогрупи відновлюються в токсичні нітрозогідроксиламіногрупи.
Метаболіт, що депонує, викликає множинні порушення структури ДНК.
Нуклеозидфосфотранзферази.
Багато найпростіших не здатні синтезувати
пуринові нуклеотиди de novo, але експресують трансферази, пуринові, що
фосфорилюють, і піримідинові основи.
·
У лейшманій пуриннуклеозид фосфотрансфераза переносить фосфатну
групу в 5 ' - положення пуринових нуклеозидів. Цим же шляхом фермент фосфорилює
структурні аналоги пуринових нуклеозидів - алопуринол рібозид, форміцин В і
тіопуринол рібозид. У формі трифосфатів ці препарати можуть вбудовуватися в
нуклеїнові кислоти або інгібувати активність ферментів, що беруть участь в
метаболізмі пуринів.
·
У трихомонад конверсію екзогенного тимідину в тимідин 5 ' - фосфат
здійснює тимідин фосфотрансфераза, її активність вибірково пригнічує гуанозин.
Тріпанотіонредуктаза.
Природний трипептид глутатіон у відновленій формі
діє як донор, а в окисленій - як акцептор водню. У клітинах трипаносом
глутатіон є присутнім у формі трипанотіона - унікального кон'югата із спермідином. За
допомогою трипанотіон редуктази трипанотіон виконує важливу роль в підтримці у
відновленому стані тіолов клітинних мембран.
Ніфуртимокс і меларсопрол інгібують активність
цього ферменту, що призводить до надмірного накопичення токсичних кисневих
продуктів в трипаносомах. В результаті відбувається окиснення тіолів і загибель
паразитів, оскільки вони не синтезують каталази і глутатіон пероксидази.
Незамінні ферменти найпростіших.
Ці ферменти синтезуються як в клітинах
найпростіших, так і в клітинах ссавців. Але на відзнаку від ссавців для
найпростіших ці ферменти абсолютно незамінні. Крім того, ферменти, які
синтезуються клітинами ссавців та найпростіших, відрізняються по специфічності
до субстратів.
Пуринофосфорибозилтрансферази.
У лейшманій та трипаносом ключовим ферментом
утворення пуринів є гіпоксантин-гуанін-фосфорибозол трансфераза. Аллопуринол
рибозид - структурний ізомер гіпоксантина, слугує субстратом для ферментів
паразитів, але не для фермента, який синтезується клітинами ссавців. Препарат
перетворюється в риботид і після фосфорилювання вбудовується в РНК. Аналогічним
чином препарат діє на лямблії, у яких ключовими ферментами синтеза пуринових
нуклеотидів виступають аденін - та гуанінфосфорибозил трансферази.
Орнітиндекарбоксилаза.
Орнітин декарбоксилаза регулює синтез поліамінів
у трипаносом, плазмодіїв та лямблій. Ефлорнітин інгібує фермент та призводить
до дестабілізації молекул ДНК та порушенням її реплікації.
Гліколітичні ферменти.
Трипаносоми, які циркулюють у крові, не мають
мітохондріальних дихальних ферментів та для відновлення НАД використовюють
гліцерол-3-фосфатоксидазу та гліцерол-3-фосфатдегідрогеназу. Препарат сурамін
блокує дію обох ферментів та чинить опір окисненню НАДФ та тим самим порушую
синтез АТФ.
Препарати для лікування та профілактики малярії.
Протималярійні препараті включають похідні
хіноліна (хлорохін, хінін, примахін) та похідні піримідина (хлоридин). Так як
ці препарати діють на різні стадії розвитку малярійного плазмодія, ії
підрозділяють на декілька груп:
гематошизотропні засоби (подавляють
еритроцитарну шизогонію) - хінін, артемізин
- гістошизотропні засоби (подавляють
тканеву шизогонію) - хлорідин, прімахін
засоби, що діють на прееритроцитарні
(первинні тканеві) форми - хлорідин, прімахін, прогуаніл
препарати, що діють на параеритроцитарні
(вторинні тканеві) форми
гамонотропні засоби (подавляють статеві
форми) - прімахін, хлорідин
Препарати для лікування амебіазу.
Універсальним засобом, ефективним при кишковому
та внєкишковому амебіазі, вважають метронідазол. Механізм його
протипаразитарної дії схожий з його дією на бактерії. Крім того, метронідазол,
який взаємодіє з нуклеотидами, подавляє синтез ДНК та РНК. Препарат дає мало
ефекту у відношенні до амеб, які знаходяться у просвіті кишковика та не діє на
цисти паразитів.
Препарат хініофон інгібує синтез ДНК та РНК та
подавляє життєдіяльність вегетативних форм а також утворення цист у просвіти
товстої кишки.
Препаратом вибору, який діє на амеб в стінці
кишковика та в печінці прийнято вважати еметин - алкалоїд корня іпекакуани.
Трихомоніаз, лямбліоз, балантидіаз та
токсоплазмоз.
Для лікування лямбліоза придатні похідні
нітромідазолу (метронідазол, тінідазол). Хіміотерапію тріхомоніазу іноді
доповнюють похідними нітрофурану (фуразолідон, фурагін). При лікуванні
балантидіазу добре діють антибиотики тетрацикліни та хініофрон. Для подавлення
життєдіяльності Toxoplasma gondii призначають піріметамін, інгібуючий дигідрофолат
редуктазу та порушуючий синтез ДНК, а також хлоридин та сульфаніламіди.
Лейшманіози.
Серед засобів хіміотерапії лейшманіозів препарати
вибору - п’ятивалентні сполучення окису сурьми. Ці лікарськи засоби
трансформуються у трьохвалентні сполучення, які мають змогу зв’язувать SH-групи білків, що
призводить до блокади ферментів, які беруть участь у циклі Кребса. Для
лікування шкіряних уражень місцево вживають мепракін та метронідазол, я в
якості альтернативи - пентамідин, призначаємий також при пнєвмоцистозах.
Складність отримання противірусних засобів
обумовлена тісним зв'язком етапів репродукції вірусів з метаболічними,
енергетичними і ферментативними реакціями зараженої клітини. В результаті
будь-який противірусний препарат практично завжди чинить токсичну дію і на
внутрішньоклітинні процеси. Саме тому досі не знайдений "пеніцилін"
для вірусів. Розробка противірусних засобів вимагає залучення досягнень у
вивченні молекулярної біології вірусів, інфекційної імунології і принципів
лікування бактерійних інфекцій. У цьому плані особливу увагу привертають
природні з'єднання (в першу чергу ІФН), що індукують антивірусний стан клітини,
і перспективи виділення з клітин макро- і надмолекулярних продуктів, що
проявляють антивірусний ефект. По характеру дії і клінічній значущості
препарати, вживані для лікування вірусних інфекцій, підрозділяють на чотири
основні групи - етіотропні, імуномодулюючі (коригуючі дефекти імунного
реагування, що розвиваються при захворюванні), патогенетичні (спрямовані на
боротьбу з інтоксикацією, зневодненням, судинними і органними поразками,
алергічними реакціями, а також на профілактику бактерійних суперінфекцій) і
симптоматичні (що купірують супутню симптоматику, наприклад кашель, головний
біль та ін.). Більшість етіотропних препаратів мають вузький спектр активності
(у кращому разі, в межах одного сімейства). Відомі лише декілька препаратів, що
впливають на ранні етапи репродукції, і жодного лікарського засобу,
подавляючого зборку дочірніх популяцій. Великим досягненням в розробці
противірусних засобів виявилися лікарські засоби - аналоги нуклеотидів
(аномальні нуклеотиди). Ці лікарські засоби діють як антіметаболіти, що
обумовлено їх структурною схожістю з пуриновими і пиримидиновыми основами.
Основні механізми антивірусної дії препаратів пов'язані з пригніченням
активності вірусних полімераз. Аналогію з нуклеотидами лікарські засоби
здобувають в результаті їх фосфорилювання клітинними і деякими вірусними
кіназами. У формі нуклеотидных аналогів препарати інгібують вірусні
ДНК-полімерази і виступають субстратами для вірусних ферментів; в результаті
лікарські засоби вбудовуються у вірусні нуклеїнові кислоти, утворюючи дефектні
полінуклеотиди або обриваючи їх подальший ріст. Селективний ефект лікарських
засобів забезпечує більший їх аффінитет до вірусних полимераз в порівнянні з
природними нуклеотидами. Крім того, вірусні ферменти більше лабільні до їх дії
в порівнянні з полімеразами клітин ссавців [12].
Протипухлинні антибіотики представлені
препаратами, що мають цитотоксичну дію. Більшість з них застосовують при
багатьох видах пухлин, наприклад мітоміцин С [11]. Нині досліджені тисячі зразків
антибіотиків для виявлення такових, які б мали високу протипухлинну
ефективність. Проте для клінічного використання доки допущено усього лише
декілька антибіотиків: з групи антрациклінів - доксорубіцин (адріаміцин),
акларубіцин і рубомицин (даунорубіміцин); з групи актіноміцинов - актіноміцины
С і Д; з групи ауреолової кислоти - олівоміцин; з групи стрептонігрина -
брунеоміцин [7].
Антибактеріальна дія антибіотиків може бути
бактерицидною (наприклад у пеніцилінів, цефалоспоринів) та бактеріостатичною
(наприклад у тетрациклінів, левоміцетину). При збільшенні дози бактеріостатичні
антибіотики також можуть викликати загибель бактерій. Аналогічними типами дії
володіють протигрибкові антибіотики: фунгіцидним та фунгістатичним.
Зазвичай при тяжких захворюваннях призначають
бактерицидні та фунгіцидні антибіотики. Дія антибіотиків на мікроорганізми
пов’язана з їх здатністю подавляти ті або інші біохімічні реакції, які
протікають в мікробній клітині. В залежності від механізму дії розрізняють п’ять груп
антибіотиків:
антибіотики, порушуючі синтез клітинної
стінки. До цієї групи належать, наприклад, В-лактами. Препарати цієї групи
характеризуються найвищою вибірковістю дії: вони вбивають бактерії та не чинять
ніякої дії на клітини макроорганізма, так як останні не мають головного
компоненту клітинної стінки бактерій - пептидоглікану. В зв’язку з цим В-лактамні
антибіотики є найменш токсичними для макроорганізму [11].
До В-лактамних антибіотиків відносяться
цефалоспорини, карбапенеми, пеніціліни, монобактами. Усі В-лактамні антибіотики
володіють схожою структурою та механізмами антимікробної дії. Вони гальмують
синтез пептидоглікану та селективно пригнічують активність ферментів, які
беруть участь у термінальній перехресній сшивці лінійних молекул глікопептидів
[12].
антибіотики які порушують молекулярну організацію
та синтез клітинних мембран. Прикладами подібних препаратів є поліміксини та
полієни [11].
ЦПМ слугує селективно проникним бар’єром,
порушення її функцій призводить до виходу з клітини білків, пуринових та
піримідинових нуклеотидів, іонів з послідуючою її загибеллю. До препаратів цієї
групи належать поліміксини, полієнові антибіотики та граміцидини [12].
Антибіотики, які порушують синтез білка. Це
найбільша група препаратів. Передставниками цієї групи є аміноглікозиди,
тетрацикліни, макроліди, лєвоміцетин, які викликають порушення синтезу білка на
різних рівнях [11].
Бактерії мають 70 S рибосоми, а клітини
ссавців - 80 S рибосоми. Субодиниці цих типів рибосом та їх функціональна
специфічність сильно різняться, що і пояснює подавлення синтезу білка
антибиотиками на бактеріальних рибосомах без вираженої дії на рибосоми ссавців
[12].
антибіотики - інгібітори синтезу
нуклеїнових кислот. Наприклад, хінолони порушують синтез ДНК; рифампіцин -
синтез РНК [11].
Рифампіцини - продукти життєдіяльності Streptomyces mediterranei. Найбільш відомий
полусинтетичний препарат рифампіцин. Бактеріальна активність рифампіцина
зумовлена інгібуванням ДНК-залежної РНК-полімерази, що призводить до
гальмування любих видів бактеріальної РНК, а також пізніх стадій самосборки
поксвірусів [12].
антибіотики, які подавляють синтез пуринів та
амінокислот. До цієї групи відносяться, наприклад, сульфаніламіди [11].
Сульфаніламіди - перші антибактеріальні засоби
широкого спектру дії, які знайшли призначення в медицині як системні
бактеріостатики [12].
Антибактеріальна дія сульфоніламідів було
виявлено емпірично (Домач); лише пізніше ключ до поняття механізму цієї дії
було знайдено в структурному сходстві між сульфоніламідами та р-амінобензойною
кислотою. р-Амінобензойна кислота входить до складу одного з коферментів,
точніше тетрагідрофолієвої кислоти. У більшості бактерій тетрагідрофолієва
кислота синтезується з більш простих компонентів. Але при додаванні до
поживного середовища р-амінобензойну кислоту або сульфоніламідів ці речовини
без усіляких зусиль проникають у клітину та включаються у фолієву кислоту [15]. Сульфаніламідні
препарати проявляють бактеріостатичну дію, конкурентно пригнічуя дігідроптероат
синтетазу, що попереждає утворення дигидрофолієвої кислоті та відповідно
тетрагідрофолієвої кислоти, необхідної для синтеза пуринових та пірамідинових
основ. У результаті пригнічується ріст та розмноження мікроорганізмів.
Активність сульфоніламідів: більшість грампозитивних бактерій (стрептококи,
актіноміцети, паличка сибірської виразки), гриби та найпростіші. Багато
грамнегативних бактерій резистентні до сульфаніамідів. Клітини ссавців
відчувають невелику дію препаратів, так як неспроможні до синтезу фолієвої
кислоти (основні потреби задовільняються за рахунок потрапляння її з їжею) [12]. Тому в організмі
ссавців сульфонамід не може включатися в цей кофермент і не може, таким чином,
чинити шкоду [15].
Структурно близькі до сульфаніламідів
парааміносаліцилова кислота (ПАСК) та сульфони (наприклад, дапсон) проявляють
аналогічну дію та ефективні при дікуванні різних мікобактеріозів (туберкульоз,
лєпра) [12].
4.2
Зміни мікроорганізмів, викликані антибіотиками
Окрім того, що антибіотики чинять негативну
побічну дію на макроорганізм, вони можуть викликати небажані для людини зміни
самих мікроорганізмів.
І група небажаних змін - поява атипових форм
мікроорганізмів. У мікробів можуть змінюватися морфологічні, біохімічні та
другі властивості. Наприклад, наслідком антибіотикотерапії може бути утворення L-форм бактерії.
Мікроби із зміненими властивостями важко розпізнати (ідентифікувати) та, як
наслідок, важко встановити діагноз хворому, у якого вони знайдені.
ІІ група - формування антибіотикостійкості [2].
Відомо два типи стійкості мікроорганізмів до
антимікробних засобів - природна та придбана. Природна резистентність
відноситься до видових ознак мікроба. Вона в основному пов’язана з відсутність
мішеней на клітинній стінці або непроникністю останньої для певних лікарських
засобів.
Хіміорезистентність у бактерій.
До основних механізмів резистентності до дії
антибактеріальних засобів відносять здатність до синтезу інактивуючих ферментів
та модифікацію мішеней, з якими взаємодіє лікарський препарат.
Стійкість, непов’язана з наслідуємими формами.
Більшість антибактеріальних засобів ефективно
подавляє життєдіяльність тільки тих клітин, що активно ростуть. Значна частина
збудників, залишаючись в латентній стадії, здатна виживати в тканинах багато
років, залишаючись при цьому резистентними до дії лікарських засобів
(наприклад, мікобактерії туберкульозу).
Хіміотерапія здатна зменшувати кількість мішеней
для дії препрату. Наприклад, під дією пеніцилінів окремі бактерії здатні
трансформуватися у L-форми, які позбавлені клітинної стінки і тому резистентні до
дії антибиотиків з подобним механізмом дії.
Стійкість, зумовлена змінами генома.
Мутації призводять до зміни структурних білків
(наприклад, в структурі 30 S субодиниць рибосом, поринів або
пеніцилін-зв’язуючих білків клітинної стінки) та ферментів. Також можливі
мутації в локусі гена, що кодує чутливість до лікарських засобів [12].
Існує три умови, при яких антибіотик може
спричинити бактерицидну чи бактеріостатичну дію на мікробну клітину:
антибіотик повинен проникнути в клітину;
- антибіотик повинен взаємодіяти з так
званою мішенню, тобто зі структурою яка виконує важливу для життєдіяльності
бактерій функцію та подавити цю функцію;
антибіотик повинен при цьому зберегти
свою структуру.
Якщо деяка з цих умов не виконується, бактерія
отримує стійкість [11].
4.3
Побічна дія антибіотиків
З отриманих тисяч антибіотиків в клінічній
практиці знаходять застосування лише 150-200 препаратів. Пояснюється це тим, що
велика кількість антибіотиків, які є ефективними антимікробними засобами,
спричинюють виражену негативну дію на макроорганізм і для лікування не можуть
бути використані. Навіть ті кілька десятків антибіотиків, котрі
використовуються, як і всі лікарські препарати, мають побічну дію.
Розрізнюють кілька груп ускладненої
антибіотикотерапії.
Токсичні реакції. Токсична дія антибіотиків
залежить від властивостей препарату, його дози, способу введення, стану
хворого. Серед ускладнень цієї групи на першому місці стоїть ураження печінки.
Такої дією володіють наприклад тетрацикліни. Друге місце посідають антибіотики
з нефротоксичною дією, наприклад аміноглікозиди. Левоміцетин може порушувати
органи кровотворення, він же володіє ембріотоксичною дією. Цефалоспорини ІІІ
покоління порушують синтез вітаміну К, в результаті чого можливі кровотечі.
Найменш токсичний із використовуваних антибіотиків пеніцилін, але при тривалому
його застосуванні можливе ураження ЦНС.
Дисбіози. При використанні антибіотиків широкого
спектру дії поряд зі збудниками захворювання, для знищення яких їх
застосовують, гинуть і деякі представники нормальної мікрофлори, чутливі до цих
антибіотиків. Звільняється місце для антибіотикорезистентних мікроорганізмів,
які починають швидко розмножуватись та можуть стати причиною вторинних
ендогенних інфекцій, як бактеріальних так і грибкових.
Дія на імунітет. Застосування антибіотиків може
викликати алергічні реакції, виникнення яких залежить від властивостей
препарату (найбільш сильними алергенами є пеніциліни та цефалоспорини), способу
введення та індівідуальної чутливості хворого. Можуть з’являтися висип, зуд,
кропивниця та ін. Дуже рідко виникає таке тяжке ускладнення як анафілактичний
шок.
Імунодепресивна дія. Наприклад, левоміцетин
пригнічує утворення антитіл, тетрациклін пригнічує фагоцитоз. В останні роки
при операціях по трансплантації органів та тканин дуже широко застосовують
циклоспорин, який попереджає їх відторгнення. Цей препарат було вилучено як
протигрибковий засіб, але його імунодепресивна дія значно перевищує його
антимікробні властивості. Велика кількість антибіотиків діє негативно на різні
відділи імунної системи. Що викликає необхідність призначати їх дуже обережно
[11].
5.
Принципи раціональної антибіотикотерапії
Раціональна антибіотикотерапія інфекційних
захворювань базується на результатах бактеріологічної діагностики захворювання
з виділенням та ідентификацією збудника. При цьому дуже важливо мати інформацію
про чутливість збудника захворювання до антибактеріального препарату, вибраного
для лікування.
У клінічній практиці чутливими до антибіотика
вважаються ті мікроорганізми, на які випробуваний антибіотик в концентрації,
оптимальній у джерелі інфекції, спричинює бактеріостатичну або бактерицидну дію
[9].
Практичне використання антибіотиків полягає у
слідуючому:
при лікуванні інфекційних захворювань
людини та тварин. Але вони можуть мати побічну дію: викликати алергії,
дисбактеріози. Анафілактичний шок та навіть смерть, тому приймати антибіотики
слід цілком обережно;
- для захисту рослин від захворювань, які
викликають бактерії та гриби;
для стимуляції росту
сільськогосподарських тварин;
для попередження псування м’яса, риби та інших
продуктів;
як інструменти для дослідження
специфічних функцій клітини [10].
Мікробіологічний принцип. Антибіотики слід
використовувати лише по показанням, коли захворювання викликане
мікроорганізмами, по відношенню до яких існують ефективні препарати. Для їх
підбору необхідно до призначення лікування взяти у хворого матеріал для
дослідження, виділити чисту культуру збудника та виявити його чутливість до
антибіотиків [11]. Часто в якості
епідемічного маркера використовують резистограму штаммів - дані по їх
стійкості/чутливості до хіміопрепаратів, що дозволяє оцінити ідентичність
штамів, виділених з різних джерел. При використанні антибіотиків на практиці
важливо визначити чутливість до них клінічно важливих штаммів мікроорганізмів [3].
Чутливість до антибіотиків, або антибіотикограму,
визначають за допомогою методів розведення та дифузії (до них відноситься метод
паперових дисків) [11]. Методи розведення є більш чутливими: за їх допомогою
виясняють, який антибіотик має ефект по відношенню до даного мікроорганізму, та
визначають його необхідну кількість - мінімальну подавляючу концентрацію (МПК)
[2]. Чутливість мікроорганізмів до антибіотиків та іншим ХТП необхідно
визначати в кожному випадку інфекції та періодично - в ході лікування.
Головним показником чутливості є мінімальна
інгібуюча концентрація - МІК (мкг/мл), тобто мінімальна концентрація
антибіотика, яка здатна затримувати ріст мікроба-збудника в стандартному
досліді. Значення величини МІК визначають методом серійних розведень або
методом дифузії в агар (дисками або Е-тестами).
В кожному випадку критерієм чутливості є значення
величини терапевтичного індексу Т = МІК/К, де К - концентрація даного
антибіотику (мкг/мл) у місці інфекції (або у крові) при введенні терапевтичних
доз препарату.
Мікроб чутливий, а антибіотик звичайно ефективний
при Т<0,3.
Значення
К можливо знайти в спеціальних таблицях [3].
По ступеню чутливості до антибіотиків патогенні
мікроорганізми діляться на чотири групи:
) чутливі - звичайні терапевтичні дози
антибіотиків є достатніми для досягнення лікувального ефекту при загальних
захворюваннях;
2) середньо чутливі - лікувальний ефект
препарата при загальних захворюваннях досягається тільки в результаті
призначення збільшених доз антибіотику;
) помірно стійкі - лікувальний ефект
досягається тільки при локалізації середовища інфекції в місці, де має місце
концентрація антибіотика, або якщо антибіотик можливо ввести безпосередньо у
середовище інфекції;
4) стійкі - лікувальній ефект при призначенні
антибіотика відсутній [9].
Ефект антибіотику для лікування залежить від
чутливості збудника, можливості досягнення середовища інфекції без зниження
активності антибіотика та від його побічної дії [3].
Фармакологічний принцип. При призначенні
антибіотика необхідно визначити правильне дозування препарату, необхідні
інтервали між введенням лікарського засобу. Тривалість антибіотикотерапії,
методи введення. Слід знати фармакокінетику препарату, можливості взаємодії
різних лікарських засобів.
Як правило, лікування інфекційних захворювань
триває за допомогою одного антибіотику (моноантибіотикотерпія). При
захворюваннях довготривалих (септичний ендокардит, туберкульоз та інші) для
попередження формування антибіотикорезистентності застосовують комбіновану
антибіотикотерапію.
Клінічний принцип. При призначенні антибіотиків
враховують загальний стан хворих, вік, стать, стан імунної системи, супутні
захворювання, наявність вагітності.
Епідеміологічний принцип. При виборі антибіотику
необхідно знати, до яких антибіотиків стійкі мікроорганізми у середовищі, що
оточує хворого (відділення, лікарня, географічний регіон). Розповсюдження
стійкості до даного антибіотика не залишається постійною, а змінюється в
залежності від того, наскільки широко використовується антибіотик.
Фармацевтичний принцип. Необхідно враховувати
строк та умови зберігання препарату, так як при його тривалому та неправильному
зберіганні утворюються токсичні продукти деградації [11].
Антибіотикотерапія - це лікування інфекційних та
пухлинніх захворювань антибактеріальними препаратами, які не є продуктами
реакції організма на збудника.
До таких препаратів пред’являють ряд вимагань.
Антибіотик повинен володіти етіотропністю, тобто пригнітять життєдіяльність та
розвиток збудника захворювання або пухлинних клітин. Антибіотики повинні
достатньо добре розчинятися у воді, так як тільки в розчинному стані вони
можуть потрапити у внутрішнє середовище організму. Антибіотики, з одного боку,
повинні бути достатньо стабільні у внутрішньому середовищі організму, але, з другого
боку не повинні мати кумулятивного ефекту [8]. Антибіотики повинні бути ефективні в низьких
концентраціях; не спричиняти імунодепресивного ефекту [13].
Крім того, речовини, які використовуються для
антибіотикотерапії, повинні бути нешкідливі. Не дивлячись на те, що любий
антибактеріальний препарат володіє тією чи іншою побічною дією на
макроорганізм, ця дія повинна бути по можливості мінімальною, а тератогенний та
мутагенний ефекти по можливості повинні бути відсутні [8].
Висновки
Виконавши огляд літератури з теми "Поняття
про антибіотики. Основні властивості, класифікація" можна зробити наступні
висновки:
антибіотики це хіміотерапевтичні
речовини, що продукуються мікроорганізмами, тваринними клітинами, рослинами, а
також їх похідні і синтетичні продукти, які володіють виборчою здатністю
пригноблювати і затримувати ріст мікроорганізмів, а також пригнічувати розвиток
злоякісних новоутворень.
- антибіотики це відносно молоде наукове
відкриття. Історія розвитку антибіотиків для застосування у медицині та інших
отраслях нараховує менш ніж сто років. Відкриття антибактеріальних речовин,
продукуємих мікроорганізмами стало революційною подією в мікробіології та
започаткувало розвиток нового напрямку досліджень.
На сьогодні винайдено та розроблюється
кілька тисяч антибіотичних засобів, та у медичній практиці знайшли своє
застосування лише 150 - 200 антибактеріальних препаратів. Причиною того, що не
всі антибіотики можна застосовувати для лікування інфекційних та онкологічних
хвороб є те, що антибіотики можуть негативно впливати на макроорганізм і таким
чином приносити не тільки користь, але й завдавати шкоди. Тому найважливіше
питання при дослідженні антибактеріальних речовин є поєднання у одному
лікувальному засобі високої ефективності та мінімального негативного впливу на
організм хворого.
Друге питання постає при виробництві
антибактеріальних препаратів. Виробництво повинно бути високопродуктивним та
рентабельним. Це змушує робити інтенсивні дослідження, спрямовані на підвищення
продуктивності процесу. Особливо успішним виявився в цьому плані генетичний
відбір.