Выбор реактора для проведения реакции гидрирования ацетона до спирта
Содержание
Введение
1. Получение изопропилового спирта из ацетона
2. Тепловой и материальный баланс адиабатического РИВ и
РПС
. Программы расчета и результаты
3.1 Выбор реактора
3.2 Расчет Ad
коэффициента
.3 Производительность в зависимости от начальной температуры
.4 Производительность в зависимости от давления
.5 Производительность в зависимости от начальной
концентрации
Выводы
Список использованная литература
Введение
Под технологией в широком значении этого слова понимают научное описание
методов и средств производства в какой-то отрасли промышленности. Процессы
механической технологии основаны преимущественно на механическом воздействии,
изменяющем внешний вид или физические свойства обрабатываемых веществ, но не
влияющем на их химический состав. Процессы химической технологии включают
химическую переработку сырья, основанную на сложных по природе химических и
физико-химических явлениях.
Таким образом, химическая технология - это наука о наиболее экономичных и
экологически обоснованных методах химической переработки сырых природных
материалов в предметы потребления и средства производства.
Современная химическая технология, используя достижения естественных и
технических наук, изучает и разрабатывает совокупность физических и химических
процессов, машин и аппаратов, оптимальные пути осуществления этих процессов и
управления ими при промышленном производстве различных веществ, продуктов,
материалов.
Химическая технология базируется на химических науках, таких, как
физическая химия, химическая термодинамика и химическая кинетика, а также
развивает закономерности этих наук в приложении к крупномасштабным промышленным
процессам, она тесно связана с экономикой, физикой, математикой, кибернетикой,
прикладной механикой, другими техническими науками.
По мере развития химической промышленности содержание химической
технологии обогащалось новыми сведениями, закономерностями. Значительный
прогресс науки в последние годы связан с применением современных вычислительных
средств для решения теоретических и прикладных задач. Применение вычислительной
техники не только позволило ставить и решать сложные задачи, но и обогатило
химическую технологию новыми подходами к их решению, связанными с
математическим моделированием и системными исследованиями, также развивается
кибернетика химико-технологических процессов. Новые открытия тесно связывают
науку с производством, что позволяет более рационально использовать сырье и
топливно-энергетические ресурсы, создавать безотходные производства, где
процессы протекают с высокими скоростями в оптимальных условиях с получением
продуктов высокого качества.
Химическая технология играет важную роль в химической промышленности,
которая является одной из ведущих отраслей народного хозяйства, ей принадлежит
определяющая роль в ускорении научно-технического прогресса, повышении
эффективности общественного производства и, материального и культурного уровня
жизни людей.
Химическая технология является материальной базой химизации народного
хозяйства. Цель химизации - интенсификация и повышение эффективности
промышленного и сельскохозяйственного производства, улучшение условий труда и
повышение уровня медицинского, культурного и бытового обслуживания населения.
Химизация обеспечивает: совершенствование структуры сырьевого баланса, снижение
затрат на производство и эксплуатацию изделий, совершенствование
топливно-энергетической базы путем интенсификации процессов и комплексной
переработки нефти, природного газа, сланцев и угля, использования теплоты
реакций, усиление охраны окружающей среды.
Материальной основой всех химико-технологических процессов являются
машины и аппараты химических производств. Эффективность химического
производства обеспечивается за счет систематического повышения его технического
уровня на основе использования мощных, непрерывных, малостадийных и менее
энергоемких аппаратов. Так, выбор и расчет аппарата, ректификационной колонны,
реактора является важным критерием, определяющим технологический процесс.
Химико-технологический процесс представляет собой совокупность операций,
позволяющих получить целевой продукт из исходного сырья. Скорость всех этапов
операций будет зависеть от температурного режима, наличия примесей, а самое
главное - от гидромеханических, тепло- и массообменных, химических процессов,
протекающих в аппарате. Анализ единичных процессов, их взаимного влияния
позволяет разработать технологический режим и рассчитать аппараты, реакторы,
необходимые для проведения этих процессов в оптимальных условиях (сочетание
основных параметров - температуры, давления, состав исходной реакционной смеси,
катализаторов), т.е. таких, которые позволяют получить наибольший выход
продукта с высокой скоростью или обеспечить наименьшую себестоимость.
Разработка и построение рациональной технологической схемы, а
соответственно и выбор реактора, аппарата - важная задача химической
технологии.
1. Получение изопропилового спирта из ацетона
ацетон спирт химический
реактор
ЗАО "Химтэк Инжиниринг" владеет высокоэффективной технологией
гидрирования ацетона в жидкой фазе на никельсодержащем катализаторе.
Процесс ведется при давлении в реакторе 0,7-1,0 Мпа и температуре 70-1200С.
Срок службы катализатора составляет 1,5-2 года. Селективность гидрирования
близка к 100%. В реакторе достигается практически полное превращение ацетона.
Технология позволяет использовать водородсодержащие газы с концентрацией Н2
> 80%. Процесс ведется в адиабатическом режиме на стационарном слое
катализатора в жидкой фазе, при контактной нагрузке на катализатор 0,8-1 1/ч.
Уравнение реакции
3H60 + H2 < == > C3H80
Удельный расход сырья и энергетики
|
Ацетон
|
0,97 т/т
|
|
Водород
|
4 нм3/т
|
|
Катализатор
|
0,1 кг/т
|
|
Электроэнергия
|
10 кВт/т
|
|
Охлаждающая вода
|
8 м3/т
|
Для производства изопропилового спирта из ацетона необходима установка
гидрирования. Капитальные вложения на строительство установки гидрирования
мощностью 15-20 тысяч тонн составляют около 0,5 млн. долларов. В данном
технологическом процессе используется водород, поэтому наличие производства
водорода является преимуществом.
Стоимость переработки ацетона невелика и практически определяется
стоимостью водорода. Цена на ацетон подвержена резким колебаниям, бывают
сезонные периоды, когда его реализация затруднена и наблюдается избыток ацетона
на рынке. В среднем удельный вес затрат на ацетон в себестоимости ИПС
составляет около 80%, поэтому эта технология выгодна для предприятий,
располагающих дешевым ацетоном.
Ацетон.
Свойства
Диметилкето́н (ацето́н, 2-пропанон) - простейший представитель кетонов
<#"580997.files/image001.gif">

Материальный
баланс РИВ
Рассмотрим химическую реакцию в общем виде:
aA + bB ↔ cC + dD
Выберем бесконечно малый объём реактора dV.
Физический приход:
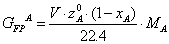
[кг/c]=[(м3/с)/(м3/кмоль)]∙(кг/кмоль)
Физический
расход:
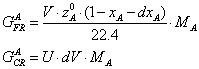
[кг/с]=[(кмоль/м3∙с)∙(м3)∙(кг/кмоль)
Согласно
закону сохранения массы веществ, экстраполируя его на случай реактора приравниваем
расходную и приходную часть, сокращая на 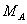 :
:
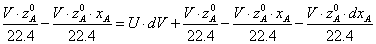
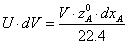
Учитывая,
что 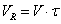 , а
, а 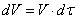 получим
получим
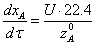 -
уравнение материального баланса РИВ
-
уравнение материального баланса РИВ
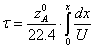 -
характеристическое уравнение
-
характеристическое уравнение
Тепловой
баланс РИВ
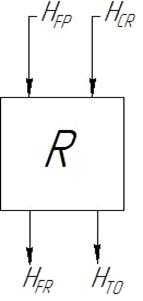
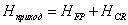
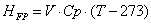 -
теплота физического прихода
-
теплота физического прихода
[кДж/с]=[(м3/c)∙(кДж/м3/град)∙(град)]
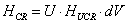 - теплота
химической реакции
- теплота
химической реакции
[кДж/c]=[(кмоль/м3∙c)∙(кДж/кмоль)∙(м3)]
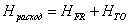
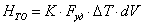 -
теплота, расходуемая на теплообменные устройства
-
теплота, расходуемая на теплообменные устройства
[кДж/c]=[(кДж/м2∙град∙с)∙(м2/м3)∙(град)∙(м3)]
[кДж/с]=[(м3/c)∙(кДж/м3/град)∙(град)]
По
закону сохранения энергии:
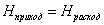
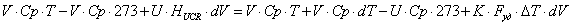
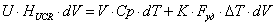 -
уравнение политермы
-
уравнение политермы
Согласно
уравнению материального баланса РИВ имеем:
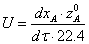
Заменив
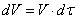 и опустив индексы перед переменными, имеем
и опустив индексы перед переменными, имеем
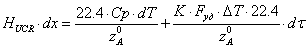 -
уравнение политермы
-
уравнение политермы
В
случае работы реактора в адиабатическом режиме слагаемое
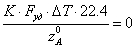 так как
отсутствует теплообменное устройство, и тогда получим:
так как
отсутствует теплообменное устройство, и тогда получим:
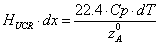 отсюда,
разрешая уравнение относительно
отсюда,
разрешая уравнение относительно 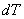 , получим
, получим
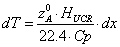
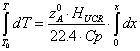
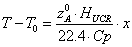
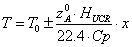 ,
,
где
верхний знак(+) относится к экзотермической реакции, а нижний(-) - к
эндотермической.
Введём
обозначения:
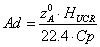 -
адиабатический коэффициент
-
адиабатический коэффициент
Физический
смысл адиабатического коэффициента: на столько градусов изменится температура
реакционной смеси, если степень превращения будет равна 1, то есть, если
ключевой реагент прореагировал полностью.
Тогда
уравнение адиабаты примет вид:
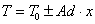
Материальный
баланс РПС
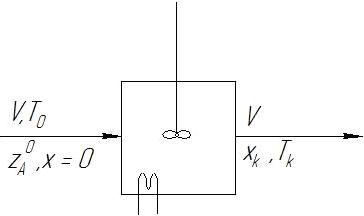
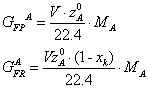
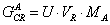
Составим
материальный баланс:
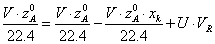
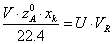
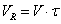
Таким
образом,
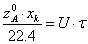
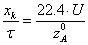 -
уравнение материального баланса РПС
-
уравнение материального баланса РПС
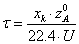 -
характеристическое уравнение РПС
-
характеристическое уравнение РПС
Тепловой
баланс РПС
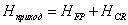
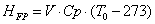 -
теплота физического прихода
-
теплота физического прихода
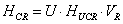 - теплота
химической реакции
- теплота
химической реакции
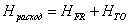
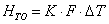 - теплота
на теплообменные устройства
- теплота
на теплообменные устройства
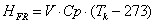 -
теплота физического расхода
-
теплота физического расхода
По
закону сохранения энергии:
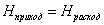
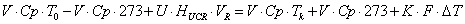
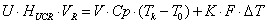 -
уравнение политермы
-
уравнение политермы
Согласно
уравнению материального баланса РИВ имеем:
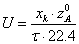
Заменим
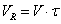 и получим
и получим
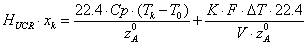 -
уравнение политермы
-
уравнение политермы
При
адиабатическом режиме работы реактора слагаемое
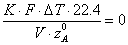 и тогда
получим:
и тогда
получим:
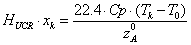
отсюда
получим
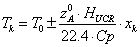 -
уравнение адиабаты
-
уравнение адиабаты
Верхний
знак(+) в этом уравнении относится к экзотермической реакции, а нижний(-) - к
эндотермической.
Введём
обозначения:
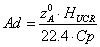 -
адиабатический коэффициент
-
адиабатический коэффициент
Тогда
уравнение адиабаты примет вид:
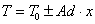
3. Программные расчеты и результаты
.1 Выбор реактора
Обоснование выбора адиабатического реактора для гидрирования ацетона.
Сравнивая работу ректоров идеального вытеснения и полного смешения в
адиабатическом режиме при одном и том же времени, мы нашли значение степени
превращения и температуры, на основе этих данных вычислили значение скорости
реакции и получили, что скорость в РПС больше значения скорости РИВ при прочих
равных условиях, следовательно выбираем реактор полного смешения.
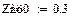

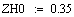
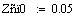
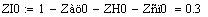
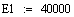
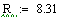
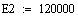

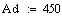
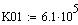
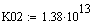
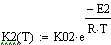
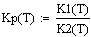
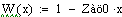
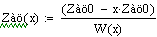
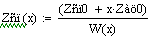
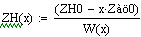
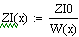
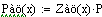
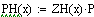
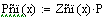
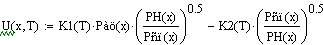
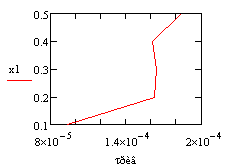

Выбираем одно фиксированное время τ=0.0001 с, при этом времени для РИВ степень
превращения х будет равно 0.11, а для РПС х получается равная 0.123
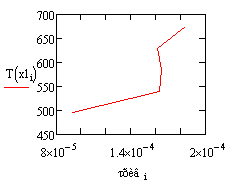

Выбираем фиксированном времени τ=0.0001 с, при это времени для РИВ
температура T=500, а для РПС Т=506.
Считаем скорость для РИВ и РПС при фиксир. степени превращения и температуре
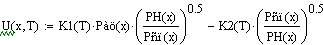
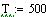
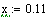
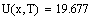
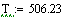
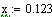
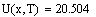
Скорость в РПС будет больше чем в РИВ, следовательно, выбираем РПС.
.2 Расчет Ad коэффициента
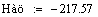
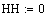
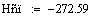
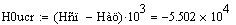
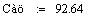
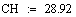
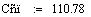
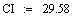
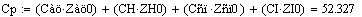
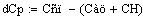
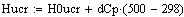
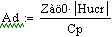
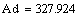
Анализ производительности реактора от T0, P, ZAo
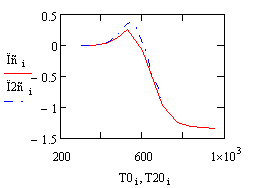
3.3 Производительность реактора от начальной температуры

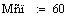
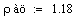
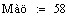


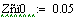
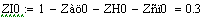
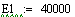
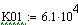
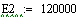
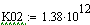
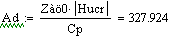

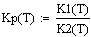
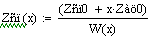
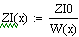
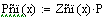
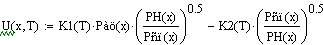
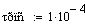
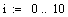
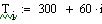
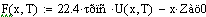
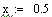
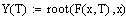
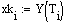
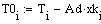
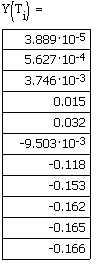
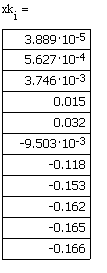
Производительность реактора
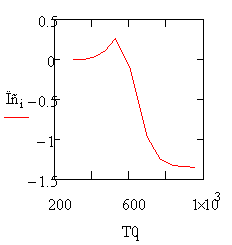

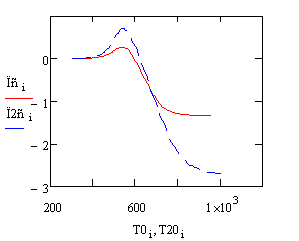
Из этого графика мы видим что самая высокая производительность в реакторе
получается при начальной температуре 529.39 градусов.
.4 Производительность от давления
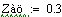
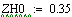
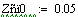
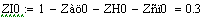
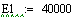
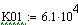
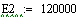
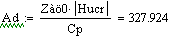
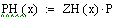
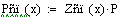
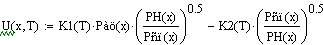
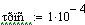
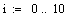
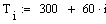
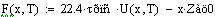
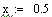
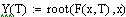
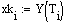
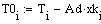
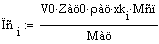
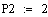
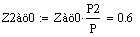

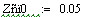
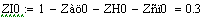
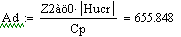
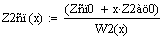
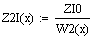
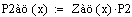
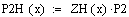
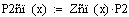
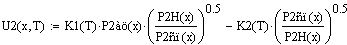
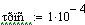
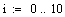
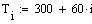
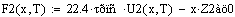
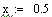
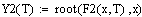
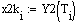
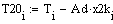
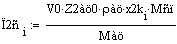


Из этого графика видно что при увеличении давления увеличивается
производительность реактора. Чем больше давление, тем и больше
производительность
.5 Производительность от концентрации ключевого реагента


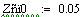
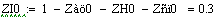

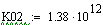
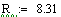
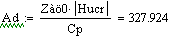

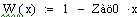
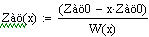
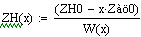
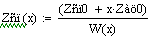
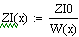
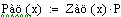
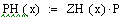
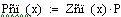
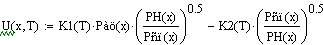
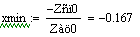
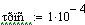
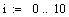
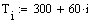
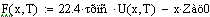
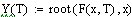
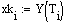
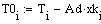
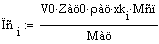
Увеличиваем начальную концентрацию ключевого реагента
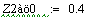

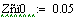
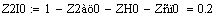
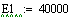
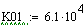
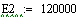
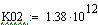
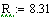


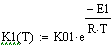
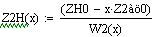
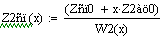
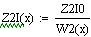
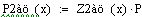
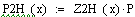
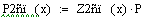
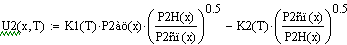
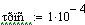
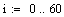
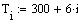
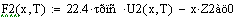
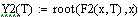
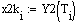
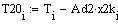
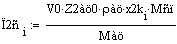

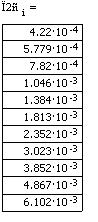
При увеличении начальной концентрации ключевого реагента увеличивается
производительность реактора.
Выводы
1. Обоснование выбора адиабатического реактора для гидрирования ацетона.
Сравнивая работу ректоров идеального вытеснения и полного смешения в
адиабатическом режиме при одном и том же времени, мы нашли значение степени
превращения и температуры, на основе этих данных вычислили значение скорости
реакции и получили, что скорость в РПС больше значения скорости РИВ при прочих
равных условиях, следовательно выбираем реактор полного смешения.
2. Зависимость производительности от начальной температуры.
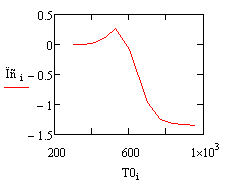
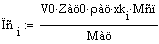
При увеличении температуры производительность сначала увеличивается до
достижения оптимальной температуры равной 530 градусов, а затем начинает
падать. Это объясняется тем что:
Производительность зависит только от степени превращения все остальные
факторы остаются постоянные, следовательно рассмотрим зависимость степени
превращения от начальной температуры.
График зависимости начальной температуры от времени имеет максимум,
следовательно зависимость степени превращения от начальной темпер. Так же будет
иметь максимум по уравнению адиабаты: 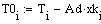
Так как производительность пропорциональна степени превращения то она так
же будет иметь максимум на графике в зависимости от степени превращения.
3. Зависимость производительности от давления.
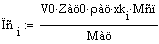
При увеличении давления производительность увеличивается, так как при
увеличении давления увеличивается концентрация ключевого реагента, а следовательно
возрастает и производительность.
. Зависимость производительности от начальной концентрации ключевого
реагента.
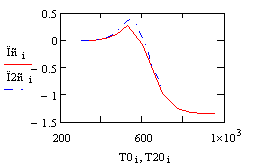
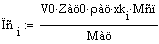
При увеличении начальной концентрации ключевого реагента увеличивается
производительность реактора. Так как в уравнен. производительн. Из всех
факторов изменяется только начальная концентрация.
Список использованной литературы
1. Власов Е.А. Основы химической технологии. Курс лекций,
2008.
2. Расчеты химико-технологических процессов: Учебное
пособие для вузов/Туболкин А.Ф., Тумаркина Е.С., Тарат Э.Я. и др.; под ред.
И.П. Мухленова - 2-е изд.,перераб. и доп. - Л.: Химия, 1982.-248 с.,ил
. Технология основного органического синтеза. И.И.
Юкельсон - издательство - химия- Москва 1968
. Справочник по физической химии Н.М. Барон, А.А.
Равдель, З.Н. Тимофеева-издательство-химия 1983.