|
Размер зерна,
мкм
|
Число
поверхностных атомов углерода (расчет), 1017 атомов С/г
|
Концентрация
спинов, 1016 спин/г
|
|
57±7
|
5
|
8
|
|
34±6
|
8
|
14
|
|
8,6±2
|
30
|
70
|
|
1
|
250
|
600
|
В работе [8] рассмотрены температурные эффекты структурных и
примесных дефектов в природных алмазах. На основе этих исследований авторы
предлагают уточненную модель парамагнитного центра, состоящего из
"разорванных" С-С связей, расположенных по краям азотных пластинок
("platelets") внутри кристалла алмаза (рис.1).
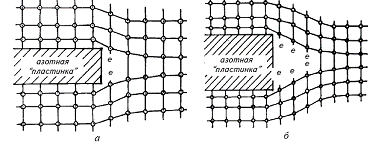
Рис.1. Модель парамагнитных центров на краю азотных
"пластинок" - "тонких" (а) и "толстых" (б).
Данные по исследованию ЭПР наноалмазов
Наноалмазы детонационного синтеза также как и другие типы
алмазных материалов, обладают парамагнитными свойствами. Вместе с тем, к
настоящему времени остается неясным вопрос о том, какова природа ЭПР сигнала
наноалмаза, а именно, обусловлен ли он поверхностными или объемными дефектами.
По-видимому, это связано со сложностью структуры наноалмазной частицы.
Авторы [9] показали, что образцы наноалмаза обладают высокой
концентрацией парамагнитных центров (до 1020 спин/г). Они объясняют
это структурными дефектами ("оборванные" С-С связи) на поверхности
алмазного кластера. Точнее, они относят возникновение сигнала ЭПР к поверхности
остова наночастицы, лежащего под слоями поверхностных групп и атомов
неалмазного углерода. Ими указан g-фактор, равный 2,00282+0,00003.
Дополняет эти данные работа [10]. В ней с помощью ЯМР-спектроскопии
изучены наноалмазы детонационного синтеза. На основе полученных данных авторы
предположили, что наночастица состоит из алмазного ядра, частично покрытого
фуллереноподобным покровом углерода в sp2-гибридизации; непокрытая
часть ядра содержит углеводородные группы, насыщающие "разорванные"
С-С связи. Примечательно, что для образцов УДА характерно большее время
спин-решеточной релаксации в сравнении с природным алмазом. Этот факт авторы
объясняют взаимодействием внутрирешеточных спинов со свободными радикалами,
расположенными между алмазным ядром и sp2-покровом.
В работе [12] исследованы субмикропорошки и наноалмазы
детонационного синтеза. Показано, что вид спектра ЭПР меняется с изменением
размеров частиц образцов. Формирование спектра авторы относят к разоpванным связям С-С на
поверхности наноалмаза.
Сходные явления описаны и авторами [11], которые изучали
отжиг образцов наноалмаза при 1600 °С и переход их в
нанографитовые частицы. По данным [11], ЭПР-сигнал УДА при 293 К представляет
собой синглет с g-фактором 2,003 и полушириной DН½ = 6,3-8,3 Э, что очень схоже с сигналом ЭПР,
полученным в [9] предположительно от "разорванных" связей на
поверхности алмаза. Причем, несмотря на высокую концентрацию атомов азота в
УДА, триплетный сигнал, обычно обусловленный примесными атомами азота,
замещающими углерод в решетке кристаллов алмаза других типов, не был
зарегистрирован.
Согласно [13], алмазные сферы и полиэдры диаметром 3-6 нм
содержат неспаренные спины в количестве 4·1019 спин/г, т.е. примерно
1 спин на частицу, и дают сигнал с g = 2,0027+0,0001. Причем эти
характеристики не зависят от природы функциональных групп, температуры,
состава, методов получения и очистки наноалмаза. Авторы объясняют это
существованием диамагнитной сердцевины и парамагнитной оболочки, определяемой
электронной плотностью поверхностных состояний.
В исследовании [14] отмечается, что наноалмазы размерами 4-5
нм весьма интересны как новый материал в исследовании электронных и магнитных
свойств. Показано, что такие наноалмазы несут многочисленные дефекты,
происходящие от "разорванных" С-С связей, расположенных в основном
внутри нанокристаллов. В таких наноалмазах наблюдается высокая (до 1021
спин/г) концентрация внешних свободных радикалов, образовавшихся на поверхности
после высокотемпературной обработки водородом. Обнаружено сильное
антиферромагнитное взаимодействие между спинами на поверхности.
В другом исследовании наноалмазов [15] в спектре ЭПР был
получен одиночный пик, соответствующий g = 2,003. Зарегистрированная ширина
линии и рассчитанная концентрация спинов составили 9,6 Г, 1100 ppm и 8,8 Г,
1300 ppm для мокрого и сухого способов синтеза образцов, соответственно. Также
было показано, что, хотя НА и был получен из смеси, содержащей сравнимые
концентрации атомов углерода и азота, не было зарегистрировано относящихся к
азоту парамагнитных центров. Таким образом, азот внедрялся в частицу наноалмаза
не в виде одиночных замещающих атомов, а в виде групп атомов. Возможно, он
находился в поверхностном слое или был частью неалмазных структур, которые были
удалены при очистке образцов.
Авторы [16], изучавшие температурное воздействие на
наноалмазы и их переход в графит, отметили, что значение g-фактора для
образца наноалмаза (2,0028) находится в хорошем соответствии со значением g-фактора
микрокристаллических алмазных порошков, приготовленных механическим
измельчением алмазных кристаллов.
Таким образом, из приведенных данных следует, что в
литературе нет единого мнения о природе ЭПР-сигнала наноалмазов и, как
следствие, о природе парамагнитных центров.
1.1.2 Методы
получения искусственных алмазов
Широкое использование, как отдельных свойств алмаза, так и их
сочетаний в научной и производственной практике долгое время сдерживалось
ограниченностью природных ресурсов алмаза, что вызвало необходимость его
синтеза.
1.1.2.1
Синтез алмаза методом статических сверхвысоких давлений
Впервые теоретически обосновал возможность синтеза алмаза из
графита советский ученый О.И. Лейпунский [17], который в 1937 г. построил
фазовую диаграмму "графит-алмаз".
Но синтезировать искусственный алмаз удалось лишь в 1953 г.
группе шведских учёных под руководством Э.Г. Лундблада [18]. Синтез проводился
при давлении 80000 атм и температуре 2500 оС. Алмаз кристаллизовался
из раствора графита в расплавленном железе. Идентификацию полученных кристаллов
производили по рентгенограммам.
Годом позже искусственные алмазы из графита были получены
этим методом группой учёных из США: Ф. Банди, Г. Холл, Г. Стронг и Р. Венторф
[19, 20]. Затем синтетические алмазы были получены в Швеции, Великобритании,
Голландии, ЮАР, Японии [21] и чуть позже во Франции и Чехословакии [22]. В
нашей стране первым синтезировал алмазы коллектив сотрудников АН СССР под
руководством академика Л.Ф. Верещагина [23].
После многочисленных экспериментов учёные определили ряд
условий и закономерностей образования алмаза рассматриваемым методом [24]:
давление и температура в системе должны
соответствовать области термодинамической стабильности алмаза;
- температура должна быть достаточно высокой для
плавления насыщенного углеродом металла-катализатора;
в качестве металлов-катализаторов можно использовать
Cr, Mn, Fe, Co, Ni, Ru, Rh, Pd, Ir, Os, Pt, Ta;
новый алмаз может образовываться как в присутствии
затравочных кристаллов, так и без них;
скорость роста алмазного кристалла может достигать
0,1 мм/мин;
градиент температуры может ускорять рост алмаза;
алмазы легко растут вокруг посторонних частиц,
присутствующих в смеси, особенно при высокой скорости роста.
Синтез алмаза при статическом давлении может быть осуществлён
не только из графита, но и из других углеродсодержащих веществ различной
природы, например, углеводородов (ароматических и неароматических), углеводов и
др. [25-26].
1.1.2.2
Синтез алмаза методом динамических сверхвысоких давлений
В динамическом синтезе реакционная масса,
представляющая собой графит или иной углеродсодержащий материал, либо их смесь
с металлами, подвергается кратковременному ударному воздействию, причем
температура, в отличие от статического синтеза, не может быть выбрана произвольно,
а является функцией состояния исходного материала и давления ударного сжатия
[29].
Существует три динамических способа синтеза.
. Собственно динамический синтез, в котором исходные вещества
помещают в прочные металлические контейнеры (ампулы сохранения) и подвергают
воздействию ударных волн, генерируемых детонацией взрывчатого вещества или
ударом пластин, разгоняемых продуктами детонации. При соударении на скоростях 1
км/с и более в ампуле и ее содержимом создаются давление до 100 ГПа и
температура до 3000 К. В ампулу закладывают смесь графита и металла. Последний
способствует повышению давления в реакционной смеси и снижению температуры, а
также служит для быстрого охлаждения алмаза после снятия давления. Достаточные
для синтеза алмаза температура и давление сохраняются в течение нескольких
микросекунд. При этом образуются поликристаллы размером до нескольких десятков
микрон. Основная доля алмазов имеет размер 7-10 мкм. Из-за специфических
условий ударноволнового взрывного синтеза полученные поликристаллы имеют много
режущих кромок и повышенную абразивную способность, превышающую в два раза
аналогичную способность естественных и искусственных алмазов. По этой причине
цена технических алмазов, производимых по такой технологии, в два раза
превышает цену других технических алмазов.
В 1961 г. американскими учёными П.С. Де Карли и Дж.Л.
Джемисоном [29] был впервые осуществлён синтез алмаза методом сжатия графита в
ударной волне при давлении до 300000 атм. Для получения столь высокого давления
рядом с исследуемым объектом производился взрыв мощного взрывчатого вещества
(ВВ). Одновременно с увеличением давления возрастает и температура.
Температура, возникающая на фронте ударного сжатия, зависит от свойств
исходного вещества, таких как сжимаемость, теплоёмкость, пористость и т.д. В
частности, чем больше сжимаемость, тем сильнее нагревается вещество (при
фиксированном давлении). Таким образом, при динамическом сжатии, в отличие от
статического, давление и температура оказываются функционально связанными между
собой.
В качестве углеродсодержащего материала в данном методе могут
использоваться графит, сажа или различные органические соединения. Процесс
завершается за очень короткий промежуток времени, поэтому размеры получающихся
алмазов не превышают нескольких микрон, что значительно меньше, чем в случае
синтеза при статических давлениях. Кроме того, в продуктах синтеза
обнаруживается как алмазный, так и неалмазный углерод [30, 31].
. В 1973 г. был развит новый метод синтеза сверхтвердых
материалов, в частности алмазов, основанный на детонации смесей ВВ с
превращаемым материалом [32, 33]. Детонация смесевых зарядов ВВ осуществляется
в герметичной взрывной камере, заполненной инертным газом во избежание
окисления и отжига частиц алмаза. Выход алмаза из различных форм углерода может
достигать 50%, при этом в зависимости от параметров детонации могут быть
синтезированы либо чистый алмаз (кубическая форма), либо смесь кубической и
гексагональной (лонсдейлит) форм углерода. Алмаз, полученный этим способом,
является дисперсным материалом с удельной поверхностью 20-150 м2/г,
малыми областями когерентного рассеяния (ОКР), порядка 6-10 нм.
. В работах Г.В. Саковича с сотр. (1990 г.) [34-36] и В.Ф.
Локтева сообщается, что алмазы могут образовываться из конденсированных ВВ с
отрицательным кислородным балансом (например, тринитротолуола), т.е.
разлагающихся с выделением "свободного углерода", при детонации
зарядов в охлаждающей среде. В результате получаются так называемые
ультрадисперсные алмазы (УДА), или наноалмазы детонационного синтеза,
являющиеся сравнительно новым и весьма перспективным для практического
использования материалом.
В работе Г.И. Саввакина (1991 г.) [37] отмечается, что крайне
неравновесные условия формирования и очень большие скорости роста обусловливают
образование алмазов с уникальными физико-химическими свойствами. Образуется
очень дефектная структура алмазной фазы, в которой наряду с вакансиями в
кристаллической решётке и разорванными связями, имеются включённые атомы
химических элементов, присутствующих во взрывчатом веществе, в виде структурных
и неструктурных примесей. Высокая дисперсность (размер частиц 2-6 нм), развитая
поверхность (300-350 м2/г) определяют повышенную сорбционную ёмкость
и химическую активность детонационных алмазов.
Многие авторы, например [37], считают, что образование как
алмазного, так и неалмазного углерода при взрыве органического вещества
происходит в результате конденсации паров углерода, образующихся в
высокотемпературной плазме.
Чтобы достичь заметного выхода алмаза при детонации ВВ,
используют различные смеси. Так, например, ещё в 1986 г.В.И. Лямкин с сотр.
[31] при детонации смеси тротил: гексоген (1:
) получили практически полный переход "свободного"
углерода в алмаз. Средний размер полученных алмазных частиц составлял около 4 нм.
За последние два десятилетия на нескольких
научно-производственных предприятиях России, СНГ и за рубежом было организовано
промышленное производство ультрадисперсных алмазов.
Так, например, в Санкт-Петербурге на ЗАО "Алмазный
центр" производят УДА различных марок из различных ВВ [38]. Синтез
проводят во взрывных камерах объёмом от 1 до 20 м3, которые
изготавливают из низколегированных или высоколегированных сталей. Подрываемый
заряд представляет собой смесь, содержащую 50-70% масс. тротила. Подрыв осуществляют
в трёх вариантах: в газовой среде, в воде или при орошении водой, или в ледяной
бронировке.
Из всех типов синтетических алмазов именно алмазы
детонационного синтеза представляют наибольший интерес для химического
модифицирования. Этому способствует несколько факторов:
- малый размер частиц наноалмаза и, как
следствие, высокая удельная поверхность и большое количество поверхностных
функциональных групп;
- коммерческая доступность наноалмазов и,
что не мало важно, их не высокая стоимость (1 г наноалмаза стоит $ 5);
- лабильность функционального покрова, что
позволяет проводить разнообразные реакции модифицирования.
1.1.2.3
Синтез алмаза из газовой фазы
Синтез алмаза осуществляют и из газовой фазы (метод CVD [39-47]), если в ней
содержатся углеродсодержащие молекулы или их фрагменты. При этом алмазное
вещество может осаждаться как на гранях затравочных алмазных кристаллов или на
пластинках, так и на подложках из неалмазных материалов. Синтез происходит при
давлениях и температурах, соответствующих области метастабильности алмаза на
фазовой диаграмме углерода. Поэтому долгое время (а иногда и сейчас) его
называли "метастабильным синтезом алмаза".
Наиболее успешно идет такой синтез, если создать вокруг
зародыша среду, содержащую атомы углерода в достаточной, но не слишком большой
концентрации [39, 40]. Такие условия можно создать:
- если поместить алмаз в среду атомов
углерода, например, испаряемых нагретым до высокой температуры графитом, или в
раствор углерода в расплавленных металлах [41];
- или не прибегать к графиту, а использовать
какой-нибудь углеродсодержащий газ, молекулы которого способны разлагаться при
повышенной температуре, выделяя атомы углерода, например химический синтез
алмаза можно осуществить при атм. давлении и температурах 600-900 оС
из СО, СО+Н2, СН4 + СО2 при их каталитической
поликонденсации [42].
В 1962 г. американский исследователь В. Эверсол получил
патент [41] на наращивание затравочных кристаллов алмаза в потоке оксида
углерода или углеродсодержащих газов, способных при диссоциации образовывать
метильные радикалы. Процесс осуществлялся при температурах 600-1600 оС
и парциальном давлении углеродсодержащих газов до 75 мм рт. ст. При этом наряду
с алмазом на затравочных кристаллах осаждался и неалмазный углерод.
В настоящее время описанные основные методы получения
синтетических алмазных материалов реализованы в промышленных масштабах.
1.2.1
Химическое состояние поверхности алмаза
Поверхность алмазных материалов в нативном состоянии всегда
покрыта слоем кислородсодержащих функциональных групп (карбоксильные, кетонные,
спиртовые, ангидридные и др.), образовавшихся за счет насыщения свободных
валентностей поверхностных атомов углерода кислородом воздуха во время их
синтеза и последующих обработок. Несмотря на наличие уже "готового"
функционального покрова модифицирование поверхности алмаза затруднено
вследствие полифункциональности покрова, приводящего к неселективности
протекающих реакций.
Методами ИК-спектроскопии, микрогравиметрии, дифракции
электронов, рентгенофотоэлектронной спектроскопии и другими на поверхности
алмаза были идентифицированы различные функциональные группы [48-50, 52-55]:
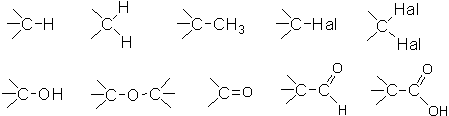
Помимо приведённых углеводородных, галоидных и кислородсодержащих
групп, синтезированные алмазы, в зависимости от условий их обработки, на своей
поверхности могут содержать азотсодержащие (аминные, амидные, циано- и
нитрогруппы), сульфоновые и др. группы [57].
Алмаз способен адсорбировать водород, кислород, моно - и диоксид
углерода. Кислород физически адсорбируется на поверхности алмаза уже при 195 К,
а при 273-417 К наряду с обратимой физической адсорбцией наблюдается
необратимая хемосорбция. Десорбция хемосорбированного кислорода возможна лишь
при повышенных температурах с одновременным отрывом поверхностных атомов
углерода в виде СО или СО2. На разных гранях количество
хемосорбированного кислорода приблизительно одинаково, но на грани {100}
хемосорбированный кислород существует в двух формах, что обусловлено
возможностью образования двойной или одинарной связей между кислородом и
поверхностными атомами углерода [52-54].
Р. Саппок и Н. Боэм [58, 59] исследовали изотермы адсорбции
водяного пара на поверхности алмаза, окисленной кислородом при 693 К, нагретой
в вакууме при 1173 К и обработанной водородом при 1073 К. При этом наиболее
сильная адсорбция водяного пара наблюдалась на окисленной поверхности, а
наиболее слабая - на поверхности, обработанной водородом. В такой же
последовательности уменьшались теплоты смачивания водой алмазных поверхностей.
Е.П. Смирнов и С.К. Гордеев [60] исследовали влияние состава и
строения функциональных групп поверхности алмаза на адсорбцию паров воды.
Показано, что активность функциональных групп к адсорбции уменьшается в ряду:
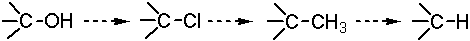
Это связано с полярностью поверхностных групп и склонностью их
вступать во взаимодействие по типу образования водородных связей.
В зависимости от наличия тех или иных поверхностных групп алмаз
по-разному смачивается водой. Так, наличие кислородсодержащих групп делает
поверхность алмаза гидрофильной [58, 59, 61-63], а метильных, гидридных,
галогенидных - гидрофобной [59].
В связи с наличием сложного функционального покрова на поверхности
алмаза необходимо проводить предварительную обработку алмазного материала с
целью получения однородного по функциональному составу поверхностного слоя, так
называемую монофункционализацию поверхности.
1.3
Химическое модифицирование поверхности алмаза
1.3.1
Монофункционализация поверхности алмаза
Как было показано выше, поверхность алмаза является
полифункциональной, что затрудняет ее дальнейшее химическое модифицирование.
Таким образом, полифункциональность поверхности вызывает необходимость
унификации ее функционального покрова. Наиболее удобным способом создания
унифицированной функциональной поверхности, согласно литературным данным,
являются её гидрирование и окисление. Поскольку доля поверхностных атомов
повышается с увеличением дисперсности материала, то все исследования по
модифицированию алмаза выполнены преимущественно на алмазных микро - и
ультрадисперсных порошках.
1.3.1.1
Гидрирование поверхности алмаза
Существует несколько способов гидрирования поверхности
алмаза.
Высокотемпературная обработка водородом представляет собой
один из удобных и распространенных способов монофункционализации исходной
поверхности как УДА, так и других алмазных материалов [64-72, 75]. Обычно
гидрирование алмаза проводят посредством обработки его поверхности газообразным
водородом при 1073 - 1173 К в течение 1-5 ч. В ходе восстановительной обработки
происходит образование новых С-Н групп на поверхности, преимущественно в
результате деструкции и восстановления кислородсодержащих групп, что показано
методами ИК-спектроскопии диффузного отражения и элементного анализа
поверхности (на основе данных РФЭС).
Помимо этого, описаны способы обработки природных кристаллов
алмаза микроволновой водородной плазмой [73, 76, 77]. Этот способ является
более трудоёмким и сложным в техническом исполнении. Однако при значительно
меньшем времени проведения процесса (~20-30 мин) он имеет ту же эффективность,
что и обычная высокотемпературная водородная обработка.
Таким образом, и высокотемпературная водородная обработка
алмаза, и его восстановление с помощью водородной плазмы, согласно литературным
данным, позволяют получить унифицированную поверхность, подготовленную к
дальнейшим реакциям.
1.3.1
Окисление поверхности алмаза
Окисленная поверхность алмаза также может служить матрицей
для проведения на ней различных реакций. Так, например, описаны [62] реакции
хлорирования окисленной поверхности с использованием тионилхлорида (кипячение в
течение 12 ч без растворителя) и радикальные реакции фторирования на ней, что,
в свою очередь, открывает большие возможности для дальнейшего модифицирования.
Окисление поверхности алмазных материалов можно проводить как в жидкой, так и в
газовой фазе.
Жидкофазное окисление поверхности алмаза. Кислородсодержащие группы
на поверхности алмаза могут быть синтезированы обработкой его целым рядом
жидкофазных окислителей, такими как: концентрированные кислоты H2SO4, HNO3, HClO4; смеси
кислот-окислителей HNO3+H2SO4, HNO3+H2SO4+олеум; расплавы солей NaOCl, (NH4) 2S2O8 и др. [60, 62].
Применение к окисленным алмазным порошкам методов щелочной
нейтрализации показало, что окисленная поверхность алмаза имеет кислые
свойства. Соответствие между количеством кислотных центров на поверхности
алмаза, определённым методом щелочного титрования раствором гидрокарбоната
натрия, и количеством групп, вступивших в реакцию с ацилхлоридом и
тионилхлоридом, указывает на присутствие на поверхности сильнокислых групп,
вероятнее всего - карбоксильных [60, 62].
Химико-аналитические исследования показали, что окисленный
алмаз содержит карбоксильные и гидроксильные группы. Помимо этих групп, на
своей поверхности алмаз содержит кислород в виде карбонильных и эфирных групп,
что подтверждается характерными полосами в ИК-спектрах (полоса в области 1760
см-1 свидетельствует о присутствии на поверхности карбонильных, а в
области 1270 и 1120 см-1 - эфирных групп).
Более информативным методом, позволяющим обнаружить и
конкретизировать формы связи кислорода с поверхностью алмаза, является
рентгенофотоэлектронная спектроскопия. Взаимодействие алмаза с различными
окислительными реагентами приводит к существенному увеличению концентрации
кислорода, причем рассматриваемые реагенты избирательно воздействуют на
поверхность. Так, например, расщепление линии О 1s в случае {100} поверхности
алмаза позволяет заключить о присутствии на этой поверхности, по крайней мере,
двух типов кислородсодержащих групп: карбонильных и эфироподобных.
Газофазное окисление. При определенных условиях
в атмосфере кислорода происходит связывание последнего поверхностью алмаза по
реакциям полиприсоединения с образованием кислородсодержащих групп. Детальные
исследования поверхностных окислов на алмазе были предприняты Н. Боэмом и др.
[58]. Использовав природный алмазный порошок, они показали, что в чистом
кислороде образование поверхностных окислов начинается при 260°С. Реакции
термоокислительной деструкции становились заметными выше 360°С. Следует
отметить, что максимальная концентрация присоединенного кислорода близка к
концентрации атомов углерода, выходящих на поверхность алмаза, что
свидетельствует о полном насыщении углеродной поверхности кислородсодержащими
группами. При продолжении этих исследований авторами [79] была изучена кинетика
хемосорбции кислорода на алмазных порошках, предварительно прошедших стадию
вакуумной термодесорбции при 1000°С. Была определена энергия активации
хемосорбции и показано ее линейное увеличение от степени заполнения поверхности
кислородом, предполагая при этом фиксацию кислорода только на поверхности
{111}.
1.3.2
Галогенирование поверхности алмаза
Создание на поверхности алмазных материалов покрова из атомов
галогенов используется либо для активации поверхности алмаза, обычно по
отношению к различным нуклеофильным реагентам, либо для получения материалов с
низкими адгезионными свойствами, что имеет место в случае фторированных
поверхностей. Стоит отметить, что, как правило, фторированные алмазы или алмазы
с привитыми перфторалкильными группами представляют собой конечные продукты,
которые непосредственно используются в технике и технологии. Заметим, что
процессы фторирования играют существенную роль в модифицировании различных
углеродных материалов, позволяя создавать материалы с принципиально новыми
физико-химическими свойствами [79].
Рассмотрим основные методы галогенирования алмазных
материалов, которые известны на данный момент. Сразу стоит отметить, что
подавляющее большинство работ относится к процессам фторирования, либо введения
перфторалкильных групп, и к процессам хлорирования. Бромирование и, тем более,
йодирование в силу очевидных недостатков и трудностей этих процессов
практически не исследовались.
1.3.2.1
Фторирование
Для фторирования алмазных материалов использовались различные
фторирующие реагенты: молекулярный фтор [80-83], безводный фтористый водород
[81], трифторид хлора [81], атомарный фтор [84, 85], плазма CF4 и других
фторуглеводородов [86-88], а также смесь молекулярного фтора с водородом
[89-91]. Кроме того, довольно широко в литературе представлены методы введения
перфторалкильных групп на поверхность алмазных материалов [92 - 95], которые
будут рассмотрены ниже в разделе, посвященном радикальным реакциям на
поверхности алмаза.
Обычно фторирование проводят при повышенных температурах:
250-500 оС и часто фторированию предшествует обработка водородом при
температурах 800-900 оС. Следует отметить, что при
высокотемпературном фторировании отмечается образование сложных смесей фторуглеводородов
в качестве побочных продуктов, что указывает на протекание процессов деструкции
в поверхностном слое алмаза [81]. При фторировании при комнатной температуре
образуется лишь фтористый водород [81]. Данные сканирующей электронной
микроскопии показали, что для микропорошков алмаза не наблюдается существенного
изменения морфологии частиц [81].
Несмотря на разнообразие предложенных методов фторирования,
только В.Н. Хабашеску и сотр. [89-91] был предложен эффективный метод
фторирования наноалмаза без предварительной высокотемпературной обработки
водородом.
Полученная фторированная поверхность использовалась ими для
дальнейшего синтеза привитых поверхностных соединений. В данном процессе
порошок исходного нанолмаза помещали в реактор из монель-металла и нагревали
при требуемой температуре (150-470 оС) в течение 3-4 ч. Затем в этот
реактор отдельно друг от друга подавали газообразные фтор и водород в
соотношении 3:
. Использование небольшого количества водорода в данном
процессе, как пишут авторы, необходимо для образования фтороводорода,
катализирующего процесс фторирования. Реакцию проводили в течение 48 ч, после
чего из охлаждённого до комнатной температуры реактора извлекли серый порошок
фторированного наноалмаза.
Процесс может быть описан следующей обобщенной схемой:
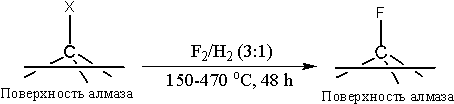 ,
,
где Х - различные функциональные группы.
В ИК-спектрах образцов после фторирование при 310 оС
регистрируются лишь интенсивные полосы поглощения связей С-F. По мнению
авторов, им удалось получить наноалмаз с практически монофункциональной
фторированной поверхностью. При фторировании УДА при 150 оС продукт
содержит 5,0% ат. фтора, при 310 оС - 6,5% ат., при 410 оС
- 7,9% ат., а при 470 оС - 8,6% ат.
С помощью атомносиловой микроскопии и динамического лазерного
светорассеяния авторами было показано, что предложенный ими процесс
фторирования приводит к полной дезинтеграции наноалмазных агрегатов с
образованием первичных частиц наноалмаза. Этот факт обусловлен тем, что
происходит полное удаление кислородсодержащих групп, обусловливавших сильные
межмолекулярные взаимодействия между первичными частицами наноалмаза.
Фторирование алмаза с помощью микроволновой плазмы CF4 проводят обычно при температурах 300-1000 оС, а для
наноалмаза сообщается о возможности фторирования в условиях тлеющего разряда
при комнатной температуре [88]. Так, в работе [87] показано, что применение
микроволновой плазмы CF4 приводит к поверхностной концентрации
фтора 0,0071 ат/Å2, тогда как применение смеси 98% CF4/2% О2 позволяет на порядок увеличить концентрацию
фтора - до 0,074 ат/Å2. Причем, авторы с помощью ЯМР-19F спектроскопии показали, что до 90% фтора относится к
связям C-F, а
5-10% к CF3-группам. Также с помощью ЯМР-19F спектроскопии установлена подвижность атомов фтора на
поверхности алмаза и их неравномерное распределение по ней, что, по мнению
авторов, указывает на протекание фторирования, по-видимому, преимущественно в
местах дефектов поверхности.
В близкой по используемому процессу фторирования работе [86]
показано, что простой нагрев образца алмаза в атмосфере CF4 вплоть до 1000 оС не приводит к фторированию
поверхности: для протекания процесса необходимо создание плазмы. Также авторы
показали, что предварительно восстановленный алмаз фторируется при значительно
более низкой температуре, чем исходный. Однако количественных данных о
содержании фтора в работе не приведено.
Для наноалмаза также использовалась плазма CF4, правда, полученная в условиях тлеющего разряда [88]. Применение
в аналогичных условиях SF6 оказалось менее эффективным. Как отмечают
авторы, фторирование протекает за несколько минут и, согласно данным РФЭС,
приводит к 4-6% ат. фтора на поверхности. В ИК-спектре, как и в случае других
фторированных алмазов, были зарегистрированы интенсивные полосы поглощения, относящиеся
к связям C-F.
1.3.2.2
Хлорирование
Наиболее распространенным хлорирующим агентом для алмазных
материалов является молекулярный хлор, также применение находит и хлористый
сульфурил. В отличие от фторированной хлорированная поверхность алмаза обычно является
промежуточным этапом на пути к синтезу привитых поверхностных соединений.
Хлорированию, как правило, подвергают предварительно гидрогенизированную
поверхность алмаза либо в газовой фазе при фотоинициировании [81, 82, 84, 85,
97, 98] или повышенной температуре [97, 98], либо в жидкой фазе (CHCl3) с помощью
сульфурилхлорида с использованием 2,2'-азобисизобутиронитрила в качестве
инициатора [101-103]. В настоящее время опубликована лишь одна работа [101], не
считая наших данных, по хлорированию наноалмаза. Однако, на наш взгляд,
приведенные в ней условия хлорирования, а именно температура процесса 850 оС,
вызывают серьезные сомнения в возможности получения и стабильности
хлорированной поверхности при столь высокой температуре, т.к. ранее на примере
алмазных микропорошков было убедительно показано, что хлорированная поверхность
алмаза стабильна лишь до ~300 оС [98]. Тем не менее, авторы [97]
приводят содержание хлора в модифицированном образце на уровне 8 масс. %. Одним
из достижений данного процесса является радикальное уменьшение содержания
металлических примесей (Al, Cr, Fe) и кремния в наноалмазе.
В работе [99] показано, что оба способа инициирования
(термический и фотохимический) при газофазном хлорировании приводят к
одинаковым результатам. Максимальная поверхностная концентрация хлора, которую
удалось достигнуть, для алмазных микропорошков составила 0,091 ат. Cl/Å2 (425 оС, 15 ч) и 0,079 ат. Cl/Å2 (фотоинициирование, 15 ч). Причем, как было отмечено авторами, в
случае термоинициирования поверхностная концентрация 0,079 ат. Cl/Å2 достигается уже через 1 ч после начала процесса. При
фотохимическом инициировании идет более равномерное увеличение концентрации
хлора. По-видимому, это связано с тем фактом, что при термоинициировании
активации подвергается и поверхность алмаза и молекулы хлора, тогда как при
фотоинициировании, в основном активируются молекулы хлора. Следует отметить,
что в работе [103] процесс хлорирования проводили при 425 оС, и
хлорированная поверхность была более стабильна, что несколько противоречит
данным работы [98]. В работе [99] отмечено, что в условиях регистрации
Оже-спектров происходит индуцированная десорбция хлора с поверхности, что
позволяет использовать для изучения привитых слоев только РФЭС. В обеих работах
для хлорированных образцов зарегистрированы пики хлора (Cl 2p) при 198,4 и 200 эВ [98]
и 199,8 и 200,1 эВ [99].
Жидкофазному хлорированию с помощью SO2Cl2 подвергали также только
предварительно восстановленные алмазы [101-103]. Типичная методика заключается
в суспендировании навески алмаза в растворе 2,2'-азобисизобутиронитрила и SO2Cl2 в безводном хлороформе.
Реакцию обычно ведут при 50 оС (температура, при которой начинается
распад инициатора с образованием изобутиронитрильных радикалов) в атмосфере
аргона в течение 8 ч. Данные о содержании хлора в образцах после хлорирования
авторы ни в одном случае не приводят. Кроме того, авторы [101] не смогли
зарегистрировать пик хлора (Cl 2p) методом РФЭС. Также следует отметить, что во всех работах,
посвященных хлорированию, указывается, что в ИК-спектрах диффузного отражения
не регистрируются полосы поглощения C-Cl
1.3.2.3
Бромирование
Данные по бромированию алмаза практически отсутствуют в
литературе.
Так, в работе [68] осуществлено бромирование алмазного
микропорошка молекулярным бромом при нагревании до 50 оС в течение 8
ч. В качестве растворителя использовали хлороформ. Контроль за ходом реакции
вели с помощью ИК-спектроскопии диффузного отражения. Авторы [68] отмечают, что
бромирование селективно для грани {100}. К сожалению, они не сообщают об
условиях процесса и характере механизма (ионный он или радикальный). Можно
предположить, что к бромированию по ионному механизму будет способна лишь
октаэдрическая грань, атомы углерода на поверхности которой могут быть сравнены
с третичными атомами углерода молекулы адамантана. Кубическая же грань способна
лишь к радикальному бромированию. Ромбододекаэдрическая грань из-за стерических
затруднений вообще не способна к бромированию ни по радикальному, ни по ионному
механизму. В обсуждении результатов будет приведен более корректный эксперимент
по изучению ионного бромирования восстановленного наноалмаза.
1.3.3 Реакции
нуклеофильного замещения на галогенированной поверхности алмаза
Логично, что галогенированная поверхность алмаза использовалась
для модифицирования различными нуклеофилами, правда, число таких работ, как и
круг нуклеофилов, задействованных в модифицировании, крайне мало. В литературе
описаны методы модифицирования N-нуклеофилами (аммиак, этилендиамин, метиламин, n-бутиламин, глицинэтиловый
эфир), С-нуклеофилами (ряд литийорганических соединений) и S-нуклеофилами (H2S). Также описана
макромолекулярная реакция прививки фторированных частиц наноалмаза на
предварительно аминированную поверхность стекла.
1.3.3.1
Реакции с N-нуклеофилами
Модифицирование хлорированного микронного порошка алмаза
газообразным аммиаком при различных температурах было изучено в [96], а при
облучении УФ светом в [104]. Показано [96], что температура процесса оказывает
существенное влияние на химический состав поверхности, который авторы
характеризовали с помощью ИК-спектроскопии диффузного отражения. Так, при
комнатной температуре происходит образование солей аммония, по-видимому,
вследствие взаимодействия аммиака с адсорбированным HCl, несмотря на предпринятые
меры по удалению адсорбатов после хлорирования. При увеличении температуры
аминирования до 200 оС регистрируются полосы поглощения при 1610 и
1514 см-1, которые авторы относят к валентным колебаниям C=N в группе >С=NH и деформационным
колебаниям H-N-H в группе С-NH2, соответственно. После
обработки при 300 оС регистрируется лишь полоса поглощения при 1610
см-1 и авторы делают вывод, что на поверхности остаются лишь
иминогруппы. В работе [98] аминирование проводили при более высоких
температурах (рис.2). При этом авторы также отмечают образование аммонийных
групп на поверхности при комнатной температуре и аминогрупп при повышенных
температурах. Также ими отмечается образование нитрильных групп при проведении
аминирования при 450 оС, что вызвано дегидрированием группы С-NH2. Авторы работы [104]
провели аминирование хлорированной поверхности при комнатной температуре и
облучении УФ-светом с помощью аммиака и метиламина.
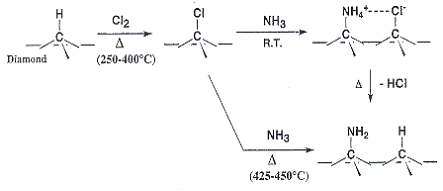
Рис.2. Схема аминирования хлорированной поверхности алмаза.
В работе [103] в качестве N-нуклеофила использовали н-бутиламин.
Модифицирование проводили при комнатной температуре в атмосфере аргона. Анализ
модифицированного образца проводили на основе ИК-спектра, в котором были
зарегистрированы полосы поглощения связей СН, в то время как характерных полос
поглощения аминогруппы не наблюдалось. Для количественной оценки
модифицированный образец подвергли пиролизу (528-1313 К), а полученные вещества
анализировали на газовом хроматографе, детектор которого зафиксировал ряд
углеводородов. Это позволило авторам сделать вывод о прививке н-бутиламина
к поверхности алмаза.
В работе [89] описан способ модифицирования поверхности
предварительно аминированной стеклянной пластинки фторированными наноалмазами
(рис.3). Реакцию проводили при 130 оС в течение 1-2 дней, в качестве
растворителя использовали 1,2-дихлорбензол. Как отмечают авторы, размер
пришитых наночастиц (измерен с помощью атомносиловой микроскопии) составлял
10-40 нм.
Наслаивание на полученную систему дополнительных порций
фторированного наноалмаза посредством образования новых слоёв с помощью
диаминов, по-видимому [89], позволит использовать подобные материалы, например,
для создания сенсоров и для получения различных защитных поверхностей.
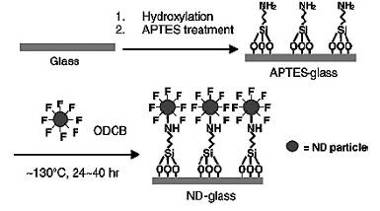
Рис.3. Схема реакции между
3-аминопропилтриэтоксисиланом, привитым гидроксильными группами к стеклянной
подложке, и фторированным УДА [89].
В работах [90, 91] для аминирования поверхности
фторированного УДА использовали этилендиамин (реакцию с УДА проводили в
атмосфере азота при 130 оС в присутствии небольшого количества
пиридина в течение 24 ч) и гидрохлорид глицинэтилового эфира (при 130-140 оС
в о-дихлорбензоле в течение 8-12 ч). ИК спектры поглощения промытого и
просушенного после аминирования порошка УДА свидетельствуют о прививке
указанных веществ к его поверхности.
1.3.3.2
Реакции с С-нуклеофилами
Наиболее используемыми реагентами для проведения этих реакций
являются литийорганические соединения. Модифицированию такими соединениями (MeLi, n-BuLi, sec-BuLi, t-BuLi, n-HexLi) подвергали
хлорированные микропорошки алмаза [101, 102] и фторированный наноалмаз [89-91].
В общем виде процесс описывается схемой:

Во всех работах модифицирование проводили в инертном растворителе
(ТГФ, гексан) при комнатной температуре в атмосфере инертного газа. По данным
пиролитического эксперимента, авторам [102] удалось привить бутильные группы к
~6% поверхностных атомов углерода. Контроль за ходом реакции авторы
осуществляли, как и в работе [72], с помощью газохроматографического метода: в
продуктах пиролиза были обнаружены метан, этан, пропан, пропен, n-бутан, sec-бутан.
При аналогичном анализе исходного гидрированного образца не удалось
зафиксировать даже метан.
1.3.3.3
Реакции с S-нуклеофилами
Авторы [104] пытались провести модифицирование
восстановленной и хлорированной поверхности монокристалла алмаза с помощью
сероводорода. Модифицирование проводили при пониженном давлении и УФ-облучении
в течение 0,5 ч. В обоих случаях авторы регистрировали появление полос
поглощения при 2970 см-1, которые они отнесли к валентным колебаниям
S-H. Однако, это вызывает
серьезные сомнения, так как обычно полосы поглощения групп S-H находятся существенно
ниже, при 2600-2550 см-1. Тем не менее, авторам удалось
зарегистрировать пик S 2p в РФЭС для обоих образцов. При этом отмечается, что в случае
модифицирования хлорированного алмаза интегральная интенсивность пика S 2p выше, чем в случае
восстановленного. Это дало авторам основание полагать, что хлорированная
поверхность более реакционно способна по отношению к сероводороду, чем
восстановленная.
1.3.4
Радикальные реакции на поверхности алмаза
В данном разделе описан ряд методов получения привитых
поверхностных соединений, основанных на радикальных процессах. Разумеется,
ранее рассмотренные процессы гидрировании и галогенирования также являются
радикальными, однако, они обычно используются для получения промежуточных
продуктов, которые далее вовлекаются в процессы модифицирования.
В литературе подробно рассмотрены три радикальных процесса,
приводящих к определенным привитым соединениям на алмазе: прививка
перфторалкильных групп пиролизом перфторалкилйодидов или азосоединений,
прививка ацильных групп и прививка алкенов с образованием С-С связи с
поверхностью.
Идея использовать перфторалкилйодиды или перфторазоалканы
основывается на их способности образовывать перфторалкильные радикалы в
условиях фото - или термохимического инициирования. Образующиеся радикалы
взаимодействуют далее с поверхностью алмаза, как представлено на схеме:
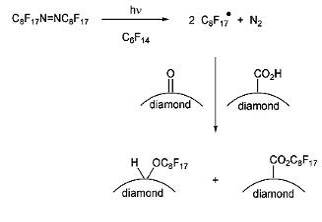
Типичный эксперимент включает в себя УФ-облучение суспензии
алмаза в перфторированном растворителе в присутствии азосоединения [105-108].
Факт ковалентной прививки перфторалкильных групп был установлен на основе
данных РФЭС и ИК-спектров.
Используя фотохимическую реакцию образующихся из C4F9I и СF3I перфторалкильных
радикалов с восстановленной поверхностью кристалла алмаза, авторы [108-111]
получили поверхность с привитыми перфторалкильными группами.
Стоит отметить, что похожая стратегия была применена и в
[112], где для модифицирования кристалла алмаза использовали и монофторалканы
и, даже, предельные углеводороды.
Авторы [112-115] реализовали ещё один способ модифицирования
восстановленной поверхности алмаза (алмазной плёнки). Используя в качестве
модификатора N-трифторацетил-10-аминодецен-1,
они получили на поверхности алмазного материала ω-аминодецильные группы
(рис.4), что в дальнейшем позволило им через гетеробифункциональный
кросс-линкер прикрепить к нему молекулу ДНК.
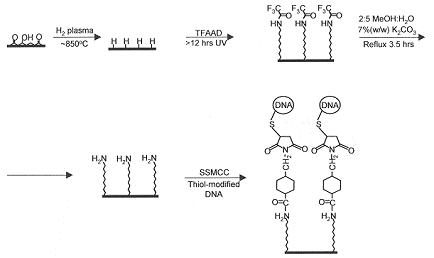
Рис.4. Схема прививки к алмазной плёнке молекул ДНК с
помощью гетеробифункционального кросс-линкера.
В серии работ T. Цубота с сотр. показано [64, 65, 67, 69, 75], что при
обработке гидрированной поверхности алмаза ароматическими и алифатическими
карбоновыми кислотами в присутствии перекисных инициаторов происходит их
прививка к поверхности за счет образования сложноэфирной связи. Схема процесса
модифицирования поверхности алмаза уксусной кислотой в присутствии перекиси
бензоила приведена на рис.5. Авторы отмечают, что при использовании перекисных
инициаторов происходит прививка инициатора на поверхность. Этого можно
избежать, если применять в качестве инициатора 2,2´-азобисизобутиронитрил.
Было установлено, что реакция гидрированной поверхности алмаза с толуолом
возможна лишь при её фотохимической активации (при термовозбуждении реакция не
идёт) или использовании в качестве радикального инициатора бензоилпероксида
(при использовании же, например, 2,2´ - азобисизобутиронитрила
привить к поверхности толуол не получилось).
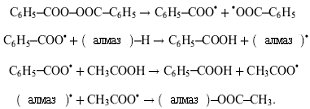
Рис.5. Схема
модифицирования поверхности алмаза уксусной кислотой.
Реакцию проводили в различных растворителях (толуол, ацетонитрил,
ТГФ, ДМФ, циклогексан, n-гексан), а
контроль за её ходом осуществляли с помощью методов ИК спектроскопии. Помимо
самой прививки, для радикальных реакций с карбоновыми кислотами [69] (СH3 (CH2) nCOOH, где 0 ≤ n ≤
16), были рассчитаны константы скоростей реакций. Использование в качестве
модификатора муравьиной кислоты не привело к удовлетворительным результатам.
Дж. Ванг с сотр. [73] провели электрохимическую обработку
поверхности нанокристаллической плёнки алмаза солями арилдиазония. Для этого
изготовленный из восстановленной в водородной плазме алмазной плёнки электрод
(второй электрод был стеклянным) погружали в растворы 3,5-дихлорфенилдиазониевой
и 4-нитрофенилдиазониевой солей. Факт протекания реакции был установлен
методами РФЭС и циклической вольтамперометрии.
1.3.5 Реакции
[2+2] и [2+4] циклоприсоединения на реконструированной
поверхности алмаза
Термодесорбция водорода при 1037 оС с полностью
гидрированной поверхности алмаза позволяет получить, как указывают авторы [116,
77], чистую реконструированную поверхность алмаза. Авторы полагают, что
реконструкция поверхности в данных условиях позволяет получить на кубической
грани алмаза двойные углерод-углеродные связи, аналогично тому, как это имеет
место на поверхности кремния и германия [117]. Экспериментально показано, что
бутадиен-1,3 вступает в поверхностные реакции Дильса - Альдера и [2+2]
циклоприсоединения. Причем первое направление является доминирующими. К
подобным выводам пришли и авторы работы [118], в которой было проведено
квантово-химическое моделирование указанных процессов.
В работах [116, 77] описаны реакции циклоприсоединения на
практически идеальной поверхности монокристалла алмаза (рис.6). В качестве
реагентов были использованы бутадиен-1,3 (реакция [2+4] - циклоприсоединения) и
циклопентен (реакция [2+2] - циклоприсоединения).
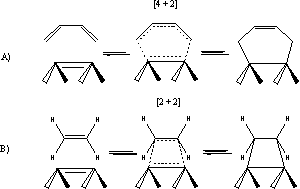
Рис.6. Реакции
циклоприсоединения на поверхности алмаза [77].
Контроль за ходом реакции авторы ввели с помощью ИК спектроскопии
диффузного отражения. Судя по приведённым в работе спектрам (рис.7), можно
сделать вывод о действительном протекании этих реакций. Для того чтобы
описанные реакции могли реализоваться, поверхностные атомы углерода должны быть
связаны двойными связями, что исключает наличие на поверхности функционального
покрова
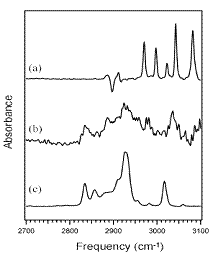
Рис.7. ИК-спектры
продуктов реакций циклоприсоединения на поверхности алмаза [116]. а - Физически
адсорбированный бутадиен-1,3; b - продукт
реакции поверхности с бутадиеном-1,3; c -
физически адсорбированный циклогексен
1.4
Сорбционные свойства наноалмазов
Большой интерес к использованию наноалмазов в качестве
адсорбентов обусловлен:
высокоразвитой поверхностью, которая изменяется в
интервале 150-450 м2/г, вследствие чего наноалмазы обладают большой
сорбционной емкостью;
- набором уникальных механических свойств, таких как
жесткость и высокая прочность матрицы, отсутствие набухания в растворителях, а
также высокая термостабильность;
высокой гидролитической стабильностью во всем
интервале рН;
возможностью модифицирования поверхности.
Сорбционные свойства любого сорбента определяются в первую
очередь природой функциональных групп, находящихся на его поверхности.
Исследования поверхностных свойств наноалмазов [121, 124] показали, что они
обладают выраженными катионообменными свойствами, проявляющимися при их
контакте с водными растворами. Отмечено некоторое увеличение взаимодействия
поверхностных групп наноалмаза с гидроксидами металлов от калия к литию,
несмотря на увеличение радиуса гидратированного иона металла. Следовательно,
происходит обращение лиотропного ряда селективности катионов, принимающего для
наноалмаза следующий вид: К+ < Na+ < Li+. Полученный ряд
совпадает с данными для окисленных синтетических алмазов [123].
Обменная емкость наноалмазов по отношению к ионам тяжелых
металлов (Fe2+, Ni2+, Cr6+) существенно зависит от способа очистки и химического
модифицирования, т.е. от гидрофильно-гидрофобных свойств их поверхности, а
также от концентрации катионов в растворе [123].
Сорбционные свойства наноалмазов в суспензиях зависят от
наличия заряда на поверхности агрегатов [125]. Возникновение последнего
обусловлено присутствием на поверхности кислородсодержащих групп, обладающих
кислотными свойствами. Знак и величина заряда зависят от концентрации и
константы диссоциации этих групп, рН раствора и концентрации фонового
электролита.
Сорбционные свойства наноалмазов определяются не только
химией поверхности, но и природой сорбата: при взаимодействии с различными
сорбатами один и тот же образец проявляет разные сорбционные свойства [41].
Так, сорбционная емкость сухого порошка УДА-СТП (табл.4) составляет по бензолу
9 моль/кг, а по хлороформу - 10,5 моль/кг; различается и емкость разных фракций
одной партии наноалмазов. При этом порошки, полученные разными производителями,
обладают разной сорбционной емкостью. Большая сорбционная емкость по отношению
к хлороформу, по-видимому, обусловлена гидрофильностью поверхности алмазных
частиц, которая создается в процессах очистки наноалмазов.
Таблица 4.
Сорбционные свойства наноалмазов [41]
|
Образец
наноалмаза (производитель)
|
Сорбционная
емкость по парам, моль/кг
|
Сорбция, в %,
за первые двое суток
|
|
бензола
|
хлороформа
|
|
|
УДА - СТП (СКТБ
"Технолог")
|
9,0
|
10,5
|
90-95
|
|
Фракции УДА -
ТАН (СКТБ "Технолог")
|
8
|
8,5
|
95-100
|
|
УДА (РФЯЦ -
ВНИИТФ)
|
10-16
|
12-19
|
55-65
|
Авторы работы [126] изучили сорбционную емкость по иону цезия
для наноалмазов, полученных в разных условиях и очищенных различными способами.
Установлено, что сорбционная емкость наноалмазов, синтезированных в одинаковых
условиях, но очищенных с использованием различных окислителей и режимов
очистки, колеблется в диапазоне от 0,01 до 0,5 моль/кг. Это указывает на ее
зависимость от природы окислителя и условий выделения (время, температура)
наноалмазов из продуктов синтеза. Наибольшей сорбционной емкостью (0,4-0,5
моль/кг) обладают образцы, полученные очисткой алмазной шихты озоном. Найденное
значение превышает сорбционную емкость известных природных сорбентов (0,01-0,15
моль/кг по цезию) и сравнимо с сорбционной емкостью смолы КУ-8-2 (0,8 моль/кг)
- широко используемого сульфокатионообменника. Поэтому предложено использовать
наноалмазы в качестве сорбента радионуклидов.
Установлено также, что наноалмазы представляют собой сорбенты
с высокой активностью по газам [133].
Частицы наноалмаза способны адсорбировать биологические
молекулы и взаимодействовать с ними, а следовательно, и воздействовать на живые
организмы. В литературе сообщается [128], что наноалмазы могут быть
использованы в качестве сорбента для хроматографического разделения и очистки
биологических жидкостей. Так, установлено, что из множества белков клетки
наноалмазы адсорбируют на своей поверхности только рекомбинантный белок
апообелин [129]. Из грубых экстрактов E. Coli с помощью наноалмаза
были выделены рекомбинантный апообелин и рекомбинантная бактериальная
люцифераза (этот метод является экспрессным (30-40 мин) и не требует
специального оборудования).
1.4.1
Наноалмазы как новый вид сорбентов для хроматографии
Расширение применения хроматографии в значительной мере
связано с созданием новых поколений сорбентов с хорошими кинетическими
характеристиками и разнообразными термодинамическими свойствами. В различных
вариантах хроматографии широкое распространение получили сорбенты на основе
химически модифицированных кремнеземов. Это обусловлено большим набором как
самих кремнеземов, так и методов, позволяющих направленно модифицировать их
поверхность, создавая мономолекулярный слой привитого вещества с заданными
сорбционными характеристиками [1]. Однако для всех этих сорбентов связь
между якорной группой модификатора и поверхностью осуществляется за счёт
системы связей Si-O-Si, которая характеризуется
невысокой гидролитической стойкостью, что не позволяет проводить анализ в
сильно щелочных или кислых средах. Обычный диапазон работы этих сорбентов в
единицах pH составляет от ~2 до 9. Ряд октадецилсилан-сорбентов способен к
рутинному использованию при высоких значениях pH (pH = 9-11) [130].
Полимерные сорбенты, несмотря на то, что позволяют преодолеть эту трудность, не
удовлетворяют другим важным требованиям (по прочности частиц, ненабухаемости в
различных растворителях), предъявляемым к сорбентам для ВЭЖХ. В связи с этим,
задача поиска и разработки сорбентов с гидролитически стойкой системой связей
между поверхностными группами и якорной группой модификатора и одновременно
удовлетворяющих требованиям, предъявляемым к сорбентам для ВЭЖХ, является
актуальной.
Перспективными материалами для создания подобных сорбентов
могут быть дисперсные алмазы, поскольку в них связь якорной группы с
поверхностью может быть осуществлена за счёт С-С связи. В работе [131] было
предложено использование синтетических алмазов для разделения агрессивных
газов. Однако применение синтетических алмазов в ВЭЖХ сдерживалось, очевидно,
доступностью алмазных материалов с хорошо развитой поверхностью. Если учесть,
что алмаз является непористым материалом, то очевидно, что высокая удельная
поверхность может быть достигнута лишь за счёт увеличения его дисперсности. В
последние десятилетия стали широко доступны синтетические алмазы детонационного
синтеза - ультрадисперсные алмазы, или наноалмазы (см. раздел 1.1.2), удельная
поверхность которых достигает 300 - 400 м2/г [125]. Однако алмазные
наночастицы, как было сказано выше, обычно образуют агрегаты, размер которых
меняется от 0,1 до нескольких десятков и даже сотен микрон. Причем крупные
агрегаты - механически непрочные и разрушаются, например под действием
ультразвука, до субмикронных (~0,2 мкм), более прочных агрегатов. Очевидно, что
из-за размера таких агрегатов и их механической непрочности, сами
ультрадисперсные алмазы малопригодны в качестве сорбента для ВЭЖХ.
Очень малые размеры алмазных частиц значительно ограничивают
возможности и непосредственного применения ультрадисперсных алмазов для
изготовления каких-либо инструментов или приборов. Практический интерес для
изготовления, например, режущего инструмента могут представлять технические алмазы
с размерами частиц на два-три порядка больше размера наноалмазов. Поэтому
промышленное использование детонационных алмазов потребовало разработки
технологии их укрупнения (компактирования).
Компания АЛИТ (Украина) разработала методику получения
алмазных спеков или поликристаллических дисперсных алмазных порошков (PDD) [132]. Путём
"спекания", осуществляемого при давлении 4-12 ГПа и температуре 1000
- 3000 ºC, и последующего дробления компактов получены различные узкие
фракции PDD, которые обладают всеми положительными свойствами классического
алмаза (высокой термической и химической стабильностью) и в то же время имеют
развитую поверхность (до 200 м2/г) с узким распределением нанопор
(1-7,5 нм) по радиусам. Следует отметить существенную механическую прочность
частиц PDD (твёрдость по Виккерсу (HV) ~10 GPa). Такие PDD представляют собой
перспективный сорбент для ВЭЖХ.
В литературе имеются сведения об исследовании
физико-химических свойств наноалмазов методами жидкостной и газовой
хроматографии. Так, в работах [133, 134] изучено удерживание ряда ароматических
соединений в обращено-фазовом (ОФ) варианте ВЭЖХ на PDD фирмы "АЛИТ".
При использовании воды в качестве элюента наблюдали следующий порядок
элюирования для колонки размером 100×4,6 мм при объемной скорости
1 мл/мин: бензол (1,99 мин) < метилбензоат (3,1 мин) < анилин (3,27 мин)
< фенол (5,90 мин). В этих условиях бензойная кислота не элюировалась из
хроматографической колонки. Авторы обнаружили корреляцию между диэлектрической
проницаемостью и временем удерживания этих соединений. Однако авторы не
приводят каких-либо хроматограмм в ОФ ВЭЖХ, а единственное разделение веществ
получено в варианте НФ ВЭЖХ для о - и п - ксилолов, но пики при
этом не разрешены и задний фронт хроматограммы размыт. Вероятно, отсутствие
других хроматограмм в работе связано с низкой эффективностью хроматографической
колонки и неудачным выбором условий разделения.
В работе группы авторов ИФХЭ им.А.Н. Фрумкина [135] для
образцов наноалмазов, предварительно очищенных двумя различными способами,
изучено удерживание производных бензола на колонке (80×2 мм) с использованием изооктана в качестве подвижной фазы при
объемной скорости 0,15 мл/мин. Порядок удерживания веществ одинаков для всех
обарзцов (в порядке увеличения времен удерживания): толуол < бромбензол <
о-дихлорбензол < бензофенон < анизол. Показано, что на УДА,
обработанном хромовой смесью (УДА-Хр), сорбаты удерживаются слабее, чем на УДА,
подвергнутом жидкофазной очистке с последующей обработкой в газообразном озоне
(УДА-О). Газохроматографическим методом определены времена удерживания девяти
тестовых соединений различной природы при разных температурах, что позволило
рассчитать удельные удерживаемые объемы и термодинамические характеристики
адсорбции изученных соединений на УДА-О и УДА-Хр [136]. Показано, что теплоты
адсорбции исследованных n-углеводородов на ультрадисперсных порошках
алмаза, особенно на УДА-О, близки к теплотам адсорбции на графитированной
термической саже. Для бензола и полярных соединений определены вклады специфического
взаимодействия в общую энергию адсорбции. Показано, что эти вклады больше для
УДА-О, чем для УДА-Хр, т.е. образец УДА−О содержит большее количество
активных функциональных групп.
Итак, анализ литературных данных показывает, что собственно
синтезу привитых соединений на поверхности наноалмазных материалов посвящено
лишь несколько работ, не представляющих собой результаты систематических
исследований. Кроме того, даже для наиболее исследованных алмазных
микропорошков и пленок число предложенных и тщательно изученных методов
модифицирования крайне мало. Следует отметить, что одной из основных проблем
при синтезе привитых поверхностных соединений на алмазе является количественная
оценка этого процесса. Только в редких случаях авторам удавалось определить
концентрацию привитых функциональных групп. В основном это было сделано только
для атомов галогенов по данным РФЭС. Кроме того, интерпретация ИК спектров,
которая во многих работах является основным критерием прививки, зачастую
вызывает серьезные сомнения, особенно в случае микропорошоков алмаза, что не
позволяет однозначно судить об эффективности предложенного метода
модифицирования. К тому же во многих работах, особенно это касается методов
галогенирования, используются экзотические экспериментальные приемы (например,
фторирование в плазме тлеющего разряда или использование фторида хлора),
которые вряд ли могут представлять практический интерес.
В этой связи, важной и актуальной задачей является разработка
химических и физико-химических методов направленного химического
модифицирования поверхности алмазных материалов, что позволит создать новый
класс перспективных материалов, так как в них будут сочетаться уникальные
свойства алмаза и специфические свойства привитого химического соединения.
1.5 Роль
наноалмазных присадок к смазочным маслам
1.5.1
Ультрадисперсные алмазные частицы как основа многофункциональной
алмазосодержащей присадки
Начиная с 20-х годов ХХ века, для повышения качества моторных
масел проводятся разработки и применение индивидуальных присадок
(антифрикционных, противозадирных, антикоррозионных, моющих и т.д.). В
настоящее время моторные масла представляют компаундированное масло, содержащее
пакет присадок. В пакет присадок (достигает до 25 %) входят как
маслорастворимые ингредиенты, так и частицы, находящиеся в мелкодисперсном
коллоидном состоянии. Современные масла содержат частицы карбонатов металлов
(моюще-диспергирующий компонент), дисперсии твердых смазок - графит, дисульфид
молибдена, соединения бора и др. (антифрикционный компонент).
В настоящее время в технических областях находят применение
три углерод содержащих продукта, полученных взрывным синтезом. Первый продукт -
ультрадисперсный алмазографит или шихта получается при подрыве литьевых зарядов
тротил - гексоген. Шихта является смесью "не сгоревшей" органики
взрывчатых веществ, не алмазного углерода (графит, сажа), наноалмазов и
примесей металлов. Второй продукт - кластерный наноалмаз, выделяемый из шихты,
полученной при подрыве зарядов тротил - гексоген. Третий продукт - поликристаллический
наноалмаз, выделяемый из шихты, которая образуется при подрыве прессованных
зарядов из смеси гексогена с графитом.
Шихта находит основное применение в качестве антифрикционной
добавки в маслах и консистентных смазках. Наноалмазы, в зависимости от
размеров, используются в качестве абразивов. На последнем технологическом этапе
при выделении наноалмазов из шихты производится удаление используемых реагентов
промывкой наночастиц водой. Основным недостатком общеизвестных наноалмазов
является их свойство к агрегированию после высушивания и трудности в повторном
получении гидрозолей. Поэтому, как правило, наноалмазы хранятся и
транспортируются в виде золей с содержанием наночастиц 5-10масс. %. С одной
стороны, это является экономически не выгодным (перевозится до 90 - 95 % воды).
С другой стороны, в суровом климате России транспортировка в зимнее время может
привести к замерзанию золей. При этом наблюдается эффект аналогичный
высушиванию, т.е. агрегирование наночастиц, потеря ими коллоидной устойчивости
и выпадение в осадок.
В настоящее время существуют и используются модифицированные
наноалмазы с принципиально новыми свойствами. Такие наноалмазы позволяют
производить продукты в виде сухих порошков с сохранением размерных
характеристик и получением коллоидных систем с высокой устойчивостью
наночастиц. Первоначально модифицированные наноалмазы были разработаны для
биологических применений. Однако оказалось, что они с успехом могут применяться
и в технических направлениях.
Наличие частиц в коммерческих маслах легко проверяемо разными
способами.
Способы обнаружения частиц, требующие специального
оборудования: 1 - проведение анализа на специализированных приборах; 2 -
уменьшение вязкости масла путем введения растворителя (чистый бензин, ацетон,
петролейный эфир) и осаждение частиц центрифугированием.
Способы - легко реализуемые в бытовых условиях: пропускание
луча лазерной указки (лазера) через масло - виден след от частиц, рассеивающих
свет; и, наконец, обнаружение осадка частиц на дне канистр, при длительном хранении
масла.
Поэтому предпринимаемые попытки введения в масла шихты или
наноалмазов лежат в русле развития технологий, направленных на улучшение
эксплуатационных свойств масел.
Анализ доступных патентов показывает, что введение в масла
шихты, получаемой в процессе взрывного синтеза, дает положительный
антифрикционный эффект. В настоящее время, например, в России, Украине, Китае
выпускаются добавки к моторным маслам, содержащие шихту. Только согласно одного
патента в масло вводится порошок ультрадисперсного алмаза dср =
0,005 мкм в количестве 0,7-1,0 масс. %. При этом в состав так же входит
ультрадисперсное железо dср = 0,07 мкм в количестве 3,0-4,0 масс. %.
Однако даже при таких соотношениях размеров и масс введенных частиц
представляется возможным определить коллоидную устойчивость частиц наноалмаза и
оценить его вклад в происходящие процессы трения.
Современные масла и смазки представляют композиции, в которые
входят собственно масляные основы и набор функциональных присадок, придающий им
улучшенные характеристики, которые должны приводить к сохранности агрегатов,
имеющих узлы трения. В связи с этим, наноалмазы детонационного синтеза можно
рассматривать как еще один новый компонент, способствующий улучшению
эксплуатационных характеристик масел и смазок, который не только позволяет
сохранить агрегат, за счет снижения коэффициента трения, но и обладает
"моющим" и восстанавливающим эффектами.
Наблюдающиеся положительные эффекты с большой долей
вероятности позволяют предположить, что использование масел с наноалмазами
может быть полезно уже на стадии обкатки двигателей при их производстве.
Улучшение характеристик выпускаемых двигателей, связанное с уменьшением
токсичности отработанных газов, снижением уровня шума, расхода топлива и т.д.,
может явиться тем элементом, который наравне с другими (оснащение системами
нейтрализации отработавших газов, улавливания паров топлива и пр.) позволит
перевести продукцию завода изготавливающего двигатели на более высокий
экологический стандарт.
Данная работа посвящена модификации поверхности наноалмазов,
чтобы сделать их совместимыми с серийными моторными маслами.
В работе были использованы ультрадисперсные алмазы,
разработанные и производимые НПО ЗАО "Синта" по оригинальной
промышленной технологии.
Ультрадисперсные алмазы (зарегистрированная торговая марка
"УльтраАлмазы”) выпускаются по ТУ РБ 28619110.001-95 и 28619110.002-96.
УльтраАлмазы применяются в гальванических производствах для повышения
твердости, износостойкости и коррозионной стойкости покрытий.
Разработанный в НПО "Синта" технологический процесс
получения металл-алмазных покрытий выгодно отличается от известных аналогов
экономным расходованием алмазной добавки, простотой приготовления и
эксплуатации электролита при высоком качестве хромирования инструмента и деталей.
Покрытие характеризуется высокой химической стойкостью в
атмосфере сернистых соединений, в растворах органических и неорганических
кислот, в условиях тропического климата. Так же отличается термостойкостью и
склонностью к пассивированию на воздухе. Покрытие повышает поверхностную
твердость и износоустойчивость деталей, хорошо выдерживает равномерно
распределенную нагрузку.
Наличие в электролите заряженных наноразмерных частиц алмаза,
осаждающихся совместно с хромом, увеличивают на 2-3 порядка количество центров
кристаллизации, что, соответственно, уменьшает размер зерна, снижает пористость
и уровень внутренних напряжений, увеличивает адгезию и твердость покрытия и как
следствие перечисленного выше в 2-3 раза и более увеличивает абразивную
стойкость и срок службы хромированного покрытия.
Металл-алмазное покрытие имеет уникальные характеристики по
адгезии, коэффициенту трения, повышенной коррозионной и эрозионной стойкости,
износостойкости и стойкости к истиранию.
Применение УДА в покрытии магнитных головок (аудио, видео,
дисководов, стримеров и т.д.) повышает их износостойкость в 6 раз.
Покрытия на основе кадмия и кластерных алмазов используют для
защиты от коррозии деталей и изделий и придания поверхностям притирочных
свойств. Покрытие характеризуется прочным сцеплением с основным металлом,
хорошей притираемостью, высокой пластичностью и эластичностью при развальцовке;
обладает способностью к пайке и устойчивостью в среде морских испарений,
туманов и морской воды.
Покрытия на основе палладия и кластерных алмазов используют
для защитно-декоративной отделки, повышения отражательной способности,
повышения твердости и износостойкости деталей и изделий. Покрытие
характеризуется высокой химической стойкостью в атмосферных условиях, не
тускнеет под действием влаги, сероводорода и атмосферы, загрязненной парами
йода, не окисляется при нагревании до 300°С, хорошо поддается механической
обработке.
Пакет технических предложений по металл-алмазным покрытиям
включает:
. УльтраАлмазы как компонент электролита хромирования в виде
водной суспензии с гарантией поставок необходимого количества в течение всего
периода эксплуатации процесса;
. Промышленно апробированную технологию нанесения
металл-алмазных покрытий на детали; и инструмент;
. Инженерное сопровождение внедрения и эксплуатации
техпроцесса в объеме, согласованном с Заказчиком;
. Технологические рекомендации и частные технические решения
("ноу-хау”) по нанесению покрытий на отдельные виды инструмента.
Уникальные свойства металл-алмазных покрытий позволяют с
успехом применять технологию для повышения износостойкости режущего инструмента
и штамповой оснастки, повышения срока службы деталей машин и оборудования,
таких как валы печатных машин, запорная арматура, нефтяные насосы изделий,
работающих в условиях эрозионного воздействия.
НП ЗАО "Синта" специализируется на производстве
ультрадисперсных алмазов (УДА), алмазосодержащих композиционных материалов и
покрытий, научных исследованиях и опытно-технологических разработках в области
наноматериалов.
Существующие производственные мощности "Синты"
позволяют выпускать 2 тонны УДА в год, до 8 тонн алмазосодержащей шихты,
150-200 тонн алмазосодержащей антифрикционной присадки к смазочным маслам и до
10 тыс. м2 композиционных металл-алмазных покрытий с использованием
УДА. Соответствующие технологии защищены патентами и заявками на патенты РБ,
апробированы на ряде промышленных предприятий РБ, РФ, Украины, Китая.
Ультрадисперсные алмазные частицы (УДА) размером не более 10
нм (0,01 мкм) составляют основу многофункциональной алмазосодержащей присадки.
После специальной обработки и диспергирования в масляной
основе такие частицы обеспечивают снижение момента и коэффициента трения,
улучшение качества поверхностей трения, уменьшение зазоров в сопряжённых
деталях. В результате возрастает компрессия в цилиндрах, срок службы масла,
фиксируется заметная экономия горюче-смазочных материалов, упрощается
обслуживание и увеличивается ресурс работы машин и механизмов. Эффективность
алмазосодержащей присадки подтверждена испытаниями как на машинах трения и
специальных стендах, так и в условиях эксплуатации легковых автомобилей,
сельскохозяйственной техники и некоторых механизмов.
Присадка экологически безопасна, так как не содержит тяжелых
металлов и галогенов. Отличительной особенностью присадки, является использование
высококачественной алмазосодержащей шихты сухого синтеза, модифицирование
ультрадисперсных частиц, а также технологическая цепочка обработки, включающая
интенсивные процессы диспергирования, дезинтегрирования и гомогенизации
углеродно-масляной смеси. Технология обеспечивает стабильное воспроизводимое
качество присадки.
.5.2 Механизм
действия присадки
Алмазные частицы проникают в кристаллическую решетку укрепляя
ее и обеспечивают идеальную подгонку трущихся поверхностей. Частицы
УльтраАлмазов, имея малые размеры, насыщают поверхности трения, заполняя
неоднородности на них. Таким образом, создаются новые поверхности с уменьшенным
граничным трением и износом, что особенно важно при больших нагрузках и
дефиците смазочного материала. При этом УльтраАлмазы не разрушаются,
препятствуют слому микрорельефа, исключают схватывание и образование задиров на
поверхности трения.
Мелкодисперсные алмазные частицы собирают вокруг себя
масляные глобулы размером до 6 мкм и обуславливают повышение вязкости смазочной
композиции в тонких пленках на поверхностях трения. При этом возрастает динамическая
прочность пленки, исключается ее разрушение при высоких скоростях
деформирования, уменьшаются потери масла от утечек через зазоры и уплотнения.
При низких температурах присадка обеспечивает снижение
вязкости смазочной композиции за счет снижения порога загустевания масла на
5-10°С. Следует отметить, что вышеописанный процесс чрезвычайно устойчив и
объясняется прочным механическим адсорбционным и диффузионным закреплением
частиц УльтраАлмазов на поверхностях трения.
Устойчивый эффект от внесения присадки наступает через 1000 -
2000 км пробега. УльтраАлмазы создают сверхустойчивое к высокой температуре и
активной среде противоизносное противозадирное покрытие с высокими адгезионными
свойствами, обеспеченными на уровне молекулярных связей.
УльтраАлмазы - экологически безопасная добавка к смазочным
материалам, устойчивая к воздействию агрессивных сред.
Присадка предназначена для применения в смазочных
композициях, используемых в автомобильных, тракторных, судовых и авиационных
двигателях, тепловозах, дизелях речного флота, металлообрабатывающих станках и
других механизмах.
1.5.3
Перспективные направления применения присадки
Присадка эффективно используется при эксплуатации двигателей
внутреннего сгорания, при этом имеют место: снижение износа и трения, экономия
горюче-смазочных материалов, повышение (восстановление) мощности и ресурса
работы, увеличение межремонтного периода, снижение токсичности отходящих газов
за счет более полного и правильного сгорания топлива.
В сочетании с обкаточными маслами присадка эффективно
работает при обкатке новых двигателей после сборки или после капитального
ремонта. В процессе обкатки происходит постепенное и мягкое выглаживание
микронеровностей без их слома, в результате чего обеспечивается высокоточная
подгонка сопрягаемых поверхностей при минимальных износах, а время обкатки
сокращается в 2-3 раза. Отмечено, что при такой обработке двигателей
внутреннего сгорания компрессия в цилиндрах стремится к расчетной и одинакова
во всех цилиндрах, что существенно улучшает эксплуатационные параметры. [125]
Аналогично имеет место улучшение эксплуатационных свойств при
использовании присадки для смазки различного промышленного оборудования
(компрессоры, гидро- и пневмоприводы редуктора и подшипники, и др.), в том
числе направляющих высокоточных станков, а также в качестве добавки в масляные
и эмульсионные СОЖ при обработке металлов резанием обеспечивают увеличение
стойкости инструмента, улучшение качества обрабатываемых поверхностей.
Бурильные установки нефтедобывающих и газодобывающих компаний
как правило расположены в труднодоступных местах, в сложных и суровых
климатических условиях, где требуется высокая надежность работы и затруднен
ремонт. Каждая установка оснащена не менее чем 5 дизелями. Часовой расход масла
одного дизеля составляет от 1 до 1,5 кг/час. Если принять среднюю временную
загрузку каждого дизеля 50% годовой, то расход масла на 1 буровой установке
составит 20 тонн масла, что соответствует 4 000 г алмазного концентрата.
Потребитель может рассчитывать на увеличение межремонтного
срока службы в 2-3 раза, облегченный запуск в холодное время, выравнивание
компрессии во всех цилиндрах и вследствие этого снижение расхода топлива на
5-15% и снижение расхода масла на 10-15%.
Для стационарных компрессорных тепловых электростанций и
промышленных предприятий потребитель может рассчитывать на восстановление
технических характеристик компрессоров до паспортных данных и, соответственно,
сокращение времени работы для обеспечения давления внутризаводской сети.
Присадка на основе ультрадисперсных алмазов представляет
собой смесь твердого модификатора трения и масла. В качестве
модификатора трения используется ультрадисперсный порошок синтезированного в
детонационной волне алмазографита ("ноу-хау") с размером частиц 4 - 8
нм (менее 0,01 мкм). Размеры УльтраАлмазов, синтезированных в детонационной
волне, в 1000 раз меньше неоднородностей микрорельефа трущихся поверхностей,
что категорически исключает абразивные свойства алмаза в смазочных композициях.
Микродобавка УльтраАлмазов в масла и смазки обеспечивает:
снижение момента трения на 20-40%;
снижение износа трущихся поверхностей в 1,5-3 раза;
уплотнение сальниковых узлов;
снижение расхода масел и топлива до 20%;
увеличение срока службы смазок в 1,5-2 и более раз (в
зависимости от условий работы) раза
легкий запуск двигателя в зимнее время.
Присадка к маслам увеличивает безремонтный ресурс двигателя
не менее чем в 2 раза и обеспечивает защиту трущихся деталей двигателя от
износа до 20000 км без повторного внесения (таким образом гарантирован эффект
действия присадки после смены масла), а также защищает двигатель в случае
возникновения экстремальных ситуаций (броски мощности, отсутствие охлаждения,
отсутствие смазки). [125]
Использование присадки для двигателей с предремонтным
состоянием дает дополнительно эффекты:
повышает компрессию на 20-60%;
повышает давление масла на 15-50%;
уплотняет сальниковые узлы;
снижает расход горюче-смазочных материалов;
снижает шум и вибрацию при работе двигателя;
восстанавливает мощность двигателя.
Таким образом присадка предназначена для применения в
смазочных композициях, используемых в автомобильных, тракторных, судовых и
авиационных двигателях, тепловозах, дизелях речного флота,
металлообрабатывающих станках и других механизмах.
Глава 2.
Экспериментальная часть
2.1 Методика
проведения эксперимента
В настоящее время в технических областях находят применение
три углеродсодержащих продукта, полученных взрывным синтезом. Первый продукт -
ультрадисперсный алмазографит или шихта получается при подрыве литьевых зарядов
тротил - гексоген. Шихта является смесью "не сгоревшей" органики
взрывчатых веществ, не алмазного углерода (графит, сажа), наноалмазов и
примесей металлов. Второй продукт - кластерный наноалмаз, выделяемый из шихты,
полученной при подрыве зарядов тротил - гексоген. Третий продукт -
поликристаллический наноалмаз, выделяемый из шихты, которая образуется при
подрыве прессованных зарядов из смеси гексогена с графитом.
. Для проведения эксперимента использовались
наноалмазы и масло
И-20А индустриальное без каких-либо добавок. (рис.1)
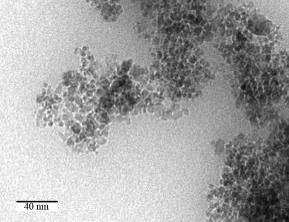

Рис.1 - Микрофотографии использованных образцов НА по данным
просвечивающей
(а) и сканирующей (б) электронной микроскопии,
предоставленных фирмой "Синта".
Как известно из анализа литературного обзора на поверхности
наноалмазов находятся остаточные группы:
карбоксильная (-СООH)
гидроксильная (-ОН)
кетонная (=О).
При хранении образцов масла с диспергированными в них
наноалмазами происходит их оседание. По данным ГОС стандарта оседание не должно
происходить в течении года.
При попадании в масла необработанных наноалмазов просходит их
оседание.
Наша задача состояла в такой обработке, чтобы связать
остаточную ОН группу, находящуюся на поверхности наноалмазов.
Обработка поверхности наноалмазов осуществлялась
хлорсиланами:
триметилхлорсиланом (СH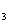 )
) 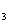 SiCL
SiCL
диметилхлорсиланом (СH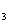 )
) 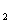 SiCL
SiCL
октилтрис (этокси) силан (С H
H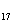 ) Si (OEt)
) Si (OEt) 
2.1.1
Основная реакция для проведения эксперимента
Реакция взаимодействия триметилхлорсилана с ОH группой на поверхности
наноалмаза, представлена следующей схемой:
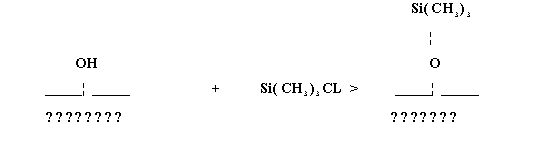
2.1.2
Характеристика используемого оборудования
Для исследования готовились 4 пробы:
а) В начале эксперимента проводилась обработка поверхности
наноалмазов в эксикаторе, емкостью 2 литра, закрывающемся стеклянной крышкой.
Внутрь эксикатора снизу помещали фарфоровую чашку с хлорсиланами, а сверху
наноалмазы. (рис.2)

Рис.2 - Эксикатор для обработки образцов: б) Затем помещали
эксикатор с наноалмазами (без смазки) в сушильный шкаф на 10-12 часов.
Сушильный шкаф представляет собой прямоугольный корпус из
тонколистовой стали, в котором размещены камера нагрева и блок управления.
Камера нагрева герметически закрывается дверкой.
Камера нагрева выполнена из тонколистовой стали, имеет патрубок
отсоса газов, гнездо для ввода регулирующей термопары, уплотнитель дверки и
трубку водяного охлаждения уплотнителя.
Внутри камеры нагрева размещены съемные полки. Пространство между
корпусом и камерой нагрева заполнено теплоизоляционным материалом.
Блок управления шкафом служит для автоматического поддержания
заданной температуры с точностью, указанной в технической характеристике.
Далее производилась подготовка наноалмазов к обработке.
Для исследования готовились 4 пробы в чашечках Петри.
К первой и второй пробе добавляли - по 1 грамму наноалмазов,
обработанных кремнийорганикой - силанами.
К третьей и четвертой пробе - по 1 грамму наноалмазов без
обработки.
в) В ходе эксперимента использовался дициклодиметикон -
смачиватель BASF
Ко второй и четвертой пробе добавляли по 1 капле смачивателя -
силиконовое масло 0,2% от веса.
Первую и третью оставляли неизменными.
г) Следующим этапом проводили взвешивание бюксов с приготовленными
наноалмазами.
Вес бюкса со второй пробой до внесения смачивателя составлял m=69,75г
после внесения смачивателя - m=69,77г
Четвертая проба: до внесения самчивателя - m=16.8743г
после внесения самчивателя - m=16,8943
. Вторым этапом были приготовлены 4 колбы с индустриальным маслом
И-20А без каких либо добавок.
В каждую из них добавили приготовленные пробы.
Таким образом к дальнейшим испытаниям были готовы 4 колбы, две из
которых содержали навеску наноалмазов обработанных хлорсиланами и две не
подвергавшиеся обработке.
. Определение установки и режим наблюдения (не центрифугировали)
Полученные и приготовленные колбы с маслом и наноалмазами
подвергали озвучиванию на УЗДН-1.
Ультразвуковое эмульгирование основано на кавитационном действии
ультразвука, приводящего к микровзрывам, а также способствующему энергичному
растягиванию капель дисперсной фазы до неустойчивых жидких цилиндров
критической длины и инициирующему распад образующихся жидких цилиндров на ряд
мелких капель, которые и создают стойкие эмульсии. Стойкость эмульсии,
полученной ультразвуком, значительно превышает стойкость систем полученных
другим путём, например, с помощью ротационного дезинтегратора. Диспергирование
жидкости в жидкости и твёрдого компонента в жидкости, широко используется в
различных технологических процессах пищевой промышленности, например, при
эмульгировании, смешивании компонентов, гомогенизации в процессе изготовления
майонеза, маргарина, всевозможных жировых эмульсий в мясной, кондитерской и
хлебопекарной промышленностях.
Подготовка ультразвукового диспергатора:
· включить сетевой шнур в розетку, включить
УЗДН-1 сетевым тумблером;
· включить воду, убедиться в срабатывании
гидрореле, по световому индикатору;
· поместить стакан со смесью внутрь, под
активный элемент УЗДН, таким образом, чтобы он (элемент) был практически
полностью погружен в стакан с жидкостью, во избежание перегорания его же, в
активной части эксперимента;
· проверить срабатывание вентилятора по
световому индикатору;
· нажать кнопку "излучение";
· установить мощность на уровне 20 Вт,
повернув ручку с одноименной надписью "мощность";
· установить максимальную частоту, повернув
ручку "частота" на 45 градусов, таким образом, чтобы стрелка
показывала строго вверх, появится характерный свист (звуковой край
ультразвукового сигнала);
Озвучиванию подвергали каждую пробу, опуская в стакан
излучатель, в течении 15 минут.
. После проведения ряда экспериментов мы поставили полученные
колбы и наблюдали время просветления (оптическая плотность на длине волны 650
нм становится меньше, чем 0,3 ед оптической плотности на 1 см). Результаты
испытаний приведены в табл.1.
2.1.3
Результаты эксперимента
Результаты испытаний приведены в табл.5
Таблица 5.
Время оседания наноалмазной шихты, диспергированной в масле
при различных условиях приготовления и диспергирования
|
Тип образца
|
В
индустриальном масле И20А безо всяких добавок
|
В
индустриальном масле И20А с добавлением смачивателя фирмы BASF (дициклодиметикона)
|
В коммерческ.
автомобильном масле
|
|
Образцы без
обработки силанами
|
1 день
|
1 день
|
7 дней
|
|
Образцы,
обработанные триметилхлорсиланами и диметилхлорсиланами
|
10 дней
|
10 дней
|
70 дней
|
|
Образцы,
обработанные октилтриc (этокси)
силаном
|
60 дней
|
Не осело до сих
пор
|
Не осело до сих
пор
|
2.1.4
Обсуждение результатов
Как видно из таблицы, обработанные силанами наноалмазы
существенно медленнее оседают в масле. Влияние смачивателя фирмы BASF (дициклодиметикона) на
время оседания наноалмазов отсутствует. Особенно сильные изменения происходят
при обработке наноалмазов октилтриc (этокси) силаном. Время, отведенное на дипломную
работу, недостаточно, чтобы решить, соответствуют ли созданные композиции
требованиям ГОСТ (время оседания не менее 1 года). Время оседания в
коммерческом автомобильном масле больше. Возможно, за счет присутствия
поверхностноактивных веществ в самом автомобильном масле. Разработанная
модификация поверхности наноалмазов привели к повышению смазочных композиций на
их основе. Обработанные хлорсиланами наноалмазы по крайней мере в десятки раз
медленнее осаждаются после диспергирования в масле.
2.2 Выводы
1) Предложена методика модификации наноалмазов детонационного
синтеза хлорсиланами и октилтриоксиэтилсиланом, основанная на использовании
остаточных ОН-групп на поверхности наноалмазов;
) Установленно, что предложенная обработка приводит к
существенной гидрофобизации поверхности алмазов детонационного синтеза. Для
этого предложена простая процедура оценки эффективности гидрофобности;
) Произведено пробное диспергирование модификацированных и
исходных наноалмазов в реальном индустриальном и моторном масле. Установлено,
что время оседания наноалмазов после модификации возрастает по крайней мере в
10 раз;
) Обсуждается механизм влияния модификации поверхности
наноалмазов на скорость оседания.
Глава 3.
Экономическая часть
3.1 Введение
Начиная с 20-х годов ХХ века, для повышения качества моторных
масел проводятся разработки и применение индивидуальных присадок
(антифрикционных, противозадирных, антикоррозионных, моющих и т.д.). В
настоящее время моторные масла представляют компаундированное масло, содержащее
пакет присадок. В пакет присадок (достигает до 25 %) входят как
маслорастворимые ингредиенты, так и частицы, находящиеся в мелкодисперсном
коллоидном состоянии. Современные масла содержат частицы карбонатов металлов
(моюще-диспергирующий компонент), дисперсии твердых смазок - графит, дисульфид
молибдена, соединения бора и др. (антифрикционный компонент).
Наличие частиц в коммерческих маслах легко проверяемо разными
способами.
Способы обнаружения частиц, требующие специального
оборудования: 1 - проведение анализа на специализированных приборах; 2 -
уменьшение вязкости масла путем введения растворителя (чистый бензин, ацетон,
петролейный эфир) и осаждение частиц центрифугированием.
Способы - легко реализуемые в бытовых условиях: пропускание
луча лазерной указки (лазера) через масло - виден след от частиц, рассеивающих
свет; и, наконец, обнаружение осадка частиц на дне канистр, при длительном
хранении масла.
Поэтому предпринимаемые попытки введения в масла шихты или
наноалмазов лежат в русле развития технологий, направленных на улучшение
эксплуатационных свойств масел.
Данная работа посвящена разработке методики модификации
поверхности наноалмазов.
В работе использовалась многофункциональная алмазосодержащая
присадка к моторным маслам, разработанная и выпускаемая по оригинальной
технологии ЗАО "Синта".
Используемая присадка экологически безопасна, так как не
содержит тяжелых металлов и галогенов.
Основу присадки составляют ультрадисперсные алмазные частицы
размером не более 10 нм (0,01 мкм). После специальной обработки и
диспергирования в масляной основе такие частицы обеспечивают снижение момента и
коэффициента трения, улучшение качества поверхностей трения, уменьшение зазоров
в сопряжённых деталях. В результате возрастает компрессия в цилиндрах, срок
службы масла, фиксируется заметная экономия горюче-смазочных материалов,
упрощается обслуживание и увеличивается ресурс работы машин и механизмов.
Эффективность алмазсодержащей присадки подтверждена испытаниями как на машинах
трения и специальных стендах, так и в условиях эксплуатации легковых
автомобилей, сельскохозяйственной техники и некоторых механизмов.
Присадка эффективно используется при эксплуатации двигателей
внутреннего сгорания, при этом имеют место: снижение износа и трения,
экономия горюче-смазочных материалов, повышение (восстановление) мощности и
ресурса работы, увеличение межремонтного периода, снижение токсичности
отходящих газов за счет более полного и правильного сгорания топлива.
В сочетании с обкаточными маслами присадка эффективно
работает при обкатке новых двигателей после сборки или после капитального ремонта.
В процессе обкатки происходит постепенное и мягкое выглаживание
микронеровностей без их слома, в результате чего обеспечивается высокоточная
подгонка сопрягаемых поверхностей при минимальных износах, а время обкатки
сокращается в 2-3 раза. Отмечено, что при такой обработке двигателей
внутреннего сгорания компрессия в цилиндрах стремится к расчетной и одинакова
во всех цилиндрах, что существенно улучшает эксплуатационные параметры.
Результаты испытаний показывают, что благодаря
алмазсодержащей присадке к моторным маслам увеличилась мощность и приемистость
двигателей, выровнялась и повысилась компрессия в цилиндрах, повысилось
давление масла, устранены шумы и вибрация при работе двигателей, уменьшился до
паспортных значений расход масла и топлива.
При "воздействии" наноалмазов на масла значительно
экономится энергия, уменьшается износостойкость масел.
В настоящее время используют различные присадки к маслам:
антиокилительные, антикоррозионные, моющие, вязкостные, противопенные.
Использование алмазосодержащей присадки является наиболее выгодным по
экономическим показателям.
Необходимо сравнить стоимость затрат на использование масла в
технологических процессах и машинах без воздействия наноалмазов
(алмазосодержащей присадки-НА), например вязкостной (ВП) и себестоимости метода
с использованием наноалмазов (алмазосодержащей присадки).
3.2 Время
работы лаборатории, расчет количества анализов за год на приборах и во всей
лаборатории
Время работы лаборатории определяется как
максимальное количество рабочих часов в год за исключением выходных и
праздничных дней (91) при 6-часовом рабочем дне.
Таблица 6.
Время работы лаборатории с учётом выходных и
праздничных дней в год.
|
№
|
Наименование
|
дни
|
часы
|
|
1.
|
Календарный
фонд рабочего времени
|
365
|
2190
|
|
2.
|
Выходные и
праздничные дни
|
91
|
546
|
|
3.
|
Фактическое
время работы
|
274
|
1644
|
В лаборатории каждый час производится
анализ 2-х образцов.
Ориентировочное количество исследований в
год при 2х анализах в час на установке:
n1=2*1644=3288
Принимаем количество видов детектирования в лаборатории 20.
3.3
Определение стоимости основных фондов
Основные фонды представляют собой средства
труда, являющиеся наиболее дорогостоящей частью средств производства и
обслуживающие большое число производственных циклов в течении длительного
времени. Причем, основные фонды в процессе переработки сохраняют свою
натуральную форму, а их стоимость переносится на стоимость выпускаемой
продукции по частям по мере износа, в виде амортизационных отчислений.
Затраты на приобретение и строительство основных
фондов (оборудование, машины, измерительные и регулирующие устройства,
транспортные средства, здания и сооружения), а также затраты, связанные с
монтажом аппаратуры, составляют капитальные затраты на основные фонды.
Стоимость вспомогательного оборудования
(пункт "Кроме того") берем по каталогу ЗАО "Вектон" и
"Лабтех", а также принимаем 60000 руб по рекомендации.
Стоимость атомного адсорбера
"Спектр-5" (выбран по рекомендации) берём рыночную из интернета.
Стоимость "НА" берем по прайсу
компании производителя "Синта".
Стоимость КИП и АиВТ (комп-ры и прогр.
обеспечение) определяем как среднюю рыночную стоимость ПК - 20000 руб и
стоимость WindowsXP SP2 - 2000 руб.
Размеры помещения лаборатории берём 7
метров на 4 метра. Стоимость аренды помещения рассчитывается исходя из средней
цены аренды за 1 м2 1800 руб в месяц:
*12*28=604800 руб/год
Площадь, занимаемая методом атомной
абсорбции 4 м.
Площадь, занимаемая методом с наноалмазной
присадкой (НА) 2 м. Стоимость аренды помещения для метода атомной абсорбции:
*12*1800=86400 руб/год
Стоимость аренды помещения для метода НА:
*12*1800=43200 руб/год
Таблица 7. Структура основных фондов по
двум вариантам:
|
ВП
|
НА
|
|
1. Стоимость
аренды помещения, руб/год
|
86400
|
43200
|
|
2. Стоимость
лабораторного оборудования руб.
|
|
|
а) Стоимость
установки для проведения анализа
|
700000
|
56400
|
|
б) Другие КИП и
АиВТ (комп-ры и прогр. обеспечение)
|
22000
|
22000
|
|
в) Стоимость
вспомогательного оборудования
|
60000
|
60000
|
|
Кроме того:
|
|
|
|
Пипет дозатор
1см3
|
1
|
штука
|
4000
|
-
|
|
Микропипетка
100 мкл
|
1
|
штука
|
70
|
70
|
|
Автоматическая
пипетка
|
1
|
штука
|
20000
|
-
|
|
3. Прочее
(дистиллятор и др.), руб
|
20000
|
20000
|
|
Итого:
|
806070
|
208670
|
3.4
Определение показателей по труду и расчет оплаты труда
Баланс рабочего времени лаборанта
соответствует балансу работы лаборатории.
Таблица 8. Баланс рабочего времени лаборанта за
год при 6-часовом рабочем дне:
|
Наименование
|
дни
|
часы
|
|
1.
|
Календарный
фонд рабочего времени
|
365
|
2190
|
|
2.
|
Выходные и
праздничные дни
|
91
|
546
|
|
3.
|
Номинальный
фонд рабочего времени
|
274
|
1644
|
|
4.
|
Невыходы на
работу
|
27
|
162
|
|
отпуск основной
и дополн.
|
22
|
132
|
|
прочие причины
|
1
|
6
|
|
выполнение
гособязанностей
|
1
|
6
|
|
временная
нетрудоспос-ть
|
3
|
18
|
|
5.
|
Эффективный
фонд рабочего времени
|
247
|
1482
|
Таблица 9. Плановая численность
работающих:
|
Наименование
профессий
|
Категория
|
Тарифный разряд
|
Явочное число
сотрудников
|
|
1. Начальник
лаборатории
|
ИТР
|
|
1
|
|
2.
Инженер-лаборант
|
ИТР
|
|
1
|
|
Итого:
|
|
|
2
|
|
3. Лаборант 5
категории
|
Рабочий
|
5
|
1
|
|
5. Лаборант 4
категории
|
Рабочий
|
4
|
3
|
|
Итого:
|
|
|
6
|
Расчет фонда оплаты труда лаборантов
делают исходя из тарифных ставок.
Для работы на установке с НА достаточно
квалификации лаборанта 3-го разряда.
Метод атомной абсорбции сложен и может
представлять определённую опасность из-за использования газа ацетилена. Для
работы на нём требуется квалификация лаборанта 5-го разряда.
Фонд основной оплаты труда (ФООТ)
лаборанта 4-го разряда:
Тарифная ставка лаборанта 4-ого разряда
равна 75 руб. /час.
а). Оплата по тарифу за отработанное
время:
Опо т = Ст*tэфф = 75*1482 = 111150 руб.
б). Премия за 100% выполнение плана:
Пр = Опо т*0,4 = 111150*0,3 =
33345 руб.
ΣФООТ =111150+33345=144495
руб.
Фонд дополнительной оплаты труда (ФДОТ)
лаборанта 4-го разряда:
а). Оплата отпуска (основного и
дополнительного):
Оот. = ΣФООТ*tотп/tэф. = 144495*22/247= 12870руб.
б). Оплата гособязанностей:
Ого. = ΣФООТ*tго/tэф = 144495*1/247= 585руб.
ΣФДОТ =12870+585=13455
руб.
Фонд оплаты труда составит:
ΣФОТ = ΣФООТ +ΣФДОТ =
144495+13455=157950руб.
Фонд основной оплаты труда (ФООТ)
лаборанта 5-го разряда:
Тарифная ставка лаборанта 5-ого разряда
равна 80 руб. /час.
а). Оплата по тарифу за отработанное
время:
Опо т = Ст*tэф = 80*1482 = 118560 руб.
б). Премия за 100% выполнение плана:
Пр = Опо т*0,4 =118560*0,3
=35568 руб.
ΣФООТ=118560+35568=154128руб.
Фонд дополнительной оплаты труда (ФДОТ)
лаборанта 5-го разряда:
а). Оплата отпуска (основного и
дополнительного):
Оот. = ΣФООТ*tотп/tэф = 154128*22/247=13728 руб.
б). Оплата гособязанностей:
Ого. = ΣФООТ*tго/tэф =154128* 1/247= 624 руб.
ΣФДОТ =13728+624= 14352руб.
Фонд оплаты труда составит:
ΣФОТ = ΣФООТ +ΣФДОТ =
154128+14352=168480 руб.
Таблица 10. Фонд оплаты труда лаборантов:
|
Разряд
|
Кол-во человек
|
Тарифная
ставка, руб/час
|
Основная
зарплата одного рабочего, руб
|
Дополнительная
зарплата одного рабочего, руб
|
Общая зарплата
одного рабочего, руб
|
Общая зарплата
всех рабочих, руб
|
|
|
|
Оплата по
тарифу
|
Премия
|
Оплата отпуска
|
ос. обязанности
|
|
|
|
4
|
3
|
70
|
111150
|
33345
|
12870
|
85
|
157950
|
473850
|
|
5
|
1
|
80
|
118560
|
35568
|
13728
|
24
|
168480
|
168480
|
|
Итого
|
|
642330
|
Расчет фонда оплаты труда инженера-лаборанта:
а). Оплата за отработанное время:
Оотр. = 18000* 11=198000 руб.
б). Оплата отпуска:
Оотп. = 18000*1 = 10000 руб.
в). Доплата за вредность:
Овр. = Оотр. *0,1 =
198000 *0,1 =19800 руб.
ΣФОТ = 198000+18000+19800
=235800руб.
Расчет фонда оплаты труда начальника
лаборатории:
а). Оплата за отработанное время:
Оотр. = 20000* 11 = 220000 руб.
б). Оплата отпуска:
Оотп. = 20000*1 = 20000 руб.
в). Доплата за вредность:
Овр. = Оотр. *0,1 =
220000*0,1 = 22000 руб.
ΣФOT = 220000+20000+22000 =
262000 руб
Таблица 11. Фонд оплаты ИТР
|
Категория ИТР
|
Кол.
|
Оклад месяц
|
Должн. оклад
|
Доплата за
вредность
|
Отпуск
|
Итого: тыс .
руб /год
|
|
Начальник
лаборатории
|
1
|
20000
|
22000
|
20000
|
262
|
|
Инженер-лаборант
|
1
|
18000
|
198000
|
19800
|
18000
|
235,8
|
|
Итого:
|
|
497,8
|
ФЗП=ΣФОТлаб+ ΣФОТитр=642330+497800=1140130 руб=1140,1тыс. руб
Отчисления на социальное страхование
составляют 26% от фонда оплаты труда.
Соц. Стр. = 1140130*0,26=296443,8
руб=296,4 тыс. руб
3.5 Расчет
затрат на анализ
Стоимость реактивов берем по каталогу ЗАО
"Вектон" и "Лабтех".
Информацию по приборам берем в
соответствующей и сопроводительной документации. Принимаем амортизационные
отчисления за оборудование за 10% от стоимости оборудования для анализа.
А= (0,1*Стлаб. обор.
/3) + (0,1*Стпр. /20), где
Стлаб. обор. - стоимость
лабораторного оборудования, руб;
,1 - 10% амортизационных отчислений;
- общее количество видов детектирования в
лаборатории;
/20 - доля амортизационных отчислений,
приходящаяся на данный метод от общего числа видов детектирования в
лаборатории;
Стар - стоимость аренды;
Стпр - стоимость прочего
оборудования.
ААА= (0,1*806070) + (0,1*20000)
/20) = 80707 руб/год,
АВА= (0,1* 138470) +
(0,1*20000) /20) = 13947 руб/год.
А) Расчет затрат на анализ методом ВП
Реактивы используются только в качестве
стандартов и на одно определение расходуется ничтожно малое количество.
Лимитирующим фактором является срок годности реактивов. Таким образом
расходуется только 1 кг/год реактива каждого вида.
Таблица 12. Стоимость реактивов
|
Реактив
|
Цена, руб
|
Срок годности,
лет
|
|
Натрий
сернокислый хч, кг
|
87
|
1
|
|
Калий
сернокислый хч, кг
|
200
|
1
|
|
Кальций
сернокислый хч, кг
|
180
|
1
|
|
Итого:
|
467
|
|
Затраты на воду: на одно детектирование требуется 0,2 л воды.
Зв=0,0002* Ств, где
Ств - стоимость м3 воды.
Зв=0,0002*11,8=0,00236руб
Затраты на электричество:
Электричество требуется для работы ПК и дистиллятора.
Мощность дистиллятора 2,4 кВт/ч, мощность ПК 0,5 кВТ/ч. В сутки требуется 1ч
работы дистиллятора и 24 часа работы ПК. На одно детектирование требуется:
Э= (Pд*tд+Pпк*tпк) / (24*n), где
Pд и Pпк-мощность дистиллятора и ПК соответственно,
tд и tпк - время работы дистиллятора и ПК в сутки,
n - кол-во детектирований в час.
Э= (2,4*1+0,5*24) /24*2=0,3кВт
Зэ=0,3*2,02=0,606 руб.
Затраты на газ (время пропускания
ацетилена для одного детектирования 0,5 мин):
г=V*tп*CTr, где V - обьемный расход,
л/мин;
tп - время пропускания,
мин;
Стг - стоимость газа, руб/л.
Зг=10*0,5*0,13=0,65 руб.
Таблица 13. Расчет затрат на реагенты и
энергетические затраты для метода ВП на год
|
Наименование
|
Ед. изм.
|
Норма расхода
на 1 детектирование
|
Цена, руб/ед
|
Кол-во
детектирований в год
|
Годовой расход
|
Затраты за
год,руб
|
|
Реагенты
|
кг
|
-
|
467
|
3288
|
1
|
467
|
|
Вода
|
м3
|
0,0002
|
11,8
|
3288
|
0,66
|
7,8
|
|
Ацетилен
|
л
|
5
|
0,13
|
3288
|
16440
|
2137
|
|
Эл. Энергия
|
кВт
|
0,3
|
2,02
|
3288
|
986,4
|
1990
|
Ремонтный фонд составляет 5% от стоимости оборудования:
Зрем=0,05*806070=40303,5 руб/год
По полученным данным составляем сводный баланс затрат
Таблица 14. Сводный баланс затрат для метода ВП
|
Наименование
|
Ед. изм.
|
Цена, руб/ед
|
Годовой расход
|
Затраты за год,
тыс. руб
|
|
Реагенты
|
кг
|
467
|
1
|
0,467
|
|
Вода
|
м3
|
11,8
|
0,66
|
0,008
|
|
Ацетилен
|
л
|
0,13
|
16440
|
2,137
|
|
Эл. энергия
|
кВт
|
2,02
|
986,4
|
1,990
|
|
ФЗП
|
|
|
|
1140,13
|
|
Соц.
страхование
|
|
|
|
296,44
|
|
Рем. фонд
|
|
|
|
40,3
|
|
Амортизация
|
|
|
|
80,6
|
|
Итого:
|
|
1562,1
|
Б) Расчет затрат на метод НА
Рассчитывается аналогично.
Для данного метода не используется ацетилен но в датчике
находится сменный элемент, рассчитанный на 500 элементоопределений. Стоимость
одного элемента 500 руб.
Таблица 15. Расчет затрат на реагенты и
энергетические затраты для метода ВА на год
|
Наименование
|
Ед. изм.
|
Норма расхода
на 1 детектирование
|
Цена, руб/ед
|
Кол-во
детектирований в год
|
Годовой расход
|
Затраты за
год,руб
|
|
Реагенты
|
кг
|
-
|
467
|
3288
|
1,0
|
467
|
|
Вода
|
м3
|
0,0002
|
11,8
|
3288
|
0,66
|
7,8
|
|
Сменный элемент
|
шт
|
-
|
500
|
3288
|
3,0
|
1500
|
|
Эл. Энергия
|
кВт
|
0,3
|
2,02
|
3288
|
986,4
|
1990
|
Текущий ремонт не учитывается, т.к. его
осуществляет поставщик, и его стоимость входит в изначальную стоимость прибора.
Капитальный ремонт не осуществляется, т.к. прибор находится на гарантийном
сроке эксплуатации. По полученным данным составляем сводный баланс затрат
Таблица 16. Сводный баланс затрат для метода НА
|
Наименование
|
Ед. изм.
|
Цена, руб/ед
|
Годовой расход
|
Затраты за
год,руб
|
|
Реагенты
|
кг
|
467
|
1,0
|
0,467
|
|
Вода
|
м3
|
11,8
|
0,66
|
0,008
|
|
Сменный элемент
|
шт
|
500
|
3,0
|
1,5
|
|
Эл. энергия
|
кВт
|
2,02
|
986,4
|
1,99
|
|
ФЗП
|
|
|
|
1140,13
|
|
Соц.
страхование
|
|
|
|
296,44
|
|
Амортизация
|
|
|
|
13,95
|
|
Итого:
|
|
1452,5
|
Таблица 17. Изменение стоимости затрат на применение
присадок.
|
Показатель
|
Метод ВП, руб
|
Метод НА, руб
|
Изменение
|
|
|
|
Абсолютное, руб
|
Относительное,
%
|
|
Затраты
|
1562,1
|
1452,5
|
109,6
|
7,0
|
Таким образом получаем, что затраты на
детектирование методом НА на 7,0% дешевле, чем методом ВП
3.6 Вывод по
экономической части
Из расчета затрат на анализ видно, что
метод с использованием алмазосодержащей присадки на 7,0% дешевле, чем метод ВП.
На практике такое большое число анализов по указанным компонентам проводится
редко и при использовании алмазосодержащей присадки затраты на 1 анализ будут
существенно ниже, чем при использовании вязкостной присадки. Последняя может
применяться с этой целью в крупных заводских лабораториях с большим числом
анализов в год и высокими требованиями к точности получаемых результатов.
Таким образом, методы НА в целом дешевле в
сравнении с использующимся сейчас методом ВП.
Глава 4.
Безопасность и экологичность
4.1 Техника
Безопасности и охрана труда в химической лаборатории
Система охраны труда - это система правил, организационных,
технических, санитарно - гигиенических мероприятий, направленных на
оздоровление труда работающих. В соответствии с ГОСТ 12.0.002 - 80 охрана труда
предусматривает способы обеспечения полной безопасности, безвредности и
облегчения условий труда при достижении его наибольшей производительности и
высоких экономических показателей.
. Рабочее место в лаборатории должно быть всегда хорошо
освещено.
Площадь рабочего места должна быть чистой, свободной от
мусора, отходов и всякого рода загрязнений.
. Работа в химической лаборатории сопряжена с возможностью
воздействия на работающего опасных и вредных факторов. Они обусловлены
использованием в экспериментах углеводородных газов, индивидуальных жидких
углеводородов, высокотемпературных электропечей, вакуум-насосов и прочего
электрооборудования, баллонов под давлением и др.
. К средствам индивидуальной защиты работающего относятся
халат, маска, очки, противогаз, рукавицы.
. Необходимо помнить, что углеводородные газы и
легковоспламеняющиеся жидкости могут вызывать не только пожар, но и взрыв, т.к.
в определенных концентрациях с воздухом или кислородом эти газы и пары являются
взрывоопасными.
. При прикосновении к высокотемпературным частям установок
работающий может получить ожоги различной степени тяжести и удар электрическим
током в результате прикосновения к клеммам электропечей и лабораторных
трансформаторов.
. При утечке в атмосферу лаборатории углеводородных газов,
органических жидкостей и других токсичных веществ работающий подвергается
опасности отравления.
. Следует соблюдать осторожность при работе с жидким азотом,
так как при попадании его на кожу возможно обморожение.
. Перед работой с водородом, находящимся в баллоне под
давлением, необходимо удалить все источники взрыва.
. Каждый работающий должен уметь оказывать первую помощь при
ожоге, отравлении, поражении электрическим током или травме. После этого
необходимо отправить пострадавшего к врачу.
. Если в результате нарушения техники безопасности
обнаружились тяжкие последствия в отношении других лиц, то непосредственно
виновные в этом могут быть подвергнуты уголовной ответственности.
4.2 Опасные и
вредные факторы
При выполнении эксперимента имеют место следующие вредные
факторы:
физические: микроклимат, освещение, шум, вибрации,
электромагнитное излучение, создаваемое ЭВМ, опасность поражения электрическим
током, тепловое излучение;
химические: при работе с химическими реактивами, реагентами и
газами возможны отравления и (или) химический ожог (характеристика опасных и
вредных веществ приведена в таблице 8.1);
психофизиологические: количественная оценка тяжести и
напряженности трудового процесса проводится в соответствии с P 2.2.2006-05
"Руководством по гигиенической оценке факторов рабочей среды и трудового
процесса. Критерии и классификация условий труда". Основными показателями тяжести
трудового процесса являются: физическая динамическая нагрузка, масса
поднимаемого и перемещаемого груза вручную, стереотипные рабочие движения,
статическая нагрузка, рабочая поза, наклоны корпуса, перемещение в
пространстве.
К факторам напряженности труда относятся: интеллектуальные
нагрузки, сенсорные нагрузки, режим работы, степень монотонности нагрузки,
эмоциональные нагрузки.
Исходя из степени отклонения фактических уровней факторов
рабочей среды и трудового процесса от гигиенических нормативов условия труда по
степени вредности и опасности условно подразделяются на 4 класса: оптимальные,
допустимые, вредные и опасные.
После проведения оценки тяжести и напряженности труда по P
2.2.2006-05 "Руководством по гигиенической оценке факторов рабочей среды и
трудового процесса. Критерии и классификация условий труда" был установлен
2 класс (допустимые условия труда), т.е. допустимые условия труда, т.к.
большинство показателей относятся к допустимым, характеризующиеся такими
уровнями факторов среды и трудового процесса, которые не превышают
установленных гигиенических нормативов для рабочих мест, а возможные изменения
функционального состояния организма восстанавливаются во время
регламентированного отдыха или к началу следующей смены и не оказывают неблагоприятного
действия в ближайшем и отдаленном периоде на состояние здоровья работников и их
потомство.
4.3 Вредные
вещества
При работе в лаборатории студент сталкивается с таким опасным
фактором, как токсичные вещества. Они могут находиться в газообразном, жидком
или твердом состоянии. Выделение в воздух или розлив токсичных веществ создает
опасность отравления работающих или развития у них профессиональных
заболеваний.
Различные вещества поступают в организм тремя путями:
через органы дыхания;
через органы пищеварения;
через кожу.
Вредное действие химических веществ определяется как
свойствами самого вещества (химическая структура, физико-химические свойства,
доза вредного вещества, попавшего в организм), так и особенностями организма
человека (индивидуальная чувствительность к химическому веществу, общее
состояние здоровья, возраст, условия труда).
К токсичным химическим веществам, воздействующим на
работников аналитической лаборатории, относятся: органические вещества, щелочи,
кислоты.
Таблица 18. Показатели токсичности веществ
|
Вещество
|
ПДКр. з, мг/м3
|
Класс опасности
|
Характер
воздействия
|
|
H2SO4
|
1
|
2
|
общетоксический
|
|
Метан
|
300
|
4
|
Общетоксический,
вызывает наркотическое действие
|
|
Ацетон
|
200
|
4
|
Раздражение
слизистых оболочек, дыхательных путей, глаз, головные боли, слабость
|
|
Этиловый спирт
|
1000
|
4
|
Общетоксический,
вызывает сначала возбуждение, а затем паралич нервной системы
|
Во избежании отравлений токсичными веществами в лаборатории
должны строго соблюдаться правила хранения и использования таких веществ. Персонал
должен регулярно проходить инструкцию по технике безопасности. Кроме того, в
работе с токсичными веществами должны допускаться только те сотрудники, которые
прошли медосмотр и не имеют противопоказаний по состоянию здоровья.
В лаборатории регулярно проводится инструктаж по технике
безопасности, все токсичные вещества хранятся в строго отведенном месте в
герметичной таре. Персонал лаборатории при работе с токсичными веществами
использует средства индивидуальной защиты (халаты, перчатки, защитные очки и маски).
4.4
Микроклимат
Микроклимат производственного помещения определяется
совокупностью параметров состояния воздушной среды (температура, влажность,
скорость движения воздуха, атмосферное давление, тепловое излучение,
температура поверхности и др.).
При благоприятном сочетании этих параметров сохраняется
нормальное функциональное состояние организма и создаются предпосылки для
плодотворного труда. Неблагоприятные условия снижают работоспособность, могут
вызывать изменения частоты пульса, дыхания, артериального давления, напряжения
нервной системы и т.п.
С целью обеспечения высокой производительности труда и
сохранения здоровья, работающих СанПиН 2.2.4.548-96 "Гигиенические
требования к микроклимату производственных помещений" устанавливает
оптимальные и допустимые параметры микроклимата в зависимости от времени года и
категории выполняемой работы. Научно-исследовательская лаборатория относится к
производственным помещениям с незначительным избытком явного тепла (не более 23
Дж/м). Категория выполняемой работы I б (легкие физические работы, производимые сидя,
стоя или связанные с ходьбой, но не требующие систематического напряжения или
поднятия и переноски тяжестей). В лаборатории проводился эксперимент, связанный
с модификацией поверхности наноалмазов. Работа при подготовке необходимых
реактивов и снятии результатов измерения производилась сидя или стоя. В таблице
19 указаны оптимальные и допустимые параметры микроклимата в химической
лаборатории.
Таблица 19. Оптимальные и допустимые параметры микроклимата в
химической лаборатории
|
Параметр
|
Значения
|
|
Оптимальное
|
Допустимое
|
|
Период года
|
|
холодный
|
теплый
|
холодный
|
теплый
|
|
Температура
воздуха, оС
|
21-23
|
22-24
|
15-17/23,1-24
|
28-30/ 22-20
|
|
Относительная
влажность, %
|
40-60
|
40-60
|
15-75
|
15-75
|
|
Скорость
движения воздуха, м/с
|
0,1
|
0,2
|
0,1-0,2
|
0,1-0,3
|
|
Температура
поверхностей, оС
|
20-24
|
21-25
|
18-25
|
19-29
|
Для поддержания оптимальных параметров микроклимата в
лаборатории используются различные современные средства вентиляции и системы
отопления.
Таким образом, для работников лаборатории созданы
благоприятные условия труда.
4.5 Освещение
При выполнении работ освещение производственного помещения
играет очень важную роль. От устройства освещения в значительной степени
зависит утомляемость глаз, расстройство нервной системы, производительность
труда, качество выполняемой работы. Недостаточная освещенность помещения может
привести к росту травматизма.
Производственное освещение делится на естественное,
искусственное и совмещенное.
Нормирование производственного освещения производится на
основании СНиП 23-05-95 "Естественное и искусственное освещение. Нормы
проектирования".
Естественное освещение зависит от времени дня, года,
характера облачности и отражающих свойств земного покрова. В качестве
нормируемой величины для естественного освещение принята относительная величина
- коэффициент естественной освещенности (КЕО) - ен
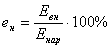
Евн - освещенность внутри помещения, лк
Е нар - освещенность вне помещения, лк
Нормированное значение КЕО определяется с учетом размеров
рассматриваемого объекта, т. е по характеристике зрительной работы, системы
освещения, района расположения.
Искусственное освещение применяется в помещении при недостатке
естественного света и для освещения в те часы, когда естественное освещение
отсутствует.
Норма освещения рабочего места определяется по наименьшему размеру
объекта, контрасту и фону.
Сначала устанавливают характеристику зрительной работы по
наименьшему размеру объекта различения в мм (8 разрядов), затем устанавливают контраст
объекта различения с фоном (малый, средний, большой) и характеристику фона
(светлый, средний, темный). В соответствии с этими характеристиками
устанавливают норму искусственного освещения для помещения.
В лаборатории к основным видам зрительной работы относятся письмо,
чтение, работа с микроскопом. Эти виды работ относятся ко второму разряду
(размер объекта различения 0,15-0,3 мм), подразряд г (контраст объекта
различения с фоном - большой), фон - светлый.
Таблица 20. Освещение помещения
|
Наименование
помещения
|
Разряд и
подразряд работ
|
Контраст
объекта с фоном
|
Фон
|
Естественное
освещение
|
Искусственное
освещение
|
Сочетание
нормируемых величин
|
|
|
|
|
КЕО, %
|
Освещенность,
лк
|
Кп,%
|
Р
|
|
|
|
|
по СНиП
|
Факт.
|
по СНиП
|
Факт.
|
|
|
|
Лаборатория
анализа масел
|
II г
|
Бол.
|
Светл.
|
2,5
|
2,5
|
300
|
320
|
10
|
10
|
Искусственное освещение в лаборатории создается при помощи
четырех люминесцентных ламп белого света, которые обладают всеми необходимыми
параметрами для зрительных работ категории 2г.
4.6 Шум
Производственный шум оказывает на человека крайне негативное
влияние. При воздействии шума на организм развивается усталость, повышается
раздражительность, происходит повышение кровяного давления, понижается
способность к сосредоточению мысли при умственном труде. Все это приводит к
ухудшению общего самочувствия и снижению трудоспособности.
Нормирование шума производится по ГОСТ 12.1.003-83 ССБТ
"Шум. Общие требования безопасности" и СН 2.2.4/2.1.8.562-96
"Санитарные нормы. Шум на рабочих местах, в помещениях жилых, общественных
зданий и на территориях жилой застройки".
В лаборатории источниками шума являются мешалки, сушильные и
вытяжные шкафы, термостаты и т.д.
. уменьшение шума в источнике его образования;
. изоляция источников шума средствами звукоизоляции и
звукопоглощения;
. архитектурно-планировочные решения, предусматривающие
рациональное размещение технологического оборудования, машин, механизмов,
акустическая обработка помещений.
Таблица 21.
Предельно допустимые уровни звука и эквивалентные
уровни звука на рабочих местах для трудовой деятельности разных категорий
тяжести и напряженности, дБА
|
Категория напряжен.
трудового процесса
|
Категория
тяжести трудового процесса
|
|
Легкая
физическая нагрузка
|
Средняя
физическая нагрузка
|
Тяжелый труд 1
степени
|
Тяжелый труд 2
степени
|
Тяжелый труд 3
степени
|
|
Напряженность
легкой степени
|
80
|
80
|
75
|
75
|
75
|
|
Напряженность
средней степени
|
70
|
70
|
65
|
65
|
65
|
|
Напряженность 1
степени
|
60
|
60
|
-
|
-
|
-
|
|
Напряженность 2
степени
|
50
|
50
|
-
|
-
|
-
|
Т.к. работа, проводимая в лаборатории относится ко второй
степени категории напряженности трудового процесса и тяжесть трудового процесса
соответствует средней физической нагрузке, то допустимый уровень шума в
лаборатории равен 50 дБА.
Фактический уровень шума в лаборатории не превышает
допустимый, что отвечает требованиям стандартов.
4.7 Вибрация
Вибрация - это механические колебания,
передаваемые по жидким или твердым средам. Нормирование уровней вибрации
осуществляется по ГОСТ 12.1.012-90 ССБТ. "Вибрационная безопасность. Общие
требования". Воздействие вибрации на человека классифицируется: по способу
передачи вибрации на человека; по направлению действия вибрации; по источнику
возникновения.
Причиной возбуждения вибраций являются возникающие при работе
машин и агрегатов неуравновешенные силовые воздействия.
Источниками вибрации в химической лаборатории являются:
мешалки, сушильные шкафы, вытяжные шкафы, лабораторные приборы.
Зачастую производственная вибрация - сложные колебания,
состоящие из нескольких простых колебаний различной амплитуды и частоты.
Различают вибрацию общую и локальную. Общая вибрация поражает
нервную и сердечно-сосудистую системы, желудочно-кишечный тракт,
опорно-двигательный аппарат; может развиться виброболезнь.
При длительном воздействии локальной вибрации наблюдается
онемение пальцев, заболевание суставов и нервозы рук.
Согласно СН 2.2.4/2.1.8.566-96 "Производственная
вибрация, вибрация в помещениях жилых и общественных зданий", вибрация
нормируется в зависимости от следующих факторов:
способа передачи на человека;
направления действия;
источника возникновения; (для общей вибрации)
Гигиеническая оценка вибрации производится одним из следующих
методов:
частотным (спектральным) анализом нормируемого параметра;
интегральной оценкой по частоте нормируемого
параметра;
- дозой вибрации;
Методы борьбы с вибрацией:
виброизоляция, вибродемпфирование, динамическое гашение;
кинематические и технологические методы, изменение
конструктивных решений, повышение класса точности обработки и снижение
шероховатости поверхностей;
При работе в условиях общей вибрации применяется спецобувь. К
средствам индивидуальной защиты (СИЗ) против вибрации относятся: виброзащитные
перчатки, коврики, виброзащитные рукоятки у вибрирующих ручек управления.
В химической лаборатории уровень вибрации находится в
пределах нормы.
4.8
Электромагнитные излучения
Диапазон промышленной частоты в нашей стране представлен частотой
50Гц. Гигиеническая регламентация ЭМП ПЧ (электромагнитные поля промышленной
частоты) осуществляется раздельно для электрического (ЭП) и магнитного (МП)
полей. Нормируемым параметром ЭП является напряженность (Е), которая
оценивается в кВ/м, МП - магнитная индукция (В) или напряженность магнитного
поля (Н), измеряемые соответственно в мТл или мкТл и А/м или кА/м. Источниками
ЭМИ являются: вся проводка, электроплиты, мешалки, баня и др.
В настоящее время в России существуют гигиенические нормативы
производственных воздействий ЭП и МП ПЧ в соответствии с требованиями и
Санитарными нормами и правилами Минздрава №5802-91
Таблица 22. Предельно-допустимые уровни (ПДУ) электрических
полей промышленной частоты
|
Диапазон частот
|
ПДУ (Е)
|
Нормативный
документ
|
|
50Гц
производст- венное
|
Е пд=50/
(Т (ч) +2), кВ/м. для Е=5-20кВ/м Е ид. макс. =25 кВ/м, при
Т<=10 мин
|
ГОСТ
12.1.002-84 "ССБТ. Электрические поля промышленной частоты. Допустимые
уровни напряженности и требования к проведению контроля на рабочих
местах". "Санитарные нормы и правила выполнения работ в условиях
воздействия переменных электрических полей промышленной частоты (50 Гц)"
№5802-91, утв. Минздравом.
|
Требования к магнитным полям промышленной частоты установлены
СанПин 2.2.4.723-98 (табл.23)
Таблица 23. Предельно допустимые уровни МП
|
Время
пребывания, час
|
Допустимые
уровни МП, Н (А/м) / В (мкТл) при воздействии:
|
|
Общем
|
Локальном
|
|
<=1
|
1600/2000
|
6400/8000
|
|
2
|
800/1000
|
3200/4000
|
|
4
|
400/500
|
1600/2000
|
|
8
|
80/100
|
8000/1000
|
Магнитные поля промышленной частоты не превышают
установленных норм.
Лаборатория оснащена персональным компьютером. Значения
предельно допустимых уровней ЭМИ (по СаНПиН2.2.2 /2.4.1340-03.), создаваемые
ПЭВМ (персональным компьютером) представлены в таблице 24.
Таблица 24.
Предельно допустимые уровни ЭМИ
|
Место измерения
|
Нормируемый
параметр, диапазон частот
|
ПДУ
|
|
На расстоянии
50 см от стенок ПЭВМ
|
Напряженность
элекрического поля в диапазонах частот
|
|
|
5Гц-2кГц
|
25В/м
|
|
2-400кГц
|
2,5В/м
|
|
Плотность
магнитного потока в диапазонах частот:
|
|
|
5Гц-2кГц
|
250нТл
|
|
2-400кГц
|
25нТл
|
|
На растоянии
10см от экрана
|
Поверхностный
электростатический потенциал
|
500В
|
Способы защиты (в соответствии с СанПиН 2.2.2 /2.4.1340-03):
1)
Расстояние
между рабочими столами с видеомониторами - не менее 2м.
Плошадь на одно рабочее место не менее 6м2, объем
- не менее 20м3.
Растояние между боковыми поверхностями не менее 1,2м.
При этом следует учитывать, что пластик, масляные краски,
тепло отражают излучение.
) Для защиты от статического электричество все персональные
компьютеры должны быть заземлены.
) Все кабели должны быть расположены таким образом, чтобы они
не образовывали колец и не сворачивались вокруг блока питания.
) Вентиляция помещения должна соответствовать нормам.
) Защита временем: не более 4ч в день и не более 2ч
непрерывно.
4.9
Электробезопасность
Электронасыщенность современного производства формирует
опасность поражения электрическим током, источником которой могут быть
электрические сети, электрифицированное оборудование и инструменты,
вычислительная и организационная техника, работающая на электричестве.
Так как в лаборатории используются различные электроприборы,
то может возникнуть опасность поражения электрическим током. Во избежание этого
при работе с электроприборами должны выполняться основные правила
электробезопасности:
. Запрещается к штепсельным розеткам, выключателям, пусковым
приборам, установленным в лаборатории, подключать электрические приборы,
потребляющие ток больше номинального.
. Все приборы и электроустановки, потребляющие мощность свыше
1кВт*час, могут быть включены в сеть только после согласования и проверки
подсоединения главным электриком института.
. Запрещена эксплуатация электрооборудования с нарушенной
изоляцией токопроводящих элементов, неисправными выключателями, вилками; замена
сгоревших предохранителей на токораспределительных щитах производится только
главным электриком института.
. Все нагревательные приборы независимо от их мощности должны
находиться на своем постоянном месте с достаточной тепловой изоляцией.
. В помещениях, в которых по роду работы может происходить
накопление паров легковоспламеняющихся или взрывоопасных веществ, категорически
запрещается использование искрящего электрооборудования. Если искрение является
следствием неисправности прибора, то он должен быть отключен и отремонтирован,
если - результат нормальной работы оборудования, последнее должно быть
выполнено во взрывоопасном исполнении или вынесено за пределы помещения.
. При возгорании проводов или электрооборудования необходимо
немедленно их обесточить и гасить огонь при помощи огнетушителя или асбестовым
полотном.
Для обеспечения безопасной работы с электрооборудованием в
лаборатории приняты все необходимые меры. На случай загорания проводов или
электроприборов под током предусматривается отключение подачи тока общим
рубильником, использование песка, порошковых огнетушителей.
4.10
Пожаровзрывоопасность
Пожаровзрывоопасность производственных помещений во многом
определяется наличием горючих газов (ГГ.), паров легковоспламеняющихся
жидкостей (ЛВЖ), паров горючих жидкостей (ГЖ) и горючих пылей.
К основным показателям пожаровзрывоопасности веществ
относятся: - нижний (НКПВ) и верхний (ВКПВ) концентрационные пределы
воспламенения газов, паров и пылей;
температура вспышки, самовоспламенения и воспламенения
горючих жидкостей;
минимальная энергия зажигания смесей горючих газов и паров с
воздухом.
Эти показатели рассчитываются или определяются
экспериментальным путем.
Согласно "НПБ 105-03. Определение категории помещений,
зданий и наружных установок по взрывопожарной и пожарной опасности",
производственные помещения и здания подразделяют по взрывопожарной и пожарной
опасности на категории А, Б, В1-В4, Г, Д. Категории взрывопожарной и пожарной
опасности помещений и зданий определяются для наиболее неблагоприятного в
отношении пожара или взрыва периода, исходя из вида находящихся в аппаратах и
помещениях горючих веществ и материалов, их количества и пожаровзрывоопасных
свойств, особенностей технологического процесса.
Основные показатели пожаровзрывоопасности химических веществ,
представлены в таблице 25:
Таблица 25. Основные показатели пожаровзрывоопасности
химических веществ.
|
Химические
вещества
|
Характеристика
пожаровзрывоопасности
|
Твсп
|
Тсв
|
НКПВ
|
ВКПВ
|
|
|
оС
|
об. %
|
|
Ацетон
|
ЛВЖ
|
-18
|
540
|
2,9
|
13
|
|
Бензол
|
ЛВЖ
|
-11
|
562
|
1,43
|
8
|
|
Гексан
|
ЛВЖ
|
-23
|
243
|
1,24
|
6,9
|
|
Водород
|
ГГ
|
-
|
510
|
4,12
|
75
|
|
Толуол
|
ЛВЖ
|
7
|
536
|
1,27
|
6,8
|
|
Метиловый спирт
|
ЛВЖ
|
6
|
440
|
6,98
|
35,5
|
|
Этиловый спирт
|
ЛВЖ
|
13
|
400
|
3,61
|
17,77
|
Таким образом ориентируясь на классификацию помещений по
пожаровзрывобезопасности, данную в "НПБ 105-03. Определение категории
помещений, зданий и наружных установок по взрывопожарной и пожарной
опасности", помещение химической лаборатории можно отнести к категории А
(взрывоопасное).
На случай возникновения пожара в лаборатории имеются в наличии
необходимые средства пожаротушения: пенные огнетушители, ящики с песком,
асбестовые одеяла.
4.11
Обеспечение безопасности трудового процесса
1. Перед началом работы на лабораторной установке необходимо
удалить с территории, непосредственно прилегающей к рабочему месту, все лишнее,
убрать предметы, которые препятствуют безопасному началу работы, убедиться в
наличии и исправности средств индивидуальной защиты и противопожарной
безопасности.
. Перед началом работы необходимо включить приточно-вытяжную вентиляцию
и, при необходимости, освещение.
. Перед включением лабораторной установки необходимо
проверить ее на герметичность.
. В интересах безопасности экспериментатор должен соблюдать
правильную последовательность выключения установки (по окончании опыта):
отключить температурный процессор, перекрыть все краны установки, снять
реактор, отключить насосы, напустить воздух в систему. Рабочее место после
окончания работы следует привести в порядок, закрыть все краны и вентили на
всех линиях.
Выполнение работы не предусматривает использование веществ,
имеющих класс опасности 1. Отходы собираются в специальные емкости, затем
сливаются в специальные цистерны, которые вывозятся с территории Университета и
сжигаются.
4.12 Расчет
избыточного давления взрыва для горючих газов, паров легковоспламеняющихся и
горючих жидкостей
В процессе анализа полученных металлокомплексов для
проведения восстановительной обработки использовался баллон с водородом. Т.к.
водород является взрывоопасным газом, то существует вероятность разгерметизации
баллона и возможность образования горючей смеси. Помимо этого в лаборатории
имеется баллон с метаном, который также является горючим газом. Чтобы отнести
помещение к определенной категории взрывоопасности, необходимо произвести
расчет избыточного давления, которое может образоваться при утечке газов.
Расчет проводится по методике "НПБ 105-95. Определение категории помещений
и зданий по взрывопожарной и пожарной опасности". Порядок расчета
представлен ниже. Избыточное давление взрыва ∆P для индивидуальных
горючих веществ, состоящих из атомов C,H,O,N,Cl,Br, I,F, определяется по формуле
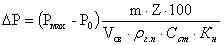 , (1)
, (1)
где Pmax - максимальное давление взрыва
стехиометрической газовоздушной или паровоздушной смеси в замкнутом объеме, определяемое
экспериментально или по справочным данным. При отсутствии данных допускается
принимать Pmax равным 900 кПа;
P0 -
начальное давление, кПа (допускается принимать равным 101 кПа);
m - масса горючего газа (ГГ.) или паров легковоспламеняющихся (ЛВЖ)
и горючих жидкостей (ГЖ), вышедших в результате расчетной аварии в помещение.
Вычисляемая для ГГ и для ЛВЖ и ГЖ по формулам, приведенным ниже, кг;
Z - коэффициент участия горючего во взрыве, который может быть
рассчитан на основе характера распределения газов и паров в объеме помещения
согласно приложению. Допускается принимать значение Z по табл.8.8;
Vсв -
свободный объем помещения, м3;
rг. п - плотность газа или пара при расчетной температуре tр, кг*м-3 вычисляется по формуле:
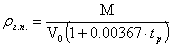 , (2)
, (2)
где M - молярная масса, кг*кмоль-1;
V0 -
мольный объем, равный 22,413 м3*кмоль-1;
tp - расчетная температура, 0С. В
качестве расчетной температуры следует принимать максимально возможную
температуру воздуха в данном помещении в соответствующей климатической зоне или
максимально возможную температуру воздуха по технологическому регламенту с
учетом возможного повышения температуры в аварийной ситуации. Если такого
значения расчетной температуры tp по
каким - либо причинам определить не удается, допускается принимать ее равной 610С;
Сст - стехиометрическая концентрация ГГ или паров ЛВЖ и
ГЖ, % (об.), вычисляемая по формуле:
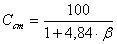 , (3)
, (3)
где 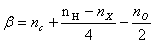 - стехиометрический коэффициент кислорода
в реакции сгорания;
- стехиометрический коэффициент кислорода
в реакции сгорания;
nc, nx, no, nx - число атомов С, Н, О и галоидов в
молекуле горючего;
Кн - коэффициент, учитывающий негерметичность помещения
и неадиабатичность процесса горения. Допускается принимать Кн равным
3.
Таблица 26. Значение коэффициента Z для веществ
|
Вид горючего
вещества
|
Значение Z
|
|
Водород
|
1,0
|
|
Горючие газы
(кроме водорода)
|
0,5
|
|
Легковоспламеняющиеся
и горючие жидкости, нагретые до температуры вспышки и выше
|
0,3
|
|
Легковоспламеняющиеся
и горючие жидкости, нагретые ниже температуры вспышки, при наличии
возможности образования аэрозоля
|
0,3
|
|
Легковоспламеняющиеся
и горючие жидкости, нагретые ниже температуры вспышки, при отсутствии
возможности образования аэрозоля
|
0
|
Масса m, кг, поступившего в помещение при расчетной аварии газа
определяется по формуле:
m= (Va+Vт) 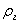 , (4)
, (4)
где Va - объем газа, вышедшего из аппарата, м3;
Vт - объем
газа, вышедшего из трубопроводов, м3; Vт =0
При этом Vа=0,01P1V, (5),
Где P1 - давление в аппарате, кПа;
V - объем аппарата, м3;
1). Баллон с
водородом.
Объем баллона =5л=5*10-3м3, Давление в
баллоне=100атм. =10000 кПа,
Объем газа, вышедшего из аппарата: V =0,01*10000*5*10-3=0,5 м3,Масса газа,
поступившего в помещение при возможной аварии: m = 0,5*0,0729=0,03646 кг
Плотность водорода при максимально высокой температуре в помещении
и при нормальных условиях:
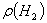 =2/22.413 (1+0.00367*61) =0.0729 кг/м3
=2/22.413 (1+0.00367*61) =0.0729 кг/м3
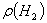 =2/22,413=0,0892 кг/м3
=2/22,413=0,0892 кг/м3
Стехиометрическая концентрация водорода:
Сст=100/ (1+4,84*0,5) =29,2398
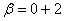 /4=0,5;
/4=0,5;
Свободный объем помещения (длина=6м, ширина =5м, высота=3м)
Vсв=6*5*3=90м3
Z=1,0 (из таблицы 4.8);
Кн=3;
Избыточное давление взрыва:
∆Р= (900-101) *0,03646*1*100/90*0,0729*29,2398*3=5,0618 кПа.
) Баллон с метаном
Объем баллона =50л=50*10-3м3;
Давление в баллоне=1,6мПа=1600кПа (16атм);
Объем газа, вышедшего из аппарата: V =0,01*1600*50*10-3=0,8 м-3;
Масса газа, поступившего в помещение при возможной аварии: m =0,8*0,5833=0,4666 кг;
Плотность метана при максимально высокой температуре в помещении и
при нормальных условиях:
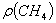 =16/22,413 (1+0,00367*61) =0,5833 кг/м3;
=16/22,413 (1+0,00367*61) =0,5833 кг/м3;
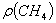 =16/22,413=0,7139 кг/м3;
=16/22,413=0,7139 кг/м3;
Стехиометрическая концентрация метана:
Сст100/ (1+4,84*2) =9,3633;
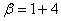 /4=2;
/4=2;
Свободный объем помещения (длина=6м, ширина =5м, высота=3м)
Vсв=6*5*3=90м3
Z=0,5 (таблица 8.8); Кн=3;
Избыточное давление взрыва:
∆Р= (720-101) *0,4666*0,5*100/90*0,5833*9,3633*3=9,7931 кПа
Исходя из полученных величин избыточного давления взрыва, можно
провести отнесение лаборатории к определенной категории по взрывоопасности и
пожарной опасности.
4.13
Категории помещений по взрывопожарной и пожарной опасности
Категории помещений по взрывопожарной и пожарной опасности
принимаются в соответствии с таблицей 8.9.
Определение категорий помещений следует осуществлять путем
последовательной проверки принадлежности помещений к категориям, приведенным в
таблице 8.9, от высшей (А) к низшей (Д).
Таблица 27. Расчет избыточного давления взрыва (НПБ 105-03).
Определение категорий помещений
|
Категории
помещения
|
Характеристика
веществ и материалов, находящихся (обращающихся) в помещении
|
|
1
|
2
|
|
А
взрывопожароопасная
|
Горючие газы,
легковоспламеняющиеся жидкости с температурой вспышки не более 280С
в таком количестве, что могут образовывать взрывоопасные парогазовоздушные
смеси, при воспламенении которых развивается расчетное избыточное давление
взрыва в помещении, превышающее 5 кПа. Вещества и материалы, способные
взрываться и гореть при взаимодействии с водой, кислородом воздуха или друг с
другом в таком количестве, что расчетное избыточное давление взрыва в
помещении превышает 5 кПа
|
|
Б
взрывопожароопасная
|
Горючие пыли
или волокна, легковоспламеняющиеся жидкости с температурой вспышки более 280С,
горючие жидкости в таком количестве, что могут образовывать взрывоопасные
пылевоздушные или паровоздушные смеси, при воспламенении которых развивается
расчетное избыточное давление взрыва в помещении, превышающее 5 кПа
|
|
В1-В4
пожароопасная
|
Горючие и
трудногорючие жидкости, твердые горючие и трудногорючие вещества и материалы
(в том числе пыли и волокна), вещества и материалы, способные при
взаимодействии с водой, кислородом воздуха или друг с другом только гореть
при условии, что помещения в которых они имеются в наличии или обращаются, не
относятся к категориям А или Б
|
|
Г
|
Негорючие
вещества и материалы в горячем, раскаленном или расплавленном состоянии,
процесс обработки которых сопровождается выделением лучистой теплоты, искр и
пламени; горючие газы, жидкости и твердые вещества, которые сжигаются или
утилизируются в качестве топлива
|
|
Д
|
Негорючие
вещества и материалы в холодном состоянии
|
Таким образом, помещение лаборатории относится к категории А
- пожаровзрывоопасная, т.к. расчетное избыточное давление для водорода и метана
в случае разгерметизации баллонов составляет 5,1 и 9,8 кПа соответственно, что
превышает величину 5 кПа, данную в первой графе таблицы 8.9.
Выполнение санитарных и противопожарных норм
проектирования, правил техники безопасности
Перечень нормативных документов по охране
труда:
1.
Федеральный
закон №181 "Об основах охраны труда в РФ" от 17.07.99. Трудовой
кодекс Российской Федерации. - М.: ИКФ "ЭКМОС", 2002.
2.
ГОСТ
12.0.003-74 ССБТ. Опасные и вредные производственные факторы. Классификация.
3.
ГОСТ
12.1.007-76 ССБТ. Вредные вещества. Классификация.
4.
Общие
требования безопасности.
5.
Р
2.2.2006-05. Руководство по гигиенической оценке факторов рабочей среды и
трудового процесса. Критерии и классификация условий труда.
6.
ГОСТ
12.1.005-88 ССБТ. Общие санитарно-гигиенические требования к воздуху рабочей
зоны.
7.
СанПиН
2.2.4.548-96. Гигиенические требования к микроклимату производственных
помещений.
8.
СНиП
2.04.05-91. Отопление, вентиляция и кондиционирование воздуха.
9.
ГОСТ
12.1.011-78 ССБТ. Смеси взрывоопасные. Классификация и методы испытаний.
10.
СНиП
23-05-95. Естественное и искусственное освещение.
11.
ГОСТ
12.1.003-83 ССБТ. Шум общие требования безопасности.
12.
ГОСТ
12.1.012-90 ССБТ. Вибрационная безопасность. Общие требования.
13.
ПУЭ.
Правила устройства электроустановок/ Минэнерго России.
13. ГОСТ 12.2.003-91 ССБТ. Оборудование
производственное. Общие требования безопасности.
. ГОСТ 12.1.004-91 ССБТ. Пожарная
безопасность. Общие требования.
. ГОСТ 12.1.010-76 ССБТ.
Взрывобезопасность. Общие требования.
. СН 2.2.4/2.1.8.562-96 Шум на рабочих
местах, в помещениях жилых, общественных здании и на территории жилой
застройки.
. НПБ 105-03 Определение категорий
помещений, зданий и наружных установок по взрывопожарной и пожарной опасности.
Список
литературы
1. Химия
привитых поверхностных соединений / Г.В. Лисичкин, А.Ю. Фадеев, А.А. Сердан и
др.: М.: Физматлит, 2003. - 592 с.
2. Спицын
Б.В. Физико-химия поверхности алмаза // Сборник статей седьмой сессии
международной школы повышения квалификации "Инженерно-химическая наука для
передовых технологий". Проблемы и достижения физико-химической и
инженерной науки в области наноматериалов. М.: ГНЦ РФ НИФХИ им.Л.Я. Карпова,
2002. С.
. Природные
и синтетические алмазы (под ред.И. И. Шафрановского). М.: Наука. 1986.
С.7-45.
. Полиморфные
модификации углерода и нитрида бора / Курдюмов А.В., Малоголовец В.Г., Новиков
Н.В. и др: Справочник. М.: Металлургия, 1994. - С.247-273.
. Самсоненко
Н.Д., Соболев Е.В. Электронный парамагнитный резонанс обусловленный
поверхностью алмаза // Письма в ЖЭТФ. - 1967. - Т.5; № 9. - С.304-307.
. Особенности
электронного парамагнитного резонанса поверхностных центров алмаза / Самсоненко
Н.Д., Жмыхов Г.В. и др. // Журн. структур. химии. - 1979. - Т. 20; № 3 -
С.1116-1118.
. ЭПР
и ИК-спектроскопия синтетических алмазов, близких по свойствам природным
алмазам типов Ia и IIa / Начальная Т.А., Малоголовец В.Г., Подзярей
Г.А. и др. // Сверхтвердые материалы. - 2000. - № 6. - С.57-64.
. Температурные
эффекты в ЭПР некоторых примесных и структурных дефектов в природных алмазах /
Самсоненко Н. Д, Зон В.Ш., Самсоненко С.Н., Сельская И.В. // Сверхтвердые
материалы. - 2000. - № 1. - С.53-62.
9. Defects
and impurities in nanodiamonds: EPR, NMR and TEM study / Shames A.I., Panich A.
M., Kempinski W. et al. // J. of Phys. and Chem. of Solids. - 2002. - V.63 - P.
1993-2001.
. Nuclear
magnetic resonance study of ultrananogrystalline diamonds /Panich A. M., Shames
A.I., Vieth H. - M., Osawa E. et al. // Eur. Phys. J. B. - 2006. - V.52. -
P.397-402.
. Magnetic
and high resolution TEM studies of nanographite derived from nanodiamond / Osipov
V., Enoki T., Takai K. et al. // Carbon. - 2006. - V.44; № 7. - P.1225-1234.
12. Маевский
В.М., Моздор Е.В., Падалко В.И. ЭПР субмикро - и наноразмерных синтетических
алмазов // Сверхтвердые материалы. - 2002. - № 6. - С.1-8.
. Парамагнитные
свойства наноалмаза / Белобров П.И., Гордеев С.К., Петраковская Э.А., Фалалеев
О.В. // Докл. АН. - 2001. - Т.379; № 1. - С.38-41.
14. Magnetic
properties of hydrogen-terminated surface layer of diamond nanoparticles /
Osipov V., Baidakova M., Takai K. et al. // Fullerenes Nanotubes and Carbon
Nanostructures. - 2006. - V.16; № 2-3. - P.565-572.
. Structure
and defects of detonation synthesis nanodiamond / Iakubovskii K., Baidakova M.
V., Wouters B. H. et al. // Diamond Relat. Mater. - 2000. - V.9; № 3-6. -
P.861-865.
. Heat-treatment
effect on the nanosized graphite p-electron system during diamond to graphite conversion
/ Prasad B. L. V., Sato H., Enoki T., et al. // Physical Review B. - 2000. -
V.62; № 16. - P.11209-11218.
17. Лейпунский
О.И. Об искусственных алмазах // Успехи химии. - 1939. - Т.8; вып.10. -
С.1519-1534.
18. Liander
H., Lundblad E. Some observations on the synthesis of diamonds // Ark. Kemi. - 1960. - ?? 16. - P.139-149.
. Искусственные
алмазы / Банди Ф., Холл Г., Стронг Г. и др. // Успехи физ. наук. - 1955. -
Т.57; вып.4. - С.691-699.
20. Manmade
diamonds / Bundy F. P., Hall H. T., Strong H. M., Wentorf R. H. // Nature. -
1955. - V.176; № 4471. - P.51.
21. Шафрановский
И.И. Алмазы. - М. - Л.: Наука, 1964. - 173 с.
. Дерягин
Б.В., Федосеев Д.В. Алмазы делают химики. - М.: Педагогика, 1980. - 128 с.
. Верещагин
Л.Ф. Сверхвысокие давления. // Наука и жизнь. - 1957. - № 12. - С.11-16.
24. Preparation
of diamond / Bovenkerk H. P., Bundy F. P., Hall H. T. et al. // Nature. - 1959.
- V.184; № 4693. - P.1094-1098.
25. Яковлев
Е.Н., Воронов О.А. Алмазы из углеводородов // Алмазы и сверхтвёрдые материалы.
- 1982. - Вып.7. - С.1-2.
. Яковлев
Е.Н., Воронов О.А., Рахманина А.В. Синтез алмазов из углеводородов //
Сверхтвёрдые материалы. - 1984. - № 4. - С.8-11.
. Синтез
алмазов из углеводородов / Яковлев Е.Н. Шалимов М.Д. Куликова Л.Ф., Слесарев
В.И. // Журн. физ. химии. - 1985. - Т.59; № 6. - С.517-518.
28. Wentorf
R. F. The behavior of carbonaceous materials at very high pressure and high
temperature // J. of Phys. Chem. - 1965. - V.69; № 5. - P.3063-3069.
. De
Carli P. S., Jamieson J. C. Formation of diamond by explosive shock // Science.
- 1961. - V.133. № 3467.
- P.1821-1822.
30. Ультрадисперсные
алмазные порошки, полученные с использованием энергии взрыва / Ставер А.М.,
Губарева Н.В., Лямкин А.И., Петров Е.А. // Физика горения и взрыва. - 1984. -
Т. 20; № 5. - С.100-104.
. Лямкин
В.И., Петров В.А. Получение алмаза из взрывчатых веществ // Докл. АН СССР. -
1986. - Т.302. - С.611-613.
. Ададуров
Г.А. Физико-химические превращения веществ в ударных волнах с участием газов //
Журн. ВХО им. Менделеева. - 1990. - Т.35; № 5. -
С.595-599.
. Дробышев
В.Н. Детонационный синтез сверхтвёрдых материалов // Физика горения и взрыва. -
1983. - Т. 19; № 5. - С.158-160.
. Получение
алмазных кластеров взрывом и их практическое использование / Сакович Г.Е.,
Брыляков Д.М., Губаревич В.Д. и др. // Журн. ВХО им.Д.И. Менделеева. - 1990.
Т.35; № 5. - С.600-608.
35. Surface
modification of ultradispersed diamonds / Loktev V. F., Makalskii V.I.,
Stoyanova I. V. et al. // Carbon. 1991. - V.29;
№ 7. - P.817-819.
. Сакович
Г.В., Губаревич В.Д. Получение алмазных кластеров взрывом и их практическое
применение // Журн. ВХО им.Д.И. Менделеева. - 1990. - Т.30; № 2. - С.402-404.
. Саввакин
Г.И., Сердюк В.А., Трефилов В.И. Влияние условий кристаллизации алмазов при
высокотемпературном ударном сжатии на их оптические свойства. // Докл. АН СССР.
- 1983. - Т.270; № 2. - С.329-332.
. Долматов
В.Ю. Ультрадисперсные алмазы детонационного синтеза. - С-Пб.: из-во СпбГУ,
2003. - 344 с.
. Дерягин
Б.В., Федосеев Д.В. Эпитаксиальный синтез алмаза в метастабильной области //
Успехи химии. - 1979. - Т.54; вып.12. - С.234-246.
. Федосеев
Д.В., Варнин В.П., Дерягин Б.В. Синтез алмаза в области его метастабильности //
Успехи химии. - 1984. - Т.53; вып.5. - С.753-771.
41. Patent
- 3030187 USA, Synthesis of diamond, W. G. Eversole, Union Carbide Corporation,
N 750309, Filed 23.07.1958, patented 17.04.1962
42. Руденко
А.П., Кулакова И.И., Скворцова В.Л. Химический синтез алмаза. Аспекты общей
теории // Успехи химии. - 1993. - Т.62. - С.99-117.
43. Patent
- 3371996 USA, Diamond growth process, H. J. Hibshman, N338776, Filed
20.01.1964, patented 5.03.1968
. Angus
G. C., Will. H., Stanko W. Growth of diamond seed crystals by vapor deposition
// J. Appl. Phys. - 1968. - V.39. - P.2915.
45. Синтетические
алмазы в промышленности. / Ангус Дж., Гарднер Н., Поферл Д., и др. - Киев:
Наукова думка, 1974. - С.30.
. Спицын
Б.В., Дерягин Б.В. Способ наращивания граней алмаза // Патент СССР, №339134.
Заявл.10.07.1956 г. Опубл. в 1980 г.
. Спицын
Б.В. Кристаллизация алмаза методом химической транспортной реакции, в: Труды I Международного семинара по алмазным
плёнкам. - М.: 1991. - С.7-17.
. Физико-химический
синтез алмаза из газа. / Дерягин Б.В., Федосеев Д.В., Бакуль В.И. и др. - Киев:
Техника. - 1971. - С. 193.
. Химия
поверхности алмаза. / Алёшин В.Т., Смехнов А.А., Богатырёва Г.П., Крук В.Б. -
Киев: Наукова думка, 1990. - 200 с.
50. Thomas
J. M., Evans E. V. Surface properties of diamond: a review. // Diamond Rev. -
1975. - P.2-8.
. Evans
S., Thomas J. M. Surface properties of diamond - the recent developments. //
Diamond Research. - 1978. - P.31-36.
52. Sappok
R., Boehm H. P. Chemie der Oberflache des Diamanten.I. Benetzungswarten,
Electronenspinresonanz und Infrarotspektren der Oberflachen-hydride, -
halogenide und - oxide. II. Bilding, Eigenschaften und Structur der
Oberflachenoxide // Carbon. - 1968. - V.6; № 4. - P.283-295.
53. Shergold
H. L., Hartley C. J. The surface chemistry of diamond // Int. J. Miner.
Process. - 1982. - V.9; № 3. - P.219-233.
. Pepper
S. V. Diamond {111} studies by electron energy loss spectroscopy in the
characteristic loss region // Surf. Sci. - 1982. - V.123; № 1. - P.47-60.
. Derry
T. E., Madiba C. C. P., Sellshop J. P. F. Oxygen and hydrogen on the surface of
diamond. // Nucl. Instrum. Methods Phys. Res. - 1983. - V.218; № 1-3. - P.559-562.
57. Кулакова
И.И. Химия поверхности наноалмазов // Физика твердого тела. - Т.46; вып.4. -
2004. - С.621-628.
58. Sappok
R., Boehm H. P. Chemie der oberflashe des diamanten-II. Bildung, eigenschaften
und structur der oberflachenoxide // Carbon. - 1968. - V.6; № 5. - P.573-588.
. Boehm
H. P. Die chemie der oberflache fester stoff // Kolloid. Z. und Z. Polymere. -
1968. Bd.127. - № 1-2. - P.17-27.
60. Гордеев
С.К., Смирнов Е.П. Исследование влияния химической природы поверхности алмаза
на адсорбционные свойства // Коллоидн. журнал. - 1982. - Т.44; вып.3. -
С.554-556.
. Плаксин
И.Н., Алексеев В.С. Адсорбция кислорода на свежеобнажённой поверхности алмазов
// Цветная металлургия. - 1963. - № 1. - С.32-34.
. Гордеев
С.К., Смирнов Е.П., Кольцов М.М., Никитин Ю.И. Влияние жидкофазного окисления
на поверхностные свойства синтетических алмазов. // Сверхтвёрдые материалы. -
1979. - № 3. - С.27-29.
. Богатырёва
Г.П. Исследование гидрофильности и гидрофобности поверхности синтетических
алмазов // Сверхтвёрдые материалы. - 1980. - № 2. - С.23-27.
64. Chemical
modification of diamond surface with CH3 (CH2) nCOOH
using benzoyl peroxide / Tsubota T., Shunsuke T., Ida S. et al. // Phys. Chem.
Chem. Phys. - 2003. - V.5. - P.1474-1480.
. Chemical
modification of hydrogenated dimond surface using benzoyl peroxides / Tsubota
T., Hirabayashi O., Shunsuke T., et al. // Phys. Chem. Chem. Phys. - 2002. -
V.4. - P.806-811.
. Effect
of treatment temperature on the amination of chlorinated diamond / Sotowa K. -
I., Amamoto T., Sobana A. et al. // Diamond Relat. Mater. - 2004. - V.13. -
P.145-150.
. Surface
modification of hydrogenated diamond powder by radical reactions in chloroform
solutions / Tsubota T., Urabe K., Egawa S. et al. // Diamond Relat. Mater. -
2000. V.9. - P.219-223.
. Halogenation
and butylation of diamond surfaces by reactions in organic solvents / Ikeda Y.,
Saito T., Kusakabe K. et al // Diamond Relat. Mater. - 1998. - V.7; № 6. - P.830 - 834.
. Chemical
modification of diamond surface with various carboxylic acids by radical
reaction in liquid phase / Tsubota T., Tanii S., Ida S., et al // Diamond
Relat. Mater. - 2004. - V.13; № 4-8. - P.1093 - 1097.
. Reactivity
of the hydrogen atoms on diamond surface with various radical initiators in
mild condition / Tsubota T., Hirabayashi O., Ida S., et al. // Diamond Relat.
Mater. - 2002. - V.11. - P.1360-1365.
. Incorporation
of butyl groups into chlorinated diamond surface carbons by organic reactions
at ambient temperature / Saito T., Ikeda Y., Egawa S. et al. // J. Chem. Soc.,
Faraday Trans.1. - 1998. - V.94; № 7. - P.929 - 932.
. Chemical
modification of diamond surfaces using a chlorinated surface as an intermediate
state / Ando T., Rawles R., Yamamoto K. et al. // Diamond Relat. Mater. - 1996.
- V.5. - P.1136-1142.
. Surface
functionalization of ultrananocrystalline diamond films by electrochemical
reduction of aryldiazonium salts / Wang J., Firestone A., Auciello O., Carlisle
J. // Langmuir. - 2004. - V. 20. - P.11450-11456.
. Chemical
modification of diamond powder using photolysis of perfluoroazooctane /
Nakamura T., Ishihara M., Ohana T., Koga Y. // Chem.commun. - V. 203. -
P.900-901.
. Chemical
modification of diаmond surface using a
diacyl peroxide as radical initiator and CN group-containing compounds for the
introduction of the CN group / Tsubota T., Hirabayashi O., Ida S. et al. //
Phys. Chem. Chem. Phys. - 2002. - V.4. - P.3881-3886.
. DNA-modified
diamond surfaces / Knickerbocker T., Strother T., Schwartz M. et al //
Langmuir. - 2003. - V. 19. - P. 1938-1942.
. Cycloaddition
chemistry at surfaces: alkenes with the diamond (001) - 2x1 surface / Hovis J.,
Coutler S., Hamers R. et al. // J. Am. Chem. Soc. - 2000. - V.122. - P.732-733.
78. Вansa I R., Vast1a F.,
Walker P. Kinetiks of chemosorption on diamond // Carbon. - 1972. V.10. -
P.443-448.
. Touhara
H., Okino F. Property control of carbon materials by fluorination // Carbon. -
2000. - V.38. - P.241-267.
. Chemisorption
of fluorine, hydrogen and hydrocarbons on the diamond C (111) surface / Yamada
T., Chuang T. J., Seki H., Mitsuda Y. // Mol. Phys. - 1991. - V.76; № 4. -
P.887-908.
. Fluorination
of polycrystalline diamond films and powders. An investigation using FTIR
spectroscopy, SEM, energy-filtered TEM, XPS and fluorine-18 radiotracer methods
/ Kealey Ch. P., Klapotke Th. M., McComb D. W. et al. // J. Mater. Chem. -
2001. - V.11. - P.879-886.
. The
effect of diamond surface termination species upon field emission properties /
May P. W., Stone J. C., Ashfold M. N. R. et al. // Diamond and Relat. Mater. -
1998. - V.7; № 2-5. - P.671-676.
. Hadenfeldt
S., Benndorf C. Adsorption of fluorine and chlorine on the diamond (100)
surface // Surf. Science. - 1998. - № 402-404. - P.227-231.
. Freedman
A., Stinespring C. D. Fluorination of diamond (100) by atomic and molecular
beams // Appl. Phys. Lett. - 1990. - V.57. - P.1194 - 1196
. Freedman
A. Halogenation of diamond (100) and (111) surfaces by atomic beams // J. of
Appl. Phys. - 1994. - V.75; № 6. - P.3112-3120.
. Diffuse
Reflectance Fourier-transorm Infrared Study of the Plasma-fluorination of
Diamond Surfaces using a Microwave Disharge in CF4/T. Ando, J.
Tanaka, M. Ishii et al. // J. Chem. Soc. Faraday Trans. - 1993. - V.89; № 16. -
P.3105-3109.
. Scruggs
B. E., Gleason K. K. Analysis of Fluorocarbon Plasma-Treated Diamond Powders by
Solid-State Fluorine-19 Nuclear Magnetic Resonance // J. Phys. Chem. - 1993. -
V.97. - P.9187-9195.
. Cool
plasma functionalization of nanodiamond particles / G. McGuire, M. A. Ray, O.
Shenderova // Joint International conference "Nanodiamond and Nanocarbon
2006”. - 2006. - St. Petersburg, Russia.
. Yu
L., Khabashesku V. N., Naomi J. H. Fluorinated Nanodiamond as a Wet Chemistry
Precursor for Diamond Coatings Covalently Bonded to Glass Surface // J. of the
Am. Chem. Soc. - 2005. - V.127; № 11. - P.3712
. Khabashesku
V. N., Margrave J. L., Barrera E. V. Functionalized carbon nanotubes and
nanodiamonds for engineering and biomedical applications // Diamond Relat.
Mater. - 2005. - V.14, Issues 3-7. - P.859-866.
. Functionalization
of Nanoscale Diamond Powder: Fluoro-, Alkyl-, Amino-, and Amino
Acid-Nanodiamond Derivatives // Liu Y., Gu Z., Margrave J. L., Khabashesku V.
N. // Chem. Mater. - 2004. - V.16; № 20. - P.3924-3930.
. Smentkowski
V. S.,Yates Jr., John T. Fluorination of diamond surfaces by irradiation of
perfluorinated alkyl iodides // Science. - 1996. - V.271; № 5246. - P. 193-195.
. Photochemical
Attachment of Fluorobutyl Moieties on a Diamond (110) - Oriented Surface: A
Multiple Internal Reflection Infrared Spectroscopic (MIRIRS) Investigation / C.
S. Kim, R. C. Mowrey, J. E. Butler, J. N.russell, Jr. // J. Phys. Chem. B. -
1998. - V.102. - P.9290-9296.
. Photochemical
modification of nanodiamond films with perfluorooctyl functionalities / T.
Nakamura, M. Hasegawa, K. Tsugawa et al. // Diamond Relat. Mater. - 2006. -
V.15; № 4-8. - P.678-681.
. Chemical
modification of DLC films with perfluorooctyl functionality / T. Nakamura, T.
Ohana, M. Suzuki et al. // Diamond Relat. Mater. - 2005. - V.14. - P.1019-1022.
. Effect
of treatment temperature on the amination of chlorinated diamond / K. - I.
Sotowa, T. Amamoto, A. Sobana et al. // Diamond Relat. Mater. - 2004. - V.13; №
1. - P.145 - 150.
. Inroad
to modification of detonation nanodiamond / B. V. Spitsyn, J. L. Davidson, M.
N. Gradoboev et al. // Diamond Relat. Mater. - 2006. - V.15; № 2-3. - Pages
296-299.
. Chemical
modification of diamond surfaces using a chlorinated surface as an intermediate
state / T. Ando, R. E. Rawles, K. Yamamoto et al. // Diamond Relat. Mater. -
1996. - V.5; № 10. - P.1136-1142.
. Miller
J. B., Brown D. W. Photochemical Modification of Diamond Surfaces // Langmuir.
- 1996. - V.12; № 24. - P.5809-5817.
. Chaney
J. A., Feigerle C. S. Characterization of chlorinated chemical vapor deposited
and natural (100) diamond // Surf. Science. - 1999. - V.425; № 2-3. -
P.245-258.
. Halogenation
and butylation of diamond surfaces by reactions in organic solvents / Y. Ikeda,
T. Saito, K. Kusakabe et al. // Diamond Relat. Mater. - 1998. - V.7; № 6. -
P.830-834.
. Incorporation
of butyl groups into chlorinated diamond surface carbons by organic reactions
at ambient temperature / T. Saito, Y. Ikeda, S. Egawa et al. // J. Chem. Soc.
Faraday Trans - 1998. - V.94; № 7. - P.929-932.
. Surface
modification of hydrogenated diamond powder by radical reactions in chloroform
solutions // T. Tsubota, K. Urabe, Shin-ichi Egawaet al. // Diamond Relat.
Mater. - 2000. - V.9; № 2. - P.219-223.
. Miller
J. Amines and thiols on diаmond
surfaces // Surf. Science.
- 1999. - V.439. - P.21-33.
105. Chemical
modification of diamond powder using photolysis of perfluoroazooctane /
Nakamura T., Ishihara M., Ohana T., Koga Y. // Chem.commun. (Camb). - 2003. -
V.7; № 7. - P.900-901.
. Photochemical
Modification of Diamond Films: Introduction of Perfluorooctyl Functional Groups
on Their Surface / Nakamura T., Suzuki M., Ishihara M. et al. // Langmuir. -
2004. - V. 20; № 14. - P.5846-5849.
. Photochemical
modification of nanodiamond films with perfluorooctyl functionalities // T.
Nakamura, M. Hasegawa, K. Tsugawa et al. // Diamond Relat. Mater. - 2006. -
V.15; № 4-8. - P.678-681.
. Chemical
modification of DLC films with perfluorooctyl functionality / T. Nakamura, T.
Ohana, M. Suzuki et al. // Diamond Relat. Mater. - 2005. - V.14. - P.1019-1022.
. Smentkowski
V. S., Yates Jr., John T. Fluorination of diamond surfaces by irradiation of
perfluorinated alkyl iodides / // Science. - 1996. - V.271; № 5246. - P.
193-195.
. Fluorination
of diamond - C4F9I and CF3I photochemistry on
diamond (100) / V. S. Smentkowski, J. T. Yates, Ch. Jr. Xiaojie, W. A. Goddard III // Surf. science. - 1997. - V.370. - P.
209-231.
111. Photochemical
Attachment of Fluorobutyl Moieties on a Diamond (110) - Oriented Surface: A
Multiple Internal Reflection Infrared Spectroscopic (MIRIRS) Investigation //
C. S. Kim, R. C. Mowrey, J. E. Butler, J. N.russell // J. Phys. Chem. B. -
1998. - V.102. - P.9290-9296.
. Photochemical
Functionalization of Diamond Films / Strother T., Knickerbocker T., Russell J.
N. et al. // Langmuir. - 2002. - V.18; № 4. - P.968-971.
. Photochemical
attachment of amine linker molecules on hydrogen terminated diamond / C. E.
Nebel, D. Shin, D. Takeuchi et al. // Diamond Relat. Mater. - 2005. - V.15. -
P.1107-1112.
. DNA-modified
nanocrystalline diamond thin-films as stable, biologically active substrates /
Yang W., Auciello O., Butler J. E. et al. // Nat. Mater. - 2002. - № 4. - P.253-257.
. Interfacial
Electrical Properties of DNA-Modified Diamond Thin Films: Intrinsic Response
and Hybridization-Induced Field Effects / W. Yang, J. E. Butler, J. N.russell,
Jr. and Robert J. Hamers // Langmuir. - 2004. - V. 20. - P.6778-6787.
. Wang
G., Bent S., Russell J. Functionalization of diamond (100) by Diels-Alder
chemistry / // J. Am. Chem. Soc. - 2000. - V.122. - P.744-745.
. Filler
M. A., Bent S. F. The surface as molecular reagent: organic chemistry at the
semiconductor interface // Progress in Surface Science. - 2003. - V.73. -
P.1-56.
. Fitzgerald
D. R., Doren D. J. Functionalization of Diamond (100) by Cycloaddition of
Butadiene: First-Principles Theory // J. Am. Chem. Soc. -
2000. - V.122; № 49. - P.12334-12339.
. Смирнов
Е.П., Гордеев С.К. Алмазы: получение, свойства, применение. - Л.: ЛТИ им.
Ленсовета, 1984. - 73 с.
120. Machinami
T., Ueda T., Ando T. Covalent immobilization of DNA on diamond and its
verification by diffuse reflectance infrared spectroscopy // Chem. Phys. Lett.
- 2002. - V.341. - P.105-108.
121. Чиганова
Г.А. Исследование поверхностных свойств ультрадисперсных алмазов // Коллоид.
журн. - 1994. - Т.56; № 2. - С.266-268.
. Игнатченко
А.В., Солохина А.Б., Ирдынеева М.В. Электроповерхностные свойства
ультрадисперсных алмазов // Сб. Докл. V Всесоюз. совещ. по детонации. Т.1. Красноярск. - 1991. - С.164 - 170.
. Исследование
взаимодействия растворов гидроокисей щелочных и щелочноземельных металлов с
препаратами алмаза / С.К. Гордеев, О.Г. Таушканова, Е.П. Смирнов, Л.М.
Мартынова // Ж. общ. химии. - 1983. - Т.53; № 11. - С.2426 - 2428.
. Поверхностные
и электрохимические свойства наноалмаза динамического синтеза / Богатырева
Г.П., Волошин М.Н., Маринич М.А. и др. // Сверхтвердые материалы. - 1999. - №
6. - С.42 - 45.
. Долматов
В.Ю. Ультрадисперсные алмазы детонационного синтеза: свойства и применение //
Успехи химии. - 2001. - Т. 20; № 7. - С.687-708.
. Чухаева
С.И., Чебурина Л.А. Сорбционная активность наноалмазов по цезию // Сверхтвердые
материалы. - 2000. - № 2. - С.43 - 48.
. А. c.1828067 СССР, Способ выделения
синтетических ультрадисперсных алмазов. / Долматов В.Ю., Сущев В.Г., Вишневский
Е.Н. (CCCР). - Опубл.25.03.86.
. Бондарь
В.С., Позднякова И.О., Пузырь А.П. Применение наноалмазов для разделения и
очистки белков // Физика твердого тела. - 2004. - Т.46; вып.4. - С.737-739.
129. Bondar
V. A., Puzyr A. P. Use of nanodiamond particles for rapid isolation of
recombinant apoobelin from Escherichia coli. // Dokl. Biochem. - 2000. -
Т.373. - С.129-131.
. Kirkland
J. J., van Straten M. A., Claessens H. A. Reversed-phase high-performance
liquid chromatography of basic compounds at pH 11 with silica-based column
packings // J. Chromatogr. A. - 1998. - V.797; №.1-2. - P.111-120.
. Hirschmann
R. P., Mariani T. L. Synthetic diamond - a solid adsorbent for corrosive gases
// J. Chromatogr. A. - 1968. - V.34; № 1. - P.78-80.
. Effect
of sintering on structure of nanodiamond / Yushin G. N., Osswald S.,
Padalko V.I. et al. // Diamond Relat. Mater. - 2005. - V.14. - № 10. -
P.1721-1729.
. Use
of industrial diamonds in HLPC / Patel B. A., Rutt K. J., Padalko V.I.,
Mikhalovsky S. V. // Сверхтвердые материалы. - 2002. - № 6. - С.51 - 54.
. Nanoporous
diamonds as stationery phase for HLPC. / Patel B. A., Rutt K. J., Padalko V.I.,
Mikhalovsky S. V. // Pittcon 2005. - Orlando, Florida, Ferbruary 2005.
P.1 - 11.
135. Емелина
С.А., Ларионов О.Г., Спицын Б.В. Использование хроматографии для изучения химии
поверхности наноалмаза // Тезисы X
Межд. конф. "Теоретические проблемы химии поверхности, адсорбции и
хроматографии".М., 2006. С.125.
. Белякова
Л.Д., Ларионова А.О., Ларионов О.Г., Спицын Б.В. Адсорбционные свойства
ультрадисперсного алмаза по данным газовой хроматографии // Тезисы XI Межд. конф. "Теоретические
проблемы химии поверхности, адсорбции и хроматографии".М., 2007. С.53
. Органикум.
Практикум по органической химии. - М.: Мир, 1979. - 350с.
. Беллами
Л. Инфракрасные спектры сложных молекул. М.: Иностранная литература. -
1963. - 590 с.
139. Pretsch
E., Buhlmann P., Affolter C.
Structure Determination of Organic Compounds. Tables of Spectral Data. -
Springer, 2000. - 421 p.
140. Определение
изотерм адсорбции методом жидкостной хроматографии / Бусев С.А., Зверев
С.И., Ларионов О.Г., Якубов Э.С. // Ж. физ. химии. - 1982. - Т.1; № 4. -
С.929-932.
. Применение
и перспективы использования хроматографии в физико-химических исследованиях,
100 лет хроматографии. Под ред. : Ларионов О.Г., Белякова Л.Д., Буряк А.Н., М.:
Наука, 2003. - 739 с.
142. T.
Jiang, K. Xu FTIR study of ultradispersed diamond powder synthesized by
explosive detonation // Carbon. - 1995. - V.33; № 12. - P.1663 - 1671.
143. Багрий
Е.И. Адамантаны: Получение, свойства, применение. М.: Наука, 1989. - 264 с.
144. Orientational
dynamics and disorder of solid adamantane as studied by infrared spectroscopy /
R. M. Corn, V. L. Shannon, R. G. Snyder et al // J. Chem. Phys. - 1984. - V.81;
№ 12. - P.5231 - 5238.
. Beamson
G., Briggs D. High Resolution XPS of Organic Polymers The Scienta ESCA 300
Databaseю - Ed. John Wiley & Sons
Ltd. - England, 1992. - P.405.
146. Беллами
Л. Новые данные по ИК-спектрам сложных молекул. М.: Мир. - 1970. - С.318.
. Oxidation
and Ammoxidation оf Aromatics / Lucke В., Narayana К. V, Martin А., Jahnisсh К // Adv. Synth. Catal. - 2004. - V.346. - P.1407-1424.
148. Сычев
А.Я. Окислительно-восстановительный катализ комплексами металлов. - Кишинев;
Штинца, 1976. - 192 c.
149. Ohno T., Mitsui T. and Matsumura M. TiO2-photocatalyzed oxidation of adamantane in solutions containing oxygen or hydrogen peroxide // J. of Photochem.
Photobiol. A: Chemistry. - 2003. - V.160. - № 1-2. - P.3 - 9.
150. Дероум
Э. Современные методы ЯМР для химических исследований. - М.: Мир, 1992. - 401
с.
151. Yesinowski
J. P. High-Resolution NMR Spectroscopy of Solids and Surface-Adsorbed Species
in Colloidal Suspension: 31P NMR Spectra of Hydroxyapatite and
Diphosphonates // J. Am. Chem. Soc. - 1981. - V.103. - P.6266-6267
152. Merckle
Ch., Blumel J. Bifunctional Phosphines Immobilized on Inorganic // Oxides Chem.
Mater. - 2001. - V.13. - P.3617-3623.
. Posset
T., Rominger F., Blumel J. Immobilization of Bisphosphinoamine Linkers on
Silica: Identification of Previously Unrecognized Byproducts via 31P
CP/MAS and Suspension HR-MAS Studies // Chem. Mater. - 2005. - V.17. -
P.586-595.
. Evaluation
of microstructural features of a new polymeric organic stationary phase grafted
on silica surface: A paradigm of characterization of HPLC-stationary phases by
a combination of suspension-state 1H NMR and solid-state 13C-CP/MAS-NMR/
H. R. Ansarian, M. Derakhshan, M. Rahman et al. // Analytica Chimica Acta. -
2005. - V.547. - P.179-187.
. Alkanethiolate
Gold Cluster Molecules with Core Diameters from 1.5 to 5.2 nm: Core and
Monolayer Properties as a Function of Core Size/ Hostetler M. J., Wingate J.
E., Zhong Ch. - J. et al. // Langmuir. - 1998. - V.14. - P.17-30.
156. Блюменфельд
Л.А., Воеводский В.В., Семенов А.Г. Применение электронного парамагнитного
резонанса в химии. Новосибирск: Изд-во СО АН СССР, 1962. - 240 с.
. Тихомирова
Н.Н., Воеводский В.В. Метод анализа формы линий электронного парамагнитного
резонанса // Оптика и спектроскопия. - 1959. - Т.7; вып.6. - С.829-832.
. Температурные
эффекты в ЭПР некоторых примесных и структурных дефектов в природных алмазах /
Самсоненко Н. Д, Зон В.Ш., Самсоненко С.Н., Сельская И.В. // Сверхтвердые
материалы. - 2000. - №.1. - С.53-62.