Долговечность строительных материалов
Федеральное
агентство по образованию
Саратовский
государственный технический университет
Долговечность СТРОИТЕЛЬНЫХ
МАТЕРИАЛОВ
Конспект
лекций
для студентов
специальности 290600 (270106.65)
«Производство строительных материалов, изделий и конструкций»
Саратов -
2010.
содержание
1. Основные
среды, действующие на строительные материалы
.
Выветривание природных каменных материалов
.
Портландцемент, состав и химическая стойкость цементного камня
. Цементы
повышенной водо- и сульфатостойкости
Сульфатостойкий
портландцемент
Пуццолановый
портландцемент
Шлакопортландцемент
. Химическая
стойкость и виды коррозии бетона
Коррозия 1
вида (коррозия выщелачивания)
Коррозия 2
вида (кислотная и магнезиальная коррозия)
Коррозия 3
вида (сульфатная и солевая коррозия)
. Механизм
электрохимической коррозии металлов
. Коррозия
стальной арматуры в бетоне
. Способы
защиты от коррозии и повышения долговечности металлических и железобетонных
конструкций
Защита от
коррозии металлических пролетных строений мостов
Защита
железобетона от коррозии
Бетонополимеры
Полимербетоны
.
Долговечность асфальтобетона
.
Долговечность древесины и способы защиты ее от гниения и возгорания
. Химическая
стойкость полимерных материалов
Виды,
основные свойства и химическая стойкость термопластов
Виды,
основные свойства и химическая стойкость реактопластов
Строение и
коррозия полимеров
Список
литературы
ПРИЛОЖЕНИЕ.
Вопросы к контрольным заданиям по вариантам
ВВЕДЕНИЕ
Обеспечение долговечности строительных материалов и конструкций является
одной из основных проблем повышения эффективности строительства. Многообразие
номенклатуры материалов и условий их эксплуатации в промышленных зданиях,
транспортных сооружениях и других объектах, в том числе и специального строительства,
требует детального и глубокого изучения химической стойкости этих материалов
под воздействием твёрдых, газообразных или жидких агрессивных сред. Знание
причин и механизма разрушения различных материалов при эксплуатации их в
агрессивных средах даёт возможность грамотно и эффективно осуществлять меры
защиты и повышения долговечности строительных конструкций и изделий.
1. ОСНОВНЫЕ СРЕДЫ, ДЕЙСТВУЮЩИЕ НА СТРОИТЕЛЬНЫЕ МАТЕРИАЛЫ
Основными средами, действующими на строительные материалы, являются воздух
и вода. Содержащийся в воздухе углекислый газ часто агрессивно воздействует на
материалы, а водяные пары воздуха участвуют во всех коррозионных процессах,
конденсируясь на поверхности материала в виде капельно-жидкой влаги.
Особо агрессивным является воздух в некоторых промышленных районах, так
как содержит многочисленные газы и пары, выделяемые в процессе производства.
Наиболее распространенными и в то же время наиболее агрессивными являются
хлор и хлористый водород, окислы азота, сернистый газ, сероводород, аммиак. Все
газы, за исключением аммиака и кислорода, являются кислыми или
кислотообразующими. Образование из них кислот происходит только при наличии в
воздухе или на поверхности конструкций капельно-жидкой влаги (тумана или
конденсата). Поэтому повышенная влажность воздуха, особенно в сочетании с
высокой загазованностью среды, является фактором, усиливающим протекание
коррозионных процессов на поверхности строительных материалов.
Степень влагонасыщения материала весьма серьезно влияет на интенсивность
и скорость развития коррозии. При относительно низкой влажности (до 60%) кислые
газы практически не действуют разрушающе на бетон, а в отдельных случаях даже
уплотняют его в поверхностном слое. Металл в сухом воздухе также практически не
коррозирует. Увеличение влажности воздуха до 69-75% увеличивает агрессивность
газовых сред, а при относительной влажности воздуха от 75 до 95% скорость
коррозии строительных материалов под воздействием различных газов резко
возрастает.
При наличии в воздухе гигроскопической пыли величина опасной, с точки
зрения процессов коррозии, влажности снижается на 10-20%. Адсорбируя влагу из
воздуха и осаждаясь на поверхности конструкций, такая пыль создает у
поверхности зону повышенной влажности, а при наличии кислых газов - и зону
повышенного кислотосодержания.
Действие газа на пористые материалы (бетон, кирпич, древесину и т.п.)
отмечается не только на поверхности, что характерно для металла и плотных
камней, но и в более глубоких слоях. В пористых материалах газы могут поглощаться
не только химическим, но и адсорбционным путем. При увеличении влажности
материала поглощенный адсорбционным путем газ образует раствор кислоты,
который, взаимодействуя с составляющими цементного камня или кирпича, приводит
увлажненный материал к быстрому разрушению.
Агрессивные свойства воды определяет степень ее минерализации, жесткости,
а также кислотности или щелочности. Обычно вода рек и озер имеет слабощелочную
реакцию. Общее содержание солей в речных водах не превышает 0,3-0,5 г/л.
Грунтовые и подземные естественные воды обычно содержат минеральные соли и
другие примеси.
Промышленные стоки или воды могут содержать самые различные примеси, в
том числе кислоты и щелочи. Следует отметить, что и совершенно чистая,
неминерализованная или мягкая вода может быть агрессивной в отношении пористых
цементных бетонов, вызывая выщелачивание извести и других растворимых солей.
Кроме химического взаимодействия, вода разрушающе действует на пористые
камни, бетоны и древесину, попадая в микрополости и растрескивая структурные
составляющие материалов.
Разрушения, вызываемые действием растворенных в воде кислот, щелочей или
солей, весьма интенсивны и разнообразны. Характер и причины этих разрушений
применительно к отдельным строительным материалам будут рассмотрены далее.
Кислоты являются наиболее агрессивными по отношению к металлам, обычным
бетонам на щелочной основе, силикатному кирпичу и осадочным горным породам
(известнякам, доломитам и т.п.). Керамические изделия, кирпич и бетоны на
жидком стекле хорошо сопротивляются действию кислот, но быстро разрушаются
щелочами.
Агрессивность кислот определяется их природой, концентрацией, рН водных
растворов, наличием окислительных свойств и температурой среды. Разрушительное
действие кислот и кислых газов определяется также растворимостью образуемых
продуктов коррозии при взаимодействии кислот с металлами или бетонами.
Концентрированные растворы щелочей, особенно при нагреве, разрушающе
действуют на некоторые металлы, камни и бетоны. Причина разрушения объясняется
тем, что в их состав входят кислые включения в виде кремнезема, а разложение их
щелочами приводит к образованию трещин и потере прочности.
Действие на металлы, бетоны, керамику и пластмассы различных солей менее
агрессивно, чем кислот. Разрушающее действие растворов солей чаще всего
определяется их способностью взаимодействовать с водой (подвергаться гидролизу)
и образовывать водородные (кислые) или гидроксильные (щелочные) ионы. В
дальнейшем разрушение материала идет так же, как при действии кислот или
щелочей.
Действие органических веществ - сахаров, масел и растворителей - на
отдельные материалы своеобразно. Для цементных бетонов агрессивными считаются
растворы сахара, фруктовые соки и т.п. При взаимодействии их с известью
цементного камня могут образовываться растворимые сахариты кальция. По
отношению к цементному бетону весьма агрессивными являются также многие
смазочные и растительные окисляющиеся масла. При этом степень разрушения тем
больше, чем меньше плотность бетона.
2. ВЫВЕТРИВАНИЕ ПРИРОДНЫХ КАМЕННЫХ МАТЕРИАЛОВ
Каменные материалы в условиях службы в конструкциях и сооружениях,
подвергаясь длительному воздействию климатических и других природных факторов
среды, постепенно разрушаются. Этот процесс, по аналогии с разрушением горных
пород на земной поверхности, называют выветриванием. Основные причины
разрушения каменных материалов: растворяющее действие воды, усиливающееся
растворенными в ней газами (SO3, СО2 и др.); замерзание
воды в порах и трещинах, сопровождающееся появлением в материале больших
внутренних напряжений, резкое изменение температур, вызывающее появление на
поверхности материалов микротрещин. Чем больше внешняя и внутренняя (поры,
микротрещины, каверны) поверхность материала, чем больше содержание
погодонеустойчивых минералов, чем более шероховатая поверхность, тем
интенсивнее протекает процесс коррозии.
Исходя из поведения при действии щелочных или кислых сред каменные
материалы обычно делят на две подгруппы.
К первой подгруппе относятся природные известняки, доломиты, мрамор.
Общим для этих материалов является преобладание оксидов кальция или магния. Все
они обладают высокой щелочестойкостью и низкой кислотостойкостью.
Ко второй подгруппе относятся каменные материалы, состоящие
преимущественно из чистого кремнезема, различных солей кремниевых и
поликремниевых кислот, алюмосиликатов, так называемые “кислые” горные породы.
Эти породы имеют высокую кислотоустойчивость и низкую щелочестойкость. Плотные
и прочные “кислые” изверженные горные породы - кварц, гранит, диабаз, базальт и
т.п. - характеризуются весьма высокой стойкостью не только к кислотам при
высокой температуре и при любых концентрациях, но и к щелочам низких и средних
концентраций при невысоких температурах.
Механизм разрушения каменных материалов при циклическом замораживании
заключается в том, что заполняющая поры камня вода при замораживании
увеличивается в объеме приблизительно на 9% и возникающие при этом внутренние
напряжения разрывают материал. Так как давление льда во внутренних частях камня
компенсируется таким же в соседних участках, то разрушение от мороза обычно
протекает с поверхности и начинается с углов и ребер.
Морозостойкость породы зависит от минералогического состава, однородности
и крупности кристаллов, так как вследствие изменения объема при перепадах
температуры от +18 до -20°С
могут быть нарушены кристаллизационные связи.
Весьма важным оказывается и то, насколько заполнены водой поры камня.
Если они заполнены только на 80-85%, вода имеет возможность расширяться внутри
пор, при этом сильного разрушения не происходит, то есть порода является
морозостойкой. Наиболее легко разрушаются морозом относительно малопрочные,
сильнопористые и одновременно сильно насыщаемые водой камни.
Все мероприятия по защите каменных материалов от выветривания направлены
на повышение их поверхностной плотности и на предохранение от воздействия
влаги.
Стойкость материалов против выветривания можно повысить конструктивными
мерами, к числу которых относятся обеспечение хорошего стока воды, устранение в
конструктивном элементе выступов, придание камням плотной и гладкой
поверхности. Стойкость против выветривания пористых материалов существенно
повышается при создании на их лицевой поверхности плотного водонепроницаемого
слоя или гидрофобизации. Одним из способов повышения поверхностной плотности
камня является флюатирование, при котором пористые известняки пропитывают
солями кремнефтористоводородной кислоты, например, флюатом магния. В результате
реакции
MgSiF6 + 2CaCO3 = 2CaF2 +SiO2
+MgF2 + 2CO2
в поверхностных порах камня отлагаются труднорастворимые в воде фториды
кальция и магния, а также кремнезем. Некарбонатные пористые породы перед
пропиткой флюатами предварительно обрабатывают водными растворами кальциевых
солей, например, хлористым кальцием CaCl2.
Гидрофобизация, т.е. пропитка пористого каменного материала гидрофобными
(водоотталкивающими) составами, резко понижающими проникание влаги в материал,
в частности путем капиллярного подсоса, также повышает стойкость материалов
против выветривания.
3. ПОРТЛАНДЦЕМЕНТ, СОСТАВ И ХИМИЧЕСКАЯ СТОЙКОСТЬ ЦЕМЕНТНОГО КАМНЯ
Портландцементом называется гидравлическое вяжущее вещество, получаемое
тонким измельчением клинкера с гипсом (3-5%), а иногда и с активными
минеральными добавками (до 10%).
Минералогический состав цемента в процентах может колебаться в следующих
пределах:
трехкальциевый силикат (алит) 3CaO·SiO2(C3S) -
45-60;
двухкальциевый силикат (белит) 2CaO·SiO2(C2S) -
20-30;
четырехкальциевый алюмоферит 4CaO·Al2O3·Fe2O3(C4AF)
- 10 - 20.
В настоящее время выпускаются следующие основные разновидности
портландцемента:
быстротвердеющий портландцемент;
пластифицированный и гидрофобный портландцементы;
сульфатостойкий портландцемент, содержащий C3S не более 50% и
C3A не более 5%;
шлаковый портландцемент с 21-60% доменного гранулированного шлака;
пуццолановый портландцемент, содержащий до 20-40% пуццолановых добавок;
белый и цветные портландцементы.
Различные виды цементов характеризуются различной стойкостью против
действия тех или иных агрессивных факторов. Например, цементы с низким
содержанием алюминатов кальция характеризуются повышенной стойкостью против
действия гипса и других сульфатов и называются поэтому сульфатостойкими.
Пуццолановые портландцементы отличаются повышенной водостойкостью и т.д. Поэтому
выбирать цементы для бетонов различного назначения следует не только с учетом
их прочностных показателей, но и стойкости против действия тех агрессивных
сред, в которых должны работать бетонные конструкции.
По агрессивному действию на цементный камень природные воды
подразделяются на мягкие; содержащие агрессивную углекислоту; содержащие
сульфаты; содержащие повышенное количество солей магния и содержащие свободные
кислоты.
Мягкими называют воды с жесткостью менее 4 мг.экв/л. В мягких водах соли
кальция и магния присутствуют в незначительном количестве, поэтому мягкие воды
способны растворять Ca(OH)2, образующий кристаллический сросток
цементного камня, что и приводит к его разрушению.
При наличии в природных водах агрессивной углекислоты, способной реагировать
с CaCO3, гидрат окиси кальция также растворяется (выщелачивается) по
реакциям:
Ca(OH)2 + CO2 = CaCO3 +H2O
и затем
CaCO3 + CO2 + H2O = Ca(HCO3)2.
Образовавшийся бикарбонат кальция хорошо растворяется в воде, причем
растворяющее действие воды тем больше, чем выше содержание в ней агрессивной
углекислоты и чем меньше временная жесткость воды.
Разрушение портландцемента водами, содержащими сульфаты, вызывается
следующими причинами.
. Гидрат окиси кальция Ca(OH)2 вступает с сульфатами в
обменную реакцию:
Ca(OH) 2 + MgSO4 +2H2O =
CaSO4·2H2O +Mg(OH)2.
Образующийся гипс реагирует с гидроалюминатом кальция, находящимся в
цементном камне, по уравнению
3CaSO4·2H2O + 3CaO·Al2O3·6H2O
+ 19H2O =
= 3CaO·Al2O3·3CaSO4 ·31H2O.
Образование нового соединения - гидросульфоалюмината кальция -
сопровождается значительным увеличением объема твердой фазы цементного камня,
что приводит к возникновению в нем внутренних напряжений и в дальнейшем к
разрушению. При наличии в воде значительного количества хлоридов гидросульфоалюминат
кальция не образуется, поэтому агрессивность воды определяется по содержанию в
ней ионов SO42- с учетом количества ионов хлора.
. При достаточно высокой концентрации сульфатов в агрессивных водах в
порах цементного камня в результате обменных реакций образуется гипс CaSO4·2H2O.
Разрушение цементного камня в этом случае вызывается кристаллизационным
давлением растущих кристаллов двуводного гипса.
Магнезиальная коррозия портландцемента может развиваться под действием
природных вод с содержанием катионов Mg2+ свыше 5000 мг/л. Соли
магния, проникая в цементный камень, взаимодействуют с Ca(OH) 2 по
реакции
MgCl2 + Ca(OH) 2 = Mg(OH) 2 + CaCl2
или
MgSO4 + Ca(OH) 2 + 2H2O =
CaSO4·2H2O + Mg(OH) 2.
При этом труднорастворимый гидрат окиси магния осаждается в порах в виде
рыхлой массы, а CaCl2 вымывается, что приводит к разрушению
цементного камня. Двуводный сульфат кальция возникает в порах с увеличением
объема, что также ускоряет растрескивание цемента.Кислотная коррозия происходит
при действии растворов любых кислот с рН менее 7; исключение составляют
поликремниевая и кремнефтористоводородная кислоты. Свободные кислоты
встречаются в сточных водах промышленных предприятий, они могут проникать в
почву и разрушать бетонные фундаменты, коллекторы и т.д. Кислота образуется
также из сернистого газа, выходящего из топок. В атмосфере промышленных
предприятий, кроме SO2, могут содержаться ангидриды других кислот, а
также хлористый водород. При растворении его во влаге, адсорбированной на
поверхности конструкций, образуется соляная кислота. Кислота вступает в
химическое взаимодействие с гидратом окиси кальция, при этом образуются
растворимые соли (CaCl2) и соли, увеличивающиеся в объеме (CaSO4·2H2O):
Ca(OH) 2 + 2HCl = CaCl2 + 2H2O;
Ca(OH) 2 + H2SO4 = CaSO4·2H2O.
Кроме того, кислоты могут разрушать и силикаты кальция.
Органические кислоты, как и неорганические, быстро разрушают затвердевший
портландцемент. Большой агрессивностью отличаются уксусная, молочная, масляная
и винная кислоты. Жирные кислоты (олеиновая, стеариновая и др.) разрушают
цементный камень, так как при действии гидрата окиси кальция они омыляются.
Поэтому вредны и масла, содержащие кислоты жирного ряда: льняное, хлопковое.
Нефть и нефтяные продукты (керосин, бензин, мазут) не представляют опасности для
цемента, если они не содержат большого количества нафтеновых кислот или
соединений серы.
. ЦЕМЕНТЫ ПОВЫШЕННОЙ ВОДО - И СУЛЬФАТОСТОЙКОСТИ
СУЛЬФАТОСТОЙКИЙ ПОРТЛАНДЦЕМЕНТ
Сульфатостойким называют портландцемент, изготовляемый из клинкера,
минералогический состав которого нормирован по содержанию C3A и C3S.
Он отличается пониженной экзотермией при твердении и высокой стойкостью при
действии сульфатных вод.
Высокая стойкость этого цемента в сульфатных водах обусловлена тем, что в
затвердевшем состоянии он содержит пониженное количество высокоосновных
гидроалюминатов кальция. Этим устраняется возможность образования значительного
количества гидросульфоалюмината кальция, вызывающего коррозию
портландцементного камня. Развитие коррозионных процессов в затвердевшем
сульфатостойком портландцементе замедляется также вследствие ограниченного
содержания в клинкере C3S.
Такой портландцемент значительно превосходит по сульфатостойкости рядовые
портландцементы, но уступает в этом отношении пуццолановым и шлаковым портландцементам,
изготовляемым на основе клинкера того же нормированного состава. Однако эти
цементы менее морозостойки. Поэтому сульфатостойкий цемент целесообразнее всего
применять в тех случаях, когда одновременно требуется высокая стойкость против
воздействия сульфатных вод и попеременного замораживания и оттаивания,
высыхания и увлажнения.
ПУЦЦОЛАНОВЫЙ ПОРТЛАНДЦЕМЕНТ
Пуццолановым портландцементом называют гидравлическое вяжущее, получаемое
путем совместного тонкого измельчения портландцементного клинкера, кислой
активной минеральной добавки и гипса. В пуццолановом портландцементе
допускается следующее содержание активных минеральных добавок: осадочного
происхождения - не менее 20 и не более 30%; вулканического происхождения,
обожженной или топливной золы - не менее 25 и не более 40 %.
Реакция между продуктами гидратации клинкера и активными компонентами
гидравлической добавки заключается во взаимодействии Ca(OH)2 с
активным кремнеземом добавки и образовании гидросиликатов по схеме
m Ca(OH)2 + SiO2 + n H2O = m
CaO·SiO2·(n+1)H2O
Для бетонов на пуццолановом портландцементе показательна более высокая
водостойкость, чем для бетонов на портландцементе, что объясняется более
высокой их водонепроницаемостью и связыванием добавками легко вымываемого
гидрата окиси кальция.
Пуццолановый цемент более стоек в сульфатных водах вследствие того, что в
его цементном камне почти полностью отсутствуют гидроокись кальция и
высокоосновные гидроалюминаты кальция, на базе которых в присутствии сульфатных
солей возможно образование гидросульфоалюмината кальция, разрушающего цементный
камень.
В кислых и, в частности, в углекислых водах пуццолановые портландцементы,
как и обычные цементы, недостаточно стойки. Это обусловлено тем, что свободные
органические и минеральные кислоты интенсивно взаимодействуют не только с
гидратом окиси кальция, но и с гидросиликатами и гидроалюминатами кальция,
полностью разрушая цементный камень.
Щелочестойкость пуццолановых цементов ниже, чем портландцементов.
ШЛАКОПОРТЛАНДЦЕМЕНТ
Шлакопортландцементом называется гидравлическое вяжущее, получаемое путем
совместного тонкого измельчения портландцементного клинкера и гранулированного
доменного шлака с добавлением небольшого количества гипса (до 3,5% от массы
всей смеси).
Шлака в портландцементе должно быть не менее 21% и не более 60% по массе.
В затвердевшем шлакопортландцементе преобладают низкоосновные
гидросиликаты кальция, а свободный гидрат окиси кальция отсутствует или
содержится в незначительном количестве.
Стойкость шлакопортландцементов при воздействии мягких и сульфатных вод
выше, чем портландцементов. Повышенная стойкость шлакопортландцемента в мягких
водах объясняется образованием при его твердении цементирующих новообразований
пониженной основности и незначительным содержанием в цементном камне гидрата
окиси кальция. Поэтому для частей сооружений, постоянно находящихся в речной
воде, предпочтительнее шлаковые портландцементы, а не обычный портландцемент.
Значительное снижение концентрации гидрата окиси кальция в жидкой фазе
твердеющего шлакопортландцемента уменьшает возможность образования
гидросульфоалюмината кальция при проникании сульфатных вод. Поэтому в
затвердевшем цементном камне не возникают вредные объемные деформации,
нарушающие его структуру. Этим объясняется более высокая стойкость шлакопортландцемента
в минерализованных сульфатных водах по сравнению с портландцементом.
В кислых и углекислых водах, в которых степень разрушения цементного
камня мало зависит от содержания в нем Ca(OH)2, стойкость
шлакопортландцемента такая же, как у портландцемента. Однако в отличие от
портландцемента он не эффективен в частях сооружений, подвергающихся
попеременному замораживанию и оттаиванию или увлажнению и высыханию.
агрессивный коррозия долговечность
5. ХИМИЧЕСКАЯ СТОЙКОСТЬ И ВИДЫ КОРРОЗИИ БЕТОНА
КОРРОЗИЯ I ВИДА (КОРРОЗИЯ ВЫЩЕЛАЧИВАНИЯ)
Растворимость продуктов гидратации цемента в воде обусловливает
возможность коррозии цементного камня в бетонах и растворах за счет растворения
и вымывания соединений, определяющих прочность кристаллизационных контактов в
цементном камне. Так как наиболее растворимым компонентом цементного камня на
основе портландцемента является гидроокись кальция, то коррозионный процесс
определяется обычно как процесс “выщелачивания” извести. Существует прямая
зависимость интенсивности процесса выщелачивания от проницаемости (плотности)
бетона и от минералогического состава цементного камня - количества свободного
гидроксида кальция в нем.
Серьезные повреждения обычного бетона могут иметь место при действии на
него мягких вод, содержащих мало растворенных веществ. К ним относятся
конденсат, воды оборотного водоснабжения, дождевые, болотные, воды горных и
равнинных рек в половодье.
При действии на бетон мягких вод вначале выщелачивается свободная
гидроокись кальция, образовавшаяся при гидролизе трехкальциевого силиката.
Когда концентрация Ca(OH)2 становится менее 1,1 г/л, начинается
разложение гидросиликатов кальция и происходит вымывание получившейся
гидроокиси. Выщелачивание Ca(OH)2 в количестве 15-30% общего
содержания в цементном камне вызывает понижение его прочности на 40-50% и
более.
Признаки коррозии I вида
можно наблюдать в бетоне различных сооружений. Особенно заметной она становится
на участках высыхания воды, соприкасающейся с цементным камнем в бетоне. В этом
случае растворенные в воде соединения, в первую очередь гидроокись кальция,
карбонизируясь и выпадая в осадок в виде карбоната кальция, образуют на
поверхности белый налет (“белая смерть бетона”). Под влиянием углекислого газа
воздуха гидроксид кальция постепенно превращается в карбонат, что закрепляет
этот налет и не дает ему вновь раствориться при последующих увлажнениях
поверхности.
В стойкости бетона против коррозии I вида большую роль играет его плотность. Чем меньше площадь
поверхности соприкосновения бетона с водой - средой и фильтрация воды через
бетон, тем меньше и скорость развития коррозии. Таким образом, в число основных
мероприятий, в результате которых могут быть повышены стойкость и долговечность
бетона при коррозии I вида, входят все, способствующие увеличению плотности
бетона, а также использование цементов, наиболее стойких к растворяющему
действию воды и, в первую очередь, пуццолановых и шлакопортландцементов,
которые можно применять, если конструкции не находятся в условиях частой смены
замораживания и оттаивания.
Процесс выщелачивания гидрата окиси кальция замедляется также когда в
поверхностном слое бетона под воздействием углекислого газа воздуха, вследствие
карбонизации, образуется малорастворимый CaCO3. Выдерживание на
воздухе бетонных блоков и свай для карбонизации поверхностного слоя бетона
повышает их стойкость против выщелачивания.
КОРРОЗИЯ II
ВИДА (КИСЛОТНАЯ И МАГНЕЗИАЛЬНАЯ КОРРОЗИЯ)
Коррозия II вида связана с
развитием обменных реакций между кислотами или солями окружающей среды, с одной
стороны, и составляющими цементного камня - с другой. Чем энергичнее протекает
реакция взаимодействия и чем более растворимы новообразования, тем скорее и
полнее разрушается бетон.
При действии кислоты цементный камень полностью разрушается, причем
продукты разрушения частично растворяются, а частично остаются на месте
реакции. Разрушение цементного камня идет в поверхностных слоях бетона,
соприкасающихся с агрессивной средой, и процесс разрушения этих слоев может
достичь полного развития при сохранении в прилегающих слоях бетона почти без
изменения всех элементов цементного камня.
Так как кислоты взаимодействуют прежде всего с гидроксидом кальция, а
затем с гидросиликатами и гидроалюминатами кальция с образованием кальциевых
солей, то от их растворимости и структуры слоя продуктов коррозии в
значительной степени и зависит скорость разрушения бетона. Если
новообразования, не обладающие вяжущими свойствами и достаточной плотностью,
чтобы воспрепятствовать дальнейшему прониканию агрессивной среды, растворяются или
смываются механически, то обнажаются более глубокие слои бетона. Последние
также разрушаются и процесс коррозии протекает до полного разрушения всего
бетона, однако скорость этого процесса может быть различной. В данном случае
ограничивающими скорость коррозии факторами являются реакционная емкость
агрессивной среды и скорость ее обмена у поверхности бетона.
Если новообразования нерастворимы или после удаления растворимых
продуктов реакции остается достаточно плотный слой продуктов реакции, который в
конкретных условиях контакта агрессивной среды и бетона не удаляется, то они
замедляют доступ агрессивной среды к внутренним, еще не поврежденным, частям
цементного камня. В этом случае скорость коррозии зависит от толщины и
диффузионной проницаемости слоя, образовавшегося на поверхности цементного
камня.
Наиболее часто встречающаяся в природных условиях коррозия II вида - это коррозия при действии
углекислых вод. Углекислота в большем или меньшем количестве присутствует в
большинстве природных вод. При действии углекислоты на цементный камень бетона,
еще не имеющего карбонизированного поверхностного слоя, идут два процесса.
Вначале при избытке в поверхностном слое бетона ионов OH- образуется
карбонат кальция. После того, как ионы OH- в поверхностном слое бетона
будут израсходованы, начнется образование бикарбоната кальция, растворяющегося
в водной среде и уносимого ею. При наличии же карбонатного слоя будет идти лишь
образование бикарбоната. При одном и том же содержании агрессивной CO2
в растворе наличие карбонатного слоя приводит к образованию в 2 раза большего
количества бикарбоната. Следовательно, наличие карбонизированного слоя бетона
при действии на него углекислых вод ускоряет коррозию и, соответственно,
снижает стойкость бетона.
Соли магния, которые встречаются в растворенном виде в грунтовых водах и
всегда содержатся в большом количестве в морской воде, также могут вызвать
разрушение цементного камня в бетоне в результате обменных реакций с
кристаллами гидроокиси кальция. Вода является агрессивной при содержании ионов
магния более 0,5%. Наблюдения за состоянием и характером разрушения бетона,
подвергающегося в течение длительного времени действию растворов магнезиальных
солей, показывают, что сначала на поверхности бетона и в его порах образуется
белый налет, а затем и скопление белого аморфного вещества - гидроксида магния.
Чем более проницаем для морской воды бетон и чем выше относительное содержание
CaO в цементе, тем в большем количестве образуется эта белая аморфная масса и
тем в большей степени теряет бетон механическую прочность.
Для защиты бетона от разрушения при действии растворов кислот необходимо
либо заменять обычные цементы кислотоупорными и применять кислотоупорные бетоны
или полимербетоны, либо устраивать надежную изоляцию поверхности бетонов
покраской или облицовкой.
Для снижения скорости коррозии бетона в растворах магнезиальных солей
могут быть приняты следующие меры:
) повышена плотность бетона; 2) в случае сильно агрессивной среды
использованы покраски или облицовки, защищающие поверхность бетона от
соприкосновения с агрессивной средой.
КОРРОЗИЯ III
ВИДА (СУЛЬФАТНАЯ И СОЛЕВАЯ КОРРОЗИЯ)
Основным признаком коррозии III вида является накопление в порах и капиллярах бетона солей и последующая
их кристаллизация, связанная с увеличением объема твердой фазы. Соли либо
образуются вследствие химических реакций взаимодействия агрессивной среды с
составными частями цементного камня, либо привносятся извне и выделяются из
раствора вследствие постепенного испарения из него воды.
Выделение твердой фазы и рост кристаллообразований могут вызвать на
определенной ступени развития значительные растягивающие усилия в стенках пор и
капилляров и разрушение структурных элементов бетона. При коррозии III вида на начальной стадии за счет
накопления солей в порах бетона он уплотняется. Если этот процесс развивается
медленно, заполнение пор и пустот в бетоне кристаллическими новообразованиями и
связанное с ним уплотнение бетона создает картину ложного благополучия.
Прочность бетона при этом на какой-то период увеличивается и превышает
плотность бетона, не подвергавшегося действию агрессивной среды. Лишь после
возникновения значительных растягивающих усилий в стенках пор и капилляров,
вызванных продолжающимся ростом кристаллообразований, происходит разрушение
структурных элементов цементного камня бетона и наблюдается быстрое снижение
(сброс) прочности. Чем медленнее протекает коррозия, тем позднее наступает
сброс прочности.
Особенностью этих реакций является то, что и гипс, и гидросульфоалюминат
кристаллизуются с большим количеством воды при значительном увеличении объема.
Если такое образование происходит в порах уже сложившейся структуры цементного
камня, то возникают большие внутренние напряжения, приводящие бетон в
конструкциях к характерному растрескиванию или отслаиванию поверхностных слоев.
Гидросульфоалюминат кристаллизуется в виде характерных игл, поэтому обычно
называется “цементной бациллой”.
Если образование гидросульфоалюмината протекает еще до формирования
структуры бетона в жидкой фазе или в растворе присутствуют в значительном
количестве ионы хлора, усиливающие растворимость алюминатов и сульфоалюмината,
опасных напряжений может не возникать. Этим объясняется относительно невысокая
агрессивность к цементному бетону морской воды, в которой содержится большое
количество сульфатов, но еще большее количество хлоридов.
При сульфатной коррозии интенсивность коррозионного процесса определяется
количеством агрессивного вещества, проникающего в структуру цементного камня, и
химической активностью внутренней поверхности этого камня. При этом имеются в
виду условия, в которых бетон постоянно погружен в агрессивный раствор и
перемещение агрессивного компонента в порах бетона может происходить только в
результате диффузии. В случае же постоянного частичного, периодического полного
или частичного погружения бетона при контакте агрессивной среды с цементным
камнем протекают процессы, которые не происходят в условиях полного погружения
материала.
Основное отличие процессов солевой коррозии бетона при постоянном
частичном или периодическом (полном и частичном) погружении, когда протекают
коррозионные процессы, в которых химическое действие агрессивного раствора не
играет существенной роли, состоит в том, что в этом случае на движение
растворов в поровой структуре бетона оказывают решающее влияние процессы,
происходящие на поверхности бетона, оказавшейся в период воздействия на
воздухе.
В условиях, когда бетонная или железобетонная конструкция частично
погружена в жидкость, содержащую растворенные соли, интенсивность коррозии
будет зависеть от кинетики проникновения агрессивных компонентов в бетон,
которая будет определяться при частичном погружении интенсивностью испарения
воды и капиллярной проницаемостью бетона. Площадь открытой поверхности бетона,
находящейся на воздухе, расстояние от уровня агрессивного раствора до открытой
поверхности, а также внешние условия играют важную роль в переносе раствора в
теле бетона и определяют интенсивность коррозионного процесса. Когда в порах
бетона в результате испарения воды повышается концентрация агрессивного
раствора и происходит кристаллизация солей, то при накоплении солей в порах
появляется кристаллизационное давление, которое при определенных условиях может
превысить прочность материала пор на растяжение и вызвать возникновение трещин
и разрушение бетона.
Главным условием стойкости бетона при коррозии III вида является устойчивость цементного камня к
химическому действию среды, в частности, при сульфатной коррозии цементный
камень сам по себе должен обладать сульфатостойкостью, т.е. при данном
содержании сульфатов иметь наименьшую реакционную способность по отношению к
ним. Это может быть достигнуто, в первую очередь, ограниченным содержанием в
цементе трехкальциевого алюмината.
Коррозия III вида в значительной
степени зависит и от плотности бетона, поскольку степень повреждения
определяется количеством агрессивного компонента, проникающего из окружающей
среды в бетон, а оно прямо пропорционально свободному сечению пор в бетоне.
Следовательно, все технологические приемы, используемые при изготовлении бетона
с целью повышения его плотности (непроницаемости), будут способствовать
повышению стойкости бетона к сульфатной коррозии и коррозии III вида вообще.
В специфических условиях развития коррозии III вида вследствие частичного
или периодического высыхания бетона хорошим средством повышения его стойкости
является объемная гидрофобизация. Гидрофобизация прерывает пути капиллярного
движения растворов в бетоне, что исключает перемещение растворимых солей в нем и
накопление их в отдельных зонах. В подземных сооружениях гарантировать от
развития коррозии III вида в случае
действия напорных вод на бетон может только надежная гидроизоляция.
6. МЕХАНИЗМ ЭЛЕКТРОХИМИЧЕСКОЙ КОРРОЗИИ МЕТАЛЛОВ
Коррозия металлов, применительно к условиям эксплуатации строительных
конструкций и сооружений, носит преимущественно электрохимический характер
(коррозия во влажной атмосфере, в воде, солевых растворах и т.п.).
Электрохимическая коррозия является результатом работы множества микроскопических
короткозамкнутых гальванических элементов, возникающих на поверхности металла
при контакте с электролитом вследствие неоднородности металла или окружающей
среды.
Так как применяемые в строительстве металлы и сплавы неоднородны (наличие
примесей) и контактирующая с ними среда также неоднородна (почвенные условия,
загрязненная промышленная атмосфера и т.д.), то создаются все условия для
протекания процессов электрохимической коррозии.
Известно, что при погружении в электролит двух электродов из разных
металлов они приобретают различные по величине электрические потенциалы. При
замыкании электродов между ними возникает ток. Прохождение тока сопровождается
растворением электрода с более электроотрицательным потенциалом - анода.
Короткозамкнутые гальванические элементы могут возникать и на одном
металле вследствие наличия участков поверхности с различными потенциалами.
Разность потенциалов наблюдается между различными обработанными поверхностями,
разными структурными составляющими сплава, примесями и основным металлом, а
также между участками поверхности с различным состоянием пленки окислов.
На величину потенциала металла влияют и многие другие факторы, например,
состав электролита, скорость его движения, концентрация газов. Поэтому
практически всегда при соприкосновении с электролитом на поверхности металла
возникают короткозамкнутые гальванические элементы, которые называют
коррозийными микро- и макроэлементами.
Процесс электрохимической коррозии, то есть деятельности коррозийных
гальванических пар, довольно сложен и может быть разбит на ряд элементарных
процессов.
На анодных участках имеет место анодный процесс - переход в раствор ионов
металла и их гидратация с освобождением избыточного электрона, который,
оставаясь в металле, движется к катодному участку. Обычно этот процесс
схематически изображается так:
e ¬ [Me+ Є] nH2O ® Me4+
n H2O.
На катодных участках поверхности металла происходит ассимиляция
избыточных электронов каким-либо деполяризатором (атомом или ионом раствора,
способным восстанавливаться, то есть поглощать электрон):
e + D ® [De]
Наиболее практически важными разновидностями катодного процесса являются:
катодная реакция восстановления иона водорода в газообразный водород
(водородная деполяризация):
+
+ e ® H и затем H + H = H2,
и катодная реакция восстановления кислорода с превращением его в ион
гидроксида (кислородная деполяризация):
O2 + 2H2O + 4e ® 4OH-
Огромное число происходящих в природе и технике коррозийных процессов
связано с поглощением кислорода. Такому виду разрушения металлы подвергаются
при коррозии в воде, атмосфере, почве. Коррозия стали в бетоне также идет с
кислородной деполяризацией.
Катодный и анодный процессы идут на разных участках поверхности металла,
и электроны, избыточные у анодов, передвигаются в металле к катодам,
соответственно, в растворе происходит направленное перемещение ионов. Возникает
электрический ток, называемый током коррозии. При таком механизме коррозии
разрушению подвергаются лишь анодные участки поверхности металла.
Перечисленные процессы взаимозависимы и эквивалентны, то есть скорость
процесса коррозии, в целом, будет определяться скоростью того процесса, который
в данных условиях протекает медленнее. При коррозии металла в нейтральных и
щелочных средах таким контролирующим фактором чаще всего является поступление
кислорода к коррозирующей поверхности.
Скорость коррозии, выраженная в весовых потерях металла на единицу
поверхности в единицу времени, зависит от величины тока коррозии, то есть от
разности потенциалов анодных и катодных участков и омического сопротивления
внутренней цепи коррозионного элемента.
Однако начальные значения электродных потенциалов катодных и анодных
участков микропар не определяют величину коррозийного тока и скорость коррозии.
Вследствие целого ряда причин значения этих потенциалов с самого начала работы
коррозионного элемента начинают изменяться в сторону уменьшения первоначальной
разности потенциалов. Это явление, то есть изменение потенциалов электродов в
результате протекания тока, называют поляризацией.
Различают анодную и катодную поляризацию. Анодная поляризация вызывается,
главным образом, увеличением концентрации ионов растворяющегося металла в
прилегающем слое электролита, что приводит к сдвигу потенциала анода в сторону
катодного потенциала. Движение электролита, уносящего от поверхности анода ионы
металла, уменьшает анодную поляризацию. Другой причиной анодной поляризации
является образование на аноде нерастворимых соединений - пассивирование.
Катодная поляризация вызывается недостаточно быстрым связыванием
электронов, поступающих с анодных участков, то есть накоплением электронов.
Факторы разного рода, уменьшающие поляризацию электродов, называются
деполяризующими факторами.
Вещества, повышающие скорость коррозии, обычно называют стимуляторами;
вещества, которые снижают скорость коррозии, называют ингибиторами. Кислород,
например, является одновременно и стимулятором, и ингибитором. Он способствует
улучшению защитно-окисной пленки, то есть действует как ингибитор, уменьшает
вероятность коррозии, сокращает число очагов, в которых может возникнуть
коррозийный процесс. Вместе с тем кислород повышает скорость коррозии в
начавших корродировать точках, действует стимулирующе, поскольку является
сильным катодным деполяризатором.
Существует целый ряд веществ, присутствие которых в окружающей среде
влияет на скорость коррозийного процесса. Ионы хлора, SO4 и
некоторые другие разрушающе действуют на защитные окисные пленки и всегда
стимулируют коррозию. Успешно тормозят коррозийный процесс в нейтральных и
щелочных средах сильные окислители - соли щелочных металлов - хроматы, нитриты
и т.д.
По характеру разрушения поверхности металла различают следующие основные
виды коррозии:
) равномерная, или общая коррозия, равномерно распределенная по
поверхности металла;
) местная, или локальная коррозия, сосредоточенная на отдельных участках
поверхности;
) точечная коррозия, или питтинг, сосредоточенная на очень малых участках
поверхности, но отличающаяся глубоким проникновением;
) межкристаллитная (интеркристаллитная) коррозия, когда разрушение
сосредоточивается на границах кристаллов.
7. КОРРОЗИЯ СТАЛЬНОЙ АРМАТУРЫ В БЕТОНЕ
Защитный слой бетона в железобетонных конструкциях ограждает арматуру от
внешней среды, но не изолирует ее полностью. Внешняя по отношению к
железобетонным конструкциям среда воздействует прежде всего на бетон и лишь
через него - на арматуру. По существу, средой, в которой находится арматура,
является бетон.
Коррозия стальной арматуры происходит по электрохимическому механизму,
для действия которого необходимы следующие условия:
наличие разности потенциалов между отдельными участками поверхности
металла, т.е. электрохимическая неоднородность ее;
наличие электролитической связи между этими участками;
активное состояние поверхности на анодных участках, где металл
растворяется;
наличие достаточного количества деполяризатора, в частности кислорода,
необходимого для поглощения на катодных участках поверхности металла избыточных
электронов.
Поскольку структура стали и контактного слоя бетона у ее поверхности
неоднородны, то первое условие для арматуры в бетоне выполняется всегда. Так
как бетон представляет собой капиллярно-пористое тело с активной и гидрофильной
внутренней поверхностью, то второе и четвертое условия протекания коррозионного
процесса в бетоне также выполняются. Следовательно, отсутствие коррозии стали в
плотном бетоне связано с тем, что не выполняется третье условие.
Защита бетоном стальной арматуры основывается на пассивирующем действии
щелочных сред. В щелочных растворах коррозия железа уменьшается, что
объясняется образованием защитной пленки из гидрата окиси железа. С увеличением
рН уменьшается растворимость гидроокиси и защитные свойства пленки повышаются.
При гидратации зерен портландцементного клинкера в значительном
количестве образуется гидрат окиси кальция. Влага, содержащаяся в пористом теле
цементного камня, твердевшего в нормальных условиях и не претерпевшего
изменений по влиянием агрессивной среды, насыщена гидратом окиси кальция и
имеет щелочную реакцию. Величина рН жидкой фазы такого бетона находится в
пределах 12,2-13,0. В водном растворе с таким рН наступает практически полная
пассивация поверхности стали.
Однако бетон представляет собой капиллярно-пористое тело. Основную массу
пор и капилляров в бетоне составляют поры и капилляры цементного камня,
образовавшиеся в результате испарения избыточной воды затворения. В процессе
длительного твердения при полной гидратации зерен клинкера химически связанная
вода составляет до 20-25% от массы цемента (в/ц = 0,2-0,25). Практически для
получения удобоукладываемых смесей применяют в/ц не менее 0,4. Избыточная вода
затворения образует, испаряясь, разветвленную сеть пор и капилляров - мелких в
цементном камне, более крупных - на контакте цементного камня с зернами
заполнителя. Капиллярно-пористое тело бетона в зависимости от плотности
структуры обладает различной проницаемостью для газов, паров и жидкостей. Кроме
того, в зависимости от влажностных условий окружающей среды бетон может иметь
разную степень насыщения влагой.
При непосредственном длительном увлажнении бетона заполняются все поры,
включая крупные, и арматура находится в условиях полного погружения в
электролит. Аэрация поверхности стали в этом случае затруднена, т.к. поры
закрыты влагой и в таких условиях арматура в обычном плотном бетоне не
корродирует. Низкой относительной влажности окружающей среды соответствует
малая степень заполнения влагой пор бетона. Несмотря на сравнительно легкий
доступ кислорода воздуха к поверхности арматуры, на ней оказывается мало влаги
для протекания процесса электрохимической коррозии стали. Поэтому при
относительной влажности воздуха ниже 60% в обычном тяжелом бетоне коррозии
арматуры не наблюдается. Коррозия арматуры в плотном бетоне обычно происходит
при значениях относительной влажности воздуха 70-80%, либо при периодических
увлажнениях конструкций. В этих условиях влажностное состояние бетона таково,
что наряду с наличием достаточного количества влаги для работы коррозийных
гальванических пар на поверхности арматуры имеется более или менее свободный
доступ кислорода воздуха к ней через частично открытые поры и капилляры.
Чем больше пор в бетоне и чем они крупнее, тем более неоднородны условия
на поверхности арматуры как из-за несплошного обволакивания арматуры цементным
камнем и пленками щелочной влаги, так и вследствие разной степени аэрации ее
поверхности. Чем больше пористость и неоднородность структуры бетона, тем выше
опасность возникновения коррозии арматуры и скорость ее развития.
Другой особенностью бетона как среды для арматуры является то, что его свойства
изменяются во времени. Пористый цементный камень, проницаемый для паров и
газов, соприкасаясь с воздушной средой, может подвергаться интенсивной
карбонизации. В процессе карбонизации углекислый газ воздуха проникает в поры и
капилляры бетона, растворяется в поровой жидкости и реагирует с гидроокисью
кальция, образуя слаборастворимый карбонат кальция. Карбонизация снижает
щелочность содержащейся в бетоне влаги. Скорость распространения процесса
карбонизации вглубь бетона зависит от его проницаемости и концентрации
углекислоты воздуха.
Присутствующие в промышленной атмосфере кислые газы - сернистый газ,
хлор, хлористый водород - также поглощаются бетоном и реагируют с гидратом
окиси кальция, резко понижая щелочность бетона. Бетон, лишенный естественной
щелочности, перестает оказывать защитное действие на стальную арматуру, и при
определенном влажностном состоянии бетона арматура начинает корродировать,
причем скорость коррозии будет зависеть от воздухопроницаемости бетона.
Другими факторами, влияющими на состояние арматуры в бетоне, кроме
состава и влажности окружающей среды, являются: состояние поверхности и степень
напряжения арматуры; структура, состав бетона и толщина защитного слоя; вид
вяжущего и режим твердения бетона; различные добавки, вводимые в бетон в
качестве пластификаторов и ускорителей твердения; наличие трещин в бетоне
защитного слоя.
В трещинах с малым раскрытием скорость коррозии арматуры становится
меньше скорости коррозии незащищенной стали. Это объясняется тем, что растущий
в стесненных условиях слой ржавчины сильно уплотняется и начинает существенно
ограничивать как анодный, так и катодный процессы на поверхности арматуры в
зоне трещин. Этого не происходит при коррозии незащищенной арматуры, когда
образуется рыхлая ржавчина. В широких трещинах и при специфической
агрессивности среды это затухание коррозии может носить временный характер, так
как прочность бетона на растяжение в защитном слое может оказаться
недостаточной для восприятия растущего давления со стороны слоя ржавчины, произойдет
раскалывание и отпадение защитного слоя бетона с последующим ускорением
коррозии арматуры и распространением ее вдоль стержня. Практически такая
опасность тем меньше, чем выше прочность бетона и толще защитный слой у
арматуры.
8. СПОСОБЫ ЗАЩИТЫ ОТ КОРРОЗИИ И ПОВЫШЕНИЯ ДОЛГОВЕЧНОСТИ МЕТАЛЛИЧЕСКИХ И
ЖЕЛЕЗОБЕТОННЫХ КОНСТРУКЦИЙ
ЗАЩИТА ОТ КОРРОЗИИ МЕТАЛЛИЧЕСКИХ конструкций
Наиболее распространенными видами коррозионных повреждений в
металлических конструкциях являются: равномерное разъедание металла; местные
коррозионные поражения в виде каверн; щелевая и контактная коррозии; коррозия в
местах концентрации напряжений. Оптимальными способами защиты металлических
конструкций являются покрытия: металлизационные, металлизационные с последующей
их окраской и полимерные лакокрасочные - эпоксидные, полиуретановые,
поливинил-хлоридные, хлоркаучуковые и др.
Перед нанесением покрытий поверхность металла очищают механическим,
термическим или химическим способами. К механическим способам относятся:
очистка ручным или механизированным инструментом, обдувка абразивами -
пескоструйная и дробеструйная. Термический способ заключается в обработке
металлической поверхности пламенем ацетилено-кислородной или керосиновой
горелки. Группу химических способов очистки составляют обработки поверхности:
растворами кислот - для удаления окалины и ржавчины; растворами щелочей,
органическими растворителями - для удаления старых лакокрасочных покрытий;
преобразователями ржавчины - для обработки поверхностей с тонким слоем
продуктов коррозии; органическими растворителями - для обезжиривания
поверхности металла перед окраской.
В качестве основных материалов для нанесения металлизационных покрытий на
металлические пролетные строения мостов применяют цинк и алюминий.
Металлизационные покрытия из цинка обеспечивают надежную защиту от коррозии в
атмосфере, не загрязненной промышленными газами. В условиях с наличием газов,
содержащих сернистые соединения, хлор и углекислый газ, цинковые покрытия
неустойчивы и корродируют со скоростью 8-12 мкм/год. Покрытия из алюминия
особенно хорошо защищают сталь в атмосфере с содержанием промышленных газов.
Скорость коррозии этих покрытий не превышает 3-7 мкм/год. Для более эффективной
защиты применяют цинк-алюминиевые покрытия, которые в условиях атмосферной
коррозии отличаются более высокой стойкостью, чем цинковые или алюминиевые. Их
наносят расплавлением проволоки из сплава этих металлов, либо одновременным
распылением цинка и алюминия.
Металлизацию осуществляют сразу же после подготовки поверхности под окраску.
Допускаемый разрыв во времени между подготовкой поверхности и металлизацией
зависит от состава, воздуха, его влажности и температуры и не должен превышать
на открытом воздухе 3 часов в сухую погоду и 30 мин - в сырую.
Большая пористость металлизационных покрытий ограничивает область их
применения. Для устранения этого недостатка применяют комбинированные
металлизационно-лакокрасочные покрытия, представляющие собой сочетание двух
раздельно наносимых слоев: металлизационного, наносимого газоплазменным
напылением и лакокрасочного, наносимого по металлизационному слою кистью,
распылением или другим способом. Пористость и шероховатость металлизационного
слоя делают его эффективной грунтовкой для лакокрасочного материала. Первый
слой лакокрасочного покрытия, являющийся пропиточным, должен обладать высокой
смачивающей способностью, хорошей адгезией к напыляемому слою и быть достаточно
жидким, чтобы заполнить поры металлизационного покрытия. Лакокрасочные
материалы, наносимые в качестве последующих слоев, должны иметь обычную
вязкость.
Лакокрасочные материалы и систему покрытий выбирают в зависимости от
условий эксплуатации конструкций в различных климатических районах и степени
загрязненности атмосферы коррозионно-активными агентами. Выбранный материал и
тип покрытия должны отвечать следующим требованиям: 1) надежно защищать металл
от атмосферных воздействий в процессе эксплуатации и обеспечивать срок службы
покрытия не менее 8-10 лет; 2) создавать плотную эластичную пленку, прочно
сцепляющуюся с металлом, непроницаемую для воды и газов и не растрескивающуюся
при воздействии переменных напряжений; 3) иметь толщину не менее 100-120 мкм
при одном-двух слоях грунтовки и двух-трех слоях эмали.
Покрытие обычно состоит из грунтовки и покрывных слоев. Грунтовкой называют
первый слой лакокрасочного покрытия, наносимый на очищенную поверхность металла
с целью создания надежного противокоррозионного слоя, обеспечивающего прочность
сцепления с окрашиваемой поверхностью и с последующими слоями лакокрасочного
покрытия.
Покрывные слои лакокрасочного покрытия для обеспечения надежной защиты от
коррозии мостов должны обладать хорошей адгезией, высокой механической
прочностью и атмосферостойкостью, обеспечивать стойкость и непроницаемость всей
системы покрытия для окружающей среды в эксплуатационных условиях.
Лакокрасочные материалы следует накладывать на поверхность несколькими тонкими
слоями. Покрытие только одним слоем не может служить надежной защитой от
коррозии, поскольку имеет большое количество пор. Последующие слои покрытия
перекрывают эти поры и пленка становится более сплошной. Уменьшение количества
слоев за счет увеличения их толщины недопустимо, так как это снижает качество
покрытия, вызывает его растрескивание и образование подтеков.
Для лакокрасочных покрытий по металлу рекомендуются:
эпоксидная эмаль - биметаллическая смесь порошков цинка и алюминиевой
пудры в растворе эпоксидной смолы. Наносится по грунтовке распылением в два
слоя, жизнеспособность эмали не менее 7 часов. Покрытие повышенной
атмосферостойкости, рекомендуется для защиты от коррозии металлических
конструкций в условиях промышленной и морской атмосферы;
перхлорвиниловая эмаль - раствор поливинилхлоридной смолы в смеси летучих
органических растворителей с добавлением пластификатора и алюминиевой пудры. Покрытие
повышенной атмосферостойкости, предназначается для окраски металлоконструкций в
условиях повышенной влажности, морской атмосферы и холодного климата;
полиуретановая эмаль - суспензия пигментов в растворе полиэфира с
добавлением отвердителя. Жизнеспособность готовой к употреблению эмали не менее
8 часов. Покрытие атмосферостойко с высокой адгезией, твердостью,
морозостойкостью и стойкостью к истиранию. Предназначается для защиты от
атмосферных воздействий в условиях повышенной влажности, морской атмосферы и
холодного климата.
ЗАЩИТА ЖЕЛЕЗОБЕТОНА ОТ КОРРОЗИИ
Для защиты применяют гидрофобизирующие, лакокрасочные, оклеечные,
облицовочные и футеровочные материалы в различных сочетаниях.
Перед нанесением защитных покрытий поверхность бетонных и железобетонных
конструкций очищают от загрязнений, выравнивают при помощи ручных и
механизированных (песко- и дробеструйных) инструментов, обеспыливают. Жировые
загрязнения удаляют растворителем, солеобразования - чистой водой, продукты
взаимодействия с кислотами - 4-5%-м раствором кальцинированной соды. Затем
бетонные поверхности вновь промывают водой. Все раковины и трещины должны быть
заделаны бетоном или раствором одинакового состава с конструкцией. Влажность
поверхностного слоя бетона на глубине до 20 мм конструкции, подготовленной к
защите покрытиями, не должна превышать 5-6%.
Гидрофобизация.
Эффективным видом защиты бетона от увлажнения водой и водными растворами
является гидрофобизация его поверхности. Для этой цели применяются
кремнийорганические материалы: метилсиликонаты и этилсиликонаты натрия (ГКЖ-10
и ГКЖ-11) и обладающий наибольшим гидрофобизирующим эффектом
полиэтилгидросилоксан (ГКЖ-94).
Кремнийорганические соединения, осаждаясь на поверхности бетона, стенках
пор и капилляров, адсорбируются, а затем химически взаимодействуют с
гидроксильными группами, оксидами и гидроксидами металлов, входящих в состав
минералов цементного камня. Образуется тончайшая пленка, в которой связь
кремний-кислород ориентирована к поверхности цементного камня бетона, а органический
радикал - в противоположную сторону. Такая ориентация и создает
водоотталкивание.
Гидрофобизирующие составы получают, растворяя кремнийорганические
соединения в растворителях. Эти растворы благодаря низкой вязкости легко
проникают в бетон на глубину от 2 до 10 мм и после испарения растворителя
образуют на поверхности пор цементного камня пленку. Пропитанный
гидрофобизирующим раствором бетон приобретает свойство не впитывать воду.
Гидрофобная пленка образуется уже через 2-5 часов после нанесения, а устойчивые
водоотталкивающие свойства бетон приобретает в течение 5 суток.
Гидрофобизация поверхности железобетонных конструкций широко применяется
для защиты фасадов, наружных поверхностей ограждающих конструкций на
химкомбинатах, где солевая пыль, попадая на влажную поверхность стен, проникает
в глубь конструкции, вызывая ухудшение их теплоизоляционных свойств.
Лакокрасочные покрытия.
Они широко применяются для защиты бетона и железобетонных конструкций,
подвергающихся воздействию агрессивных газов и жидкостей. Их преимущества:
сравнительно высокая химическая стойкость, возможность нанесения на поверхности
сложных конфигураций, простота возобновления и ремонта. Недостатком
лакокрасочных покрытий является их ограниченная паро-, газо-,
водонепроницаемость и небольшой срок службы.
К материалам для покрытий предъявляются требования щелочестойкости и
малой чувствительности к наличию адсорбированной влаги на поверхности. Защитные
свойства покрытий зависят от состояния поверхности железобетонных конструкций.
Капиллярно-пористая поверхность бетона позволяет пропитать ее грунтовочными
составами на глубину 1-3 мм в зависимости от плотности бетона. Адгезия покрытия
к бетонной поверхности оптимальна при поверхностной пористости не более 5%. При
большей пористости требуется дополнительный расход материалов на грунтовку и
шпаклевку.
Лакокрасочные покрытия оптимальной толщины пропитывают поверхностный слой
бетона, уменьшают проницаемость и увеличивают омическое сопротивление бетона,
создают “пассивный” механический барьер на пути веществ, вызывающих коррозию
арматуры и бетона.
В практике коррозионной защиты наиболее эффективными являются покрытия из
полихлорвиниловых, хлоркаучуковых, эпоксидных, полиуретановых материалов, а
также материалов на основе хлорсульфированного полиэтилена. Особым видом
покрытий, используемых в качестве гидроизоляции и защиты подземных конструкций
от агрессивных производственных и высокоминерализованных природных вод,
являются лаки и эмульсии на основе нефтебитумов и каменноугольных смол.
Непроницаемость перхлорвиниловых покрытий толщиной 100-200 мкм на бетоне
наиболее высокая. При оптимальных толщинах перхлорвиниловые покрытия стойки к
действию большинства минеральных кислот и щелочей различной концентрации при t до 60° C и
нестойки к окислителям: 90%-й серной кислоте, азотной кислоте концентрации
более 50% и др. При толщине 150-200 мкм покрытия надежно защищают
железобетонные конструкции в парогазовых средах в течение 3-5 лет.
Перхлорвиниловые краски и эмали представляют собой растворы
перхлорвиниловой смолы в смеси органических растворителей с добавлением других
смол, пластификаторов и пигментов. Перхлорвиниловую смолу получают при
хлорировании поливинилхлорида. Содержание хлора в смоле достигает 65-68%, что
обеспечивает высокую стойкость материала в агрессивных средах.
На бетонную поверхность эти материалы наносят краскораспылителем или
кистью. Толщина одного слоя 20-25 мкм. В агрессивных условиях требуются
многослойные (4-5) покрытия. Время сушки каждого слоя при 18-20° C - 1-4 часа.
Хлоркаучуковые покрытия по степени проницаемости несколько уступают
перхловиниловым. При оптимальной толщине (200 мкм) они обладают высокой
химической стойкостью в кислотах и щелочах. Хлоркаучуковые лакокрасочные
материалы представляют собой суспензию пигментов и наполнителей в растворе
хлоркаучука (>50% хлора) с
добавлением пластификатора.
Для защиты бетонных и железобетонных конструкций применяют обычные и
тиксотропные эмали. Тиксотропные эмали представляют собой суспензию
соответствующих пигментов и наполнителей в растворе хлоркаучука с
пластификатором и тиксотропной добавкой. Тиксотропные добавки придают
хлоркаучуковым эмалям способность увеличивать вязкость при нанесении на
защищаемую поверхность. Преимущество высоковязких тиксотропных лакокрасочных
материалов состоит в возможности образования толстослойных покрытий толщиной в
200-250 мкм за два-три слоя.
Эпоксидные покрытия на бетоне стойки практически во всех
сильноагрессивных средах (кроме растворителей и уксусной кислоты). Оптимальная
толщина покрытия на бетоне 100-250 мкм, ориентировочный срок службы - 5 лет.
Эпоксидные лакокрасочные покрытия представляют собой раствор смол в
органических растворителях (лаки) и суспензии пигментов в эпоксидном лаке
(эмали). Отвердителя в состав вводят 3,5 г на 100 г эмали или лака.
Рулонная оклеечная изоляция.
В практике антикоррозионной защиты железобетонных конструкций от
проникания агрессивных жидкостей широко применяют оклеечную рулонную изоляцию.
В качестве материалов для такой изоляции применяют полиэтиленовую пленку,
гидроизол, бризол, изол, стеклорубероид и др. Высокая прочность, эластичность,
низкая проницаемость и практически универсальная химическая стойкость в
сочетании с трещиностойкостью при различных способах крепления к поверхности
делают полиэтиленовую пленку одним из наиболее перспективных видов химстойкой
изоляции для железобетонных конструкций.
Наиболее эффективным видом изоляции является наклеиваемая на бетон
изоляция с использованием эпоксидно-каучуковых клеев. Для такой изоляции
применяют активированную полиэтиленовую пленку толщиной 200-500 мкм.
Трещиностойкость покрытий при непластифицированном клее исчерпывается при
ширине раскрытия трещин в бетоне 0,5-0,7 мм. При наклеивании
пластифицированными клеями трещиностойкость покрытия на бетоне составляет более
2 мм и в нормальных условиях эксплуатации трещиностойкость до двух лет
практически не изменяется.
БЕТОНОПОЛИМЕРЫ
Существенным недостатком обычных бетонов является наличие разветвлённой
сети пор, капилляров, различных микродефектов, образующихся при формировании железобетонных
изделий, их твёрдении и в процессе эксплуатации. Дефекты и поры понижают
прочность бетона, а также его долговечность и стойкость к воздействию
агрессивных средств. Свойства бетона можно изменить, если поры и капилляры
заполнить другим веществом. Для этого железобетонные конструкции подвергаются
специальной обработке, которая включает сушку изделий, вакуумирование, пропитку
специальном составом и полимеризацию, если для пропитки используются мономеры.
Если необходимо только закрыть доступ внутрь бетона воде и агрессивным
жидкостям и газам, то используются материалы типа петролатума, разбавленных
смол, битума и битумов, модифицированных синтетическими смолами. Глубина
пропитки зависит в основном от вязкости пропитывающего состава. Вязкие вещества,
такие как битум или петролатум, пропитывают бетон на глубину всего 1-3 см.
Жидкие мономеры, стирол или метилметакрилат могут за короткое время пропитывать
бетон на глубину 10-20 см. Чем более глубокой является пропитка, тем больше
времени требуется на её осуществление. Количество мономера, потребное для
пропитки бетона, зависит от его пористости. Для полной пропитки плотного
бетона, требуется 2-5% мономера по массе, для раствора требуется на 30-70%
больше мономера, чем для бетона, а лёгкие пористые бетоны могут впитывать до
30-60% мономера.
При применении жидких мономеров требуется провести их полимеризацию
непосредственно в теле бетона. Полимеризация может осуществляться
термокаталитическим или радиационным способом. При термокаталитическом способе
в мономер перед использованием его для пропитки вводят специальные вещества
-инициаторы полимеризации. После пропитки бетона конструкцию нагревают до
температуры 70-1200 С и через несколько часов жидкий мономер
превращается в твёрдый полимер, плотно заполняя и заклеивая все поры и дефекты
бетона. При радиационной обработке полимеризация мономера протекает при
нормальных температурах.
В результате обработки либо достигают увеличения долговечности и
непроницаемости бетона, если его пропитывают вязкими составами без их
последующей полимеризации и упрочнения, например битумами, либо получают новые
материалы, по свойствам значительно превосходящие бетон, если его пропитывают
мономером с последующей его полимеризацией в теле бетона. Такие материалы
получили название бетонополимеров. Свойства бетонополимеров зависят как от
свойств бетона и полимеров, так и от технологии обработки. Чем прочнее полимер,
используемый для пропитки, и больше его содержание в бетонополимере, прочнее
сам пропитываемый бетон, тем выше прочность бетонополимера, которая оказывается
больше, чем прочность использованных бетона и полимера.
Определяющее значение для получения наибольшего эффекта при пропитке
имеет характер пористости бетона. Бетон должен обладать такой структурой,
которая по возможности легко пропитывается мономером и создаёт хорошие условия
для поляризации мономера. Для получения высокопрочных и особо плотных
бетонополимеров необходимо использовать в качестве пропиточных материалов такие
вещества, которые обладали бы минимальной вязкостью, хорошей адгезией в твёрдом
состоянии к составляющим бетона и полимеризовались бы доступными средствами.
Наиболее часто для пропитки используют метилметакрилат, стирол и их
производные. Для поляризации метилметакрилата термическим способом пропитанный
бетон нагревают в течение 4-6 ч. при температуре 50-800 С. При
радиационном способе полимеризации изделия из пропитанного бетона подвергают
облучению в течение 4-10 ч. Полимеризацию стирола в бетоне также можно
осуществлять как термическим, так и радиационным способом. В первом случае
пропитанное изделие прогревают по ступенчатому режиму в присутствии инициаторов
полимеризации: сначала при температуре 80-900 С, а затем при
температуре 100-1200 С
Пропитка бетона мономером с его последующей полимеризацией в теле бетона
приводит к резкому увеличению прочности и улучшению других свойств бетона.
Прочность бетонополимера при сжатии по сравнению с исходным контрольным бетоном
повышается в 2-10 раз и может достичь 200 МПа, а прочность при растяжении
увеличивается в 3-10 раз, достигая 18 МПа. Практически при полной пропитке
бетонополимеры являются водо- и газонепроницаемыми материалами. Непроницаемость
материала резко повышает его долговечность и морозостойкость. Если исходный
бетон выдерживает 300-400 циклов замораживания, то бетонополимер не имеет
разрушений и после 5000 циклов. Значительно возрастает стойкость бетона в
щелочах, сульфатах, соляной кислоте и других агрессивных средах.
ПОЛИМЕРБЕТОНЫ
Полимербетонами называют бетоны, в которых вяжущими служат различные
полимерные смолы, а заполнителями являются неорганические материалы: песок и
щебень. Для ускорения твердения, улучшения свойств синтетических смол применяют
отвердители, пластификаторы и другие добавки.
Наиболее часто для полимербетонов используются термореактивные смолы:
фурановые, эпоксидные и полиэфирные. Фурановые смолы являются наиболее дешевым
полимерным вяжущим. В строительстве наибольшее распространение получил мономер
ФА, получаемый при взаимодействии фурфурола и ацетона в щелочной среде. Отверждение
мономера ФА происходит в присутствии катализатора - бензосульфокислоты,
оптимальное количество которой составляет 20-30% от массы ФА.
Эпоксидные смолы - это полимерные вещества линейного строения, содержащие
эпоксигруппу. Для полимербетонов наиболее пригодны жидкие эпоксидные смолы ЭД-5
и ЭД-6. Для холодного отверждения эпоксидных смол применяют полиэтиленполиамин
(10-12% от массы смолы), а также высокомолекулярные вещества - полиамиды,
полиэфиры и др. Для улучшения деформативной способности в смолу вводят
пластификаторы - дибутилфталат в количестве 15-20% от массы смолы.
Для полимербетонов на фурановых и формальдегидных смолах применяют
заполнители, стойкие в кислой среде, так как для их полимеризации используют
кислые отвердители. Использование известняков, доломитов, цементов и др.,
имеющих щелочную реакцию, недопустимо, так как это приводит к резкому снижению
прочности бетона. Для полимербетонов на полиэфирных и эпоксидных смолах можно
применять самые различные заполнители, в том числе карбонатные породы, асбест и
др.
Свойства полимербетонов зависят от вида смолы, состава бетона и
технологии его получения. В зависимости от вида полимерного связующего и
соответствующего ему отвердителя полимербетоны делятся на классы: фурановые,
фенолоформальдегидные, полиэфирные, эпоксидные. Полимербетоны отличаются от
цементного бетона высокой прочностью, в особенности при растяжении (7-20МПа) и
изгибе (16-40 МПа), и химической стойкостью.
Фурановый полимербетон относится к самым стойким полимерным материалам.
Он стабильно сохраняет свои свойства в растворах серной и соляной кислоты,
хлоридов, щелочей, а также жирах, маслах и нефтепродуктах. Слабо сопротивляется
действию окислителей (азотная, уксусная кислота) и некоторых растворителей
(ацетон, бензол, спирт).
Фенолоальдегидный полимербетон достаточно стоек к действию кислот, кроме
окисляющих, растворителей, масел и нефтепродуктов. Полиэфирный полимербетон
характеризуется повышенной стойкостью к окислителям. В то же время
сложноэфирные связи в структуре полиэфира снижают стойкость полимербетона к
щелочам и солям, имеющим основную реакцию, а также к воде. Степень снижения
прочности полиэфирного полимербетона в воде не меньше, чем в растворах кислот и
солей.
Химическая стойкость эпоксидных связующих зависит от характера
отвердителя и вида, образующихся при твердении межмолекулярных связей.
Отвержденные ароматическими полиаминами эпоксидные полимербетоны особо
устойчивы к кислотам (соляной, хромовой, уксусной). Повышенной стойкостью к
воде, щелочам и окислительным средам обладают эпоксидно-полиамидные составы.
На стойкость полимербетонов существенное влияние оказывают наполнители,
которые сами должны обладать достаточной химической стойкостью в конкретных
агрессивных средах. Плотность структуры бетона как первое условие химической
стойкости подтверждается также количественным влиянием наполнителей на
стойкость. Любые мероприятия, повышающие водостойкость полимербетона,
обеспечивают одновременно и повышение его химической стойкости.
Способы создания плотной структуры полимербетонов обеспечивают повышение
не только водостойкости, но и морозостойкости. Разработаны составы тяжелых
полимербетонов плотностью 2200-2400 кг/м3, имеющих предел прочности
на сжатие: на основе фенолоформальдегидных смол 40-60 МПа, карбамидных - 50-80МПа,
полиэфирных - 80-120 МПа, фураново-эпоксидных - до 160МПа.
При этом водопоглощение полимербетона за 24 часа составляет не более
0,3%, морозостойкость от 300-500 циклов. Механические свойства полимербетонов
повышаются при армировании их стальной или стеклопластиковой арматурой, а также
при использовании волокнистых наполнителей - асбеста, стекловолокна и др.
Полимербетоны и армополимербетоны находят широкое применение в
транспортном строительстве. Из них изготавливают опоры контактной сети,
используют для омоноличивания опор моста, заполнения деформационных швов,
инъецирования арматурных каналов мостовых конструкций, устройства покрытий
проезжей части. Многолетняя эксплуатация сталеполимербетонных шпал показала
высокую их надежность в условиях интенсивного движения вагонов, периодического
воздействия масел, минеральных удобрений и других реагентов.
9. ДОЛГОВЕЧНОСТЬ АСФАЛЬТОБЕТОНА
Асфальтобетон - это материал, полученный в результате уплотнения
специально рассчитанной и приготовленной при соответствующей температуре смеси
щебня, песка, минерального порошка и битума. По степени насыщения
асфальтобетона основными структурообразующими компонентами в нем различают
базальную, поровую и контактную структуру.
В асфальтобетоне с базальной структурой зерна крупного компонента не
имеют взаимных контактов и как бы погружены в растворную часть. Дальнейшее
насыщение асфальтобетона структурообразующими компонентами приводит к
контактированию зерен через тонкие прослойки вяжущего, формируется поровая
структура, при которой образуется плотный каркас из зерен, способный
воспринимать значительные внешние усилия. В этом случае объем асфальтобетонного
раствора соответствует объему пустот в щебеночном каркасе. Дальнейшее
увеличение содержания щебня приводит к образованию контактной структуры, в
которой объем пустот в щебеночном остове превышает объем асфальтового раствора.
Асфальтобетон, обладающий обратимыми микроструктурными связями, в
зависимости от температуры может находиться в следующих структурных состояниях:
упруго-хрупком, при котором минеральный остов асфальтобетона строго фиксирован
застеклованными прослойками битума; упруго-пластичном, когда зерна минерального
остова соединены между собой прослойками битума, которые проявляют при
напряжениях не превышающих предел текучести, упругие и эластичные свойства, а
при больших напряжениях - упруго-вязкие свойства; вязко-пластичном, при котором
зерна минерального остова соединены полужидкими прослойками битума.
Кроме температурных факторов, асфальтобетон подвергается воздействию
атмосферных и талых вод, вода проникает в поры асфальтобетона и ослабляет
взаимную связь минеральных материалов с пленкой вяжущего. Поэтому оценку
прочности асфальтобетона дают по результатам испытаний цилиндрических образцов
на сжатие при температурах +50, +20 и 00 С. Если при температурах
+500 С ограничивается нижний предел прочности (1,0-1,2 МПа), то при
температуре 00 С ограничивается верхний предел прочности (не более
12 МПа). Показатель прочности при +500 С характеризует
сдвигоустойчивость асфальтобетона при высокой температуре и сопротивляемость
материала образованию пластических деформаций в покрытии. Показатель прочности
при 00 С косвенно характеризует трещиностойкость асфальтобетона при
низкой температуре.
Водостойкость и морозостойкость. Асфальтобетонные покрытия при длительном
увлажнении вследствие ослабления структурных связей могут разрушаться за счет
выкрашивания минеральных зерен, что приводит к повышенному износу покрытия и
образованию выбоин. Водостойкость асфальтобетона зависит от его плотности и
устойчивости адгезионных связей. Вода как полярная жидкость хорошо смачивает
все минеральные материалы и потому при длительном увлажнении возможна диффузия
воды под битумную пленку. При этом минеральные материалы с положительным
потенциалом заряда поверхности (доломит, известняк, кальцит) в большей степени
препятствуют вытеснению битумной пленки водой, чем материалы с отрицательным
потенциалом поверхности (кварц, гранит, андезит).
Вода, проникая в микродефекты структуры асфальтобетона, приводит к адсорбционному
понижению прочности материала за счет снижения поверхностной энергии стенок
трещин и ослабления структурных связей у вершины трещины по мере ее развития.
Закономерное снижение прочности асфальтобетона с увеличением срока выдерживания
его в воде объясняется постепенной диффузией воды внутрь материала и все
увеличивающимся расклинивающим действием воды. Значительно разрушает структуру
асфальтобетона его частое попеременное увлажнение и высыхание. Большое влияние
на водостойкость асфальтобетона оказывает его пористость, которая составляет
3-7%. С уменьшением размера зерен в асфальтобетоне увеличивается количество
замкнутых недоступных воде пор. Так, в крупнозернистом бетоне практически все
поры открыты, а в мелкозернистом открытые поры составляют 30-40%. Водостойкость
определяется величиной водонасыщения, набухания и коэффициентом водостойкости
(отношение прочности водонасыщенных образцов к прочности сухих). Коэффициент
водостойкости должен быть не меньше 0,9, а при длительном водонасыщении (14 сут.)
не менее 0,8.
Морозостойкость асфальтобетона связана в основном с количеством открытых
пор и характером взаимодействия между битумом и минеральным материалом.
Наиболее разрушительное действие оказывает происходящее весной и осенью
попеременное замораживание и оттаивание асфальтобетона. Знакопеременные
температуры приводят к возникновению трещин, развивающихся при многократных
циклах замораживания и размораживания.
Морозостойкость асфальтобетона обычно оценивается коэффициентом
морозостойкости Км, показывающим снижение прочности при растяжении
после определенного количества циклов замораживания и размораживания.
Морозостойкость асфальтобетона на гранитном материале значительно ниже, чем на
известняковом. Это объясняется тем, что природа сил связи битум-гранит
физическая, в то время как связь битум-известняк физико-химическая. Напряжения,
возникающие при замерзании воды, легко разрушают физические связи и не в
состоянии разрушить химические.
Износостойкость. Износ асфальтового покрытия происходит под действием сил
трения, вызываемых проскальзыванием колес автомобилей по поверхности покрытия и
вакуумных сил, возникающих под движущимся автомобилем. Износ покрытия
определяется: истиранием его структурных элементов, отрывом и уносом с его
поверхности зерен песка и раздробленных частиц щебня. Износостойкость
асфальтобетона тем выше, чем больше его плотность, чем выше твердость входящих
в его состав минеральных материалов и выше сцепление зерен щебня и песка с
битумом. Асфальтобетоны, приготовленные на гранитном щебне, более
износоустойчивы, чем бетоны на известняковом щебне. Высокую износоустойчивость
имеют асфальтобетоны, в состав которых входит щебень с наименьшей дробимостью
при укатке. Истираемость асфальтобетонного покрытия при интенсивном
автомобильном движении составляет 0,3-1,0 мм в год.
10. ДОЛГОВЕЧНОСТЬ ДРЕВЕСИНЫ И СПОСОБЫ ЗАЩИТЫ ЕЕ ОТ ГНИЕНИЯ И ВОЗГОРАНИЯ
Агрессивное воздействие на деревянные конструкции оказывают биологические
агенты - дереворазрушающие грибы, вызывая биологическую коррозию древесины, а
также агрессивные химические среды (газообразные, твердые, жидкие), вызывая
химическую коррозию древесины.
В сухих условиях и при надлежащем проветривании древесина сохраняется
долго. Столь же долговечна древесина, постоянно находящаяся в воде без доступа
воздуха. Однако попеременное увлажнение и высыхание деревянных элементов
создает благоприятную среду для гниения древесины. Так, в соответствии со СНиП
2.03.11-85 степень агрессивного воздействия биологических агентов на древесину
столбов, свай, конструкций береговых опор, элементов мостов в условиях
увлажнения атмосферными осадками следует принимать как средне агрессивную, а в
условиях контакта указанных конструкций с грунтом и в зоне переменного уровня
воды - как сильно агрессивную.
Стенки клеток, из которых сложена древесина, состоят из мицелл, т.е.
кристалликов целлюлозы микроскопических размеров, окруженных гидратными
оболочками. Гниение - это процесс разложения целлюлозы древесины, происходящий
вследствие деятельности дереворазрушающих грибов и микроорганизмов. Питательной
средой для грибов служит растворимый сахар (глюкоза), являющийся продуктом
разлагаемой ими целлюлозы. При содействии фермента, выделяемого грибом,
нерастворимая в воде целлюлоза гидратируется и переходит в растворимое вещество
- глюкозу. В теле гриба глюкоза окисляется кислородом воздуха, образуя
углекислый газ и воду. Следовательно, для жизнедеятельности гриба необходимы
влага и кислород воздуха. Вот почему легко загнивает древесина, находящаяся в
условиях переменной влажности. Споры различных грибов почти всегда имеются на
дереве, оставаясь пассивными до тех пор, пока не наступят благоприятные
условия. При достаточной влажности (более 18-20%) и положительной температуре
споры прорастают и появляется грибница, сначала в виде ватообразного, а затем в
виде плотного тела на поверхности материала.
Степень воздействия химически агрессивных газообразных и твердых сред на
конструкции из древесины зависит от состава среды и влажностного режима
помещений. С точки зрения химической коррозии, по данным СНиП 2.03.11-85
речная, озерная и морская вода, нефть и нефтепродукты, масла минеральные,
растительные и животные являются неагрессивными при воздействии на древесину.
Растворы кислот и щелочей, в зависимости от их концентраций, по степени агрессивного
воздействия на древесину могут оцениваться как слабо -, средне - или
сильноагрессивная жидкая среда. Для деревянных конструкций, предназначенных к
эксплуатации в химических средах средней и сильной степени агрессивного
воздействия, необходимо предусмотреть следующие дополнительные требования:
для изготовления конструкции следует применять древесину хвойных пород
(сосна, ель и др.);
склеивание элементов конструкций должно осуществляться фенольными,
резорциновыми, фенольно-резорциновыми клеями;
несущие конструкции следует проектировать из элементов сплошного сечения
(клееных, брусчатых).
При проектировании деревянных конструкций для эксплуатации в химических
средах средней и сильной степени агрессивности действие биологических агентов
не учитывается
Защита древесины от гниения. Основным способом борьбы с гниением является
химический способ - введение в древесину антисептиков - веществ, ядовитых для
грибов. Антисептики, обладая токсичностью по отношению к грибам, должны быть
безвредными для людей и животных, не должны понижать прочность древесины и не
вызывать коррозию металлических креплений. Для воздушных условий эксплуатации
обычно применяют антисептики, растворимые в воде. Антисептирование деревянных
элементов, подвергающихся действию воды (шпалы, столбы, сваи и т.д.),
осуществляют нерастворяющимися маслянистыми веществами.
К группе водорастворимых антисептиков относятся: фтористый натрий (Na F) в водном растворе концентрацией 2-3%, обладает высокой
токсичностью к грибам и насекомым, а при соединении с известью, цементом
переходит в нерастворимый фтористый кальций и теряет свою токсичность;
кремнефтористый натрий (Naz SiF6)применяют совместно с фтористым
натрием в виде водного раствора; хлористый цинк (Zn Cl2) применяют в водном растворе 5%- й концентрации, т.к.
вызывает коррозию металла; медный купорос (СuSO4*5H2O) используют в виде 10%-го водного
раствора.
Маслянистые антисептики не растворяются в воде, поэтому их используют для
консервации древесины, находящейся на открытом воздухе, в воде или земле.
Токсичность антисептиков этой группы обусловливается наличием в них фенола и
его производных. К ним относятся: антраценовое масло - продукт перегонки
каменноугольного дегтя (при 270-4100С), сильно токсичен, с резким
запахом; каменноугольное креозотовое масло получают при дистилляции
каменноугольного дёгтя (при 250-2800С), применяют в подогретом
состоянии, сильное антисептирующее действие, является лучшим антисептиком для
шпал, столбов, мостов; сланцевое масло применяется наряду с антраценовым.
Древесина, пропитанная маслянистым антисептиком, приобретает тёмный цвет, имеет
фенольный запах, не поддается окраске и увеличивает горючесть.
Антисептические пасты состоят из трёх частей: водорастворимого
антисептика, связующего вещества, обеспечивающего прилипание пасты к
поверхности древесины и наполнителя - торфяного порошка. Битумную пасту готовят
путём добавления в расплавленный битум зелёного масла в качестве растворителя, NaF и торфяного порошка (5-10%).
Силикатную пасту готовят из кремнефтористого натрия (15-20%), жидкого стекла
(~75%), воды и добавки каменноугольного масла для придания отвердевшей пасте
эластичности.
Способы антисептирования древесины - поверхностная обработка, пропитка в
горячехолодных ваннах, пропитка в высокотемпературной ванне и пропитка под
давлением - применяют в зависимости от типа и условий службы конструкций.
Защита древесины от возгорания. Температура воспламенения древесины,
соответствующая вспышке горючих газов, колеблется в пределах от 250 до 3000С
в зависимости от породы дерева. Горят продукты термической деструкции
древесины, образующиеся при нагревании её после удаления влаги, начиная с
температуры 1700С. Интенсивное же выделение горючих газов происходит
при 2800С. При температуре выше 3500С газы, выделяющиеся
из древесины, воспламеняются даже при отсутствии открытого пламени.
Для предохранения от огня поверхность деревянных конструкций покрывают
огнезащитными красочными составами или пропитывают антипиренами.Огнезащитное
действие краски проявляется в том, что при пожаре краска пузырится,
образующийся пористый слой замедляет нагревание древесины. Если же горючие газы
все же образуются и прорывают красочное покрытие, то их воспламенение
происходит на некотором удалении от поверхности деревянного элемента.
Защитное
действие антипиренов основано на том, что некоторые из них при пожаре плавятся
и древесина покрывается пленкой, затрудняющей доступ кислорода. Другие
антипирены выделяют при нагревании негорючие газы, снижающие концентрацию
кислорода в газовой среде вокруг конструкции. Антипиренами являются
фосфорнокислые и сернокислые соли аммония. Сернокислый аммоний при нагревании
диссоциирует и образовавшаяся сильная кислота дегидратирует слой древесины,
который защищает внутреннюю необугленную древесину от сильного нагрева. Бура -
борнонатриевая соль 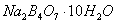 при нагревании выделяет пары воды и плавится, образуя
пленку на поверхности древесины. Растворы антипиренов применяют для
поверхностной обработки и пропитки древесины, используют для повышения
огнестойкости древесины.
при нагревании выделяет пары воды и плавится, образуя
пленку на поверхности древесины. Растворы антипиренов применяют для
поверхностной обработки и пропитки древесины, используют для повышения
огнестойкости древесины.
11. ХИМИЧЕСКАЯ СТОЙКОСТЬ ПОЛИМЕРНЫХ МАТЕРИАЛОВ
Пластичными массами называют большую группу материалов, основой которых
являются природные или искусственные высокомолекулярные соединения - вещества с
молекулами, состоящими из сотен или тысяч атомов, соединенных между собой
валентными связями.
Одной из особенностей пластических масс является их способность в
процессе переработки легко переходить в вязкотекучее состояние и под действием
внешних сил принимать заданную форму, устойчиво сохраняя ее.
Отличительным свойством многих пластмасс, особенно армированных
стекловолокном, является их высокая прочность при изгибе и растяжении.
Пластмассы хорошо сцепляются с металлом, бетоном, стеклом и деревом, что
определяет высокую эффективность при применении их в качестве клеев, красочных
покрытий, облицовок и слоистых пластиков.
Используемые в промышленности и строительстве смолы и пластмассы на их
основе подразделяют по способу получения на полимеризационные и
поликонденсационные, а по отношению к нагреванию - на термопластичные или
термопласты и термореактивные или реактопласты. В отдельную группу выделяют
полимерные материалы, обладающие высокой эластичностью - эластомеры.
ВИДЫ, ОСНОВНЫЕ СВОЙСТВА И ХИМИЧЕСКАЯ СТОЙКОСТЬ ТЕРМОПЛАСТОВ
Термопластичными называются смолы, способные при нагревании размягчаться,
а затем и плавиться и при последующем охлаждении снова затвердевать. Это
свойство термопластов обусловлено линейным строением их макромолекул,
представляющих собой цепочки, состоящие из отдельных звеньев с гибкими связями.
К термопластам относятся полиэтилен, поливинилхлорид, полистирол, полиметилметакрилат,
фторопласты, поливинилацетат, полиамидные смолы и др.
Полиэтилен. Он имеет прочность на растяжение около 14,0МПа, обладает
высокой химической стойкостью и диэлектрическими свойствами, эластичностью,
способностью образовывать прочные водо-, паро- и газонепроницаемые пленки.
Легко сваривается и перерабатывается в изделия.
К недостаткам, ограничивающим область применения полиэтилена, можно
отнести подверженность старению под действием кислорода воздуха и
ультрафиолетовых лучей, низкую теплостойкость, повышенную хрупкость при низких
температурах (ниже -200 С), горючесть и малую твердость. Полиэтилен
применяют для создания защитных слоев методами центробежного, газопламенного
или вихревого напыления. Из него изготовляют пленки, ленты и химически стойкие
трубы.
Поливинилхлорид. Имеет прочность на растяжение в пределах 40,0-50,0 МПа
(жесткий не пластифицированный), обладает высокой стойкостью в кислых и
щелочных средах, нерастворим в спиртах и маслах, трудно воспламеняется, хорошо
формуется в нагретом состоянии, легко сваривается и склеивается, хорошо
совмещается с наполнителями, что позволяет получать пластмассы с разнообразными
физико-механическими свойствами.
К недостаткам его следует отнести низкую теплостойкость при нагреве свыше
500 С, хрупкость при отрицательных температурах (ниже -200
С), слабую адгезию к некоторым материалам и способность растворяться в эфирах.
Из пластифицированного эластичного поливинилхлорида изготовляют пленки, а из
непластифицированного жесткого (винилпласта) - трубы, погонажные изделия.
Полистирол. Характеризуется прочностью на растяжение до 40,0 МПа,
теплостойкостью до 700 С, практически полной водостойкостью и
высокой химической стойкостью в кислых и щелочных средах. Он бесцветен и
прозрачен (пропускает до 90% лучей видимой части спектра ), имеет большое
электрическое сопротивление, высокую морозостойкость, хорошо сваривается при
нагреве до температур 220-2500 С, хорошо склеивается и также
подвергается механической обработке (сверлению, пилке и т.д.).
Недостатком его является повышенная хрупкость даже при комнатных
температурах, низкая теплостойкость, повышенная в сравнении с другими
полимерами подверженность старению (под действием солнечного света полистирол
темнеет и растрескивается), плохая адгезия к другим материалам. Путём прессования
или литья под давлением из него изготовляют облицовочные плитки.
Органическое стекло (полиметилметакрилат) отличается высокой прочностью
на растяжение (до 70,0 МПа2) высокой стойкостью к действию воды, а
также кислых и щелочных сред, постоянством свойств при изменении температуры в
пределах от -180 до +60 0С, прозрачностью, бесцветностью,
способностью пропускать ультрафиолетовые лучи, хорошей формуемостью в нагретом
состоянии.
Недостатком полиметилметакрилата является малая твёрдость и повышенная
хрупкость. Используют органическое стекло для изготовления стойких
светопрозрачных ограждений и как связующее в акрилатных лаках.
Фторопласты имеют прочность при растяжении в пределах 17,0-40,0 МПа,
высокую химическую стойкость, теплостойкость и диэлектрические свойства.
Фторопласт-4 (тетрафторэтилен) обладает универсальной химической
стойкостью - хорошо противостоит действию царской водки (смеси 1 ч азотной
кислоты с 3 ч соляной) при температуре 100 0С, концентрированной
серной кислоты, растворов щелочей, значительной термостойкостью (от 90 до 250 0С),
постоянством физико-механических свойств в интервале температур от -60 до +200 0С.
Однако применение тетрафторэтилена в строительстве ограничивается его высокой
стоимостью и трудной обрабатываемостью в изделия (из-за большой вязкости в
расплавленном состоянии).
Фторопласт-3 (трифторэтилен) характеризуется пониженной в сравнении с
тетрафторэтиленом химической стойкостью и термостойкостью (от 600 до
1500 С). Фторопласты применяют в виде пластин, междуслойной изоляции
и труб для транспортирования сильно агрессивных жидкостей, а также в виде
пленок для защиты стальных труб от коррозии.
Поливинилацетат обладает способностью образовывать эластичные
светостойкие бесцветные пленки, высокой адгезией к ряду материалов. Однако
невысокая водостойкость, низкая морозо- и теплостойкость ограничивают области
его применения в строительстве. Используется главным образом в производстве
лаков, в виде эмульсий он пригоден для изготовления мастичных полов.
Полиизобутилен характеризуется высокой водостойкостью, повышенной
газонепроницаемостью и высокой стойкостью к действию соляной, серной,
фосфорной, уксусной и других минеральных кислот, концентрированных едких
щелочей и других агрессивных сред. В строительстве применяется как весьма
стойкий антикоррозийный материал в виде футеровочных листов и защитных пленок.
Кроме того, он используется для уплотнения стыков в крупнопанельном
домостроении. Таким образом, рассмотрев отдельные виды термопластичных
полимеров, можно выявить основные общие для них физико-механические свойства.
Это прежде всего небольшая плотность (ρ = 1-2 г/см3), высокая прочность
при растяжении и сжатии, низкая теплопроводность, хорошие диэлектрические
свойства, малое водопоглощение, достаточная морозостойкость, высокая водо - и
химостойкость.
Общими для большинства термопластичных смол недостатками являются: низкая
теплостойкость, низкий модуль упругости, повышенная хрупкость при понижении
температуры (ниже -200 С), большая ползучесть при сравнительно
низких уровнях начальных напряжений, склонность к старению.
ВИДЫ, ОСНОВНЫЕ СВОЙСТВА И ХИМИЧЕСКАЯ СТОЙКОСТЬ РЕАКТОПЛАСТОВ
В основном термореактивными свойствами обладают смолы, получаемые
поликонденсацией (фенольные, фурановые, эпоксидные, полиэфирные), в результате
которой образуются макромолекулы полимера сетчатой структуры с прочными
химическими связями в поперечном направлении.
При образовании такой сетчатой структуры физико-механические свойства
термореактивных смол в сравнении с термопластами существенно изменяются, они
теряют способность растворяться в растворителях и переходить при повторном
нагревании в пластическое состояние (размягчаться). Термореактивные смолы
характеризуются большей прочностью, твердостью, хрупкостью, теплостойкостью и
значительно меньшими деформациями ползучести под действием постоянной нагрузки.
Фенолоформальдегидные смолы в твердом состоянии представляют собой
хрупкие стеклообразные массы янтарного цвета с высокой поверхностной
твердостью. Они способны хорошо совмещаться с наполнителями, что позволяет
получать пластмассы более прочные и теплостойкие и менее хрупкие, чем сами
смолы; характеризуются высокой адгезией и химической стойкостью, особенно в
кислых средах. Пластмассы на основе фенолоформальдегидных смол называют
фенопластами.
Они хорошо сопротивляются действию неомыляющих кислот, бензина и
органических растворителей даже при высоких температурах (до 1200
С), а при обычных температурах (до 250 С) выдерживают действия
сухого хлора и ряда окисляющих кислот (азотной 5%-й, серной 70%-й, хромовой
10%-й концентрации). Однако фенопласты могут разрушаться щелочами и основными
солями.
Мочевиноформальдегидные (карбамидные) смолы характеризуются отсутствием
запаха и цвета, светостойкостью, способностью окрашиваться в различные цвета
при введении в их состав красителей. Стоимость их ниже стоимости
фенолоформальдегидных смол, однако в сравнении с последними они менее
водостойки, имеют меньшую химическую стойкость и повышенную хрупкость.
Фурановая смола (смола ФА) является наиболее химически стойкой и
теплостойкой, хорошо совмещается с фенольными и эпоксидными смолами, обладает
достаточной прочностью и высокой адгезией к керамике, металлу и цементному
бетону. Недостатками наполненных и ненаполненных фурановых смол являются
высокая хрупкость, черный цвет, значительная деформативность (усадка,
ползучесть, температурные деформации), токсичность при нанесении.
Фурановая смола хорошо выдерживает при температурах до 1200 С
действие неокисляющих кислот, щелочей, солей, бензина и органических
растворителей, а также сернистого газа. Действие сухого хлора и 5%-й раствора
окисляющих кислот (азотной, хлорной и т. д.) она удовлетворительно выдерживает
только при обычных температурах (до 250 С). Влажный хлор и
концентрированные растворы окисляющих кислот разрушают фурановую смолу.
Эпоксидные смолы обладают высокой прочностью в затвердевшем состоянии,
исключительно высокой адгезией к металлу, бетону, древесине, керамике, стеклу и
т. д., хорошо совмещаются со многими синтетическими смолами и после отвердения
характеризуются высокой химической стойкостью и относительно высокой
теплостойкостью (100-1500 С). Недостатками эпоксидных смол являются
их высокая стоимость до отверждения, а также низкая деформативность и невысокая
ударная вязкость.
По химической стойкости эпоксидные смолы уступают только изделиям из
фенольных и фурановых смол, выдерживая воздействия любых агрессивных сред, за
исключением сильных окислителей и влажного хлора.
Полиэфирные смолы в ненасыщенном состоянии образуют высокопрочные,
плотные и стойкие, светлые и цветные гладкие покрытия, не выделяющие летучих
веществ, но дающие большую усадку в процессе отверждения. Полиэфиры могут
применяться при температурах от -600 до +1000 С. В
строительстве из полиэфиров используют в основном глифталевые смолы, которые
характеризуются повышенной хрупкостью и низкой атмосферостойкостью. При
длительном воздействии воды прочность полиэфирного полимера понижается (до
40%), уменьшается и его адгезионная способность.
Полиэфирные смолы являются стойкими к большинству кислот любой
концентрации до температуры 800,за исключением сильно окисляющих,
муравьиной, уксусной и некоторых других; они ограниченно стойки к сухим
щелочам, некоторым солям (углекислый калий, сернистый натрий) и растворителям
(ацетон, анилин и др.). Даже при высоких температурах полиэфирные смолы стойки
к различным сульфатам и хлоридам, а также к действию спиртов, хлора, нефти,
бензина, масел, ртути и многих других веществ. Активным агрессором по отношению
к полиэфирным смолам является вода.
Кремнийорганические смолы, или силиконы - это материалы, в которых
совмещаются достоинства неорганических и органических веществ. Они отличаются
высокой теплостойкостью (до 5000 С) и вместе с тем
водоотталкивающими свойствами, хорошей адгезией к бетону, металлу, стойкостью к
химическим реагентам, диэлектрическими свойствами и высокой прочностью при
сжатии и изгибе.
Силиконовые смолы характеризуются стойкостью в атмосферных условиях,
условиях тропического климата, действия агрессивных газовых сред и значительной
гидрофобностью.
Существенное влияние на свойства и стойкость реактопластов, так же как и
других видов пластмасс, оказывает введение в их состав различных наполнителей.
При введение наполнителей в смолу, как правило, увеличивается прочность
изделий при одновременном снижении их хрупкости (усадки, ползучести).
Теплостойкость и морозостойкость наполненных смол выше, чем ненаполненных, но
разные температурные перепады могут разрушающе действовать на структуру системы
смола - наполнители.
Водостойкость наполненных пластмасс обычно несколько ниже, чем чистых
смол. Кислото - или щелочестойкость наполненных смол, стойкость в органических
растворителях определяются преимущественно видом и стойкостью самих смол, но
также зависят и от стойкости наполнителя.
В качестве наполнителей используют дешевые и доступные материалы:
для щелочных и нейтральных сред - карбонаты, цементы;
для кислых сред - кремнеземистые и алюмосиликатные породы - кварц,
андезит, гранит, асбест и т.д.;
для переменных сред использования - древесная мука, шерсть, уголь, кокс,
графит, сажа.
СТАРЕНИЕ И КОРРОЗИЯ ПОЛИМЕРОВ
При применении полимерных материалов необходимо учитывать возможность их
старения, ограничивающего срок надежной эксплуатации защитных покрытий.
Старением называют самопроизвольное изменение технических свойств пластмассы
(прочности, упругости), происходящее в эксплуатационных условиях. В результате
старения повышается хрупкость, снижается сопротивление удару.
Распад или деструкция полимерных материалов происходит иногда в короткие
сроки при нормальной температуре и приводит к полному разрушению. Так например,
пленки полиэтилена, высокостойкие к действию воды, щелочей и многих кислот,
полностью разрушаются от действия воздуха и солнечных лучей в течение 1-2 лет.
Наиболее агрессивными физико-химическими факторами, вызывающими
деструкцию, является тепло, свет, вода, кислород, озон и сочетание этих
факторов. Несмотря на сложность и разнообразие механизма старения
(окислительная, фотохимическая, термическая, радиационная деструкция), общими
признаками деструкции полимеров является снижение молекулярного веса и
выделение летучих продуктов. Таким образом, старение можно рассматривать как
процесс разрыва связи между цепями и внутри цепей, то есть как деполимеризацию
полимера и его распад вплоть до мономера. Для замедления старения в состав
пластмассы вводят стабилизаторы (антистарители). Введение, например, в состав
полиэтилена тонкодисперсной сажи повышает срок его службы в атмосферных
условиях в несколько раз. Наименее стойки в отношении старения полимеры, в молекулах
которых имеются двойные связи (например каучуки).
В большинстве случаев процессы старения протекают на поверхности
полимеров, там, где происходит поглощение света, кислорода или озона. Поэтому
весьма целесообразно применять такие конструкции, где бы полимер был укрыт от
света и окисления.
Однако изделия из полимерных материалов при хранении и в процессе
эксплуатации, взаимодействуя с внешней средой, подвергаются не только процессу
старения, но и воздействию агрессивных жидкостей и газов, вследствие чего
ухудшаются рабочие свойства полимеров.
Агрессивные среды в зависимости от характера взаимодействия с полимерами
целесообразно разделить на две группы - физически и химически активные. Хотя
результаты воздействия сред обеих групп на полимеры могут быть одинаковы
(изменение жесткости, растрескивание или полное разрушение), закономерности,
определяющие такие практически важные характеристики, как скорость диффузии и
проницаемость, изменение прочности и долговечности, массы и объема,
сопротивляемость многократным деформациям и истиранию, зависят от характера
среды.
Физически агрессивные среды вызывают обратимые изменения полимера, не
сопровождающиеся разрушением химических связей (например, набухание,
растворение). К таким средам относятся обычно химически инертные углеводороды и
некоторые их производные, используемые в качестве растворителей, масел, топлив
и т. д.
Например, полистирол не стоек к бензолу и ксилолу; поливинилхлорид стоек
к этиловому и метиловому спирту, воде, но значительно набухает или растворяется
в толуоле, бензоле, ацетоне; полиамиды хорошо противостоят действию бензола и
эфиров; полиэтилен высокой плотности значительно более стоек к действию мыл,
спиртов и масел, чем полиэтилен низкой плотности.
Наличие пространственных связей, образующих структуру термореактивных
полимеров, не дает возможности макромолекулам переходить в раствор, то есть
полимер теряет способность растворяться в физически агрессивных средах. В этом
случае он может только набухать.
Вода и водные растворы также могут действовать на полимеры, как физически
агрессивная среда. Скорость диффузии воды в неполярные полимеры (полиэтилен,
полиизобутилен, полистирол) очень мала, поэтому они характеризуются высокой
водостойкостью. В полимерах, содержащих полярные группы (поливинилхлорид,
поливинилацетат), скорость диффузии воды выше, а следовательно, водостойкость
их несколько меньше. По отношению к полиэфирным и некоторым другим
поликонденсационным смолам вода является активным агрессором.
Химически агрессивные среды в отличие от физически агрессивных вызывают
необратимые изменения, сопровождающиеся изменением химической структуры
полимера. Учитывая разнообразие химически агрессивных сред, целесообразно
рассмотреть практически наиболее важные случаи взаимодействия с полимерами таких
сред, как сильные окислители (перекись водорода, азотная кислота), минеральные
кислоты (серная, соляная и др.), галогены (фтор, хлор), щелочи и водные
растворы солей.
Сильные окислительные среды - хромовая, концентрированная азотная и
серная кислота, перекись водорода и т. п. вызывают быстрое (в течение
нескольких минут) разрушение полиамидов, полиэфиров, полиуретанов,
поливинилацетатов и различных каучуков.
Минеральные кислоты (плавиковая, соляная, разбавленные азотная и серная,
фосфорная и т. п.) по сравнению с сильными окислителями являются менее
реакционными веществами по отношению к полимерам. Они практически не действуют
на полиэтилен, полиизобутилен, полистирол, поливинилхлорид, фторопласты 3 и 4
(трифторхлорэтилен и тетрафторэтилен) и т. п. В полимерах типа полиэфиров,
полиуретанов, поливинилацетатов, полиамидов и различных каучуков действие
минеральных кислот может вызвать некоторые химические изменения в структуре
макромолекул. В результате этого в указанных средах такие полимеры, как
поливинилацетат, полиамид и другие неустойчивы, а полиэфиры, полиакрилаты
устойчивы только при 200 С.
К действию галогенов - фтора, хлора, йода - устойчивы в основном те же
полимеры, которые выдерживают воздействие сред - окислителей: фторопласты,
поливинилхлорид, полистирол, фурановые смолы.
Большинство пластических масс устойчиво к воздействию органических
кислот. Из термопластических полимеров наибольшей стойкостью обладают
фторопласты, а из термореактивных - фенольные и фурановые смолы. Минимально
стойкие - полиамидные и карбамидные смолы, которые в органических кислотах
ограниченно устойчивы даже при 200 С.
Вода и водные растворы неорганических солей разрушающе действуют только
на полиэфирные смолы при нормальной температуре и вызывают деструкцию
полиамидов при высокой температуре (выше 1800 С) или повышенном
давлении.
Щелочи являются химически агрессивными средами по отношению к
фенопластам, к полиэфирам, полиамидам, полиуретановым и поливинилацетатным
смолам. Большинство остальных полимеров устойчиво к воздействию щелочных сред.
Как видно из вышеизложенного, многие полимеры при эксплуатации их в
условиях воздействия различных агрессивных сред обладают достаточно высокой и
часто практически универсальной химической стойкостью. Именно этим объясняется
широкое применение полимерных материалов для повышения долговечности изделий и
конструкций.
СПИСОК ЛИТЕРАТУРЫ
Балалаев
Г.А., Медведев В.М., Мощанский Н.А. Защита строительных конструкций от
коррозии. М.; Стройиздат, 1966.
Артамонов
В.С., Молгина Г.М. Защита от коррозии транспортных сооружений. М.; Транспорт,
1976.
Москвин В.М.,
Иванов Ф. М., Алексеев С.Н., Гузеев Е.А. Коррозия бетона и железобетона, методы
их защиты. М.; Стройиздат, 1980.
Гуревич Э.А.
Химическая стойкость строительных материалов. Учебное пособие. Саратов, СПИ,
1980.
Шейкин А.Е.
Строительные материалы. М.; Стройиздат, 1984.
СНиП
2.20.11-85. Защита строительных конструкций от коррозии. Госстрой СССР, Москва,
1986.
ПРИЛОЖЕНИЕ
Вопросы к контрольным заданиям по вариантам
Вариант 1
1. Характеристика агрессивности воздушных и газовых сред.
2. Коррозия бетона I вида
- причины и характер разрушения.
. Условия развития коррозии стальной арматуры в бетоне.
. Биологическая и химическая коррозия древесины.
Вариант 2
1. Разрушающее действие на материалы водной среды.
2. Условия возникновения и механизм электрохимической
коррозии металлов.
3. Защита бетона методом гидрофобизации.
4. Химостойкость термопластов на основе полиэтилена,
Вариант 3
1. Выветривание природных каменных материалов.
2. Сульфатная коррозия бетона.
. Водостойкость и морозостойкость асфальтобетонов.
. Защита древесины от возгорания.
Вариант 4
1. Минералогический состав и разновидности портландцементов.
2. Коррозия бетонов II
вида при действии углекислых вод.
. Факторы, влияющие на сохранность арматуры в бетоне.
. Химостойкость пластмасс в физически активных средах.
Вариант 5
1. Разрушение цементного камня мягкими водами и агрессивной
углекислотой.
2. Катодный и анодный процесс в механизме электрохимической
коррозии стали.
3. Влияние вида связующего на свойства полимербетонов.
4. Защита древесины от гниения.
Вариант 6
1. Разрушение цементного камня сульфатными водами.
. Коррозия бетонов II
вида в кислых средах.
. Металлизационные защитные покрытия по металлу.
. Старение полимерных материалов.
Вариант 7
1. Разрушение цементного камня при действии кислых вод.
2. Защитные свойства бетона по отношению к стальной арматуре.
. Полимербетоны.
. Лакокрасочные защитные покрытия по металлу.
Вариант 8
. Пуццолановый портландцемент.
. Механизм и причины разрушения бетона при коррозии III вида.
. Долговечность асфальтобетона.
. Виды и основные свойства термопластов.
Вариант 9
1. Шлакопортландцемент.
2. Способы повышения стойкости бетона в условиях коррозии
выщелачивания и сульфатной коррозии.
3. Бетонополимеры.
4. Виды и основные свойства реактопластов.
Вариант 10
1. Сульфатная коррозия бетона и сульфатостойкий
портландцемент.
2. Лакокрасочные защитные покрытия по бетону.
3. Способы защиты каменных материалов от выветривания.
. Стойкость пластмасс в химически агрессивных средах.