Пищевые цепи моря
Курсовая работа
Гопаны в нефтях и методика их изучения
Оглавление
Введение
Происхождение
гопанов
Структура
гопанов
Общие
сведения о гопанах
Методика
изучения гопанов
Применение
гопанов
Заключение
Список
литературы
Введение
Целью
написания данной курсовой работы является рассмотрение одной из групп
углеводородов-биомаркеров - группы гопанов и методики их изучения, в частности
хромато-масс-спектрометрии.
Что же такое углеводороды-биомаркеры?
Высокомолекулярные насыщенные углеводороды, обнаруженные
в нефтях, унаследовавшие липидную часть живого вещества называются
биомаркёрами. В составе исходного живого вещества, участвующего в
нефтеобразовании, доминирующая роль принадлежит липоидиновым компонентам
(липидам и липоидам). В ходе диагенетических и катагенетических преобразований
липиды превращаются в насыщенные алкановые и циклоалкановые, а также моно-,
ди-, тетрациклические и полициклические ароматические углеводороды.
Биомаркеры используются, чтобы коррелировать нефти
друг с другом и с их нефтематеринскими породами, таким образом, углубляется
понимание строения резервуаров, путей миграции и возможных подходов при
проведении поисково-разведочных работ. Биомаркеры могут использоваться, чтобы
оценить степень преобразованности и (или) биодеградации, таким образом,
предоставляя важнейшую информацию, необходимую чтобы правильно оценить
распределение и продуктивность бассейнов. Биомаркеры дают важнейшую информацию
относительно региональных изменений типов нефтей и нефтематеринских пород,
контролирующихся генотипом органического вещества и условиями обстановок
осадконакопления. Наконец, биомаркеры предоставляют возможность лучше понять
кинетику нефтеобразования и теплового режима бассейна. [4]
В составе биомаркеров в наибольших концентрациях встречаются: нормальные
алканы, стераны, трициклические и тетрациклические терпаны, гопаны и некоторые
другие углеводороды. В настоящее время определено более 600 биомаркёров,
наиболее изученными из которых являются стераны, изопренаны и терпаны.
Происхождение гопанов
Гопаны достаточно распространены в осадках и нефти,
потому что гопаноидные предшественники являются важными компонентами мембран в
живых клетках, устойчивыми к биодеградации в течение диагенеза.
Основным стуктурным предшественником гопанов является
гопаноидный спирт-бактериогопантетрол (рис.1), имеющий 35 атомов углерода в
молекуле, и некоторые другие биогопаноиды, которые в процессе диа-,
катагенетической эволюции осадков теряют гидроксильные группы (в случае
спиртов) или декарбоксилируются (в случае кислот) и в древних осадках, углях,
горючих сланцах и нефтях присутствуют в виде углеводородов гомологического ряда
гопана. Гопаны в растениях и грибах достаточно редки. Их обнаружили в некоторых
тропических деревьях и травах, а также в папоротниках. У бактерий, синезеленых
водорослей и лишайников синтез гопаноидов занимает ведущее место в
изопреноидном метаболизме. Они входят в состав клеточных мембран и выполняют
функции, подобные растительным и животным стеринам.
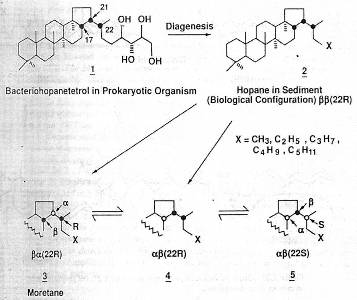
Рис.1. Происхождение гопанов в нефти из
бактериогопантетрола (1) найденный в липидных мембранах прокариотических
организмов. Стереохимия обозначена пустой (а) и черной (в) точками (водород
направлен в и из страницы. Соответственно). “биологическая” конфигурация [17β (н), 21β (н), 22r] наложена на бактериогопантетрол, и непосредственно насыщает
продукт (2) ферментами живых организмов, неустойчива в течение катагенеза и
подвергается изомеризации до “геологических” конфигураций (3,4,5). 17β,21α (н) углеводороды (з) называются
моретанами, в то время как все остальные гопанами(2,4,5).[4]
Биологическая конфигурация почти плоская, хотя
плойчатость связей углерод-углерод в кольцах приводит к трехмерной форме.
Подобно стеролам, бактериогопантетрол является амфипатическим, потому что
содержит как полярные, так и неполярные концы (рис.2). Неполярный конец
гидрофобен, и таким образом, нелегко связывается с водой или другими полярными
растворителями. Полярный конец, однако, является гидрофильным, и легко
растворим в воде. В клеточной мембране гидрофобные концы липидов расположены
внутрь к центру липидного двойного слоя, и полярные концы обращены к водной
среде окружающей клетку или цитоплазму внутри клетки. [4]
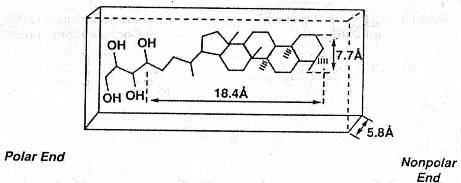
Рис.2. Бактериогопантетрол [4].
Плоская конфигурация и амфипатический характер
необходимы бактериогопантетролу, чтобы встраиваться в липидную мембранную
структуру. Так как это стереохимическое расположение термодинамически
неустойчиво, диагенез и катагенез бактериогопантетрола приводят к
преобразованию 17β (Н), 21β (Н) предшественников в 17α (Н), 21β (Н)-гопаны и 17β (Н), 21α (Н)-моретаны. [1]
Структура гопанов
Структура цилопентанопергидрохризена - основа гопанов, то есть гопан
состоит из четырёх сжатых циклогексиловых колец, каждое из которых в форме
кресла и сжатого циклопентилового кольца (рис.3).
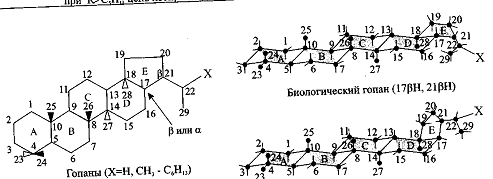

Рис.3. Структура гопанов [2].
Изопреновые звенья служат основой в структуре (Изопрен (метилбутадиен) -
основной структурный блок, состоящий из пяти атомов углерода, который найден во
всех биомаркерах). Между изопреновыми звеньями связь в гопанах «голова к
хвосту» и именно поэтому они являются регулярными соединениями. Гомологи
гопановых углеводородов отличаются всего лишь величиной алкильного заместителя(CH3-С8H17), присоединенной к боковой цепи на Е-кольце. Углеводороды
ряда гопана имеют 21 атом углерода в циклах, шесть метильных заместителей в
цикле, из которых четыре являются ангулярными. [4]
Общие сведения о гопанах
Собственно говоря, название “гопан” применимо лишь к углеводороду состава
С30. Углеводород состава С29 называют норметилгопаном,
или адиантаном, состава С27 (отсутствует заместитель при С21)-трисноргопаном.
Углеводороды состава С31, С32 и так далее называются
соответственно гомогопаном, бисгомогопаном и так далее.
Гопаны с 30 и менее атомами углерода имеют ассиметричные центры в С-21 и
на всех кольцевых швах (С-5, С-8, С-9, С - 10, С-13, С-14, С-17, и С-18).
Гопаны с более 30 атомами углерода называются гомогопанами, где приставка гомо
- касается дополнительных групп метилена в исходной молекуле, гопане. Обычные
гомогопаны имеют расширенную боковую цепочку с дополнительным центром в С22
который приводит к двум пикам для каждого гомолога (22R и 22S) на
масс-спектограммах этих соединений.
Пара С27 - гопанов (17αН-22,29,30-трисноргопан и 18αН-22,29,30-триноргопан) обычно
называют Tm и Ts (соответственно). Считается, что Tm-гопан-биологически образованная структура; Ts-гопан - образовался из него либо посредством
диагенетических, либо термальных процессов, или же посредством тех и других.
Гораздо более вероятным является расщепление одиночной
связи углерод-углерод между позициями 21 и 22 (приводящие к С27
гопану) или расщепление любой из двух других связей углерод-углерод,
присоединенных к С22 приводящему к С29 гопану), чем
последовательное расщепление двух связей углерод-углерод.
В стереохимическом плане в гопановых углеводородах
наиболее стабильной частью является правая часть молекулы, а именно хиральные
центры у С17 и С22 атомов. Гопаны состоят из трех
стереоизомерных рядов, а именно: 17α(Н),21β(Н), 17β(Н),21α(Н), 17β(Н),21β(Н)-гопанов. Соединения в ряду βα
называются моретанами.
(рис. 1)
Обозначения альфа (α) и бета (β) указывают, что водородные атомы
ниже или выше плоскости колец.
Существуют два основных типа гопанов: 17αН, 21βН - нефтяной и 17βН, 21βН - биологический. В нефтях, как
правило, присутствуют лишь следы гопанов, имеющих “биологическую” конфигурацию.
Главная масса гопанов представлена углеводородами 17α,21β ряда. Биогопаны как весьма
неустойчивые соединения найдены лишь в торфе, бурых углях, молодых сланцах и
рассеянном органическом веществе начальных этапов катагенеза.
Итак, в биогопане сочленение циклов А/В, В/С и С/D - транс, тогда как в геологических
гопанах динамически неустойчивое транс-сочленение циклов D/E меняется на более устойчивое - цис. (Сочленение циклов С/D транс - в биогопане и цис - в
нефтяном гопане.) Именно из-за термической неустойчивости транс-сочленения D/E и заслонения связей 21-22 и 17-16 (цис-ориентация
замещающего радикала) соединения ряда ββ (биологические гопаны) обнаруживают в
нефтях в очень небольших количествах. Гопаны С28
αβ редки или
отсутствуют в нефтях, так как их образование требует расщепления не одной, а
двух связей углерод-углерод, присоединенных к С22 в С35 в
гопаноидном предшественнике.
Следует также отметить, что биогопаны имеют более
высокую температуру кипения и на хромато-масс-фрагментограммах иллюстрируются
значительно позднее стереоизомерных им нефтяных гопанов (например, биогопан
состава С30 иллюстрируется в области нефтяного гопана С31).
Различные конфигурации гопанов хорошо заметно в их
масс-спектрах. Главным направлением распада гопанов под влиянием электронного
удара является разрыв связи 8-14 с образованием двух фрагментов - постоянного А
(m/z=191) и переменного (то есть зависящего от молекулярной массы
исходного углеводорода) - Б (m/z=149(С27), 163(С28),
177(С29), 191(С30), 205(С31), 219(С32),
233(С33), 247(С34) и так далее.). Кроме того, для гопанов
характерными являются молекулярные массы:370, 384, 398, 412, 426, 440 и так
далее.
Для нефтяных (17α) гопанов фрагмент А более
интенсивен, чем фрагмент Б. Для биогопанов (17β), напротив, интенсивность фрагмента
Б выше, чем интенсивность фрагмента А.
Для углеводородов ряда гопана состава С31 и
выше, то есть в тех случаях, когда атом С-22 становится хиральным, возможно
существование двух эпимеров, отличающихся R- или S-конфигурацией
хирильного центра С-22, в исходных биогопанах состава С31 и выше
атом С-22 имеет строго определённую R-конфигурацию. В то же время переход к нефтяным гопанам, кроме уже
отмечавшейся эпимеризации С-17, сопровождается эпимеризацией центра С-22, что
проявляется в ряде дублетных пиков, характерных для хроматограмм смеси нефтяных
гопанов. Следует отметить несколько большую устойчивость эпимера с S-конфигурацией. В условиях
равновесия, а также в нефтях соотношение 22S- и 22R-эпимеров
обычно равно 1.2-1.4. Изомеры, различающиеся конфигурацией С22,
несколько напоминают по- свойствам аналогичные эпимеры стеранов, различающихся
конфигурацией углеродного атома С20, особенно в βα-диастеранах. [4]
Говорить о биодеградации нефти мы можем если при m/z=177 наблюдается присутствие углеводородов гомологического
ряда 25-норгопанов. Например, при биодеградации гопан С28 мы видим
как 25,30-бисноргопан, а гопан С29 как 25-норгопанС29.
Методика изучения гопанов
В 1950-1970 годах были заложены основы современной теории нафтидогенеза,
охватывающие как геологические, так и химические стороны этого процесса.
Считается, что основная масса углеводородов, образующих скопления нефти и газа,
формируется на стадии катагенеза, но их количество и состав в значительной
степени предопределены особенностями исходной биомассы, количеством и
характером превращений органического вещества в диагенезе. Многие углеводороды
и близкородственные им соединения, обнаруженные в нефтях, наследуют структуру
молекул липидной части живого вещества, а промежуточные продукты их
биогеохимических превращений наблюдаются в органическом веществе современных
осадков.
Ранее состав и распределение углеводородов-биомаркёров изучался методом
газожидкостной хроматографии.
В настоящее время ведущую роль в изучении состава и распределения
биометок нефтей, играет метод хроматомасс-спектрометрии. Типичный
хроматомасс-спектрометр, используемый для анализов биометок, состоит из
газового хроматографа последовательно соединённого с масс-спектрометром.
Изучаемая жидкость вводится в газовый хроматограф, где различные составляющие
его компоненты разделяются в соответствии со скоростями их перемещения через
газово-хроматографическую колонку. Разделение насыщенных углеводородов
производится в соответствии с молекулярным весом и летучести компонентов.
Разделённые компоненты смеси покидают друг за другом газовый хроматограф и
попадают в масс-спектрометрическую ионизационную камеру, где они анализируются
в той же последовательности. Далее каждый компонент, попадающий в
масс-спектрометр, бомбардируется пучком электронов высокой энергии,
ионизирующих молекулы путём выбивания одного электрона (рисунок 4 [2]).
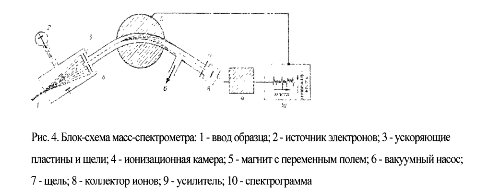
Молекулы и фрагментарные ионы, полученные этим способом, различаются по
массе, в большинстве своём имеют одинаковый заряд +1. И только благодаря этому
их различию в отношениях молекулярной массы к заряду, вызванных отличием масс,
они могут быть разделены в магнитном поле или квадрополе. После чего
разделенные ионы подходят к детектору ионного захвата, где относительное
количество массы каждого иона записывается. Полная запись содержания и масс
всех ионов, образованных из начальных компонент, называется их масс спектром.
Собственно масс-спектр изображает зависимость интенсивности сигнала (ордината)
от сооотношения массы к заряду (m/z, абцисса) для различных заряженных
продуктов, образовавшихся при распаде вещества. Постольку поскольку заряд z обычно равен единице, отношение m/z в действительности отвечает массе иона. Различные классы
фрагментарных биомаркёров имеют характерные для каждого из них пути в
масс-спектрометре, зависящие от их молекулярной структуры. Фактически, в ХМ-МС
вначале получают хроматограмму полного ионного тока (как в газо-жидкостной
хроматографии). Затем с помощью квадрупольного масспектрометра возможно
разделение этого полного ионного тока на фрагменты определённой массы.
Для отдельного хромотографического пика, вымывающегося
из колонки, обычно снимают несколько полных масс-спектров (от трёх до десяти).
Для этого необходимо очень быстрое сканирование масс (за время от 0.1 до
нескольких секунд) и запись их в цифровом виде на компьютер одновременно с
фиксацией времени удерживания соединений. В зависимости от количества
соединений, введённых в хроматограф, количество сканирований может быть очень
большим и достигать нескольких тысяч. Впоследствии возможна компьютерная
обработка полученных данных, то есть получение масс спектров для любого пика
хроматограммы. Кроме того, компьютерная обработка масс-спектров позволяет
различать индивидуальные соединения, имеющие близкие времена удерживания и
элюирующиеся на газовой хроматограмме в виде единого пика. Компьютерная
обработка также позволяет просканировать всю хроматограмму по определенным
фрагментным или молекулярным ионам и получить так называемые
масс-фрагментограммы или масс-хроматограммы. Это бывает полезно, если есть
необходимость проследить распределение индивидуальных соединений какого-либо
гомологического ряда или соединений, обладающих близким структурным строением.
Так, например, тритерпановые хорошо иллюстрируются масс-фрагментограммой по - m/z 191. [2]
Хромато-масс-спектрометрические исследования
насыщенных углеводородов проводились на системе, включающей газовый хроматограф
6890, имеющий интерфейс с высокоэффективным масс-селективным детектором Agilent 5973N. Хроматограф снабжен кварцевой капиллярной колонкой длиной
30м, а диаметром 0,25 мм, импрегнированной фазой HP-5MS. В качестве
газа-носителя служил гелий со скоростью потока 1мл/мин. Температура испарителя
300°С. Ввод пробы проводился без деления потока. Изометрическая ‘”площадка”
длительностью 4 мин. Программирование подъема температуры осуществлялось от
100°С до 290°С со скоростью 4°С в мин с последующей изотермой в течение 20 мин.
Ионизирующее напряжение источника-70eV, температура источника - 230°С. Идентификация соединений осуществлялась
по временам удерживания, которые могут меняться в зависимости от условий
съемки, путем сравнения полученных масс-фрагментограмм с уже имеющимися
спекторами в библиотеке системы и опубликованными данными.
При компьютерной обработке хроматограмм очень полезно
проводить их реконструкции по наиболее характерному для гопанов фрагментарному
иону с m/e 191. Схема распада гопана под воздействием электронного
удара представлена на рис.5.
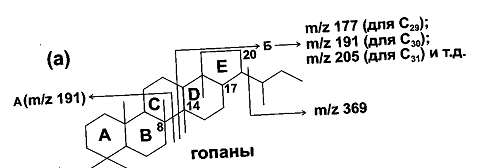

Рис.5. Схема распада гопана под воздействием электронного удара [2].
На распечатанной масс-фрагментограмме можно идентифицировать пики
гопанов, стеранов или терпанов по аналогии пользуясь типовой
масс-фрагментограммой с пронумерованными пиками и таблицей идентификации пиков.
Обрабатываемая и типовая масс-фрагментограммы сравниваются и на первой
пронумеровываются пики, на тех же позициях, как на типовой. Высоты пиков
измеряются линейкой, для этого проводятся базовые линии, проведённых от вершины
пика до пересечения с базовой линией параллельно оси игрек. Типовая
масс-хроматограмма терпанов и идентификация пиков представлены на рис.6.
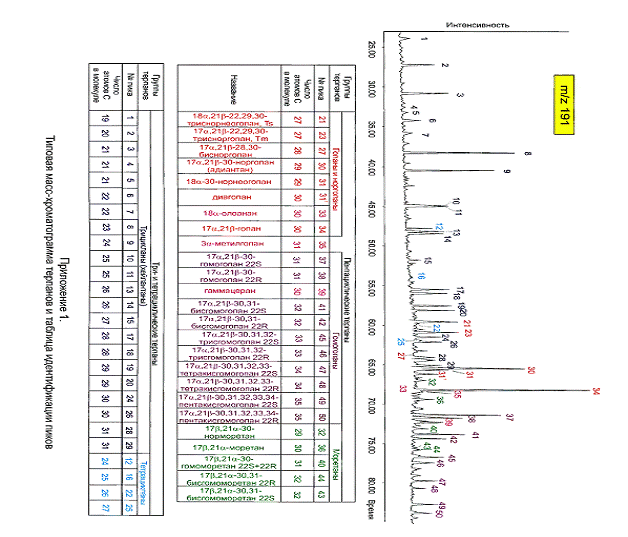

Рис.6. Типовая масс-хроматограмма терпанов [2].
Как пример использования методики хромато-массспектрометрии я приведу
лабораторную работу, по идентификации, измерении и расчету содержаний терпанов
(m/z 191) (Рис.7).
Результаты были занесены в рабочие таблицы (Табл.1, Табл.2, Табл.3,
Табл.4, Табл.5, Табл.6, Табл.7) и был произведен расчет концентраций. Исходя из
полученных данных можно сделать вывод о том, что ОВ-незрелое (Ts/Tm<1), но так как мы не видим ярко выраженных биогопанов и
рассмотрев отношение изомеров 22S/22R (изомеры 22S встречаются в больших концентрациях), можно сделать вывод,
что мы находимся в начале стадии нефтегазообразования (не ниже МК1, начале
МК2). Относительно генотипа ОВ сказать точно мы не можем, но так как С35<С34
можно предположить, что ОВ континентального происхождения. Преобладает гопан С30,
доля гопанов приблизительно 81%, трицикланов мало (из них преобладают С19
и С20), что тоже говорит о континентальном генезисе, но для полной
характеристики нужно рассмотреть также стераны, геологию региона и так далее.
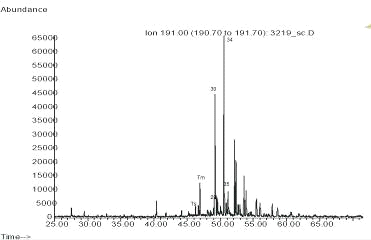
Рис.7.Изучаемая масс-хроматограмма.
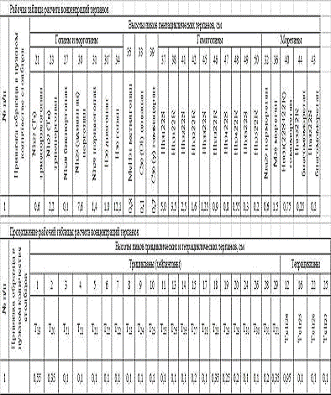
Таблица 1.
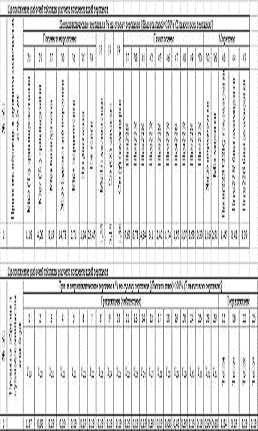
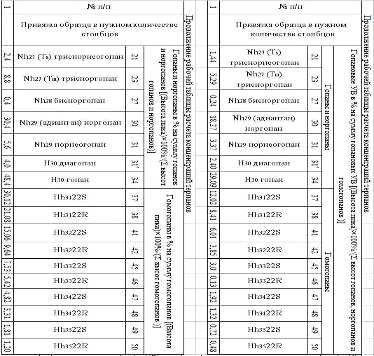
Таблица 3.
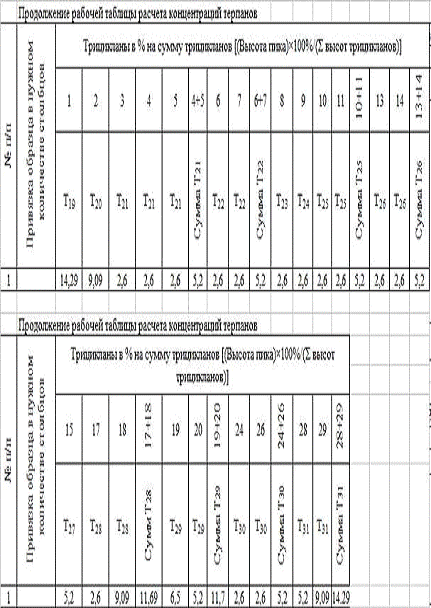
Таблица 4.
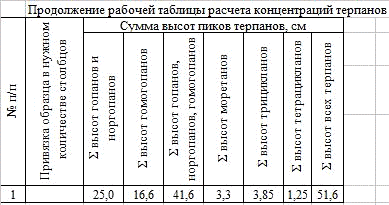
Таблица 5.
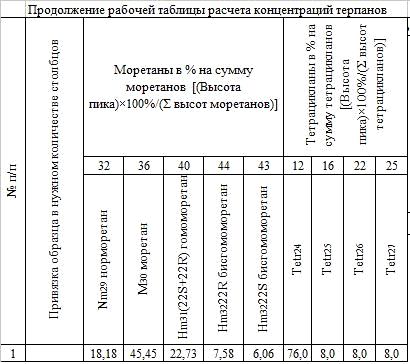
Таблица 6.
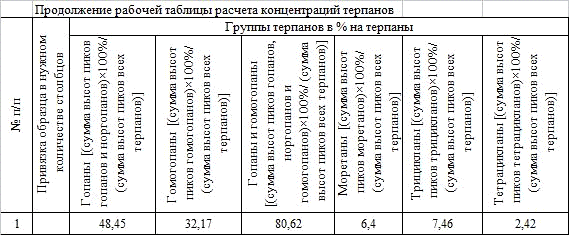
Таблица 7.
Применение гопанов
Сопоставление концентрационного распределение гопанов в нефтях и в РОВ (в
битумоидах) позволяет определить источники образования тех или иных нефтей.
В качестве индикатора оценки окислительно-восстановительной обстановки в
седиментогенезе и диагенезе используется относительное распределение
гомогопанов С31-С35. Соотношение гомогопанов C35/(C31-C35) называют гомогопановый индекс.
Относительно высокие концентрации гомогопана С35 указывают на
морские условия седиментогенеза и восстановительные условия диагенеза.
Относительно низкие концентрации С35 - на субокислительные или
слабовосстановительные условия.
Еще один показатель условий образования - соотношение С34/С35.
По данным В.А. Каширцева в нефтях морских фаций в ряду гомогопанов С34<С35,
в нефтях континентального генезиса - С34>С35. [7]
Об информативности такого показателя, как соотношение
С27 норметилгопана (адиантана) к гопану, нет единого мнения. О.А.
Арефьев считает, что в нефтях терригенно-карбонатного комплекса величина
соотношения адиантан/гопан ниже, чем в нефтях галогено-карбонатного (0,6 и 0,9
соответственно). По его данным для пермских нефтей Восточной Сибири,
генерированных материнским веществом континентально-болотных фаций, характерно
равное соотношение адиантана и гопана. По соотношению концентраций гопанов С27
и С30 четкой диагностики типов ОВ осуществить не удается, но
замечено, что в морских анаэробных обстановках он, как правило, имеет значение
ниже 0,5, а значения этого показателя, большее, чем 0,8 встречаются только в
неморском ОВ.
Гопаны также используются для оценки степени
катагенетических преобразований в ОВ и нефтях, так как в них не происходит
перестройки основного углеродного скелета под воздействием температуры. С
ростом катагенетической превращенности ОВ в гопанах происходит стереохимическая
изомеризация, которая приводит к появлению пространственных изомеров с
цис-сочленением колец C/D, трансориентацией алифатического
радикала у С-17, и стереоизомеров, с цис-сочленением колец D/E и эпимеров с S-конфигурацией
у хирального центра С-22. С учетом этого, для оценки степени катагенетического
созревания ОВ используются показатели:
) Соотношение гопанов 17α,21β/17β,21β, то есть процент новообразованных
нефтяных гопанов.
) Соотношение гопанов 22S/(22R+22S). Стереохимическая перестройка
гопанов, приводящая к увеличению S-конфигурации
по отношению к R, активизируется
со стадии MK1 (мезокатагенеза), достигая на этаже
"нефтяного окна" термодинамического равновесия. В нормально зрелых
нефтях, как правило, соотношение S/R в С32 составляет 60/40.
Стереохимические перестройки этого типа наиболее четко проявляются в
гомогопанах С30-С33.
) Соотношение 17β,21α-моретанов С29+С30
и 17α,21β-гопанов С29+С30.
Оно уменьшается с увеличением термической зрелости и достигает 0,05
(равновесный уровень) в сильнопреобразованных нефтях.
Кроме того, очень широко, для оценки степени
катагенетической превращенности нефтей используется соотношение Ts/Tm. Пара С27 - гопанов (17α(Н)-22,29,30-трисноргопан и 18α(Н)-22,29,30-триноргопан) обычно
называют Tm и Ts(соответственно). Считается, что Tm гопан - биологически образованная структура, а Ts гопан образовался из Tm либо посредством диагенетических,
либо термальных процессов, или же посредством тех и других. Таким образом,
соотношение Ts/Tm увеличивается с повышением зрелости, и в главной зоне
нефтеобразования составляет 1, а на поздних стадиях катагенеза - 5-10. Но в
последнее время появился ряд работ, где показаны значительные вариации этого
показателя при близкой степени зрелости нефтей, что указывает на влияние в изменении
этого соотношения не столько термальных условий преобразования, сколько
лито-фациальных условий осадконакопления.
Так, по данным Филпа, Рюлькеттера и Марзи высокие
значения соотношения Ts/Tm характерны для нефтей из карбонатных
пород, по Робинсону величины этого показателя велики для континентальных
нефтей. По мнению Молдована величина этого соотношения контролируется
окислительно-восстановительным потенциалом. Значения отношения Ts/Tm увеличиваются при наличии глинистых минералов
(катализаторов) в породах, гиперсолёности вод, низких значениях Eh и уменьшаются при более высоких
значениях pH среды осадконакопления. Таким
образом, применение этого показателя для оценки степени зрелости нефтей
желательно проводить только для групп нефтей, генерированных в единых
фациальных условиях. [6]
Заключение
гопан углеводород спектрометрия
Изучение биомаркеров в нефтях черезвычайно важно для познания их генезиса
и геохимической истории, для повышения достоверности прогноза
нефтегазоносности, т.к. сложные структуры биомаркеров дают подробную информацию
относительно их происхождения.
В данной курсовой работе была рассмотрена группа
гопанов. Структура этих соединений представляет собой четыре сжатых
циклогексиловых кольца, каждое из которых в форме кресла и сжатое циклопентиловое
кольцо. Основным стуктурным предшественником гопанов является гопаноидный спирт
- бактериогопантетрол, имеющий 35 атомов углерода в молекуле. Существуют два
основных типа гопанов: 17αН, 21βН - нефтяной и 17βН, 21βН - биологический, а также ряд
соединений 17β(Н),21α(Н), которые называются моретанами. (рис. 1)
В нефтях, как правило, присутствуют лишь следы биологических гопанов, а
основная масса представлена геогопанами.
Также был раскрыт актуальный сейчас метод хромато-масспектрометрии, приведена
типовая хроматограмма и таблица с идентификацией пиков. Для оценки степени
катагенетической превращенности нефтей используется соотношение Ts/Tm. Для определения генотипа ОВ мы должны использовать
полученные показатели и отношения в совокупности с другими геологическими
показателями и геологией региона. Например, показатель условий образования -
соотношение С34/С35. В нефтях морских фаций в ряду
гомогопанов С34<С35, в нефтях континентального
генезиса - С34>С35. Или, например, относительно
высокие концентрации гомогопана С35 указывают на морские условия
седиментогенеза и восстановительные условия диагенеза, а относительно низкие
концентрации С35 - на субокислительные или слабовосстановительные
условия.
Гопаны применяются для решения очень многих задач, например для
корреляции систем нефть-нефть или для системы нефть-материнские породы.
Сопоставление концентрационного распределения гопанов в нефтях и рассеянном
органическом веществе позволяет определить источники образования тех или иных
нефтей, также они позволяют определить степень преобразованности нефти, и
используются в качестве индикатора оценки окислительно-восстановительной
обстановки в седиментогенезе и диагенезе, также с помощью изучения гопанов
проводятся палеореконструкции в целях определения некоторых факторов:
источники, созревание, биодеградация. Относительное распределение гопанов
рассматривается как характерный “отпечаток пальцев” нефтей региона и поэтому
представляет интерес сводка этих данных по различным месторождениям земного
шара.
Отдельно взятый показатель не дает достоверной информации о перспективах
нефтегазоносности и продуктивности региона, нужно рассматривать в совокупности
все геохимические показатели и учитывать геологию этого региона.
Список
литературы
1. В.А.
Каширцев, Р.П. Филп, Дж. Аллен, А. Гальвес-Синибальди, И.Н. Зуева, О.Н. Чалая,
И.Н. Андреев “Биодеградация биомаркеров в природных битумах Оленекского
поднятия” 1993
2. Методическое
руководство по хромато-масспектрометрии
. Б.
Тиссо, Д.Вельте “Образование и распространение нефти” Москва, “Мир”, 1981
4. Peters
K.E., Moldowan J.M. The biomarker guide. - Prentice Hall: Englewood Cliffs. New
Jersy, 1993, 353p
5. Семинары
по предмету “Введение в геохимию нефти и газа”
. Костырева
Е.А. Геохимия и генезис палеозойских нефтей юго-востока Западной Сибири //
Новосибирск: Изд-во СО РАН. Филиал "Гео", 2005, 183 с
7. Каширцев
В.А. Органическая геохимия нафтидов востока Сибирской платформы. Якутск: СО
РАН, ЯФ, 2003. - 160 с.