Физико-химические основы производства портландцемента
Министерство образования и науки РФ
ФГБОУ ВПО
Ивановский государственный химико-технологический университет
Кафедра технологии керамики и наноматериалов
Курсовая работа на тему:
Физико-химические основы производства портландцемента
Выполнила студ. гр. 4/12
Комарова А.С.
Руководитель Косенко Н.Ф.
Иваново - 2012
АННОТАЦИЯ
В данной курсовой работе рассмотрены
физико-химические основы приготовления сырьевой смеси для производства
портландцемента по мокрому способу и ее измельчение, обжиг сырьевой смеси и
получение клинкера, измельчение клинкера.
Портландцементный клинкер является
продуктом спекания при обжиге сырьевой шихты с преобладанием в ней
высокоосновных силикатов кальция.
ВВЕДЕНИЕ
Портландцемент - гидравлический
вяжущий материал, получаемый тонким измельчением портландцементного клинкера с
гипсом и, если требуется, со специальными добавками.
Портландцементный клинкер является
продуктом спекания при обжиге сырьевой шихты надлежащего состава,
обеспечивающего преобладание в нем высокоосновных силикатов кальция, а также
наличие алюминатов и алюмоферритов кальция. После охлаждения клинкер -
спекшиеся гранулы и куски размером до 10-20 или до 50-60 мм - тонко измельчают
с небольшой добавкой гипса.
В цементе должно быть содержаться до
45-65% алита, до 20-30% белита, суммарное содержание алита и белита в клинкере
портландцемента может доходить до 80%, ограниченное количество С3А
(в пределах 4-12%), а также небольшое содержание растворимых щелочей и крайне
малое количество оксида железа (II).
Получение портландцемента возможно
лишь в результате проведения целой совокупности процессов, которые должны быть
проведены в определенных условиях.
Приготовление сырьевой смеси
заданного химического состава и с определенными физическими свойствами (влажность,
тонкость измельчения, текучесть) включает множество операций: добыча,
транспортирование и хранение сырья; дозирование и смешение сырьевых компонентов
в процессе измельчения; корректирование и гомогенизация. Далее смесь обжигают
для получения клинкера, который измельчают.
Хороший результат можно получить
лишь при тщательном регулировании физико-химических процессов.
1. ТЕОРЕТИЧЕСКИЕ
ОСНОВЫ ИЗМЕЛЬЧЕНИЯ
При приготовлении
сырьевых смесей важную роль играют энергоемкие операции измельчения -
дробление, тонкое измельчение.
Процесс измельчения
характеризуют степенью измельчения, приростом удельной поверхности, величиной
удельных затрат энергии на измельчение, гранулометрией материала, прошедшего
измельчение.
Дисперсность
порошка, получаемого в результате измельчения, выражают функцией распределения
или удельной поверхностью.
Твердые тела бывают
хрупкие и пластичные (металлы). Хрупкие тела, разрушение которых происходит в
результате увеличения упругих деформаций и роста напряжений до разрушающих.
Однако разрушение хрупких тел сопровождается небольшой пластической
деформацией. Чаще всего измельчение хрупких тел, в том числе горных пород,
производят механическим воздействием - ударным, сжимающим, изгибающим. При
измельчении в результате последовательных механических воздействий происходит
целый комплекс явлений: пластическая и упругая деформация разрушаемого тела,
деформация дробящихся тел, взаимодействие между средой (газом, жидкостью) и
измельчаемым материалом, между образующимися тонкими частицами (агрегация частиц),
между частицами материала и мелющими телами (налипание на мелющие тела). При
механическом разрушении каменных материалов происходит образование и развитие
трещин; этот процесс сопровождается комплексом явлений - тепловых, химических
(разрыв связей), электрических.
Теоретическая
прочность кристалла равна:
σT=(Еσs,/а)½,
где Е - модуль
Юнга, Па; σs - поверхностная
энергия, Дж/м2; a - межатомное расстояние, см.
При накоплении
внутренней энергии и упругих деформаций напряжения концентрируются в месте дефекта
и могут достигнуть местного превышения предела прочности. Образуется и
развивается трещина, происходит перераспределение энергии упругих деформаций,
причем лишь часть энергии превращается в поверхностную энергию новых
поверхностей. Только эта часть затрачиваемой энергии является полезной,
остальная энергия рассеивается в виде тепла и расходуется на упругие деформации
сжатия.
Существует два
подхода для объяснения механизма разрушения твердых, тел. В твердом теле
происходят непрерывный разрыв и восстановление связей вследствие теплового
движения атомов. По кинетической теории прочности, при наложении напряжений
вследствие передачи телу избыточной энергии число разорванных связей начинает
преобладать и при достаточно больших напряжениях число разорванных связей
становится достаточным для разрушения. С позиций этой теории «прочность»
связана со временем действия нагрузок, поэтому вводится понятие о
«долговечности» тела под нагрузкой. Так как при нормальных температурах
разрушающая нагрузка слабо зависит от времени, а действие разрушающих нагрузок
при измельчении твердых тел кратковременно, то эта теория не применяется при
анализе явлений измельчения.
В дробилках
материал подвергается всем видам деформаций, однако преобладают деформации
сжатия. В дробилках статических (щековых) в отличие от ударных (молотковых)
происходит медленное нарастание напряжения. При ударе рабочего органа в
материале возникает волна, распространяющаяся со скоростью 5000 м/с, а
возникающие в точке удара и локального разрушения материала радиальные трещины
распространяются со скоростью 1500 м/с. При достаточно сильном ударе со
стороны, противоположной удару, в куске образуются также трещины,
распространяющиеся со скоростью до 2000 м/с.
Зарождение трещин в
кристалле происходит в результате сдвига при наличии дислокаций или даже
дефектов атомного размера.
При измельчении
удается получить порошки с размером частиц в 1-2 мкм. Таким образом, размеры
частиц могут быть в десятки и сотни раз меньше величины «опасных» трещин. Это
показывает трудности, возникающие при анализе механизма разрушения на основе
теории трещин. При механическом воздействии энергия деформации связи
превращается в тепловую и перераспределяется между другими связями. Этой
перераспределенной избыточной энергии может быть достаточно для разрыва связей
в неравновесных состояниях. С этих позиций величина механической энергии,
необходимой для разрыва связей, может быть существенно меньше энергии связи и
оценивается в 42 кДж/моль (при 420-4200 кДж/моль для энергии связи). Таким образом,
реальная прочность твердых тел может, с одной стороны, в сотни и тысячи раз
отличаться от прочности, рассчитанной исходя из энергии связей в кристалле, а с
другой стороны, пропорциональна теоретической прочности.
Размучивание мягких осадочных пород.
При применении мягких сырьевых компонентов технологические схемы сырьевых цехов
приобретают некоторые особенности, связанные со способностью этих видов сырья
распускаться (размучиваться) в воде. Мягкие сырьевые материалы мел, мягкий
мергель, глина - состоят из тонкодисперсных природных частиц, спрессованных в
однородные конгломераты. Особенностью таких осадочных пород является их
способность легко диспергироваться в воде при интенсивном перемешивании и
дроблении, образуя стойкие водные суспензии - шламы
Для получения шлама, обладающего
достаточной текучестью (транспорт самотеком по наклонным канавам или
гидротранспорт с применением насосов), необходимо при размучивании мела
суспензию разбавить до влажности 40-50% и при размучивании глин - до влажности
50-70%.
Диспергация мела и глины в водной
среде объясняется рядом явлений:
) механическим разрушением
конгломератов природных тонкодисперсных частиц за счет дробления и интенсивного
перемешивания кусков породы в водной среде;
) расклинивающим действием пленок
воды, проникающих в поры породы; благодаря поверхностному натяжению пленка воды
в тонких капиллярах находится под значительным давлением, которое и
обусловливает их расклинивающее действие;
) физико-химическими процессами,
связанными с наличием зарядов на частичках глины, приводящими к образованию
структурированных сольватных оболочек.
Исследование процесса образования
шлама из мела показало, что меловые суспензии представляют структурированные
тиксотропные системы, и таким образом, в процессе их образования проявляются те
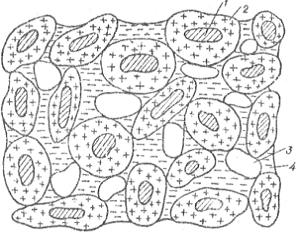
же явления, которые характерны для размучивания глинистых пород (рис.1.2).
|
|
Рис.1.2 Схема структуры известняково-глиняного сырьевого шлама:
1- ядро; 2- диффузная оболочка; 3- воздушные поры; 4- вода
|
портландцемент клинкер обжиг шихта
спекание
Грубыми частицами в глинах обычно
являются частицы кварца, который трудно усваивается в процессе спекания
клинкера. Иногда глины содержат крупные включения известняковой гальки или
гипса; мел загрязнен прожилками мелкозернистого известняка, состоящими из
частиц, более крупных по размеру, чем частицы мела. Наличие в меле и глинах
различных включений ухудшает их свойства, так как нарушает однородность
химического и гранулометрического состава.
Процесс размучивания мела или глины
приводит не только к диспергации материала и образованию
высококонцентрированной водной суспензии (шлама), но сопровождается и частичным
обогащением сырья. При размучивании из сырья выделяются различные включения,
что повышает химическую и гранулометрическую однородность материала.
При мокром способе
подготовки сырьевой смеси необходимо готовить суспензию такой влажности, чтобы
она не была слишком вязкой, иначе затрудняются гомогенизация шлама, возможность
классификации, а также гидротранспорт шлама. С точки зрения обжига повышенная
влажность сырьевой смеси вредна, так как на испарение влаги тратится излишнее
топливо. Кроме того, при повышенной влажности шлама падает производительность
печи. Повышение влажности шлама на 1% снижает производительность печи примерно
на 1,5% и на 1% увеличивает расход топлива. При мокром способе энергозатраты на
приготовления сырьевой смеси сравнительно с сухим способом невелики.
2. ОБЖИГ СЫРЬЕВОЙ
СМЕСИ И ПОЛУЧЕНИЕ КЛИНКЕРА
В процессе обжига
сырьевой смеси в результате взаимодействия главных оксидов СаО, SiO2,
Al2O3, Fe2O3, образуется четыре
основных клинкерных минерала, содержание которых может колебаться в пределах:
трехкальциевый
силикат (алит) 3СаО∙SiO2 (С3S) - 45-60%;
двухкальциевый
силикат (белит) 2СаО∙SiO2 (C2S) - 15-360%;
трехкальциевый
алюминат 3СаО∙Аl2O3 (C3A)
- 5-15 %;
четырёхкальциевый
алюмоферрит 4СаО∙Al2O3∙Fe2O3
- 10-20%.
Тонкоизмельченные и
тщательно перемешанные сырьевые смеси подвергают обжигу при 1673-1773 К в
цементообжигательных печах. Образующийся в результате обжига спекшийся
камнеподобный продукт - клинкер - характеризуется сложным минералогическим
составом и столь же сложной микрокристаллической структурой.
В процессе обжига
сырьевой смеси в результате взаимодействия главных оксидов СаО, SiO2,
Al2O3, Fe2O3, образуется четыре
основных клинкерных минерала, содержание которых может колебаться в пределах:
трехкальциевый
силикат (алит) 3СаО∙SiO2 (С3S) - 45-60%;
двухкальциевый
силикат (белит) 2СаО∙SiO2 (C2S) - 15-360%;
трехкальциевый
алюминат 3СаО∙Аl2O3 (C3A)
- 5-15 %;
четырёхкальциевый
алюмоферрит 4СаО∙Al2O3∙Fe2O3
- 10-20%.
Сырьевые смеси в
процессе их нагревания до высоких температур претерпевают сложные превращения,
сопровождающиеся изменением минералогического состава и физических свойств.
Характер изменения физических свойств сырьевых смесей, приготовленных по сухому
или мокрому способу, по мере их нагревания оказывается до определенного
интервала температур различным, однако химические превращения компонентов и
основные химические реакции в обоих видах сырьевых смесей протекают,
естественно, в одном и том же направлении.
При нагревании
сырьевых смесей до 373 К из них испаряется капельно-жидкая вода, в интервале от
373 до 573 К удаляется адсорбционная и частично кристаллизационная вода, при
673-973 К - основная масса кристаллизационной и кристаллохимически связанной
воды, а остаточные небольшие количества воды (2-3%) выходят из состава
кристаллических решеток алюмосиликатов при температуре материала 1173-1273 К.
Органические
примеси в сырьевой смеси выгорают в интервале температур от 473 до 573 К.
По мере повышения
температуры структурные элементы кристаллических решеток твердых тел (ионы,
атомы, молекулы) начинают совершать все более значительные по частоте и
амплитуде колебания вокруг своих центров. При некоторой определенной для каждой
данной кристаллической решетки температуре амплитуда колебаний частиц достигает
такой большой величины, что появляется возможность для «отрыва» элементарных
частиц от положения равновесия в данном узле решетки и для перехода их в новые
положения как внутри решетки, так и вне ее.
Диссоциация
кальцита является комплексной реакцией. На начальной стадии происходит распад
ионов СО3 по схеме СО3 → СО2 + О2.
Вначале молекулы СО2 адсорбируются остающейся твердой фазой с
образованием комплексов (СаСО3)тв. → (СаОтв.*СО2)адс.
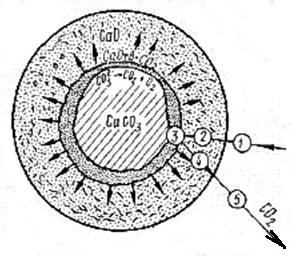
Затем молекулы СО2 десорбируются и покидают решетку кристалла СаСО3
(рис. 2.1).
|
|
Рис.2.1 Схема диссоциации зерна СаСО3
|
Кинетика процесса
диссоциации СаСО3 определяется скоростью протекания двух его стадий,
образования зародышей кристаллов СаО и их диффузионного роста.
Диссоциация
примесного доломита СаМg(СО3)2 протекает в две стадии:
) при 730оС
идет реакция разложения и диссоциации
СаМg(СО3)2
→ СаСО3 + МgО + СО2;
) при 910оС
происходит диссоциация
Перемещение
(диффузия) ионов в решетке кристалла происходит в основном по следующим
направлениям: а) из узла решетки в междоузлие; б) из междоузлия в узел решетки
с вытеснением из него в междоузлие находящегося там иона; в) из междоузлия в
междоузлие; г) из узла или междоузлия в вакантные пустоты. Разупорядоченность
кристаллической решетки, наличие в ней точечных дефектов и дислокаций
способствуют протеканию реакций в твердой фазе.
Кристаллические
решетки почти всех компонентов цементного сырья характеризуются в этих условиях
особо повышенной активностью вследствие появления в них уже при относительно
низких температурах вакантных мест, которые ранее были заняты Н2О,
ОН, СО2. Интенсивное тепловое движение структурных элементов таких
решеток, сопровождающееся «обменом мест», вначале приводит к некоторому
исправлению дефектности строения монокристаллов, а затем к взаимодействию
кристаллов различных компонентов друг с другом. Результатом этого
взаимодействия являются укрупнение кристаллов существующих фаз («собирательная
рекристаллизация») и образование кристаллов новых химических соединений
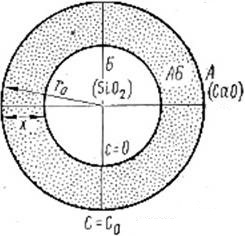
(рис.2.2).
|
|
Рисунок 2.2 Схематическое изображение процесса укрупнения
кристаллов существующих фаз и образование кристаллов новых химических
соединений между ними.
|
Диффузионные
процессы перемещения структурных элементов в твердых телах отличаются большим
разнообразием. Различают самодиффузию - перемещение в кристаллической решетке
элементы и гетеродиффузию - перемещение чужеродных ионов, атомов или молекул. В
зависимости от направленности процесса перемещения частиц различают объемную
диффузию (в глубине решетки), поверхностную (по внешней поверхности зерен) и
диффузию вдоль поверхностную (по внешней поверхности зерен) и диффузию вдоль
граней и дефектов, кристаллов (по «внутренним поверхностям» тела).
Различные ионы
перемещаются в пределах одной и той же решетки с разной скоростью, что
обусловлено различием их по размерам, величине заряда и другим свойствам. В
большинстве случаев анионы перемещаются значительно медленнее, чем катионы.
Величины коэффициента диффузии Са2+ в ряде кристаллических тел при
1473-2273 К составляли 10-9-10-12 см2/с. С
повышением температуры величины коэффициентов диффузии катионов возрастают.
Кинетика реакций в
твердом состоянии определяется скоростью диффузии наиболее активного
«покрывающего» компонента смеси сквозь слой продукта реакции.
Реакции в твердом
состоянии большей частью являются многоступенчатыми. Так, в системе СаО - SiО2 процесс
синтеза минералов осуществляется последовательно в ряду C2S→ CS→C3S→C3S. Это обстоятельство затрудняет
описание всего многоступенчатого процесса одним кинетическим уравнением.
Естественно, что механизм и, как следствие этого, кинетика реакции будут
изменяться на отдельных стадиях процесса.
По этой причине исследователями
разрабатываются пока кинетические уравнения процессов взаимодействия твердых
тел лишь для очень простых систем, а в сложных - лишь для отдельных стадий. В
качестве примера можно привести кинетическое уравнение реакции образования
двухкальциевого силиката при 1250°, которое достаточно точно отражает
действительный характер процесса:
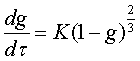
где g - степень превращения реагирующих
веществ; τ - время
протекания процесса; К - константа, зависящая от свойств материалов.
При взаимодействии оксида алюминия,
входящего в состав глинистых минералов, с оксидом кальция при температуре
800-900° по реакциям в твердом состоянии образуется однокальциевый алюминат
СаО•А12О3, который с повышением температуры насыщается
далее до 12СаО•7А12О3 и ЗСаО•А12О3.
Оксиды железа, реагируя с СаО,
приводят к образованию уже при температуре порядка 500-600° некоторого
количества однокальциевого феррита СаО•Fe2O3.
Двухкальциевый феррит начинает образовываться при температурах 900-1000°.
В смесях на основе
тонкоизмельченных известняка и кварца реакции образования силикатов кальция
начинаются также при очень низкой температуре порядка 600°, но вплоть до
800-900° они протекают с весьма небольшой скоростью. В этой системе (СаО - SiО2)
является спорным вопрос о составе соединения, образующегося в первую очередь.
По одним, более многочисленным данным, в качестве первичной фазы называют α'- или β-формы C2S, а
по другим C3S2. Однокальциевый силикат образуется в
результате вторичной реакции между двухкальциевым силикатом и кремнеземом.
Трехкальциевый силикат образуется по реакциям в твердом состоянии очень
медленно. Даже при температуре 1400-1500° синтез его оказывается затрудненным,
а при температурах 1250-1300° могут иногда наблюдаться лишь мельчайшие плохо
оформленные кристаллики этого минерала. Основное количество алита в клинкере
образуется в присутствии расплава.
При обжиге портландцементных
сырьевых смесей, приготовленных на основе глин и известняков, реакции в твердом
состоянии протекают несколько быстрее, чем при обжиге чистых двухкомпонентных
смесей, и температуры, при которых наблюдается образование минералов,
понижаются. Последовательность образования минералов в реальных смесях по
реакциям в твердом состоянии примерно такова: СА и CF образуются при
температурах ниже 800-900°, при температурах 900-1000° начинают образовываться
C2S, C2F, C12A7 и геленитС2AS,
при 1100° геленит разлагается, а в интервале температур до 1260° завершается
образование С3А и C4AF.
В присутствии некоторых веществ
(CaSО4, FeSО4 и др.) температура образования C3S
понижается, в связи с чем иногда наблюдается образование некоторого количества
C3S и при температурах 800-1000°.
При сравнительно низких температурах
в реакциях взаимодействия частиц компонентов друг с другом начинают принимать
участие жидкая и газовая фазы.
В реальных сырьевых смесях всегда
содержатся в большем или меньшем количестве примеси (серы, фосфора, марганца,
ванадия, щелочи и т. п.), которые приводят к образованию в обжигаемых смесях
«неустойчивых» псевдоэвтектических жидких фаз в виде отдельных микрокапелек
расплава или тонких пленок на поверхностях зерен. Эти первичные жидкие фазы
различного состава, образующиеся в очень небольшом количестве, способствуют
ускорению протекания твердофазовых реакций. Результаты опытов по введению в
состав сырьевых смесей легкоплавкого борного ангидрида (Тпл = 294°)
и шлаков цветных металлов подтверждают положительное действие
низкотемпературных расплавов в реакциях минералообразования.
Роль газовой фазы при низких
температурах невелика, так как процессы испарения твердых тел и взаимодействия
твердого тела с газом протекают в небольшом объеме. Однако при высоких
температурах (1400-1500°) роль газовой фазы резко возрастает, поскольку она
усиливает массопередачу между зернами реагирующих компонентов.
Таким образом, портландцементные
сырьевые смеси, нагретые до температуры 1250-1300°, состоят из ряда минералов,
образовавшихся по реакциям в твердом состоянии (С12A7, С3А,
C2F, C4AF, C2S), и непрореагировавшей
свободной извести. Повышение температуры выше 1300° приводит к появлению в системе
расплава.
В практических
условиях обжига превращение вещества весьма сложно и на разных этапах кинетика
процесса может лимитироваться различными факторами: скоростью собственно
химического взаимодействия компонентов, скоростью образования зародышей
кристаллов новых фаз, скоростью встречной диффузии ионов.
Скорость
взаимодействия отдельных компонентов (оксиды кальция с кислотными оксидами) по
реакциям в твердой фазе зависит от целого ряда факторов:
а) выше
температура;
б) более разрыхлены
кристаллические решетки реагирующих веществ при температуре реакции (за счет
разложения, присутствия примесей, полиморфизма);
в) более тонко
измельчены компоненты;
г) в газовой
атмосфере больше содержится веществ, катализирующих процесс (например, пары
воды).
Минералы,
образовавшиеся в обжигаемой сырьевой смеси в результате реакций в твердом
состоянии, с появлением расплава претерпевают значительные изменения. Одни из
них перекристаллизовываются при посредстве жидкой фазы, а другие вступают в
новые реакции и образуют новые соединения. Направление и механизм этих
превращений мало зависят от состава расплава, но скорость их определяется в
основном свойствами жидкой фазы.
Образование и
свойства жидкой фазы. Расплав возникает в грануле в виде капель и пленок
различного диаметра и толщины. Гранулы к этому периоду представляют собой
конгломерат несовершенных кристаллов СаО, MgO, C2S, C3A, C12A7, C4AF и ряда неравновесных минералов. Появившийся расплав смачивает
кристаллы конгломерата и дополнительно сближает их за счет сил поверхностного
натяжения жидкости. Одновременно с этим происходит взаимодействие между
расплавом и кристаллами, приводящее к их растворению в жидкой фазе и
кристаллизации из нее новых более термодинамически устойчивых минералов.
Процесс плавления кристалла можно
рассматривать как накопление в нем вакансий. С повышением температуры
возрастает амплитуда колебаний ионов в решетке вокруг положения равновесия и,
когда величина ее превысит среднее межатомное расстояние, начинается переход
тела в новое агрегатное состояние - жидкость, пар. В стадии предплавления
кристалл испытывает сильное термическое расширение, обусловленное большими
амплитудами колебания ионов и разрывом части химических связей. Возникающие в
кристалле вакансии склонны к флуктуационному слиянию и при их скоплении
образуются линии и поверхности разрыва, которые обособляют друг от друга
группировки ионов различного, но небольшого размера. Если с повышением
температуры химические связи в решетке разрываются постепенно и равномерно, то
кристалл тоже постепенно размягчается и превращается вначале в очень вязкую
жидкость, структура которой близка к структуре исходного твердого тела. Так
размягчаются кварц, полевые шпаты, шлаки. Если же с повышением температуры
решетка резко расширяется и химические связи в ней разрываются быстро и
неравномерно, то в кристалле вблизи точки плавления возникают хаотически
расположенные микроучастки (капли) метастабильной жидкой фазы, после чего он
сразу, же полностью (конгруэнтно) или частично (инконгруэнтно) переходит в легкоподвижную
жидкость. Так плавится большинство кристаллов кальциевых соединений, ранее
образовавшихся в обжигаемом материале по реакциям в твердой фазе. Сопутствующие
плавящемуся кристаллу различного рода примеси стимулируют процесс плавления, но
не влияют заметно на изменение его механизма и скорости.
Образования
эвтектического расплава происходит лишь в незначительной степени (1523-1553 К)
независимо от вида примесей в сырье. Поэтому при обжиге сырьевых смесей
различного состава образование минералов в них с участием жидкой фазы
начинается примерно при одинаковых температурах. Однако количество жидкости,
образующейся при соизмеримой для разных шихт температуре, и ее состав
изменяются от смеси к смеси.
Повышение
температуры обжига материала до 1673-1723 К сопровождается изменением состава и
количества эвтектического расплава. В эвтектическом расплаве при этом
дополнительно растворяются СаО и SiО2, а концентрации А12О3 и Fe2О3 понижаются. Расплав, существующий в клинкере при
1723 К и насыщенный по отношению к СаО, в одном из опытов имел состав: 57% СаО;
7,5% SiО2; 22,6% А12О3; 12,9% Fe2О3. Этот равновесный состав насыщенного при 1723 К.
Оксиды Na2О, K2O, SО3 при температурах 1673-1723 К концентрируются в
основном в расплаве. Если в клинкере содержатся щелочные сульфаты хлорида и
фторида кальция, то они также могут войти в состав расплава.
Количества жидкой
фазы, образующейся при 1673-1723 К в смеси из чистых извести, кремнезема,
глинозема и оксиды железа при постоянной сумме Al2O3 + Fe2O3 = 9%, показывают, что в
пределах изменения глиноземного модуля от 0,64.до 2,0 количество жидкой фазы в
нормальном по составу клинкере изменяется от 22,4 до 24,8%, т. е.
незначительно.
Таблица 2.1
Изменение содержания в клинкере
жидкой фазы, %, в зависимости от величины глиноземного модуля.
|
Температура, оС
|
Содержание расплава при глиноземном модуле
|
|
0,64
|
I ,25
|
2,00
|
|
1338 1400 1450
|
18,3 24,3 24,8
|
21,1 23,6 24,0
|
0 22,4 22,9
|
В отдельных
случаях, связанных с особенностями состава сырьевых смесей и технологического
процесса производства, содержание расплава в клинкере может достигать 30-35%
или быть ниже 15%. Обычно количество жидкой фазы в портландцементных клинкерах,
обжигаемых при 1723 К, составляет 20-30%.
Жидкая фаза
портландцементного клинкера в интервале температур от 1673 до 1723К не является
истинным раствором. Она представляет собой структурированную жидкость,
поскольку содержит некоторое количество агрегатов (кристаллов, сиботаксических
групп и т. п.), присутствие которых обусловлено химической природой расплава,
неустановившимся равновесием или пересыщенным состоянием расплава. Структурными
элементами расплава являются простые и сложные ионы, т. е. расплав - это ионная
жидкость. Катионы в расплаве по характеру связи с кислородом можно разделить на
две группы: катионы-модификаторы и катионы-комплексообразователи.
Катионы-модификаторы, к которым относятся главным образом ионы щелочных и
щелочноземельных металлов (Са2+, Mg2+, Na+, K+, Mn2+, Fe2+) образуют с кислородом
преимущественно ионную связь. Они не способны к полимеризации и существуют в
расплаве в виде изолированных групп Катионы-комплексообразователи (Si4+, Al3+, Р5+, В3+)
образуют с кислородом преимущественно жесткую ковалентную связь и прочно
удерживают его около себя, вследствие чего образуются комплексные ионы типа [SiO]4-, [PO4]3-, [АlO4]5- и др.
Названные комплексные ионы склонны к полимеризации и образуют сложный анионный
каркас клинкерного расплава. Комплексные анионы могут взаимодействовать
свободными связями ионов кислорода как с ионами-модификаторами, так и друг с
другом. В результате такого взаимодействия происходит непрерывный процесс
усложнения и разукрупнения комплексных анионов, причем возникающие более или
менее сложные группы ионов, называемые роями, по своей структуре приближаются к
строению соответствующих кристаллических тел. Следовательно, в алюмосиликатных
расплавах могут присутствовать анионы различной степени сложности состава и
строения.
Размер гомоцепных и
гетероцепных анионных комплексов уменьшается с повышением температуры расплава
вследствие разрывов цепей из-за возрастающей амплитуды тепловых колебаний
отдельных ионов. При определенных условиях в клинкерной жидкой фазе может
установиться кислотно-основное равновесие. Сильно выраженными основными,
свойствами обладают К2О, Na2О, CaO, MgO, FeO, а сильно выраженными
кислотными свойствами - С1-, F-, О2-, РО43-, SiО44-.
Оксиды Al2O3 и Fe2О3 могут вести себя и как слабые кислоты, и как слабые
основания в зависимости от характера кислотно-основных отношений других
элементов в расплаве. При недостатке в расплаве оснований алюминий и железо
образуют группировки [МеО6]9- и выступают как основания.
В случае же недостатка кислотных компонентов А13+ и Fe3+ образуют группировки [МеО4]5- и выступают
как кислоты. Устанавливается кислотно-основное равновесие:
[МеО4]5-=Ме3+
+ 4О2-.
Нарушение
кислотно-основного равновесия системы в любую из двух сторон сопровождается
изменением концентрации в расплаве группировок [МеО4]5- и
[МеО6]9-, что сопровождается заметным изменением его
свойств. Например, при избытке ионов Na+ и К+
увеличивается доля группировок [МеО4]5-, что вызывает
упрочнение каркасной структуры расплава и, как следствие этого, повышение его
вязкости. В присутствии же избытка, например, ионов S042- эти
группировки разрушаются и расплав становится более подвижным.
Вязкость η клинкерного расплава в
истинно жидком его состоянии определяется подвижностью наиболее крупных его
структурных элементов: чем крупнее анионные комплексы, тем они менее подвижны и
тем выше вязкость. Повышение температуры вызывает диссоциацию сложных ионов на
более простые, что сопровождается значительным понижением вязкости расплавов.
При 1723-1773 К абсолютные значения вязкости эвтектического и насыщенного при
1723 К расплавов составляли 0,03-0,4 Н∙с/м2. Дальнейшее
повышение температуры перегрева расплава (по соотношению к ТПЛ)
сопровождается небольшим изменением вязкости, что свидетельствует о разрушении
в нем большей части комплексных анионов. Так, величины вязкости расплавов при
1773-2073 К равнялись 0,02-0,1 Нс/м2.
Поверхностное натяжение
расплавов уменьшается с ростом их температуры и увеличением в них концентрации
соединений, которые сами характеризуются поверхностным натяжением. Если у
водорастворимого в расплаве металла связь Me-О слабая, то он не
удерживается в объеме жидкой фазы и вытесняется в ее поверхностный слой,
понижая тем самым поверхностное натяжение системы.
Растворение в
насыщенном при температуре 1723 К клинкерном расплаве оксидов MgO, Na2О, K2О, SО3 сопровождалось
понижением его поверхностного натяжения от 0,58 до 0,35 Н/м, т. е. для ионов Na+, K+, Mg2+, [S04]2- характерна высокая поверхностная
активность.
Плотность р
насыщенного при 1723 К клинкерного расплава при повышении температуры
снижается. Так, при увеличении температуры от 1723 до 1823 К величина р
снизилась с 3020 до 2840 кг/м3, что связано с увеличением числа
вакансий, и их размера в жидкости, т. е. с возрастанием свободного объема в
расплаве.
Диффузия разных
ионов в расплаве неодинакова, но каждый из них перемещается в жидкости
значительно быстрее, чем в твердой фазе. Скорость диффузии ионов в расплаве
зависит в основном от двух факторов:
) прочности связи
диффундирующего катиона с кислородом: чем прочнее катион связан с кислородом,
тем менее он подвижен;
) плотности
расплава: чем плотнее структура расплава, тем меньше скорость диффузии иона,
поскольку движущемуся иону в этом случае необходимо преодолеть большее число
сил отталкивания при соприкосновении с электронными оболочками других ионов.
Большое значение в
переносе растворяющегося вещества в жидкости имеет не только диффузия ионов, но
и конвективное перемещение слоев расплава, а также случайное механическое
перемещение расплава (например, движущимися пузырьками газообразного
компонента). Под влиянием указанных факторов скорость перемещения ионов может
быть во много раз больше, чем это следует из скорости их диффузии.
При растворении
кристалла в эвтектическом расплаве на его поверхности образуется адсорбционный
(пограничный) слой жидкости, насыщенный по отношению к растворяющимся оксидам.
Состав и толщина этих адсорбционных слоев на кристаллах (в частицах) разного
состава неодинаковы. Скорость дальнейшего растворения кристалла зависит от
скорости отвода из адсорбционного слоя расплава ионов, поступающих в него из
кристалла, т. е. скорость растворения кристалла в расплаве определяется двумя
компонентами:
) кинетикой
химического взаимодействия расплава с кристаллом на поверхности раздела этих
фаз с переходом структурных элементов кристалла в пограничный слой;
) кинетикой
диффузии перешедших в расплав ионов в пограничном слое - скоростью отвода,
ионов от растворяющегося кристалла.
Процесс
кристаллизации расплава с выделением новой фазы (например C3S) проходит последовательно три
основные стадии:
) пересыщение
жидкой фазы соответствующими оксидами,
) образование центров
кристаллизации,
) рост кристаллов.
Пересыщение
расплава в клинкере достигается растворением в нем несовершенных кристаллов С2S, СаО и других фаз или
переохлаждением насыщенной жидкой фазы. Процесс образования центров
кристаллизации C3S может быть самопроизвольным (гомогенным) или принудительным
(гетерогенным). В первом случае в расплаве возникают скопления ионов Са2+
и [SiO4]4-
(сиботаксические группы, ассоциаты) в результате их соударений друг с другом.
Размер этих группировок ионов является функцией температуры: при понижении
температуры величина скоплений возрастает. При достижении ими определенной для
каждого данного случая величины и устойчивости в расплаве начинается
самопроизвольная кристаллизация C3S. Ионы в жидкости, обладая значительной по сравнению с ионами
кристаллов кинетической энергией, не могут долгое время образовать
сколько-нибудь устойчивый агрегат, и всякое случайное скопление молекул быстро
распадается. Лишь при благоприятных условиях становится возможным появление
устойчивых кристаллических зародышей C3S. Во втором случае процесс зарождения кристаллов C3S облегчается из-за наличия в
расплаве твердой фазы (C2S и СаО), так как возникновение зародышей происходит на поверхности
уже имеющихся кристалликов. Устойчивые зародыши кристаллов C3S постепенно растут. Между
поверхностью растущего кристалла и расплавом образуется адсорбционный слой
(«дворик кристаллизации») из жидкости, содержащей в большом количестве ионы
кристаллизующегося вещества, который служит источником питания растущего кристалла.
В пределах этого слоя диффузия частиц из-за их повышенной концентрации
оказывается замедленной. Следовательно, рост кристаллов, так же как и их
растворение, складывается из двух процессов:
) диффузии ионов из
расплава к граням кристалла через пограничный слой жидкости;
) реакции
присоединения ионов к грани и их ориентации на ней в соответствии со строением
данной кристаллической решетки.
Между частицами в
адсорбционном слое возможны неупругие столкновения, в результате которых могут
образовываться мельчайшие кристаллики C3S, присоединяющиеся в дальнейшем к основному кристаллу.
Следовательно, рост кристаллов в расплаве с повышенной концентрацией
растворенного вещества может происходить не только благодаря последовательному
отложению молекул на поверхности кристалла, но и вследствие прилипания к ней
уже сформировавшихся мельчайших кристаллов, образовавшихся вблизи основного
кристалла. При получении клинкера в интервале температур от 1723 до 1773 К
основной фазой, кристаллизующейся в расплаве, является трехкальциевый силикат.
Преимущественное выделение C3S происходит до тех пор, пока расплав остается пересыщенным по
отношению к СаО. По мере убыли свободный СаО в системе и появления локальных
объемов насыщенного и не насыщенного кальцием расплава начинается
перекристаллизация через жидкую фазу остаточного количества несовершенных
кристаллов C2S, а также кристаллов MgO. Кристаллизация С3А и C6AхFу начинается ниже 1623 К и продолжается ниже температуры эвтектики
в переохлажденном расплаве. Кристаллизация эвтектики при низких температурах
сопровождается обычно выделением 3-5% мелкокристаллических C3S и C2S. Остаточное количество (весьма
небольшое) не успевшей закристаллизоваться жидкой фазы может образовать,
стекло.
На рис.2.3 приведена кривая роста
кристаллов алита в зависимости от температуры обжига. Пологий отрезок кривой А
- Б свидетельствует о том, что при быстром нагревании сырьевой смеси до
температуры порядка 1400° рост кристаллов алита протекает медленно. В интервале
температур 1400-1550° (отрезок Б - В) рост кристаллов минерала происходит более
интенсивно, а при температурах 1600-2000° за время обжига, равное нескольким
секундам, кристаллы алита достигают размеров 2-3 мм и более.
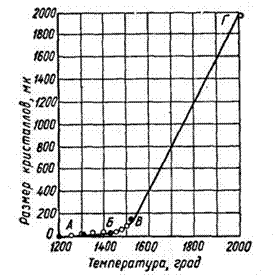
Рис 2.3 Рост кристаллов алита в
зависимости от температуры обжига
Помимо
температурного режима на кинетику кристаллизации заметное влияние оказывают и
такие факторы, как состав расплава, его вязкость, поверхностное натяжение,
наличие примесей. Оценка влияния каждого из них производится в зависимости от
конкретных условий процесса обжига.
Примеси, включенные
в кристалл, могут влиять и на его рост и облик. Адсорбируясь как на дефектных
местах кристалла, так и по всей его поверхности, примеси образуют неустойчивые
смешанные кристаллы, способные к интенсивному растворению. В результате
одновременно на одном и том же кристалле наблюдаются рост и растворение
кристалла, в результате чего снижается скорость роста кристалла и искажается
его форма. В том случае, когда сродство атомов примеси и основного вещества
велико, примесь может включиться в процесс построения основного кристалла и
образовать в массе последнего свой собственный кристалл. Такого рода
параллельный рост двух кристаллов приводит к тому, что возникают кристаллы алит
с включениями, состоящими из мельчайших кристалликов примеси. Растущий кристалл
может захватить и просто механические примеси. Такие тонкодисперсные примеси,
не дающие с основным веществом ни твердых растворов, ни химического соединения,
очень часто наблюдаются в составе кристаллов алита и белита.
При кристаллизации
минералов в стесненных условиях спекающейся гранулы возможны различные
отклонения от рассмотренного общего процесса зарождения и роста кристаллов.
Пористая гранула
обжигаемого материала, образовавшаяся в результате твердофазового спекания, при
появлении жидкой фазы испытывает сильную усадку. В процессе уплотнения гранул в
присутствии расплава различают три стадии:
) перегруппировка
мелких частиц в результате их пластического течения совместно с жидкостью;
) заполнение пор в
результате протекания реакций минералообразования по механизму «растворение -
осаждение»;
) процессы
рекристаллизации, которые могут протекать и без участия расплава.
Основной вклад в
усадку гранул вносит процесс пластической перегруппировки частиц. Он протекает
в результате смачивания частиц жидкой фазой, приводящего к развитию капиллярных
сил, оттягивающих частицы, и под воздействием сил, обусловленных поверхностным
натяжением расплава. Скорость роста контакта между срастающимися частицами,
реагирующими с жидкой фазой (и соответственно скорость усадки), по данным ряда
исследователей, прямо пропорциональна поверхностному натяжению расплава,
коэффициентам диффузии ионов, в расплаве и времени обжига и обратно пропорциональна
радиусу частиц, и температуре. С увеличением размера частиц их спекание
замедляется.
В результате усадки
при жидкофазном спекании формируются гранулы клинкера, имеющие пористость
17-32%. Примерное распределение пор по размерам следующее: более 10 мкм -
30-55%; 1-10 мкм - 15-30%; 0,1-1 мкм - 6-18%; 0,004-0,1 мкм - 15-35%. Кристаллы
минерала C3S размером 10-60 мкм в разрезе имеют форму гексагональных пластин,
а кристаллы C2S размером 10-100 мкм - округлую форму.
При понижении
температуры (охлаждении) спекающихся гранул в них протекают процессы,
оказывающие значительное влияние на свойства клинкера и цемента.
На выходе из печи
клинкер имеет температура 1000-1100 0С, поэтому его надо охладить.
3. ОХЛАЖДЕНИЕ КЛИНКЕРА
Процесс охлаждения клинкера является
одной из наиболее ответственных стадий производства цемента. В зависимости от
того, с какой скоростью охлаждается клинкер, минералогический состав его и
кристаллическая структура могут изменяться в весьма широких пределах.
Клинкерное равновесие. Кристаллизация
расплавов в системах СаО - SiO2 - А12О3 и СаО
- SiO2 - А12О3- Fe2О3
показывает, что изменение состава жидкой и твердой фаз в процессе охлаждения
расплавов, отвечающих по составу портландцементу, имеет очень сложный характер.
Сложность обусловлена тем, что алит выделяется из расплава вначале и в большем,
и в меньшем количестве, чем это соответствует фактическому равновесному
состоянию продукта. В последующем, при очень медленном охлаждении, которое
используется при построении диаграмм состояния, эти аномалии состава расплава и
твердой фазы устраняются: в определенных температурных точках системы в одних
случаях избыточный C3S разлагается, а в других - недостающий C3S
образуется. Система постепенно приходит к равновесному составу. Если же расплав
охлаждать очень быстро, то в клинкере можно зафиксировать избыточное или
пониженное количество алита. Так, при быстром охлаждении клинкера белого
портландцемента (система СаО - SiО2 - А12О3)
от температуры 1450° в продукте содержалось на 10% больше C3S, чем
при медленном равновесном его охлаждении. Наоборот, при быстром охлаждении
клинкера, характеризующегося высоким содержанием железа (глиноземный модуль
равен 0,64), от той же температуры 1450° в продукте содержалось на 12% меньше
алита, чем при равновесном охлаждении.
При обжиге портландцементного
клинкера полного равновесия между жидкой и твердой фазами не наступает.
Во-первых, цементный клинкер в практических условиях обжига плавится всего лишь
на 20-30% и в нем всегда присутствует твердая фаза, и, во-вторых, скорость
охлаждения клинкера в реальных условиях его производства оказывается
значительно, более высокой, чем этого требуют условия достижения равновесия. В
результате того, что расплав клинкера охлаждается не по равновесному режиму,
минералогический состав продукта может в значительной степени изменяться.
Влияние условий охлаждения на
минералогический состав. Практически возможны следующие различные варианты
кристаллизации расплава в клинкерах:
. Расплав в клинкере в
результате медленного охлаждения полностью закристаллизовывается (равновесный
процесс).
. Расплав в клинкере в
результате очень быстрого охлаждения полностью затвердевает в виде стекла.
. Расплав в клинкере
закристаллизовывается в большей или меньшей степени в зависимости от конкретных
условий охлаждения. При этом кристаллизация расплава происходит независимо от
ранее образовавшихся твердых фаз.
Различная степень
закристаллизованности расплава приводит к отклонению расчетного
минералогического состава клинкера от его фактического минералогического
состава и особенно в части содержания минералов C3S, С3А
и С4AF.
При независимой кристаллизации
расплава и при затвердевании его в стекло степень несоответствия расчетного и
фактического минералогического состава клинкера будет определяться величиной
глиноземного модуля последнего.
Согласно данным табл. 3.1, образцы
одного и того же клинкера с р = 2,0, охлажденные по различным режимам,
характеризуются довольно близким содержанием C3S, равным 57,5-
59,6%. Увеличение глиноземного модуля приводит к увеличению различия образцов
клинкера, охлажденных с различной скоростью, по содержанию C3S. Так,
если различие в содержании C3S в быстро и медленно охлажденном
клинкере с р = 2,0 составляет всего лишь 2,1%, то в случае аналогичных образцов
клинкера с р = 3,0 это различие составляет уже 6,1%, а клинкера с р - 3,5
составляет 7,2%.
Таблица 3.1
Влияние режима охлаждения на
изменение минералогического состава
портландцементного клинкера
|
Состав клинкера
|
Наименование фаз
|
Полная кристаллизация
|
Полное затвердевание расплава от 1450 в стекло
|
Самостоятельная кристаллизация расплава от 1450.
|
|
CaO-67%;
|
3CaO∙SiO2
|
62.7
|
55.1
|
61.3
|
|
SiO2-23%;
|
2CaO∙SiO2
|
18.6
|
19.4
|
19.4
|
|
Al2O3-4%;
|
3CaO∙Al2O3
|
0.5
|
0
|
0.5
|
|
Fe2O3-6%;
|
4CaO∙Al2O3∙Fe2O3
|
18.2
|
0
|
18.2
|
|
p=0,66
|
Свободный CaO
|
0
|
0
|
0.6
|
|
KH=0,91
|
12CaO∙7Al2O3
|
0
|
0
|
0
|
|
Стекло
|
0
|
25.5
|
0
|
|
CaO-68%;
|
3CaO∙SiO2
|
57.5
|
59.6
|
59.6
|
|
SiO2-23%;
|
22.6
|
15.6
|
21.0
|
|
Al2O3-6%;
|
3CaO∙Al2O3
|
10.8
|
0
|
9.8
|
|
Fe2O3-3%;
|
4CaO∙Al2O3∙Fe2O3
|
9.1
|
0
|
9.1
|
|
p=2,00
|
Свободный CaO
|
0
|
0
|
0
|
|
KH=0,89
|
12CaO∙7Al2O3
|
0
|
0
|
0.5
|
|
Стекло
|
0
|
24.8
|
0
|
|
CaO-66%;
|
3CaO∙SiO2
|
32.4
|
38.5
|
38.5
|
|
SiO2-24%;
|
2CaO∙SiO2
|
44.5
|
33.3
|
39.9
|
|
Al2O3-7,5%;
|
3CaO∙Al2O3
|
15.7
|
0
|
10.6
|
|
Fe2O3-2,5%;
|
4CaO∙Al2O3∙Fe2O3
|
7.6
|
0
|
7.6
|
|
p=3,00
|
Свободный CaO
|
0
|
0
|
0
|
|
KH=0,79
|
12CaO∙7Al2O3
|
0
|
0
|
3.5
|
|
Стекло
|
0
|
28.1
|
0
|
|
CaO-68%;
|
3CaO∙SiO2
|
52.2
|
59.4
|
59.4
|
|
SiO2-23%;
|
2CaO∙SiO2
|
26.5
|
15.3
|
|
Al2O3-7,0%;
|
3CaO∙Al2O3
|
15.2
|
0
|
9.7
|
|
Fe2O3-2%;
|
4CaO∙Al2O3∙Fe2O3
|
6.1
|
0
|
5.9
|
|
p=3,5
|
Свободный CaO
|
0
|
0
|
0
|
|
KH=0,90
|
12CaO∙7Al2O3
|
0
|
0
|
3.8
|
|
Стекло
|
0
|
25.5
|
0
|
При значениях глиноземного модуля
0,9-1,8 наблюдается соответствие расчетного и фактического содержания в
клинкерах C3S. Понижение значений глиноземного модуля ниже 0,9
приводит, наоборот, к уменьшению фактического содержания в клинкере C3S
по сравнению с его расчетным количеством. Так, в клинкере с р = 0,66 (табл.
3.1) различие в содержании C3S в пробах, охлажденных быстро и
медленно, составляло 7,6%, причем в быстроохлажденном клинкере наблюдалось
пониженное содержание минерала.
При быстром охлаждении клинкера,
когда весь расплав затвердевает в виде стекла, фактический минералогический
состав продукта отличается от расчетного. Во-первых, в быстроохлажденных
клинкерах отсутствуют кристаллические С3А и C4AF (вместо
них присутствует соответствующее количество стекла). Во-вторых, в
быстроохлажденных клинкерах в зависимости от величины их глиноземного модуля
содержится избыточное или недостающее по сравнению с расчетным количество
минералов C3S и C2S. При значениях р = 0,9-1,8 содержание
C3S в быстро и медленно охлажденном клинкере оказывается очень
близким, при р > 1,8 быстро охлажденные клинкеры содержат больше C3S,
чем медленно охлажденные, а при 0,9 - меньше. Соответственно содержание C2S
в быстро охлажденных клинкерах с р> 1,8 оказывается пониженным, а с р <
0,9-повышенным.
Если предположить, что клинкеры с p > 1,8 и p < 0,9 от температуры спекания
охлаждаются таким образом, что вся образовавшаяся в них твердая фаза остается
неизменной, а расплав кристаллизуется самостоятельно, то в клинкерах, несмотря
на полную кристаллизацию в них жидкой фазы, сохранится неравновесное состояние:
) в них сохранится избыточное или
соответственно пониженное количество алита;
) из расплава выкристаллизовывается
в небольшом количестве минерал С6А3, который при обычных
условиях обжига наблюдается в клинкере очень редко;
) оказывается пониженным содержанием
С3А и C4AF, поскольку часть принадлежащей им по расчету
извести пошла на реакцию с C2S с образованием избыточного количества
C3S. Соответственно оказывается пониженным содержание в клинкере и
минерала C2S.
При значениях глиноземного модуля
более 1,8 при расчете минералогического состава клинкера по принятым формулам
необходимо пользоваться следующими поправками:
C3S-(1,8А12O3
-2,8Fe2O3),
С2 S-(2,1 Fe2O
3 - 1,4 А12O3),
С3А-(2,5 Fe2O 3
- 1,6 А12O3).
При охлаждении клинкера со
скоростью, недостаточной для затвердевания всего расплава в стекло и не
обеспечивающей полной как равновесной, так и самостоятельной кристаллизации
жидкой фазы, в продукте будет содержаться некоторое количество стекла и будут
иметь место рассмотренные выше несоответствия фактического и расчетного
минералогического состава.
Влияние скорости охлаждения на
величину и форму кристаллов. Сложность процесса кристаллизации
многокомпонентного расплава дополняется не менее сложным поведением кристаллов
в процессе их охлаждения. Кристаллы при охлаждении продолжают свой рост, вместе
с тем непрерывно идет процесс зарождения новых кристаллов; возникшие кристаллы
стареют, срастаются, разрушаются, вступают, в химические реакции.
При постоянстве температуры
кристаллизации линейная скорость роста кристаллов тем больше, чем больше
скорость охлаждения. Кристаллы алита при их быстром росте оказываются в
состоянии сдвинуть со своего пути лишь незначительные по величине частички
примеси: более крупные им приходится огибать, включая в свой состав.
Следовательно, растущие кристаллы могут «отталкивать» примеси в расплаве лишь
при медленном росте, при быстрой же кристаллизации примеси захватываются
растущими кристаллами и остаются в их решетке в качестве различного рода
включений.
Обход частичек примеси или других
кристаллов является одной из причин, приводящих к появлению в клинкере
дендритообразных кристаллов. Способствует образованию ветвистых кристаллов и
очень быстрое охлаждение расплава.
Первичной кристаллической фазой,
выделяющейся из клинкерного расплава, является алит. Трехкальциевый алюминат и
алюмоферриты кальция кристаллизуются последними, но вследствие высокой
кристаллизационной способности успевают выкристаллизоваться на 70-90 % даже в
условиях охлаждения клинкера в рекуператорных холодильниках. При этом
вследствие быстрого роста кристаллы С3А могут включать в свой состав
мелкие зерна C3S, C2S и СаО, а кристаллы алюмоферритов
кальция - характеризоваться неоднородным составом.
Стабильность отдельных минералов.
Рассматривая влияние режима охлаждения клинкера на его фазовый состав, следует
иметь в виду термодинамическую нестабильность отдельных клинкерных минералов,
наблюдающуюся в определенном интервале температур при охлаждении клинкера.
Основной минерал портландцементного
клинкера ЗСаО•SiO2 стабильно существует лишь в интервале температур
1250-1900°. Ниже и выше этого интервала температур алит разлагается на C2S
и СаО. Наиболее интенсивно процесс разложения C3S протекает при
медленном охлаждении клинкера в пределах температур 1000- 1200°. На степень
распада трехкальциевого силиката, помимо скорости охлаждения, существенное
влияние оказывает состояние его структуры: количество и тип примесей,
растворенных в его решетке, наличие инородных крупнозернистых включений,
характер атмосферы и т. п. Так, процесс разложения C3S ускоряется в
присутствии CaSO4, FeO; каталитически действуют и сами продукты
разложения алита - C2S и СаО. Явление разложения C3S при
медленном охлаждении приводит к уменьшению его количества в клинкере и к
появлению в составе последнего свободного СаО. Кроме того, распад C3S
приводит к появлению в клинкере кристаллов этого минерала с сильно дефектной
структурой: трещиноватых, распавшихся по периферии и содержащих включения по
всей массе.
Двухкальциевый силикат стабилен во
всем интервале температур, который необходим для получения клинкера. Кристаллы
минерала лишь изменяют при определенных температурах константы своей
кристаллической решетки в связи с переходом из одной полиморфной модификации в
другую.
Синтетический С3А также
устойчив в интервале температур 700-1300°, как в окислительной, так и
восстановительной средах. Лишь при очень низких значениях коэффициента
насыщения C2S может разлагать С3А с образованием C3S
и С12А7.
Минералы алюмоферритной фазы при
медленном охлаждении в окислительной среде являются термически стабильными. В
восстановительной же среде они могут распадаться до алюминатов кальция и
свободных окcидов кальция и металлического железа.
4. ИЗМЕЛЬЧЕНИЕ
КЛИНКЕРА
.1 Теоретические основы измельчения в барабанных
мельницах
Существенным
элементом технологии портландцемента является процесс тонкого измельчения
клинкера в барабанных мельницах.(см.рис.4.1) Рассмотрим теоретические основы
работы барабанных мельниц.
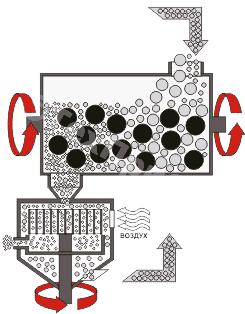
Рис.4.1.Измельчение
цементного клинкера в шаровой мельнице, работающей по закрытому циклу
Работа измельчения
в барабанных мельницах производится шаровой загрузкой - мелющей средой. При
вращении барабана мелющая загрузка за счет сил трения смещается вместе с
корпусом барабана вверх. Высота подъема определяется величиной силы трения
между загрузкой и барабаном.
Различают каскадный
и водопадный (катарактный) режимы движения шаровой загрузки. При каскадном
режиме центр тяжести шаровой загрузки смещается на 35-40° и шары, поднимаясь с
барабаном на некоторую высоту, скатываются по «зеркалу» загрузки. В загрузке
можно выделить три зоны - шары, движущиеся с барабаном, сыпучую среду -
скатывавшиеся шары и «мертвую» зону (в центре дробящей загрузки имеется
область, в которой мелющие тела практически не перемещаются и в измельчении
практически не участвуют). В слоях шаров, поднимающихся вместе с барабаном,
из-за слабого их смещения относительно друг друга измельчение протекает
малоинтенсивно. Наиболее интенсивно измельчается материал в зоне скатывающихся
шаров (в зоне сыпучей среды). Измельчение при каскадном режиме (рис.4.2(а))
осуществляется главным образом за счет истирания и частично раздавливания.
При водопадном
режиме (рис.4.2(б)) шары поднимаются на большую высоту, а затем переходят в
свободный полет и измельчение происходит главным образом за счет ударов
падающих шаров. Кроме того, при водопадном режиме материал измельчается также
раздавливанием и истиранием поднимающихся шаров. Однако почти половина шаровой
загрузки в центре контура дробящей среды неподвижна и эффективно не
используется.
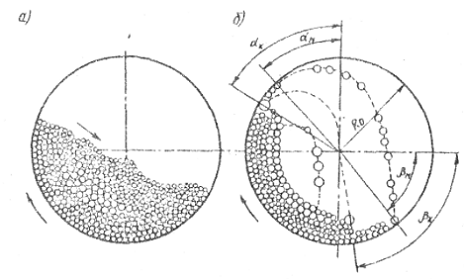
Рис. 4.2 Изменение
высоты подъёма шаров при вращении мельницы (механика мелющей среды): а) при
каскадном режиме; б)-при водопадном режиме; £к - угол отрыва крупных шаров; £м - угол отрыва мелких шаров;
βк - угол падения крупных шаров; βм - угол падения мелких шаров.
Угол подъема шаров
зависит от величины коэффициента заполнения мельницы шарами φ, так как при большом φ растет давление слоя на
шары, соприкасающиеся с барабаном, и увеличивается сила трения. Таким образом,
изменение величины φ в разных камерах мельницы позволяет получить в первой водопадный
режим, а во второй - каскадный. Обычно в камерах осуществляются смешанные
режимы: водопадно-каскадный или каскадно-водопадный. Радиус внутреннего слоя
шаровой загрузки R1 при водопадном режиме
определяют из соотношения:
R1 = k*D0,
где k - коэффициент, зависящий от φ и nраб, a Do - диаметр барабана.
Чем больше R, тем выше nраб/nкр. Для каждого значения nраб/nкр существует
разграничитель - значение k между каскадным и водопадным режимами. В области, близкой к
разграничительным значениям nраб/nкр. и k, существует смешанный режим: часть загрузки работает в каскадном,
а часть - в водопадном режиме.
Рабочая скорость
вращения мельницы п является не только функцией диаметра мельницы, но и
коэффициента заполнения φ.
Если Do= 4 м, а φ = 0,3 (тонкое
измельчение), то n=14 об/мин, а если φ =
0,4 (грубое измельчение), то п = 16 об/мин.
При ударе измельчение
осуществляется только за счет нормальной составляющей силы к поверхности
барабана или к зеркалу шаров. Касательная составляющая в точке удара
способствует смещению шаровой загрузки, в результате которой материал
раздавливается или истирается. При некотором угле отрыва (переходе в свободное
падение) вектор скорости оказывается нормальным к поверхности барабана в точке
падения шара. В этом случае мелющие тела (для слоя, соприкасающегося с
барабаном) имеют максимальную кинетическую энергию. Это способствует углу α≈54°, nраб=
0,75, пкр=32/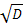
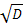 . Если в оптимальные
условия поставить всю мелющую загрузку, то nраб=
0,88 и nкр=37/
. Если в оптимальные
условия поставить всю мелющую загрузку, то nраб=
0,88 и nкр=37/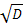
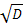 Обычно если в конструкции
мельниц не имеется устройств, повышающих зацепление между шарами и барабаном
(волнистых плит, то для nраб
принимают скорость вращения, лежащую в интервале от 0,75 до 0,88 nкр.
Обычно если в конструкции
мельниц не имеется устройств, повышающих зацепление между шарами и барабаном
(волнистых плит, то для nраб
принимают скорость вращения, лежащую в интервале от 0,75 до 0,88 nкр.
Производительность
мельницы практически пропорциональна потребляемой полезной мощности.
Nуд-nраб/nкр.
Поэтому число оборотов,
при которых Nуд максимальна, должно соответствовать максимально возможной
производительности. Однако nраб
выбирают, исходя из учета достижения минимума расхода мощности на единицу
производительности Nуд.
Потребляемая мельницей мощность возрастает с увеличением коэффициента
заполнения мельницы шарами φ по сложному
степенному закону, причем крутизна отклонения от линейной зависимости заметно
возрастает после значения >30%.
Величина коэффициента
заполнения связана с тонкостью помола. При увеличении коэффициента заполнения
возрастает давление шаровой загрузки (больше высота слоя) на барабан, что
приводит к увеличению коэффициента трения между загрузкой и барабаном и снижает
проскальзывание загрузки по отношению к барабану. Если значение φ
низкое (0,25-0,30), то сила трения между загрузкой и барабаном
невелика и шаровая загрузка проскальзывает. В результате проскальзывания шары
при движении всей нагрузки вверх вращаются, что способствует тонкому помолу.
При φ>0,45 проскальзывание шаровой загрузки
отсутствует, шары при движении не вращаются и измельчения за счет истирания не
происходит, при этом материал будет содержать мало тонких фракций.
Достигаемая в мельницах
тонкость измельчения связана также с соотношением Gш/Gм. Чем выше это соотношение, тем более тонкий продукт выдает
мельница. При этом производительность падает. Достигаемая тонкость измельчения
связана также с величиной «плотности» передаваемой материалу энергии, которая
растет с увеличением диаметра мельницы и массы шара. Однако параллельно
усиливаются агрегация частиц и налипание материала на шары, в связи с чем
начиная с диаметра более 2,8-3,0 м мельницы должны работать в замкнутом цикле,
при котором тонкие фракции материала отсеваются в сепараторе.
Производительность
мельницы выше, если в нее загружены шары разных размеров. В первой камере
предпочтительно измельчение ударом, в последующих - истиранием и
раздавливанием. Для более эффективного использования мелющей загрузки первая
камера должна работать в водопадном режиме, наиболее отвечающем ударному
измельчению, вторая - в каскадном режиме, отвечающем измельчению истиранием.
Первая камера должна быть загружена смесью более крупных шаров, вторая - смесью
более мелких шаров или цильпебсами. За счет подбора коэффициентов заполнения
камер шарами и профиля футеровки. При более высоком коэффициенте заполнения
сцепление загрузки с барабаном и слоев шаров между собой увеличивается, что
способствует работе мельницы в водопадном режиме. При меньшем
φ больше условий для возникновения каскадного режима.
Потребляемая мельницей
мощность расходуется на приведение в движение шаровой загрузки, поэтому важно
подобрать рациональный состав загрузки по гранулометрии и оптимальные значения
коэффициента заполнения шарами отдельных камер. Мелющая загрузка состоит из
шаров d=120-30 мм и цилиндрических тел d
= 18, 25, 30 мм и l= 25-40 мм. В
зависимости от диаметра в 1 т содержится от 240 шаров (d=100
мм) до 9000 (d = 30 мм). При укладке шаров по системе плотной тетраэдрической
упаковке объем пустот между шарами соответствует 30%, при укладке по плотной
кубической упаковке - 48%, при случайной укладке - 38%. Таким образом, для
шаровой загрузки характерна пустотность, оцениваемая в 38-40%. Объемную массу
шаров принимают равной 4800 кг/м3, а цильпебса - 4400-4500 кг/м3.
Оптимальный диаметр шара
dmax связан со свойствами измельченного
материала. Для случая измельчения материала (kp-
коэффициент размалываемости) со средним размером зерен, равным 10 мм,
зависимость dопт от свойств материала.
Для оптимальных условий
работы мельниц необходимо, чтобы количество находящегося в мельнице материала
было достаточно для заполнения всех пустот в мелющей загрузке и образования
слоя материала над «зеркалом» загрузки в 2-3 см. Это достигается при φш=0,3
и доле пустот между шарами, равной ~0,4 (φм=
φш* 0,4 = 0,3-0,4 = 0,12).
.2 Особенности измельчения клинкера
Для получения цемента
клинкер размалывают в тонкий порошок.
В мельницу можно
подавать клинкер, температура которого не превышает 323 К. Температура же
клинкера после холодильника колеблется от 323 до 423 К. При работе на горячем
клинкере падает производительность мельниц, увеличивается износ брони и мелющих
тел. Цемент также имеет слишком высокую температуру, затрудняющую отгрузку.
Помол горячего клинкера может привести к дегидратации двуводного гипса, и
мельница при этом выдаст «ложный быстряк». Поэтому клинкер выдерживают на
складе, что обеспечивает гашение свободной извести, улучшающее качество
цемента, частичный переход β-C2S в γ-С2S и кристаллизацию
клинкерного стекла. Оба эти процесса делают клинкерные гранулы менее прочными,
и вылежавшийся клинкер легче размалывается. Вылеживание клинкера замедляет
сроки схватывания цемента.
При обжиге различных по
составу шихт образуется переменное количество расплава (15-20%) неодинаковой
вязкости. В результате в печи образуются гранулы клинкера, различные по
размерам - от 5 до 80 мм, что сказывается как на загрузке мельницы мелющими
телами, так и в целом на ее работе. Размалываемость клинкера зависит от его
минералогического состава и режима охлаждения. Трудно размалываются клинкеры с
высоким содержанием белита и алюмоферрита, что связано с высокой твердостью
кристаллов этих минералов. Плохая размалываемость белита связана также с
повышенным налипанием материала на мелющие тела. Гранулы клинкера тем прочнее,
чем больше при спекании образуется расплава, поэтому хорошо размалывается клинкер
с повышенными значениями кремнеземного модуля. При увеличении глиноземного
модуля прочность гранул клинкера падает. Резкое охлаждение клинкера дает
хорошие результаты.
Для нормальной работы
мельницы необходима аспирация - вентиляция мельничного пространства прососом
воздуха. При аспирации из мельницы удаляются наиболее тонкие частицы, чем
предотвращаются налипание материала на мелющие тела и падение
производительности мельниц. С аспирацией воздухом удаляется до 100-300 г
готового продукта на 1 м3 воздуха. Если скорость измельчение
материала в мельницах прямо пропорциональна количеству крупного материала,
находящегося в единице объема в зоне разрушения, то аспирация, тем самым
повышая производительность мельницы.
Тепловой режим в
мельнице регулируют аспирацией и вдуванием в мельницу тонкоразбрызганной воды.
Аспирация понижает
температуру цемента и уменьшает нагревание корпуса мельницы. При недостаточной
аспирации температура в мельнице может повысится до 433-450К, а температура
цемента - до 393-413К, что приводит к дегидратации гипса, нарушению сроков
схватывания цемента и получению «ложного быстряка». Содержащаяся в материале
влага превращается в пар за счет тепла, выделяющегося при помоле.
На испарение введенной
воды затрачивается заметное количество тепла, вследствие чего предотвращается
чрезмерный разогрев цемента. Введение тонкораспыленной воды не только снижает
температуру в мельнице, но и улучшает условия размола. Образующаяся смесь
водяного пара и воздуха удаляется из мельницы через аспирационную систему. В
зависимости от размеров мельницы и режима ее работы количество вдуваемой воды
составляет 0,5-1,5% от количества вырабатываемого цемента. Если распыляется
воды 2-3% от массы измельчаемого материала, то можно уменьшить объем
аспирационного воздуха на 25-50%. Форсунка устанавливается в камере тонкого
измельчения (против движения материала) и сблокирована с питателем мельницы.
Количество подаваемой воды оптимизируется по влагосодержанию аспирационного
воздуха.
При тонком измельчении
клинкера, начиная с некоторой тонкости материала нарушается пропорциональность
между затрачиваемой энергией и приростом новых мельчайших частиц. Считают, что
одной из причин агрегирования частиц является их электризация. Агломерацию
тонких частиц можно уменьшить, увеличив электропроводность воздушной среды в
мельнице. Для этого в мельницу вводят с распыляющей водой электролиты или
органические кислоты.
Значительную роль в
интенсификации измельчения играют ПАВ, применение которых предотвращает
агрегацию образующихся тонких частиц в процессе помола, в явлениях
адсорбционного понижения прочности, а также предотвращает налипание тонких
частиц на мелющие тела. Кроме того, введение ПАВ в мельницу повышает
подвижность (текучесть) материала при продвижении его по мельнице. В этом случае
улучшаются и свойства цемента: повышается аэрируемость (пневмотранспорт,
пневморазгрузка), уменьшается слеживаемость, предотвращается снижение
активности при хранении. Однако при этом увеличивается пыление при помоле и
транспортировке и возникают затруднения при упаковке цемента в тару
(замедляется темп работы упаковочных машин). В качестве ПАВ при измельчении
клинкера используют препараты на основе:
а) аминов -
триэтаноламин, ацетилированный этаноламинацетат; иногда эти вещества смешивают
в определенной пропорции с растворимой кальциевой солью лигносульфоновой
кислоты;
б) гликолей -
этиленгликоля, пропиленгликоля, полигликолей.
Степень разделения
материала в сепараторе и величина циркуляционной нагрузки взаимосвязаны. При
степени разделения материала в сепараторе, равной 100%, циркуляционная нагрузка
содержит только крупные фракции. С увеличением циркуляционной нагрузки степень
разделения ухудшается. При подаче в сепаратор материала, в котором содержание
мелких фракций несколько меньше, чем в готовом продукте, и высока
циркуляционная нагрузка, степень разделения будет низкой. Для поддержания
высокой циркуляционной нагрузки и сохранения высокой степени разделения не
следует стремиться к очень тонкому измельчению материала, подвергаемого затем
сепарации.
Величина циркуляционной
нагрузки связана с необходимой тонкостью. Так, при выпуске цемента с Sуд=300 м2/кг. Нагрузка снижается до 75%, а при выпуске
цемента с Sуд = 400 м2/кг возрастает до 200%. Необходимая тонкость
цемента по схеме а достигается при циркуляционной нагрузке в 150-200% и подаче
на сепарацию материала с syд=150-200
м2/кг. Увеличение циркуляционной нагрузки повышает
производительность при одновременном снижении удельной поверхности готового
продукта. Повышение дисперсности достигается перенастройкой сепаратора, но при
этом падает соответственно производительность установки.
Мелющая загрузка в
мельницах, работающих в установках замкнутого цикла измельчения, должна
обеспечивать более высокую пропускную способность через мельницу измельчаемого
материала и повышение «плотности» энергии единичного удара. И то и другое
достигается увеличением диаметра шаров в первой камере, увеличенным
коэффициентом заполнения φ в первой камере и понижением φ во
второй, заменой цильпебса во второй камере шарами d=40-30
мм.
Производительность
барабанных мельниц в значительной степени определяется крупностью питания.
Оценка показала, что рационально питание мельниц крупкой клинкера с
максимальной крупностью 3-5 мм. Подача в мельницу материала такой крупности
позволяет повысить производительность установки на 20-40% или тонкость готового
продукта на 100-120 м2/кг при сохранении производительности
мельницы.
После мельницы цемент направляют в
силос, являющимся буферным складом, обеспечивающим хранение готовой продукции
при условии периодичности отгрузки. В процессе хранения гасится свободный СаО,
что улучшает свойства цемента.
ЗАКЛЮЧЕНИЕ
В данной курсовой работе были
рассмотрены физико-химические основы измельчения.
Для получения портландцемента
необходимо полностью соблюдать все тепловые режимы, протекающие в производстве.
Список
использованной литературы
1. Бутт, Ю.М. Химическая технология вяжущих материалов/ Ю.М. Бутт,
М.М Сычев, В.В. Тимашев. - М.: Высш. школа, 1980. - 472с.
. Технический контроль в производстве тугоплавких неметаллических
и силикатных материалов и изделий: учеб. пособие/ Под ред. Н.Ф. Косенко. -
Иваново: Иван. гос. хим-технол. ун-т, 2002. - 265 с.
. Рояк, С.М. Специальные цементы/ С.М. Рояк, Г.С. Рояк - М.:
Стройиздат, 1983. - 279с.
4. Таймасов, Б.Т. Технология производства
портландцемента/ Б.Т.Таймасов, Б.О.Есимов - Учеб. пособие. - Шымкент, Изд-во
ЮКГУ, 2003. - 297 с.