|
Кислая
область рН
|
Изоэлектрическая
точка
|
Щелочная
область рН
|
|
Суммарный
заряд положительный
|
Суммарный
заряд равен нулю
|
Суммарный
заряд отрицательный
|
|
Движение
к катоду
|
Движения
нет
|
Движение
к аноду
|
Таким образом, фактором, определяющим поведение
белка как катиона или аниона, является реакция среды, которая определяется
концентрацией водородных ионов и выражается величиной рН. Однако при определенных
значениях рН число положительных и отрицательных зарядов уравнивается и
молекула становится электронейтральной, то есть она не будет перемещаться в
электрическом поле. Такое значение рН среды определяется как изоэлектрическая
точка белков. При этом белок находится в наименее устойчивом состоянии и при
незначительных изменениях рН в кислую или щелочную сторону легко выпадает в
осадок. Для большинства природных белков изоэлектрическая точка находится в
слабокислой среде (рН 4,8-5,4), что свидетельствует о преобладании в их составе
дикарбоновых аминокислот. [14]
Белки активно вступают в химические реакции. Это
свойство связано с тем, что аминокислоты, входящие в состав белков, содержат
разные функциональные группы, способные реагировать с другими веществами.
Важно, что такие взаимодействия происходят и внутри белковой молекулы, в
результате чего образуется пептидная, водородная, дисульфидная и другие виды
связей. К радикалам аминокислот, а, следовательно, и белков, могут
присоединяться различные соединения и ионы. [11]
Белки обладают большим сродством к воде, то есть
они гидрофильны. Это значит, что молекулы белка, как заряженные частицы,
притягивают к себе диполи воды, которые располагаются вокруг белковой молекулы
и образуют водную или гидратную оболочку. Эта оболочка предохраняет молекулы
белка от склеивания и выпадения в осадок. Величина гидратной оболочки зависит
от структуры белка. Например, альбумины более легко связываются с молекулами
воды и имеют относительно большую водную оболочку, тогда как глобулины,
фибриноген присоединяют воду хуже, и гидратная оболочка и них меньше. Таким
образом, устойчивость водного раствора белка определяется двумя факторами:
наличием заряда белковой молекулы и находящейся вокруг нее водной оболочки. При
удалении этих факторов белок выпадает в осадок. Данный процесс может быть
обратимым и необратимым. [15]
Обратимое осаждение белков (высаливание)
предполагает выпадение белка в осадок под действием определенных веществ, после
удаления которых он вновь возвращается в свое исходное (нативное) состояние.
Для высаливания белков используют соли щелочных и щелочноземельных металлов
(наиболее часто в практике используют сульфат натрия и аммония). Эти соли
удаляют водную оболочку (вызывают обезвоживание) и снимают заряд. Между величиной
водной оболочки белковых молекул и концентрацией солей существует прямая
зависимость: чем меньше гидратная оболочка, тем меньше требуется солей. Так,
глобулины, имеющие крупные и тяжелые молекулы и небольшую водную оболочку,
выпадают в осадок при неполном насыщении раствора солями, а альбумины как более
мелкие молекулы, окруженные большой водной оболочкой - при полном насыщении. [7]
1.3 Гидратация белков
В зависимости от количества воды растворимые
белки животных тканей могут находиться в состоянии золя или геля, нерастворимые
белки - только в состоянии геля. В клетках животных тканей существуют твёрдая и
жидкая фаза. В составе твёрдой фазы находятся структурные белки, вообще не
растворимые (белки типа коллагена и эластина), а частью хотя и растворимые в
иных условиях, но остающиеся в состоянии геля при условиях, существующих в
клетке (например, актин и миозин мышечной ткани).
В связи с посмертными изменениями клеток в
твёрдую фазу переходит некоторая часть белков, которые при жизни находились в
жидкой фазе. Например, в процессе развития посмертного окоченения часть белков
саркоплазмы мышечной ткани образует гель.
Белковые вещества в водной среде являются
многовалентными амфотерными электролитами, поэтому характер их взаимодействия с
водой зависит от активной реакции среды.
В животных белках носители кислых функций -
остатки аминокислот, содержащих карбоксильные группы (аспарагиновой и
глутаминовой кислот); носители основных функций - остатки аминокислот,
содержащих аминогруппы (аргинина, лизина, гистидина). Эти группы определяют
зарядность молекулы и легко доступны для взаимодействия с ионами электролитов
(в том числе и с Н+ и ОН- ионами).
Они также обуславливают способность белковых
молекул к взаимодействию друг с другом с образованием более крупных ассоциатов.
Изменение реакции среды в кислую сторону от
изоэлектрической точки подавляет кислотную диссоциацию белков и они выступают
как основания, неся на себе положительные заряды
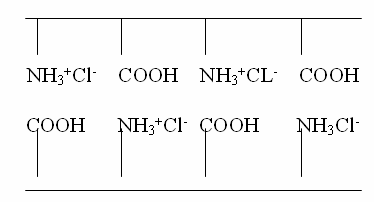
Сдвиг реакции среды в щелочную сторону вызывает
противоположные последствия
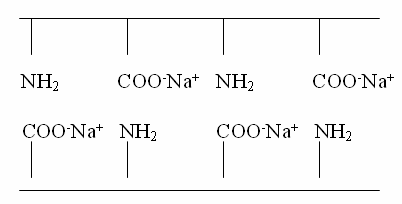
В обоих случаях способность белков мяса к
гидратации возрастает в связи с увеличением числа заряженных групп по мере
сдвига реакции среды.
Минимальная гидратация имеет место, когда число
групп одного заряда в белковой молекуле становится равным числу групп
противоположного заряда, т. е. когда суммарный заряд равен нулю и наступает
изоэлектрическое состояние белка. При этом кислотные и основные группировки
белковых молекул взаимно блокируются и роль гидрофильных центров играют лишь
другие полярные группы (полярные группы цистина, цистеина, серина, метионина,
тирозина, триптофана, оксипролина).
Кислотная и основная диссоциация белков
отличаются по величине, а число кислых и основных групп в белковой молекуле
неодинаково. Большинство белков животных тканей обладают явно выраженными
кислыми свойствами и более высокой константой диссоциации их в сравнении с
основными. Поэтому изоэлектрическое состояние этих белков наступает в кислой
среде:
Белки
Изоэлектрическая точка при рН
Миозин…………………………………… 5,1
Актин………………………………………4,7
Глобулин - Х……………………………...5,2
Миоген…………………………………….6,5
Коллаген …………………………………. 6,36 - 6,75
Желатин…………………………………... 4,5 - 5,5
Альбумин сывороточный………………...4,6
Глобулин сывороточный………………… 4,8 - 6,4
Гемоглобин сывороточный………………6,7
Фибриноген……………………………….6,4
Изоэлектрическая точка белков мышечного волокна
лежит в границах рН 5,2 - 5,5, в среднем при рН 5,3.
В отсутствии солей при изоэлектрическом значении
рН растворимые белки не только наименее гидратированы, но и наименее
растворимы.
Кислоты и щёлочи при действии на белковые
вещества, кроме изменения их растворимости за счёт изменения зарядности
молекул, могут вызывать таутомерные превращения пептидных связей и образование
нерастворимых в воде ацидальбуминов и алкалиальбуминов.
В присутствии нейтральных солей щелочных и
щелочноземельных металлов гидратация и растворимость белковых веществ
изменяются. Характер действия этих солей зависит от их химической природы и
концентрации. Неорганические ионы в той или иной мере и форме взаимодействуют с
белками. В разбавленных растворах (0,1 - 0,6 М) с ионами солей щелочных и
щелочноземельных металлов, прежде всего, реагируют наиболее активные группы белковых
молекул: аминные и карбоксильные группы боковых цепей, не участвующие в
образовании внутримолекулярных связей. При этом водородные и гидроксильные ионы
вытесняются в раствор.
Катионы и анионы нейтральных солей чаще
связываются в неодинаковых количествах. Когда в основном фиксируется катион,
раствор незначительно подкисляется вследствие преимущественного вытеснения
гидроксильных ионов, при адсорбции аниона - наоборот
Пептидные группы главных цепей обладают слабо
выраженными амфотерными свойствами и также, по-видимому, связывают
неорганические ионы. Предполагается, что эти группы способны образовывать
резонансные формы.
Общее количество ионов электролитов, связываемых
белками, велико. Оно в 10 - 20 раз меньше кислотной ёмкости белка.
При неодинаковом количестве катионов и анионов,
фиксируемых белком в разбавленных растворах, соотношение зарядов разного знака
в белковой частице меняется. Изоэлектрическое состояние белка достигается при
ином значении рН, т. е. происходит сдвиг изоэлектрической точки в ту или иную
сторону. В большинстве случаев, но не всегда, для белков животных тканей
изоэлектрическая точка сдвигается в кислую сторону.
Если белок присоединяет к себе такое количество
катионов, которое достаточно для уравновешивания избыточных отрицательных
зарядов в молекуле белка, он переходит в изоэлектрическое состояние, а его
гидратация и растворимость достигают минимума.
Если при преимущественном фиксировании иона
начинают преобладать заряды одного знака над другим, гидратация и растворимость
белка увеличиваются как в изоэлектрической точке, так и при отклонении в любую
сторону от неё. Так, например, повышение концентрации ионов калия или натрия
сверх необходимой для достижения изоэлектрического состояния миозина приводит к
повышению его гидратации и растворимости соответственно увеличению концентрации
электролита. При концентрации около 0,6 М достигается максимум растворимости
актина и миозина.
В растворах электролитов (нейтральных солей
щелочных и щелочноземельных металлов) каждая группа белковой молекулы с
адсорбированными на ней ионами оказывается окружённой слоем ионов
противоположного знака так что общий заряд всей частицы становится равен нулю,
а полярные группы её несут на себе двойной электрический слой ионов
электролита. Этот слой, взаимодействуя с диполями воды, повышает гидратацию
белковых частиц и стабилизирует белок в растворе.
Растворимость белка увеличивается соответственно
возрастанию ионной силы раствора электролита (в особенности ионов с зарядом
больше единицы). Логарифм растворимости возрастает пропорционально ионной силе
раствора. При этом действие одновалентных анионов эффективнее двухвалентных, а
двухвалентных катионов эффективнее действия одновалентных.
Соотношение количеств фиксируемых белками ионов
зависит не только от природы белка, но и от вида соли. Из растворов хлористых
солей кальция, бария, калия адсорбируются преимущественно катионы, а из
растворов оксалатов, роданатов и пирофосфатов - анионы.
Растворимость многих белков растёт с повышением
температуры, но бывает и наоборот, например, растворимость сывороточного
альбумина, инсулина уменьшается. При повышении температуры гидратация белковых
молекул, как правило, уменьшается вследствие повышения интенсивности теплового
движения молекулы воды, удерживаемых молекулярно-силовым полем гидрофильных
центров белковых молекул.
Фиксации ионов электролитов белковой молекулой
сопутствует пептизирующий эффект. Он заключается в нарушении тех
межмолекулярных связей, которые являются центрами фиксации ионов и осуществляют
межмолекулярное взаимодействие белков.
В концентрированных растворах солей щелочных и
щелочноземельных металлов, как правило, гидратация белков уменьшается и
большинство растворимых белков высаливается из растворов. Это происходит в
результате понижения активности молекул воды, связываемых силовым полем ионов.
Благодаря этому ослабляется взаимодействие между молекулами воды и полярными
группами белковой молекулы.
Характер действия ионов солей щелочных и
щелочноземельных металлов в разбавленных и концентрированных растворах определяется
их способностью к взаимодействию с полярными группами белковых молекул и
диполей воды. Ионы, способные к сильной гидратации и характеризующиеся слабой
адсорбируемостью полярными группами белков (например SO42-,
CO32-),
обладают сильным обезвоживающим действием. Ионы, хорошо взаимодействующие с
заряженными центрами белковой молекулы, и сами менее склонные к гидратации, в
умеренных концентрациях увеличивают гидратацию и растворимость белков.
По характеру влияния неорганических солей на
гидратацию и растворимость животных белков их можно разбить на три группы. [16]
1. Соли, вызывающие высокую гидратацию
белков. К ним можно отнести соли бария, кальция, магния. Они вызывают сильное
набухание коллагена, сопровождающееся резким укорочением и утолщением коллагеновых
волокон и снижением температуры сваривания коллагена. В концентрированных
растворах этих солей коллаген сваривается при комнатной температуре. В их
присутствии золи желатина не застудневают.
2. Соли, не вызывающие резких изменений
способности белков к гидратации. Это такие, как хлористый натрий, хлористый
калий. Они в умеренных концентрациях несколько повышают гидратацию и
способствуют растворению белков, а в высоких - вызывают неполное их
обезвоживание.
. Соли с невысокой адсорбируемостью, но с
большим обезвоживающим действием. К ним относятся сульфаты и (в меньшей
степени) карбонаты. В концентрированных растворах этих солей происходит сильное
обезвоживание белков. Насыщенные растворы сульфатов осаждают желатин и
применяются для выделения клея из клеевых бульонов. Сульфаты используются для
усиления обезвоживающего действия рассолов при консервировании шкур.
Белковые вещества с различными катионами и
анионами способны образовывать плохо растворимые соли, а с другими белками и
нуклеиновыми кислотами - комплексы. Для этого необходимо, чтобы
взаимодействующие молекулы несли противоположные заряды в области рН, лежащей
между их изоэлектрическими точками. В образовании таких комплексов существенная
роль принадлежит водородным связям.
Органические соли способны вызывать пептизацию
белковых комплексов. Пептизирующее действие возрастает в такой
последовательности: янтарная кислота → лимонная → винная →
молочная → щавеливая → пропионовая.
Нагревание белков в водной среде до достаточно
высокой температуры, специфичной для каждого белка, приводит к их денатурации.
Она сопровождается изменением гидрофильных свойств белков. Уменьшается
гидратация и резко падает растворимость, особенно вблизи изоэлектрической
точки, в результате агрегирования белковых частиц за счёт межмолекулярных сил.
Изоэлектрическая точка белков смещается в щелочную сторону. [17]
1.4 Влияние температуры и рН на свойства
белков мышечной ткани
1.4.1 Влияние температуры на свойства белков
Структура молекул белков сравнительно легко
изменяется при воздействии различных физических и химических факторов, при этом
теряется ряд первоначальных свойств, и прежде всего растворимость белков. Это
явление получило название денатурации. Под влиянием теплоты, ультразвука,
ультрафиолетового и ионизирующего излучений, высокого давления, при воздействии
солей тяжёлых металлов и других химических веществ происходит поверхностная
денатурация белковых молекул - изменение нативной пространственной четвертичной
структуры, не сопровождающееся разрывом ковалентных связей. При этом
развёртывается в пространстве спираль полипептидной цепочки и образуется
беспорядочный клубок. В зависимости от степени денатурации могут разрушаться
также вторичная и третичная структуры белка, что приводит к потере
биологической активности. Денатурация белков происходит в присутствии воды.
При тепловой денатурации (60 - 100о
С) белки теряют способность растворяться в воде, растворах солей и органических
растворителях, снижается и их способность к набуханию. Изменение белка при
тепловой денатурации тем значительнее, чем выше температура и продолжительность
нагревания, причём белок в водном растворе денатурирует быстрее, чем в
высушенном состоянии.
Денатурация белков играет важную роль при
изготовлении колбасных изделий, производстве кормовой муки, сушке яичного
порошка, крови и кровепродуктов, варке мяса, стерилизации мясных баночных
консервов.
Изменения белка мяса при тепловой обработке
влияют на технологические и качественные показатели готовых изделий. [3]
Деструкция белков. При длительной тепловой
обработке белки подвергаются более глубоким изменениям, связанным с разрушением
их макромолекул. На первом этапе изменений от белковых молекул могут
отщепляться функциональные группы с образованием таких летучих соединений, как
аммиак, сероводород, фосфористый водород, углекислый газ и др. Накапливаясь в
продукте, они участвуют в образовании вкуса и аромата готовой продукции. При
дальнейшей гидротермической обработке белки гидролизуются, при этом первичная
(пептидная) связь разрывается с образованием растворимых азотистых веществ
небелкового характера (например, переход коллагена в глютин). Деструкция белков
может быть целенаправленным приемом кулинарной обработки, способствующим
интенсификации технологического процесса (использование ферментных препаратов
для размягчения мяса, ослабления клейковины теста, получение белковых
гидролизатов и др.).
1.4.2 Влияние рН на свойства белков
Кислотность (рН), обусловленная наличием ионов
водорода, является важным показателем качества мяса. Данный показатель всегда
возрастает после убоя. Показатель рН мяса влияет на его микроструктуру,
развитие микрофлоры, интенсивность процессов гниения и аутолитические изменения
после убоя, а в конечном итоге на органолептические характеристики и
способность кулинарной переработки.
Сдвиг рН мяса в кислую сторону запускает
механизм превращений миофибриллярных белков:
изменяется проницаемость мембран миофибрилл;
ионы кальция выделяются из каналов
саркоплазматического ретикулума, концентрация их возрастает;
ионы кальция повышают АТФ-азную активность
миозина;
глобулярный Г-актин переходит в фибриллярный
(Ф-актин), способный вступать во взаимодействие с миозином в присутствии
энергии распада АТФ;
энергия распада АТФ инициирует взаимодействие
миозина с фибриллярным актином с образованием актомиозинового комплекса.
Результатом сокращения является нарастание
жёсткости мяса, уменьшение эластичности и уровня водосвязывающей способности.
Уменьшение гидратации белков влияет на жесткость
мяса, поскольку рН мышечной ткани приближается к рН изоэлектрической точки
основных белков. Наибольшая жесткость мяса наблюдается при рН = 5,5. При
смешении рН в любую сторону от изоэлектрической точки белков увеличивается
нежность мяса. Смещение рН приводит к расклиниванию полипептидных цепей
отдельных белков, увеличению гидрофильных центров и соответственно росту
влагопоглощающей способности мяса. [5]
.5 Влияние экзогенного кальция на свойства
белков
.5.1 Структурные изменения мышечной ткани
под действием различных концентраций лактата
кальция
В
последние годы большое внимание уделяется использованию молочной кислоты и ее
солей при выработке широкого ассортимента мясных продуктов для придания им
различных потребительских свойств, в том числе для повышения стойкости
продуктов при хранении и увеличения сроков их годности. Однако имеющаяся
информация посвящена главным образом исследованию воздействий на продукты,
прошедшие тепловую обработку. В связи с этим изучение механизма действия и
возможностей целенаправленного изменения процессов, протекающих при обработке мясного
сырья солями молочной кислоты, позволит выявить их потенциальные свойства и
способность сохранения качества мясных продуктов.
Ранее было
показано, что обработка парного мяса рассолом, содержащим 100 ммоль СаС12,
ускоряет процесс деградации белков цитоскелета, ответственных за нежность мяса,
и тем самым способствует более быстрой тендеризации мышечной ткани (за трое
суток).
Целью
настоящей работы было изучение структурных изменений мышечной ткани и ее белков
под действием различных концентраций лактата кальция.
Объект
исследований - длиннейшая мышца спины говядины I категории упитанности с рН
5,74. Через 1-1,5 ч с момента убоя животного парное мясо подвергали жиловке с
отделением видимой жировой и соединительной ткани.
Для
проведения опытов отбирали образцы мышечной ткани массой 500 г, которые
шприцевали соответствующими рассолами в количестве 15 % от массы мяса. Были
исследованы образцы мышечной ткани, обработанные 10%-ным рассолом в отсутствие
или в присутствии лактата кальция в интервале концентраций от 4 до 100 ммоль.
Образцы, обработанные таким образом, хранили при 4±2 °С в течение 120 ч. Через
каждые 24 ч от каждого образца отбирали пробы для исследований с помощью
микроструктурного анализа и дифференциально-сканирующей микрокалориметрии.
В результате
проведенных исследований микроструктуры мышечной ткани контрольных и опытных
образцов установлено, что с увеличением концентрации экзогенного кальция
выраженность деструктивных процессов возрастала.
Наибольшую
глубину деструкции мышечной ткани отмечали при использовании ионов кальция в
концентрации, равной 100 ммоль. Уже через 72 ч хранения в мышечных волокнах
наблюдали множественные микротрещины, а к 96 ч - гомогенизацию, разрыхление
миофибрилл в мышечных волокнах и множественный распад их по Z-пластинам. При созревании мяса в
таких условиях к 120 ч инкубации деструктивные процессы принимали
распространенный характер, охватывая основную массу мышечных волокон в образце,
в то время как в контрольных образцах нарушение целостности мышечных волокон к
120 ч хранения носило локальный характер. Необходимо отметить, что обработка
мышечной ткани рассолами, содержащими лактат кальция, приводила к нарушению
структуры Z-линий, служащих опорным аппаратом
саркомеров, их гомогенизации и деструкции. Отмеченные изменения в конечном
итоге лежали в основе нарушения целостности волокон и обусловили ускорение
процесса автолиза и повышение нежности мяса по сравнению с контрольными
образцами.
Термодинамические
характеристики мышечных белков исследовали с помощью современного метода -
дифференциально-сканирующей микрокалориметрии. Наиболее информативным
параметром, описывающим структурную и температурно-денатурационную стабильность
белков мышечной ткани, служит зависимость температуры середины денатурационных
переходов от времени хранения посоленных образцов. Ранее было показано, что
ионы кальция действуют в первую очередь на миофибриллярные структуры и
индуцируют деструкцию цитоскелетных белков. Первый денатурационный переход,
вероятнее всего, отражает изменения в структурно-денатурационной стабильности
белков цитоскелетного матрикса. Второй переход обусловлен в основном
изменениями в структурно-денатурационной стабильности белков актомиозинового
комплекса. По мнению этих же авторов, третий переход можно отнести к тепловой
денатурации соединительнотканных белков и коагуляции мышечных белков.
Были
исследованы изменения температуры в середине необратимых денатурационных
переходов для образцов, обработанных рассолом, содержащим разные концентрации
лактата кальция в течение 120 ч. Температуры рассчитывали по гауссовым кривым,
описывающим каждый необратимый переход. Этот параметр отражает изменение
структурной стабильности белков мышечной ткани.
При
хранении образцов мяса, обработанных 10%-ным рассолом без лактата кальция
(контроль), выявляли постепенное понижение температуры первого денатурационного
перехода с 58°С при 24 ч посола до 55°С после 120 ч посола. Это свидетельствует
о постепенном уменьшении термостабильности и структурной стабильности
миофибриллярных белков в процессе автолиза посоленного мяса. Изменение
температур второго и третьего денатурационных переходов в этих образцах не
обнаружено даже после 120 ч хранения.
Обработка
мясного сырья рассолом, содержащим 4 ммоль лактата кальция, приводит к
аналогичному уменьшению температуры первого денатурационного перехода, как и в
контроле. В то же время в присутствии 4 ммоль лактата кальция обнаруживается
уменьшение температуры второго денатурационного перехода с 69,5 до 65 °С. Это
может свидетельствовать о деструктивном действии такой концентрации ионов
кальция на белки актомиозинового комплекса. Третья денатурационная компонента в
данном случае не претерпевает изменений.
Наиболее
показательны изменения термодинамических характеристик в случае обработки
мышечной ткани 10%-ным рассолом в присутствии 100 ммоль лактата кальция.
Температура первого денатурационного перехода снижается с 60,6 °С через 24 ч
хранения до 55,5 °С через 120 с. Изменение температуры второго денатурационного
перехода носит такой же характер (69 °С при 24 ч, 64 °С при 120 ч посола).
Температура третьего перехода, отражающего тепловую денатурацию
соединительнотканных белков и переход всех мышечных белков в коагулированное
состояние, также понижается с 77 °С (24 ч посола) до 72 °С (120 ч посола).
Таким
образом, методом микроструктурного анализа установлено, что наибольшая глубина
деструкции мышечной ткани отмечается при использовании 10%-ного рассола,
содержащего 100 ммоль лактата кальция, введенного в сырье в количестве 15 % к
исходной массе. К 96 ч хранения в мышечных волокнах обнаруживаются
множественные микротрещины, гомогенизация, разрыхление миофибрилл и
множественный распад их по Z-пластинам.
Микрокалориметрические исследования мышечной
ткани показали, что структурная стабильность и термостабильность белков мышечной
ткани, обработанной 10%-ным рассолом, содержащим 100 ммоль лактата кальция,
значительно ослабляются по сравнению с контрольными образцами. [18]
.5.2 Влияние экзогенных ионов кальция на
деструкцию мышечной ткани post
mortem
Нежность
текстуры мясного сырья определяется общей суммой механического напряжения
мышечной ткани и ее ослабления в процессе послеубойного созревания. Стадии
созревания и соответственно тендеризации (повышения нежности) мяса при его
технологической обработке длятся достаточно долго: от 3-4 недель до 10-14 дней
для говядины, 7-10 дней для баранины и 5-6 дней для свинины.
Для
сокращения времени созревания и улучшения нежности мяса необходима разработка
технологического режима, включающего стадии предотвращения/минимизации
жесткости и ускорения/повышения тендеризации мясного сырья.
Тендеризация
мяса проходит в две стадии - быструю и медленную. В быстрой стадии происходит
структурное ослабление миофибрилл, а в медленной - структурное ослабление
эндомизия и перимизия. Основные факторы, влияющие на послеубойную модификацию
миофибрилл, - ослабление Z-дисков,
разрушение актомиозинового комплекса, расщепление коннектиновых филаментов и
фрагментация небулиновых филаментов.
Процесс
тендеризации, вероятнее всего, включает два вида механизмов. Первый из них
обусловлен протеолизом мышечных белков, который до сих пор считается первичным
и основным механизмом. Другой механизм - физико-химический, рассматривает
значительное увеличение осмотического давления в клетках мышечной ткани post mortem как причину существенных изменений в структуре
миофибрилл и ее ослабления.
В качестве
еще одного физико-химического механизма была предложена «кальциевая теория»
тендеризации. На основе многочисленных экспериментальных данных были
сформулированы основные ее постулаты:
уровень Са2+
в саркоплазме вполне достаточен для ослабления Z-дисков и ригорных сшивок;
в
присутствии 0,1 мМ Са2+ происходят расщепление коннектиновых
филаментов, фрагментация небулиновых филаментов и деполимеризация промежуточных
(десминовых) филаментов;
увеличение
концентрации Са2+ в мышечной ткани ускоряет процессы созревания и
тендеризации мяса.
К
настоящему времени опубликованы экспериментальные данные, подтверждающие
влияние экзогенных ионов Са2+ на скорость процессов созревания и
тендеризации мяса разных видов животных. Однако в этих работах не
рассматриваются возможные механизмы деструктивного действия экзогенных ионов Са2+
на структуру мышечной ткани post mortem.
Обсуждается лишь традиционный взгляд на их роль как активаторов Са2+-зависимых
протеаз.
Настоящая
работа посвящена изучению действия различных концентраций СаС12
(0,2-5 мМ) на структуру мышечной ткани и ее клеточных компонентов в процессе
созревания. Степень деструкции исследуемых образцов регистрировали методом
световой микроскопии.
Для проведения
исследований использовали участок длиннейшей мышцы спины (М. longissimus dorsi), отобранный между 9- и 12-м позвонками от пяти
животных (телочки в возрасте 30 мес.) не позднее 45 мин после убоя. Парное мясо
подвергали жиловке с отделением видимой жировой и соединительной тканей.
Мышечную ткань измельчали в мясорубке на холоде. Навески фарша массой не более
15 г выдерживали при 4 °С в течение 1-5 сут в буферном или солевом растворах (в
соотношении 1:4 по массе) следующего состава: 1 - фосфатный буфер: 0,01 М КН2Р04,
0,075 М КС1, 0,02 % (w/v) NaN3, рН 5,8; 2 - 10%-ный раствор NaCl. Растворы содержали СаС12 в концентрациях
от 0,2 до 5 мМ. В качестве контроля использовали образцы фарша, обработанные
растворами в отсутствие СаС12.
Срезы
толщиной 10-12 мкм получали с помощью микротома-криостата МК-25 (Россия). Для
дифференцирования структурных элементов тканей и клеток срезы окрашивали
гематоксилином Эрлиха с дополнительной окраской 0,5%-ным (w/v) раствором эозина.
Окрашенные
срезы изучали под световым микроскопом Jenoval (Германия) при увеличении 400 раз.
Контрольные
и опытные образцы мышечной ткани при созревании в течение 1-5 сут
характеризовались структурными особенностями, свойственными комплексу
посмертных изменений: послеубойному сокращению мышечных волокон (rigor mortis), расслаблению послеубойного сокращения и последующей
деструкции мышечных волокон. Проведенные исследования показали, что динамика и
глубина этих изменений находятся в прямой зависимости от концентрации
экзогенного Са2+.
Наименьшие
изменения в структуре мышечных волокон наблюдали при введении в опытные образцы
0,2 мМ Са2+. Однако, начиная с концентрации 0,6 мМ и до 5 мМ Са2+
отчетливо выявляются деструктивные процессы в мышечной ткани опытных образцов
по сравнению с контролем. Так, если в контрольных образцах разрешение rigor mortis наступает через 72 ч (рис. 2), то в присутствии 3 мМ
Са2+ - через 48 ч, а 5 мМ Са2+ к этому времени индуцируют
образование множественных микротрещин в волокнах.
Через 72 ч
инкубации при этой концентрации Са2+ обнаруживаются гомогенизация
мышечных волокон, нарушения упорядоченного расположения миофибрилл в волокнах и
множественный их распад по Z-пластинкам
- опорному аппарату саркомеров. На это же указывают данные по динамике
изменения величин коэффициента деструкции мышечной ткани.
Таким
образом, введение в мышечную ткань экзогенного Са2+ сокращает сроки rigor mortis, ускоряет процесс послеубойного расслабления мышечной
ткани, приводит к деструкции миофибрилл и их ультраструктуры, индуцирует, как
было ранее показано, разрушение цитоскелетных белков. Все Са2+-индуцируемые
процессы деструкции напрямую зависят от его концентрации и максимально
проявляются в присутствии 5 мМ Са2+. При замене буферного раствора
рассолом (10%-ный раствор NaCl)
деструкция мышечной ткани даже в контрольных образцах (в отсутствие Са2+)
развивается в более ранние сроки по сравнению с контролем в буферных растворах.
Процесс rigor mortis мышечных волокон к 48 ч инкубации сглаживается,
отмечаются усиление набухания волокон, ослабление или исчезновение поперечной
исчерченности, гомогенизация и пикноз ядер, появление зернистой массы в
поверхностных слоях ткани. Это связано с физико-химическим воздействием рассола
на мышечные волокна: изменением осмотического давления, повышением
проницаемости клеточных мембран, выходом из клеток солерастворимых белков.
Наибольший
эффект на деструкцию мышечной ткани оказывало совместное действие СаС12
и рассола. При инкубации образцов в рассоле, содержащем 5 мМ Са2+,
деструктивные изменения отмечались уже через 24 ч, а через 48 ч деструкция
приобретала множественный характер: восстановление поперечной исчерченности,
набухание волокон, множественные микротрещины в них, мелкозернистая белковая
масса между пучками волокон и в соединительнотканных прослойках.
Дальнейшая
инкубация (до 120 ч) мышечной ткани в этих условиях приводила к чрезмерному
разрушению волокон и коагуляции белков, что ухудшало ее текстуру. Таким
образом, наиболее приемлемым временем обработки мясного сырья в этих условиях
можно считать 48 - 72 ч.
Представленные
результаты показывают, что сочетание Са2+ с рассолом значительно
сокращает периоды rigor mortis и его последующего разрешения,
ускоряет деструкцию миофибриллярных структур. Вследствие этого сокращаются
периоды созревания и тендеризации мясного сырья.
Возникает
вопрос, какие механизмы лежат в основе вызываемых ионами Са2+
процессов созревания и тендеризации мяса. Сторонники протеолитической гипотезы
полагают, что ионы Са2+ являются лишь активаторами Са2+-зависимьгх
эндогенных протеаз (в основном кальпаинов), играющих ключевую роль в этих
процессах.
Тем не
менее все авторы подчеркивают, что улучшение текстуры и нежности мясного сырья
наступает после его обработки 30-150 мМ СаС12. Эти концентрации
более чем на два порядка превышают концентрацию Са2+, необходимую
даже для активации m-кальпаина. На
это же указывают в своих публикациях Neyraud и Dransfield [18] и Gerelt и др., причем отмечается, что
причины этого явления до сих пор не исследованы.
Представленные
экспериментальные данные о концентрационной зависимости Са2+-индуцированной
деструкции мышечной ткани дают основание предполагать, что этот процесс
обусловлен не только активацией Са2+-зависимых протеаз, но и другими
механизмами. Ранее было показано, что ослабление Z-дисков миофибрилл скелетных мышц, обработанных 0,1 мМ СаС12
в присутствии кальпастатина, приводит к вымыванию из них только фосфолипидного
матрикса, не затрагивая структуру Z-филаментов. Авторы показали, что этот процесс обусловлен взаимодействием
фосфатных групп фосфолипидов с ионами Са2+. Z-филаменты, состоящие из молекул α-актинина, сохраняют свою структуру.
В мышечной
ткани post mortem все регуляторные и сигнальные системы разрушены, саркоплазматический
ретикулум и митохондрии не способны аккумулировать Са2+ при
нефизиологических условиях. Его предельная концентрация может возрастать в
миоплазме до 2-10-4 М. В этих условиях происходит насыщение всех
центров связывания Са2+ в белковых и мембранных структурах мышечной
ткани. Это, в свою очередь, приводит к необратимым структурным изменениям в Са2+-связывающих
доменах некоторых цитоскелетных белков, диссоциации межмолекулярных
взаимодействий в тропонин-тропо-миозиновом и актомиозиновом комплексах, что
вызывает ослабление ригорных сшивок и ослабление структуры Z-дисков. Введение в послеубойную
мышечную ткань СаС12 в более высоких концентрациях ускоряет эти
деструктивные процессы и сокращает время послеубойного окоченения и его
последующего разрешения, интенсифицируя процессы созревания и тендеризации
мяса.
Из
вышепредставленных результатов следует, что обработка мясного сырья 5 мМ СаС12
ускоряет первую стадию тендеризации - структурное ослабление миофибрилл.
Таким
образом, и представленные результаты, и данные, опубликованные другими
авторами, еще раз экспериментально подтверждают основное положение «кальциевой
теории» о том, что увеличение концентрации свободного Са2+ ускоряет
процессы созревания и тендеризации мяса.
Вышеизложенные
собственные экспериментальные данные и анализ опубликованных ранее результатов
показывают, что созревание и тендеризация - это сложный мультифакторный процесс
включающий множество взаимосвязанных эндогенных и других биологических
механизмов.
Процесс Са2+-индуцированной
тендеризации может протекать следующим образом. Вначале, под влиянием высокой
ионной силы (10%-ный раствор NaCl)
и избыточной концентрации Са2+ происходит разрушение миофибриллярных
структур, индуцируемое Са2+ ослабление Z-дисков и ригорных сшивок. В результате этого значительно
сокращается время послеубойного окоченения мышечной ткани и его последующего
разрешения. Далее ионы Са2+ инициируют изменения в третичной
структуре молекул цитоскелетных белков, белков актомиозинового и
тропомиозин-тропонинового комплекса. Благодаря этому уменьшается их структурная
стабильность и увеличивается доступность многих пептидных связей в молекулах
этих белков для действия тканевых протеаз.
Предлагаемый
вариант механизма Са2+-индуцированной тендеризации мясного сырья не
исключает участия эндогенных протеаз в этом процессе. Однако, несмотря на
громадное количество исследований, до сих пор не получены убедительные
экспериментальные данные о том, какие именно ферменты играют ключевую роль в
протеолизе мышечной ткани. [19]
.5.3 Интенсификация процессов
структурообразования цельномышечных и фаршевых мясных продуктов при
использовании различных биотехнологических приемов
Одной из важнейших проблем мясной промышленности
до сих пор является создание оптимальной технологии тендеризации мяса. Несмотря
на более чем полувековую историю эта задача актуальна и в настоящее время.
Использование неорганических солей кальция (в
качестве источника ионов кальция) является экономически оправданным и более
предпочтительным по сравнению с применением для мягчения мяса ферментных
препаратов.
Проведенные исследования позволили установить,
что инкубация парной мышечной ткани в растворе СаС12 оказывает
влияние на процессы автолиза мышечной ткани, сокращая сроки послеубойного
окоченения мышечных волокон, ускоряя наступление процесса их послеубойного
расслабления и углубляя деструкцию миофибрилл в послеубойный период. Введение в
мясную систему ионов кальция в количествах, превышающих физиологическую
концентрацию, ускоряет кальций-индуцированное расщепление основных
структурообразующих белков мышечной ткани - коннектина и небулина, что
способствует ускорению процесса тендеризации мяса.
Воздействие на мясную систему хлорида кальция
приводило к нарушению структуры Z-линий,
являющихся опорным аппаратом саркомеров, их гомогенизации, разрушению или
расщеплению. Отмеченные изменения в конечном итоге лежали в основе нарушения
целостности волокон и повышении нежности мяса в процессе автолиза.
Установлено, что при введении в мясную систему
ионизированного кальция в концентрации равной 5 мM процессы деградации
цитоскелетных белков - коннектина и небулина, а также разрыхление и деструкция
мышечных волокон наиболее выражены и наблюдаются в более короткие сроки
инкубации.
При использовании хлорида кальция с целью
ускорения созревания мясного сырья необходимо учитывать метаболический профиль
мышц.
Анализ данных, полученных с помощью
микроструктурных исследований показал, что влияние хлорида кальция на структуру
мышечной ткани в комплексе с хлоридом натрия выявляется в набухании волокон,
выходе солерастворимых белков в межволоконные пространства и под сарколемму,
ослаблении поперечной исчерченности мышечных волокон, увеличении размеров
отдельных щелевидных пространств мышечных волокон вследствие деструкции и
лизиса их фибриллярных структур. Глубина деструктивных изменений в мышечной
ткани, инъецированной хлоридом кальция в комплексе с хлоридом натрия, выше по
сравнению с образцами, обработанными только хлоридом натрия.
Сравнительные микроструктурные исследования
парной и охлажденной мышечной ткани, инъецированной хлоридом кальция, показали,
что изменения в структуре мышечных волокон, свойственные для воздействия
хлорида кальция, в охлажденной мышечной ткани не выражены. В то же время,
степень деструкции волокон мышечной ткани, инъецированной хлоридом кальция в
парном состоянии в 1,8 раза выше по сравнению с охлажденной на тот же срок
созревания (14 суток). В связи с чем, необходимо отметить, что использование
хлорида кальция с целью интенсификации процесса созревания, более эффективно
для обработки парного мяса по сравнению с охлажденным.
1.6.
Влияние Са+2 на белки в зависимости от его концентрации
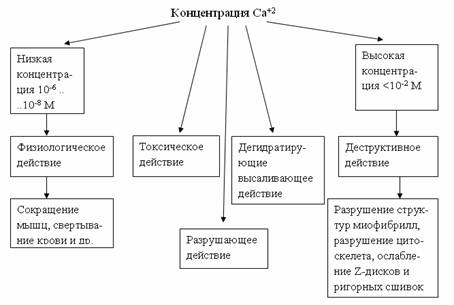
Са +2 оказывает токсическое действие
на белки мышечной ткани, потому что когда Са+2 связывается с
фосфатными группами, он образует нерастворимый Са3(РО4)2
и, тем самым, Са+2 выводится из процесса фосфорилирования, т.е. при
этом нарушается вся энергетика клетки. При этом концентрации Са+2
могут быть самые разные.
По своим электрохимическим свойствам белок, как
и аминокислоты, являются амфотерными электролитоми. Они содержат кислотные, а
также основные группировки и меняют суммарный заряд в зависимости от величины
рН среды. При величине рН, равной изоэлектрической точке белка, заряд белка
становится равным 0, и белок теряет способность растворяться в воде.
Растворимость белка снижается или полностью утрачивается также при разрушении
гидратных оболочек вокруг белковых молекул. Дегидратацию белков вызывают
высокие концентрации солей катионов, и органические растворители, смешивающиеся
с водой. [21]
.7 Выводы из обзора литературных источников
Способность белков к дополнительной гидратации
имеет в технологии пищи большое значение. От нее зависят сочность готовых
изделий, способность полуфабрикатов из мяса, птицы, удерживать влагу и т. д.
Примерами гидратации в кулинарной практике являются: приготовление омлетов,
котлетной массы из продуктов животного происхождения, набухание белков круп,
бобовых изделий и т.д. Дегидратацией называется потеря белками связанной воды
при сушке, замораживании и размораживании мяса, при тепловой обработке
полуфабрикатов и т.д. От степени дегидратации зависят такие важные показатели,
как влажность готовых изделий и их выход.
Ионы Са2+ оказывают стабилизирующее
влияние на пространственную структуру белка, прежде всего на спиральность, и
способствуют ренатурации - процессу самопроизвольного свертывания белковых
цепей после термической денатурации. Изменение белковой молекулы под действием
катионов кальция оказывает существенное влияние на
функционально-технологические свойства белка. Под влиянием Са2+ в
белковой молекуле происходит перераспределение гидрофильных и гидрофобных
центров, что, в свою очередь оказывает влияние на термолабильность и
растворимость белка, его гелеобразующие, эмульгирующие свойства.
Кальцийсвязывающие белки образуют между собой постоянные или временные
комплексы. При этом влияние ионов металлов на структуру белка в составе
комплекса может существенно отличаться по сравнению с влиянием на изолированный
белок.
2. ОБОЗНАЧЕНИЕ ЦЕЛЕЙ И ЗАДАЧ ИССЛЕДОВАНИЯ НА
ОСНОВЕ ЛИТЕРАТУРНОГО ОБЗОРА
Данная работа ставит своей целью разработать
новые многофункциональные смеси, применение которых позволит регулировать
функционально - технологические свойства мяса, а также уточнение данных о
применяющихся смесях и их сопоставление с новыми разработками. Компонентами
этих многофункциональных смесей являются лактат кальция и хлорид кальция. Вводя
экзогенный Са+2 можно регулировать функционально-технологические
свойства мяса. В зависимости от концентрации можно получить мясо в определенный
день с определенными свойствами.
Сырьем для проведения эксперимента является
охлажденная свинина. Используемая часть туши - вырезка, то есть то мясо,
которое берется из той части, которая находится посредине туши над
позвоночником под слоем сала <#"551196.files/image004.gif">
Рис. 1. Зависимость рН от концентрации: 1 -
лактата кальция; 2 - хлорида кальция (1 сутки)
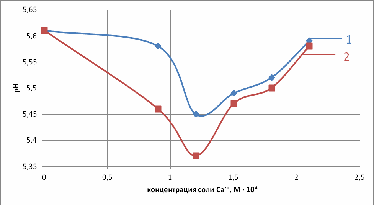
Рис. 2. Зависимость рН от концентрации: 1 -
лактата кальция; 2 - хлорида кальция (2 сутки)
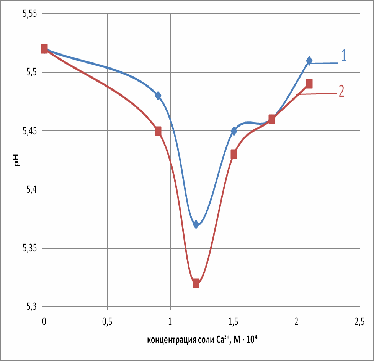
Рис. 3. Зависимость рН от концентрации: 1 -
лактата кальция; 2 - хлорида кальция (3 сутки)
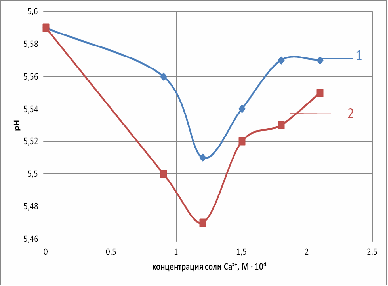
Рис. 4. Зависимость рН от концентрации: 1 -
лактата кальция; 2 - хлорида кальция (4 сутки)
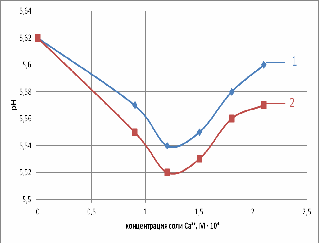
Рис. 5. Зависимость рН от концентрации: 1 -
лактата кальция; 2 - хлорида кальция (5 сутки)
4.2 Графики зависимости влагоудерживающей
способности от концентрации лактата кальция и хлорида кальция
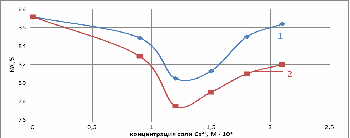
Рис. 6. Зависимость влагоудерживающей
способности от концентрации: 1 - лактата кальция; 2-хлорида кальция (1 сутки)
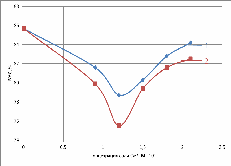
Рис. 7. Зависимость влагоудерживающей
способности от концентрации: 1-лактата кальция; 2-хлорида кальция (2 сутки)
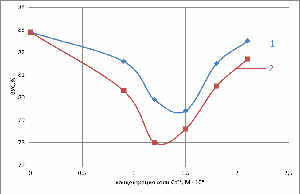
Рис. 8. Зависимость влагоудерживающей
способности от концентрации: 1-лактата кальция; 2-хлорида кальция (3 сутки)
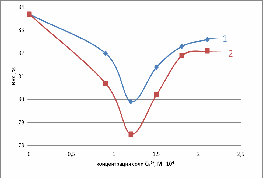
Рис. 9. Зависимость влагоудерживающей
способности от концентрации: 1-лактата кальция; 2-хлорида кальция (4 сутки)
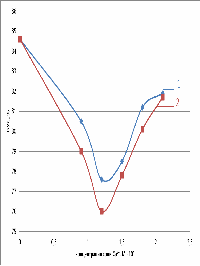
Рис. 10. Зависимость влагоудерживающей
способности от концентрации: 1-лактата кальция; 2-хлорида кальция (5 сутки)
4.3
Графики зависимости количества амино-аммиачного азота от концентрации лактата
кальция и хлорида кальция
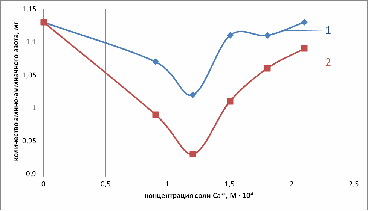
Рис. 11. Зависимость количества амино-аммиачного
азота от концентрации: 1-лактата кальция; 2-хлорида кальция (1 сутки)
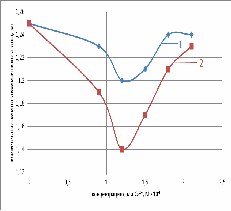
Рис. 12. Зависимость количества амино-аммиачного
азота от концентрации: 1-лактата кальция; 2-хлорида кальция (2 сутки)
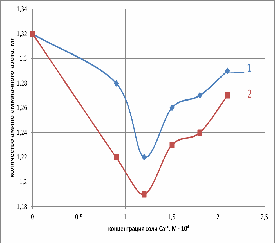
Рис. 13. Зависимость количества амино-аммиачного
азота от концентрации: 1-лактата кальция; 2-хлорида кальция (3 сутки)
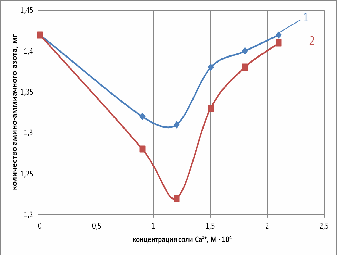
Рис. 14. Зависимость количества амино-аммиачного
азота от концентрации: 1-лактата кальция; 2-хлорида кальция (4 сутки)
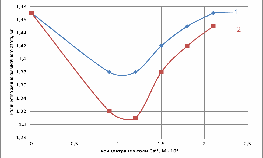
Рис. 15. Зависимость количества амино-аммиачного
азота от концентрации: 1-лактата кальция; 2-хлорида кальция (5 сутки)
4.4
Математическая обработка результатов измерений
Измерения проводились с трех кратной повторностью.
1. Среднее
арифметическое значение рН в 1 день для концентрации лактата кальция равной 1,2
· 10-4 М:
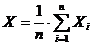 ; (1)
; (1)
где n
- число измерений.
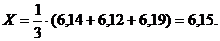
2. Среднее
квадратическое отклонение результата измерения рН в 1 день для концентрации
лактата кальция равной 1,2 · 10-4 М:
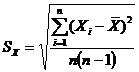 ; (2)
; (2)
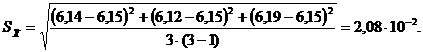
3.
Доверительный интервал при вероятности α=0,95 для рН в 1 день для концентрации
лактата кальция равной 1,2 · 10-4 М:
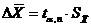 ; (3)
; (3)
где tα,n
- коэффициент Стьюдента.
Таблица 1
Зависимость коэффициента Стьюдента от числа
измерений
|
n
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
|
tα,n
|
12,7
|
4,3
|
3,2
|
2,8
|
2,6
|
2,4
|
2,4
|
2,3
|
2,3
|
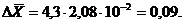
4.
Значения результатов для рН в 1 день для концентрации лактата кальция равной
1,2 · 10-4 М: 6,15 + 0,09.
5. Относительная погрешность измерения рН в 1
день для разных концентраций лактата кальция (%):
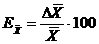 ; (4)
; (4)
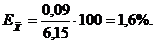
Остальные результаты измерений рассчитаны
аналогично. Относительная погрешность в пределах 2%.
4.5 Выводы
В ходе исследований влияния экзогенного кальция
на функционально-технологические свойства свинины, были сформулированы
следующие выводы:
1. Для свинины минимум ВУС находится
раньше, чем у говядины. Минимум ВУС и, соответственно, растворимость белка
находятся в изоэлектрической точке. В этой точке равенство положительных и
отрицательных зарядов на поверхности белка. Суммарный заряд равен нулю. По этой
причине белки не способны притягивать диполи воды. Следовательно, их ВУС
минимален. Кроме того, эти молекулы белков не отталкиваются друг от друга,
вследствие чего белок выпадает в осадок.
Положение изоэлектрической точки имеет
определённое значение рН. Также на её положение влияют как положительно, так и
отрицательно заряженные ионы (преимущественно положительно заряженные).
Поскольку при физиологических значениях белок заряжен отрицательно, а
разряжать, т.е. компенсировать отрицательный заряд могут только положительно
заряженные ионы - катионы металлов.
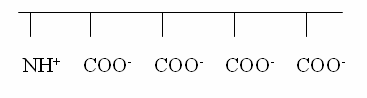
Карбоксильные группы создают отрицательный
заряд. Добавляется соль кальция. Если соль ионизирована (в случае хлористого
кальция), то Са2+ связывается с карбоксильными группами. Суммарно
этот участок белка становится электронейтральным.
Отрицательный заряд на поверхности белка
уменьшается. Соотношение между отрицательным и положительным зарядами смещается
в сторону положительного. Раз отрицательный заряд частично компенсируется
положительным зарядом, то суммарный отрицательный заряд белка становится
меньше. Соответственно белок меньше способен притягивать диполи воды. Поэтому
после такого взаимодействия ВУС уменьшается.
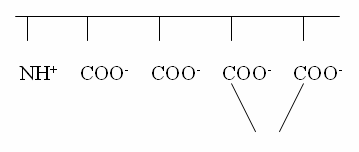
При последующем увеличении концентрации
ионизированного кальция, ещё один Са2+ присоединяется, и ещё один
участок становится электронейтральным.
NH+ COO-
COO- COO- COO-
Са2+ Ca2+
Уже появляется некомпенсированный положительный
заряд, которого может быть несколько. Раз увеличивается положительный заряд,
значит начинает возрастать притяжение диполей воды. Следовательно увеличивается
ВУС. Расти она может до некоторого предела.
Дальше ВУС начинает вновь уменьшаться, что
связано с эффектом высаливания белков. Соли уже не взаимодействуют с
поверхностью белка. Они взаимодействуют с водой. Начинается конкуренция за воду
между белком и заряженными ионами. Ионы уже будут связывать ту воду, которая
находится в растворе и отнимать (при высоких концентрациях) воду, которая была
связана с группами на поверхности белка. Следовательно белок опять будет терять
воду и выпадать в осадок.
Хлористый кальций оказывает большее понижающее
действие на ВУС, чем лактат кальция. Са2+ способен к образованию
комплексных соединений. С Сl-
он не образует этих соединений, поэтому хлористый кальций диссоциирует на Са2+
и Сl-.
С лактатом диссоциация не происходит, так как лактаты способны образовывать
довольно прочные комплексы с Са2+. В какой-то степени лактат тоже
будет подвергаться ионизации, но при одной и той же концентрации в случае
лактата ионизированного кальция будет меньше. Следовательно, он будет оказывать
меньшее разряжающее действие на поверхность белка и позже начнёт оказывать
гидратирующее действие.
В случае свинины минимум ВУС сдвинут в сторону
меньших концентраций, чем для говядины. Из-за того, что свинина содержит меньше
белка, для достижения минимума её ВУС надо затратить меньше Са2.
При рассмотрении ВУС с течением времени,
выявлено, что она понижается примерно на вторые сутки. В этот период Са2+
находит сайты на поверхности белка, с которыми может связываться и насыщает по
отношению к кальцию комплиментарные участки. В дальнейшем ВУС начинает
увеличиваться, что связано с процессом созревания мяса.
. Для клетки кальций - это токсичный элемент,
когда его концентрация повышается. При расходовании АТФ образуются АДФ и
фосфаты. С этими неорганическими фосфатами связываются Са2+.
Образуются очень устойчивые и слаборастворимые соединения. Раз фосфатов нет,
значит ресинтез фосфорной кислоты не возможен. Энергетика клетки «вырубается».
Чтобы этот процесс происходил, кальций должен находиться в ионизированном
состоянии. Если он находится в виде комплекса, как в случае с лактатом, тогда
выводить фосфат затруднеительно. В случае хлористого кальция для этого процесса
нет препятствий. С этой позиции Са2+ токсичен для микроорганизмов.
. Если кальций ионизирован (в случае хлористого
кальция), то он может образовывать соединения Са(ОН)2, так как в
воде присутствует какое-то количество ионов Н+ и ОН-.
Тогда остаются в большом количестве ионы Н+ и Сl-,
т.е. может образовываться соляная кислота. Следовательно, значение рН
понижается.
. Лактат кальция - комплексное соединение, а
хлористый кальций ионизирован. Са2+ вытесняет Н+. Когда
это происходит, рН понижается, что нежелательно для микроорганизмов. Поэтому
амино-аммиачный азот в случае хлористого кальция будет накапливаться меньше,
так как под действием ферментов микроорганизмов происходят все нежелательные
процессы. Конечно, на эти процессы влияет и автолитическое состояние мяса.
В связи с этим можно предположить, что введением
Са2+ можно регулировать функционально-технологические свойства
говядины.
5.
ТЕХНИКО-ЭКОНОМИЧЕСКОЕ ОБОСНОВАНИЕ
Перед мясной промышленностью стоит задача
интенсификации производства на основе ускорения научно-технического прогресса и
в первую очередь повышения качества продукции. Качество питания прежде всего
связано со свойствами сырья, входящего в состав продуктов. Радикальное
изменение качества перерабатываемого сырья и, прежде всего, резко возросшее
содержание в нем жира, высокий объем мяса с пороками и чрезвычайно низкими
функциональными свойствами мышечных белков, потерей вкуса, цвета, запаха
вызывает необходимость пересмотра и совершенствования традиционных способов
производства продуктов для достижения высокого качества, пищевой и
биологической ценности.
Общий дефицит мясных ресурсов, все возрастающие
объемы импортного мяса на продовольственном рынке, отличного от отечественного
по ряду наиболее важных функциональных свойств и химическому составу, лишь
прибавляет остроты проблеме стабилизации качества мясных продуктов.
При разработке технологий производства мясных
продуктов важно учитывать показатели функционально-технологических свойств
(особенно влагоудерживающую способность), так как именно они определяют
качество и выход готовой продукции. Влагоудерживающая способность определяет поведение
белка как основного компонента в сложных мясных системах во взаимодействии с
другими составляющими (жир, вода, минеральные вещества и др.) под влиянием
различных технологических факторов.
Влагоудерживающая способность - важный
показатель качества мясного сырья, она позволяет контролировать ход
технологических процессов, режимы холодильного консервирования и решать вопросы
улучшения качества продукции.
В настоящее время покупатель акцентирует свое
внимание на качество товара: его внешний вид, цвет, запах. Эти три показателя,
по его мнению, помогают выбрать доброкачественный и свежий продукт. Качество
кулинарно обработанного мяса и готовых мясных изделий зависит от его свойств.
Чем меньше его жесткость, выше влагоудерживающая способность, тем нежнее и сочнее
изготовленная из него продукция, лучше ее вкус и аромат, перевариваемость и
усвояемость, следовательно, выше пищевая и биологическая ценность. Поэтому
мясопромышленники предпринимают многочисленные попытки сохранить высокую
влагоудерживающую способность свежего мяса.
Внешний вид мяса до варки, при варке и сочность
при пережевывании определяется влагоудерживающей способностью мяса. Это
особенно относится к измельченным мясопродуктам, например, колбасам, где
структура ткани разрушена, и следовательно, невозможно предотвратить вытекание
сока, выделившегося из белков. Снижение влагоудерживающей способности
проявляется в выделении жидкости.
Влагоудерживающая способность зависит от срока
хранения мяса. В процессе хранения мяса, и, соответственно, происходящего в нем
созревания, происходит изменение и влаговыделяющей способности - она
уменьшается. Мясо, полученное сразу же после убоя животного (парное), в течение
первых 3 часов обладает высокой влагопоглотительной, и влагоудерживающей
способностью, которая и обуславливает его нежную консистенцию после тепловой
обработки. Мягкая консистенция и высокая влагоудерживающая способность парного
мяса обусловлены тем, что белки находятся в негативном состоянии и
растворимость их максимальна вследствие большого количества гидрофильных групп,
способных связывать значительное количество воды.
Данная работа проводилась в лаборатории кафедры
ТМРПиКХ. Своей целью работа ставит разработать технологию для дополнительного
повышения влагоудерживающей способности и функционально-технологических свойств
свинины в целом, что в конечном итоге будет способствовать улучшению качества
продукта и увеличению спроса на него покупателей. [23]
6.
ТЕХНИКО-ЭКОНОМИЧЕСКИЕ РАСЧЕТЫ
Экспериментальная часть работы проводилась в
лаборатории кафедры ТМРПиКХ с 11.02.10 по 1.05.10г.г.
При проведении работы было выполнено 56 опытных
исследований.
В этом разделе рассчитаны затраты на проведение
экспериментов.
Затраты на проведение исследования складываются
из:
·
материалов
и реактивов, относимых на статью стоимости всех материалов, необходимых для
выполнения работы;
·
топлива
и электроэнергии, относимых на статью стоимости и всех видов энергии;
·
основной
и дополнительной заработной платы работников, занятых этими исследованиями за
все время проведения исследовательской работы;
·
единого
социального налога, принимаемого в размере 26 % от основной и дополнительной
заработной платы;
·
накладных
расходов (в размере 10% от суммарной сметы расходов);
·
прочих
производственных расходов (в размере 2% от суммарной сметы расходов).
- амортизационных отчислений (в размере 12% от
стоимости оборудования в год).
Проведение исследований требует использование
сырья и основных материалов. Затраты по этой статье определяются умножением
стоимости материала на его количество, пошедшее на проведение всей серии опытов
таблица 3
Таблица 3
Расчет затрат на сырье и основные материалы
|
№
п.п.
|
Наименование
сырья, основных материалов
|
Единица
измерения
|
Цена
за единицу, руб.
|
Количество
сырья, израсходованного на один опыт, кг (л)
|
Количество
опытов
|
Всего
затрат, руб.
|
|
1
|
Свинина
охлажденная
|
кг
|
274
|
0,025
|
56
|
384
|
|
2
|
Лактат
кальция
|
кг
|
2331
|
0,01
|
5
|
117
|
|
3
|
Хлорид
кальция
|
кг
|
3030
|
0,01
|
5
|
152
|
|
4
|
Итого
|
-
|
-
|
-
|
-
|
653
|
При проведении некоторых анализов использовались
химические реактивы, вспомогательные материалы и лабораторная посуда. Затраты
на них фиксируются в таблицах 4 - 6.
Таблица 4
Расчет затрат на химические реактивы
|
№
п.п.
|
Наименование
сырья, основных материалов
|
Единица
измерения
|
Цена
за единицу, руб.
|
Количество
израсходованных реактивов в единицах на один опыт
|
Количество
опытов
|
Всего
затрат, руб.
|
|
1
|
Фенолфталеин
|
л
|
148
|
0,0003
|
56
|
3
|
|
2
|
Гидрооксид
натрия
|
л
|
16
|
0,003
|
56
|
3
|
|
3
|
Формалин
|
л
|
47
|
0,01
|
56
|
26
|
|
4
|
Итого
|
-
|
-
|
-
|
-
|
32
|
Таблица 5
Расчет затрат на вспомогательные материалы
|
№
п.п.
|
Наименование
материала
|
Единица
измерения
|
Цена
за единицу, руб.
|
Количество
вспомогательного материала, израсходованного на опыты
|
Всего
затрат, руб.
|
|
1
|
Фильтры
бумажные
|
шт
|
0,35
|
56
|
20
|
|
2
|
Фарфоровая
ступка и пестик
|
шт
|
16,8
|
2
|
17
|
|
3
|
Нож
|
шт
|
120
|
1
|
120
|
|
4
|
Доска
|
шт
|
80
|
1
|
80
|
|
5
|
Итого
|
-
|
-
|
-
|
237
|
Таблица 6
Расчет затрат на лабораторную посуду
|
№
п.п.
|
Наименование
посуды
|
Количество,
шт.
|
Стоимость
единицы посуды, руб.
|
Общая
стоимость, руб.
|
|
1
|
Мерный
цилиндр
|
1
|
25
|
25
|
|
2
|
Стеклянный
стакан
|
10
|
15
|
150
|
|
3
|
Бюксы
|
9
|
30
|
270
|
|
4
|
Воронка
стеклянная
|
5
|
12
|
60
|
|
5
|
Пипетка
|
1
|
39
|
39
|
|
6
|
Итого
|
-
|
-
|
544
|
Расчет затрат на лабораторную посуду
производится исходя из стоимости химической посуды и норматива боя посуды в
процентах, принятом в резмере 1,5% от стоимости посуды:
·1,5 / 100 = 8 руб.
Расчет затрат на электроэнергию при работе
приборов и лабораторного оборудования представлен в таблице 5. Затраты на
электроэнергию рассчитываются по формуле
Э = N
· t · Ц / ή,
(1)
где N
- установленная мощность, кВт; t
- продолжительность работы, ч; Ц - цена за 1 кВт·ч, руб.; ή
- коэффициент
использования мощности оборудования (0,7-0,8).
Рассчитаны затраты электроэнергии на весы ВБЭ-1:
Э = 0,35 · 14 · 2,5 / 0,75 = 16,3 руб.
Остальные затраты на электроэнергию приведены в
таблице 7.
Таблица 7
Расчет затрат на электроэнергию
|
№
п.п.
|
Наименование
оборудования, приборов
|
Мощность,
кВт
|
Продолжительность
работы, ч
|
Потребление
электроэнергии, кВт·ч
|
Цена
за 1 кВт·ч, руб.
|
Всего
затрат, руб.
|
|
1
|
Весы
ВБЭ-1
|
0,35
|
14
|
8,4
|
2,5
|
16
|
|
2
|
рН
- метр
|
0,25
|
2
|
1
|
2,5
|
2
|
|
3
|
Сушильный
шкаф
|
1,1
|
37,3
|
1,1
|
2,5
|
137
|
|
4
|
Центрифуга
|
1,3
|
3,3
|
8,2
|
2,5
|
14
|
|
5
|
Итого
|
-
|
-
|
-
|
169
|
Затраты на воду, используемую при проведении
исследований (Зв), рассчитываются исходя из фактического расхода воды (Рв) и
цены 1 м3 воды (Цв)
Зв = Рв · Цв , (2)
Зв = 0,17 · 35 = 6 руб.
где Рв = 0,17 м3 - фактический расход
воды на 56 опытов.
Расчет затрат на амортизацию (износ) приборов и
оборудования, применяемого при проведении исследований представлен в таблице 5.
Амортизация приборов и оборудования определяется по формуле
А = (На·Т·С) /100 · 295 , (3)
где На - норма амортизации (На = 14,8 % от
стоимости оборудования); Т - продолжительность работы оборудования, дни; С -
стоимость оборудования, руб.; 88 - число рабочих дней в году.
Рассчитаны затраты на амортизацию весов ВБЭ-1:
А = (14,8 · 6 · 1290) / 100 · 88 = 13 руб.
Остальные затраты на амортизацию оборудования
приведены в таблице 6.
Таблица 8
Расчет затрат на амортизацию оборудования
|
№
п.п.
|
Наименование
оборудования, приборов
|
Стоимость
оборудования, руб.
|
Продолжительность
работы, ч
|
Норма
амортизации, %
|
Всего
затрат, руб.
|
|
1
|
Весы
ВБЭ-1
|
1290
|
6
|
14,8
|
13
|
|
2
|
рН
- метр
|
2300
|
6
|
14,8
|
23
|
|
3
|
Сушильный
шкаф
|
2240
|
6
|
14,8
|
23
|
|
4
|
Центрифуга
|
3500
|
6
|
14,8
|
35
|
|
5
|
Итого
|
-
|
-
|
-
|
94
|
Таблица 9
Расчет фонда заработной платы
|
№
п.п.
|
Должность
|
Оклад
в месяц, руб.
|
Продолжительность
работы, месс.
|
Основная
заработная плата, руб.
|
Дополнительная
заработная плата, 30% от основной, руб.
|
Все-го
|
|
1
|
Старший
научный сотрудник
|
11000
|
2,5
|
27500
|
8250
|
35750
|
|
2
|
Младший
научный сотрудник
|
6000
|
2,5
|
22500
|
6750
|
29250
|
|
3
|
Итого
|
-
|
-
|
-
|
-
|
65000
|
Расчет основной и дополнительной заработной
платы производится, исходя из месячной зарплаты старшего научного сотрудника
(Зп.мес), фактической продолжительности исследований в месяцах (Кмес)
и дополнительной заработной платы в размере 30%.
Зп = (Зп.мес + Зп.мес · 0,3) · Кмес. (4)
На проведение дипломной работы старший научный
сотрудник и младший научный сотрудник затратили 30% своего времени, то фонд
заработной платы составляет:
Зп = 65000 * 0,3 = 19500 руб.
Отчисления на единый социальный налог
рассчитываются в размере 26,5% от суммы основной и дополнительной заработной
платы:
Осоц = 19500 * 0,26 = 5070 руб.
Прочие расходы (ПР) - 10% от суммы всех
расходов. Накладные расходы принимаются в размере 30% от основной и
дополнительной заработной платы:
Рнакл = 19500 * 0,3 = 5850 руб.
Общая смета затрат на проведение исследований
представлена в таблице 8. [25]
Таблица 10
Смета затрат на проведение исследований
|
№
п.п.
|
Статьи
затрат
|
Общая
сумма, руб.
|
|
1
|
Сырье
и основные материалы
|
653
|
|
2
|
Химические
реактивы
|
32
|
|
3
|
Вспомогательные
материалы
|
237
|
|
4
|
Лабораторная
посуда (бой)
|
8
|
|
5
|
Электроэнергия
|
169
|
|
6
|
Вода
|
6
|
|
7
|
Амортизация
приборов и оборудования
|
94
|
|
8
|
Заработная
плата основная и дополнительная
|
19500
|
|
9
|
Отчисления
в социальные фонды
|
5070
|
|
10
|
Накладные
расходы
|
5850
|
|
11
|
Итого
|
31619
|
|
12
|
Прочие
производственные расходы
|
3161
|
|
Всего
|
34780
|
|
|
|
|
|
Расчет стоимости одного эксперимента:
Стоимость одного эксперимента составляет
/ 56 = 621 руб.
7.
ВЫВОДЫ ПО ТЭО
В результате серии проведенных экспериментов
было выяснено, что при использовании разработанных многофункциональных смесей в
соответствии с рекомендациями к производству, улучшились
функционально-технологические свойства, а именно стала выше влагоудерживающая
способность, уменьшилось время созревания, следовательно, изготовленная из него
продукция будет сочнее и нежнее, улучшится ее вкус и аромат. В результате этого
улучшится качество вырабатываемых продуктов, спрос на изготовляемую продукцию
увеличится.
8.
ГРАЖДАНСКАЯ ОБОРОНА
Химические аварии
Химической обстановкой называют совокупность
последствий химического заражения местности. Химические вещества обладают
различными физическими, химическими и токсилогическими свойствами. В
зависимости от их поражающего действия выделяют боевые отравляющие вещества
(БОВ), сильнодействующие ядовитые вещества (СДЯВ) и аварийно-химически опасные
вещества (АХОВ). Наиболее опасны, даже при непродолжительном ингаляционном
воздействии, газообразные отравляющие вещества (ОВ) и (АХОВ), способные
образовать очаг массового поражения.
Совокупность последствий химического заражения
местности ОВ, АХОВ или СДЯВ будут называться химической обстановкой. [2,
стр.3]
1. Характеристика АХОВ - хлора
Химическое вещество хлор (Сl2)
широко используется в промышленности в качестве химического реагента, обеззараживающего
и отбеливающего средства. Хлор - газ желто-зеленого цвета, с характерным
раздражающим запахом. Молярная масса хлора 71 г/моль. Плотность при 20 °С и
101,3 кПа равна 3,214 кг/м3. Хлор тяжелее воздуха почти в 2,4 раза.
При охлаждении до минус 34,05 °С хлор конденсируется в желтую жидкость, а при
минус 101,6 °С затвердевает. Хлор хорошо растворяется в таких органических
растворителях, как дихлорэтан и тетрахлорметан. В воде при давлении 101,3 кПа и
273 К (0 °С) растворяется 461 объем хлора на 100 объемов воды. При повышении
температуры растворимость уменьшается. ПДК хлора в воздухе рабочих помещений 1
мг/м3, в воздухе населенных пунктов 0,03 мг/м3.
Раствор хлора в воде называют хлорной водой.
Раствор имеет сильнокислую реакцию, так как образуется соляная (НСl)
и хлорноватистая (НСlO)
кислоты. Хлорная вода обладает комплексом бактерицидных свойств.
[26,
стр.4-8]
2. Классы опасности химических веществ
Количественные показатели токсичности и
опасности вредных веществ называют показателями токсиметрии. По изберательной
токсичности хлор относят, главным образом, к легочным ядам. Показатели
токсикометрии определяют класс опасности вещества.
Эффективная токсичность (опасность) - это
произведение абсолютной токсичности на летучесть. При температуре окружающей
среды 293 К или 20 °С доля мгновенно испаряющегося из резервуара облака хлора
составляет около 17 % от емкости резервуара. В настоящее время опасность
химических веществ оценивают по величине коэффициента возможности
ингаляционного отравления - КВИО.
Реальную опасность развития острого или
хронического отравления оценивают величиной зоны острого или хронического
действия, соответственно. Для этого определяют порог вредного действия, т.е.
пороговую, минимальную концентрацию или дозу вещества, при воздействии которого
в организме возникают изменения биологических показателей, выходящие за пределы
приспособительных реакций.
ПДК вредных веществ в воздухе рабочей зоны - это
концентрации, которые при ежедневной (кроме выходных дней) работе в течение 8 ч
или при другой продолжительности, но не более 41 ч в неделю, в течение всего
рабочего стажа не могут вызвать заболеваний или отклонений в состоянии
здоровья, обнаруживаемых современными методами исследований, в процессе работы
или в отдаленные сроки жизни настоящего и последующих поколений.
Для химических веществ, обладающих кумулятивными
свойствами, приняты среднесменные ПДК, так как хронические отравления
развиваются вследствие накопления массы вредного вещества в организме или
вызываемых ими нарушений в организме. Кумуляция - это свойство вещества
накапливаться в организме.
По степени воздействия на организм вредные
химические вещества подразделяют на пять классов опасности: 1. Чрезвычайно
опасные; 2. Высокоопасные; 3. Умеренноопасные; 4. Малоопасные; 5. Практически
не опасные.
Классификация производственных ядов по четырем
степеням опасности представлена табл. 11.
[26,
стр.15-18]
Таблица 11
Классификация производственных ядов по степени
опасности
|
Показатель
|
Класс
опасности
|
|
1
|
2
|
3
|
4
|
|
ПДК
вредных веществ в воздухе рабочей зоны, мг/м3
|
<
0,1
|
0,1
- 1,0
|
1,0
- 10,0
|
>10
|
|
Средняя
смертельная доза при введении в желудок, DLж50, мг/кг
|
<
15
|
15
- 150
|
150
- 5000
|
>
5000
|
|
Средняя
смертельная доза при нанесении на кожу, DLж50, мг/кг
|
<
100
|
100
- 500
|
500
- 2500
|
>2500
|
|
Средняя
смертельная концентрация в воздухе, СLж50, мг/м3
|
<
500
|
500
- 5000
|
5000
- 50000
|
>50000
|
|
Зона
острого действия, Zас
|
<
6
|
6
- 18
|
18
- 54
|
>54
|
|
Зона
хронического действия, Zсr
|
<
10
|
10 - 5
|
5 - 2,5
|
<
2,5
|
|
КВИО
|
>300
|
300
- 30
|
30
- 3
|
<
3,0
|
. Классификация типовых химических аварий
Все типовые химические аварии принято
классифицировать по масштабам возможных последствий, по заражению приземного
слоя воздуха (до уровня флюгера, т.е. 10 м) аварийно химически опасными
веществами.
Классификация типовых химических аварий (с
выбросом АХОВ или розливом CДЯВ)
и привлекаемые силы для ее ликвидации на территории России представлены в табл.
12. [1, стр.19-21]
Таблица 12
Классификация типовых химических аварий
|
Тип
аварии
|
Масштаб
последствий
|
Силы
для ликвидации последствий
|
|
Частная
|
Одна
установка, цех; незначительная утечка АХОВ или СДЯВ
|
Штатный
персонал предприятия
|
|
Объектовая
|
Территория
объекта; глубина зоны заражения меньше радиуса санитарно-защитной зоны
|
Специализированные
и гражданские организации гражданской обороны
|
|
Местная
|
Город,
район, область; облако достигает жилой зоны; эвакуация населения
|
Территориальные
силы ГО и МЧС, воинские части ГО
|
|
Региональная
|
Несколько
субъектов РФ или регион; эвакуация населения
|
Организации,
соединения и воинские части ГО и МЧС, спец. подразделения министерств и
ведомств
|
|
Глобальная
|
Полное
разрушение хранилищ АХОВ, СДЯВ. Несколько регионов и сопредельные страны.
Эвакуация населения
|
Все
виды сил ГО, МЧС, спецподразделения и подразделения вооруженных сил России
|
. Защита окружающей среды
.1. Защита аппаратов и трубопроводов хлора
от разрушения
Защита окружающей среды в первую очередь
обеспечивается промышленной безопасностью эксплуатации технических и
технологических устройств системы хлорного хозяйства. В хлорных производствах
должна применяться только специальная арматура в коррозионно-стойком
исполнении, давление рабочей среды обычно не превышает 1,6 МПа. Однако там, где
используется хлор в жидком виде (испарители жидкого хлора, трубопроводы с
жидким хлором) применяют арматуру среднего давления на 2,5 или 4 МПа рабочего
давления.
Для защиты аппаратов и трубопроводов хлора от
разрушения при аварийном повышении в них рабочего давления, а также для защиты
рабочих органов предохранительных клапанов (ПК) от агрессивной среды используют
мембранные предохранительные устройства (МПУ). Их изготавливают из никеля,
серебра, монель-металла, тантала, нержавеющей стали. Для аппаратов, работающих
под вакуумом до 10 кПа, используют графитовые (ломающиеся) мембраны. Для защиты
печей синтеза хлористого водорода в условиях отсутствия отечественных
производителей МПУ используют самодельные паронитовые мембраны. [26,
стр.69-70]
.2. Требования к системе выброса воздуха в
атмосферу
Воздух, выбрасываемый в атмосферу постоянно
действующими вентиляционными системами хлордозаторных, должен удаляться через
трубу высотой на 2 м выше конька кровли самого высокого здания, находящегося в
радиусе 15 м, а постоянно действующей и аварийной вентиляцией из расходного
склада хлора - через трубу высотой 15 м от уровня земли.
При необходимости следует предусматривать
очистку выбрасываемого вентиляторами воздуха. Для этого применяют орошаемые
скрубберы (санитарные колонны) высотой не менее 3 м. Скорость движения воздуха
не более 1,2 м/с, интенсивность орошения не менее 20 м3/(м2 ·
ч). [26, стр.71-72]
. Коллективные и индивидуальные средства
защиты от хлора и хлористого водорода
К рабочим местам должны быть проведены шланги с
легко открывающимися кранами для подачи воды. Для промывки глаз устанавливаются
фонтанчики.
При работах, связанных с дозировкой
гипохлоритов, следует обязательно использовать прорезиненный фартук, резиновые
сапоги, печатки, косынку или другой головной убор, респиратор типа ШБ-1,
«Лепесток» и др.
Для защиты органов дыхания при работах,
связанных с небольшим превышением ПДК в 10 - 15 раз могут использоваться
газопылезащитные респираторы. В экстренных случаях при объемном содержании
кислорода в воздухе не менее 18% и превышении ПДК токсичных веществ в воздухе
от 10 до 100 раз необходимо использовать промышленный фильтрующий противогаз
ГП-5 или ГП-7.
При необходимости проведения работ или аварийной
ситуации, когда содержание хлора в воздухе превышает ПДК более, чем в 100 раз,
надо использовать изолирующие противогазы марок КИП-7, КИП-8, ИП-4, изолирующий
самоспасатель СПИ-20, дыхательный аппарат АСВ-2 (на сжатом воздухе) и другие. [26,
стр.28]
. Техника безопасности при работе с
хлором
Работы с хлором должны проводиться с применением
средств защиты кожи, глаз и органов дыхания. Не разрешается проведение работ с
хлором без спецодежды и средств индивидуальной защиты. Все работы, связанные с
подключением аппаратуры и подачей хлора, снятием заглушек с емкостного
оборудования и трубопроводов являются газоопасными работами и должны
проводиться при наличии у работающих средств защиты органов дыхания. Для защиты
органов дыхания от хлора допускается применение промышленных фильтрующих
противогазов при условии наличия у пользователей переносных или носимых
(индивидуальных) сигнализаторов утечек хлора и только в том случае, когда концентрация
хлора в воздухе находится в пределах возможных измерений сигнализатора, но не
превышает 0,5% по объему. При более высокой концентрации хлора необходимо
применять изолирующие дыхательные аппараты, самоспасатели и изолирующие
костюмы. Средства индивидуальной защиты для проведения аварийных работ должны
храниться в двух местах, исключающих одновременное попадание в "хлорную
волну". Спецодежда, спецобувь и другие средства индивидуальной защиты
персонала, работающего с хлором, должны выдаваться в соответствии с отраслевыми
нормами бесплатной выдачи спецодежды, спецобуви и предохранительных
приспособлений, утвержденными в установленном порядке. Персонал организаций,
где производится или потребляется хлор, должен знать:
а) отличительные признаки и потенциальную
опасность хлора;
б) пути эвакуации при возникновении хлорной
волны;
в) способы и средства индивидуальной защиты от
поражения хлором;
г) правила оказания первой помощи пострадавшим.
Для оказания первой доврачебной помощи на каждом
производственном участке должна быть медицинская аптечка. [26,
стр.41-44]
. Ликвидация некоторых аварийных ситуаций
В случае утечки хлора необходимо перекрыть краны
и задвижки на трубопроводах с помощью бандажей, хомутов, тампонов, заглушек,
затем перекачать жидкость из аварийной емкости в резервную.
При проливе жидкого хлора проводят: обвалование
емкостей или разлившейся жидкости, сбор жидкого хлора в углубления.
Для снижения скорости испарения хлора и
ограничения распространения облака зараженного воздуха (ОЗВ) надо: создать
водяную завесу, обеспечив поглощение хлора водой; засыпать пролитый хлор слоем
сыпучих адсорбирующих хлор материалов (грунт, песок, шлак, уголь, керамзит,
опилки); обезвредить пролитый хлор нейтрализующими растворами.
В зоне заражения категорически запрещено
принимать воду, пищу, курить и справлять естественные надобности! [26,
стр.73-74]
. Практическое расчетное задание
.1. Исходные данные
Цель: оценить максимальные масштабы заражения
при разрушении баллонов, содержащих 10 т хлора.
Метеоусловия: авария произошла при самых
неблагоприятных для ее ликвидации условиях: ночь, инверсия, скорость ветра V
= 1 м/с, азимут α = 270°, ветер
западный, температура воздуха +40 °С.
Расстояние до ближайших домов железнодорожной
станции Х = 1 км.
Условия розлива АХОВ - хлора: «свободно» на
подстилающую поверхность; h
= 0,05 м.
Обеспеченность населения противогазами: ωi
= 50%.
Количество людей, находящихся:
на открытой местности N1
=
1000 чел.;
в зданиях N2
= 500 чел.
Требуется: провести оценку химической
обстановки.
.2. Решение
.2.1. Максимальное количество возможного
выброса хлора Q0
= 10 т.
.2.2. Расчет эквивалентного количества хлора по
первичному облаку:
Qэ1=К1
К3 К5 К7 Q0
,
где К1 - коэффициент, зависящий от
условия хранения АХХОВ, в этой формуле принимается равным 0,18;
К3 - коэффициент, равный отношению
пороговой токсодозы хлора к пороговой токсодозе данного АХОВ. В данном случае
принимается равным 1,0;
К5 - коэффициент, учитывающий степень
вертикальной устойчивости воздуха, в условиях инверсии равен 1,0;
К7 - коэффициент, учитывающий влияние
температуры воздуха для первичного облака, в данном случае принимается равным
1,4;
Q0 -
количество выброшенного при аварии аммиака равен 10 т.
Qэ1=
0,18 · 1,0 · 1,0 · 1,4 · 10 = 2,52 т.
.2.3. Расчет времени испарения хлора:
Т=h d /
(K2 K4 K7
),
где K2
-
коэффициент, зависящий от физико-химических свойств АХОВ, для хлора принимается
0,052;
K4 -
коэффициент, учитывающий скорость воздуха, в нашем случае принимается равным
1,0;
K7 -
принимается равным 1,0;
d - плотность
сжиженного аммиака, равна 1,553 т/м3.
Т = 0,05 · 1,553 / (0,052 · 1,0 · 1,0) = 1,49 ч.
.2.4. Расчет эквивалентного количества хлора по
вторичному облаку:
Qэ2=(1-
К1) K2
К3
K4 К5
K6 К7
Q0
/ (h d),
где K6
= В0,8 ; В = Т, так как Т< 4, следовательно В = 1,49 ч; K6
=
1, 490,8 = 1,4.
Qэ2=
0, 82 · 0,052 · 1,0 · 1,0 · 1,0 · 1,4 · 1,0 ·10 / (0,05 · 1, 553) = 7,69 т.
.2.5. Определение глубины зоны заражения:
а) первичным облаком: Qэ1=
2, 52 т.
По данным приложения вычисляем:
если Q
= 3 т, то Г = 9,18 км;
если Q
= 1 т, то Г = 4,75 км;
Г1 = 4,75 + (9,18 - 4,75) (2,52 -
1,0) / (3 - 1) = 8,12 км;
б) вторичным облаком: Qэ2=
7, 69 т.
По данным приложения вычисляем:
если Q
= 10 т, то Г = 19,20 км;
если Q
= 5 т, то Г = 12,53 км;
Г2 = 12,53 + (19,20 - 12,53) (7,69 -
5) / (10 - 5) = 16, 12 км.
Результаты расчета количества первичного и
вторичного эквивалентных облаков и времени подхода зараженного хлором облака на
заданное расстояние 1 км приведены в табл. 13.
Таблица 13
Результаты расчета количества первичного и
вторичного эквивалентных облаков и времени подхода зараженного хлором облака на
заданное расстояние 1 км
|
Наименование
объекта (район аварии)
|
Наименование
АХОВ
|
Количество
выброшенного хлора, т
|
Время,
ч
|
|
|
Q0
|
Qэ1
|
Qэ2
|
испарение
хлора Т
|
от
момента аварии В
|
подхода
к объекту ОЗВ t
|
|
Баллоны
железнодорожного состава, станция
|
Хлор
|
10,0
|
2,52
|
7,69
|
1,5
|
1,5
|
0,2
|
.2.6. Расчет полной глубины зоны заражения:
Гпол = Г1 + 0,5 Г11,
где Г1 - наибольший, а Г11
- наименьший из размеров Г1 и Г2:
Г1 = 16,12 км; Г11 = 8,12
км;
Гпол = 16,12 + 0,5 · 8,12 = 20,18 км.
.2.7. Расчет предельно возможной глубины
переноса воздушных масс:
Гпр=В·ν,
где ν
- скорость переноса переднего фронта облака зараженного воздуха, принимается
равной 5 км/ч,
Гпр= 1,5 · 5 = 7,5 км.
.2.8. Определение окончательной расчетной
глубины зоны заражения:
Гпол = 20,18 км; Гпр= 7,5
км; так как Гпр < Гпол, то Г = Гпр; Г = 7,5
км.
.2.9. Определение времени перемещения облака
зараженного воздуха на расстояние Х = 1 км от места аварии с розливом хлора:
t = Х / ν;
= 1 / 5 = 0,2 ч = 12 мин.
.2.10. Определение площади заражения:
а) возможно:
Sв =
8,72
·
10-3 · Г²·φ,
где φ- угловой
размер зоны, равен 180º,
Sв =
8,72 · 10-3 · 7,52 · 180 = 88,29 км2;
б) фактического:
Sф =
Кв · Г² · В0,2
;
где Кв - коэффициент, зависящий от
степени вертикальной устойчивости воздуха, принимаем равным 0,081;
В0,2 = 1,50,2 = 1,05 ;
Sф =
0,081 · 7,52 · 1,05 = 4,78 км2.
.2.11. Построение схемы зоны возможного
заражения и ориентировочно, при условии неизменного направления ветра, зоны
фактического заражения:
Рис.16. Схема зоны возможного заражения и
ориентировочно зоны фактического заражения
.2.12.
Расчет возможного количества и структуры потерь.
Общие потери при обеспеченности
производственного персонала и населения, оказавшегося в очаге химического
поражения, средствами защиты на 60 %:
на открытой местности возможные потери
составляют 100 - - 60 = 40 %, т.е. N1пор
= 1000 · 40 / 100 = 400 чел.;
в простейших укрытиях (зданиях) N2пор
= 500 · 22 / 100 = 110 чел.;
общее число пораженных Nпор
= 400 + 110 = 510 чел.
Учитывая, что отношение площади зоны возможного
заражения к площади зоны заражения составляет Sв
/
Sф =
88,3 / /4,78 = 18,5 раз, и допуская, что население на данной территории
возможного заражения распределено равномерно, ориентировочно фактическое число
потерь и структура поражений составят
Nпор
= 510 / 18,5 = 28 чел.;
из них:
с летальным исходом - 179/18,5 = 10 чел.;
со средней и тяжелой степенями поражения -
204/18,5 = 11 чел.;
с легкой степенью поражения - 127/18,5 = 7 чел.
Результаты расчета глубины и площади зон
возможного и фактического заражения, количество и структура потерь приведены в
табл.4.
мышечный
свинина экзогенный кальций
Таблица 14
Результаты расчета глубины и площади зон
возможного и фактического заражения, количество и структура потерь
|
Глубина
зоны заражения облаком, км
|
Площадь
зон возможного Sв (фактического Sф )
заражения, км2
|
Структура
и число пораженных, ориентировочно: возможно (фактически), чел.
|
вторичным
Г2
|
полная
Гпол
|
предельная
Гпр
|
расчетная
Г
|
|
Легкой
степени
|
Средней
и тяжелой степени
|
С
летальным исходом
|
Общее
число
|
|
8,12
|
16,12
|
20,18
|
7,5
|
7,5
|
88,29
(4,78)
|
127
(7)
|
204
(11)
|
179
(10)
|
510
(28)
|
.2.13. Выводы
Результаты расчета показали, что 0,2 ч
достаточно для своевременного оповещения людей о происшедшей аварии и эвакуации
или снабжения их противогазами. При заданной обеспеченности СИЗ люди защищены
недостаточно.
Рекомендации:
персонал объекта должен быть обеспечен СИЗ на
100%;
на железнодорожной станции (в населенном пункте)
с заданным количеством людей (1500 чел.) необходимо выстроить инженерные
сооружения (убежища). [27,
стр.17-21]
9.
ОХРАНА ТРУДА И ТЕХНИКА БЕЗОПАСНОСТИ
1. Анализ опасных производственных
факторов
Данная дипломная работа выполнялась в
учебно-исследовательской лаборатории кафедры технологии мясных, рыбных
продуктов и консервирования холодом. При выполнении дипломной работы
использовались токсичные вещества, действие которых на человека может оказаться
опасным. Характеристика этих веществ представлена в таблице 15:
Таблица 15
Характеристика вредных веществ
|
Наименование
вещества
|
Величина
ПДК, мг/м3
|
Класс
опасности
|
|
Формальдегид
|
0,5
|
2
|
Опасность действия этого вещества: ядовитость
при вдыхании чистых паров или в смеси с воздухом, способно вызывать аллергические
заболевания в производственных условиях, обладает токсичностью
<http://ru.wikipedia.org/wiki/%D0%A2%D0%BE%D0%BA%D1%81%D0%B8%D1%87%D0%BD%D0%BE%D1%81%D1%82%D1%8C>,
негативно воздействует на генетический материал <http://ru.wikipedia.org/w/index.php?title=%D0%93%D0%B5%D0%BD%D0%B5%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D0%BC%D0%B0%D1%82%D0%B5%D1%80%D0%B8%D0%B0%D0%BB&action=edit&redlink=1>,
репродуктивные органы
<http://ru.wikipedia.org/wiki/%D0%9F%D0%BE%D0%BB%D0%BE%D0%B2%D1%8B%D0%B5_%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D1%8B>,
дыхательные пути
<http://ru.wikipedia.org/wiki/%D0%94%D1%8B%D1%85%D0%B0%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D1%8B%D0%B5_%D0%BF%D1%83%D1%82%D0%B8>,
глаза <http://ru.wikipedia.org/wiki/%D0%93%D0%BB%D0%B0%D0%B7>, кожный
покров <http://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D0%B6%D0%B0>. Оказывает
сильное действие на центральную нервную систему
<http://ru.wikipedia.org/wiki/%D0%A6%D0%B5%D0%BD%D1%82%D1%80%D0%B0%D0%BB%D1%8C%D0%BD%D0%B0%D1%8F_%D0%BD%D0%B5%D1%80%D0%B2%D0%BD%D0%B0%D1%8F_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D0%B0>.
Смертельная доза 35 % водного раствора формальдегида (формалина
<http://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%80%D0%BC%D0%B0%D0%BB%D0%B8%D0%BD>)
составляет 10 - 50 г. Категория взрывоопасности II B, группа взрывоопасности
Т2. Концентрационные пределы воспламенения
<http://ru.wikipedia.org/wiki/%D0%9E%D0%B1%D0%BB%D0%B0%D1%81%D1%82%D1%8C_%D0%B2%D0%BE%D1%81%D0%BF%D0%BB%D0%B0%D0%BC%D0%B5%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F>
7-73 % об.; температура самовоспламенения <http://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D0%BC%D0%BF%D0%B5%D1%80%D0%B0%D1%82%D1%83%D1%80%D0%B0_%D1%81%D0%B0%D0%BC%D0%BE%D0%B2%D0%BE%D1%81%D0%BF%D0%BB%D0%B0%D0%BC%D0%B5%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F>
- 435 °C. [51]
При работе с тонкостенной химической посудой, и
особенно при нагревании и переносе ее существует опасность травмирования рук
острыми кромками разбитой посуды и термических ожогов от раскаленной посуды.
Оборудование, используемое в лаборатории:
холодильник, центрифуга, весы, рН-метр, сушильный шкаф.
Основным фактором на рабочем месте также
является возможность поражения электрическим током U
= 380/220 В, полная потребляемая мощность 8,5 кВт. Этот фактор является
значимым, поскольку лаборатория полна оборудованием, работающим под
напряжением, а, следовательно, возрастает опасность поражения электрическим
током вследствие неправильной эксплуатации и других причин.
С учетом этого обстоятельства лабораторию
следует отнести ко 1-му классу, т.е. к помещениям с умеренной опасностью по
поражению электрическим током. [56]
2. Анализ пожаро- и взрывоопасности
В лаборатории хранятся и используются в ходе
исследований взрывоопасные вещества и материалы, горючие вещества. Такие
вещества хранятся в специальной, обеспечивающей безопасность посуде,
производится контроль их расхода и применения. Однако этот фактор является
значимым, так как при возникновении экстренных ситуаций представляет
определенную опасность.
К потенциальным источникам возгорания относятся:
· Искрение контактов разъемов в
электроприборах нормального использования.
· Воспламенение электропроводки при
коротком замыкании.
· Самовоспламенение (при нарушении
технических режимов).
· Прямой удар молнии.
Обстоятельства, усугубляющие пожароопасность для
обслуживающего персонала:
· Наличие сети коммуникаций.
· Большая протяженность и этажность
помещений.
· Наличие в лаборатории веществ и
материалов, способных усилить горение и задымление
Лабораторию кафедры технологии мясных, рыбных
продуктов и консервирования холодом относится к категории В пожароопасных
производств. Здание имеет вторую степень опасности по огнеопасности.
3. Анализ вредных производственных
факторов
Источником тепло- и хладопоступления является
теплоизолированная стенка холодильника (Т=160С; F=1,2
м2), трубы с горячей водой (Т=700С; d=0,02
м; l=5 м), батареи
(Т=700С; F=3 м3)
- теплый период, (Т=900) - холодный период, теплоизолирующая
поверхность термостата (Т=120С; F=1,6
м2).
Источник вибрации - центрифуга (n=1670
об/мин). Вибрация при работе с центрифугой незначительная, передается через
опорные поверхности телу человека.
Источником шума в лаборатории является вытяжная
вентиляция и холодильники. Вытяжная вентиляция работает непродолжительное время
в течение дня, а, следовательно, фактор шума не является особенно значимым.
Характер зрительных работ: взвешивание на
быстродействующих весах с подсветкой - шкальная лампа 6В; 3В; работа с
градуированными пипетками на химическом стекле; определение цвета раствора при
титровании.
Лаборатория кафедры технологии мясных, рыбных
продуктов и консервирования холодом относится к помещениям, в которых
проводились исследования с незначительным теплоизбытком. Отсюда следует, что
микроклимат способствует созданию удовлетворительных санитарно-гигиенических
условий труда.
Освещение смешанное: естественное и
искусственное. Естественное освещение боковое, осуществляется через оконные
проемы. Искусственное освещение обеспечивается люминесцентными лампами.
Применяется общая система освещения, предназначенная для всего помещения,
фактическая освещенность составляет 300лк.
По степени точности выполняемую работу можно
отнести к работе средней точности (3 разряд, подразряд «Г»). По данным СНиП II
23-05-95 норма освещенности рабочих мест составляет 200 лк. Следовательно,
освещенность в лаборатории на рабочих местах достаточна (300 лк). [4]
Общая фактическая площадь лаборатории - 80 м2
. Площадь, занимаемая оборудованием, фактическая - 40 м2. Общая
кубатура, фактическая - 540 м3. Кубатура, занимаемая оборудованием,
фактическая - 85 м3. Количество рабочих мест 6.
Площадь, приходящаяся на одного работающего:
(100-55)/6 = 5,9 м2
Кубатура, приходящаяся на одного рабочего:
(540-85)/6=74,2 м3
По СНиП 2.09.02-85 площадь производственных
зданий на одного работающего должна быть не менее 4,5 м2, кубатура -
не менее 15 м3. Следовательно, в лаборатории кафедры обеспечиваются
санитарно-гигиенические условия работы.
В лаборатории поддерживаются постоянные
параметры, которые соответствуют действующим нормативам, приведенным в таблице
(для I кат.):
Таблица 16
Параметры воздуха в холодный и теплый период
|
Холодный
период
|
Теплый
период
|
|
t,0C
φ,% υвозд, м/с
|
t,0C
φ,% υвозд, м/с
|
|
20-23
40-60 0,2
|
22-25
40-60 0,2
|
4. Анализ отходов, стоков и выбросов
Мусор собирается в корзины и выносится
техническими работниками, собирается в контейнеры, а затем вывозится городскими
службами к месту утилизации.
Промывные воды после мойки и дезинфекции посуды
и установок сбрасываются в канализацию, на городские очистные сооружения без
всякой обработки.
Кислоты нейтрализуются, а затем также сливаются
в канализацию. [10]
5. Мероприятия по обеспечению безопасных
условий труда
Поверхности аппаратов, в которых поддерживается
высокая температура: автоклав, термостат, места доступных для обслуживающего
персонала предусмотрено покрывать таким слоем изоляции, при котором температура
наружной поверхности не превысит +450С.
Основное лабораторно-производственное
оборудование изготовлено специализированными предприятиями с соблюдением всех
требований безопасности и используются по прямому назначению.
При наличии в помещениях холодильных установок
следует учитывать, что в них как хладагент используется фреон (F-12
ПДК 3000 мг/м3). Фреоны - бесцветные без запаха газы или жидкости.
Они не горят, не взрывоопасны. Большую опасность представляет работа с открытым
огнем при утечке фреона, т.к. при нагревании они разлагаются с образованием
высокотоксичных продуктов (перфторизобутелен C4F8,
фторфосген CF2O
и др.). [3]
При работе с тонкостенной посудой (химической)
во избежание травмирования, необходимо соблюдать следующие меры безопасности:
тонкостенную посуду нужно нагревать на огне с
асбестовой сеткой или водяной бане;
нагретый сосуд нельзя закрывать притертой
пробкой, пока он не охладится;
при переносе сосуда с горячей жидкостью нужно
пользоваться полотенцем, держать сосуд за горловину, поддерживать под дно.