Никель и его соединения
Федеральное агентство по образованию
и науке Российской Федерации
Государственное образовательное
учреждение высшего профессионального образования «Пермский государственный
университет»
Химический факультет
Кафедра неорганической химии
КУРСОВАЯ РАБОТА
на тему: Никель и его соединения
Крылов К.А.
Студент 1 курса
Проверили:
Шульгина Н.П.
Мочалова Н.К.
Пермь 2011
Содержание
Общие
сведения
История
открытия
Основные физические и механические свойства никеля
Нахождение в природе
Получение
Неорганические соединения никеля
Органические соединения никеля
Физические и химические свойства
Применение
Биологическое действие
Вывод
Список использованной литературы
Общие
сведения
НИКЕЛЬ (лат. Niссolum) − химический элемент таблицы Менделеева,
металл.
Символ элемента: Ni.
Атомный номер: 28.
Положение в таблице: 4-й период, группа - VIIIВ (10).
Относительная атомная масса: 58,69.
Степени окисления (жирным шрифтом выделена наиболее характерная): +2, +3, +1 и +4.
Валентности (жирным шрифтом выделена наиболее характерная): II, III, I и IV.
Электроотрицательность:
Электронная конфигурация: [ Ar ] 3 s 2 p 6 d 8 4 s 2.
Природный никель состоит из пяти стабильных нуклидов: 58 Ni (67,88% по массе), 60 Ni (26,23%), 61 Ni (1,19%),62 Ni (3,66%) и 64 Ni
(1,04%).
Простое вещество никель в компактном виде - блестящий серебристо-белый
металл.
Строение атома
Число электронов: 12.
Число протонов: 12.
Радиус нейтрального атома никеля 0,124 нм.
Радиус иона никеля 0,124 нм. Радиус иона Ni 2+ - от 0,069 нм (координационное число 4) до 0,083 нм
(координационное число 6).
Энергии последовательной ионизации атома никеля 7,635, 18,15, 35,17, 56,0
и 79 эВ.
История
открытия
Уже с 17 в. рудокопам Саксонии (Германия) была известна руда, которая по
внешнему виду напоминала медные руды, но меди при выплавке не давала. Ее
называли купферникель (нем. Kupfer
- медь, а Nickel - имя гнома, подсовывавшего горнякам
вместо медной руды пустую породу). Как оказалось впоследствии, купферникель -
соединения никеля и мышьяка, NiAs.
История открытия никеля растянулась почти на полвека. Первым вывод о
присутствии в купферникеле нового «полуметалла» (то есть, по тогдашней
терминологии, простого вещества, промежуточного по свойствам между металлами и
неметаллами) сделал шведский металлург А.Ф. Кронстедт в 1751 году. Однако более
двадцати лет это открытие оспаривалось и господствовала точка зрения, что
Кронстедт получил не новое простое вещество, а какое-то соединение с серой то
ли железа, то ли висмута, то ли кобальта, то ли какого- то другого металла.
Только в 1775 г., через 10 лет после смерти Кронстедта, швед Т. Бергман
выполнил исследования, позволявшие заключить, что никель - это простое
вещество. Но окончательно никель как элемент утвердился только в начале 19 -го
века, в 1804 году, после скрупулезных исследований немецкого химика И. Рихтера,
который для очистки провел 32 перекристаллизации никелевого купороса (сульфата
никеля) и в результате восстановления получил чистый металл.
Основные физические и механические свойства никеля
Атомная масса 58,71.
Плотность при 20ОС, г/см3 − 8, 9.
Температура, ОС:
плавления -
1453.
- кипения -
2140.
Скрытая теплота, кал/г:
- плавления - 73.
испарения
- 1450.
Удельное электросопротивление при 20o С, Ом. мм2/м − 0, 068.
Модуль нормальной упругости, кг/мм2 - 20000.
Временное сопротивление, кг,/мм2:
отожжённого − 40-50.
деформированного − 70-90.
Относительное удлинение, %
отожжённого - 35-40.
деформированного − 2-4.
Твёрдость НВ никеля:
- отожжённого - 70-90.
деформированного - 200.
литого - 60-70.
Теплопроводность при 0-100
oС, кал/(см. сек. град) − 0, 142.
Коэффициент линейного расширения при 20 - 100О, 1/град − 0, 000013.
Предел упругости никеля отожжённого, кг/мм2 - 8.
Предел текучести никеля, кг/мм2:
- отожжённого - 12.
деформированного - 70.
Модуль сдвига, кг/мм2 - 7300.
Предел усталости никеля на базе 107 циклов, кг/мм2:
деформированного - 29.
Ударная вязкость отожжённого никеля, кг. м/см2 - 18.
Нахождение
в природе
В земной коре содержание никеля составляет около 8·10-3% по
массе. Возможно, громадные количества никеля - около 17·1019 т -
заключены в ядре Земли, которое, по одной из распространенных гипотез, состоит
из железоникелевого сплава. Если это так, то Земля примерно на 3% состоит из
никеля, а среди составляющих планету элементов никель занимает пятое место -
после железа, кислорода, кремния и магния. Никель содержится в некоторых
метеоритах, которые по составу представляют собой сплав никеля и железа (так
называемые железоникелевые метеориты). Разумеется, как практический источник
никеля такие метеориты значения не имеют. Важнейшие минералы никеля: никелин
(современное название купферникеля) NiAs, пентландит [сульфид никеля и железа состава (Fe,Ni)9S8], миллерит NiS, Герсфордит (никелевый блеск) NiAsS гарниерит(Ni, Mg)6Si4O10(OH)2 и другие никельсодержащие силикаты. В морской
воде содержание никеля составляет примерно 1 ·10-8%
Элементы железо, кобальт и никель образуют триаду железа, или семейство
железо. Атомы элементов триады железа имеют на внешнем энергетическом уровне по
2 электрона, которые они отдают в химических реакциях. Однако в образовании
химических связей участвуют и электроны 3 d-орбиталей второго снаружи уровня. В своих устойчивых
соединениях, эти элементы проявляют степень окисления +2, +3. Образуют оксиды
состава RO и R2О3. Им соответствуют гидроксиды состава R(OH) 2 и R(ОН) 3.
Для элементов триады (семейства) железа характерно свойство присоединять
нейтральные молекулы, например, оксида углерода (II). Карбонилы Ni(CO)4, Fe(CO)5 (жидкости при t = 20-60°C) и
Со(СО)8 (кристаллы с t пл
>200 ° C, нерастворимые в воде и ядовитые)
используются для получения сверхчистых металлов.
Кобальт и никель менее реакционноспособны, чем железо. При обычной
температуре они устойчивы к коррозии на воздухе, в воде и в различных
растворах. Разбавленные соляная и серная кислоты легко растворяют железо и
кобальт, а никель - лишь при нагревании. Концентрированная азотная кислота все
три металла пассивирует.
Металлы семейства железа при нагревании взаимодействуют с кислородом,
парами воды, галогенами, серой, фосфором, кремнием, углем и бором. Наиболее
устойчивыми являются соединения железа (III), кобальта (II) и никеля (II) - для них
известны почти все соли.
Железо, кобальт и никель в ряду стандартных электродных потенциалов
расположены до водорода. Поэтому они распространены в природе в виде соединений
(оксиды, сульфиды, сульфаты, карбонаты), в свободном состоянии встречаются
редко - в виде железных метеоритов. По распространенности в природе за железом
следует никель, а затем кобальт. Соединения элементов семейства железа в
степени окисления +2 сходны между собой. В состоянии высших степеней окисления
они проявляют окислительные свойства.
Железо, кобальт, никель и их сплавы - весьма важные материалы современной
техники.
Получение
Около 80% никеля от общего его производства (без России) получают из
сульфидных медно-никелевых руд. После селективного обогащения методом флотации
из руды выделяют медный, никелевый и пирротиновый концентраты.
Никелевый рудный концентрат в смеси с флюсами плавят в электрических
шахтах или отражательных печах с целью отделения пустой породы и извлечения Н.
в сульфидный расплав (штейн), содержащий 10-15% Ni. Обычно электроплавке
(основной метод плавки в России) предшествуют частичный окислительный обжиг и
окускование концентрата. Наряду с Ni в штейн переходят часть Fe, Со и
практически полностью Сu и благородные металлы. После отделения Fe окислением
(продувкой жидкого штейна в конвертерах) получают сплав сульфидов Cu и Ni -
файнштейн, который медленно охлаждают, тонко измельчают и направляют на
флотацию для разделения Cu, и Ni. Никелевый концентрат обжигают в кипящем слое
до NiO.
Ni2S3+O2=NiO+SO2
Металл получают восстановлением NiO в электрических дуговых печах. NiO+C=Ni+CO Из чернового никеля отливают аноды и
рафинируют электролитически. Содержание примесей в электролитном никеле. (марка 110) 0,01%. ля разделения Cu и Ni используют также т. н.
карбонильный процесс, основанный на обратимости реакции:
+4CO=Ni(CO)4
Получение карбонила проводят при 100-200 атм. и при 200-250°С, а его
разложение - без доступа воздуха при атмосферном давлении и около 200°С.
Разложение Ni(CO)4 используют также для получения никелевых
покрытий и изготовления различных изделий (разложение на нагретой матрице). В
современных "автогенных" процессах плавка осуществляется за счёт
тепла, выделяющегося при окислении сульфидов воздухом, обогащенным кислородом.
Это позволяет отказаться от углеродистого топлива, получить газы, богатые SO2,
пригодные для производства серной кислоты или элементарной серы, а также резко
повысить экономичность процесса. Наиболее совершенно и перспективно окисление
жидких сульфидов. Всё более распространяются процессы, основанные на обработке
никелевых концентратов растворами кислот или аммиака в присутствии кислорода при
повышенных температурах и давлении (автоклавные процессы). Обычно никель
переводят в раствор, из которого выделяют его в виде богатого сульфидного
концентрата или металлического порошка (восстановлением
водородом под давлением). Из силикатных (окисленных) руд никель также может быть сконцентрирован в штейне при введении
в шихту плавки флюсов - гипса или пирита. Восстановительно-сульфидирующую
плавку проводят обычно в шахтных печах; образующийся штейн содержит 16-20% Ni,
16-18% S, остальное - Fe. Технология извлечения никеля из штейна аналогична
описанной выше, за исключением того, что операция отделения Cu часто выпадает.
При малом содержании в окисленных рудах Со их целесообразно подвергать
восстановительной плавке с получением ферроникеля, направляемого на
производство стали.
Для извлечения никеля из окисленных руд применяют также
гидрометаллургические методы - аммиачное выщелачивание предварительно
восстановленной руды, сернокислотное автоклавное выщелачивание и др.
Неорганические
соединения никеля
. Оксиды.
Монооксид никеля(II) NiO образуется в результате реакции
никеля с кислородом при нагревании выше 500°C.Оксид представляет собой кристаллическое соединение зеленого
цвета, нерастворимое в воде. Его применяют в керамическом производстве при
изготовлении эмалей и красок и в стекольном производстве для окрашивания стекла
в серый цвет.
Сесквиоксид никеля Ni2O3 получают медленным нагреванием нитрата никеля (II) или хлората
никеля (II). Прменяют для изготовления анодов
щелочных аккумуляторов.
. Гидроксиды.
Гидроксид никеля (II) Ni(OH)2 получают действием
щелочей на водные растворы солей никеля. Он имеет вид светло-зеленого рыхлого
осадка.
Гидратированный оксид никеля NiO(OH). Простые соли иона Ni3+ неизвестны, но гидратированный оксид
существует. Получают гидратированный оксид, действуя на Ni(OH)2 окислителем в щелочной среде. На его
образовании при анодном окислении Ni(OH)2 основано действие
щелочного аккумулятора Эдисона. Один из электродов изготовлен из железа, другой
- из гидратированного оксида никеля три, к которому примешаны для лучшей
проводимости никелевые опилки. Электроды помещены в раствор гидроксида калия.
При разрядке и зарядке идут реакции:
Fe+2NiO(OH)+2H2O-2e=Fe(OH)2+2Ni(OH)2
Достоинство железоникелевого аккумулятора в том, что он долгое время
может оставаться в незаряженном состоянии в отличие от обычного свинцового.
. Соли.
Хлорид никеля, хлорид никеля(II), хлористый никель NiCl2
получается в безводном состоянии при сгорании никеля в токе хлора или при
нагревании его гидрата или аммиаката. Он образует блестящие золотисто-желтые
мягкие (на ощупь похожие на тальк), легковозгоняющиеся кристаллические чешуйки
удельного веса 2,56. При умеренном прокаливании на воздухе NiCl2
переходит в окись никеля (П) (моноокись никеля). Он легко растворим в воде и в
спирте (в 100 г воды при 20° растворяется 64,0 г, а при 60° - 81,2 г NiCl2). Из
светло-зеленого водного раствора он кристаллизуется с водой обычно в виде
гекса-гидрата NiСl2*6Н2O - травянисто-зеленых зернистых
кристаллов в форме моноклинных призм, изоморфных кристаллам гексагидрата
хлорида кобальта. При выдерживании над концентрированной серной кислотой
гексагидрат постепенно переходит в дигидрат. Известен также моногидрат.
Со щелочными и другими хлоридами хлорид никеля образует двойные соли
(хлорникелаты) например:4Cl*NiCl2*6H2O -
зеленые ромбические призмы;
СsCl*NiCl2 - мелкие желтые кристаллы.
Бромид никеля NiBr2 и иодид никеля NiI2 вполне
аналогичны хлориду. Они кристаллизуются из водных растворов тоже обычно в виде
гексагидратов. Для бромида, кроме того, известны три- и нонагидраты. Существуют
так же и двойные бромиды.
Фторид никеля NiF2. Безводную соль легче всего получать
термическим разложением двойного фторида никеля и аммония. NiF2
образует длинные призматические кристаллы, в сухом состоянии имеющие окраску от
светло-коричневой до зеленой. Они очень слабо растворимы в воде и нерастворимы
в спирте и в эфире. При упаривании раствора гидроокиси никеля (II) в водной
плавиковой кислоте образуется тригидрат NiF2*3H2O в виде
зернистых бледно зеленых кристаллов. Двойные соли фторида никеля
(фтороникелаты) были получены сплавлением его с соответствующими солями или
смешиванием растворов NiF2 с растворами этих солей. Примером может
служить соль KF*NiF2*Н2O, образующая осадок окрашенный в
цвет серы.
При действии F2 на смесь NiCl2, и KCl получаются
соединения K3[NiF6] и K2[NiF6]. K2[NiF6]
является пока единственной фторидной солью которая, судя по магнитным
свойствам, является «Комплексом внедрения». В случае всех остальные фтористых
солей речь идет о «нормальных комплексах».
Основные галогениды никеля. При неполном осаждении из раствора хлористого
никеля едким натром образуется основной хлорид никеля в среднем состава NiCl2*3Ni(OH)2,
однако состав изменяется в довольно широких пределах (при соотношении Cl : ОН
от 1:1,9 до 1:4,3). Он образует «простую» слоистую решетку, отличающеюся от
структуры гидроокиси никеля тем, что в ней ионы ОН- частично
замещены на Cl-,(причем в решетке они распределены совершенно
беспорядочно) и одновременно ячейка значительно расширяется - вдоль оси). Такое
увеличение параметра объясняется тем, что между структурами гидроокиси и
основной соли не существует непрерывного перехода.
Основной бромид никеля имеет ту же структуру и средний состав, что и
основной хлорид. Однако в случае бромида состав варьирует в значительно более
узком интервале (Вг : ОН = 1 : 2,8-1 : 3,3). Существует еще один основной
хлорид никеля Ni(ОH)С1 постоянного состава, Он образуется при неполном
осаждении едким натром из концентрированного раствора хлористого никеля при
нагревании. Ni(ОH)Cl также образует «простую слоистую решетку». Она является
производной от структуры NiCl2: половина ионов Cl-
замещена на ОН-, тогда все ионы хлора оказываются расположенными на
одной стороне слоя, состоящего из ионов никеля, а все гидроксильные ионы - на
другой.
Цианид никеля и двойные цианиды. при добавлении к растворам никелевых
солей ионов СN- выпадает цианид никеля в виде яблочно-зеленого
осадка, содержащего воду. При нагревании до 180 градусов, он переходит в
желто-коричневую безводную соль Ni(CN)2. Свежеосажденный цианид
никеля растворяется в избытке щелочных цианидов с золотисто-желтым
окрашиванием. Из полученного раствора при упаривании выделяются двойные соли
(цианоникелаты), например Na2(NiCN4)3H2O, в
виде длинных желтых шестигранных призматических кристаллов, теряющих воду при
умеренном нагревании. Сильные кислоты разлагают двойные цианиды, причем
происходит осаждение Ni(CN)2.
При действии на растворы щелочных цианоникелатов водорода в момент
выделения они окрашиваются в красный цвет. Как показал в 1914 г Белуччи, эта
реакция основана на восстановлении никеля до одновалентного состояния. Беллуччи
удалось изолировать и проанализировать красное соединение K2Ni(СN)3.
Соединение диамагнитно ни только в кристаллическом состоянии, но и в растворе.
Уже это обстоятельство позволяет заключить, что в данном случае речь идет о
двухядерном комплексном соединении. Этот вывод был подтвержден Настом при
рентгенографическом определении структуры. Было показано что рассматриваемый
комплекс представляет собой тетрациано-ди-цианодиникелат(I) калия.
Роданид никеля и двойные роданиды. При растворении, карбоната никеля в
водном растворе роданистоводородной кислоты или при реакции между сульфатом
никеля и роданидом бария образуется роданид никеля Ni(SCN)2 (обычно
содержащий некоторое количество воды) в виде желтовато-коричневого осадка,
довольно легко растворимого в воде с появлением зеленой окраски. При упаривании
растворов содержащих щелочные и некоторые другие роданиды, можно получить
хорошо кристаллизующиеся двойные роданиды (роданоникелаты), например Na2[Ni(SCN)4]*8Н20
- светло-зеленые кристаллы и K4[Ni(SCN)6]*4Н2О
- синие кристаллы; эти соли можно без разложения перекристаллизовать из спирта,
а некоторые и из воды.
Нитрат никеля кристаллизуется из водных растворов обычно в виде
гексагидрата Ni(N03)2*6H20, образующего
зеленые, моноклинные кристаллы, изоморфные соответствующей соли кобальта. Выше
54,0° кристаллизуется тетрагидрат, а выше 85,4°- дигидрат; ниже - 3° устойчивой
твердой фазой является нонагидрат. Нитрат никеля применяют для окраски
керамических изделий в коричневый цвет.
Из основных нитратов никеля особый интерес в структурном отношении
представляет соль состава Ni(NO3)2*Ni(OH)2*6Н2О.
В отличие от большинства основных солей никеля, обладающих слоистой структурой,
в решетке этого нитрата, по данным Файткпехта, по-видимому, существуют
комплексные ионы соответственно формуле [Ni(OН2)6][Ni(OH)2(NО3)2].
Нитрит никеля и двойные нитриты. При действии на сульфат никеля нитрита
бария и после упаривания раствора получается нитрит никеля Ni(NO2)2
в виде красно-желтых кристаллов, устойчивых на воздухе. Нитрит никеля растворим
в воде с образованием зеленого раствора. Из растворов, содержащих нитриты
щелочных и щелочноземельных металлов, кристаллизуются двойные нитриты типа M4[Ni(NO2)6)
(гексанитроникелаты), например устойчивый на воздухе никельнитрит
(гексанитроникелат) калия K4[Ni(NO2)6] -
коричнево-красные октаэдры, нерастворимые в спирте; их можно перекристализовать
из воды.
Сульфат никеля получается при растворении металлического никеля, его
окиси или карбоната в разбавленной серной кислоте. В технике его получают
следующим образом: никель растворяют в разбавленной серной кислоте, содержащей
некоторое количество азотной кислоты; раствор нейтрализуют карбонатом никеля и
упаривают. При охлаждении из раствора выделяется гексагидрат NiSО4*6Н2О;
он существует в виде двух модификаций: в интервале температур 31,5-53,3° образуются синевато-зеленые
тетрагональные кристаллы, а выше 53,3° -
зеленые моноклинные. Последние изоморфны кристаллам гексагидрата сульфата
магния. В сухом воздухе они выветриваются, а во влажном - не изменяются. Из
водных растворов при обычной температуре кристаллизуется изумрудно-зеленый,
ромбический гептагидрат. - никелевый купорос NiSO4*7H2O.
Никелевый купорос иногда встречается в природе в виде моренозита. В
противоположность железному и кобальтовому купоросам он кристаллизуется
ромбически. кристаллы имеют ту же форму, что и кристаллы горькой соли -
сульфата магния, они образуют друг с другой непрерывный ряд твердых растворов.
В ромбическом купоросе никель может замещаться железом только в пределах до
21%, в моноклинном возможно замещение половины атомов железа.
Из растворов, содержащих, помимо сульфата никеля, сульфаты щелочных
металлов или сульфат аммония, кристаллизуются двойные соли. Среди них известны
соли главным образом состава M2SO4*NiSO4*6H2O,
изоморфные двойным солям соответствующего состава железа, кобальта, магния и
других двухвалентных металлов. Сине-зеленый аммониевоникелевый сульфат (NH4)2SO4*NiSO4*6H2O
применяют при гальваническом никелировании.
Карбонат никеля и двойные карбонаты. При добавлении к растворам никелевых
солей щелочных бикарбонатов выпадает бледно-зеленый мелкокристаллический осадок
карбоната никеля NiCO3*6H2O, содержащего
кристаллизационную воду. При осаждении никелевых солей нейтральными карбонатами
щелочных металлов образуется основной карбонат никеля.
Если осаждение ведут бикарбонатом аммония, то наряду с NiCO3*6H2O
образуется двойная соль (NH4)HCО3*NiCO3*4H2O,
а при известных условиях
- только эта соль в виде мелких яблочно-зеленых кристаллов. При
осаждении в особых условиях, например при нагревании до 150° одного раствора
хлорида никеля с карбонатом кальция в запаянной трубке, удается получить
карбонат никеля; в безводном состоянии. Кроме приведенной выше двойной
аммониевой соли, известны и другие двойные карбонаты никеля, например K2CO3*NiCO3*4H2O
(яблочно-зеленые иглы) и Na2CO2*NiCO3*10H2O
(микроскопические мелкие ромбоэдры травянистого цвета).
Карбонат никеля применяют для окрашивания керамических изделий, а он
является исходным материалом для получения других соединений никеля.
Оксалат никеля получается при растворении гидроокиси или карбоната никеля
в водном растворе щавелевой кислоты (металлический никель в щавелевой кислоте
не растворяется). Оксалат ocaждается в виде зеленовато-белых хлопьев также при
добавлении щавелевой кислоты к растворам солей никеля. После высушивания при
100° это соединение имеет состав NiC2O4 *2H2О.
В воде оксалат никеля практически нерастворим, но легко растворяется в
разбавленных кислотах или в водном растворе аммиака (с который он образует комплексную соль). В кипящем растворе
оксалата калия оксалат никеля слегка растворим; при охлаждении из таких
растворов кристаллизуется светло-зеленая труднорастворимая двойная соль состава
K2C2O4 *NiC2O4 *6H2O.
Ацетат никеля Ni(CH3CОO)2*4H2O при
упаривании на холоду выделяется в виде кристаллов яблочно-зеленого цвета из
раствора гидроокиси никеля в уксусной кислоте. В воде ацетат растворяется легко
(1:6), но нерастворим в абсолютном спирте. Его водный раствор имеет сладкой
вкус и при нагревании быстро гидролизуетсяс выделением гидроокиси никеля.
Фосфаты никеля. Из довольно значительного числа соединений, образуемых
никелем с кислотами фосфора, в качестве примера следует указать ортофосфат
никеля. При добавлении к растворам солей никеля вторичного фосфата натрия
выпадает в воде бледного яблочно-зеленого, нерастворимого в воде, но
растворимого в кислотах хлопьевидного осадка, который в воздушно-сухом
состоянии имеют примерный состав Ni3(PO4)2*7H2O.
При осаждении фосфатом аммония выпадает соединение (NH4)NiPO4,
первоначально также в виде хлопьевидного осадка, который при соприкосновении с
раствором вскоре переходит в кристаллическое состояние.
Силикаты никеля. При нагревании NiO с SiO2 образуется
ортосиликат никеля Ni 2 [SiO4], кристаллизующийся по типу
оливина. В природе
В виде мелких кристаллических зерен или листочков встречается конарит -
Ni2Si3O8*8H2O - гидрат силиката
никеля. Землистая разновидность его называется реттизитом. Гораздо чаще, чем
эти чистые силикаты никеля (которые залегают лишь в небольших количествах),
встречается гарниерит, образовавшийся при выветривании оливиновых горных парод,
содержащих никель. Он окрашен от яблочно-зеленого до смарагдового цвета и
является гидратом никелево-магниевого силиката, с сильно меняющимся содержанием
никеля. В очень больших количествах гарниерит находится в Нумее в новой
Каледонии, а также в Оригоне в качестве никелевой руды.
Аммиакаты. Большинство солей никеля способно присоединять аммиак при
пропускании его в газообразном состоянии или при добавлении к растворам. Так,
из хлорида никеля и аммиака образуется гексааммиакат хлорида никеля NiCl2*6NH3
в виде почти белого порошка со слегка фиолетовым оттенком, растворимого без
разложения в воде, содержащей аммиак. При пропускании аммиака над безводным
сульфатом никеля образуется NiSO4*6NH3 в виде
бледно-фиолетового порошка. Из раствора никелевого купороса в концентрированном
водном аммиаке кристаллизуется NiSO4*4NH3*2H2O
в виде темно-синих прямоугольных кристаллических столбиков. Аналогично
получается и Ni(N03)2*4NH3*2H20,
образующий большие сапфирово-синие кристаллы.
В указанных аммиакатах существуют ионы [Ni(NH3)6]2+
и [Ni(H2O)2(NH3)4]2+.
Соединения, являющиеся производными этих и других ионов аммиаката никеля, легко
растворимы в воде. Образованием этих комплексов объясняется растворимость в
водном растворе аммиака многих соединений никеля, нерастворимых в чистой воде,
например его гидроокиси и фосфата
Никель очень склонен также к образованию внутрикомплексных солей. К ним
относятся соли, в которых атом металла, заместившего водород, например никеля,
одновременно связан координационной связью с другим кислотным остатком.
Внутрикомплексные соли отличаются часто исключительно низкой растворим остью.
По этому в последнее время они приобретают все более важное значение в
аналитической химии. Одним из наиболее известных представителей этого класса
комплексных соединений является никельдиметилглиоксим, широко применяющийся для
аналитического определения никеля.
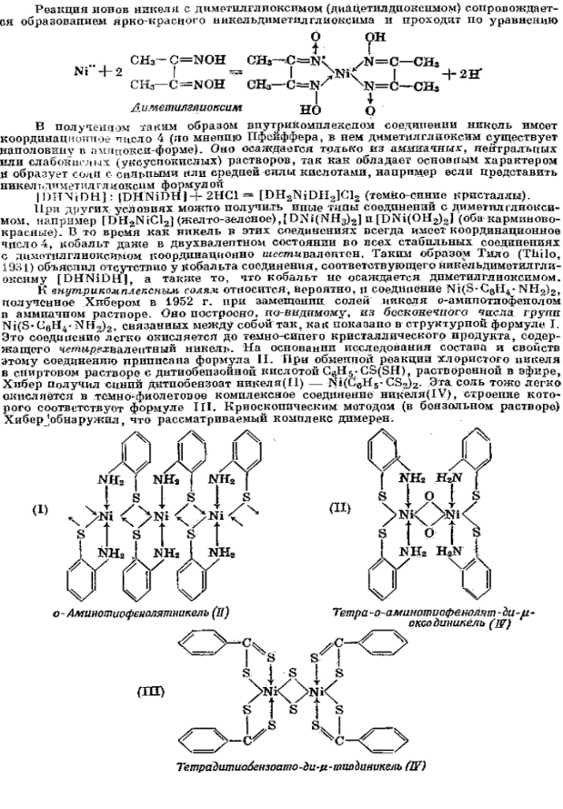
Органические соединения никеля
Связь Ni-C может осуществляться двумя способами: по у- и р-типу, а
соответствующие соединения именуются у- и р-комплексами. Так, к у-комплексам
относятся соединения вида [Ni(R2)L2] и [NiX(R)L2], где R=Alk или Ar, L=PR3, амины и др., X - ацидолиганд; к р-комплексам - алкеновые и полиеновые
никельорганические соединения, содержащие никель в нулевой степени окисления и
имеющие тригональную или тетраэдрическую структуру, например: тригональный
комплекс [Ni(cdt)] (cdt -
циклододекатриен); тетраэдрический комплекс никеля
бис-(1,5-циклооктадиен)никель [Ni(cod)2] - реагент в химии
никельорганических соединений и в органическом синтезе.
Физические
и химические свойства
Никель - ковкий и пластичный металл. Он обладает кубической
гранецентрированной кристаллической решеткой Температура плавления 1455°C, температура кипения около 2900°C, плотность 8,90 кг/ дм3.
Никель - ферромагнетик, точка Кюри около 358°C
На воздухе компактный никель стабилен, а высокодисперсный никель
пирофорен. Поверхность никеля покрыта тонкой пленкой оксида NiO, которая прочно предохраняет металл
от дальнейшего окисления. С водой и парами воды, содержащимися в воздухе,
никель тоже не реагирует. Практически не взаимодействует никель и с такими
кислотами, как серная, фосфорная, плавиковая и некоторыми другими.
Металлический никель реагирует с азотной кислотой, причем в результате
образуется нитрат никеля
(II) Ni(NO3)2 и выделяется соответствующий
оксид азота, например:
3Ni+ 8HNO3 = 3Ni(NO3)2 + 2NO
+ 4H2O
Только при нагревании на воздухе до температуры выше 800°C металлический никель начинает
реагировать с кислородом с образованием оксида NiO.
Оксид никеля обладает основными свойствами. Он существует в двух
полиморфных модификациях: низкотемпературной (гексагональная решетка) и
высокотемпературной (кубическая решетка, устойчива при температуре выше 252°C). Имеются сообщения о синтезе
оксидных фаз никеля состава NiO
1,33-2,0.
При нагревании никель реагирует со всеми галогенами с образованием
дигалогенидов NiHal2. Нагревание порошков никеля и серы приводит к
образованию сульфида никеля NiS. И
растворимые в воде дигалогениды никеля, и нерастворимый в воде сульфид никеля
могут быть получены не только «сухим», но и «мокрым» путем, из водных
растворов.
С графитом никель образует карбид Ni3C, c фосфором - фосфиды составов Ni5P2, Ni2P, Ni3P. Никель реагирует и с другими неметаллами, с азотом никель
не реагирует даже при высоких температурах (до 1400°С). Растворимость азота в
твёрдом никеле приблизительно 0,07% по массе (при 445°С). Нитрид Ni3N
может быть получен пропусканием NH3 над NiF2, NiBr2
или порошком металла при 445°С. Интересно, что никель способен поглощать
большие объемы водорода, причем в результате образуются твердые растворы
водорода в никеле.
Известны такие растворимые в воде соли никеля, как сульфат NiSO4, нитрат Ni(NO3)2 и многие другие. Большинство этих солей
при кристаллизации из водных растворов образует кристаллогидраты, например, NiSO4*7 Н2О, Ni(NO3) 2*6 Н2О. К числу нерастворимых
соединений никеля относятся фосфат Ni 3 (PO 4) 2 и силикат Ni 2 SiO 4. При добавлении щелочи к раствору соли никеля(II) выпадает зеленый осадок гидроксида
никеля:
Ni(NO3) 2 + 2 NaOH = Ni(OH) 2
+ 2 NaNO 3
Ni(OH)2 обладает слабоосновными
свойствами. Если на суспензию Ni(OH)2 в щелочной среде
воздействовать сильным окислителем, например, бромом, то возникает гидроксид
никеля(III):
2 Ni(OH)2 + 2NaOH +Br 2 = 2Ni(OH)3
+ 2NaBr
Для никеля характерно образование комплексов. Так, катион Ni2+ с аммиаком образует гексаамминовый
комплекс [Ni(NH3)6]2+ и диакватетраамминовый комплекс [Ni(NH3)4(Н2О)2]2+. Эти
комплексы с анионами образуют синие или фиолетовые соединения.
+3 - (K3[NiF6]) и +4 - (K2[NiF6]).
Порошок никеля реагирует с оксидом углерода (II) СО, причем образуется легко летучий
тетракарбонил Ni(CO)4, который находит большое практическое
применение при нанесении никелевых покрытий, приготовлении высокочистого
дисперсного никеля и т. д.
Характерна реакция ионов Ni2+ с диметилглиоксимом, приводящая к
образованию розово-красного диметилглиоксимата никеля. Эту реакцию используют при
количественном определении никеля, а продукт реакции - как пигмент
косметических материалов и для других целей.
Применение
никель органический соединение биологический
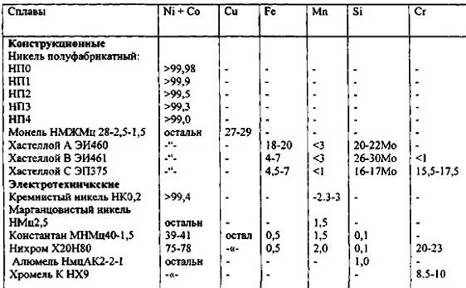
Основная доля выплавляемого никеля расходуется на приготовление различных
сплавов. Так, добавление никеля в стали позволяет повысить химическую стойкость
сплава, и все нержавеющие стали обязательно содержат никель. Кроме того, сплавы
никеля характеризуются высокой вязкостью и используются при изготовлении
прочной брони. Сплав железа и никеля, содержащий 36-38% никеля, обладает
удивительно низким коэффициентом термического расширения (это - так называемый
сплав инвар), и его применяют при изготовлении ответственных деталей различных
приборов.
При изготовлении сердечников электромагнитов широкое применение находят
сплавы под общим названием пермаллои. Эти сплавы, кроме железа, содержат от 40
до 80% никеля. Общеизвестны применяемые в различных нагревателях нихромовые
спирали, которые состоят из хрома (10-30%) и никеля. Из никелевых сплавов чеканятся
монеты. Общее число различных сплавов никеля, находящих практическое
применение, достигает нескольких тысяч.
Высокая коррозионная стойкость никелевых покрытий позволяет использовать
тонкие никелевые слои для защиты различных металлов от коррозии путем их
никелирования. Одновременно никелирование придает изделиям красивый внешний
вид. В этом случае для проведения электролиза используют водный раствор
двойного сульфата аммония и никеля (NH4)2Ni(SO4)2.
Никель широко используют при изготовлении различной химической
аппаратуры, в кораблестроении, в электротехнике, при изготовлении щелочных
аккумуляторов, для многих других целей.
Специально приготовленный дисперсный никель (так называемый никель Ренея)
находит широкое применение как катализатор самых разных химических реакций.
Оксиды никеля используют при производстве ферритных материалов и как пигмент
для стекла, глазурей и керамики; оксиды и некоторые соли служат катализаторами
различных процессов.
Биологическое
действие
Токсическое действие никеля и его неорганических соединений. Общий
характер действия
Никель - необходимый микроэлемент, в частности для регуляции обмена ДНК.
Однако, его поступление в избыточных количествах может представлять опасность
для здоровья. Здесь особенно отчетливо видна справедливость слов Парацельса о
том, что “нет токсичных веществ, а есть токсичные дозы”.
Никель в сочетании с кобальтом, железом, медью также участвует в
процессах кроветворения, а самостоятельно - в обмене жиров, обеспечении клеток
кислородом. В определенных дозах никель активизирует действие инсулина.
Потребность в никеле вполне обеспечивается рациональным питанием, содержащим, в
частности, мясо, овощи, рыбу, хлебобулочные изделия, молоко, фрукты и ягоды.
При повышенных концентрациях обычно может проявляться в виде
аллергических реакций (дерматит, ринит и пр.), анемии, повышенной возбудимости
центральной и вегетативной нервной системы. Хроническая интоксикация никелем
повышает риск развития новообразований (легкие, почки, кожа) - никель влияет на
ДНК и РНК.
Соединения никеля играют важную роль в кроветворных процессах, являясь
катализаторами. Повышенное его содержание оказывает специфическое действие на
сердечнососудистую систему. Никель принадлежит к числу канцерогенных элементов.
Он способен вызывать респираторные заболевания. Считается, что свободные ионы
никеля (Ni2+) примерно в 2 раза более токсичны, чем его комплексные
соединения.
Повышенное содержание никеля в окружающей среде приводит к появлению
эндемических заболеваний, бронхиального рака. Соединения никеля относят к 1
группе канцерогенов.активирует или угнетает ряд ферментов (аргиназу,
карбоксилазу, 5-нуклеозидфосфатазы и др.); влияет на дефосфорилирование
аминотрифосфата. В крови человека Ni связывается преимущественно с
гамма-глобулином сыворотки. После введения NiCI2 кроликам в
сыворотке крови обнаружен белок - никелоплазмин, идентифицированный как
a1-микроглобулин. Однако, 90% Ni в крови кроликов через 24 ч связываются с
альбуминами, лишь незначительная часть поступившего NiCI2 выявлена
во фракциях а2-глобулина. В организме Ni образует комплексы с биокомплексонами.
Ni имеет особое сродство к легочной ткани, в эксперименте при любом пути
введения поражает ее. Оказывает влияние на кроветворение, углеводный обмен.
Металлический Ni и его соединения вызывают образование опухолей у животных, а
также профессиональный рак. Канцерогенное действие Ni связывают с нарушением
метаболизма клеток. Соли Ni вызывают поражение кожи человека с развитием
повышенной чувствительности к металлу.
Острое отравление.
При однократном введении в желудок белых крыс NiCl2 - возбуждение,
затем угнетение; покраснение слизистых и кожи; понос. Комплексные соли Ni с
ЭДТА менее токсичны, чем соли неорганических кислот. Введение в трахею
мелкодисперсного Ni в дозах 5 и 100 мг вызывает гибель белых крыс в короткие
сроки от воспаления легких с периваскулярным отеком, кровоизлияниями во всех
внутренних органах. У выживших животных в отдаленные сроки - гиперплазия лимфоидной ткани вокруг сосудов и бронхов.
У кроликов, кроме того, исхудание, повышение проницаемости сосудов,
изменения на ЭКГ, нарушение функций печени и почек. Аналогичную картину
вызывает Ni2O3 в несколько больших дозах. После введения
в трахею крыс 50 мг Ni(OH)2 или Ni(OH)3 животные погибают
в 1-2 сутки при резких кровоизлияниях и
отеке легких; такая же доза Ni203 переносится без видимых
признаков отравления, кроме похудания и увеличения массы легких. Однократное
введение в трахею крыс. 60 мг пыли, содержащей 95% NiO, через 3 месяца вызвало
развитие мелких пылевых очажков, позднее узелки, состоящие почти, исключительно
из макрофагов. Пыль, содержавшая 64% NiO и NiS, в тех же условиях опыта привела
к гибели 2/3 животных в первые 5 суток. У выживших крыс через 9-12 месяцев - диффузный умеренный перибронхиальный
и периваскулярный склероз.
Хроническое отравление.
Животные.
Длительное поступление NiSO4 с водой при суточной дозе 0,54
мг/кг вызывало у кроликов резкие дегенеративные изменения в печени, почках,
сердечной мышце и гиперплазию селезенки. У крыс, получавших в течение 13 недель
NiCI по 0,3 мг/кг (по Ni),-снижение числа эритроцитов, каталазной активности
крови, массы тела. Введение через рот по 4-12 мг/кг Ni(С2H3O2) и NiС12
в течение 200 дней переносится кошками и собаками без видимых проявлений токсического
действия. Исхудание, снижение содержания аскорбиновой кислоты и щелочной
фосфатазы во внутренних органах и слизистой кишечника отмечали у крыс при
ежедневной дозе NiCI2 0,5-5
мг/кг (по Ni) в течение 7 месяцев. При добавлении к корму 0,01% NiSО4
(по Ni) у молодых бурых крыс - нарушение активности ряда ферментов в крови и
внутренних органах, повышение активности церулоплазмнна в печени. Указывают
также на повреждение семенников у крыс при длительном введении NiSO4.
Круглосуточное вдыхание в течение 3 месяцев аэрозоля металлического NI в
концентрации 0,02-0,5 мг/м3 сказалось у крыс
повышением артериального давления, эритроцитозом, сдвигом в активности
аргиназы, каталазы, нарушением выделительной функции печени, повышением
копропорфирина в моче. Аэрозоль NiCl2 в концентрации 0,1 мг/м3
при вдыхании крысами по 12 ч в день 6 раз в неделю уже через 2 недели вызвал
разрастание бронхиального эпителия, клеточную инфильтрацию альвеолярных
перегородок. Круглосуточное воздействие концентраций 0,005-0,5 мг/м3 (по Ni) сопровождалось также угнетением
иодфиксирующей функции щитовидной железы. Вдыхание NiO в концентрации 120 мг/м3
по 12 ч в день уже через 2 недели вызвало макрофагальную реакцию и клеточную
инфильтрацию альвеолярных перегородок у крыс, а при 80-100 мг/м* по 5 ч в день
в течение 9-12 месяцев развивался умеренный склероз легких с, образованием
клеточных узелков в лимфатических железах и слущиванием бронхиального эпителия.
У молодых хомяков вдыхание 39-170
мг/м3 по 6 ч в день в течение 3 недель и 61,6 мг/м3 в
течение 3 месяцев не вызывало заметных сдвигов. В легких задержалось ~20%
вдыхаемой NiO, которая удалялась довольно медленно. Аэрозоль Ni2O3
в концентрации 340-360мг/м3 по 1,5 ч
в день в течение 4 месяцев сначала увеличил число эритроцитов и содержание
гемоглобина, а затем эта показатели вернулись к норме. Из 20 крыс 7 пали в
первый период затравки. При микроскопическом изучении погибших и убитых после 4
месяцев отравления − воспалительные изменения слизистой верхних
дыхательных путей, очаговая десквамативная или катарально-геморрагическая
пневмония.
Вдыхание пыли файнштейна (11,3% металлического Ni, 58,3% Си) или пыли из
электрофильтров (52,3% NiO) по 5 ч в день 5 раз в неделю в течение 6 месяцев в
концентрации 70 мг/м3 привело к гибели 24 крыс в первом случае и 6 во втором. В
обоих случаях - фазное изменение уровня сахара в крови, нарушение соотношения
белковых фракций в сыворотке крови и снижение в ней содержания холестерина.
Несколько повысилось число эритроцитов и уровень гемоглобина, число ретикулоцитов
и эритробластическая реакция костного мозга. Патологоанатомически - бронхит,
пневмонии и фиброзные изменения. В печени - обеднение гликогеном и
дистрофические изменения; в почках - повреждения эпителия канальцев и атрофия
клубочков. При концентрации обоих аэрозолей 7 мг/м3 и той же длительности
воздействия уловимых изменений не отмечено. При вдыхания пыли цинк-никелевых
ферритов (FeO, ZnO и NiO) в концентрации 100-120 мг/м у крыс картина отравления, сходная с полученной при
ингаляции одной NiO.
Человек.
В производстве аккумуляторных батарей при содержании в исходном продукте
72% Ni выявлено отсутствие или снижение обоняния при концентрации N1 в воздухе
16-560 мг/м3. При 10-70 мг/м3 (в воздухе еще и
Cd) и стаже 8 лет и более
- белок в моче. При стаже 5-10 лет 84% рабочих жаловались на головные боли,
головокружение, раздражительность, понижение аппетита, эпигастральные боли,
одышку. Часто наблюдались снижение кровяного давления, функциональные нарушения
центральное нервной системы, гипо- и анацидные гастриты, нарушения
антитоксической и протромбинообразовательной функции печени, тенденция к
лейкопении, лимфо- к моноцитозу. Сходные изменения обнаружены у рабочих
производства щелочных аккумуляторов при получении массы, содержащей Ni(OH)2
и NiSO4. При электролитическом получении Ni у рабочих основных
специальностей частые носовые кровотечения, полнокровие зева и бронхов, резкие
изменения слизистой носа и даже прободение носовой перегородки, трудно
снимаемый серый налет на краю десен, темные налеты на языке. Концентрация NiSO4
обычно не превышала 0,2-8 мг/м3,
но иногда доходила до 70 мг/м'. Но одновременно в воздухе был туман H2S04
в концентрациях 25-195 мг/м3.
Из обследованных 458 рабочих цехов электролитического рафинирования Ni при концентрации Ni в воздухе 0,02-4,53 мг/м3 (дополнительно в воздухе H2S04;
стаж 10 лет и выше) у 357 человек - носовые кровотечения, частый насморк, нарушение обоняния,
хронические синуситы. Изменения придаточных полостей носа обнаружены у 302
человек. Поражения лобных пазух протекают довольно скрытно и выявляются
рентгенологически. При получении Ni гидрометаллургическим способом из
сульфидных руд при концентрации гидрозоля солей никеля 0,021-2,6 мг/м3 (в воздухе также
пары H2SO4) - поражения слизистой носоглотки в 4-7 раз
чаще, чем у рабочих других цехов. Описаны случаи бронхиальной астмы у
работающих с Ni. При повышенном содержании Ni в атмосферном воздухе - сдвиги в периферической крови, анемия, ретикулоцитоз, а
также снижение кислотности желудочного сока. В производстве никелевых ферритов
(концентрация пыли в воздухе 11-180
мг/м3) среди 145 рабочих при среднем стаже до 4 лет у 88 человек -
умеренная анемия, лейкоцитоз или лейкопения, нарушение стойкости эритроцитов.
Канцерогенное действие.
Предполагают, что канцерогенное действие Ni связано с внедрением его в
клетки, где он вызывает нарушения ферментных и обменных процессов, в результате
которых, возможно, образуются канцерогенные продукты. Никель связывается с РНК,
значительно меньше с ДНК, вызывая нарушения структуры и функции нуклеиновых
кислот, и с гистамином. Опасность бронхогенного рака при вдыхании Ni, возможно,
зависит и от задержки его в легких.
Животные.
В эксперименте опухоли получены от металлического Ni, NiO, сульфидов, но
не от растворимых солей. Бластомогенный эффект по-видимому, не зависит от
степени растворимости, а возможно, от проникания Ni в клетку и изменений,
вызываемых в клеточных мембранах. Металлический Ni, введенный в носовую
полость, в плевру и бедренную кость, вызвал злокачественные опухоли
(частично-остеогенные саркомы) у 30% белых крыс, погибших в течение 7-16
месяцев после введения. В результате вдыхания пыли чистого Ni, полученного из
Ni(CO)4, с дисперсностью до 4 мкм (6 ч в день 4-5 раз в неделю в течение 21 месяца) белые мыши, белые крысы и
морские, свинки погибали чаще всего в течение первых 12-15 месяцев. У морских свинок и большинства крыс-множественные
аденоматозные разрастания в альвеолах легких и гиперпластическая пролиферация
эпителия конечных бронхов. У 6 морских свинок-раковые опухоли. У крыс и
хомяков, вдыхавших пыль металлического Ni вместе с SO, развивались
воспалительные изменения, бронхоэктазы, метаплазия легочного эпителия, но не
выявлено раковых опухолей в легких. По-видимому, раздражающее действие SO2
не стимулировало бластомогенное действие Ni. На месте имплантации NiS в мышцах
крыс возникали фибромио-саркомы, дающие метастазы в легкие.
Человек.
Рак носа, придаточных полостей и легких в Англии давно отнесен к
профессиональным заболеваниям. Показано, что у работающих с Ni и его соединениями
риск заболевания раком легких в 5 раз, а раком носа и его придаточных полостей
в 150 раз превышает нормальную частоту этих заболеваний. На повышенную
опасность рака легких среди рабочих, занятых рафинированием Ni и производством
его солей. К 1974 г., было известно 253 случая профессионального рака верхних
дыхательных путей и легких у рабочих производства Ni. У рабочих, занятых
электролитическим получением Ni, при вдыхании паров электролита, содержащего
NiSO4 через 6-7 лет
на фоне аносмии, перфорации носовой перегородки развивался рак носа и его
придаточных полостей. Известен случай развития ретикулосаркомы носовой полости
у работницы, занимавшейся 5 лет никелированнем и вдыхавшей туман (аэрозоль)
солей Ni. Возможно, усугубляющим было раздражающее действие других ингредиентов
ванн. Описаны случаи рака легких среди работающих, по добыче, обогащению и
переработке медно-никелевых руд.
По некоторым данным, смертность от рака легких, полости носа и его пазух
составляет 35,5% всех смертей рабочих, занятых электролизом и рафинированием
Ni. Среди работающих на никелевых производствах выявлена повышенная смертность
от рака по сравнению с контрольными данными. На первом месте был рак легких, на
втором - желудка. Наиболее часто страдали работавшие при пирометаллургических
процессах в обжиго-восстановительных цехах (стаж 12-23 года, концентрации пыли колебались в пределах порядка
10-103 мг/м3; в ней содержалось 7% Ni в виде сульфидов, NiO или металлического
Ni). Высока смертность от рака в цехах электролиза при наличии в воздухе
аэрозолей NiCl2 и NiSO4. Средний стаж работы у умерших от
рака легких 7-13 лет, от рака желудка - 10-14.
Действие на кожу.
Считают, что Ni не обладает прямым раздражающим действием на кожу. Однако
у никелировщиков, у работающих на производстве Ni электролизом и имеющих
контакт с его солями наблюдаются никелевая экзема, “никелевая чесотка”:
фолликулярно расположенные папулы, отек, эритема, пузырьки, вздутие.
Профессиональные никелевые дерматиты составляют 11% всех профессиональных
заболеваний кожи, а в электролитическом производстве Ni - 15%. У работающих в
гидрометаллургическом производстве Ni заболевания кожи в 2- 4 раза чаще, чем в
других цехах, и обнаружены у 5,5% среди 651 осмотренных рабочих.и его
соединения-сильные сенсибилизаторы. У морских свинок сенсибилизация вызывается
внутрикожным введением NiSO4. Соединяясь с белками эпидермиса, Ni
образует истинный антиген. У больных никелевыми дерматозами определяли
циркулирующие в крови антитела. Связывание Ni в комплексные соединения снижает
его сенсибилизирующее, но не раздражающее действие. В опытах на морских
свинках лаурилсульфат натрия предотвращал развитие сенсибилизации к Ni.
Диметилдитиокарбамат натрия и диметилглиоксим ослабляют кожные реакции у
чувствительных к Ni лиц, по-видимому, при этом образуются и соответствующие
комплексные соединения.
Чувствительность человека к сенсибилизирующему действию Ni очень велика.
Описаны случаи аллергических поражений у кассирш банков, имевших дело с
металлическими монетами. Источником аллергии могут быть даже инъекционные иглы.
У кроликов аппликация Ni на кожу вызвала картину отравления и гибель. Металл
обнаруживался в мальпигиевом слое кожи, в сальных и потовых железах. Через
изолированную кожу трупа человека проходит 1,45 мкг Ni / см3, Применение растворителей
вместе с соединениями Ni способствует, их прониканию в кожу.
Поступление в организм, распределение и выделение.
Из желудочно-кишечного тракта всасываются не только соли, но и
высокодисперсный металл и окислы. В крови Ni образует комплекс с белками плазмы
- никелоплазмин. Никель, поступивший в результате вдыхания или через рот,
распределяется в тканях более или менее равномерно, однако в дальнейшем
проявляется тропность Ni к легочной ткани. Выделение осуществляется через
почки, и желудочно-кишечный тракт. Преимущественный путь выделения зависит как
от свойств соединения (растворимости и др.), так и от пути поступления в
организм. Содержание Ni в моче работающих с ним лиц до 1 мг/л, хотя и
превосходит нормальное, по-видимому, не сигнализирует о возможности
интоксикации.
Предельно
допустимая концентрация
Окись никеля (ІІ), окись никеля (ІІІ), сульфиды
никеля (в пересчете на Ni) 0,5 мг/м3.
Соли никеля в виде гидроаэрозоля (в пересчете на Ni) 0,0005 мг/м3.
Аэрозоль медно-никелевой руды- 4 мг/м*. Для аэрозолей файнштейна,
никелевого концентрата, пыли электрофильтров никелевого производства
рекомендуется 0,1 мг/м3.
Вывод
Никель является одним из чрезвычайно важных металлов; он имеет свою
замечательную историю и заманчивые перспективы дальнейшего применения.
Как химический элемент никель известен немногим более 200 лет, но
практическое применение его в виде различных сплавов уходит в глубокую
древность.
С развитием многих отраслей техники появилась потребность в
высоколегированных сталях и сплавах с особыми физическими, химическими и
механическими свойствами. В этом отношении первостепенная роль принадлежала и
принадлежит никелю, никелевым сталям и никелевым сплавам. К настоящему времени
насчитывается более 3000 составов различных сталей и сплавов, где никель является
основой или присутствует как легирующий элемент.
Применение никеля в современной технике весьма разнообразно. Он
применяется в чистом виде как химически стойкий, ферромагнитный материал в
аппаратостроении, как катализатор и как материал для аккумуляторов. Чистый
никель применяется в значительных масштабах для защитных поверхностных
покрытий: так называемое никелирование имеет большое значение для придания
поверхности металлических материалов высокой химической стойкости.
Большое развитие получило применение никеля в виде различных сплавов на
его основе. Следует особо отметить широкое применение сплавов никеля с хромом и
железом (нихромы и ферронихромы), коррозионно- и кислотостойких никелевых
сплавов, жаропрочных сплавов, сплавов никеля с медью, бериллием, кобальтом,
твердых сплавов, где никель необходим как связующий материал.
Список
использованной литературы
1. Вредные
вещества в промышленности. / Т. 3. - Химия, 1977.
. Антоньев
А.А. Гигиена труда.− 1964.
. Михеев М.И.
Материалы по токсикологии карбонила никеля. − 1970.
. Ицкова А.И.
Фармакология и токсикология. / Т. 32. − 1969.
.
Смолеговский А.М. Энциклопедия химических элементов. − 2000.
. Крицман
В.А. Энциклопедический словарь химика. − 1982.
7. www.wikipedia.ru
. www.chemistry.ru
. www.google.ru
. www.ximikov.net