Развитие учения о кислотах и основаниях. Типы и правила составления ОВР
Казахский
национальный университет имени аль-Фараби
СРС
№6
Развитие
учения о кислотах и основаниях.
Типы
и правила составления ОВР
Алматы 2011
Развитие учения о кислотах и
основаниях
Теории кислот и оснований - совокупность фундаментальных
физико-химических представлений, описывающих природу и свойства кислот и
оснований.
Кислотно-основные взаимодействия чрезвычайно
распространены в природе и находят широкое применение в научной и
производственной практике. Теоретические представления о кислотах и основаниях
имеют важное значение в формировании всех концептуальных систем химии и
оказывают разностороннее влияние на развитие многих теоретических концепций во
всех основных химических дисциплинах.
На основе современной теории кислот и оснований
разработаны такие разделы химических наук, как химия водных и неводных
растворов электролитов, рН-метрия в неводных средах, гомо- и гетерогенный
кислотно-основный катализ, теория функций кислотности и многие другие.
Существует несколько концепций, лежащих в основе
классификации веществ на кислоты и основания. Каждая последующая концепция, в
приведенном ниже списке, включает содержание всех предшествующих, обладает
большей степенью общности.
Эволюция представлений о кислотно-основных
взаимодействиях
Взаимодействие паров соляной кислоты
и аммиака
Представления о кислотно-основных
взаимодействиях относятся к числу фундаментальных химических положений. Понятия
«кислота» и «основание» сформировались еще в XVII веке, однако их содержание
неоднократно пересматривалось и уточнялось.
Представления о природе кислот и оснований
начали формироваться в конце XVIII в. В работах А. Лавуазье кислотные свойства
связывались с наличием в составе вещества атомов кислорода. Известные тогда
минеральные и органические кислоты, действительно, содержали кислород. Эта
гипотеза быстро показала свою несостоятельность, когда благодаря работам Г.
Дэви и Ж. Гей-Люссака стал известен целый ряд кислот, не содержащих кислорода
(например, галогеноводороды, синильные кислоты), в то время, как многие
кислородсодержащие соединения не проявляют кислотных свойств.
С начала XIX века кислотами стали считать
вещества, способные к взаимодействию с металлам с выделением водорода (Ю.
Либих, 1839). Примерно в это же время Й. Берцелиус выдвинул идею, объясняющую
кислотно-основные свойства веществ их электрической «дуалистической» природой.
Так, к кислотам он относил электроотрицательные оксиды неметаллов и некоторых
металлов (например, хрома, марганца и др.), а электроположительные оксиды металлов
считал основаниями. Таким образом, кислотность или основность Берцелиусом
рассматривается как функциональное, а не абсолютное свойство соединения.
Берцелиус впервые сделал попытку количественной оценки и предсказания силы
кислот и оснований.появлением теории электролитической диссоциации С. Аррениуса
(1887) возникла возможность описания кислотно-основных свойств исходя из
продуктов ионизации электролита. Благодаря работам В. Оствальда теория получила
развитие для слабых электролитов.
В начале XX в. американские химики Г. Кэди, Э.
Франклин и Ч. Краус создали теорию сольвосистем, распространившую положения
теории Аррениуса-Освальда на все растворители, способные к автоионизации: 2S
S1+ + S2-. Тогда вещество, отщепляющее при растворении в данном растворителе тот
же катион, который образуется при автоионизации растворителя (S1+), будет
кислотой; соответственно, вещество, отщепляющее тот же анион, который
образуется при автоионизации растворителя (S2-), будет основанием. Теория
позволила распространить закономерности кислотно-основного равновесия на весьма
большое число растворителей. Подобно тому как в воде реакция нейтрализации
ведет к образованию соли и воды, в растворителе S при взаимодействии кислот и
оснований в данной сольвосистеме должны образовываться молекулы соли и
растворителя S.
В основу современных теорий кислот и оснований
положены представления Й. Брёнстеда и Г. Льюиса. Имеются вполне успешные
попытки создать обобщенные теории (М. Усанович, 1939), но они не находят
широкого применения.
Теория электролитической диссоциации
Аррениуса-Оствальда
Согласно теории электролитической диссоциации,
кислоты - это вещества, образующие в водном растворе гидратированные катионы
водорода Н+ (ионы гидроксония) и анионы кислотного остатка; основания в водном
растворе диссоциируют с образованием катионов металла и гидроксид-анионов ОН−.
В общем случае, кислотно-основное взаимодействие сводится к нейтрализации с
образованием соли и воды.
Теория Аррениуса-Оствальда вполне
удовлетворительно описывала свойства водных растворов кислот и оснований,
гидролиз солей. На основе представлений о степени и константе диссоциации было
закреплено деление электролитов на сильные и слабые, введено понятие
водородного показателя. Вместе с тем, её весьма затруднительно использовать для
неводных сред. Теория не позволяет объяснить наличие основных свойств аммиака,
фосфина и других соединений, не содержащих гидроксогрупп.
Протонная теория Брёнстеда-Лоури
Протолитическая (протонная) теория кислот и
оснований была предложена в 1923 году независимо друг от друга датским учёным
Й. Брёнстедом и английским учёным Т. Лоури. В ней понятие о кислотах и
основаниях было объединено в единое целое, проявляющееся в кислотно-основном
взаимодействии: А В + Н+ (А - кислота, В - основание). Согласно этой теории
кислотами являются молекулы или ионы, способные быть в данной реакции донорами
протонов, а основаниями являются молекулы или ионы, присоединяющие протоны
(акцепторы). Кислоты и основания получили общее название протолитов.
Сущностью кислотно-основного взаимодействия
является передача протона от кислоты к основанию. При этом кислота, передав
протон основанию, сама становится основанием, так как может снова присоединять
протон, а основание, образуя протонированную частицу, становится кислотой.
Таким образом, в любом кислотно-основном взаимодействии участвуют две пары
кислот и оснований, названные Бренстедом сопряженными: А1 + В2 А2 + В1.
Одно и то же вещество в зависимости от условий
взаимодействия может быть как кислотой, так и основанием (амфотерность).
Например, вода при взаимодействии с сильными кислотами является основанием: H2O
+ H+ H3О+, а реагируя с аммиаком, становится кислотой: NH3 + H2O NH4+ + OH−.
Электронная теория Льюиса
В теории Льюиса (1923 г.) на основе электронных
представлений было ещё более расширено понятие кислоты и основания. Кислота
Льюиса - молекула или ион, имеющие вакантные электронные орбитали, вследствие
чего они способны принимать электронные пары, например ионы водорода - протоны,
ионы металлов (Ag+, Fe3+), оксиды некоторых неметаллов (например, SO3, SiO2),
ряд солей (AlCl3), а также такие вещества как BF3, Al2O3. Кислоты Льюиса, не
содержащие ионов водорода, называются апротонными. Протонные кислоты
рассматриваются как частный случай класса кислот. Основание Льюиса - это молекула
или ион, способные быть донором электронных пар: все анионы, аммиак и амины,
вода, спирты, галогены. Примеры химических реакций между кислотами и
основаниями Льюиса:
+ Cl− → AlCl4−+ F− →
BF4−+ Cl− → PCl6−.
Общая теория Усановича
Наиболее общая теория кислот и оснований была
сформулирована М. Усановичем в 1939 году. В основе теории лежит представление о
том, что всякое кислотно-основное взаимодействие - это реакция солеобразования.
Согласно этой теории «кислота - это частица, которая может отщеплять катионы,
включая протон, или присоединять анионы, включая электрон. Основание - частица,
которая может присоединять протон и другие катионы или отдавать электрон и
другие анионы» (формулировка 1964 г.). В отличие от Льюиса Усанович в основе
понятий «кислота» и «основание» использует знак заряда частицы, а не строение
электронной оболочки.
По Усановичу в реакции гидролиза SO3 + 2H2O H3O+
+ HSO4- - вода, отдавая анион O2-, является основанием, а триоксид серы,
присоединяя этот анион - кислотой, аналогично в реакции: SnCl4 + 2KCl K2SnCl6 -
тетрахлорид олова, присоединяющий анионы хлора, выступает в роли кислоты. Таким
образом, данная формулировка кислот и оснований позволяет отнести к
кислотно-основным взаимодействиям и все окислительно-восстановительные реакции.
Теория Усановича фактически отменяет один из
основополагающих принципов классической химии - представления о классах кислот
и оснований: «кислоты и основания - это не классы соединений; кислотность и
основность - это функции вещества. Будет ли вещество кислотой или основанием,
зависит от партнера».
К недостаткам теории Усановича относят её
слишком общий характер и недостаточно чёткую определённость формулировки
понятий «кислота» и «основание». К недостаткам относят также то обстоятельство,
что она не описывает неионогенные кислотно-основные превращения. И, наконец,
она не позволяет делать количественные предсказания.
Окислительно-восстановительные
реакции
Окислительно-восстановительные реакции (ОВР)
(реакции окисления-восстановления) происходят с изменением степени окисления
атомов, входящих в состав реагирующих веществ. При окислении веществ степень
окисления элементов возрастает, при восстановлении - понижается.
Первоначально окислением называли только реакции
веществ с кислородом, восстановлением - отнятие кислорода. С введением в химию
электронных представлений понятие окислительно-восстановительных реакций было
распространено на реакции, в которых кислород не участвует.
Особенностью ОВР в растворах (в частности, в
водных) является возможность участия в этих реакциях растворителя (воды), а
также продуктов автопротолиза растворителя (в случае воды - ионов оксония и
гидроксид-ионов). В случае водных растворов это приводит к возможности
протекания между одними и теми же исходными веществами разных реакций в разных
средах: кислотной, нейтральной или щелочной. Так, между KMnO4 и KNO2 в растворе
в зависимости от реакции среды могут протекать следующие химические реакции:
2MnO4 + 5NO2 + 6H3O = 2Mn + 5NO3 +
9H2O (кислотная
среда);
MnO4 + 3NO2 + H2O = 2MnO2 + 3NO3 +
2OH (нейтральная
среда);
MnO4 + NO2 + 2OH = 2MnO4 + NO3 + H2O
(щелочная
среда).
Если известны все исходные вещества и продукты
реакции, то, составляя уравнения таких реакций, можно пользоваться методом
электронного баланса. Если же участники реакции не очевидны, то удобнее
использовать метод электронно-ионного баланса (другое название - метод
полуреакций). Использование этого (более сложного) метода оправдано еще и тем,
что коэффициенты в уравнениях ОВР, протекающих в растворах, бывают довольно большими,(известна,
например, реакция между тремя неорганическими веществами, сумма коэффициентов в
уравнении которой равна 8600) и их подбор методом электронного баланса
оказывается очень трудоемким.
Алгоритм составления уравнения ОВР
методом электронно-ионного баланса таков:
ü Составить перечень веществ и частиц,
присутствующих в системе до начала реакции.
ü Найти среди них окислитель и
восстановитель; определить реакцию среды.
ü Составить уравнение полуреакции
окислителя.
ü Составить уравнение полуреакции восстановителя.
ü Уравнять число принятых и отданных
электронов.
ü Составить ионное уравнение.
ü Составить молекулярное уравнение.
Составляя этим методом уравнений ОВР, необходимо
учитывать следующие основные правила:
) при составлении уравнений полуреакций можно
использовать только те вещества и частицы, которые присутствуют в данной
системе;
) продуктами полуреакций могут быть только те
вещества и частицы, которые устойчивы в данной системе;
) при составлении уравнения полуреакции
окислителя нельзя использовать частицы восстановителя и наоборот, при
составлении уравнения полуреакции восстановителя нельзя использовать частицы
окислителя.
В неорганической химии
окислительно-восстановительные реакции (ОВР) формально могут рассматриваться
как перемещение электронов от атома одного реагента (восстановителя) к атому
другого окислителя например:
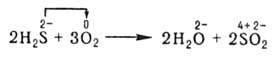
При этом окислитель восстанавливается, а
восстановитель - окисляется. При протекании реакций в гальваническом элементе
переход электронов осуществляется по проводнику, соединяющему электроды
элемента, и изменение энергии Гиббса ΔG в
данной реакции может быть превращено в полезную работу. В отличие от реакций
ионного обмена окислительно-восстановительные реакции (ОВР) в водных растворах
протекают, как правило, не мгновенно.
При окислительно-восстановительных реакциях
атомы в высшей степени окисления являются только окислителями, в низшей -
только восстановителями; атомы в промежуточной степени окисления в зависимости
от типа реакции и условий ее протекания могут быть окислителями или
восстановителями. Многие окислительно-восстановительные реакции (ОВР) -
каталитические (см. Окислительно-восстановительный катализ).
По формальным признакам
окислительно-восстановительные реакции (ОВР) разделяют на межмолекулярные
(например, 2SO2 + O2 → SO3) и внутримолекулярные, например:
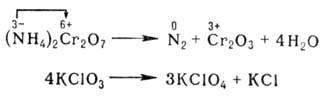
Последняя реакция представляет собой
самоокисление-самовосстановление .
Окислительно-восстановительные реакции (ОВР)
часто сопровождаются высоким энерговыделением, поэтому их используют для
получения теплоты или электрической энергии. Наиболее энергичные
окислительно-восстановительные реакции (ОВР) протекают при взаимодействии
восстановителей с окислителями в отсутствие растворителя; в растворах такие
реакции могут быть невозможны вследствие окислительно-восстановительного
взаимодействия одного или обоих реагентов с растворителем. Так, в водном
растворе нельзя непосредственно провести реакцию 2Na + F2 → 2NaF,
поскольку натрий и фтор бурно взаимодействуют с водой. На
окислительно-восстановительные свойства ионов сильно влияет
комплексообразование, например: комплекс [Co2+(CN)6]4-, в отличие от
гидратированного иона Со2+, является сильным восстановителем.
Сравнение
окислительно-восстановительной активности различных веществ
кислота основание аммиак вещество
взаимодействие
Из определений понятий "
атом-окислитель" и " атом-восстановитель" следует, что только
окислительными свойствами обладают атомы в высшей степени окисления. Наоборот,
только восстановительными свойствами обладают атомы в низшей степени окисления.
Атомы, находящиеся в промежуточных степенях окисления, могут быть как
окислителями, так и восстановителями.
Вместе с тем, основываясь только на степени
окисления, невозможно однозначно оценить окислительно-восстановительные
свойства веществ. В качестве примера рассмотрим соединения элементов VA группы.
Соединения азота(V) и сурьмы(V) являются более или менее сильными окислителями,
соединения висмута(V) - очень сильные окислители, а соединения фосфора(V)
окислительными свойствами практически не обладают. В этом и других подобных
случаях имеет значение, насколько данная степень окисления характерна для
данного элемента, то есть, насколько устойчивы соединения, содержащие атомы
данного элемента в этой степени окисления.
Любая ОВР протекает в направлении образования
более слабого окислителя и более слабого восстановителя. В общем случае
возможность протекания какой-либо ОВР, как и любой другой реакции, может быть
определена по знаку изменения энергии Гиббса. Кроме того, для количественной
оценки окислительно-восстановительной активности веществ используют
электрохимические характеристики окислителей и восстановителей (стандартные
потенциалы окислительно-восстановительных пар). Основываясь на этих
количественных характеристиках, можно построить ряды
окислительно-восстановительной активности различных веществ. Известный вам ряд
напряжений металлов построен именно таким образом. Этот ряд дает возможность
сравнивать восстановительные свойства металлов в водных растворах, находящихся
в стандартных условиях (с = 1 моль/л, Т = 298,15 К), а также окислительные
свойства простых аквакатионов. Если в верхней строке этого ряда поместить ионы
(окислители), а в нижней - атомы металлов (восстановители), то левая часть
этого ряда (до водорода) будет выглядеть
|
Li+
|
K+
|
Cs+
|
Вa2+
|
Rb+
|
Ca2+
|
Na+
|
Мg2+
|
Be2+
|
Al3+
|
Мn2+
|
Zn2+
|
Cr3+
|
Fe2+
|
Co2+
|
Ni2+
|
Sn2+
|
Pb2+
|
Н3О+
|
|
Li
|
K
|
Cs
|
Ba
|
Rb
|
Sr
|
Ca
|
Na
|
Mg
|
Be
|
Al
|
Mn
|
Zn
|
Cr
|
Fe
|
Co
|
Ni
|
Sn
|
Pb
|
H2
|
В этом ряду окислительные свойства ионов
(верхняя строка) усиливаются слева направо, а восстановительные свойства
металлов (нижняя строка), наоборот, справа налево.
Учитывая различия в
окислительно-восстановительной активности в разных средах, можно построить
аналогичные ряды и для окислителей. Так, для реакций в кислотной среде (pH = 0)
получается " продолжение" ряда активности металлов в направлении
усиления окислительных свойств
|
H3O
|
Cu2
|
I2
|
O2
|
Fe3
|
Ag
|
HNO2
|
Br2
|
O2
|
MnO2
|
Cr2O72
|
Сl2
|
PbO2
|
MnO4
|
H2O2
|
O3
|
CaO2
|
Na2O2
|
F2
|
|
H2
|
Cu
|
I
|
Н2O2
|
Fe2
|
Ag
|
NO
|
Br
|
H2O
|
Mn2
|
Cr3
|
Cl
|
Pb2
|
Mn2
|
H2O
|
H2O
|
H2O
|
HF
|
Как и в ряду активности металлов, в этом ряду
окислительные свойства окислителей (верхняя строка) усиливаются слева направо.
Но, используя этот ряд, сравнивать восстановительную активность восстановителей
(нижняя строка) можно только в том случае, когда их окисленная форма совпадает
с приведенной в верхней строке; в этом случае она усиливается справа налево.
Ссылки
http://ru.wikipedia.org/wiki/%D2%E5%EE%F0%E8%E8_%EA%E8%F1%EB%EE%F2_%E8_%EE%F1%ED%EE%E2%E0%ED%E8%E9://www.tryphonov.ru/tryphonov5/terms5/acdbas.htm://www.chem100.ru/text.php?t=150a://www.chem.msu.su/rus/school/zhukov/18.html