Фармакогностическое изучение сырья фенхеля обыкновенного в сравнительном аспекте
Дипломная
работа
Фармакогностическое
изучение сырья фенхеля обыкновенного в сравнительном аспекте
Введение
фенхель обыкновенный фармакологический
липофильный
В последние десятилетия актуальность изучения растительного
сырья и лекарственных препаратов на его основе возрастает с каждым днем.
Преимущество растительных препаратов перед синтетическими заключается в том,
что содержащиеся в них биологически активные вещества действуют на организм
комплексно, имеют низкую токсичность и меньший риск возникновения побочных
реакций.
Сельскохозяйственные и пищевые растения являются
приоритетными в фитохимическом изучении, так как имеют достаточную сырьевую
базу.
Фенхель обыкновенный (Foeniculum vulgare) - растение семейства
зонтичных (Apiaceae) - является одним из таких растений с богатым опытом применения
его плодов в медицине. Плоды данного растения достаточно хорошо изучены и
являются источником эфирного масла. После извлечения плодов остается надземная
часть - трава, которая, на наш взгляд, заслуживает детального изучения, так как
содержит другие группы БАВ в различных количествах, отличные от состава плодов,
и может выступать потенциальным дополнительным источником сырья. Прежде всего,
к таким БАВ относят флавоноиды, комплексное изучение которых было проведено
ранее на кафедре фармацевтической химии и фармакогнозии [33].
Фаза вегетации растения, как известно, оказывает значительное
влияние на синтез и накопление биологически активных веществ (БАВ).
Каждая группа БАВ выполняет определенную биохимическую
функцию в жизнедеятельности растения, совокупность которых обеспечивает его рост и
развитие. Учитывая тот факт, что растения являются источником фитопрепаратов,
изучение динамики накопления отдельных групп БАВ в сырье в зависимости от фазы
вегетации является важной задачей, решение которой позволит максимально
оптимизировать сроки заготовки сырья и, как следствие, обеспечить его
рациональное использование.
Поэтому, качественный и количественный анализ сырья фенхеля
обыкновенного является актуальной задачей.
Цель и задачи исследования. Целью данной работы было
идентификация и определение количественного содержания БАВ в сырье фенхеля
обыкновенного, а так же изучение динамики накопления отдельных групп БАВ в
надземных органах фенхеля, заготовленного в различные фазы вегетации.
Для достижения цели нами были поставлены следующие задачи:
. Провести идентификацию основных групп
биологически активных компонентов в объектах исследования.
2. Определить количественное содержание и динамику
накопления БАВ в надземных органах фенхеля обыкновенного.
3. Получить и исследовать липофильные комплексы из
объектов исследования.
В качестве объектов исследования было выбрано следующее сырье фенхеля
обыкновенного: трава в фазе до цветения, трава в фазе цветения трава в фазе зеленого
плодоношения, плоды и зонтики, остающиеся после обрушения плодов, которое было
заготовлено на территории Луганской области в июне-сентябре 2010 г.
Предмет исследования. Состав и содержание БАВ
в надземных органах фенхеля обыкновенного.
Методы исследования. Специфические
качественные реакции на вещества гликозидной природы, полисахариды,
гидроксикоричные кислоты, органические кислоты, аминокислоты, кумарины,
флавоноиды, конденсированные дубильные вещества и сапонины; хроматография в
тонких слоях сорбента, титриметрические методы анализа, УФ - спектрофотометрия,
экстракция липофильных комплексов.
Новизна полученных результатов. Впервые
проведено комплексное исследование всего растения - фенхеля обыкновенного в
сравнительном аспекте динамики накопления отдельных групп БАВ.
Практическое значение полученных результатов. Полученные
результаты дают возможность использовать исследуемое ЛРС в качестве
альтернативного источника сырья для дальнейшего выделения БАВ с целью создания
лекарственных препаратов, а так же позволит максимально оптимизировать сроки заготовки сырья
и, как следствие, обеспечить его рациональное использование.
Апробация результатов. Основные результаты
дипломной работы докладывались на VІ Региональной научно - практической
конференции молодых ученых и студентов «Фармацевтическая наука: исторические аспекты
формирования и пути усовершенствовани» и на І Всеукраинской научно -
практической конференции молодых ученых и студентов «Современная фармация и
медицина: опыт, пути усовершенствования и развития».
Публикации. Материалы работы
отражены в сборниках тезисов VІ Региональной и І Всеукраинской конференций
молодых ученых и студентов.
Объем и структура дипломной работы. Работа состоит
из введения, обзора литературы, раздела собственных исследований, выводов,
списка литературы, который состоит из 46 источников. Работа изложена на 56 листах
текста, иллюстрирована 16 рисунками, содержит 11 таблиц.
1. Ботаническая характеристика, химический состав
и применение фенхеля обыкновенного (обзор литературы)
.1 Общая характеристика семейства сельдерейные
Семейство сельдерейные (Apiaceae) объединяет около 300 родов
и 3000 видов, распространенных почти по всему земному шару, но главным образом
в северной умеренной зоне (меньше - в горах тропиков). Это в основном многолетние
травянистые растения, иногда очень большие - выше 3 метров, иногда однолетние,
редко кусты или полукустарники [28].
Диагностические признаки семейства представлены на рис. 1.1.
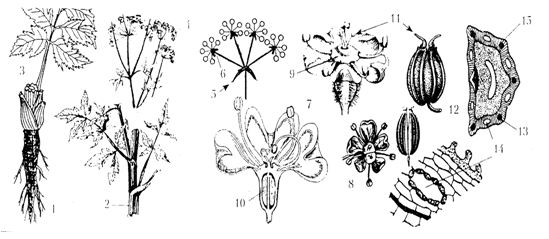
Рис. 1.1 Диагностические признаки семейства зонтичные
Подземным органом некоторых видов является корнеплод (1).
Стебли (2) имеют полую сердцевину, часто ребристые или бороздчатые. Листья без
прилистников, влагалищные, с перистой пластинкой, изрезанной в различной
степени. Низовые листья собраны в прикорневую розетку (3), стеблевые -
очередные или супротивные, черешковые или сидячие. Во всех частях растения
находятся эфиромасличные канальца, а в стеблях - хорошо развитая колленхима,
благодаря чему они могут достигать значительной высоты. Соцветие - сложный
зонтик (4), редко - головка. Иногда имеются прицветники, образующие обвертку
(5) сложного зонтика, и прицветнички, формирующие обверточки элементарных
соцветий - зонтичков (6). Цветки актиноморфные (7), обоеполые, иногда (по краю
зонтичков) зигоморфные (8), обоеполые или однополые. Чашечка редуцирована до
зубчиков или небольшой окраины. Тычинки чередуются с лепестками, прикреплены к
железистому нектарному диску (9). Гинецей ценокарпный из 2 плодолистиков,
завязь (10) нижняя, двухгнездная, с дисковидным кольцом или двумя подушечками и
парой столбиков (11).
Формула цветка: 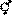
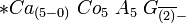 [22]
[22]
Схизокарпный плод - вислоплодник, или двумерикарпий (12), зачастую
разделяется на пару односеменных, нераскрывающихся полуплодиков - мерикарпиев,
свисающих на нитевидном карпофоре. На поверхности околоплодника заметны 5
продольных первичных ребер (13), где проходят проводящие пучки. Между ребрами
имеются углубления - бороздки, где располагаются схизогенные эфирномасличные
канальцы (14), количество и форма которых являются видовыми диагностическими
признаками. Семена обычно с эндоспермом и небольшим зародышем, но иногда
наблюдается формирование семени без эндосперма. Форма эндосперма на поперечном
разрезе может быть плоской, выпуклой, вогнутой, сердцевидной, что также
является видовым признаком [5,7,28,].
1.2 Исторические аспекты использования фенхеля
Фенхель - растение, ставшее известным человеку за много лет до
нашей эры. Еще древние греки, римляне, египтяне, индийцы и китайцы использовали
его как пряность и лекарство. Первое упоминание о целительной силе фенхеля
можно найти у Плиния [26]. Как и любая пряность, фенхель тоже имеет свою
историю. В 490 году до н.э. в битве с персами одержавшие победу греки обратили
внимание на сладко пахнущую траву, которая росла возле поля боя. Так фенхель
стал символом воинской победы и успеха, а в честь места, где была битва, его
назвали "марафон" [30].
Долгое время считалось, что фенхель оказывает, необыкновенно
сильное влияние на восстановление зрения. Фенхелем лечили катаракту,
конъюнктивиты и т. д. «И прозреешь, и похудеешь» - утверждали в старину, ибо
греческое название фенхеля - marathron происходит, видимо, от глагола,
означающего «худеть». Древние считали, что отвар из корня фенхеля изгоняет
«плод из утробы», дробит камень, открывает закупорку печени [26]. Авиценна
говорил, что если человек, начиная с первого весеннего дня, когда солнце
вступает в созвездие Овна, и вплоть до того дня, когда оно вступит в созвездие
Рака, то есть до первого летнего дня, будет съедать ежедневно по 4,5 г семян
фенхеля с равным количеством сахара, то в течение года он будет здоровым [39].
В истории британской медицины, упоминается лекарство Стефенсона,
которое помогало при лечении почечных и почечнокаменных болезней, а его
основным компонентом был фенхель. В индийских ресторанах после обеда часто
подают семена, обваленные в сахаре, как десерт и освежитель дыхания [21].
В более близкие нам времена эфирное масло плодов фенхеля входило в
знаменитые "капли датского короля", употреблявшиеся против кашля и
представлявшие собой не что иное, как раствор эфирного масла в воде с
добавлением лакрицы и нашатыря. Плоды фенхеля под названием "семена
встреч" заменяли нашим предкам жевательную резинку [30].
Существуют две разновидности этого растения - фенхель
обыкновенный, или аптечный, волошский укроп; и итальянский (флорентийский), или
овощной, фенхель, сладкий анис.
3. Морфолого-анатомическая характеристика фенхеля обыкновенного
.1 Макроскопическая характеристика
Русские названия: фенхель обыкновенный,
волошский, аптечный укроп, сладкий укроп.
Украинское название: фенхель звичайний.
Английское название: Fennel.
Французское название: Fenouil sauvage, Aneth doux, Fenouil commun.
Фенхель обыкновенный (Foeniculum vulgare Mill.) - дву- или
многолетнее травянистое растение семейства сельдерейных (Apiaceae).
Корень стержневой, веретеновидный, толстый, мясистый,
желтовато-белого цвета. Стебель прямой, круглый, тонкоребристый, очень
ветвистый, особенно наверху, с синеватым налётом, высотой до 2 м. Листья
очередные, черешковые, по краям с пленчатыми влагалищами,
яйцевидно-треугольные, трижды- или четыреждыперисто-рассеченные, отдельные
дольки листа узколинейные или нитевидные, оттопыренные. Нижние листья крупные,
длинночерешковые, средние и верхние - сидячие на узкопродолговатых по краям
пленчатых влагалищах. Все растение покрыто сизым налетом. Цветки мелкие, с
желтыми лепестками, собраны в сложные зонтики, достигающие до 20 см в диаметре,
без обертки и оберточки. Плод - буровато-серая продолговатая, в верхней части
слабо утолщенная двусемянка длиной 6-14 мм, толщиной 3-4 мм с пятью рёбрами.
Масса 1000 семян - 3-4 г.
Несмотря на внешнюю схожесть с укропом, запах и вкус фенхеля
совсем не укропные, а скорее анисовые. Цветет в июне - августе, плоды созревают
в сентябре - октябре [24, 31,37].
3.2 Микроскопическая характеристика
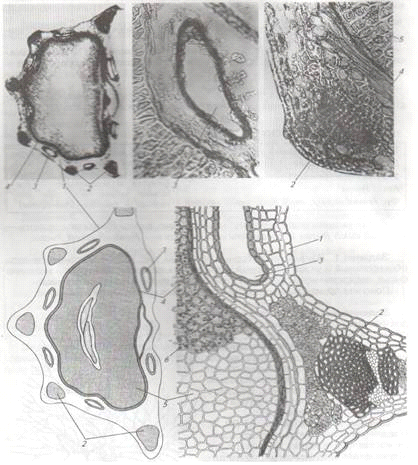
Рис. 1.2 Микроскопия плода фенхеля
Примечание: 1 - однослойный экзокарпий; 2 -
сосудисто-волокнистые проводящие пучки в мезокарпии ребрышек; 3 - крупные
эфиромасличные канальцы в межреберьях околоплодника: с наружной стороны -
четыре, с внутренней - два; 4 - эндокарпий желто-коричневого цвета, сросшийся с
семенной кожурой; 5 - клетки эндосперма семени с алейроновыми зернами и каплями
эфирного масла; 6 - клетки с мелкими друзами[14].
4. Распространение и биологические особенности
культивирования фенхеля обыкновенного
Родиной фенхеля обыкновенного считают страны Средиземноморья,
в частности Италию, где его, начиная с античных времен выращивали как
лекарственное растение, а потом и как овощную культуру. Об итальянском происхождении
фенхеля говорит и его, сохранившееся до сих пор, старинное русское название
"волошский укроп", которое происходит от древнерусского
"волохи" - общего названия романских народов.
В Среднюю Европу попал еще в средних веках. В России фенхель
стали разводить с XVII века как лекарственное растение.
Фенхель обыкновенный - пряная (листья), эфиромасличная
(семена) и лекарственная (масло, семена) культура, культивируемая на Украине, в
России, на юге Африки, в Молдавии, Южной и Западной Европе, в Китае, Новой
Зеландии, Восточной Индии, Японии, Южной Америке (особенно в Аргентине), но в
одичавшем состоянии встречается в Крыму, Средней Азии и Закавказье. Существует
5 видов, произрастающих, в основном, в Европе и Африке.
Произрастает на сухих каменистых склонах, по канавам,
травянистым местам, а также около дорог и жилья, на сорных местах. Опыляется
насекомыми. Хороший медонос.
Возделывание
В культуре фенхель одно-двулетнее растение. Любит тепло и
свет, к почвам нетребователен, поэтому хорошо зимует в южных регионах.
Продолжительность вегетационного периода 130-170 дней, сумма активных
температур должна быть не менее 2500 °С. Растения начинают
цвести в первый год. Размножается семенами, реже - делением куста. Семена
начинают прорастать при температуре 6-8°С. Всходы появляются через 12-14 дней.
Переносит заморозки до - 8°С. Цветение растянуто и продолжается с июня по
август. Плоды созревают в августе - начале сентября, созревшие легко осыпаются
[21].
Заготовка и сушка сырья
Цветение растения и созревание плодов происходит
неодновременно, поэтому сбор плодов производится в два срока: вначале собирают
центральные зонтики, как только они начинают желтеть, затем срезают все
растение, когда созревают плоды на большинстве зонтиков (вполне развитые плоды
остальных зонтиков еще зеленые). Урожай убирают механизированно или вручную.
Растения, собранные в пучки, дозревают и высыхают при ясной погоде - в поле,
при пасмурной - в специальных сушилках. Срок годности сырья 3 года. Вкус сырья
сладковатый, пряный, запах сильный анисовый, ароматный. Хранят плоды фенхеля
отдельно от других видов сырья в сухом, хорошо проветриваемом помещении [25].
Элементы агротехники
Технология возделывания фенхеля
обыкновенного во многом сходна с технологией выращивания укропа. Высевают
семена рядовым способом с междурядьями 50 см или ленточным - с расстоянием
между рядами в ленте 20 см, между лентами - 50 см и растениями в ряду - 8-10
см. Семена хорошо сохраняют всхожесть в течение 2-3 лет. За вегетационный
период проводят 2-3 междурядные обработки и прополки. При выращивании на
низкоплодородных почвах проводят 1-2 подкормки азотными удобрениями. Наиболее
распространенный сорт фенхеля - Балонский, в нашей стране возделывают фенхель
сортов Перечный, Огородный и Гребневый и эфирномасличные: Крымский, Черновицкий.
Выращивают также сорта зарубежной селекции: Итальянский крупный, Сицилийский
[4,32].
5. Химический состав
Все растение содержит эфирное масло, количество которого в
различных органах неравномерно. На диаграмме (Рис. 1.3.) приведено содержание
эфирного масла в различных надземных органах фенхеля обыкновенного.
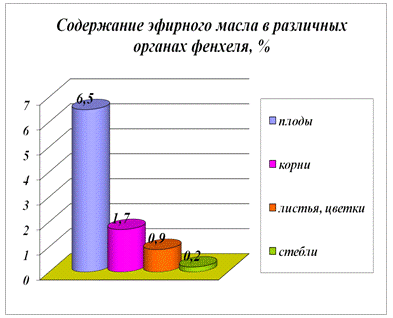
Рис. 1.3 Содержание эфирного масла в различных органах
фенхеля
Корни содержат органические кислоты, эфирное масло (1,7%),
полиацетиленовые соединения, кумарины.
В надземных частях имеются эфирное масло (0,27-5%), кумарины
(до 1,28%), флавоноиды (0,9%); в стеблях - органические кислоты, эфирное масло
(0,2-1,1%), флавоноиды, антоцианы [33].
В листьях и цветках обнаружены флавоноиды, органические
кислоты, витамин С (до 130 мг %), каротин, (10 мг %), эфирное масло (до 0,9%).
Плоды фенхеля содержат белки (до 20%), сахара (5%), до 6,5 %
эфирного масла с характерным ароматным запахом и сладковато-пряным вкусом, в
состав которого входят: анетол (до 68 %), а-пинен, а-фелландрен, лимонен,
цинеол, n-цимол, метилхалвикол (до 10 %), терпинолен, камфора, фенхон (до 20
%), борнилацетат, цитраль, анисовый альдегид, следы анисовой кислоты и другие
соединения [35]. Кроме того, в плодах фенхеля содержится до 18 % жирного масла,
состоящего из глицеридов петрозелиновой, олеиновой, линолевой и пальмитиновой
кислот.
В плодах содержатся: зола - 6,48 %;
макроэлементы (мг/г); К - 20,60, Ca - 21,10, Mn - 5,80, Fe -
0,20;
микроэлементы (КБН): Мg - 0,11, Cu - 1,05, Zn - 0,48, Cr - 0,02,
Al -0,03, Se - 10,70, Ni - 0,03, Sr - 0,42, Pb - 0,04. В - 0,60 мкг/г; не
обнаружены Со, Mo, V, Cd, Li, Ag, Au, Ва; концентрирует Cu, Se [34].
В 100 граммах фенхеля содержиться, г: белки - 15.8,жиры -
14.9; углеводы - 52.3; клетчатка - 15.7; вит. В1 -0,41; вит. С - 12; вит. В2
-0.35; вит. А- 0,011[7,9,24].
6. Фармакологические свойства и применение
фенхеля обыкновенного
Спектр фармакологического действия фенхеля обыкновенного
достаточно широк:
Эффективен для ликвидации кишечных газов и симптомов метеоризма.
Оказывает антиспастическое действие на мышечные ткани ЖКТ.
Улучшает пищеварение, обладает, обволакивающим действием.
Снимает боль в желудке, очень помогает при невротической
диспепсии.
Обладает слабительным действием.
Оказывает антибактериальный и противовоспалительный эффект.
Способствует отхождению мокроты.
Успокаивает нервную систему.
Оказывает лактогенное действие.
Стимулирует половое развитие при инфантилизме.
Снимает боль при болезненной менструации.
Заживляющее, антиоксидантное.
Глистогонное, мочегонное, ветрогонное.
Расширяет сосуды сердца .
Неоспоримы и дезинфицирующие свойства фенхеля. Отваром семян
его промывают глаза при конъюнктивитах, кожу при гнойничковых заболеваниях .
Эфирное масло фенхеля великолепно очищает организм, выводит
шлаки и токсины, особенно у тех, кто увлекается обильной едой и алкоголем.
Обладает мочегонным и мягким слабительным действием.
Воздействуя на пищеварительную систему, устраняет запоры, метеоризм, тошноту.
Из семян в аптеках раньше готовили «укропную воду» для грудных и маленьких
детей, используемую при вздутии живота. Эфирное масло и масло «фенхелевое»
назначают как отхаркивающее, жаропонижающее, противогрибковое и корригирующее
средство. Оно входит в комплексный препарат «солутан», применяемый при бронхитах
и бронхиальной астме [11].
Эффективно масло фенхеля и в климактерический период [12],
так как стимулирует выработку собственного эстрогена. Способствует увеличению
лактации, поэтому его рекомендуют кормящим женщинам. Наряду с этим, фенхель
обладает высокой противогрибковой активностью. При санации помещений снижает
содержание грибков в атмосфере в 4-5 раз [2,31].
Масло фенхеля обладает гепатозащитным действием при
токсических поражениях печени [11]. Повышает аппетит, секрецию пищеварительных
и бронхиальных желез. Оказывает благотворное влияние на кожу. Полоскание
ротовой полости отваром фенхеля устраняет боль в горле и охриплость голоса
[13]. Фенхель широко используется в диете больных сахарным диабетом. Кашица из
зеленой травы используется для удаления веснушек и кровоподтеков в
косметологии.
Фенхелевое масло используется и в ароматерапии, так как
обладает биоэнергетическим действием. В частности, выводит из эмоционального
кризиса, восстанавливает душевное равновесие, препятствует возникновению
чувства одиночества, обостряем ум [2].
Противопоказания: фенхель в любых видах
противопоказан при беременности, так как анетол стимулирует мускулатуру матки!
Информация о лекарственных препаратах на основе фенхеля
представлена в таблице.
Таблица 1. Характеристика лекарственных препаратов на основе
фенхеля
|
Название ЛП
|
ЛФ, доза
|
Состав
|
Производитель
|
Показания и
применение
|
|
Плантекс
|
Гран. раств.
250 мг/5 г пакетик 5 г, № 1, № 10, № 50
|
Экстракта
фенхеля 250 мг; эфирное масло фенхеля с минимальным содержанием анетола 0,5 г,
фенхона 0,2 г
|
Lek, Словения
|
Нарушение
пищеварения у детей (спастические боли в кишечнике, метеоризм). Профилактика
метеоризма у детей.
|
|
Софтовак
|
Порошок для
приема внутрь по 100 г в пластиковом флаконе
|
Подорожника
яйцевиднолистного листьев экстракт сухой- 40 г; сенны индийской листьев
экстракт сухо - 15 г; миробалана чебуля плодов экстракт сухой - 10 г; кассии
дудчатой плодов экстракт сухой- 10 г; солодки голой корней экстракт сухой- 5
г; шиповника столистного цветков экстракт сухой- 5 г; фенхеля обыкновенного
плодов экстракт сухой- 5 г; масло фенхеля - 1 г
|
"Люпин
Лтд.", Индия
|
Запор,
регулирование стула при геморрое, проктите, анальных трещинах.
|
|
Гастрофит
|
Сбор в
упаковках по 100 г
|
Кора крушины,
ромашки цветки, тысячелистника трава, календулы цветки, фенхеля масло
|
Эйм, Украина
|
Дискинезия
желчевыводящих путей, атонический запор, метеоризм.
|
|
Д-р Тайс
леденцы Анис и фенхель+ вит С*
|
Леденцы
|
Анисовое масло,
масло фенхеля, масло мяты перечной, ментол, изомальт, аскорбиновая кислота,
аспартам, ароматизатор медовый, ароматизатор кокосовый, карамель
|
Doctor Theiss
Naturwaren, Германия
|
Кашель, боль в
горле, охриплость голоса, метеоризм, спазм кишечника и других нарушениях ЖКТ
|
|
Холенорм
фитоконцентрат
|
Капли для
приема внутрь
|
Экстракты из
листьев зеленого чая, листьев мяты перечной, травы зверобоя, травы полыни,
плодов фенхеля, цветов бессмертника песочного, кукурузных рылец.
|
ООО
"Екомед", Украина
|
Гипертоническая
болезнь;атеросклероз; нарушение мозгового кровообращения;эндартериит;
ангиопатия.
|
|
Чистосил*
|
Таблетки по 500мг,
50 таблеток во флаконе
|
Подорожник
(семена) - 250мг, мята - 10мг, фенхель - 25мг, солодка (корень) - 50мг,
пектин - 25мг, лактоза - 135мг, стеарат Са - 5мг
|
Украина, ЧП
«Рослина Карпат»
|
Хронический
запор, диcбактериоз, синдром раздраженной толстой кишки, хронический колит
|
|
Фитоглистоцид*
|
Капсулы № 90
|
Плоды фенхеля
обыкновенного, трава тимьяна ползучего, тысячелистника обыкновенного, плоды
гвоздики ароматной, цветки пижмы обыкновенной, корни куркумы длинной, листья
ореха грецкого, корни валерианы лекарственной, корни солодки голой, чеснок
огородный.
|
Украина, ЧП
"Компания "Дана, Я"
|
Диетическая
добавка в рационе питания как источник витаминов С, В1, рутина, каротина,
минеральных веществ, органических кислот с целью профилактики и смягчения
протекания заболеваний органов пищеварения;имеет глистогонные свойства,
спазмолитическое, слабительное, противовоспалительное действие; способствует
улучшению функции печени и желчного пузыря;
|
|
Бебинос
|
Кап. д/перорал.
прим. фл.-капельн. 30 мл
|
Экстракт жидкий
спиртовой (1:1) из горького фенхеля - 320 мг/г; Экстракт жидкий спиртовой
(1:1) из кориандра - 200 мг/г; Экстракт жидкий спиртовой (1:1) из цветков
ромашк - 200 мг/г.
|
Dentinox
Германия
|
Метеоризм,
кишечная колика (у грудных детей, детей младшего и школьного возраста, в т.ч.
связанные с переходом на искусственное вскармливание)
|
|
Уголь
карбоактив активир.мята,фенхель*
|
Таб. 0.25г N10
|
|
Украина,Фармаком,
Харьков
|
Улучшает
секреторной функцию кишечника;уменьшает процессы брожения и газообразования
|
Хозяйственное использование
Фенхелевое масло используют в парфюмерно-косметическом
производстве и пищевой промышленности для ароматизации кондитерских изделий,
маринадов, чая. В ликероводочной промышленности для ароматизации алкогольных
напитков, в частности ликеров и абсентов, иногда используется вместо
можжевельника для ароматизации джина.
В кулинарии листья употребляют как пряную приправу для
салатов, супов, мясных, рыбных и овощных блюд, при засолке огурцов. Плоды
фенхеля содержат масло, которое применяют как заменитель масла какао. Они
входят в состав пряных смесей карри, в европейскую смесь для рыбы [4].
1. Анализ литературных данных свидетельствует о богатом
химическом составе и широком использовании в медицине фенхеля обыкновенного.
2. Данные литературы относительно химического состава и
биологической активности свидетельствуют, что фенхель является перспективным
для углубленного фармакогностического изучения с целью создания новых
лекарственных средств.
7.Фитохимическое изучение травы фенхеля
обыкновенного
Для проведения идентификации отдельных групп БАВ нами были
получены вытяжки из ЛРС - объектов исследования.
Для получения водных экстрактов 5,0 г
сухого сырья, измельченного до размера частиц 2-3 мм, заливали 25 мл воды (1:5)
и нагревали с обратным холодильником на кипящей водяной бане в течение 1 ч.
Полученное извлечение отфильтровывали через складчатый фильтр. Экстракцию сырья
проводили дважды новыми порциями растворителя. Объединенный экстракт
использовали для определения углеводов, аминокислот, органических кислот,
дубильных веществ, гидроксикоричных кислот.
Водно-спиртовые экстракты получали
аналогично. В качестве экстрагента использовали 70% спирт этиловый.
Водноспиртовые извлечения использовали для определения кумаринов, флавоноидов и
сапонинов.
7.1 Общие реакции на гликозиды
Реакция с реактивом Фелинга. В две мерные пробирки
наливали по 2 мл водного извлечения, в одну из них добавляли 5 к.
концентрированной хлористоводородной кислоты, а в другую равное количество воды
очищенной. Нагревали на кипящей водяной бане в течение 15 минут.
Подкисленный раствор нейтрализовали 10% раствором едкого
калия до рН 7 по универсальному индикатору, а объем другой пробирки доводили
водой очищенной до объема первой пробирки. К растворам в пробирках добавляли по
2 мл реактива Фелинга, кипятили в течение 1 минуты, оставляли в штативе на 10
минут и сравнивали объемы выпавшего кирпично-красного осадка закиси меди,
свидетельствующего о наличии углеводов.
Наблюдения: объем выпавшего осадка в пробирке после
проведения кислотного гидролиза намного больше осадка, выпавшего в пробирке без
гидролиза.
Реакция с β-нафтолом. К 2 мл водного
извлечения прибавляли 3 к. 20% спиртового раствора β-нафтола и осторожно по стенкам пробирки прибавляли 2 мл
концентрированной сульфатной кислоты.
Наблюдения: на границе раздела слоев жидкости появлялось
вишнево-красное кольцо, свидетельствующее о наличии веществ гликозидного
характера. При стоянии окраска перешла в фиолетовую.
Обнаружение полисахаридов
В мерный цилиндр вместимостью 25 мл помещали 10 мл 96% этанола
и постепенно прибавляли 2 мл исследуемого извлечения.
Наблюдения: появление аморфного осадка свидетельствует о
присутствии полисахаридов в изучаемом извлечении.
Обнаружение аминокислот
С 1% спиртовым раствором нингидрина. При нагревании водного
извлечения с 1% спиртовым раствором нингидрина образуется фиолетово-сиреневое
окрашивание, что свидетельствует о наличии аминокислот в исследуемом сырье.
Хроматографическое изучение аминокислотного
состава
Аминокислоты идентифицировали в водном экстракте в сравнении
с 0,01% растворами референтных образцов 14 аминокислот. В качестве подвижной
фазы была выбрана система растворителей бутанол-уксусная кислота-вода (БУВ)
(4:1:2). По характерному фиолетовому окрашиванию пятен после обработки 0,2%
раствором нингидрина в спирте с последующим нагреванием до 100°С были
идентифицированы следующие аминокислоты: аланин, аспарагин, валин, серин,
треонин, фенилаланин.
Схема хроматограммы представлена на рисунке 2.1.
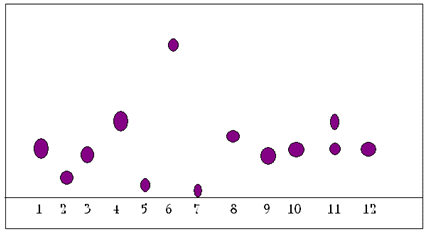
Рис. 2.1 Схема хроматограммы аминокислот в водном извлечении
травы фенхеля
Примечание: 1 - аланин, 2 - аргинин, 3 - аспарагин, 4
- валин, 5 - гистидин, 6 - изатин, 7 - орнитин, 8 - пролин, 9 - серин, 10 -
треонин, 11 - вытяжка из травы фенхеля, 12 - фенилаланин.
Обнаружение дубильных веществ
Реакция с 1% раствором желатина. К 2 мл водного извлечения
изучаемого сырья прибавляли несколько капель 1% раствора желатина.
Наблюдения: появилась муть, исчезающая при добавлении избытка
желатины.
Реакция с раствором железоаммониевых квасцов. К 2 мл водного
извлечения изучаемого сырья прибавляли 4к. раствора железоаммонийных квасцов.
Наблюдения: появлялось черно-зеленое окрашивание, что
свидетельствует о наличии конденсированной группы дубильных веществ.
Обнаружение
гидроксикоричных кислот
Гидроксикоричные кислоты в сырье изучали методом тонкослойной
хроматографии в системе растворителей 15% кислота уксусная. Пятна кислот имели
голубую флуоресценцию в УФ-свете. После обработки парами аммиака голубая
флуоресценция усилилась. Схема хроматограммы водного извлечения представлена на
рисунке 2.2.
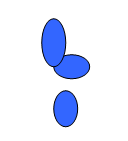
Рис 2.2 Схема хроматограммы обнаружения гидроксикоричных
кислот в водном извлечении травы фенхеля
Как видно из рисунка 2.2. в результате хроматографического
анализа водного извлечения травы фенхеля в сравнении со значениями Rf,
приведенными в литературных источниках [10], были идентифицированы феруловая,
хлорогеновая и неохлорогеновая кислоты.
Обнаружение органических кислот
Органические кислоты изучали методом тонкослойной
хроматографии в системе растворителей эилацетат-уксусная кислота-муравьиная
кислота-вода (100:11:11:25) в сравнении с референтными образцами органических
кислот (в виде 0,1% водного раствора). Высушенные пластины обрабатывали
раствором смеси бромфенолового синего и метиленового красного (0,3 г
бромфенолового синего, 0,1 г метиленового красного в 100 мл хлороформа).
Кислоты проявились в виде желтых пятен на синем фоне. Схема
хроматограммы обнаружения органических кислот представлена на Рис. 2.3.
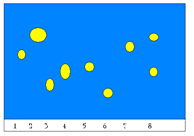
Рис. 2.3. Схема хроматограммы обнаружения органических кислот
в водном извлечении травы фенхеля
Примечание: 1 - яблочная кислота, 2- валериановая, 3
- щавелевая, 4 - лимонная, 5 - аскорбиновая, 6 - винная, 7 - янтарная, 8 - водное
извлечение травы фенхеля.
Данные рисунка 2.3. свидетельствуют о присутствии
валериановой, лимонной и аскорбиновой кислот в сырье фенхеля обыкновенного.
Обнаружение кумаринов
Приготовление вытяжки. 3,0 г измельченного сырья помещают в
колбу на 100 мл со шлифом, заливают 30 мл 95%-го спирта этилового, колбу
закрывают обратным холодильником и кипятят на водяной бане 20 минут. После
охлаждения вытяжку фильтруют и используют для проведения качественных реакций.
Лактонная проба. К 5 мл полученного раствора прибавляли 5
к. 10% раствора калия гидроксида и нагревали на водяной бане в течение 5 минут.
Наблюдения: появлялось желтое окрашивание.
Затем к окрашенному раствору прибавляли 10 мл воды очищенной
и 10к. 10% кислоты хлористоводородной.
Наблюдения: раствор обесцветился и появилась муть.
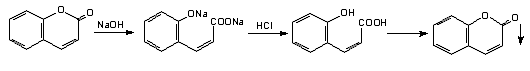
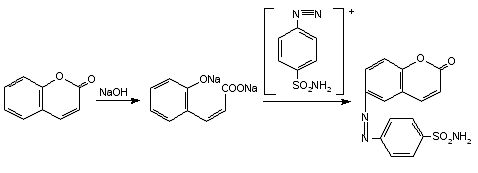
Реакция со щелочью и диазореактивом. К 3 мл полученного
раствора прибавляли 5к. 10% раствора калия гидроксида и нагревали на водяной
бане несколько минут.
Наблюдения: содержимое пробирки окрасилось в желтый цвет.
Затем к окрашенному раствору прибавили 5к.
свежеприготовленной диазотированной сульфаниловой кислоты.
Наблюдения: раствор приобрел красно-оранжевое окрашивание.
Обнаружение флавоноидов
Цианидиновая реакция по Брианту. К 2 мл водно-спиртового
извлечения изучаемого сырья прибавляли 5-7к. концентрированной
хлористоводородной кислоты и 10-15 г металлического магния.
Наблюдения: появлялось розовое окрашивание, указывающее на
присутствие веществ флавоноидной природы.
К окрашенному раствору прибавляли 1 мл бутанола и встряхивали
пробирку.
Наблюдения: органическая фаза приобретала розовое окрашивание
более слабое, чем окрашивание водной фазы, что говорит о преобладании
гликозидов над агликонами.
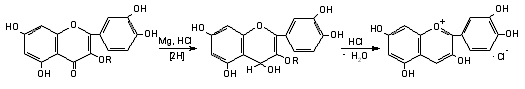
Хромонол Цианидин
Реакция с 10% раствором железа (III) хлорида (на
фенольные гидроксилы). К 1 мл водно-спиртового извлечения изучаемого сырья
прибавляли 1-2к. 10% раствора железа (III) хлорида.
Наблюдения: появлялось темно-зеленое окрашивание.
Реакция со щелочью. К 1 мл водно-спиртового
извлечения изучаемого сырья прибавляли 2 мл 10% водно-спиртового раствора
гидроксида калия.
Наблюдения: интенсивность окраски усилилась.
Реакция с раствором алюминия хлорида. К 1 мл водно-спиртового
извлечения изучаемого сырья прибавляли 1 мл 2% раствора алюминия хлорида.
Наблюдения: появилось желтое окрашивание.
Реакция с раствором свинца ацетата. К 1 мл водно-спиртового
извлечения изучаемого сырья прибавляли 1 мл 10% раствора свинца ацетата.
Наблюдения: выпал желтый осадок.
7.2 Хроматографический анализ флавоноидного
состава
Флавоноиды в траве фенхеля изучали с помощью тонкослойной
хроматографии в двух системах растворителей: 1) н-бутанол - уксусная кислота -
вода (4:1:2) и 2) хлороформ - уксусная кислота - вода (13:6:2) в сравнении с
достоверными образцами флавоноидов в виде 0,5% спиртовых растворов.
Идентификацию флавоноидов проводили в УФ и видимом свете до и после обработки
2% спиртовым раствором алюминия хлорида. Пятна флавоноидов окрашивались в
грязно-желтый цвет и имели желтую флуоресценцию. Схемы хроматограмм
флавоноидного состава представлены на рисунке 2.4. и 2.5.
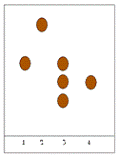
Рис. 2.4
Рис.2.5
Примечание: 1 - гиперозид, 2 - кверцитин, 3 - вытяжка
из травы фенхеля, 4 - рутин.
Таким образом, было установлено, что трава фенхеля содержит
гиперозид, рутин и одно неидентифицированное вещество флавоноидной природы.
Обнаружение сапонинов
Проба пенообразования. В пробирку помещают 3 мл
водного извлечения и энергично встряхивали в течение одной минуты.
Наблюдения: появилась устойчивая пена (8 мм), не исчезающая в
течение часа.
Реакции осаждения:
К 1 мл водного извлечения добавляют 4к. баритовой воды.
Наблюдения: появилось ярко-желтое окрашивание, усиливающееся
при стоянии.
К 1 мл водно-спиртового извлечения добавляли 4к. 10% раствора
плюмбума ацетата.
Наблюдения: появляется муть и осадок желто-бурого цвета.
К 1 мл водно-спиртового извлечения добавляли 1 мл 1%
спиртового раствора холестирина.
Наблюдения: происходит помутнение вытяжки.
Цветные реакции:
Реакция Сальковского. К 2 мл водно-спиртового
экстракта прибавляли 1 мл хлороформа и 5к. концентрированной сульфатной
кислоты.
Наблюдения: появлялась буро-краная окраска.
Реакция Лафона. К 2мл водно-спиртового
извлечения в пробирке прибавляли 1к. 10% раствора сульфата меди, 1мл
концентрированной сульфатной кислоты и осторожно нагревали.
Наблюдения: раствор окрасился в сине-зеленый цвет .
Определение химической природы сапонинов:
В одну из пробирок поместить 5 мл 0,1М
раствора хлористоводородной кислоты, а в другую - 5 мл 0,1М раствора гидроксида
натрия. В обе пробирки прибавили по 3к. водного извлечения. Встряхивали в
течение 1 минуты.
Наблюдения: в первой пробирке высота столбика пены - 1,5 см,
пена рыхлая; во второй пробирке - 1,3 см, пена плотная, что свидетельствует о
присутствии сапонинов тритерпеновой природы.
С помощью качественных реакций и хроматографических методов
анализа в траве фенхеля были обнаружены вещества гликозидной природы,
полисахариды, гидроксикоричные кислоты, органические кислоты, аминокислоты,
кумарины, флавоноиды, конденсированные дубильные вещества, сапонины. Данные
представлены в таблице 2.
Таблица 2. Обобщенная таблица идентификации БАВ в сырье
фенхеля обыкновенного
|
Качественный
состав водной вытяжки
|
|
Углеводы
|
Дубильные
вещества
|
Аминокислоты
|
|
С реактивом
Феллинга
|
+ +
|
С железоам-
монийными квасцами
|
+
|
С 1% спиртовым
раствором нингидрина
|
+
|
|
С α - нафтолом (на инулин)
|
- +
|
С 1% р-ром
желатины
|
-
|
|
|
|
Качественный состав
водно-спиртовой вытяжки
|
|
Флавоноиды
|
Сапонины
|
Кумарины
|
|
Цианидиновая
проба
|
+
|
Реакция
пенообра- зования
|
+ +
|
Лактонная проба
|
+
|
|
С 1% р-ром FeCl3
|
+ +
|
С р-ром ацетата
свинца
|
+ +
|
С
диазореактивом
|
+
|
|
C
10% р-ром КОН
|
+
|
Реакция
Сальковского
|
+ -
|
|
|
|
С 2% р-ром AlCl3
|
+
|
С 1% р-ром
холестерина
|
+ +
|
|
|
|
C р-ром ацетата свинца основного
|
+ +
|
Реакция Лафона
|
+
|
|
|
8. Определение количественного содержания
биологически активных веществ в сырье фенхеля обыкновенного в зависимости от
фазы вегетации
.1 Определение содержания полисахаридов
г сырья помещали в колбу со шлифом вместимостью 250 мл,
добавляли 200 мл воды очищенной, колбу присоединяли к обратному холодильнику и
кипятили при перемешивании в течение 30 минут. Экстракцию повторяли еще дважды,
используя первый раз 200 мл, второй - 100 мл воды. Водные экстракты объединяли,
центрифугировали и надосадочную жидкость декантировали в мерную колбу
вместимостью 500 мл через 5 слоев марли, вложенной в стеклянную воронку
диаметром 55 мм и предварительно промытую водой. Фильтры промывали водой и
доводили объем водой до метки (раствор А). 25 мл раствора А переносили в
центрифужную пробирку, добавляли 75 мл 95% спирта, перемешивали, подогревали на
водяной бане до 30ºС в течение 5 минут.
Через 1 час содержимое пробирки центрифугировали с частотой вращения 5000
об/мин в течение 30 минут. Надосадочную жидкость фильтровали под вакуумом при
остаточном давлении 13-16 кПа через высушенные до постоянной массы при
температуре 100-105ºС стеклянный фильтр
ПОР-16 диаметром 40 мм. Осадок количественно переносили на фильтр,
последовательно промывая 15 мл раствора 95% спирта в воде (3:1), 10 мл ацетона
и 10 мл этилацетата. Фильтр с осадком высушивали на воздухе, а потом при
температуре 100-105ºС до постоянной массы.
Содержание полисахаридов (Х, %) в пересчете на абсолютно
сухое сырье рассчитывали по формуле:
(m2 - m1) * 500 * 100 * 100
Х = -----------------------------------,
m * 25 * (100 - W)
где m1 - масса фильтра, г;2 - масса
фильтра с осадком, г;- масса сырья, г;- потеря в массе при высушивании, %.
Результаты определения содержания полисахаридов в
представлены в таблице 3.
Таблица 3. Содержание полисахаридов в объектах исследования
(среднее из 5 измерений)
|
ЛРС
|
Хср
|
Доверительный
интервал, %
|
ε, %
|
|
Трава в фазе до
цветения
|
3,43
|
3,4262±0,024401
|
0,71
|
|
Трава в фазе
цветения
|
6,86
|
6,8636±0,03719
|
0,54
|
|
Трава в фазе
зеленого плодоношения
|
3,00
|
3,002±0,144083
|
4,79
|
|
Плоды
|
4,91
|
4,9094±0,212677
|
4,33
|
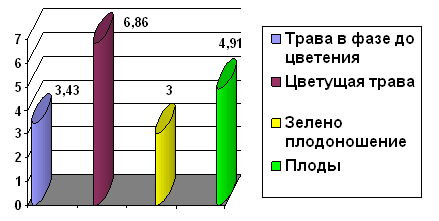
Рис. 3.1. Диаграмма содержания полисахаридов в объектах
исследования, %
Как видно из данных таблицы и диаграммы максимальное
количество полисахаридов накапливается в траве в фазе цветения. Для удобства
восприятия мы представили результаты в виде диаграммы (Рис. 3.1).
8.2 Изучение фракционного состава полисахаридов
Полисахариды - обширная группа веществ первичного синтеза,
которая оъединяет разнообразные соединения, различные не только по
физико-химическим свойствам, но и по направленности действия. Поэтому следующим
этапом нашей работы стало изучение фракционного состава группы полисахаридов в
плодах фенхеля обыкновенного. Выбор объекта исследования мотивирован наибольшей
рентабельностью переработки.
Изучение фракционного состава полисахаридов проводили по
следующей методике. Из шрота, оставшегося после получения липофильным фракции,
последовательно выделяли спирторастворимые (СРПС), водорастворимые (ВРПС)
фракции полисахаридов, пектиновые вещества (ПР) и гемицеллюлозу (ГЦ).
г воздушно-сухого шрота экстрагировали 82% спиртом этиловым
(при соотношении сырье-экстрагент 1:10) при нагревании на водяной бане в
течение 2 часов, периодически взбалтывая для смывания частиц сырья со стенок
колбы. Экстракцию проводили дважды. Полученные вытяжки отделяли от сырья,
фильтровали, объединяли, упаривали до минимального объема, который высушивали в
сушильном шкафу до постоянной массы и взвешивали. Получали фракции СРПС.
Воздушно-сухой шрот сырья, оставшегося после получения СРПС,
использовали для получения ВРПС. Шрот экстрагировали 200 мл горячей воды при
нагревании до 95°С в течение 1 ч при постоянном перемешивании.
Повторное экстрагирование проводили в соотношении сырье-экстрагент 1:10.
Полученные вытяжки объединяли и упаривали до 1 / 5 первоначального объема.
Полисахариды осаждали трехкратным количеством 96% этанола. Осадок
отфильтровывали, последовательно промывали 96% этанолом, ацетоном, эфиром,
высушивали до постоянной массы и взвешивали. Получали фракцию ВРПС.
Из шрота, оставшегося после получения СРПС, ВРПС, выделяли
ПР. Экстракцию сырья проводили дважды смесью 0,5% растворов кислоты оксалатной
и аммония оксалата (1:1) в соотношении сырье-экстрагент 1:20 при температуре
80-85°С
в течение 2 ч. Полученные вытяжки объединяли, концентрировали и осаждали
пятикратным количеством 96% этанола. Полученные осадки отфильтровывали,
промывали этанолом, высушивали до постоянной массы и взвешивали. Получали
фракции ПР.
ГЦ выделяли из шрота, оставшегося после последовательного
получения СРПС, ВРПС и ПР. Экстракцию проводили дважды 7% раствором натрия
гидроксида в соотношении сырье-экстрагент 1:5 при комнатной температуре в
течение 12 ч. Щелочные экстракты объединяли, добавляли двукратное количество
96% этанола. Осадок отфильтровывали, промывали этанолом, высушивали до
постоянной массы и взвешивали. Получали фракции ГЦ. Результаты изучения
фракционного состава представлены в таблице 4 и на диаграмме (Рис. 3.2).
Таблица 4. Содержание фракций полисахаридов в плодах фенхеля
обыкновенного
|
Фракции
полисахаридов
|
Содержание, г/
10 г сырья
|
|
СРПС
|
1,1912
|
|
ВРПС
|
0,1417
|
|
ПВ
|
0,5997
|
|
ГЦ
|
0,9365
|

Рис. 3.2. Диаграмма содержания фракций полисахаридов в плодах
фенхеля обыкновенного
Как видно из полученных данных в плодах фенхеля обыкновенного
в максимальном количестве накапливается спирторастворимая фракция
полисахаридов.
8.3 Определение содержания гидроксикоричных
кислот
,0 г (точная навеска) измельченного сырья помещали в колбу
вместимостью 200 мл и добавляли 20 мл воды очищенной. Колбу присоединяли к
обратному холодильнику и нагревали на водяной бане в течение 15 минут.
Экстракцию повторяли дважды. Экстракты объединяли и после охлаждения
фильтровали через бумажный фильтр на воронке Бюхнера.
Извлечение количественно переносили в мерную колбу
вместимостью 200 мл и доводили объем раствора водой до метки (раствор А). В
мерную колбу вместимостью 50 мл вносили 3 мл раствора А и доводили объем
раствора до метки 20% этанолом. Оптическую плотность полученного раствора
измеряли на спектрофотометре при длине волны 327 нм. Раствором сравнения служил
20% этанол. Содержание суммы гидроксикоричных кислот (Х, %) в пересчете на
хлорогеновую кислоту вычисляли по формуле:
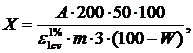
где А - оптическая плотность испытуемого раствора;- навеска сырья
в граммах;- потеря в массе при высушивании сырья, %.
e1%1см - удельный показатель поглощения
хлорогеновой кислоты, равный 531.
Результаты количественного определения гидроксикоричных кислот в
представлены в таблице 5.
Таблица 5. Содержание гидроксикоричных кислот в сырье фенхеля
обыкновенного (среднее из 5 измерений)
|
ЛРС
|
Доверительный
интервал, %
|
ε, %
|
|
Трава в фазе до
цветения
|
1,27
|
1,2674±0,042956
|
3,39
|
|
Трава в фазе
цветения
|
3,58
|
3,584±0,077557
|
2,16
|
|
Трава в фазе
зеленого плодоношения
|
1,18
|
1,183±0,058301
|
4,93
|
|
Плоды
|
0,54
|
0,5364±0,00436
|
0,81
|
|
Зонтики
|
0,99
|
0,9998±0,043152
|
4,32
|
Как видно из данных таблицы наибольшее количество
гидроксикоричных кислот накапливается в траве, собранной в фазе цветения.
8.4 Определение содержания кумаринов
,0 г (точная навеска) измельченного сырья помещали в колбу
вместимостью 200 мл, добавляли 50 мл 96% спирта этилового и кипятили в колбе с
обратным холодильником 30 минут. Смесь фильтровали, колбу и фильтр промывали
дважды 96% этанолом по 10 мл. Фильтраты объединяли, прибавляли 2 мл 10%
раствора свинца ацетата и кипятили еще 3 минуты.
Горячую смесь фильтровали, колбу дважды промывали 96%
этанолом по 10 мл. Спиртоводные вытяжки упаривали до водного остатка. Водные
вытяжки обрабатывали 4 раза хлороформом порциями по 25 мл каждая. Объединенные
хлороформные вытяжки промывали 5 мл воды, воду отделяли, хлороформные вытяжки
сушили безводным натрия сульфатом.
Натрия сульфат отфильтровывали, промывали 3 раза по 10 мл
хлороформом и раствор упаривали до сухого остатка, который растворяли в 12 мл
96% этанола.
К полученному раствору добавляли 20 мл 0,1 М раствора натрия
гидроксида и нагревали 5 минут на водяной бане при температуре 50-60°С. К охлажденному
раствору прибавляли 8 мл свежеприготовленной диазотированной кислоты
сульфаниловой и измеряли оптическую плотность окрашенного раствора на
спектрофотометре (UV/VIS 2800) в кювете с толщиной слоя 10 мм при длине волны 490 нм.
Концентрацию кумаринов в полученном растворе находили по калибровочному
графику.
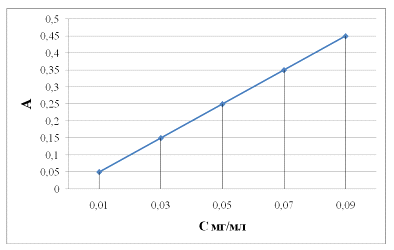
Рис. 3.3. Калибровочный график зависимости оптической
плотности от концентрации кумаринов в пересчете на умбелиферон
Количественное содержание кумаринов (Х, %) в пересчете на
абсолютно сухое сырье вычисляли по формуле:
х V x K x 100 x100
Х = ----------------------------,x 10000 x
(100 - W)
где С - концентрация, найденная по калибровочному графику,
мг/мл;- объем вытяжки, мл;
К - коэффициент разведения;- масса навески, г;- потеря в
массе при высушивании, %.
Результаты количественного определения кумаринов в объектах
исследования представлены в таблице 6.
Таблица 6. Содержание кумаринов в сырье фенхеля обыкновенного
(среднее из 5 измерений)
|
ЛРС
|
Хср
|
Доверительный
интервал, %
|
ε, %
|
|
Плоды
|
0,09
|
0,091±0,008105
|
8,91
|
|
Зонтики
|
0,11
|
0,1136±0,003688
|
3,25
|
8.5 Определение содержания суммы окисляемых
полифенолов ( по Левенталю)
Определение содержания суммы окисленных полифенолов проводили
перманганатометрическим методом в модификации по Левенталю. Около 2 г (точная
навеска) измельченного сырья, просеянного сквозь сито с диаметром отверстий 3
мм, помещали в коническую колбу вместимостью 500 мл, заливали 250 мл нагретой
до кипения воды очищенной и кипятили с обратным холодильником на электрической
плитке в течение 30 мин. Жидкость охлаждали до комнатной температуры и
процеживали около 100 мл в коническую колбу вместимостью 200-250 мл через вату.
Затем отбирали пипеткой 25 мл полученного извлечения в другую коническую колбу
вместимостью 750 мл, прибавляли 500 мл воды очищенной, 25 мл раствора
индигосульфокислоты и титровали при постоянном перемешивании раствором
перманганата калия (0,02 моль/л) до золотисто-желтого окрашивания. Параллельно
проводили контрольный опыт.
Содержание суммы окисляемых полифенолов (Х, %) в
пересчете на абсолютно сухое сырье вычисляли по формуле:
(V - V1) . 0,00582 . 250 .
100 . 100
Х = -------------------------------------------,.
25 . (100 - W)
где V - объем раствора перманганата калия (0,02 моль/л),
израсходованный на титрование извлечения, мл;1 - объем раствора
перманганата калия (0,02 моль/л), израсходованный на титрование в контрольном
опыте, мл;
,00582 - количество дубильных веществ, соответствующее 1 мл
раствора перманганата калия (0,02 моль/л) (в пересчете на танин), г;- масса сырья,
г;- потеря в массе при высушивании сырья, %;
- общий объем извлечения, мл;
- объем извлечения, взятого для титрования, мл.
Результаты определения содержания суммы окисляемых
полифенолов представлены в таблице 7.
Таблица 7. Содержание суммы окисляемых полифенолов в сырье
фенхеля обыкновенного (среднее из 5 измерений)
|
ЛРС
|
Хср
|
Доверительный
интервал, %
|
ε, %
|
|
Трава в фазе до
цветения
|
3,65
|
3,6544±0,085018
|
2,28
|
|
Трава в фазе
цветения
|
6,94
|
6,943±0,019559
|
0,28
|
|
Трава в фазе
зеленого плодоношения
|
1,74
|
1,735±0,01946
|
1,12
|
|
Плоды
|
0,92
|
0,918±0,032181
|
3,51
|
|
Зонтики
|
2,19
|
2,192±0,005697
|
0,26
|
Как видно из данных таблицы трава, заготовленная в фазе
цветения, избирательно накапливает окисляемые полифенолы.
8.6 Определение содержания полифенольных
соединений в пересчете на галловую кислоту
,0 измельченного сырья (точная навеска) помещали в колбу со
шлифом, добавляли 50 мл 40% спирта этилового, подсоединяли к обратному
холодильнику и нагревали на водяной бане 30 минут. Горячую вытяжку фильтруют
через вату. Вату переносят в колбу для экстрагирования и добавляют 25 мл 40%
спирта этилового. Экстракцию проводили дважды в выше описанных условиях по 15
минут. Полученные вытяжки объединяли и помещали в мерную колбу на 100 мл,
доводили объем раствора 40% спиртом до метки (раствор А).
,0 мл раствора А помещали в мерную колбу на 25 л, доводили
объем раствора 40% спиртом до метки и перемешивали. Измеряли оптическую
плотность полученного раствора на спектрофотометре (UV/VIS 2800) при длине волны
270 нм в кювете на 10 мм. Раствор сравнения - 40% спирт этиловый.
Содержание суммы полифенольных соединений (Х, %) в сырье в
пересчете на галловую кислоту вычисляли по формуле:
А . 25 . 100 . 25.
100
Х = --------------------------------,
. m . 1 . (100 - W)
где А - оптическая плотность;- масса навески, г;
- коэффициент удельного поглощения раствора кислоты галловой
в 40% спирте этиловом при длине волны 270 нм;- потеря в массе при высушивании
сырья, %.
Результаты определения содержания полифенольных соединений
представлены в таблице 8.
Таблица 8. Содержание полифенольных соединений в сырье
фенхеля лекарственного (среднее из 5 измерений)
|
ЛРСХсрДоверительный
интервал, %ε, %
|
|
|
|
|
Трава в фазе до
цветения
|
3,73
|
3,7346±0,13957
|
3,79
|
|
Трава в фазе
цветения
|
8,65
|
8,6466±0,069919
|
0,81
|
|
Трава в фазе
зеленого плодоношения
|
8,25
|
8,2528±0,125447
|
1,52
|
|
Плоды
|
5,83
|
5,8346±0,127537
|
2,19
|
|
Зонтики
|
2,95
|
2,9468±0,041285
|
1,4
|
Как видно из данных таблицы 8 содержание полифенольных
соединений (в пересчете на галловую кислоту) также максимально в траве,
собранной в фазе цветения.
Для проведения сравнительного анализа результаты
количественного определения суммы окисляемых полифенолов по двум методам мы
представили в виде диаграммы на Рис. 3. 4.
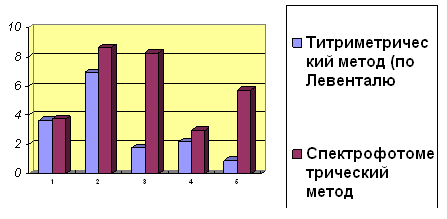
Рис. 3.4. Диаграмма результатов сравнения содержания
окисляемых полифенолов по двум методам
Данные диаграммы свидетельствуют о том, что содержание суммы
полифенольных соединений в пересчете на галловую кислоту, определенное
спектрофотометрическим методом, значительно выше нежели данные, полученные в
ходе титриметрического метода. Это можно объяснить тем, что
спектрофотометрический метод более чувствителен и, как следствие, дает более
точные результаты. А также тем, что содержание фенольных соединений
определяется в сумме и в случае пересчета на галловую кислоту возможно
определение и других фенольных соединений.
8.7 Определение содержания органических кислот
,0 г (точная навеска) измельченного сырья помещали в колбу со
шлифом на 250 мл, заливали 200 мл воды очищенной и выдерживали 2 часа на кипящей
водяной бане, охлаждали, количественно переносили в мерную колбу на 250 мл,
доводили объем до метки (раствор А). 10 мл раствора А помещали в колбу на 500
мл, добавляли 250 мл свежепрокипяченой воды, 2 капли 1% спиртового раствора
фенолфталеина, 1каплю 0,1% раствора метиленового синего и титровали 0,1 М
раствором гидроксида натрия до появления в пене лилово-фиолетового окрашивания.
Содержание свободных органических кислот (Х, %) в пересчете на яблочную кислоту
в абсолютно сухом сырье высчитывали по формуле:
V . 0,0067. 250 . 100 . 100
.КП
Х = ---------------------------------------,. 10 .
(100 - W)
где 0,0067 - количество яблочной кислоты которая
соответствует 1 мл раствора 0,1 М гидроксида натрия, г;
V - объем гидроксида натрия, мл;- масса навески, г;- потеря в
массе при высушивании сырья, %.
Таблица 9. Содержание органических кислот в сырье фенхеля
обыкновенного (среднее из 5 измерений)
|
ЛРС
|
Хср
|
Доверительный
интервал, %
|
ε, %
|
|
Трава в фазе до
цветения
|
4,75
|
4,752±0,008791
|
0,18
|
|
Трава в фазе
цветения
|
3,59
|
3,5934±0,014909
|
0,41
|
|
Трава в фазе
зеленого плодоношения
|
2,69
|
2,686±0,079907
|
2,97
|
|
Плоды
|
1,69
|
1,686±0,01295
|
0,77
|
|
Зонтики
|
2,29
|
2,2936±0,017879
|
0,779502
|
Данные таблицы свидетельствуют, что органических кислоты
максимально накапливаются в траве, собранной в фазе до цветения.
8.8 Определение содержания аскорбиновой кислоты
,0 г грубо измельченного сырья (точная навеска) помещали в
фарфоровую ступку и растирали с 5,0 г стеклянного порошка. Постепенно добавляли
при перемешивании 300 мл воды очищенной. Настаивали 10 минут и отфильтровывали.
В коническую колбу на 50-100 мл вносили 1 мл извлечения, 1 мл 2%
хлористоводородной кислоты, 13 мл воды очищенной, перемешивали. Оттитровывали
0,001 М раствором 2,6 - дихлорфенолиндофенолятом натрия до розовой окраски, не
исчезающей 30-60 секунд. Титрование проводили не более 2-х минут. Содержание
аскорбиновой кислоты (Х, %) в абсолютно сухом сырье высчитывали по формуле:
V . 0,000088. 300 . 100 .
100. КП
Х = ---------------------------------------,. 1 .
(100 - W)
где 0,000088 - титр тиранта по определяемому веществу, г/мл;
V - объем титранта, пошедшего на титрование, мл;- масса
навески, г;- потеря в массе при высушивании сырья, %.
Таблица 10. Содержание аскорбиновой кислоты в сырье фенхеля
обыкновенного (среднее из 5 измерений)
|
ЛРС
|
Хср
|
Доверительный
интервал, %
|
ε, %
|
|
Трава в фазе до
цветения
|
0,03
|
0,0318±0,001844
|
5,79
|
|
Трава в фазе
цветения
|
0,06
|
0,0636±0,001418
|
2,23
|
|
Трава в фазе
зеленого плодоношения
|
0,05
|
0,0484±0,001418
|
2,93
|
|
Плоды
|
0,08
|
0,0764±0,001418
|
1,86
|
|
Зонтики
|
0,03
|
0,028±0,001243
|
4,44
|
Как видно из данных таблицы содержание аскорбиновой кислоты в
объектах исследования незначительно и максимально в плодах.
Данные диаграммы на Рис. 3.5. позволяют сделать вывод о
динамике накопления различных групп БАВ в зависимости от фазы вегетации.
Наибольшее количество органических кислот накапливается в
траве, заготовленной в фазе до цветения. Гидроксикоричные кислоты, аскорбиновая
кислота, полисахариды и дубильные вещества количественно преобладают в траве,
собранной в фазе цветения, а содержание кумаринов максимально в зонтиках,
остающихся после обрушения плодов.
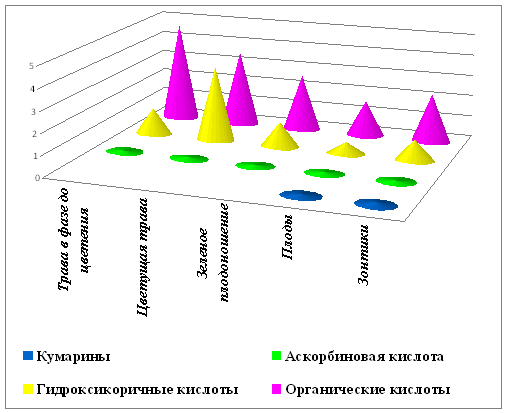
Рис. 3.5. Обобщенная диаграмма содержания определенных групп
БАВ в сырье фенхеля обыкновенного
9.Получение липофильной фракции из плодов
фенхеля
.1 Получение липофильной фракции
Липофильную фракцию получали из двух видов сырья: плодов и
травы фенхеля в аппарате Сокслета (рис. 4.1.) путем исчерпывающего
обезжиривания сырья хлороформом по стандартной методике [10].
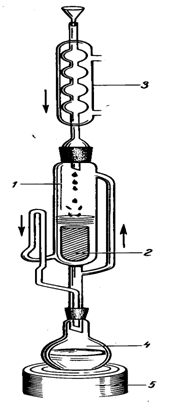
Рис. 4.1 Схема аппарата Сокслета
Примечание: 1 - экстрактор; 2 - пакетик с сырьем; 3 -
холодильник; 4 - приемник; 5 - электрическая плитка с закрытой спиралью.
Достигнув полноты извлечения, растворитель отгоняли и
приемник взвешивали, предварительно высушив его в сушильном шкафу при 90-950
до постоянного веса. Выход липофильных веществ (%) вычисляли по формуле:
(А - Б) . 100
Х = ------------------- ,
В
где А - вес приемника с липофильным экстрактом;
Б - вес пустого приемника;
В - навеска сырья.
Результаты определения содержания липофильных веществ в
плодах фенхеля представлены в таблице 11.
Таблица 11. Содержание липофильных веществ в плодах фенхеля
обыкновенного (среднее из 5 измерений)
|
ЛРС
|
Хср
|
Доверительный
интервал
|
ε, %
|
Органолептические
и физико-химические свойства
|
|
Плоды
|
7,88
|
7,876±0,114824
|
1,46
|
Маслянистая
жидкая масса темно-буро-зеленого цвета. Имеет сильный специфический запах
анетола, легко растворима в хлороформе, гексане, эфире, мало растворима в
спирте и практически нерастворима в воде.
|
|
Трава
|
6,04
|
6,038±0,126299
|
2,09
|
Плотная
маслянистая масса буро-зеленого цвета. Имеет сильный специфический запах.
Легко растворима в хлороформе, гексане, эфире, мало растворима в спирте и
практически нерастворима в воде.
|
Как видно из таблицы 11, содержание липофильных веществ в
плодах фенхеля составило 7, 88 %, что на 1,84 % больше, чем в траве.
9.2 Хроматографическое изучение качественного
состава липофильной фракции
Изучение качественного состава липофильной фракции из травы и
плодов фенхеля проводили методом двумерной тонкослойной хроматографии на
пластинках «Силуфол UV254» в системах растворителей гексан-ацетон (6:2) - I направление и
гексан-ацетон (6:4) - II направление. Идентификацию веществ проводили по
характерной окраске в видимом, УФ-свете и после обработки соответствующими
хромогенными реактивами.
Локализацию хлорофиллов на хроматограмме определяли по
характерной темно-зеленой окраске пятен в видимом свете и по ярко-красной
флуоресценции в УФ-свете. Кумарины имели голубую флуоресценцию в УФ-свете и
оранжевое окрашивание после обработки диазореактивом. После обработки 10%
раствором кислоты фосфорномолибденовой в этаноле пятна окрасились в темно-синий
цвет на зеленом фоне, а после обработки хроматограммы 2% раствором n-диметиламинобензальдегида
в смеси с хлористоводородной кислотой с последующим высушиванием хроматограммы
при 80-90ºС в течение 5 минут приобрели
розово-сиреневое окрашивание, что позволило отнести их к каротиноидам.
Флавоноиды идентифицировали по желтой флуоресценции в УФ-свете и по
грязно-желтой окраске после обработки 2% спиртовым раствором алюминия хлорида.
Схемы хроматограмм представлены на рисунке 5.2. и 5.3.

Рис. 4.2. Схема хроматограммы липофильного экстракта из травы
фенхеля обыкновенного
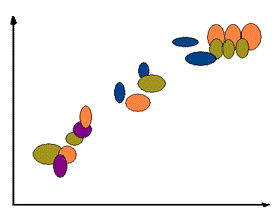
Рис. 4.3. Схема хроматограммы липофильного экстракта плодов
фенхеля обыкновенного
В результате хроматографического изучения липофильной фракции
из плодов и травы фенхеля было обнаружено 18 и 12 веществ соответственно, из
них идентифицировано 3 темно-зеленых вещества в траве, что свидетельствует о
наличии хлорофиллов, 2 вещества в траве и 6 веществ в плодах имели
грязно-желтую окраску и были отнесены к флавоноидным агликонам, окрашенные в
синий и сиреневый цвета 5 веществ в траве и 6 веществ в плодах были определены
как каротиноиды, 2 и 6 оранжевых вещества в траве и плодах соответственно
идентифицированы как кумарины.
Таким образом, в липофильных фракциях, полученных из плодов и
травы фенхеля обыкновенного, были обнаружены вещества флавоноидного и
терпеноидного характера, кумарины и хлорофиллы.
Выводы
1. Анализ данных литературы показал, что фенхель обыкновенный
широко культивируется на территории Украины и используется не только как
пищевое, но и как лекарственное растение. Однако основным видом лекарственного
сырья фенхеля являются плоды, содержащие значительное количество эфирного масла
и которые достаточно хорошо изучены, химический состав травы изучен
недостаточно. Поэтому углубленные фитохимические исследования травы являются
актуальными.
. С помощью качественных реакций и тонкослойной хроматографии
в траве фенхеля были обнаружены вещества гликозидной природы, полисахариды,
гидроксикоричные кислоты, органические кислоты, аминокислоты, кумарины,
флавоноиды, конденсированные дубильные вещества, сапонины.
. Определенное количественное содержание отдельных групп БАВ
показывает, что наибольшее их количество накапливается именно в траве,
заготовленной в фазе цветения, которая может стать их сырьевым источником.
Кумарины же превалируют в зонтиках, оставшихся после обрушения плодов, что
может быть основой для более рационального использования всего растения -
фенхеля обыкновенного.
. Методом тонкослойной хроматографии изучен качественный
состав полученных липофильных фракций. Установлено наличие каротиноидов,
хлорофиллов, флавоноидов и кумаринов.
5. Трава фенхеля обыкновенного содержит разнообразные группы
БАВ, отличные от состава плодов, которые при данной комбинации могут служить
основой для дальнейшего исследования этого сырья с целью создания новых,
усовершенствованных ЛС с расширенным спектром действия, что немаловажно для
комплексного лечения ряда заболеваний.
Список литературы
.Атлас ареалов и ресурсов лекарственных растений СССР. - М.: ГУГК,
1983. - 340с.
.Бестужева А. А. Аромомасла, фенхель / А. Бестужева // Perfect
Lady. - 2007. - № 2. С. 17.
.Блинова К.Ф., Яковлева Г. П. Ботанико - фармакогностический
словарь. - М.: Высшая школа, 1990.
.Бондаренко А.К., Чуб В.Г., Бондаренко Б.С., Овдиенко О.А.
Лекарственные растения Украины. Заготовка, воспроизводство, применение.-
К.-1992.-262 с.
.Ботаника. Учебник для вузов: в 4 т. = Lehrbuch der Botanik für Hochschulen Begründet von E.
Strasburger, F.Noll / Под ред. А. К. Тимонина, И. И. Сидоровой. - М.: Изд.
центр «Академия», 2007. - Т. 3. - С. 379. - 576 с.
.Гаммерман А.Ф. Лекарственные растения (растения-целители). Справ.
пособие/ А.Ф. Гаммерман, Г.Н. Кадаев, А.А. Яцена и др. -4-е изд., испр. и
доп.-М.: Высшая школа,1990.-544с.
.Гончарова Т.А. Энциклопедия лекарственных растений. - М.: Дом
МСП, 1997. - 824с.
.Государственная фармакопея СССР. - Вып.2 Общие методы анализа.
Лекарственное растительное сырье / МЗ СССР. - 11-е изд., доп.-М.:
Медицина,1989.-400с.
.Гродзинський А.М. Лікарські рослини: К.: Вид-во «Українська
радянська енциклопедія», 1992. - 542с.
.Державна фармакопея України/ Державне підприємство, «Науково -
експертний фармакологічний центр». - 1-е вид. - Доповнення 2. - Харків:
Державне підприємство, «Науково - експертний фармакологічний центр», 2008. -
620с.
.Иванов В.И. Лекарственные растения в народной медицине. - М.:
Воениздат, 1992. - 448с.
.Иващенко Н.В., Самылина И.А., Нестерова О.В., Сорокина А.А.,
Зорин Е.Б. Лекарственные растения и лекарственное растительное сырье,
содержащее эфирные масла и горечи (учебно-методическое пособие), М., «Чародей»,
2001.
.Кобзар А. Я. Фармакогнозія в медицині: Навч. посібник. - К.:
Медицина, 2007. - 544 с.
.Ковалев Н.В. Попова, В.С.и др. Практикум по фармакогнозии:
Учеб.пособие для студентов вузов/ Под общ. ред. В.Н. Ковалева.-Х.: НФаУ;
Золотые страницы, 2003.-512с.
.Ковальов В.М., Павлій О.І., Ісакова Т.І. Фармакогнозія з основами
біохімії рослин. За ред. Професора В.М. Ковальова. Підручник для студентів
вищих фарм.установ освіти та фарм факультетів вищих медичних установ освіти
ІІІ-ІV рівнів акред. -Х.: «Прапор»,Вид-во НФАУ,2000 - 703с.
.Кьосев Г.А. Полный справочник лекарственных растений. - М.:
ЭКСМО-Пресс, 2001. - 992с.
.Лекарственое растительное сырье. Фармакогнозия: Учеб. пособие /
Под. ред. Г. П. Яковлева и К. Ф. Блиновой. - СПб.: СпецЛит, 2004. - 765 с.; ил.
.Лекарственное сырье растительного и животного происхождения.
Фармакогнозия: учеб. Пособие под ред. Яковлева Г.П.- СПб.: СпецЛит,
2006.-845с.: ил.
.Лекарственные растения Государственной фармакопеи.
Фармакогнозия./Под. ред. Самылиной И.А., Северцова В.А./.-М.: «АНМИ»,
2003.-534с.
.Лікарські рослини: Енциклопедичний довідник / Відп. ред. А. М.
Гродзінський. - К.: Видавництво «Українська Радянська Енциклопедія» ім. М. П.
Бажана, український виробничо-комерційний центр «Олімп», 1992. - 544 с.: іл.
.Мазулін О.В., Калошина Н. О. Вирощування лікарських рослин на
присадібних ділянках. - Х.: Прапор, 2001. - 240 с., іл.
.Миркин Б.М., Наумова Л.Г., Мулдашев А.А. Высшие растения: краткий
курс систематики с основами науки о растительности: Учебник. - 2-е, перабот. -
Москва: Логос, 2002. - 256 с.
.Моно- та біциклічні монотерпеноїди ефірної олії Ptarmica speciosa
DC. / О.А. Кисличенко, А.М. Ковальов, А.М. Комісаренко, С.М. Комісаренко //
Вісник фармації. - 2007. - №3(51). - С. 18-20.
.Муравьева Д.А., Самылина И.А., Яковлев Г.П. Фармакогнозия:
Учебник - Н-е изд.,перераб. и доп. - М.: Медицина,2002. - 656с.
.Правила сбора и сушки лекарственных растений: Сборник инструкций.
- М.: Медицина, 1997. - 275с.
.Савельева Л. Ф. Фенхель - волошский укроп / Л. Савельева //
Здоровье и экология. - 2007. - № 7. С. 43-45.
.Сапронова Н.Н., Сорокина А.А. Формулы биологически активных
соединений (справочник), М., «Русский врач», 2000.
.Сербін А.Г., Сіра Л.М., Слободняк Т.О. Фармацевтична ботаніка.
Підручник / Під. Ред.. М.М. Сірої. - Вінниця: НОВА КНИГА, 2007. - 488с.
.Сировинні джерела продуктів біотехнології та їх аналіз: навч.
посібник для студ. вищ. навч. закл. / В. С. Кисличенко, І. О. Журавель, О.В.
Бухаріна та ін.; за ред. В. С. Кисличенко. - Х.: НфаУ: Золоті сторінки, 2009. -
304 с.
.Сокольский И. А. Сельдерей и фенхель / И. Сокольский // Наука и
жизнь. - 2006. - №. 6. - С. 64-65.
.Солодовніченко Н.М., Журавльов М.С., Ковальов В.М. Лікарська
рослинна сировина та фітопрепарати: Навч .посіб. з фармакогнозії з основами
біохімії лікар. рослин для студ. вищих фарм. навч. Закладів ІІІ-ІV рівнів
акред. (2-е вид.).- Х.: НФаУ; МТК-книга,2003.-408с.
.Справочник по заготовкам лекарственных растений / Д. С. Ивашин,
З. Ф. Катина, И. З. Рыбачук и др. - 6 -е изд., испр. И доп. - К.: Урожай, 1989.
- 288 с.: ил.
.Тернинко І. І. Визначення кількісного вмісту флавоноїдів у
надземних частинах окремих представників родини Селерових / Тернинко И.И.,
Кисличенко В.С., Онищенко У.Е. // Фармацевтичний часопис.-2009.- №4(9). -
С.11-15.
.Тернинко І. І. Дослідження елементного складу представників
родини Apiaceae / Тернинко И.И., Кисличенко В.С., Онищенко У.Е. // Фітотерапія.
Часопис. - 2009. - №2. - С. 59 - 63.
.Тернинко І. І. Порівняльне хромато-мас-спектрометричне вивчення
ефірних олій плодів анісу та фенхелю / Тернинко И.И., Кисличенко В.С., Онищенко
У.Е. // Український журнал КЛМ. 2009. - Т. 4, № 3. - С. 73 - 75.
.Тонкослойная хроматография в фармации и клинической биохимии: В 2
ч. / М. Шаршунова, В. Шварц, А. Михалец; Под. ред. В. Г. Берукина и С. Д.
Соколова. - М.: Мир, 1985. - Ч. 1. - 386 с.
.Фармакогнозия. Атлас: Учебное пособие / Под ред. проф.
Н.И.Гринкевич, Е.Я.Ладыгиной. - М.: Медицина, 1989 - 512с.
.Фенхель - кандидат на грядку / ред. Дриго А. В. // Пряно-ароматические
растения. - 2007. - № 5. С. 93.
.Харбон Дж. Биохимия фенольных соединений. - М.: Мир, 1968. 572 с.
.Яковлев Г.П., Челомбитько В.А. Ботаника: Учебное пособие для
фармацевтических университетов и фармацевтических факультетов мед. ВУЗов/ Под
ред. И.В. Грушвицкого. - М.: Высшая школа., 1990. - 367с.
.Davides N.W.//J. Chromatogr. - 1990. - Vol. 503. - P. 1-24.
.European Pharmacopoea 1998. - 5- th ed. - Strasbourg:
Maisonneuve, 1998. - 520 p.