Исследования иммунобиохимической лаборатории ГНУ СИБНИИЖ
Министерство сельского хозяйства РФ
ФГОУ ВПО Новосибирский
государственный аграрный университет
Кафедра ветеринарной генетики и
биотехнологии
Отчёт
о прохождении производственной
практики в ГНУ СИБНИИЖ
Выполнил: студент 2401 гр.
Шатохин К.С.
Руководитель: д.б.н.,
профессор Кочнев Н.Н.
Новосибирск 2011
Содержание
Введение
1. Общие сведения
2. Выделение ДНК
. Серологические реакции
. ПЦР-диагностика
Выводы
Список используемой литературы
Введение
ГНУ СИБНИИЖ представляет собой научно-исследовательский институт,
занимающийся решением различных проблем в области животноводства. К их числу
относятся:
1. Разработка новых рационов и систем кормления для сельскохозяйственных
животных;
2. Выведение новых пород, родственных групп, внутрипородных типов и
линий сельскохозяйственных животных;
. Разработка стандартов для различных пород, родственных групп,
внутрипородных типов и линий сельскохозяйственных животных;
. Проведение иммунологических, биохимических и ПЦР-реакций с целью
установления у животных маркёрных признаков;
. обоснование методов создания перспективных моделей технологий
производства продукции животноводства;
. совершенствование существующих и разработка новых технических средств,
технологических проектов реконструкции действующих и новых животноводческих
ферм.
Полное название этого научного учреждения - государственное научное
учреждение Сибирский ордена «Знак Почета» научно-исследовательский и
проектно-технологический институт животноводства Сибирского отделения
Российской академии сельскохозяйственных наук.
1. Общие сведения
ГНУ СИБНИИЖ расположен в посёлке Краснообск, недалеко от остановки
автобусов «институты». Как уже было сказано в разделе «введение», ГНУ СИБНИИЖ -
представляет собой государственное научное учреждение Сибирский ордена «Знак
Почета» научно-исследовательский и проектно-технологический институт
животноводства Сибирского отделения Российской академии сельскохозяйственных
наук. ГНУ СИБНИИЖ является одним из ведущих информационных центров по сельскому
хозяйству в нашей стране ЦНСХБ призвана оказывать максимальную помощь в
организации систематической оперативной информации о новейших достижениях
сельскохозяйственной науки и имеющемся передовом сельскохозяйственном опыте.
Поэтому одной из ее главных задач является организация такой системы
обслуживания пользователей, которая обеспечивала бы наиболее полное и
оперативное удовлетворение информационных потребностей всех ученых и
специалистов сельскохозяйственной отрасли с учетом их профессиональных
интересов и запросов.
Фонд ЦНСХБ насчитывает более 3 млн. единиц хранения носителей информации
по проблемам сельского и лесного хозяйства, пищевой промышленности,
продовольственных ресурсов, охраны окружающей среды в условиях
агропромышленного производства и смежных отраслей. Информация предоставляется в
виде отечественных и иностранных книг, журналов, газет, сериальных изданий,
CD-ROM, видеоматериалов и т.п., а также путем доступа к ряду баз данных, как
зарубежных, так и собственной генерации [5]. На сегодняшний день одним из основных
направлений деятельности СИБНИИЖА является изучение наследуемости мраморности
мяса у герефордского скота сибирской селекции. В результате проделанной работы,
был обнаружен так называемый ген мраморности мяса - TG5 [2]. Куратором данного направления является нынешний
директор института животноводства Владимир Андреевич Солошенко. Так же
сотрудниками института под руководством вышеупомянутого Владимира Андреевича
Солошенко ведётся разработка принципиально нового типа кормления,
заключающегося в снижении удельного веса воды в рационе животных, а
соответственно - повышению питательности рациона на 1 кг кормов. Кроме этого
ведётся работа и в других направлениях: свиноводстве, птицеводстве и т.п.
Прохождение производственной практики осуществлялось мной на базе
иммунобиохимической лаборатории. К основным задачам этой лаборатории можно
отнести:
1. Постановка серологических реакций с целью выявления групп крови
крупного рогатого скота и свиней
2. Постановка ПЦР-реакций с целью идентификации генотипов генов каппа-казеина,
пролактина, соматотропина, тиреоглобулина КРС и H-FABR свиней.
. Выделение ДНК из крови свиней и КРС.
. Статистическая обработка полученных результатов.
Лично мне пришлось принимать участие во всех перечисленных операциях.
Исследования проводят на крови животных, присылаемой из различных
хозяйств НСО, а так же из соседних регионов. Полученные данные используются в
дальнейших научных исследованиях и их статистической обработке. Так же данные
отсылаются в хозяйства, где они используются для ведения отбора, подбора и
выбраковки животных.
. Выделение ДНК
На месте прохождения производственной практики использовали метод
выделения ДНК из крови свиней и КРС с помощью набора реагентов фирмы «Медиген»
согласно инструкции, прилагающейся к набору. Перед началом работы необходимо
было протереть пинцет, микропипетки, рабочий стол и руки 70% раствором этанола.
Для выделения ДНК с помощью микропипетки брали 100мкл образца крови,
предварительно встряхнув пробирку с образцом. К 100 мкл крови с помощью
микропипетки добавляют 300 мкл раствора I, а затем - 10 мкл сорбента, в качестве которого
использовалось жидкое стекло. После этого смесь тщательно перемешивали на
вертексе до гомогенного состояния, а затем - инкубировали при комнатной
температуре 10-15 минут. Затем центрифугировали на микроцентрифуге около 60
секунд, после чего отбирали и отбрасывали супернатант.
Далее к осадку приливали 150 мкл раствора II, разбивали остаток на вертексе и перемешивали до гомогенного
состояния. После этого - центрифугировали на микроцентрифуге около 60 секунд,
после чего отбирали и отбрасывали супернатант. Затем к осадку приливали 700 мкл
раствора III, после чего разбивали остаток на
вертексе и перемешивали до гомогенного состояния. После этого -
центрифугировали на микроцентрифуге около 60 секунд, после чего отбирали и
отбрасывали супернатант.
Далее пробирки помещали в микротермостат и инкубировали около 30 минут
(хотя в инструкции сказано - 5 минут!) с целью удаления остатков раствора III, содержащего этанол, который
является ингибитором последующих реакций. Далее к осадку добавляли 50 мкл
стерильной воды, перемешивали на вертексе до гомогенного состояния и
инкубировали в термостате 5 мин при температуре 550С. Вода содержала
выделенное ДНК, пригодное для дальнейших ПЦР-реакций.
3. Серологические
реакции
Реакции между антигенами и антителами in vitro или серологические реакции широко используются в
микробиологических и серологических (иммунологических) лабораториях с самыми
разнообразными целями:
· серодиагностики бактериальных, вирусных, реже других инфекционных
заболеваний,
· сероидентификации выделенных бактериальных, вирусных и других
культур различных микроорганизмов
Серодиагностику проводят с помощью набора специфических антигенов,
выпускаемых коммерческими фирмами. По результатам серодиагностических реакций
судят о динамике накопления антител в процессе заболевания, о напряженности
постинфекционного либо поствакцинального иммунитета.
Сероидентификацию микробных культур проводят для определения их вида,
серовара с помощью наборов специфических антисывороток, также выпускаемых
коммерческими фирмами.
Каждая серологическая реакция характеризуется специфичностью и
чувствительностью. Под специфичностью понимают способность антигенов или
антител реагировать только с гомологичными антителами, содержащимися в
сыворотке крови, либо с гомологичными антигенами соответственно. Чем выше
специфичность, тем меньше ложноположительных и ложноотрицательных результатов.
В серологических реакциях участвуют антитела, принадлежащие главным
образом к иммуноглобулинам классов IgG и IgM [6].
Реакции, протекающие с укрупнением антигена
Реакция агглютинации и ее варианты. Реакция агглютинации (agglutinacio - склеивание) внешне проявляется в
склеивании и выпадении в осадок корпускулярных антигенов: бактерий, эритроцитов,
а также частиц с адсорбированными на них антигенами под влиянием антител в
среде с электролитом. Реакция протекает в две фазы. В первой фазе происходит
специфическая адсорбция антител на поверхности клетки или частицы, несущей
соответствующие антигены, во второй - образование агрегата (агглютината) и
выпадение его в осадок, причем этот процесс происходит только в присутствии
электролита (раствор хлорида натрия). Механизм реакции агглютинации описывается
теорией «решетки», согласно которой агглютинат образуется при соединении одного
активного центра двухвалентного антитела с детерминантной группой одного
антигена, а второго активного центра - с детерминантной группой другого
антигена. Избыток или недостаток антител препятствует проявлению агглютинации.
Для постановки реакции агглютинации используют корпускулярные антигены
(суспензии бактерий, эритроцитов). Характер и скорость реакции зависят от
антигенного строения. бактериальной клетки. Мелкозернистую О-агглютинацию дают
бактерии, лишенные жгутиков. О-агглютинация протекает медленно. При наличии
Н-антигена реакция проявляется в образовании крупно-хлопьевидного осадка и
протекает значительно быстрее.
Реакция агглютинации недостаточно специфична и чувствительна. По данным
признакам она уступает другим серологическим реакциям (преципитации, связывания
комплемента и т.д.). Повысить специфичность и чувствительность реакции можно
путем разведения исследуемой сыворотки до ее титра или половины титра. Титром
сыворотки называется то ее максимальное разведение, в котором обнаруживается
агглютинация антигена. Чем выше титр сыворотки, тем достовернее результаты
реакции. Чтобы дифференцировать причину положительной реакции (ранее
перенесенная инфекция, вакцинация или текущее заболевание), оценивают динамику
нарастания титра антител, которое наблюдается только при текущей инфекции.
При наличии у разных бактерий одинаковых или сходных групповых антигенов
они могут агглютинироваться одной и той же антисывороткой, что затрудняет их
идентификацию. В таких случаях применяют реакцию адсорбции антител по
Кастеллани. Данная реакция основана на способности родственных групп бактерий
адсорбировать из антисыворотки групповые антитела при сохранении в ней
типоспецифических антител. Полученные сыворотки называются монорецепторными,
так как содержат антитела только к одному определенному антигену. Они
применяются для детального изучения антигенной структуры бактерий с целью
определения их серовара.
Реакция непрямой, или пассивной, агглютинации (РПА). Под непрямой, или пассивной, агглютинацией
понимают реакцию, в которой антитела взаимодействуют с антигенами,
предварительно адсорбированными на клетках или частицах. В качестве сорбентов
чаще всего применяют эритроциты различных животных, частицы целлюлозы,
бентонита или латекса. В некоторых случаях пользуются обратным вариантом, т.е.
адсорбируют на эритроцитах или иных частицах не антигены, а антитела.
Реакция преципитации и ее варианты. Сущность данной реакции состоит в
осаждении (преципитации) антигена, находящегося в дисперсном коллоидном
состоянии, воздействием специфических антител в растворе электролита. Механизмы
реакций агглютинации и преципитации аналогичны и описываются теорией «решетки».
Реакция преципитации является высокочувствительным тестом, так как
позволяет обнаружить малые количества антигена или гаптена. Высокая
чувствительность реакции преципитации позволяет использовать ее для выявления
антигенов с помощью известных антисывороток. В одном из вариантов
последовательные разведения антигена наслаивают на стандартное разведение
диагностической сыворотки в пробирках, при этом осадок образуется в виде кольца
на границе двух сред (кольцепреципитация). Реакцию оценивают по максимальному
разведению антигена, при котором наблюдается кольцо преципитации визуально.
Кроме того, помутнение может быть зафиксировано инструментальными методами -
нефелометрией и др.
Реакция преципитации применяется в лабораторной практике при диагностике
инфекционных заболеваний, а также в судебной медицинской экспертизе для
определения видовой принадлежности белков, в частности белков кровяных пятен,
спермы и т.д. С помощью этой реакции в санитарной практике определяют
фальсификацию рыбных и мясных изделий. В биологии реакция прециации
используется для установления степени филогенетического родства различных ядов
животных и растений.
Иммунодиффузия. Методы иммунодиффузии представляют собой вариант реакции
преципитации, в которой взаимодействие антигена с антителами происходит не в
жидкости, а в геле, что позволяет лучше выявлять и фиксировать результаты взаимодействия.
В качестве геля чаще всего используется агаровый или полиакриламидный гель.
Существует несколько вариантов постановки реакций. Чаще всего
используется метод двойной диффузии, при котором растворы, содержащие антигены
и антитела, помещают в лунки, вырубленные в пластинке геля, находящегося на
стекле. При экспозиции антигены и антитела диффундируют из лунок и на месте их
встречи образуется полоса преципитации, хорошо видимая невооруженным глазом.
Если в растворах содержалось несколько антигенных компонентов и соответствующие
антитела, то они диффундируют в геле с разной скоростью и могут образовать
несколько полос преципитации. Это позволяет выявить не только факт присутствия
антигена, но и число составляющих компонентов. Взаимное расположение полос при
помещении в соседние лунки сравниваемых антигенов дает возможность судить об
идентичности составляющих их антигенов [6].
В другом варианте реакции раствор, содержащий антитела, смешивается с
гелем до его застывания и помещения на стекло. Антиген помещается в лунку и при
его диффузии в гель, содержащий антитела, образуется зона помутнения, диаметр
которой пропорционален количеству антигена. Эта модификация метода, часто
называемая по имени автора - метод Манчини, позволяет количественно определять антигены.
Обычно тесты иммунодиффузии используют для идентификации белков в
биологических жидкостях, таких, как сыворотка крови, цереброспинальная
жидкость, секреты желез или экстракты различных органов и т.д. [6].
Иммуноэлектрофорез (ИЭФ) представляет собой сочетание электрофореза в геле с
иммунодиффузией. Принцип ЙЭФ состоит в следующем. Сначала проводят
электрофоретическое разделение белков (смеси антигенов) в забуференном агаровом
геле. Затем в канавку, которая идет параллельно направлению миграции белков,
вносят преципитирующую иммунную сыворотку. Антигены и антитела диффундируют в
геле навстречу друг другу, в месте их взаимодействия образуются дугообразные
линии преципитации, количество, расположение и форма которых дают представление
о составе исходной смеси антигенов. С помощью ИЭФ успешно анализируются белки
сыворотки крови, спинномозговой жидкости, мочи, белки микробного происхождения.
В клинической практике ИЭФ используют при диагностике иммунодефицитных
состояний, проявляющихся дисгаммаглобулинемией.
В результате комбинации с другими методами анализа предложены
дискиммуноэлектрофорез, иммуноэлектрофокусирование, ракетный
иммуноэлектрофорез, радиоиммуноэлектрофорез, иммуноблотинг [6].
Иммуноблотинг - один из современных высокоточных вариантов электрофореза с
анализом разделенных белков иммунологическим методом. Тест осуществляется в три
этапа: сначала проводится электрофорез в полиакриламидном геле в присутствии
ионного детергента додецилсульфата натрия. Разделенные антигены переносятся за
счет капиллярных сил или дополнительного электрофореза на иммобилизующую
нитроцеллюлозную мембрану. Находящиеся на мембране антигены анализируются с
помощью меченых ферментной или радиоактивной меткой антител (иммуноферментным
или радиоиммунным методом) [6].
Реакция Кумбса (антиглобулиновый тест). Неполные антитела в отличие от
нормальных моновалентны, поскольку они имеют один активный центр, способный
взаимодействовать только с одним эпитопом: в то время как другие эпитопы
остаются не связанными. В результате этого не происходит образования крупных
комплексов, выпадающих в осадок в растворе электролита. Последние проявляются
только в реакциях с бивалентными антителами. Для исправления этого положения
вводится антиглобулиновая сыворотка (АГС), содержащая бивалентные антитела к
глобулину, которая свяжет между собой моновалентные антитела, содержащиеся в
исследуемом материале Таким образом произойдет визуально видимая реакция
гемагглютинации или агглютинация, свидетельствующая о наличии в исследуемой
сыворотке неполных (моновалентных) антител. Например, в случае беременности
резус-отрицательной женщины резус-положительным плодом у нее в сыворотке крови
появятся неполные антитела. Для их выявления в пробирку с исследуемой
сывороткой крови вносят резус-положительные эритроциты, а затем АГС. Появление
гемагглютинации свидетельствует о положительной реакции [6].
Реакции, протекающие с нейтрализацией антигена
Реакции нейтрализации основаны на способности антител нейтрализовать in vitro биологически-активные
антигенсодержащие субстраты: токсины, вирусы, яды змей и т.п. Реакция состоит в
смешивании биологически-активного вещества с сывороткой, содержащей антитела, и
выявлении нейтрализации его активности в биологическом тесте на животном или в
культуре ткани [6].
Реакция флоккуляции применяется для титрования антитоксических сывороток,
токсинов и анатоксинов, а также для определения типа токсина. Реакция
флоккуляции основана на способности токсина или анатоксина при смешивании в
эквивалентных соотношениях с антитоксической сывороткой образовывать
помутнение, а затем рыхлый осадок (флоккулят). Механизм реакции флоккуляции
аналогичен таковому реакции преципитации [6].
Одним из вариантов реакции нейтрализации токсина антитоксином является
реакция нейтрализации гемолитических свойств токсина специфической
антисывороткой [6].
Реакция нейтрализации in vivo может быть поставлена для выявления
антитоксина в организме исследуемого человека. С этой целью в область
предплечья внутрикожно вводят незначительное количество токсина, измеряемое в
кожных дозах. Отсутствие покраснения и припухлости в месте введения токсина
свидетельствует о его нейтрализации циркулирующим в крови антитоксином. Данная
реакция была предложена Шиком для выявления иммунитета к дифтерии и получила
название кожной пробы Шика. Она применяется для решения вопроса о
целесообразности иммунизации детей дифтерийным анатоксином с целью профилактики
дифтерии [6].
Реакция торможения гемагглютинации (РТГА) является вариантом реакции
нейтрализации вируса. Она основана на способности противовирусной антисыворотки
подавлять вирусную гемагглютинацию эритроцитов определенных видов животных
(кур, гусей и др.). Это объясняется способностью специфических антисывороток
нейтрализовать вирусные гемагглютинины. РТГА широко применяется для
идентификации и типирования вирусов, а также для выявления антигемагглютининов
в сыворотке крови исследуемых людей [6].
Реакции, протекающие с участием
комплемента
Реакция связывания комплемента (РСК). Предложена Ж. Бордэ и О. Жангу в
1901 г. и, несмотря на столь длительное применение в лабораторной практике, не
утратила своего значения по настоящее время. Более того, диапазон ее применения
значительно расширился по мере открытия ранее неизвестных возбудителей новых
инфекционных заболеваний: бактерий, микоплазм, вирусов, грибов и других
патогенов. Данная реакция используется для серодиагностики и обнаружения
антигена в исследуемом материале, сероидентификации выделенных культур.
Она характеризуется высокой чувствительностью и достаточной
специфичностью, а также возможностью применения как корпускулярных, так и
растворимых антигенов. Последнее связано с тем, что комплемент связывается с
Fc-фрагментом антител независимо от их специфичности. Таким образом,
способность комплемента связываться только с комплексом антиген - антитело за
счет Fc-фрагментов последнего и не вызывать гемолиз сенсибилизированных
эритроцитов (тест-система) послужила основой для широкого применения РСК в
лабораторной практике в течение прошедшего столетия.
Для постановки РСК требуется предварительная подготовка ингредиентов
реакции, особенно комплемента, в качестве которого используют сыворотку крови
морской свинки с установкой рабочей дозы. Однако за последние десятилетия
выпускается сухой оттитрованный комплемент, что значительно облегчило
постановку реакции. Исследуемые сыворотки крови и антигены обязательно
контролируются на антикомплементарность [6].
Постановку основного опыта производят в пробирках путем внесения в нее
определенных объемов сыворотки крови, антигена и рабочей дозы комплемента.
Смесь инкубируют в термостате при 37°С в течение часа. Регистрацию результатов
реакции проводят по гемолизу сенсибилизированных эритроцитов барана. Их
приготавливают при смешивании гемолитической сыворотки кролика с эритроцитами
барана. При внесении комплемента в эту смесь происходит реакция гемолиза. Таким
образом, в тех случаях, когда комплемент не связывается с исследуемой системой
антиген - антитело, т.е. остается свободным, наблюдается полный гемолиз
бараньих эритроцитов, который свидетельствует об отрицательной реакции.
Отсутствие гемолиза указывает на связывание комплемента системой антиген -
антитело, т.е. на положительную реакцию, которая обозначается крестами.
Интенсивность задержки гемолиза оценивается по четырехкрестной системе, при
этом полное отсутствие гемолиза обозначается ++++.
Реакция иммунного лизиса. В основе реакции лежит способность специфических
антител образовывать иммунные комплексы с клетками, в том числе с эритроцитами,
бактериями, что приводит к активации системы комплемента по классическому пути
и лизису клеток. Из реакций иммунного лизиса чаще других применяется реакция
гемолиза и редко - реакция бактериолиза (главным образом при дифференциации
Холерных и холероподобных вибрионов).
Реакция гемолиза. Под влиянием реакции с антителами в присутствии комплемента
мутная взвесь эритроцитов превращается в ярко-красную прозрачную жидкость -
«лаковую кровь» вследствие выхода гемоглобина. При постановке диагностической
реакции связывания комплемента (РСК) реакция гемолиза используется как
индикаторная: для тестирования присутствия или отсутствия (связывания)
свободного комплемента.
Реакция локального гемолиза в геле (реакция Ерне) является одним из
вариантов реакции гемолиза. Она позволяет определить число антителообразующих
клеток. Количество клеток, секретирующих антитела - гемолизины, определяют по
числу бляшек гемолиза, возникающих в агаровом геле, содержащем эритроциты,
суспензию клеток исследуемой лимфоидной ткани и комплемент.
Реакция иммобилизации. Способность антисыворотки вызывать иммобилизацию подвижных
микроорганизмов связана с реакцией между микробными антигенами и специфическими
антителами в присутствии комплемента. Иммобилизующие антитела обнаружены при
сифилисе, холере и некоторых других инфекционных заболеваниях, возбудители
которых являются подвижными микроорганизмами [6].
Реакции, протекающие с участием фагоцитов
Опсонофагоцитарная реакция проводится для определения способности антител и
комплемента усиливать фагоцитоз. Антитела, стимулирующие фагоцитоз, называют
опсоншами (греч. opsonion -
готовить пищу). Опсонизация определяется тем, что антитела, присоединившиеся к
микроорганизму, обуславливают его быстрое поглощение фагоцитом благодаря тому,
что фагоцит обладает рецепторами для Fc-фрагмента иммуноглобулина,
присоединившегося к микробной клетке. Комплемент тоже обладает опсонизирующими
свойствами, так как фагоцит содержит рецепторы и к компонентам комплемента. Для
количественной оценки опсонического эффекта определяют опсонический индекс -
отношение показателей фагоцитоза неопсонизированных микроорганизмов к
показателям фагоцитоза (фагоцитарный индекс и фагоцитарное число) после
обработки фагоцитоза антителами и/или комплементом [6].
Реакции, протекающие с участием меченых антигенов или антител
Тесты основаны на выявлении взаимодействия антигена с антителом с
образованием иммунного комплекса антиген - антитело по метке одного из
участников реакций, выявляемой либо визуально, либо с помощью специальных
высокочувствительных приборов, позволяющих количественно выявить меченый
субстрат и, следовательно, искомый антиген или антитело. В качестве метки
используют либо флюоресцирующий в ультрафиолетовом свете краситель (изоционат
флюоресцеина), либо фермент (пероксидаза, щелочная фосфатаза), выявляемый по
изменению окраски соответствующего субстрата (иммуноферментный анализ - ИФА),
либо изотоп, выявляемый радиометрией (радиоиммунный анализ - РИА).
В отечественных лабораториях в течение многих лет используется
иммунофлюоресцентный метод, разработанный Альбертом Кунсом и получивший его
имя. Одна модификация метода, получившая название прямого метода Кунса,
включает обработку материала на предметном стекле (мазок мокроты, срез ткани)
меченой флюорохромом диагностической антисывороткой. Если на предметном стекле
был искомый антиген, антитела фиксируются на антигене, и после отмывки стекла
от несвязавшихся антител антиген выявляется в люминесцентном микроскопе по
яркому свечению.
Другая модификация - непрямой метод Кунса - основан на использовании
меченой антиглобулиновой сыворотки. От прямого метода Кунса этот вариант
отличается тем, что используется немеченая диагностическая сыворотка, а ее
присоединение к антигену выявляется с помощью меченой антиглобулиновой
сыворотки, выявляющей иммуноглобулин немеченой диагностической сыворотки,
присоединившийся к искомому антигену.
Более современные методы выявления антигенов либо антител имеют множество
вариантов. Большинство из них используют «твердофазную» технологию, основанную
на том, что один из стандартизованных компонентов реакции (антиген или
антитело) заранее в производственных фирменных лабораториях фиксируется в
лунках специально приготовленных полистироловых или поливинилхлоридных панелей.
Исследуемый материал помещается в эти лунки. Для выявления антигена могут быть
использованы лунки, в которых фиксированы антитела. Если в материале содержался
антиген, то он присоединяется к фиксированным антителам и сам оказывается
фиксированным в лунке.
Для выявления этого антигена используются меченые антитела, и после ряда
отмывок для удаления несвязывавшихся компонентов эти антитела выявляются в
соответствии со своей меткой. Для выявления антител могут быть использованы
лунки, в которых фиксирован антиген. Добавленные антитела фиксируются на
антигене, остаются в лунке и могут быть выявлены с помощью меченых
антиглобулиновых антител. Мы привели примеры вариантов использования
твердофазных методов и меченых компонентов реакций. Могут быть и другие
варианты.
Так, например, клетки крови или костного мозга могут быть обработаны
флюоресцирующими антителами в жидкости. При этом клетки могут быть обработаны
разными антителами, помеченными разными флюорохромами. Пропуская такие взвеси
через специальный проточный флюориметр, можно одновременно выявить и подсчитать
разные виды клеток. Присоединив к проточному флюориметру прибор, именуемый
сортером, можно выделить или удалить из взвеси те клетки, которые необходимы
исследователю или врачу.
Современные иммунофлюоресцентные, иммуноферментные и радиоиммунные методы
отличаются высокой чувствительностью (выявление 0,0005-0,00005 мкг/мл белка),
специфичностью, воспроизводимостью, возможностью выявления широкого круга
биологических веществ. Современные производственные фирмы готовят все
необходимые ингредиенты и оборудование для их использования.
Таким образом, развитие серологических методов диагностики происходит в
настоящее время в следующем направлении:
· использование меченых антигенов или антител с помощью флюорохрома,
фермента либо радиоактивной метки;
· постановка реакции на твердофазном носителе - полистероловом
планшете с лунками с нанесенными в них антигенами или антителами.
Это позволяет повысить чувствительность метода, автоматизировать
постановку реакции и использовать специальную аппаратуру для снятия
результатов.
4. ПЦР-диагностика
кровь серологический антиген фагоцит
Метод основан на многократном избирательном копировании определённого
участка ДНК при помощи ферментов в искусственных условиях (in vitro). При этом происходит копирование
только того участка, который удовлетворяет заданным условиям, и только в том
случае, если он присутствует в исследуемом образце. В отличие от амплификации
ДНК в живых организмах, (репликации), с помощью ПЦР амплифицируются
относительно короткие участки ДНК. В обычном ПЦР-процессе длина копируемых
ДНК-участков составляет не более 3000 пар оснований (3 kbp [8]). С помощью
смеси различных полимераз, с использованием добавок и при определённых условиях
длина ПЦР-фрагмента может достигать 20-40 тысяч пар нуклеотидов. Это всё равно
значительно меньше длины хромосомной ДНК эукариотической клетки. Например,
геном человека состоит примерно из 3 млрд. пар оснований.
Для проведения ПЦР в простейшем случае требуются следующие компоненты:
· ДНК-матрица, содержащая тот участок ДНК, который требуется амплифицировать.
· Два праймера, комплементарные противоположным концам разных цепей
требуемого фрагмента ДНК.
· Термостабильная ДНК-полимераза - фермент,
который катализирует реакцию полимеризации ДНК. Полимераза для использования в
ПЦР должна сохранять активность при высокой температуре длительное время,
поэтому используют ферменты, выделенные из термофилов - Thermus aquaticus (Taq-полимераза), Pyrococcus furiosus (Pfu-полимераза), Pyrococcus woesei (Pwo-полимераза) и другие.
· Дезоксирибонуклеозидтрифосфаты (dATP, dGTP, dCTP, dTTP).
· Ионы Mg2+, необходимые для работы полимеразы.
· Буферный раствор, обеспечивающий необходимые условия реакции - рН,
ионную силу раствора. Содержит соли, бычий сывороточный альбумин.
Чтобы избежать испарения реакционной смеси, в пробирку добавляют
высококипящее масло, например, вазелиновое. Если используется амплификатор с
подогревающейся крышкой, этого делать не требуется.
Добавление пирофосфатазы может увеличить выход ПЦР-реакции. Этот фермент
катализирует гидролиз пирофосфата, побочного продукта присоединения
нуклеотидтрифосфатов к растущей цепи ДНК, до ортофосфата. Пирофосфат может
ингибировать ПЦР-реакцию [10].
Специфичность ПЦР основана на образовании комплементарных комплексов
между матрицей и праймерами, короткими синтетическими олигонуклеотидами длиной
18-30 оснований. Каждый из праймеров комплементарен одной из цепей двуцепочечной
матрицы и ограничивает начало и конец амплифицируемого участка.
После гибридизации матрицы с праймером (отжиг [11]), последний служит
затравкой для ДНК-полимеразы при синтезе комплементарной цепи матрицы (см.
ниже).
Важнейшая характеристика праймеров - температура плавления (Tm)
комплекса праймер-матрица.m - температура, при которой половина
ДНК-матриц образует комплекс с олигонуклеотидным праймером. Температуру
плавления можно приблизительно определить по формуле
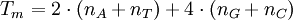 ,
,
где:
nX - количество нуклеотидов Х в праймере.
В
случае неверного выбора длины и нуклеотидного состава праймера или температуры
отжига возможно образование частично комплементарных комплексов с другими
участками матричной ДНК, что может привести к появлению неспецифических
продуктов. Верхний предел температуры плавления ограничен оптимумом температуры
действия полимеразы, активность которой падает при температурах выше 80°C.
При
выборе праймеров желательно придерживаться следующих критериев:
· GC-состав ~ 40-60%;
· близкие Tm праймеров (отличия не более, чем на
5°C);
· отсутствие неспецифических вторичных структур - шпилек [12] и
димеров [13];
· желательно, чтобы на 5’-конце был гуанин или цитозин,
поскольку они образуют три водородные связи с молекулой матрицы, делая
гибридизацию более стабильной.

Рис.
1. − Амплификатор для проведения ПЦР
ПЦР проводят в амплификаторе - приборе, обеспечивающем периодическое
охлаждение и нагревание пробирок, обычно с точностью не менее 0,1°C.
Современные амплификаторы позволяют задавать сложные программы, в том числе с
возможностью «горячего старта», Touchdown ПЦР (см. ниже) и последующего хранения амплифицированных молекул при
4°C. Для ПЦР в реальном времени выпускают приборы, оборудованные флуоресцентным
детектором. Существуют также приборы с автоматической крышкой и отделением для
микропланшет, что позволяет встраивать их в автоматизированные системы.
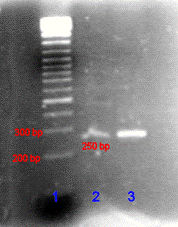
Фотография
геля, содержащего маркерную ДНК (1) и продукты ПЦР-реакции (2, 3). Цифрами
показана длина фрагментов ДНК в парах нуклеотидов
Обычно при проведении ПЦР выполняется 20-35 циклов, каждый из которых
состоит из трёх стадий (рис. 2).
Двухцепочечную ДНК-матрицу нагревают до 94-96°C (или до 98°C, если
используется особенно термостабильная полимераза) на 0,5-2 мин., чтобы цепи ДНК
разошлись. Эта стадия называется денатурацией, так как разрушаются
водородные связи между двумя цепями ДНК. Иногда перед первым циклом (до
добавления полимеразы) проводят предварительный прогрев реакционной смеси в
течение 2-5 мин. для полной денатурации матрицы и праймеров. Такой приём
называется горячим стартом, он позволяет снизить количество
неспецифичных продуктов реакции.
Когда цепи разошлись, температуру понижают, чтобы праймеры могли
связаться с одноцепочечной матрицей. Эта стадия называется отжигом.
Температура отжига зависит от состава праймеров и обычно выбирается на 4-5°С
ниже их температуры плавления. Время стадии - 0,5-2 мин. Неправильный выбор
температуры отжига приводит либо к плохому связыванию праймеров с матрицей (при
завышенной температуре), либо к связыванию в неверном месте и появлению
неспецифических продуктов (при заниженной температуре).
ДНК-полимераза
реплицирует <http://ru.wikipedia.org/wiki/%D0%A0%D0%B5%D0%BF%D0%BB%D0%B8%D0%BA%D0%B0%D1%86%D0%B8%D1%8F_%28%D0%B1%D0%B8%D0%BE%D0%BB%D0%BE%D0%B3%D0%B8%D1%8F%29>
матричную цепь, используя праймер в качестве затравки. Это - стадия элонгации.
Полимераза начинает синтез второй цепи от 3'-конца праймера, который связался с
матрицей, и движется вдоль матрицы в направлении от 3' к 5'. Температура
элонгации зависит от полимеразы. Часто используемые полимеразы Taq и Pfu
наиболее активны при 72°C. Время элонгации зависит как от типа ДНК-полимеразы,
так и от длины амплифицируемого фрагмента. Обычно время элонгации принимают
равным одной минуте на каждую тысячу пар оснований. После окончания всех циклов
часто проводят дополнительную стадию финальной элонгации, чтобы
достроить все одноцепочечные фрагменты. Эта стадия длится 7-10 мин. Количество
специфического продукта реакции (ограниченного праймерами) теоретически
возрастает пропорционально 2n, где n - число циклов реакции. На
самом деле эффективность каждого цикла может быть меньше 100%, поэтому в
действительности P ~ (1+E)n, где P - количество продукта, Е -
средняя эффективность цикла.
Число
«длинных» копий ДНК тоже растет, но линейно, поэтому в продуктах реакции
доминирует специфический фрагмент.
Рост
требуемого продукта в геометрической прогрессии ограничен количеством
реагентов, присутствием ингибиторов, образованием побочных продуктов. На
последних циклах реакции рост замедляется, это называют «эффектом плато» [14].
· «Вложенная» ПЦР (Nested PCR (англ.)) -
применяется для уменьшения числа побочных продуктов реакции. Используют две
пары праймеров и проводят две последовательные реакции. Вторая пара праймеров
амплифицирует участок ДНК внутри продукта первой реакции.
· «Инвертированная» ПЦР (Inverse PCR (англ.)) - используется в том случае, если известен
лишь небольшой участок внутри нужной последовательности. Этот метод особенно
полезен, когда нужно определить соседние последовательности после вставки ДНК в
геном. Для осуществления инвертированной ПЦР проводят ряд разрезаний ДНК
рестриктазами с последующим соединением фрагментов (легирование). В результате
известные фрагменты оказываются на обоих концах неизвестного участка, после
чего можно проводить ПЦР как обычно.
· ПЦР с обратной транскрипцией (Reverse Transcription PCR, RT-PCR (англ.)) - используется
для амплификации, выделения или идентификации известной последовательности из
библиотеки РНК. Перед обычной ПЦР проводят на матрице мРНК синтез
одноцепочечной молекулы ДНК с помощью ревертазы и получают одноцепочечную кДНК,
которая используется в качестве матрицы для ПЦР. Этим методом часто определяют,
где и когда экспрессируются данные гены.
· Асимметричная ПЦР (англ. Asymmetric PCR) - проводится тогда, когда нужно амплифицировать
преимущественно одну из цепей исходной ДНК. Используется в некоторых методиках
секвенирования и гибридизационного анализа. ПЦР проводится как обычно, за
исключением того, что один из праймеров берется в большом избытке.
· Количественная ПЦР (Quantitative PCR, Q-PCR (англ.)) - используется для быстрого измерения
количества определенной ДНК, кДНК или РНК в пробе.
· Количественная ПЦР в реальном времени (Quantitative real-time
PCR) - в этом методе используют флуоресцентно меченые реагенты для точного
измерения количества продукта реакции по мере его накопления.
· Touchdown (Step-down)
ПЦР (Touchdown PCR (англ.)) - с помощью этого метода
уменьшают влияние неспецифического связывания праймеров на образование
продукта. Первые циклы проводят при температуре выше температуры отжига, затем
каждые несколько циклов температуру снижают. При определённой температуре
система пройдёт через полосу оптимальной специфичности праймеров к ДНК.
· Метод молекулярных колоний (ПЦР в геле, англ. Colony - PCR Colony) - акриламидный гель полимеризуют со
всеми компонентами ПЦР на поверхности и проводят ПЦР. В точках, содержащих
анализируемую ДНК, происходит амплификация с образованием молекулярных колоний.
· ПЦР с быстрой амплификацией концов кДНК (англ. Rapid amplification of cDNA ends, RACE-PCR)
· ПЦР длинных фрагментов (англ. Long-range PCR) - модификация ПЦР для амплификации протяженных
участков ДНК (10 тысяч оснований и больше). Используют две полимеразы, одна из
которых - Taq-полимераза с высокой процессивностью (то есть, способная за один
проход синтезировать длинную цепь ДНК), а вторая - ДНК полимераза с 3'-5'
экзонуклеазной активностью. Вторая полимераза необходима для того, чтобы
корректировать ошибки, внесённые первой.
· RAPD PCR (англ. Random Amplification of Polymorphic DNA PCR,
ПЦР со случайной амплификацией полиморфной ДНК - используется тогда, когда
нужно различить близкие по генетической последовательности организмы, например,
разные сорта культурных растений, породы собак или близкородственные
микроорганизмы. В этом методе обычно используют один праймер небольшого размера
(около 10 п.н.). Этот праймер будет частично комплементарен случайным участкам
ДНК исследуемых организмов. Подбирая условия (длину праймера, его состав,
температуру и пр.), удаётся добиться удовлетворительного отличия картины ПЦР
для двух организмов.
· PCR с использованием горячего старта (англ. Hot-start PCR - модификация ПЦР с использованием парафина для
разделения верхней (содержащей буферный раствор, полимеразу, матрицу и, если
необходимо, деионизованную воду) и нижней (содержащей деионизованную воду,
праймеры и дезоксирибонуклеотиды) смесей с целью недопущения раннего смешивания
компонентов реакции. До начала реакции амплификатор необходимо прогреть до
температуры плавления парафина (60-80°C).
ПЦР используется во многих областях для проведения анализов и в научных
экспериментах [7].
Выводы
1. ГНУ СИБНИИЖ является одним из крупнейших научно-исследовательских
центров в области сельского хозяйства на территории России.
2. Разработки ГНУ СИБНИИЖ в области кормления, разведения и
содержания сельскохозяйственных животных вносят большой вклад в развитие
животноводства.
. Исследования сотрудников иммунобиохимической лаборатории вносят
огромный вклад в изучение генотипов животным по ряду локусов, а так же в
представление научной общественности об антигенах крови.
. В ходе прохождения производственной практике мной был получен
бесценный опыт в области выделения ДНК, ПЦР-реакций и серологических реакций на
антигены крови.
Список используемой литературы
1. Глик Б.,
Пастернак Дж. Молекулярная биотехнология. Принципы и применение. / Пер. с англ.
ISBN 5-03-003328-9. - М.: Мир, 2002. - 589 с., ил.
2. Ларионова
П.В. Разработка и эксперементальная апробация систем анализа полиморфизма
генов-кандидатов липидного обмена у крупного рогатого скота. / Дисс. на соиск.
уч. степени к.б.н. - Дубровицы, 2006. - 127 с.
. Патрушев
Л.И. Искусственные генетические системы. / В 2 т. - ISBN 5-02-033278-X. - М.:
Наука, 2005.
. Щелкунов
С. Н. Генетическая инженерия. / ISBN 5-94087-098-8. - Новосибирск: Сиб. унив.
изд-во, 2004. - 496 с.; ил.
. http://www.cnshb.ru/AKDiL/rashn/base/i00244.shtm.
. http://www.eurolab.ua/microbiology-virology-immunology/3662/3681/31649/.
. http://ru.wikipedia.org.