Коллигативные свойства растворов, их роль в повседневной жизни
Министерство
образования Республики Беларусь
«Международный
государственный экологический университет им. А.Д.Сахарова»
Реферат
на
тему: Коллигативные свойства растворов, их роль в повседневной жизни.
Минск,
2009 г.
Содержание
1. Общая
характеристика растворов
. Коллигативные
свойства разбавленных растворов
. Осмос
и осмотическое давление
. Криоскопия
. Эбуллиоскопия
. Давление
насыщенного пара растворителя
. Оборудование
. Практическое
значение осмоса
. Применение
методов криоскопии и эбуллиоскопии
Использованная
литература
Растворы
Растворами называются твердые, жидкие или
газообразные однородные системы, состоящие из двух или более компонентов,
относительные компоненты которых могут изменяться в довольно широком диапазоне
без скачкообразного изменения свойств системы. Наибольшее практическое значение
имеют жидкие растворы, в частности те, в которых растворителем служит вода.
От простых смесей растворы отличаются тем, что
составляющие их молекулы равномерно распределены по всему объёму.
В отличие от химических соединений растворы
имеют переменный состав и не подчиняются закону кратных соотношений.
Процесс растворения является не просто
механическим распределением одного вещества в другом, а более сложным
процессом, характеризующимся взаимодействием растворённого вещества с
растворителем, которое отличается от химического характером и энергией связи
частиц.
Следовательно, растворы не только однородные
смеси двух и более веществ, но и продуктов их взаимодействия.
Растворы многими свойствами отличаются от чистых
растворителей. Например, давление пара растворителя над раствором ниже, чем над
чистым растворителем. Это понижение прямо пропорционально мольной доле
растворённого нелетучего неэлектролита (закон Рауля).
Закон Рауля.
Парциальное давление насыщенного пара данного компонента над раствором равно
давлению насыщенного пара этого компонента в чистом состоянии умноженному на
его молярную долю в растворе:
ΔР=Кх,
где р - понижение давления пара, х - мольная
доля растворённого вещества, К - константа, равная Δр
при х=1.
Растворённое вещество, занимая часть объёма
раствора, понижает концентрацию частиц растворителя и соответственно этому
уменьшает число их, переходящих в пар.
Коллигативные свойства разбавленных
растворов
Коллигативные свойства
- свойства растворов, которые не зависят от природы растворённого вещества, а
определяются числом частиц в растворе.
К коллигативным свойствам относят:
. повышение осмотического давления
. понижение давления насыщенного пара
растворителя над раствором
. понижения температуры замерзания
раствора (криоскопия)
. повышение температуры кипения раствора
(эбуллиоскопия)
Осмос и осмотическое давление
Если разделить раствор и
растворитель при помощи полупроницаемой перегородки (мембраны),
пропускающей свободно молекулы растворителя и задерживающей молекулы
растворенного вещества, то наблюдается односторонняя диффузия растворителя.
Такого рода диффузия
обусловливается тем, что число молекул растворителя в единице объема больше,
чем в таком же объеме раствора, так как в растворе часть объема занимают
молекулы растворенного вещества. В результате молекулярного движения
перемещение молекул растворителя через мембрану из растворителя в раствор
преобладает над перемещением их в обратном направлении.
Односторонняя диффузия
растворителя к раствору называется осмосом, а сила, обусловливающая
осмос, отнесенная к единице поверхности полупроницаемой мембраны, называется осмотическим
давлением.
В результате осмоса и диффузии
выравнивается концентрация, причем способы, которыми достигается это
выравнивание, принципиально различны. В процессе диффузии равенство
концентраций достигается перемещением молекул растворенного вещества, а в
случае осмоса - перемещением молекул растворителя.
Механизм осмоса нельзя
объяснить только тем, что полупроницаемые мембраны играют роль сита с ячейками,
через которые свободно проходят молекулы растворителя, но не проходят молекулы
растворенного вещества.
По-видимому, механизм осмоса
значительно сложнее. Здесь большую роль играют строение и состав мембраны.
В зависимости от природы
мембраны механизм осмоса будет различен. В одних случаях через мембрану
свободно проходят только те вещества, которые в ней растворяются, в других
случаях мембрана взаимодействует с растворителем, образуя промежуточные
непрочные соединения, которые легко распадаются, и, наконец, она может
представлять и пористую перегородку с определенными размерами пор.
Для измерения осмотического
давления в сосуд с полупроницаемыми стенками наливают исследуемый раствор и
плотно закрывают пробкой, в которую вставлена трубка, соединенная с манометром.
Такой прибор для измерения осмотического давления называется осмометром.
Осмометр с раствором погружают
в сосуд с растворителем. В начале процесса растворитель из наружного сосуда
диффундирует в осмометр с большей скоростью, чем из него, поэтому уровень
жидкости в трубке осмометра поднимается, что создает в ней гидростатическое
давление, которое постепенно увеличивается. По мере увеличения
гидростатического давления скорости диффузии растворителя в осмометр и из
осмометра уравниваются, в результате чего наступает состояние динамического
равновесия, подъем жидкости в трубке осмометра прекращается.
Гидростатическое давление,
установившееся в результате осмоса, служит мерой осмотического давления.
Измерение осмотического
давления при помощи осмометра не всегда возможно с достаточной точностью, так
как не существует мембран, способных задерживать все частицы растворенного
вещества. Измеряемое значение осмотического давления для одного и того же раствора
будет, следовательно, в какой-то мере зависеть от природы мембраны.
Осмотическое давление возникает
лишь на границе между раствором и растворителем (или раствором другой
концентрации), если эта граница образована полупроницаемой перегородкой. Раствор,
содержащийся в обыкновенном сосуде, не оказывает на его стенки никакого иного
давления, кроме обычного гидростатического. Поэтому осмотическое давление надо
рассматривать не как свойство растворенного вещества, или растворителя, или
самого раствора, а как свойство системы из растворителя и раствора с
полупроницаемой перегородкой между ними.
Закон Вант-Гоффа
для осмотического давления. Осмотическое давление раствора
на границе раствор - растворитель равно тому газовому давлению, которое было
бы, если бы растворенное вещество находилось в газообразном состоянии и
занимало бы объем раствора при той же температуре:
Росм
·V=n·R·T
где Росм - осмотическое
давление в н/м2, V
- объём раствора в м3
Закон Вант-Гоффа применим
только к разбавленным «идеальным» растворам, в которых взаимодействие между
молекулами растворенного вещества бесконечно мало.
Криоскопия
Температурой
замерзания жидкости является такая температура, при
которой давление насыщенного пара над кристаллами льда и над жидкостями
одинаково. Разность температур замерзания растворителя и раствора называют понижением
температуры замерзания раствора.
Понижение температуры
замерзания раствора связано с понижением давления пара над раствором по
сравнению с чистым растворителем. Всякая жидкость начинает замерзать при той
температуре, при которой она будет иметь такое же давление пара, каково оно над
ее льдом.
Давление пара растворителя над
раствором становится равным давлению пара над льдом, т.е. при более низкой
температуре, чем То, и температура Т3. отвечает точке
замерзания данного раствора. Всегда Т3.<То и понижение
температуры замерзания ΔТ3.
= То - Т3. растет с концентрацией
ΔТ3.
= Е3 ·m,
где Е3 -
криоскопическая постоянная растворителя, m
- моляльная концентрация.
Криоскопическая постоянная
растворителя показывает понижение температуры замерзания, которое наблюдалось
бы для раствора, содержащего на 1000 г растворителя 1 моль растворенного
неэлектролита.
Криоскопическая постоянная не
зависит от концентрации и природы растворенного вещества, а зависит только от
природы растворителя.
Способ определения молярной
массы неэлектролита, основанный на понижении температуры начала кристаллизации
жидкости при растворении в ней исследуемого вещества называется криоскопией.
Для Е3 найдено
следующее выражение:
Е3 = 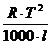
где l -удельная
теплота плавления растворителя, T - абсолютная температура его
замерзания.
При смешивании соли со снегом или
мелко раздробленным льдом происходит образование раствора, сопровождающееся
сильным охлаждением вследствие большого поглощения теплоты льдом при его
плавлении и солью при ее растворении. Охлаждающие смеси имеют большое
практическое применение в лабораторной технике и промышленности.
На практике применяются еще так называемые
антифризы, представляющие собой водный раствор некоторых неорганических
солей или спиртов. Из неорганических солей для приготовления антифризов
применяют хлориды аммония, натрия, магния, кальция, а также карбонат калия
(поташ).
Из спиртов чаще всего используют
этиловый спирт, глицерин и этиленгликоль. В зависимости от природы и отношений
масс составных частей антифриз не замерзает при температуре от -15 до -55°С и
ниже. Применяют антифризы для охлаждения цилиндров автомобильных, тракторных и
авиационных двигателей при эксплуатации их в зимнее время, а также для
заполнения противопожарных трубопроводов в не отапливаемых помещениях.
Эбуллиоскопия
Так как давление пара раствора
всегда меньше давления пара растворителя, то раствор должен кипеть при более
высокой температуре, чем растворитель. Для того чтобы раствор кипел, нужно
достичь равенства между давлением пара над раствором и атмосферным давлением, а
для этого он должен быть нагрет до более высокой температуры.
Повышение температуры кипения
ΔTК.=Tк.-То
ΔТк,
= ЕкТ,
где ΔТк
- повышение температуры кипения, Ек - эбуллиоскопическая постоянная
растворителя.
Эбуллиоскопическая постоянная
растворителя показывает повышение температуры кипения, которое наблюдалось бы
для раствора, содержащего на 1000 г растворителя 1 моль растворенного
неэлектролита.
Эбуллиоскопическая постоянная не
зависит от концентрации и природы растворенного неэлектролита, а зависит только
от природы растворителя и имеет размерность град-моль.
Измерив повышение температуры
кипения раствора по сравнению с температурой кипения чистого растворителя, а
также навеску растворителя и навеску растворенного вещества, можно вычислить
его молекулярную массу. Такой метод определения молекулярной массы называется
эбуллиоскопическим или эбуллиоскопией.
Однако эбуллиоскопический метод
из-за недостаточной точности и невозможности работать с веществами,
разлагающимися при кипячении раствора, применяется реже криоскопического
метода.
Понижение давления насыщенного пара
растворителя
При испарении жидкости над ее
поверхностью образуется пар. Процесс испарения обратим, одновременно с ним идет
и конденсация пара. Когда скорость испарения и скорость конденсации сравняются,
установится равновесие и насыщенный пар при данной температуре будет иметь
постоянное давление.
С повышением температуры давление
насыщенного пара увеличивается. При растворении небольшого количества
какого-либо нелетучего вещества (нелетучим можно считать вещество,
температура кипения которого примерно на 150 °С выше температуры кипения
растворителя.) в данном растворителе снижается концентрация молекул
растворителя и, следовательно, уменьшается число молекул растворителя,
вылетающих с поверхности жидкости в единицу времени. В этом случае равновесие между
жидкостью и насыщенным паром устанавливается при более низком давлении по
сравнению с давлением пара над одним растворителем.
Давление насыщенного пара
растворителя над раствором всегда меньше, чем над чистым растворителем.
Чем больше концентрация раствора,
т.е. чем меньше молекул растворителя содержится в единице объёма, тем меньше
давление насыщенного пара.
А) Давление насыщенного пара
растворителя над раствором равно давлению его над чистым растворителем,
умноженному на мольную долю растворителя.
Б) Относительное понижение давления
насыщенного пара растворителя над разбавленным раствором нелетучего вещества
равно молярной доле растворённого вещества.
А, Б - закон Рауля в разных
формулировках.
Понижение давления насыщенного пара
растворителя над раствором зависит не от природы растворителя и растворенного
вещества, а определяется концентрацией последнего.
Оборудование для эбуллиоскопического
и криоскопического определения молекулярных весов
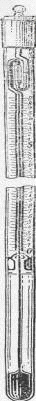
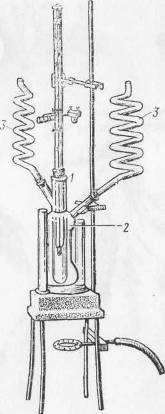
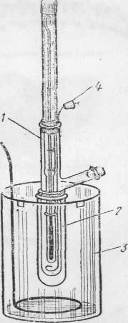
Дифференциальный Аппарат для
эбуллиоскопического определения
термометр Бекмана
Аппарат для криоскопического
определения молекулярных весов молекулярных весов
Практическое значение осмоса
Осмос имеет большое значение в
жизнедеятельности растительных и животных организмов. Известно, что все
биологические ткани состоят из клеток. Каждая клетка имеет оболочку, внутри ее
находится жидкость, которая представляет собой раствор различных веществ в
воде. Оболочка клетки полупроницаема и через нее достаточно легко проходит
вода.
Давлением, которое вызывается
проникающей в клетки водой, объясняется упругость тканей растений, их плодов,
листьев, стеблей, лепестков. Осмотическое давление в клетках зрелых плодов и
овощей обычно колеблется от 0,49 до 0,98 МПа. В срезанных растениях, благодаря
испарению воды объем внутриклеточной жидкости уменьшается, снижается давление и
растение вянет. Увлажнение растений, погружение их в воду вызывает осмос и
снова сообщает тканям упругость.
В концентрированных растворах идет
диффузия воды из клетки в раствор, так как осмотическое давление внешнего
раствора больше, чем давление внутри клетки. Потеря воды ведет к уменьшению
объема клетки, нарушает нормальное течение физических и химических процессов в
ней. Это явление называют плазмолизом.
Плазмолиз имеет большое значение при
консервировании овощей и плодов в растворах поваренной соли или сахарозы.
При солении или квашении овощей
поваренная соль является, во-первых, консервантом. Растворы соли (5-7 %)
задерживают развитие большинства микроорганизмов, так как вызывают у них
плазмолиз. Однако главное назначение поваренной соли заключается в том, что она
вызывает плазмолиз растительных клеток, нарушает полупроницаемость клеточных
оболочек. В результате происходит выделение клеточного сока, содержащего
сахара. Эти сахара служат основой для молочнокислого брожения. Молочная кислота
придает продукту специфический вкус и, являясь антисептиком, подавляет
деятельность других микроорганизмов.
При варке плодов в концентрированном
сахарном растворе (варка варенья) растительные клетки теряют воду, т. е. идет
плазмолиз. Если скорость удаления воды больше, чем скорость диффузии сахара в
плодовую ткань, то плоды после варки сморщиваются и становятся жесткими.
Правильно выбранный режим варки предусматривает равенство скоростей этих
процессов. В таком случае плоды сохраняют свой начальный объем и вид.
В данном случае сахар не только
придает продукту вкусовые качества и питательность, но является и консервирующим
веществом. В концентрированном сахарном растворе с высоким осмотическим
давлением происходит плазмолиз клеток почти всех микроорганизмов.
Можно подобрать раствор такой
концентрации, что его осмотическое давление будет равно осмотическому давлению
внутриклеточной жидкости. В таком растворе состояние клетки не изменится.
Растворы, имеющие одинаковое осмотическое давление, называются изотоническими.
Кровь, лимфа и другие тканевые
жидкости человека и животных имеют осмотическое давление около 0,8 МПа. Такое же
давление имеет 0,9%-ный раствор хлорида натрия. Относительно кропи он является
изотоническим, не вызывает каких-либо изменений в клетках. Такой раствор
называется физиологическим. Физиологический раствор часто служит основой
для лекарственных препаратов, вводимых в организм инъекций.
Если к раствору, находящемуся в
сосуде с полупроницаемыми стенками, приложить давление большее, чем его
осмотическое давление, то из раствора через полупроницаемую перегородку будет
вытесняться растворитель, а растворенное вещество останется в более
концентрированном растворе. Этот метод удаления растворителя получил название обратного
осмоса или гиперфильтрации. Он весьма перспективен для опреснения
соленой морской воды. Осмотическое давление морской воды примерно составляет
0,27 МПа. При большем давлении из нее можно отфильтровать чистую воду. В
качестве мембран для обратного осмоса морской воды используют полупроницаемые
материалы на основе целлюлозы, пористые стекла и пористую керамику.
Применение методов криоскопии и эбуллиоскопии
В лабораторной практике криоскопический метод
нашёл значительно большее распространение по сравнению с методом эбуллиоскопии:
измерять точки замерзания растворов значительно проще и безопаснее, чем их
точки кипения. Но они являются основными методами для определения степени и
константы диссоциации, а также коэффициента активности электролитов в
растворах.
На понижении температуры замерзания жидкостей
при растворении в них нелетучих веществ основано действие антифризов - веществ,
добавление которых к охлаждающей воде в радиаторах автомобилей снижает
температуру ее замерзания и предотвращает возможность «размораживания»
двигателей.
Хладагенты, применяемые в химической технологии
для доставки «холода» к теплообменникам, - обычно растворы каких-либо солей в
воде.
В ряде случаев хладагенты готовят на специальных
предприятиях и выпускаются под фирменными наименованиями, например, фреон,
хладон, тосол. Используются такие хладагенты в бытовых и промышленных
холодильниках, автомобилях, самолётах.
эбуллиоскопический криоскопический молекулярный растворитель
Использованная литература
1. Б.В.Ахметов,
Ю.П.Новиченко, В.И.Чапурин «Физическая и коллоидная химия»
. А.Б.Лукьянов
«Физическая и коллоидная химия»
. К.И.Евстратова,
Н.А.Кулина, Е.Е.Малахова «Физическая и коллоидная химия»
. М.И.Равич-Щербо,
В.В.Новиков «Физическая и коллоидная химия»
. С.А.Балезин,
Б.В.Ерофеев, Н.И.Подобаев «Основы физической и коллоидной химии»