Термодинамический исследование реакции
Новотроицкий
филиал
Федерального
государственного образовательного учреждения
высшего
профессионального образования
«Национальный
исследовательский технологический университет
«МИСиС»
Кафедра
математики и естествознания
Контрольная
работа №1
Термодинамический
анализ реакции
По
дисциплине физическая химия
вариант №2
Выполнил: Гагаринский И.В
Проверил: Нефедова Е.В.
Новотроицк,
2010 г.
1. ФОРМУЛИРОВКА
ЗАДАНИЯ
.1 Исследование 1
Для реакции: C+O2=CO2 выполнить следующее:
Составить уравнение зависимости от
температуры величины 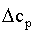 = f (T),
теплового эффекта
= f (T),
теплового эффекта 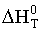 = f(T) и
изменения энтропии
= f(T) и
изменения энтропии 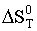 = f(T).
= f(T).
Вычислить величины 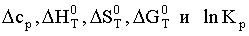 при
температурах:
при
температурах:
-1500 K. Полученные значения
использовать при построении графиков в координатах 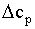 - Т;
- Т; 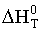 - T;
- T; 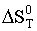 - T;
- T; 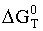 - T; ln Kp
- T; и
- T; ln Kp
- T; и 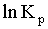 - 1/T. энтропия термодинамический реакция
- 1/T. энтропия термодинамический реакция
Дать термодинамический анализ
реакции на основании полученных результатов.
Пользуясь графиком lnКр - 1/T ,
вывести приближенное уравнение вида 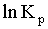 = А/T + B, где А, В - постоянные и
оценить среднее значение теплового эффекта реакции в изученном интервале
температур..
= А/T + B, где А, В - постоянные и
оценить среднее значение теплового эффекта реакции в изученном интервале
температур..
1.2 Исследование 2
Используя правило фаз Гиббса, для
рассматриваемой системы определить количества фаз, независимых компонентов и
число степеней свободы.
Установить направление смещения состояния
равновесия рассматриваемой системы при:
а) увеличении давления (постоянная температура);
б) увеличении температуры (постоянное давление).
2. РЕШЕНИЕ ЗАДАЧИ
Зависимость теплового эффекта реакции от
температуры определяется законом Кирхгофа:
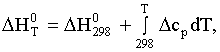 (1)
(1)
где: 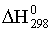 - стандартный тепловой эффект
реакции при 298 К;
- стандартный тепловой эффект
реакции при 298 К;
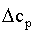 - изменение теплоёмкости системы в
результате протекания реакции.
- изменение теплоёмкости системы в
результате протекания реакции.
Последняя величина рассчитывается по
уравнению
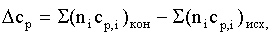 (2)
(2)
где 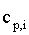 - мольная изобарная теплоёмкость
i-го вещества; - стехиометрический коэффициент i-го вещества в уравнении
реакции.
- мольная изобарная теплоёмкость
i-го вещества; - стехиометрический коэффициент i-го вещества в уравнении
реакции.
После подстановки значений
зависимости 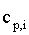 от
температуры в выражение (2) оно примет вид:
от
температуры в выражение (2) оно примет вид:
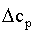 = Da + Db
T + DcT-2 , (3)
= Da + Db
T + DcT-2 , (3)
где: Da = S(ni
ai)кон - S(ni ai)исх .
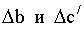 - рассчитываются аналогично
- рассчитываются аналогично 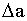 .
.
Значение 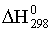 определяется
по стандартным теплотам образования
определяется
по стандартным теплотам образования 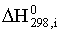
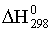 = S(ni
= S(ni 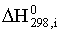 )кон - S (ni
)кон - S (ni 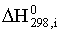 )исх. (4)
)исх. (4)
После расчета Da, 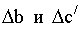 и их
подстановки в уравнение (3) и (1) получим следующее выражение:
и их
подстановки в уравнение (3) и (1) получим следующее выражение:
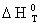 = Х + Da Т + Db/2
Т2 - Dс/ Т-1 (5)
= Х + Da Т + Db/2
Т2 - Dс/ Т-1 (5)
Постоянная интегрирования Х
определяется из граничных условий:
Т=298 К; 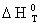 =
= 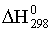
X = 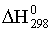 - Da 298 -1/2 Db
2982 + Dc/ 298-1
- Da 298 -1/2 Db
2982 + Dc/ 298-1
Изменение энтропии системы в
результате протекания процесса определяется по уравнению:
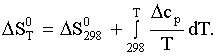 (6)
(6)
В этом уравнении 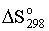 -
cтандартное изменение энтропии для реакции при 298К, определяемое по мольным
стандартным энтропиям веществ
-
cтандартное изменение энтропии для реакции при 298К, определяемое по мольным
стандартным энтропиям веществ 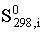 :
:
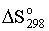 = S(ni
= S(ni 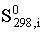 )кон - S(ni
)кон - S(ni 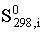 )исх (7)
)исх (7)
Подстановка выражения (3) в
уравнение (6) приводит в результату:
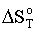 = Y + Da ln Т + Db Т - Dс//2 Т-2 (8)
= Y + Da ln Т + Db Т - Dс//2 Т-2 (8)
Постоянная интегрирования Y
определяется из граничных условий:
Т=298 К; 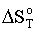 =
= 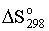 .
.
= 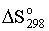 - Da ln298 - Db
298 + Dc/ 298-2/ 2
- Da ln298 - Db
298 + Dc/ 298-2/ 2
При расчете изменения стандартной
энергии Гиббса для реакции воспользуемся точным уравнением энтропийного
варианта Гиббса-Гельмгольца:
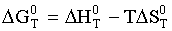 (9)
(9)
Для реакций, в которых участвуют
только газы или газы и конденсированные фазы, представляющие собой чистые
вещества, константу равновесия Ка выражают обычно через равновесные парциальные
давления (Pi) и обозначают символом Kp.
Константа равновесия связана с
изменением стандартной энергии Гиббса соотношением:
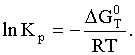 (10)
(10)
После подстановки выражения (8) в
уравнение (9) получим :
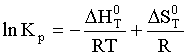 . (11)
. (11)
3. ПОДГОТОВКА
ДАННЫХ ДЛЯ РАСЧЕТОВ
Для удобства последующих расчетов составляем
таблицу исходных данных.
Таблица 1 Исходные
данные для термодинамического исследования реакции (по данным [1])
|
вещество
|
H298
|
S298
|
a
|
b
|
c
|
0
|
5,74
|
17,5
|
0,00427
|
-879000
|
|
O2
|
0
|
205,03
|
31,46
|
0,00339
|
-377000
|
|
CO2
|
-393510
|
213,6
|
44,14
|
0,00904
|
-853000
|
|
ИЗМЕНЕНИЯ:
|
-393510
|
2,83
|
-4,82
|
0,00138
|
403000
|
|
|
|
|
|
|
4. УРАВНЕНИЯ ДЛЯ
РАСЧЕТОВ
С учетом данных, представленных в табл.1
получаем следующие уравнения для расчета:
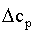 = 17,5 +0,00427 · T +(-879000)
· T-2=0,935777778 ,
= 17,5 +0,00427 · T +(-879000)
· T-2=0,935777778 ,
Х = 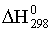 - Da 298 - Db/2
2982 + Dс/ 298-1 =
-390910,4435 Дж =
- Da 298 - Db/2
2982 + Dс/ 298-1 =
-390910,4435 Дж = 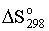 - Da ln 298 - Db 298 + Dс//2 298-2 = 31,28955 Дж/К
- Da ln 298 - Db 298 + Dс//2 298-2 = 31,28955 Дж/К
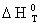 = Х + Da Т + Db/2
Т2 - Dс/ Т-1 =
-390910,4435 + 17,5 Т + 0,00427 Т2 +879000 Т-1 = -393508,0769 Дж
= Х + Da Т + Db/2
Т2 - Dс/ Т-1 =
-390910,4435 + 17,5 Т + 0,00427 Т2 +879000 Т-1 = -393508,0769 Дж
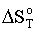 =Y + Da ln Т + Db
Т - Dс//2 Т-2
=31,28955 + 17,5 ln Т + 0,00427 Т +879000Т-2=2,836432123Дж/К
=Y + Da ln Т + Db
Т - Dс//2 Т-2
=31,28955 + 17,5 ln Т + 0,00427 Т +879000Т-2=2,836432123Дж/К
Решение задачи выполнено на
персональном компьютере и представлено в таблице 2.
Таблица 2 Сводная
таблица термодинамических характеристик реакции


5.
ТЕРМОДИНАМИЧЕСКИЙ АНАЛИЗ РЕАКЦИИ
.1. На рисунке 1 и
в таблице 3 представлено изменение теплоемкости в реакции
Таблица 3 Величина 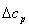 при
различных температурах реакции:
при
различных температурах реакции:
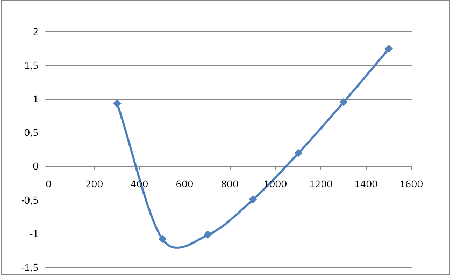
Рисунок 1.
Изменение изобарной теплоемкости в реакции
Из приведенных данных следует:
Величина 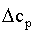 меняет знак
при температуре Т1= 400 К. Такое изменение значений
меняет знак
при температуре Т1= 400 К. Такое изменение значений 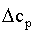 определяет
вид зависимости от температуры теплового эффекта и изменения энтропии в реакции
( рисунки 2 и 3).
определяет
вид зависимости от температуры теплового эффекта и изменения энтропии в реакции
( рисунки 2 и 3).
Значение 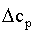 реакции
меняет знак при Т = 400 К, поэтому на кривых зависимости
реакции
меняет знак при Т = 400 К, поэтому на кривых зависимости 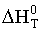 и
и 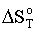 от
температуры ( рис.2 и рис.3) при этой температуре появляется экстремум..
от
температуры ( рис.2 и рис.3) при этой температуре появляется экстремум..
5.2 При комнатной температуре
тепловой эффект реакции 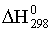 =-393510
кДж, т.е. реакция протекает с выделением теплоты. Изменение теплового эффекта с
температурой приведено в таблицах 2 и 4 и на рисунке 2
=-393510
кДж, т.е. реакция протекает с выделением теплоты. Изменение теплового эффекта с
температурой приведено в таблицах 2 и 4 и на рисунке 2
Таблица 4 Тепловой эффект реакции 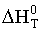 при
различных температурах
при
различных температурах
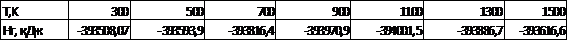
По данным табл.4 построим
зависимость 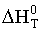 = f(T) на
рис.2.
= f(T) на
рис.2.
Вид кривой на рисунке 2 определяется
законом Кирхгофа
(dDН)/(dT ) = 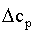
Знак 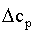 определяет вид кривой на рисунке 2
(убывающая, возрастающая и экстремальная зависимость).
определяет вид кривой на рисунке 2
(убывающая, возрастающая и экстремальная зависимость).
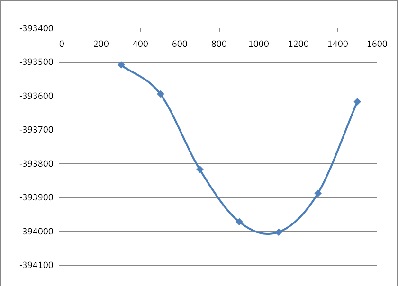
Рис. 2. Зависимость
теплового эффекта от температуры
Зависимость на рис.2 позволяет
найти не только значения теплового эффекта при любой температуре в заданном
интервале температур, но и определить величину 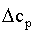 в пределах 300-1500 К. Например,
определим
в пределах 300-1500 К. Например,
определим 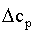 рассматриваемой
реакции при температуре 700 К. Из дифференциальной формы закона Кирхгофа (dDН)/(dT) =
рассматриваемой
реакции при температуре 700 К. Из дифференциальной формы закона Кирхгофа (dDН)/(dT) = 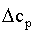 , следует,
что тангенс угла наклона касательной, проведённой к кривой при выбранной
температуре, даёт искомую величину
, следует,
что тангенс угла наклона касательной, проведённой к кривой при выбранной
температуре, даёт искомую величину 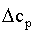 (см. рис. 1).
(см. рис. 1).
Чтобы определить численное значение 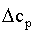 возьмём на
касательной две произвольные точки “a” и ”b” (рис.2). Можно записать:
возьмём на
касательной две произвольные точки “a” и ”b” (рис.2). Можно записать:
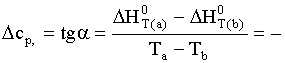 0.95Дж/к
0.95Дж/к
Расчет 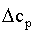 по
уравнению (3а) даёт близкие к найденному графическим способом значения..
по
уравнению (3а) даёт близкие к найденному графическим способом значения..
В изученном интервале температур
знак 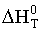 не
меняется, а по сравнению с
не
меняется, а по сравнению с 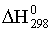 величина
величина 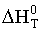 изменилась
примерно на 0,1%.
изменилась
примерно на 0,1%.
.3 При комнатной температуре
изменение энтропии составляет 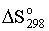 = ……..Дж/К, т.е. реакция протекает с
увеличением (уменьшением) беспорядка
= ……..Дж/К, т.е. реакция протекает с
увеличением (уменьшением) беспорядка
Значения 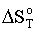 при всех
выбранных температурах, приведенные в таблице 2, данные сведём в таблицу 4.
при всех
выбранных температурах, приведенные в таблице 2, данные сведём в таблицу 4.
Таблица 5 Изменение энтропии в
реакции 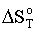 при различных
температурах
при различных
температурах
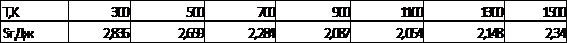
По данным табл. 4 построим
зависимость 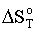 = f(Т) на
рис. 3.
= f(Т) на
рис. 3.
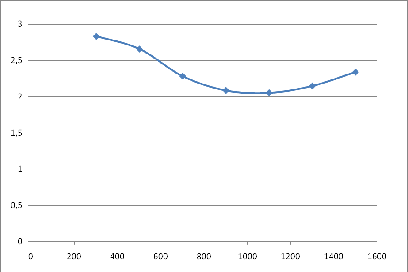
Рисунок 3.
Изменение энтропии в реакции
На рисунке 3 видно, что изменение энтропии в
реакции с температурой аналогично изменению энтальпии на рисунке 2, и
объясняется знаком и величиной производной
d(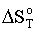 ) / dT =
) / dT = 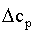 /T
/T
При расчете изменения стандартной
энергии Гиббса для реакции воспользуемся точным уравнением Гиббса-Гельмгольца:
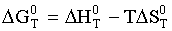 (8)
(8)
Найденные величины изменения
стандартной энергии Гиббса приведены в табл. 6, по данным которой построена
зависимость 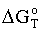 = f(Т),
изображенная на рис. 4.
= f(Т),
изображенная на рис. 4.
Таблица 6. Значения изменения
стандартной энергии Гиббса (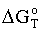 ) при различных температурах
) при различных температурах
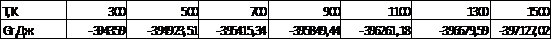
Рис. 4. Стандартное
химическое сродство в реакции
Из таблицы 5 и рис. 4 следует что во
всём периоде температур 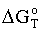 <0.
Характер зависимости стандартного химического сродства от температуры
определяется знаком и величиной изменения энтропии:
<0.
Характер зависимости стандартного химического сродства от температуры
определяется знаком и величиной изменения энтропии:
(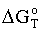 ) / dT = -
) / dT = -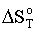 ,
,
т.е.
видом графика на рисунке 4.
5.4 Константа
равновесия реакции
Для реакций, в которых участвуют только газы или
газы и конденсированные фазы, представляющие собой чистые вещества, константу
равновесия Ка выражают обычно через равновесные парциальные давления (Pi) и
обозначают символом Kp.
Константа равновесия связана с изменением
стандартной энергии Гиббса соотношением:
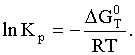 (9)
(9)
После подстановки выражения (8) в
уравнение (9) получим :
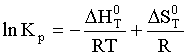 . (10)
. (10)
Если полагать, что в сравнительно
небольшом интервале температур тепловой эффект реакции (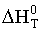 ) и
изменение энтропии (
) и
изменение энтропии (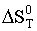 )
практически постоянные величины (это подтверждают и результаты табл. 3 и 4).
Отсюда уравнение можно записать в виде:
)
практически постоянные величины (это подтверждают и результаты табл. 3 и 4).
Отсюда уравнение можно записать в виде:
= (A/T) + B, (11)
Где А и В - постоянные, которые
соответственно равны:
= - 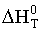 /R (12)
/R (12)
B = 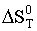 /R (13)
/R (13)
Уравнение (11) отвечает линейной
зависимостью lnКp = f(1/T). Определим коэффициенты А и В графически. С этой
целью по уравнению (9) и данным табл.5 расcчитаем величину lnKp в заданном
интервале температур. Например, для температуры 300К :
, … = -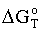 / (R•1500) =
(-397127,02)/(8,31•1500) = 31,859
/ (R•1500) =
(-397127,02)/(8,31•1500) = 31,859
Константа равновесия,
соответствующая полученному значению lnKp,,… , вычисляется следующим
образом:,1500 = е31,859 = 6,46*1013; Kp =6,46*1013
Аналогично рассчитываем lnKp и Кp и
при других температурах. Полученные значения этих величин сведем в табл. 7.
Таблица 7. Величины
констант равновесия при различных температурах
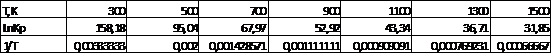
По данным табл. 6 строим зависимость lnKз =
f(1/Т), на рис.5.
Т.к. К>>4 отсюда следует, что идёт прямая
реакция. Причём, чем ниже температура (Т), тем больше равновесие сдвинуто в
сторону продукта реакции.
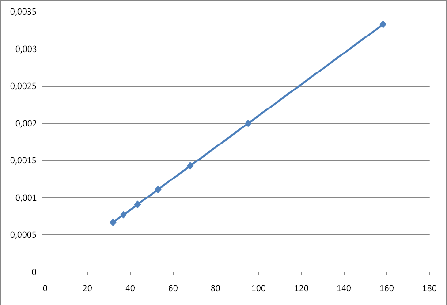
Рис. 5. Зависимость
константы равновесия реакции от температуры
Вид кривой на рис. 5 определяется уравнением
изобары реакции (уравнением Вант-Гоффа):
d (ln Kp) / dT = 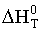 / RT2
/ RT2
Реакция сопровождается выделением
теплоты (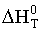 < 0)
поэтому на рис. 5 зависимость ln Kp от температуры убывающая.
< 0)
поэтому на рис. 5 зависимость ln Kp от температуры убывающая.
Если точки на графике (рис. 5)
практически ложатся на прямую, выполняются следующие действия. Тангенс угла
прямой к оси абсцисс численно равен коэффициенту А в уравнении (11). Для
нахождения величины тангенса проведем на рис. 6 прямую, возьмём на ней
произвольно две точки “а” и ”b” и определим численные значения их ординат и
абсцисс. Можно записать:
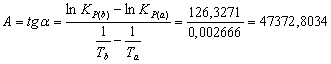

Для определения численного значения
В поступим следующим образом. Из табл. 7 возьмём значение ln Кр при 300 К
(158,1865), подставим его вместе с численным коэффициента А (47372,8034),
найденным ранее, в уравнение (11), предварительно выразив его через В.
= lnKp - A/T =
158,1865-47372,8034/300= 0,2771
Итак, приближенное уравнение
зависимости константы равновесия от температуры имеет вид:= (47372,8034/T) -
0,2771. (14)
Последнее уравнение позволяет
рассчитать значение Кр при любой температуре, если последняя находится в
заданном интервале (т.е. в пределах 300 -1500 К) или незначительно выходит за
этот интервал.
По значениям коэффициента А и В
рассчитаем величину среднего теплового эффекта реакции (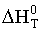 )и изменения
энтропии (
)и изменения
энтропии (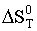 ). Согласно
уравнениям (12) - (13) имеем:
). Согласно
уравнениям (12) - (13) имеем:
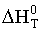 = -A•R = -47372,8034•8,31
=-393667,99 Дж
= -A•R = -47372,8034•8,31
=-393667,99 Дж
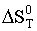 = B•R = 0,2771•8,31 =2,302 Дж/К
= B•R = 0,2771•8,31 =2,302 Дж/К
Полученные данные должны согласуются
с данными, приведенными в табл. 2 и 4.
Исследование 2
В этом исследовании нужно для
рассматриваемой системы рассчитать число степеней свободы.
Определение числа фаз, независимых
компонентов и степеней свободы..
Число независимых компонентов (k)
равно наименьшему числу веществ, необходимых для выражения состава всех фаз
системы. Это число определяют как общее число веществ в системе (m) за вычетом
числа связей между ними (r). Связь между веществами, входящими в
рассматриваемую систему, выражается уравнением реакции. Следовательно, для
нашего уравнения:
т+O2газ =CO2газ
= m - r = 2 (15)
Число степеней свободы (C -
вариантность системы) равно числу независимых компонентов системы (давления,
температуры, концентрации компонентов), которые можно изменить в некоторых
пределах так, чтобы число и природа фаз оставались прежними. По правилу фаз
Гиббса:
С = K + n - f, (16)
где n - число внешних параметров,
влияющих на состояние равновесия системы. Для нашей системы n=1т.к. P,T=const ,
а f-число фаз =2.
=2+1-2=1
Значит, равновесный состав газовой
фаза, зависит от 1 фактора: концентрации.
Установление направления смещения
равновесия.
Качественно направления смещения
состояния равновесия определяется принципом Ле- Шателье: если на систему,
находящуюся в равновесии, оказывается воздействие, то в системе происходят
такое смещение равновесия, которое ослабляет это воздействие.
Реакция:
C+O2 óCO2+Q
идет с выделением тепла(∆H0т<
0), следовательно, при понижением температуры равновесие должно смещаться слева
направо, так как реакция экзотермическая. Этот вывод согласуется с характером
изменения величины Kp в зависимости от температуры при повышении температуры Кр
уменьшается.(см. табл.7).
СПИСОК ЛИТЕРАТУРЫ
1. Краткий
справочник физико-химических величин. Ред. А.А.Равдель и А.М.Пономарева - СПб:
Иван Федоров, 2003. -240 стр.
2. Пономарёва
К.С., В.Г. Гугля, Никольский Г.С. Сборник задач по физической химии. - Москва:
МИСИС, 2007. - 337с.
Приложение 1
Химические реакции
к контрольной работе № 1
|
Вариант
№
|
Уравнение
реакции
|
Т1
К
|
Т2
К
|
Шаг,
град.
|
|
1
|
2
C + O2 = 2 CO
|
300
|
1500
|
200
|
C
+ O2 = CO2
|
300
|
1500
|
200
|
|
3
|
2
CO + O2 = 2 CO2
|
300
|
1500
|
200
|
|
4
|
C
+ CO2 = 2 CO
|
300
|
1500
|
200
|
|
5
|
2
H2 + O2 = 2 H2Oгаз
|
300
|
1500
|
200
|
|
6
|
С
+ Н2Огаз = СО + Н2
|
300
|
1500
|
200
|
|
7
|
С
+ 2 Н2Огаз = 2 Н2 + СО2
|
300
|
1500
|
200
|
|
8
|
CO
+ H2Oгаз = CO2 + H2
|
300
|
1500
|
200
|
|
9
|
CaCO3
= CaO + CO2
|
300
|
1500
|
200
|
|
10
|
MgCO3
= MgO + CO2
|
300
|
1500
|
200
|
|
11
|
PbCO3
= PbO + CO2
|
300
|
1500
|
200
|
|
12
|
FeO
+ CO = Fea + CO2
|
300
|
1500
|
200
|
|
13
|
FeO
+ H2 = Fea + H2Oгаз
|
300
|
1500
|
200
|
|
14
|
Fe3O4
+ CO = 3 FeO + CO2
|
300
|
1500
|
200
|
|
15
|
Fe3O4
+ H2 = 3 FeO + H2Oгаз
|
300
|
1500
|
200
|
|
16
|
300
|
1500
|
200
|
|
17
|
NiO
+ CO = Nia + CO2
|
300
|
1500
|
200
|
|
18
|
MnO
+ H2 = Mn + H2Oгаз
|
300
|
1500
|
200
|
|
19
|
MnO
+ CO = Mn + CO2
|
300
|
1500
|
200
|
|
20
|
FeO
+ Cграфит = СО + Fea
|
300
|
1500
|
200
|
|
21
|
Fe2O3
+ Cграфит = 3 FeO + CO
|
300
|
1500
|
200
|
|
22
|
Si
+ O2 = SiO2 кварц
|
300
|
1500
|
200
|
|
23
|
2
Fea + O2 = 2
FeO
|
300
|
1500
|
200
|
|
24
|
NiO
+ Cграфит= Nia + CO
|
300
|
1500
|
200
|
|
25
|
MnCO3
= MnO + CO2
|
300
|
1500
|
200
|
|
26
|
2
FeSa + 3 O2 =
2FeO + 2SO2
|
300
|
1500
|
200
|
|
27
|
2
FeO + Si = 2Fe+ SiO2
|
300
|
1500
|
200
|
|
28
|
SiO2+2Mn=Si+2MnO
|
300
|
1500
|
200
|
|
29
|
SiO2+2C=Si+2CO
|
300
|
1500
|
200
|
|
30
|
CaO+3C=CaC2+CO
|
1500
|
200
|
|
31
|
3FeO+2Al=Al2O3+3Fe
|
300
|
1500
|
200
|
|
32
|
MnO
+ C = Mn + COг
|
300
|
1500
|
200
|
|
33
|
2/3Fe2O3
+ Si = 4/3 Fe + SiO2
|
300
|
1500
|
200
|
|
34
|
2/3Fe2O3
+ C = 4/3 Fe + 2CO
|
300
|
1500
|
200
|
|
35
|
3Fe2O3
+ CO = 2 Fe3O4 + CO2
|
300
|
1500
|
200
|
|
36
|
Fe3O4
+ CO = 3 FeO + CO2
|
300
|
1500
|
200
|
|
37
|
3Fe2O3
+ H2 = 2 Fe3O4 + H2O
|
300
|
1500
|
200
|
|
38
|
Fe3O4
+ H2 = 3 FeO + H2O
|
300
|
1500
|
200
|