Оксогидроксид марганца (III) MnO(OH) и его синтез
1.
Оксогидроксид марганца (III)
MnO(OH)
Исходное
вещество MnO(OH)
относительно устойчиво, и даже встречается в природе в виде минерала манганата.
Это вещество бурого цвета. Образование этого соединения можно представить
реакцией:
2MnSO4 + H2O2 + 4NH3
+ 2H2Oà 2MnO(OH) +2 (NH4)2SO4
В
начале возможно образование соединения Mn(OH)3,
которое в результате оксоляции теряет воду.
Mn(OH)3àMnO(OH)
+ H2O
MnO(OH)
обладает индивидуальными рентгеновскими характеристиками. Он темно-коричного
цвета. Кристаллическая решетка у гаммы MnO(OH)
ромбическая. Встречается в природе в виде минерала манганита. Используется для
получения гамма Mn2O3.
2.
Триоксалатоманганат (III)
калия K3[Mn(C2O4)3]*3H2O
Как
правило, синтез комплексов MnIII
сводится
к окислению соединений MnII
перманганатом калия в присутствии соответствующего лиганда. Так, при синтезе
триоксалатоманганата (III)
калия сначала восстанавливают перманганат калия щавелевой кислотой до MnII
а затем после подщелачивания раствора карбонатом калия окисляют MnII
до MnIII постепенным
добавлением твердого KMnО4,
суммарно:
KMnO4 + 5H2C2O4
+ 10H2O + K2CO3àK3[Mn(C2O4)3]*3H2O + 5CO2
+ 5CO2 +12H2O
+12H2O
Кристаллы
комплекса K3[Mn(C2O4)3]*3H2O
темного красно-фиолетового цвета в темноте при 200С устойчивы продолжительное
время. В очень разбавленных растворах красно-фиолетовый цвет комплекса переходит
в желтовато-коричневый вследствие практически мгновенной замены одного
оксалатного лиганда на две молекулы воды, что является свидетельством
лабильности (кинетической неустойчивости) комплекса:
[Mn(C2O4)3]3-
+ 2H2O 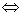 [Mn(C2O4)2(H2O)2]-
+ C2O42-
[Mn(C2O4)2(H2O)2]-
+ C2O42-
Очень
чистые препараты K3[Mn(C2O4)3]*3H2O
устойчивы в темноте при 200С в течение продолжительного времени. При
-60С могут храниться неограниченно долго. Растворимость в воде
хорошая. Концентрированные растворы окрашены в глубокий красно-фиолетовый цвет.
3.
Диоксалатодиакваманганат (III) калия
K3Mn(C2O4)
в воде и на свету дает K
[Mn(C2O4)2(H2O)2].
Оно желто-коричного цвета. Изменение окраски объсняется протекающей мгновенно
равновесной реакцией:
[Mn(C2O4)3]3-
+ 2H2O 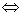 [Mn(C2O4)2(H2O)2]-
+ C2O42-
[Mn(C2O4)2(H2O)2]-
+ C2O42-
Экспериментальная
часть
Синтез
MnO(OH).
В
большом химическом стакане растворила 4,46г MnSO4*4H2O
в 90 мл воде. Потом прибавила 68 мл 3 % – ного раствора H2O2,
а затем при температуре раствора 200C
и при очень сильном перемишивании добавила 120 мл разбавленный раствор аммиака.
Выделяющую
кислород темную коричнево-черную суспензию нагрела 4 мин. тотчас же после
приливания раствора аммиака. После этого отфильтровала раствор. Получила MnO(OH).
При осторожном обезвоживании 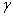 - MnO(OH)
в вакууме при 2500С можно получить
- MnO(OH)
в вакууме при 2500С можно получить 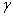 -Mn2O3.
-Mn2O3.
оксогидроксид триоксалатоманганат диоксалатодиакваманганат
Синтез
K3 [Mn(C2O4) 3]*3H2O.
Я
использовала MnO(OH),
H2C2O4,
K2C2O4
для получения триоксолатоманганат (III)
калия. Я взяла 0.75 г. H2C2O4
и 0.75 г. K2C2O4
и каждый растворила в 6 мл воды. Дальше смешала растворы этих двух соединений и
добавила к ним 0.5 г. MnO(OH).
Образовалась смесь красно-фиолетового цвета. Отфильтровала через воронку
Бюхнера и увидела получившиеся кристаллы K3
[Mn(C2O4)
3]*3H2O.
Получение
K [Mn(C2O4)2(H2O)2]
Для
получения этого комплекса мы повторим путь синтеза MnO(OH),
и K3[Mn(C2O4)3]*3H2O.
Только в случае, когда образовался последний комплекс, при отфильтрованиа
осадка K3[Mn(C2O4)3]*3H2O
мы специально добавили дистиллированной воды, с тем чтобы быстро произошло
реакция:
K3[Mn(C2O4)3]*3H2Oà
K [Mn(C2O4)2(H2O)2]
+ K2C2O4
+ H2O(раствор)
K3[Mn(C2O4)3]*3H2Oàкрасно-фиолетовый
K [Mn(C2O4)2(H2O)2]à
желто-коричневый
Две
молекулы воды при этом входят во внутреннюю координационную сферу и молекулы
воды уводят K2C2O4
из
реакционной зоны т. е. Последняя часть синтеза произошла в воронке со
стеклянным пористым дном. В результате получился желто-коричневый осадок (цвет
характерен для K [Mn(C2O4)2(H2O)2]).
Осадок окончательно отфильтровали на этой воронке, высушили на фильтровальной
бумаге на воздухе. Ясно, что во всех операциях мы не проводим затемнения
стаканов, сосудов, воронки.
В
доступный литературе мы не нашли сведений об устойчивости манганатов (III).
Но можно предложить, что комплекс, содержащий воду во внутренней координационной
среде, будет устойчивее, поскольку в стехиометрическом ряду лигандов H2O
стоит правее чем C2O42-
Cl-<F-<C2O42-<H2O<NH3<CN-
Список
литературы
1.
Брауэр. Руководство по неорганическому синтезу. М.: Мир. 1985. Т. 5. с. 1684,
1694–1695.
2.
Ю.Д. Третьяков, Л.И. Мартыненко, А.Н. Григорьев, А.Ю. Цивадзе.
Неорганическая Химия. Химия элементов. Том 1. с. 4/0.
3.
М.Е. Тамм, Ю.Д. Третьяков. Неорганическая химия в трех томах. Том 1.
Физико-химические основы неорганической химии. 2004. с. 189–195.
Размещено на