|
Вещество
|
∆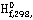
кДж/моль
|
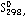
Дж/моль*К
|
∆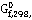
кДж/моль
|
Коэффициенты
уравнения
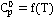
|
|
a
|
b*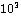
|
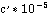
|
|
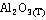
|
-1675,69
|
50,92
|
-1582,27
|
114,55
|
12,89
|
-34,31
|
|
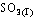
|
-395,85
|
256,69
|
-371,17
|
64,98
|
11,75
|
-16,37
|
|
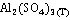
|
-3441,80
|
239,20
|
-3100,87
|
366,31
|
62,59
|
-112,47
|
1.1
Расчет
теплового эффекта реакции
Расчет
теплового эффекта реакции в изобарном процессе в стандартных условиях (DH):
∆ = ∆
= ∆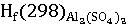 -(∆
-(∆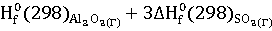 )
)
∆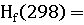 -3441,80-(-1675,69+3(-395,85))=-578,56
кДж
-3441,80-(-1675,69+3(-395,85))=-578,56
кДж
Вывод:
В стандартных условиях данный процесс является экзотермический, реакция идет с
выделением тепла.
Расчет
теплового эффекта реакции в изобарном процессе при заданной температуре(DH):
∆с=0,
т.к. все вещества неорганические
∆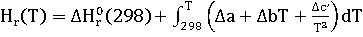
∆a
=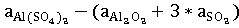 =366,31-(114,55+3*64,98)=56,82
=366,31-(114,55+3*64,98)=56,82
∆b
=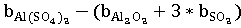 =62,59-(12,89+3*11,75)=14,45*1
=62,59-(12,89+3*11,75)=14,45*1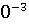
∆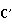 =
=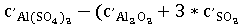 )=-112,47-(-34,31-3*16,37)=-29,05*1
)=-112,47-(-34,31-3*16,37)=-29,05*1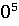
∆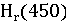 =-578560+
=-578560+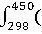 56,82+14,45*1
56,82+14,45*1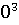 T-29,05*1
T-29,05*1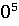 /
/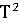 )dT= -578560+56,82
)dT= -578560+56,82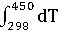 +14,45*1
+14,45*1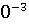
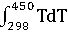 -29,05*1
-29,05*1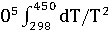 = -578560+56,82(450-298)+14,45*1
= -578560+56,82(450-298)+14,45*1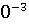 /2*(45
/2*(45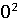 -29
-29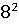 )-29,05*1
)-29,05*1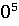 ((450-298)/298*450)=-578560+8636,64+821,45-3292,77=-572,39
кДж
((450-298)/298*450)=-578560+8636,64+821,45-3292,77=-572,39
кДж
Вывод:
При увеличении температуры на 152 К тепловой эффект реакции изменился на 6,17
кДж, реакция осталась экзотермической.
Расчет
теплового эффекта реакции в изохорном процессе в стандартных условиях(DU):
∆Н=∆U+p∆V
;
∆U=∆H-p∆V
p∆V=∆nRT
∆U=∆H-∆nRT
∆n=∆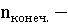 ∆
∆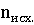 = 0 – 3 = -3; ∆n
= -3
= 0 – 3 = -3; ∆n
= -3
R=8,314
Дж/моль*К
∆U(298)=-578,56-(-3)*0,008314*298=-571,13
кДж
Вывод:
В изохорно-изотермическом процессе, при стандартных условиях реакция протекает
с выделением тепла, т.е. процесс экзотермический.
Расчет
теплового эффекта реакции в изохорном процессе при заданной температуре (DU):
∆U(450)=-572,39-(-3)*0,008314*450=-561,17
кДж
Вывод:
При увеличении температуры на 152 К тепловой эффект данной реакции в
изохорно-изотермическом процессе уменьшился на 9,96 кДж, реакция идет с
выделением тепла.
1.2
Определение направления протекания химического процесса
а)
в стандартных условиях:
∆ (298) =
(298) =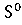 (298
(298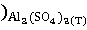 - (
- (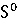 (298
(298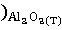 + 3*
+ 3*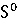 (298
(298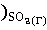 )
)
∆ (298)
=239,2-(50,92+3*256,69)=-581,79 Дж
(298)
=239,2-(50,92+3*256,69)=-581,79 Дж
Вывод:
При взаимодействии оксида алюминия с оксидом серы (VI)
в изолированной системе получилось, что ∆S<0,
поэтому процесс невозможен.
б)
при заданной температуре:
∆с=0,
т.к. все вещества неорганические
∆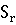 (T)=∆
(T)=∆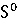 (450)+
(450)+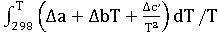
∆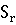 (450)=-581,79+
(450)=-581,79+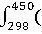 56,82+14,45*1
56,82+14,45*1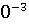 *T-29,05*1
*T-29,05*1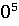 /
/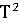 )dT/T= -581,79+56,82
)dT/T= -581,79+56,82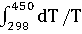 +14,45*1
+14,45*1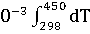 -29,05*1
-29,05*1 = -581,79+56,82*ln450/298+14,45*1
= -581,79+56,82*ln450/298+14,45*1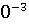 (450-298)- 29,05*1
(450-298)- 29,05*1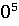 *1/2*((45
*1/2*((45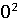 -29
-29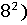 /29
/29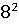 *45
*45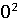 )=-581,79+23,42+2,196-9,15=-565,32
Дж
)=-581,79+23,42+2,196-9,15=-565,32
Дж
Вывод:
При увеличении температуры на 152 К энтропия увеличилась на 16,466 Дж, но
осталась отрицательной. В изолированной системе процесс невозможен. Расчет
изобарно-изотермического потенциала (DG):
а)
в стандартных условиях
∆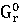 (298) =
(298) =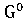 (298
(298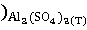 - (
- (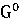 (298
(298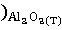 + 3*
+ 3*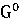 (298
(298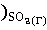 )
)
∆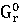 (298) =-3100,87-(-1582,27+3*(-371,17))=-405,13
кДж/моль
(298) =-3100,87-(-1582,27+3*(-371,17))=-405,13
кДж/моль
Вывод:
При взаимодействии оксида алюминия с оксидом серы (VI)
в стандартных условиях ∆G<0,
поэтому процесс самопроизвольный.
∆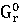 (298) = ∆Н(298)-Т∆
(298) = ∆Н(298)-Т∆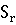 (298)
(298)
∆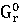 (298) =
-578560-298*(-581,79)=-405,19 кДж
(298) =
-578560-298*(-581,79)=-405,19 кДж
%
ош.=((-405,13+405,19)/(-405,13))*100=0,01% ,
т.к
процент ошибки очень мал, следовательно, можно использовать для расчета оба метода.
Вывод:
В закрытой системе изобарно-изотермический процесс будет протекать
самопроизвольно, т.к. ∆G<0.
б)
при заданной температуре
∆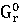 (450) = ∆Н(450)-450*∆
(450) = ∆Н(450)-450*∆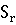 (450)
(450)
∆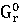 (450) =
-572390-450*(-565,32)=-317,996 кДж
(450) =
-572390-450*(-565,32)=-317,996 кДж
При
увеличении температуры на 152 К, энергия Гиббса увеличилась на 87,194 кДж,
отсюда следует, что чем больше температура, тем больше энергия Гиббса. В
закрытой системе изобарно-изотермический процесс остался самопроизвольным, т.к.
∆G<0. Дальнейшее
повышение температуры не выгодно, т.к. ∆G
стремится к нулю и процесс от самопроизвольного перейдет в равновесный, а затем
в не самопроизвольный.
Расчет
изохорно-изотермического потенциала (DF):
а)
в стандартных условиях
1
способ:
∆F
= ∆U-T∆S
∆F(298)=-571130-298*(-581,79)=-397,76
кДж
2
способ:
∆F(298)=∆G-∆nRT
∆F(298)=-405,13-(-3)*298*0,008314=-397,7
кДж
%ош.=((-397,76+397,7)/(-397,76))*100=0,02%,
т.к
процент ошибки очень мал, следовательно, можно использовать для расчета оба
метода.
Вывод:
В закрытой системе при стандартных условиях изохорно-изотермический процесс
будет протекать самопроизвольно, т.к. ∆F<0.
б)
при заданной температуре
1
способ:
∆F(450)=
-561170-450*(-565,32)=-306,78 кДж
2
способ:
∆F(450)=-317,996-(-3)*450*0,008314=-306,78
кДж
%ош.=((-306,78-306,78)/(-306,78))*100=0%,
т.к
процент ошибки равен нулю, следовательно, можно использовать для расчета оба
метода.
Вывод:
При увеличении температуры энергия Гельмгольца увеличилась. В закрытой системе
изохорно-изотермический процесс будет протекать самопроизвольно.
Вывод:
|
Т,
К
|
∆Н,
кДж
|
∆U,
кДж
|
∆G,кДж/моль
|
∆F, кДж
|
∆S, Дж
|
|
298
|
-578,56
|
-571,13
|
-405,19
|
-397,76
|
-581,79
|
|
450
|
-572,39
|
-561,17
|
-317,996
|
-306,78
|
-565,32
|
С
увеличением температуры тепловые эффекты изобарно-изотермического и изохорно-изотермического
процессов увеличились.
В
данной работе ∆Н, ∆S,
∆G получились
отрицательными, отсюда следует, что процесс протекает самопроизвольно, но при
невысоких температурах.
При
увеличении температуры энергия Гиббса и энергия Гельмгольца увеличились, значит
система стремиться к равновесию (в условиях равновесия ∆F,
∆G достигают минимума).
2.
Задание: Определить ΔH,
ΔU, ΔS,
ΔF, ΔG,
реакции при постоянном давлении P=1.013
* 105 Па.
СdO(т)
+ H2SO4 (ж)
= CdSO4 (т)
+ H2O (г)
Реакция
протекает при температуре 511 градусов Цельсия .
Исходные
данные
|
Вещест-во
|
ΔHf˚298
кДж/моль
Дж/моль*К
|
ΔGf˚298
кДж/моль
|
Ср298
Дж/моль*К
|
Коэф.
уравнения
Ср˚=
f(T)
|
|
a
|
b * 103
|
c΄ * 10-5
|
|
H2O
|
-241,81
|
188,72
|
-228,61
|
33,61
|
30,00
|
10,71
|
0,33
|
|
CdO
|
-258,99
|
54,81
|
-229,33
|
43,64
|
48,24
|
6,38
|
-4,90
|
|
H2SO4
|
-813,99
|
156,90
|
-690,14
|
138,91
|
156,9
|
28,3
|
-23,46
|
|
Cd SO4
|
-934,41
|
123,05
|
-828,88
|
99,62
|
77,32
|
77,40
|
-
|
2.1
Расчёт теплового эффекта реакции
Расчёт
теплового эффекта реакции в изобарном процессе в стандартных условиях
ΔНr˚
(298) = (ΔНf˚
(298) CdSO4
+ ΔНf˚
(298) H2O)
– (ΔНf˚
(298) CdO
+
ΔНf˚
(298) H2SO4)
ΔНr˚
(298) = (-934,41 – 241,81) –
(-258,99 – 813,99) = -103,24 кДж.
Вывод:
При реакции в стандартных условиях ,произошло выделение тепла в количестве
103,24 кДж как следствие реакция является экзотермической.
Расчёт
теплового эффекта реакции в изобарном процессе при заданной температуре
ΔH(T)
= ΔНr˚
(298)
+ 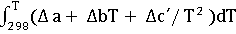 ;
;
Δa
= ( Δa
CdSO4+
Δa
H2O)
- ( Δa
CdO+ Δa
H2SO4)
Δa
= (77,32+30,00) – (48,94+156,90) = -97,82 ;
Δb
= (Δb CdSO4+
Δb H2O)
- (Δb
CdO+ Δb
H2SO4)
Δb
= (77,40+10,71) – (6,38+28,30) = 53,43 * 10-3
Δc΄
=( Δc΄CdSO4+
Δc΄H2O)
- (Δc΄CdO+
Δc΄H2SO4)
Δc΄
= (0 + 0.33) – (-4,90-23,46) = 28,69 * 105
Δc
= 0, т.к. все вещества неорганические.
ΔH(511)
= -103,24 * 103 + 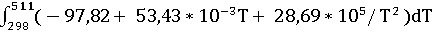 =
=
=
-103,24 * 103 + (-97,82) * (511-298) + 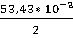 * (5112 –
2982) +
* (5112 –
2982) + 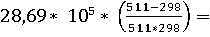 -103240 – 20835,66 +
4603,45 + 4050,80 = -115,42 kДж.
-103240 – 20835,66 +
4603,45 + 4050,80 = -115,42 kДж.
Вывод:
Увеличение температуры привело к увеличению количества теплоты выделившегося в
следствии реакции.
Расчёт
теплового эффекта реакции в изохорном процессе в стандартных условиях
ΔU
= ΔН – ΔnRT
Δn
= Δnкон.
– Δnнач
Δn=1-0=1
Газовая
постоянная R = 8.314 Дж/моль*К
ΔU(298)=
ΔНr˚
(298) –Δn*R*T
ΔU(298)
= -103,24 * 103 -1 * 8,314 * 298 = -103240 – 2477,57 = -105,72 кДж.
Вывод:
Внутренняя энергия реакции в изохорном процессе составила 100,76 килоджоуля.
Расчёт
теплового эффекта реакции в изохорном процессе при заданной температуре
ΔU(511)=
ΔНr˚
(511) –Δn*R*T
ΔU(511)
= -115,42 * 103 - 1 * 8,314 * 511 = -115420 – 4248,45
= - 119,67 кДж.
2.2
Определение направления протекания химического процесса
Определение
направления протекания данной реакции в изолированной системе
Определение
направления протекания реакции в стандартных условиях
ΔS˚
(298) = (S (298) Cd SO4 + S
(298) H2O) – (S(298) Cd O + S
(298) H2SO4)
ΔS˚
(298) = (123,05+188,72)-(
54,81+156,90)= 100,06 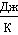
Вывод:
Так как энтропия S больше ноля
100,06>0 то процесс реакции в изолированной системе протекает
самопроизвольно без внешнего воздействия. Определение направления протекания
реакции при заданной температуре.
ΔS(T)
= ΔS˚ (298)
+ 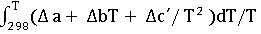 ;
;
ΔS
(511) = 100,06 + 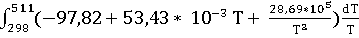 = 100,06 – 97,82
= 100,06 – 97,82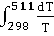 + 53,43 * 10-3
+ 53,43 * 10-3
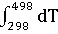 + 28,69 * 105
+ 28,69 * 105 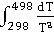 = 100,06 – 97,82
= 100,06 – 97,82 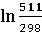 + 53,43 * 10-3 *
(511-298) +
+ 53,43 * 10-3 *
(511-298) + 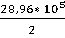 *
* 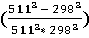 = 121,66
= 121,66 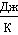
Вывод:
Изменение температуры привело к увеличению энтропии по сравнению с процессом
при стандартных условиях . Следовательно повышение температуры ведёт к увеличению
неупорядоченности и увеличению количества соударений молекул при реакции.
Определение
направления протекания химического процесса в закрытой системе
Расчёт
изобарно – изотермического потенциала в стандартных условиях
ΔGr˚
(298) = (G (298) Cd SO4 + G
(298) H2O) – (G (298) Cd O +
G(298) H2SO4)
ΔGr˚
(298)= (-823,88 – 228.61) –
(-229,33 – 690.14) = -133,02 кДж/моль.
Вывод:
Изобарно – изотермический потенциал показывает что процесс в закрытой системе
идёт самопроизвольно ΔGr˚
<
0 ; -133,02<0 .
Произведем
расчет изобарно – изотермического потенциала по другой формуле:
ΔGr˚
(298) = ΔНr˚
(298) - Т* ΔS˚
(298)
ΔGr˚
(298) = -103,24 * 103 –
298 * 100,06 = -133,06 кДж/моль.
Найдем
процент ошибки:
%
ошибки = 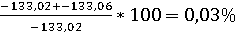
Расчет
можно производить любым способом, т.к. процент ошибки не существенен. Расчёт
изобарно – изотермического потенциала при заданной температуре
ΔGr˚
(511) = ΔНr˚
(511) - Т* ΔS˚
(511)
ΔGr˚
(511) = -119,46 * 103 –
511 * 121,66 = -181,63 кДж/моль.
Вывод:
Увеличение температуры никак не повлияло на процесс реакции в закрытой системе,
она по прежнему идёт самопроизвольно ΔGr˚
<
0; -181,63<0. Расчёт изохорно – изотермического потенциала в стандартных
условиях.
ΔF(298)
= ΔU(298)
– T* ΔS˚
(298)
ΔF(298)
= -105,72 * 103 – 298 * 100,06 = -135,53 кДж.
Вывод:
Изохорно – изотермический потенциал показывает что процесс в закрытой системе
идёт самопроизвольно ΔF
<
0 ; -135,53<0
Расчёт
изохорно – изотермического потенциала при заданной температуре
ΔF(511)
= ΔU(511)
– T* ΔS˚
(511)
ΔF(511)
= - 123,70 * 103 – 511 *121,66 = -185,87кДж.
Вывод:
Изменение температуры привело к уменьшению потенциала по сравнению с процессом
при стандартных условиях, а это означает что глубина реакции в закрытой системе
увеличилась ΔF
<
0 ; -185,87>0.
Вывод
Рассмотренная
реакция оксида кадмия и серной кислоты идёт самопроизвольно на это указывают
все характеристики реакции, а рассмотренное увеличение температуры реакции её
ничуть не замедляет. Всё это позволяет сделать вывод о том что увеличение температуры
реакции позволяет увеличить её глубину и полноту. При этом реакция останется
самопроизвольной.
|
T, K
|
ΔH, кДж
|
ΔU,
кДж
|
ΔS,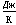
|
ΔG,
кДж/моль
|
ΔF, кДж
|
|
298
|
-103,24
|
-105,72
|
100,06
|
-133,02
|
-135,53
|
|
511
|
-115,42
|
-119,67
|
121,66
|
-181,63
|
-185,87
|