Характеристика алкадієнів
АЛКАДІЄНИ
1. Номенклатура.
Класифікація
Назви алкадієнів
утворюються як похідні від назв відповідних алканів при заміщенні суфікса -н
закінченням -дієн, після якого через дефіс зазначаються локанти,
тобто номери атомів карбону, з яких починаються подвійні зв¢язки. При цьому головний
ланцюг нумерують таким чином, щоб до нього входили обидва подвійних зв¢язки, а атоми карбону,
сполучені подвійними зв¢язками, одержали найменші номери.
Для деяких
алкадієнів користуються тривіальною номенклатурою, наприклад:
CH3
½
CH2=CH-CH=CH2
CH2=C-CH=CH2 CH3-CH=CH-CH=CH2
Бутадієн-1,3 2-Метилбутадієн Пентадієн-1,3
(дивініл) (ізопрен) (піперилен)
Залежно від
взаємного розміщення подвійних зв¢язків алкадієни
поділяються на три групи:
-ізольовані, в яких подвійні зв¢язки в ланцюгу розділені
одним чи декількома sp3-гібридизованими атомами карбону:
>C=CH-(CH2)n-CH=C<,
де n = 1,2,3…;
Ізольовані
алкадієни виявляють хімічні властивості, подібні до звичайних алкенів з тією
лише різницею, що у реакцію може вступати не один, а два подвійних зв¢язки незалежно один від
одного;
-кумульовані алкадієни, в яких обидва подвійні
зв¢язки знаходяться поруч і належать одному атому карбону, наприклад:
СН2=С=СН2
Пропадієн (ален)
Цю групу
алкадієнів часто називають аленовими вуглеводнями за першим членом
гомологічного ряду; аленові вуглеводні є нестійкими сполуками, вони швидко
ізомеризуються в алкіни, тому не мають самостійного значення;
-спряжені алкадієни, в яких подвійні зв¢язки розділені лише одним
s-зв¢язком С-С:
>C=CH-CH=C<.
Саме спряжені
алкадієни мають найважливіше значення в органічному синтезі.
2.
Електронна будова спряжених алкадієнів
Спряжені
сполуки з почерговим розміщенням подвійних і одинарних зв¢язків між атомами карбону
в ланцюгу відрізняються за хімічними властивостями від інших ненасичених
вуглеводнів, що зумовлюється наявністю електронного ефекту спряження.
Спряження – це виникненя єдиної
π-електронної хмари внаслідок перекривання негібридизованих рZ-орбіталей
атомів карбону, які одночасно утворюють подвійні та одинарні зв¢язки С-С.
Найпростішим
спряженим алкадієном є бутадієн-1,3, в якому всі чотири атоми карбону
перебувають у sp2-гібридизованому стані і складають s-скелет молекули (рис.1).
Причому осі sp2-гібридизованих орбіталей знаходяться на одній
площині, а негібридизовані рz-орбіталі кожного атома карбону
перпендикулярні до площини s-скелета і паралельні одна відносно одної. Це
створює умови їх взаємного перекривання не тільки між атомами С1-С2
і С3-С4, але й частково між С2-С3.
Завдяки такому боковому перекриванню чотирьох рz-орбіталей
утворюється єдина p-електронна хмара – так зване p,p-спряження зв¢язків, при якому p-електрони вже не
належать окремим зв¢язкам, а делокалізуються по спряженій системі в
цілому.
Делокалізація електронної густини – це
її розподілення по всій спряженій системі, по всіх зв¢язках і атомах.
Рисунок 1 –
Утворення спряженої системи в молекулі бутадієну-1,3: жирним пунктиром показане
перекривання негібридизованих рz-орбіталей над і під площиною
s-скелета
Делокалізація
p-електронів супроводжується
виділенням енергії. Оскільки спряжені системи мають менший запас енергії, вони виявляють
більшу стійкість порівняно з ізольованими алкадієнами. Енергія, що
вивільняється за рахунок спряження, називається енергією делокалізації, або енергією спряження; для
бутадіну-1,3 вона складає 15кДж/моль.
У результаті
утворення спряженої системи довжини зв¢язків частково
вирівнюються і стають меншими, ніж довжина одинарного зв¢язку в алканах (0,154нм),
але більшими, ніж довжина подвійного зв¢язку в алкенах (0,133нм):
Н Н
½ ½
 Н 0,137 нм С 0,146 нм С
Н 0,137 нм С 0,146 нм С
С С 0,137 нм Н
½ ½
Н Н
Схематично ефект
спряження та вирівнювання довжин зв¢язків зображують
стрілками чи крапками:
СН2===СН---СН===СН2
 СН2 СН
СН СН2
СН2 СН
СН СН2
3.
Ізомерія алкадієнів
Алкадієни
здатні виявляти структурну і просторову
(геометричну) ізомерію. Наприклад, для складу С7Н12
ізомери можуть відрізнятися різним положенням як подвійного зв¢язку і бокових радикалів,
так і різним просторовим розташуванням вуглецевого ланцюга.
Приклади
структурних ізомерів:
СН2=СН-СН-СН=СН–СН3
СН3-С=СН-СН=СН-СН3
½ ½
СН3 СН3
3-Метигексадієн-1,4 2-Метилгексадієн-2,4
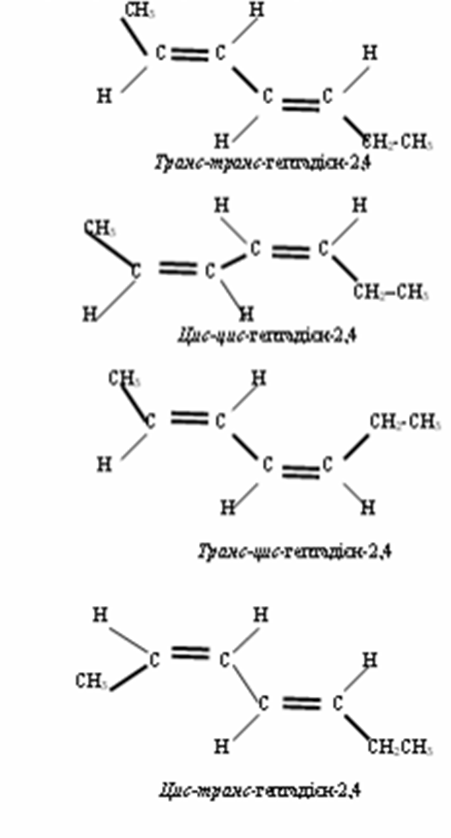
Просторові
ізомери гептадієну–2,4
4. Фізичні
властивості
За
звичайних умов тільки ізомери С4Н6 перебувають у газовому
стані, ізопрен – рідина, решта дієнових вуглеводнів є рідинами чи твердими
речовинами залежно від довжини і розгалуженості вуглецевого скелета. Всі вони
малорозчинні у воді, але добре розчиняються в органічних розчинниках.
5. Хімічні
властивості спряжених алкадієнів
Для алкадієнів найбільш
характерними є реакції електрофільного приєднання АЕ, однак
на відміну від алкенів наявність спряженої системи дає деякі особливості в
реакціях АЕ. Це зумовлює можливість одержання двох продуктів. Один з
них отримується за рахунок приєднання за місцем будь-якого подвійного зв¢язку – такий шлях реакції позначають терміном 1,2-приєднання. А
інший продукт утворюється внаслідок приєднання до крайніх атомів С, що
складають спряжену систему, – так зване 1,4-приєднання. Переважний напрямок
проходження реакції залежить від умов її проведення та природи реагентів.
І
Реакції електрофільного приєднання АЕ.
1
Гідрування при використанні паладієвого каталізатора проходить за
1,2-положенням. Якщо гідрування проводять за допомогою водню у момент його
виділення (наприклад, внаслідок дії натрієм на спирт), то реакція проходить переважно
за 1,4-положенням. На першій стадії утворюються алкени:
+Н2 [Pd]
 -------------------à CH3-CH2-CH=CH2
-------------------à CH3-CH2-CH=CH2
1,2-Приєднання Бутен-1
СН2=СН-СН=СН2---–
Бутадієн-1,3
+Н2 (2С2Н5ОН +2Na)
-----------------------àCH3-CH=CH-CH3.
1,4-Приєднання Бутен-2
При надлишку
водню відбувається повне гідрування з утворенням алканів:
Pt
СН2=СН-СН=СН2+ 2Н2(надл.)--------à CH3-CH2-CH2-CH3.
Бутадієн-1,3 Бутан
1,4-Приєднання
 -------------------à CH2-CH=CH-CH2
-------------------à CH2-CH=CH-CH2
½ ½
СН2=СН-СН=СН2 +
Hal2--- Нal Нal
Дивініл 1,4–Дигалогенбутен–2
1,2-Приєднання
--------------------à CH2-CH-CH=CH2
½ ½
Нal Нal
3,4-Дигалогенбутен–1
При надлишку галогену
утворюються тетрагалогеналкани:
СН2=СН-СН=СН2 + 2Br2
(надл.)à H2Br-CHBr-CHBr-CH2Br.
Дивініл 1,2,3,4- Тетрабромбутан
3 Гідрогалогенування. Приєднання галогеноводнів
підлягає тим самим закономірностям. Якщо реакція проходить за 1,2-положенням,
то діє правило Марковникова:
1,4-Приєднання
 -----------------------à CH3-CH=CH-CH2Br
-----------------------à CH3-CH=CH-CH2Br
1-Бромбутен-2
СН2=СН-СН=СН2 +
HBr---
Дивініл 1,2-Приєднання
-------------------------à CH2=CH-CHBr-CH3
3-Бромбутен-1
1,4-Приєднання
 -----------------à
CH3-CH2-CHBr-CH2Br
-----------------à
CH3-CH2-CHBr-CH2Br
1,2-Дибромбутан
СН2=СН-СН=СН2 +
2HBr----
Дивініл
(надл.) 1,2-Приєднання
-------------------à CH3-CHBr-CHBr-CH3
2,3-Дибромбутан
4 Гіпогалогенування на відміну від
попередніх реакцій АЕ проходить переважно у 1,2-положенні згідно із
правилом Марковникова:
d- d+ 1,2-
CH2=CH-CH=CH2 + HO-Br
-----à CH2Br-CH(OH)-CH=CH2
Дивініл 4- Бромбутен-1-ол-3
ІІ Синхронні
(молекулярні) реакції
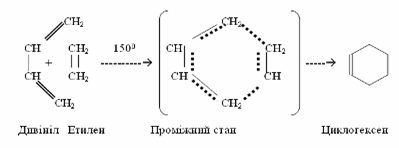
Прикладом
синхронних реакцій, при яких розрив хімічних зв’язків проходить одночасно в
обох вихідних речовинах, є синтез Дильса-Альдера – нагрівання
дієнових вуглеводнів з алкенами чи іншими сполуками, які містять один подвійний
зв¢язок >C=C< у ланцюгу. Цей процес широко використовується для
одержання шестичленних циклів.
ІІІ Ди-
і полімеризація
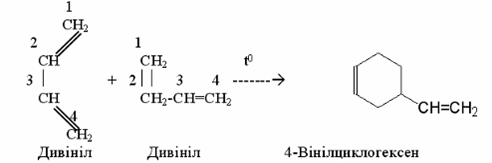
1Димеризація - це сполучення двох
молекул алкадієну,
причому одна
з молекул реагує за 1,2-, а інша – за 1,4-положенням, наприклад:
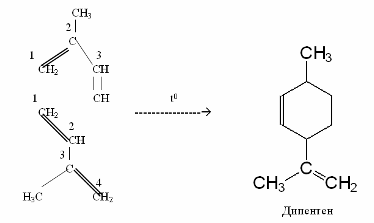
Таким чином
можна одержувати штучні терпени, наприклад, дипентен:
2 Полімеризація. Алкадієни легко
піддаються полімеризації з утворенням каучукоподібних полімерів.
Приєднання
молекул мономеру одна до одної може проходити як за 1,2-, так і за
1,4-положенням – залежно від умов проведення реакції та природи каталізатора.
Al(C2H5)3
× TiC
n CH2=CH-CH=CH2
-------------------à (-CH2-CH=CH-CH2-)n
Дивініл
Бутадієновий каучук
ІV.
Окиснення
1 Реакція
Вагнера приводить до багатоатомних спиртів
[O] CH2-CH-CH-CH2
CH2=CH-CH=CH2
------------à ½ ½ ½ ½
KMnO4, H2O OH OH OH OH
Дивініл
Бутантетрол-1,2,3,4
2 Сильні
окисники руйнують подвійні зв¢язки:
[O] CH2-CH-CH-CH2
CH2=CH-CH=CH2
------------à ½ ½ ½ ½
KMnO4, H2O OH OH OH OH
Дивініл Бутантетрол-1,2,3,4
3 Озонування
(реакція Гарієса) дозволяє встановити будову вихідного алкадієну за складом
продуктів, що утворилися, наприклад
 O O
O O
CH2=C-CH=CH2
+ 2О3 –> CH2 C–CH
CH2 à
½ O––O ½
O––O
CH3
CH3
Ізопрен Озонід ізопрену
2H2O
–––––––––>
2HCHO + CH3-C-CHO + 2H2O2
(Zn) ½½
Метаналь 2-Оксопропаналь
(формальдегід)
6.
Одержання алкадієнів
Завдяки
великому промисловому значенню алкадієнів розроблено багато способів їх
добування.
1 Ступеневе
дегідрування бутану та ізопентану над
змішаним
каталізатором – оксидом хрому (ІІІ) на оксиді алюмінію:
t0, kat t0, kat
СН3-СН2-СН2-СН2
–––––à CH3-CH2-CH=CH2 –––––à
–H2 –H2
––––––>
CH2=CH-CH=CH2.
2Реакція
Лебедєва – одночасне дегідрування і дегідратація етанолу:
4400C
2СН3-СН2-ОН
–––––––à CH2=CH-CH=CH2 + 2H2O
+ H2.
ZnO/Al2O3
Лабораторні
способи
-дегалогенування
віцинальних
тетрагалогеналканів за допомогою цинку чи магнію:
CH2Br-CHBr-CHBr-CH2Br +2
Zn à CH2=CH-CH=CH2 +2 ZnBr2.
1,2,3,4-Тетрабромбутан
Дивініл
-дегідрогалогенування
1,4-дигалогеналканів спиртовим розчином лугу:
CH2Br-CH2-CH2-CH2Br+2КОН(спирт.)à
1,4-Дибромбутан ––––>CH2=CH-CH=CH2+2KBr+
2H2O.
Дивініл
-дегідратація g-гліколів (двоатомних
спиртів з гідроксильними групами в 1,4-положеннях):
СН2-СН2-СН2-СН2
t0
½ ½ –––––––––à CH2=CH-CH=CH2
+ 2H2O.
OH OH H2SO4(к)
Бутандіол-1,4
7.
Застосування алкадієнів
Алкадієни
(ізопрен, дивініл) використовуються для одержання синтетичних каучуків.
Натуральний
каучук – високоеластичний матеріал природного походження, який
одержують із латексу – соку каучуконосних рослин (гевея, гваюла, кок-сагиз,
тау-сагиз та ін.) - при дії на нього коагулянтом – оцтовою кислотою.
За
складом і будовою натуральний каучук являє собою ізопреновий полімерний ланцюг
із цис-конфігурацією, при якій всі однакові групи (у даному випадку –СН2–)
розміщені з одного боку від подвійного зв¢язку. Такий полімер
називається стереорегулярним:
 ---СН2
СН2---
---СН2
СН2---
С===С
СН3 Н n
Макромолекула
натурального каучуку складається у середньому з 250 елементарних ланок, а
молекулярна маса коливається у межах 150000-500000.
Для
надання каучуку міцності та стійкості до зношування, перепадів температур, дії
розчинників і агресивних хімічних реагентів, його піддають вулканізації
– нагріванню із сіркою (вулканізатор) у суміші з наповнювачем (найчастіше
це сажа), внаслідок чого ланцюги нормальної будови зшиваються у сітчасті тривимірні
макромолекули. Вулканізований каучук називають гумою. Гума
містить значно менше подвійних зв¢язків, ніж каучук,
оскільки частина їх руйнується при взаємодії із сіркою (рис. 2).
Якщо
вміст сірки досягає 32%, подвійних зв¢язків не залишається,
окремі ланцюги фіксуються сульфідними містками, а каучук перетворюється на ебоніт
–– тверду речовину з іншими властивостями.
Натуральний
каучук – дефіцитний дорогий продукт, тому розроблені способи добування
синтетичних каучуків із заданими властивостями. Для цього застосовують процес сополімеризації
– сумісної полімеризації алкадієнів з іншими ненасиченими сполуками, які можна
розглядати як похідні етилену: з вінілхлоридом СН2=СНСl, стиреном СН2=СН-С6Н5,
акрилонітрилом СН2=СН-CN.
Наприклад,
сополімер бутадієну і стирену – бутадієнстиреновий каучук, який завдяки великій
міцності та стійкості до зношування використовується для виробництва
автомобільних шин. Схема сополімеризації:
n CH2=CH-CH=CH2 + n CH2=CH ---à
½
C6H5
Бутадієн-1,3 Стирен
С6Н5
½
–––––> (-CH2-CH=CH-CH2-CH-CH2-)n
Бутадієнстиреновий каучук (БСК)
Із
галогенопохідних дієнових вуглеводнів також одержують цінні види каучуків,
наприклад, хлоропреновий каучук, який має високу світло- і
термостійкість, а також стійкість до дії розчинників, бензинів, олій, тому на
його основі виробляють бензопроводи, шланги для нафтопромислів тощо.
n CH2=CH-C=CH2
-------à (-CH2–CH=C-CH2- )n
½ ½
Cl Cl
2-Хлорбутандієн-1,3 Хлоропреновий каучук
(хлоропрен)
½ ½
СH3 S H3C
S H3C


 ½ ½
½ ½ ½
½ ½
½ ½ ½
…--CH2—C—CH—CH2—CH2—C==C—CH2—CH2––C––CH––CH2—…
½
½
H3C S CH3
H3C S


 ½ ½
½ ½ ½
½ ½
½ ½ ½
…--CH2—C—CH — CH2—HC ==C—CH–– CH2—
CH==C—CH—CH2–…
½ ½
S
S
½ ½
Рисунок 2 –
Схема утворення сітчастої структури внаслідок вулканізації натурального каучуку
(пунктиром показані межі елементарних ланок)