Термодинамические характеристики (H,S,G) и возможность самопроизвольного протекания процесса
Федеральное агентство по образованию
Государственное учреждение высшего
профессионального образования
Московский государственный университет
Кафедра химии
Курсовая работа
"Термодинамические характеристики (H,S,G) и возможность
самопроизвольного протекания процесса"
Выполнил:
студент группы 420681
Проверил:
доцент кафедры химии
Москва 2009
План курсовой работы
Уравнять реакцию, используя электронно-ионный метод, указать
процесс окисления, восстановления (окислитель, восстановитель).
Найти потенциалы окислителя и восстановителя указать
направления протекания процесса.
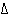
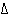
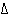 Определить термодинамические
характеристики (H, S, G) и возможность самопроизвольного протекания процесса.
Определить термодинамические
характеристики (H, S, G) и возможность самопроизвольного протекания процесса.
Определить, изменение каких параметров может сместить
равновесие в сторону продуктов реакции (написать кинетическое уравнение).
Написать электронную формулу всех элементов по 2 и 4
квантовым числам. Для отмеченного атома определить высшую и низшую валентность
(составить формулу для гидроксидов, оксидов, солей и их химических соединений).
Может ли взаимодействовать отмеченный металл с кислотами (HCL,
H2SO4 (р),
H2SO4 (к),
HNO3 (P),
HNO3 (K),
растворами щелочей) (ответы обосновать). Отмеченный металл находиться в
контакте с железом. Как будут протекать процессы коррозии во влажном воздухе и
кислой среде. Способы защиты металла от коррозии.
Уравнять, используя электронно-ионный метод.
 3Pb*O2 + Cr2 (SO4) 3 +16NaOH
3Na2PbO2+2
Na2CrO4 +
3Na2SO4+8H2O
3Pb*O2 + Cr2 (SO4) 3 +16NaOH
3Na2PbO2+2
Na2CrO4 +
3Na2SO4+8H2O
1 Cr2 +2 - 6e 2Cr +6 - Окисление восстановителя
3 Pb+4 +2e Pb+2 -
Восстановление окислителя
Метод полу-реакции
1 Cr2 +2 +16OH - 6e 2CrO4-2 +8H2O - Окисление восстановителя
3 Pb+4 +2e Pb+2 -
Восстановление окислителя
PbO2+Cr2+3+16OH
PbO2+2CrO4+8H2O
2. Потенциалы окислителя и восстановителя.
E0 Pb+4/Pb+2 = 2, 33 - окислитель
E0 Cr+2/CrO4-2
= 0, 53 - восстановитель
∆E= E
окислителя - E восстановителя = 2,33-0,56=1,80
∆E>0, следовательно, ∆G<0 - самопроизвольное протекание процесса
3. Приведены стандартные образования H и S при
температуре 298K.
|
Вещество
|
∆H KДж/моль
|
S0 Дж/ моль*K
|
|
Cr2 (SO4) 3
|
-3308
|
288
|
|
PbO2
|
-276,6
|
-218,3
|
|
NaOH
|
- 425,88
|
64,43
|
|
Na2PbO2
|
-819,3
|
189,1
|
|
Na2CrO4
|
-1343
|
176,6
|
|
Na2SO4
|
-1387,9
|
149,58
|
|
H2O
|
-285,8
|
70,1
|
4. Определить, изменением каких параметров можно сместить
равновесие в сторону продуктов реакции
Согласно принципу Ле-Шателье при повышении температуры
химическое равновесие смещается в сторону эндотермической реакции. Поскольку
данная реакция является эндотермической, то для того чтобы сместить равновесие
в сторону обратной реакции, необходимо понизить температуру.
5. Написать электронную формулу 2 и 4 квантовым числам
H 1s1
O 1s2 2s2 2p4
Na 1s22s22p63s1
S 1s22s22p63s23p4
Cr 1s22s22p63s23p63d54s1
Pb 1s22s22p63s23p63d104s24p64d104f145s25p65d106s26p2
6. Определить высшую и низшую валентность
Pb - химический элемент IV группы; конфигурация внешней оболочки атома 6s26p2. Наиболее
характерны 2 степени окисления +2 и +4.
Pb+2 Pb+4
PbO PbO2
Оксид олова (II) Оксид олова (IV)
Pb (OH) 2 Pb (OH) 4=H2PbO3
KNO3 + Pb = KNO2 + PbO
1 N +5 +2e N +3 - пр. восстановление (KNO3)
окислитель
1 Pb0 - 2e Pb+2 -
пр. окисление (Pb) восстановитель
2РbО + РbO2
= Рb2РbO4
(Pb3O4)
Pb (NO3)
2 (конц) + Na2CO3
(конц) = PbCO3↓ + 2NaNO3
PbSO4 + Na2S = PbS↓
+ Na2SO4
Pb (OH) 2 + 2NaOH (конц) = Na2 [Pb (OH) 4] (р)
7. Взаимодействие отмеченного металла с кислотами
(HCL, H2SO4 (р),
H2SO4
(к), HNO3 (P), HNO3 (K) ), растворами щелочей.
PbO2 + Pb + 2H2SO4
(конц., гор) = 2PbSO4+2H2O
1 Pb0 - 2e Pb+2
- пр. Окисление (Pb) восстановитель
2 H+ +1e H0 - пр. Восстановление (H2SO4) окислитель
Pb
+ 2HCl = PbCl2 + H2
1 Pb0 - 2e Pb+2
- пр. Окисление (Pb) восстановитель
2 H+ +1e H0 - пр. Восстановление (HCl) окислитель
Pb + H2SO4 (р) = PbSO4 + H2
1 Pb0 - 2e Pb+2 - пр. Окисление (Pb) восстановитель
1 2H+ +2e 2H0 - пр. Восстановление
(H2SO4) окислитель
Pb + 4HNO3 (р) = Pb (NO3) 2 +
2NO2 + 2H2O
1 Pb 0
- 2e Pb +2 - пр. Окисление (Pb) восстановителя
2 N+5 +1e N+4 - пр. Восстановление
(HNO3) окислителя
PbO2 +MnSO4 +2NaOH Na2PbO2+
Na2MnO3 +Na2SO4+H2O
8. Анодное и катодное покрытие гальвано-пары Fe/Pb. Процесс коррозии сплава
железа со свинцом и способ ее устранения.
Eo pb2+ = 1,23 катод
Eo Fe2+ = - 0,44 анод
В кислой среде процесс проходит с водородной деполяризацией:
Pb/H2SO4/Fe+
Продукт коррозии: PbSO4 и
H2O
В нейтральной среде для активного металла процесс идёт с
водородной деполяризацией:
Pb/H2O,O2/Fe+
2Pb+2 H2O+ O2=Pb+4OH
А (Fe): Fe - 2e = Fe2+ K (Pb): O2
+ H2O + 4e = 4OH-
Список литературы
1.
Глинка Н.Л. Общая химия: Учебное пособие для вузов. - / Под ред.В.А. Рабиновича.
- Л.: Химия, 2006.
2.
Глинка Н.Л. Задачи и упражнения по общей химии: Учеб. пособие для вузов/
Под ред.В.А. Рабиновича и Х.М. Рубиной. - Л.: Химия, 2007
3.
Блинов Л.Н., Перфилова И.Л., Чувиляев РГ. Химия. Основные понятия,
реакция, законы, схемы: Учеб. Пособие. СПб. 2004.92с.
4.
Химия. Классы химических соединений: Учеб. Пособие / Н.П. Танцура, А.В. Горелова,
И.Н. Семенов, Л.Н. Блинов. (Серия "Школа-вуз"). СПб. 2005.67с.
5.
Семенов И.Н., Перфилова И.Л. Химия. СПб.: Химия, 2000.656с.
6.
Коровин Н.В. Общая химия. М.: Высшая школа, 2009.558с.